"Клинические рекомендации "Герминогенные опухоли у мужчин"
МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ
КЛИНИЧЕСКИЕ РЕКОМЕНДАЦИИ
ГЕРМИНОГЕННЫЕ ОПУХОЛИ У МУЖЧИН
МКБ 10: C38, C48, C62
Год утверждения (частота пересмотра): 2018 (пересмотр каждые 3 года)
ID: КР584/1
URL
Профессиональные ассоциации
- Ассоциация онкологов России Российское общество клинической онкологии
Ключевые слова
- Герминогенные опухоли
- Семинома
- Несеминомные опухоли
- Эмбриональный рак
- Опухоль желточного мешка
- Тератома
Список сокращений
IGCCCG - International Germ Cell Cancer Collaborative Group
АФП - альфа-фетопротеин
ВГННТ - внутрипротоковая герминогенная неоплазия неклассифицированного типа
ГКСФ - гранулоцитарный колониестимулирующий фактор
КТ - компьютерная томография
ЛДГ - лактатдегидрогеназа
МРТ - магниторезонансная томография
НС-ЗЛАЭ - нервосберегающая забрюшинная лимфаденэктомия
ОФЭ - орхофуникулэктомия
ПЭТ-КТ позитронно-эмиссионная томография, совмещенная с КТ
УЗИ ультразвуковое исследование
ХГЧ -  хорионического гонадотропина человека
хорионического гонадотропина человека
ЭКГ - электрокардиография
Термины и определения
Новые термины и определения не используются в рекомендациях.
1. Краткая информация
1.1 Определение
Герминогенные опухоли - группа злокачественных опухолей, исходящих из герминативного эпителия.
1.2 Этиология
Причина возникновения герминогенных опухолей до сих пор четко не установлена. Сообщается о повышении риска возникновения опухолей при экзогенной гиперэстрогении (внутриутробной на фоне гестозов, поступление с пищей фитоэстрогенов) (1). Факторами, ассоциированными с возникновением герминогенных опухолей, являются крипторхизм (риск повышается в 5 - 10 раз), бесплодие (риск повышается в 10 - 20 раз), синдром тестикулярной дисгенезии, наличие герминогенной опухоли у родственника первой степени родства (риск повышается в 5 - 10 раз) (2) (3) (4).
1.3 Эпидемиология
Герминогенные опухоли являются редким заболеванием, составляя около 0,5% от всех опухолей у мужчин. Однако в возрастной группе 20 - 25 лет наряду с лимфомами являются наиболее частыми злокачественными новообразованиями. В ![]() они локализуются в яичке (составляя до 95% всех злокачественных опухолей яичка), реже в забрюшинном пространстве, переднем средостении или головном мозге. Данных по эпидемиологии герминогенных опухолей внегонадной локализации в РФ нет. В 2012 году в России зарегистрировано 1330 новых случаев опухолей яичка и одновременно умерло по этой причине 400 больных, что в несколько раз хуже, чем в странах Западной Европы (5).
они локализуются в яичке (составляя до 95% всех злокачественных опухолей яичка), реже в забрюшинном пространстве, переднем средостении или головном мозге. Данных по эпидемиологии герминогенных опухолей внегонадной локализации в РФ нет. В 2012 году в России зарегистрировано 1330 новых случаев опухолей яичка и одновременно умерло по этой причине 400 больных, что в несколько раз хуже, чем в странах Западной Европы (5).
1.4 Кодирование по МКБ 10
Злокачественное новообразование сердца, средостения и плевры (C38):
C38.1 Переднего средостения;
C38.2 Заднего средостения;
C38.3 Средостения неуточненной части;
C38.8 Поражение сердца, средостения и плевры, выходящее за пределы одной и более вышеуказанных локализаций.
Злокачественное новообразование забрюшинного пространства и брюшины (C48):
C48.0 Забрюшинного пространства;
C48.8 Поражение забрюшинного пространства и брюшины, выходящее за пределы одной и более вышеуказанных локализаций.
Злокачественное новообразование яичка (C62):
C62.0 Неопустившегося яичка;
C62.1 Опущенного яичка;
C62.9 Яичка неуточненное.
1.5 Классификация
1.5.1 Международная гистологическая классификация ВОЗ (2013)
9061/3 Семинома, БДУ (C62._)
9062/3 Семинома, анапластическая (C62._)
9063/3 Сперматоцитарная семинома (C62._)
9064/2 Внутриканальцевые (интратубулярные) злокачественные зародышевые клетки (C62._)
9065/3 Герминогенная опухоль, несеминомная (C62._)
9070/3 Эмбриональный рак, БДУ
9071/3 Опухоль желточного мешка
9072/3 Полиэмбриома
9073/1 Гонадобластома
9080/0 Тератома, доброкачественная
9080/1 Тератома, БДУ
9080/3 Тератома, злокачественная, БДУ
9081/3 Тератокарцинома
9082/3 Злокачественная тератома, недифференцированная
9083/3 Злокачественная тератома, промежуточная
9084/0 Дермоидная киста, БДУ
9084/3 Тератома со злокачественной трансформацией
9085/3 Смешанная герминогенная опухоль
1.6 Стадирование
Стадирование опухолей яичка осуществляется в соответствие с классификацией TNM, а внегонадных опухолей забрюшинного пространства и средостения, а также пациентов с IS, II и III стадиями опухолей яичка - по классификации International Germ Cell Cancer Collaborative Group (IGCCCG).
1.6.1 Стадирование опухолей яичка по системе TNM7 (2009)
T - Первичная опухоль
За исключением pTis и pT4, когда для целей классификации выполнение орхофуникулэктомии (ОФЭ) не является абсолютно необходимым, степень распространения первичной опухоли классифицируется после ОФЭ.
Критерий pT:
pTX - Недостаточно данных для оценки первичной опухоли (без ОФЭ применяется категория pTx);
pT0 - Первичная опухоль не определяется (например, гистологически - рубец в яичке);
pTis - Внутрипротоковая герминогенная неоплазия неклассифицированного типа (ВГННТ, бывшая carcinoma in situ);
pT1 - Опухоль ограничена яичком и придатком без сосудистой/лимфатической инвазии, опухоль может врастать в белочную оболочку яичка, но не во влагалищную оболочку;
pT2 - Опухоль ограничена яичком и придатком, имеется сосудистая/лимфатическая инвазия, или опухоль прорастает через белочную оболочку яичка и врастает во влагалищную оболочку;
pT3 - Опухоль распространяется на семенной канатик с или без сосудистой/лимфатической инвазии;
pT4 - Опухоль распространяется на мошонку с или без сосудистой/лимфатической инвазии.
N - Регионарные лимфатические узлы
К регионарным относятся забрюшинные и подвздошные лимфоузлы. Паховые лимфоузлы являются для опухолей яичка отдаленными и поражаются редко. Однако, если у пациента нормальные пути лимфооттока были нарушены вследствие ранее выполненных оперативных вмешательств в паховой области (низведение яичка, грыжесечение и др.), то метастазы в паховые лимфоузлы в данном случае стадируются как регионарные.
Клиническая оценка:
NX - Недостаточно данных для оценки состояния регионарных лимфатических узлов;
N0 - Нет признаков поражения метастазами регионарных лимфатических узлов;
N1 - Имеются метастазы в одном или нескольких лимфатических узлах до 2 см в наибольшем измерении;
N2 - Имеются метастазы в одном или нескольких лимфатических узлах до 5 см в наибольшем измерении;
N3 - Имеются метастазы в лимфатических узлах более 5 см в наибольшем измерении.
Патоморфологическая оценка:
pNX - Недостаточно данных для оценки регионарных лимфатических узлов;
pN0 - Метастазы в регионарных лимфатических узлах отсутствуют;
pN1 - Имеются метастазы до 2 см в наибольшем измерении с поражением до 5 узлов;
pN2 - Имеются метастазы до 5 см в наибольшем измерении с поражением до 5 узлов или распространение опухоли за пределы узла;
pN3 - Метастазы в лимфатических узлах более 5 см в наибольшем измерении.
M - Отдаленные метастазы:
MX - Недостаточно данных для определения отдаленных метастазов;
M0 - Нет признаков отдаленных метастазов;
M1 - Имеются отдаленные метастазы:
M1a - Поражены метастазами нерегионарные лимфатические узлы или легкие;
M1b - Другие отдаленные метастазы.
S - Опухолевые маркеры сыворотки крови:
Sx - Невозможна оценка маркеров сыворотки;
S0 - Уровни маркеров соответствуют норме;
S1 - ЛДГ < 1,5 x N и ХГЧ < 5,000 (мМЕ/мл) и АФП < 1,000 (МЕ/мл);
S2 - ЛДГ 1,5 - 10 x N или ХГЧ 5,000 - 50,000 (мМЕ/мл) или АФП 1,000 - 10,000 (МЕ/мл);
S3 - ЛДГ > 10 x N или ХГЧ > 50,000 (мМЕ/мл) или АФП > 10,000 (МЕ/мл).
Таблица 1. Группировка по стадиям в соответствие с классификацией TNM7 (2009).
Стадия
Критерий T
Критерий N
Критерий M
Критерий S
Стадия 0
pTis
N0
M0
S0
Стадия IA
pT1
N0
M0
S0
Стадия IB
pT2-4
N0
M0
S0
Стадия IS
pTлюбая
N0
M0
S1 - 3
Стадия IIA
pTлюбая
N1
M0
S0 - 1
Стадия IIB
pTлюбая
N2
M0
S0 - 1
Стадия IIC
pTлюбая
N3
M0
S0 - 1
Стадия IIIA
pTлюбая
Любое N
M1, M1a
S0 - 1
pTлюбая
Любое N
Стадия IIIB
pTлюбая
pN1 - 3
M0
S2
pTлюбая
Любое N
M1a
S2
Стадия IIIC
pTлюбая
pN1 - 3
M0
S3
pTлюбая
Любое N
M1a
S3
pTлюбая
Любое N
M1b
Любое S
1.6.2. Классификация International Germ Cell Cancer Collaborative Group
Таблица 2. Классификация IGCCCG (для опухолей IS, II и III стадиями TNM, первичных опухолей забрюшинного пространства и средостения) (6).
Клинико-морфологический вариант
Несеминома
Семинома
Прогностическая группа
Благоприятный прогноз
56% пациентов, 5-летняя общая выживаемость - 92%
Клинико-лабораторная характеристика пациентов
- Локализация первичной опухоли в яичке или забрюшинном пространстве
- Отсутствие нелегочных висцеральных метастазов
- АФП < 1000 нг/мл#, ХГЧ < 5000 мМЕ/мл и ЛДГ < 1,5 x ВГН
- Любая локализация первичной опухоли
- Отсутствие нелегочных висцеральных метастазов
- Нормальный АФП, любые ХГЧ и ЛДГ
Прогностическая группа
Промежуточный прогноз
28% пациентов, 5-летняя общая выживаемость - 80%
Клинико-лабораторная характеристика пациентов
- Локализация первичной опухоли в яичке или забрюшинном пространстве
- Отсутствие нелегочных висцеральных метастазов
- АФП 1000 - 10000 нг/мл# и/или
- ХГЧ 5000 - 50000 мМЕ/мл и/или
- ЛДГ 1,5 - 10 x ВГН
- Любая локализация первичной опухоли
- Наличие нелегочных висцеральных метастазов
Прогностическая группа
Неблагоприятный прогноз
16% пациентов, 5-летняя общая выживаемость - 48%
Клинико-лабораторная характеристика пациентов
- Локализация первичной опухоли в средостении и/или
- Наличие нелегочных висцеральных метастазов и/или
- АФП > 10000 нг/мл# и/или
- ХГЧ > 50000 мМЕ/мл и/или
- ЛДГ > 10 x ВГН
Варианта неблагоприятного прогноза для семиномы не предусмотрено
--------------------------------
<*> ВГН - верхняя граница нормы.
# для пересчета уровня АФП из МЕ/мл в нг/мл необходимо первые умножить на поправочный коэффициент 1,21 (например, 1000 МЕ/мл = 1210 нг/мл).
2. Диагностика
2.1 Жалобы и анамнез
- Рекомендуется тщательный сбор жалоб и анамнеза у пациента с целью выявления факторов, которые могут повлиять на выбор тактики лечения (7).
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - IV)
2.2 Физикальное обследование
- Рекомендуется тщательный физикальный осмотр, включающий пальпацию яичек (7).
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - IV)
2.3 Лабораторная диагностика
- Рекомендуется выполнять: развернутые клинический и биохимический анализы крови, онкомаркеры АФП, ХГЧ и ЛДГ, исследование свертывающей системы крови, анализ мочи (7).
Уровень убедительности рекомендаций - A (уровень достоверности доказательств - Ia).
2.4 Инструментальная диагностика
- Рекомендовано выполнение УЗИ яичек (датчик 7,5 МГц), позволяющий непосредственно визуализировать опухоль (7).
Уровень убедительности рекомендаций - B (уровень достоверности доказательств - IIb)
- Рекомендуется выполнить КТ органов грудной клетки, брюшной полости и малого таза с внутривенным контрастированием (7).
Уровень убедительности рекомендаций - B (уровень достоверности доказательств - III)
Комментарии: КТ органов брюшной полости и грудной клетки является стандартом уточняющей диагностики при герминогенных опухолях яичка, забрюшинного пространства и средостения в большинстве развитых стран. На практике данные исследования могут быть отчасти заменены УЗИ органов брюшной полости и рентгенографией грудной клетки в двух проекциях).
- Рекомендуется выполнить МРТ головного мозга с внутривенным контрастированием при высоком уровне ХГЧ (свыше 50000 мМЕ/мл или множественных метастазах в легкие) в связи с высоким риском метастатического поражения головного мозга (8).
Уровень убедительности рекомендаций - B (уровень достоверности доказательств - III)
- Рекомендуется выполнить остеосцинтиграфию при подозрении на метастатическое поражение костей скелета (7).
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - IV)
- Рекомендуется выполнить биопсию под контролем УЗИ/КТ при внегонадной локализации первичной опухоли (7).
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - IV)
2.5 Иная диагностика
- Рекомендуется гистологическое исследование хирургически удаленного опухолевого препарата, при этом в морфологическом заключении рекомендуется отразить следующие параметры:
1. Гистологическое строение опухоли в соответствие с действующей классификацией ВОЗ. Желательно указание доли каждого компонента опухоли;
2. Размеры опухоли;
3. pT (наличие или отсутствие лимфоваскулярной инвазии, распространение в rete testis, оболочки яичка, семенной канатик);
4. pN (с указанием общего числа исследованных и пораженных лимфоузлов);
5. Наличие поражения края резекции семенного канатика (отрицательный результат также должен быть констатирован);
6. Наличие лечебного патоморфоза (если ранее проводилась химиотерапия) (7).
Уровень убедительности рекомендаций B (уровень достоверности доказательств - IIa).
Комментарии: при семиноме не может быть повышенного уровня АФП. В последнем случае, несмотря на гистологическое заключение, лечение должно осуществляться, как при несеминомных опухолях. Высокий (свыше 200 мМЕ/мл) уровень ХГЧ также позволяет заподозрить наличие несеминомного компонента, и данные опухоли также лучше лечить по принципам несеминомных. Возможно выполнение биопсии здорового контралатерального яичка, особенно при его атрофии (объем < 12 мл) в молодом возрасте (до 30 лет). В этом случае риск ВГННТ (внутрипротоковая герминогенная неоплазия неклассифицированного типа, ранее - carcinoma in situ) достигает 33% (9).
3. Лечение
3.1 Консервативное лечение
В качестве консервативного лечения рекомендуется химиотерапия, включающая препараты цисплатин, этопозид, блеомицин, карбоплатин, ифосфамид, паклитаксел, гемцитабин, оксалиплатин. Выбор препаратов, их комбинации и число курсов в зависимости от стадии представлено в разделе 3.4.
3.2 Хирургическое лечение
Хирургическое лечения при герминогенных опухолях в зависимости от клинической ситуации может включать орхофуникулэктомию, забрюшинную лимфаденэктомию, удаление опухоли средостения, резекции легких, печени. Показания к каждому вмешательству в зависимости от стадии заболевания представлено в разделе 3.4.
3.3 Лучевая терапия
- Лучевая терапия (дистанционная лучевая терапия, стереотаксическая лучевая терапия) рекомендуется к применению в лечении герминогенных опухолей редко. Показания к применению, поля облучения и дозы в зависимости от стадии заболевания представлены в разделе 3.4.
3.4 Выбор метода лечения в зависимости от стадии заболевания
3.4.1 I стадия заболевания (T1-T4N0M0, нормализация маркеров после ОФЭ)
- При герминогенных опухолях яичка I стадии на первом этапе рекомендуется выполнение ОФЭ.
Уровень убедительности рекомендаций - A (уровень достоверности доказательств - Ia)
Комментарии: показания к проведению адъювантной химиотерапии определяются факторами риска развития рецидива, возможностью и желанием пациента к интенсивному наблюдению в случае отказа от химиотерапии. Важнейший фактор риска при несеминомных опухолях I стадии: наличие лимфоваскулярной инвазии. Пациенты с опухолевой инвазией в сосуды имеют риск развития рецидива около 50%, тогда как без инвазии - около 20% (10).
- При отсутствии инвазии рекомендуется наблюдение. Больным с наличием опухолевой инвазии в сосуды яичка рекомендуется проведение 1 курса химиотерапии комбинацией ВЕР. Это позволяет достигнуть 5-летней безрецидивной и общей выживаемости 97% и 99%, соответственно (11). Тем больным, которые отказываются от наблюдения или адъювантной химиотерапии, может быть предложено выполнение профилактической нервосберегающей забрюшинной лимфаденэктомии (НС-ЗЛАЭ) (12) (7).
Уровень убедительности рекомендаций - B (уровень достоверности доказательств - IIa)
- При семиноме факторами риска являются размер первичной опухоли свыше 4 см, инвазия в rete testis. Рекомендуется динамическое наблюдение, которое должно проводиться по определенному протоколу на протяжении не менее 5 лет (7).
Уровень убедительности рекомендаций - B (уровень достоверности доказательств - IIa)
Комментарии: при невозможности/нежелании наблюдения показано проведение адъювантной терапии по одному из вариантов, обладающих равной эффективностью:
- лучевая терапия на парааортальные лимфоузлы (СОД 20Гр) и
- адъювантная химиотерапия карбоплатином (1 курс в дозе AUC7).
- В случае, когда планируется проведение химиотерапии, рекомендуется обсудить с пациентом необходимость криоконсервации спермы. Процедура должна быть выполнена до проведения химиотерапии.
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - IV)
3.4.2 Лечение распространенных стадий заболевания (II - III стадии герминогенных опухолей яичка, все первичные внегонадные злокачественные герминогенные опухоли)
- На первом этапе с диагностической и лечебной целью рекомендуется выполнение ОФЭ. Основным видом лечения является химиотерапия. Выбор терапии осуществляется на основе прогностической классификации IGCCCG. Больным с благоприятным прогнозом показано проведение 3 курсов ВЕР или 4 курса ЕР (см. таблицу 1) (13). Больные с промежуточным и неблагоприятным прогнозом согласно классификации IGCCCG должны получить 4 курса химиотерапии комбинацией BEP (7).
Уровень убедительности рекомендаций - A (уровень достоверности доказательств - Ia)
Комментарии: альтернатива режиму ВЕР - 4 курса комбинацией PEI (см. таблицу 1 с режимами химиотерапии).
Зрелая тератома при нормальных уровнях АФП и ХГЧ: в таких ситуациях показано выполнение радикального хирургического вмешательства, проведение химиотерапии не требуется.
3.4.3 Принципы проведения химиотерапии
- Все циклы химиотерапии рекомендуется проводить каждые 3 недели (считая от начала предыдущего курса химиотерапии). Возможна задержка очередного курса лечения при наличии инфекции, нейтропении менее 500/мкл или тромбоцитопении менее 50000/мкл в первый день планируемого курса (см. таблицу редукции доз препаратов). Если при проведении предыдущего курса химиотерапии отмечена фебрильная нейтропения, нейтропения IV степени длительностью свыше 7 дней или осложненная инфекцией, обосновано профилактическое назначение Г-КСФ при проведении всех последующих курсов химиотерапии.
- в связи с высоким риском развития венозных тромбозов, пациентам с метастатическим поражением забрюшинных лимфоузлов свыше 3,5 см и (или) неблагоприятным прогнозом по IGCCCG во первой линии терапии рекомендуется профилактическое применение антикоагулянтов (при отсутствии противопоказаний)
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - IV)
- У пациентов в тяжелом общем состоянии, обусловленном распространенностью опухолевого процесса, первый курс рекомендуется проводить в редуцированном виде (например, этопозид и цисплатин в течение двух дней) (14).
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - IV)
3.4.4 Лечение особых категорий больных
А. Метастатическое поражение головного мозга
На первом этапе таким больным рекомендуется проведение 4 курсов химиотерапии по программе ВЕР или PEI. При достижении полного эффекта в головном мозге дальнейшее лечение не показано. В связи с редкостью и отсутствием исследований значение локальных методов (лучевая терапия, хирургия) в отношении резидуальных метастазов в головном мозге до конца не определено. В недавнем большом ретроспективном анализе было показано, что хирургия или лучевая терапия улучшали выживаемость лишь при добавлении к химиотерапии второй-третьей, но не первой линии химиотерапии (16).
Б. Тяжелое (статус ECOG 3 - 4) состояние первичных пациентов вследствие массивной распространенности опухолевого процесса
Проведение первого курса химиотерапии у таких больных сопряжено с высокой частотой осложнений (распад опухоли, кровотечение, инфекция). Особенно это характерно для метастатической хориокарциномы, когда уровень ХГЧ превышает 50000 мМЕ/мл. По этой причине с целью стабилизации состояния пациента в качестве первого курса рекомендуется проведение редуцированного на 40 - 60% курса ЕР с дробным введением препаратов или монотерапия карбоплатином AUC 7 с последующим профилактическим назначением Г-КСФ. После улучшения состояния пациента, обычно отмечаемого в течение первой недели, проводится весь запланированный объем химиотерапии в соответствие с прогнозом IGCCCG (14).
3.4.5 Оценка эффекта, лечение после завершения химиотерапии
- Рекомендуется перед каждым курсом химиотерапии определять опухолевые маркеры, по окончании химиотерапии - повторить КТ исходных зон поражения (7).
Уровень убедительности рекомендаций - B (уровень достоверности доказательств - IIa)
- Несеминомные опухоли: остаточные образования после окончания химиотерапии размерами свыше 1 см рекомендуется удалить (7).
Уровень убедительности рекомендаций - B (уровень достоверности доказательств - IIa)
Комментарии: оптимальное время выполнения хирургического вмешательства - 4 - 6 недель после завершения химиотерапии. В случае поражения нескольких анатомических областей хирургическое лечение начинается с зоны максимального поражения. Больные с полным регрессом, либо те, у которых в резецированной резидуальной опухоли обнаружены некроз или тератома, подлежат наблюдению. При наличии в радикально резецированной опухоли жизнеспособной злокачественной опухоли рекомендуется проведение 2 курсов химиотерапии по программе TIP.
- Семинома: резидуальные метастазы < 3 см или полная регрессия - рекомендуется наблюдение. При резидуальных метастазах > 3 см рекомендуется выполнение ПЭТ-КТ не ранее, чем через 8 недель после завершения химиотерапии. При повышенном накоплении РФП рекомендуется хирургическое лечение, при отсутствии накопления - наблюдение (17) (7).
Уровень убедительности рекомендаций - B (уровень достоверности доказательств - IIb)
3.4.6 Лечение рецидивов герминогенных опухолей
- Перед началом химиотерапии рецидива необходимо исключить синдром "растущей зрелой тератомы" - появление или увеличение в размерах метастазов на фоне снижающихся/нормальных опухолевых маркеров. В данной ситуации показано хирургическое лечение в виде резекции метастазов или, при невозможности, их биопсии (14).
Уровень убедительности рекомендаций - B (уровень достоверности доказательств - IIa)
- В качестве химиотерапии рецидива рекомендуются к применению комбинации на основе ифосфамида и цисплатина (см. Приложение Г)
Уровень убедительности рекомендаций - B (уровень достоверности доказательств - IIa)
Комментарии: наиболее оптимальный режим - TIP, позволяющий добиться длительной выживаемости у 25% больных с несеминомной опухолью и у половины пациентов с семиномой (18) (19). Альтернативой могут служить режимы PEI (особенно если пациент не получал в первой линии терапии этопозид) и VeIP (20). Обычно проводится 4 цикла. Не показано преимущество того или иного режима в качестве второй линии терапии. Применение высокодозной химиотерапии с поддержкой костномозгового кроветворения достоверно не улучшает результаты лечения, однако может применяться в центрах, имеющих опыт ее проведения.
- После завершения химиотерапии рекомендуется хирургическое удаление всей резидуальной опухоли.
Уровень убедительности рекомендаций - B (уровень достоверности доказательств - IIa)
- В случае роста маркеров несмотря на проводимую терапию, исчерпанности возможностей химиотерапии, локализации опухоли в одной анатомической области рекомендуется ее удаление.
Уровень убедительности рекомендаций - B (уровень достоверности доказательств - III)
Комментарии: этот подход дает шанс спасти около 25% пациентов, особенно с поздними рецидивами, умеренно повышенным уровнем АФП и забрюшинной локализацией резидуальной опухоли. При бурном прогрессировании с ростом ХГЧ оперативное лечение бессмысленно.
- В лечении поздних рецидивов (после 2 лет по окончании предшествующей химиотерапии) в случае возможности выполнения R0-резекции рекомендуется хирургическое лечение.
Уровень убедительности рекомендаций - B (уровень достоверности доказательств - III)
Комментарии: доля поздних рецидивов от общего числа рецидивов не превышает 5%. Особенностью поздних рецидивов является низкая чувствительность к химиотерапии, что позволяет рекомендовать в случае потенциально резектабельных опухолей на первом этапе выполнять хирургическое лечение даже в случае повышенных маркеров. При невозможности радикального удаления опухоли и повышенных маркерах необходимо начинать химиотерапию второй линии с последующим выполнением операции.
4. Реабилитация
- Рекомендуется проводить реабилитацию, ориентируясь на общие принципы реабилитации пациентов после проведенных хирургических вмешательств и/или химиотерапии (7).
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - IV)
5. Профилактика
Учитывая высокую курабельность герминогенных опухолей и длительную ожидаемую продолжительность жизни пациентов, необходима профилактика и ранняя диагностика поздних осложнений химиотерапии (сердечно-сосудистых заболеваний, метаболический синдром, гипогонадизм, инфертильность, легочная токсичность и др.) с привлечением соответствующих профильных специалистов (14).
5.1 Наблюдение при I стадии несеминомы с динамическим наблюдением (химиотерапия не проводилась)
- Рекомендован следующий график наблюдения:
- физикальный осмотр, опухолевые маркеры - ежемесячно в первый год, каждые 2 месяца во второй год, каждые 3 месяца в третий год, каждые 4 месяца в четвертый год, каждые 6 месяцев в пятый год, далее - ежегодно (14);
- УЗИ органов брюшной полости, забрюшинного пространства и пахово-подвздошных областей - каждые 2 месяца в первый год, каждые 3 месяца - во второй год, каждые 4 месяца - в третий и четвертый годы, далее ежегодно (14);
- рентгенография органов грудной клетки выполняется каждый второй визит (14).
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - IV)
5.2 Наблюдение за пациентами после проведенной химиотерапии, а также при семиноме I стадии
- Рекомендован следующий график наблюдения:
- физикальный осмотр, опухолевые маркеры, УЗИ органов брюшной полости, забрюшинного пространства и паховоподвздошных областей - каждые 2 - 3 месяца в первый год, каждые 3 месяца во второй год, затем каждые 4 месяца в третий и четвертый годы, раз в полгода в пятый год и далее ежегодно (14);
- рентгенография органов грудной клетки - каждый второй визит (14).
Уровень убедительности рекомендаций - B (уровень достоверности доказательств - III)
6. Дополнительная информация, влияющая на течение и исход заболевания
Отсутствует.
Критерии оценки качества медицинской помощи
N
Критерии качества
Уровень достоверности доказательств
Уровень убедительности рекомендаций
1
Выполнена морфологическая верификация диагноза до начала лечения, за исключением случаев тяжелого состояния пациента
IV
C
2
До ОФЭ и после нее определены уровни АФП, ХГЧ и ЛДГ
Ia
A
3
При I стадии в патоморфологическом заключении содержится заключение о наличии или отсутствии сосудистой инвазии, прорастание в сеть яичка
Ia
A
3
Адъювантная химиотерапия начата в течение 4 недель после ОФЭ (при наличии показаний и отсутствии противопоказаний)
III
A
4
Пациенту предложена криопрезервация спермы до начала химиотерапии
IV
C
5
Оценена прогностическая группа по IGCCCG перед началом химиотерапии первой линии в случае распространенного опухолевого процесса
Ia
A
6
Проведен следующий курс полихимиотерапии не позднее 22 дня от момента начала предыдущего курса полихимиотерапии (при отсутствии медицинских противопоказаний)
II
A
7
Выполнено удаление резидуальной опухоли при несеминоме
IIa
B
Список литературы
1. Sharpe RM, Skakkebaek NE. Are oestrogens involved in falling sperm counts and disorders of the male reproductive tract? Lancet 1993, 341: 1392 - 1395.
2. Garner, M. J., Turner, M. C., Ghadirian, P. & Krewski, D. Epidemiology of testicular cancer: an overview. [book auth.]. Int. J. Cancer (2005) 116 331-339.
3. Chieffi P, Franco R, Portella G. Molecular and cell biology of testiculargerm cell tumors. Int Rev Cell Mol Biol 2009; 278: 277 - 308.
4. Hemminki K, Chen B. Familial risks in testicular cancer as aetiological clues.. Int J Androl. 2006 Feb; 29(1): 205-10.
5. Ferlay J, Steliarova-Foucher E, Lortet-Tieulent J, et al. Cancer incidence and mortality patterns in Europe: estimates for 40 countries in 2012. Eur J Cancer. 2013 Apr; 49(6): 1374-403.
6. International Germ Cell Collaborative Group.. International Germ Cell Consensus Classification: A prognostic Factor-Based Staging System for Metastatic Germ Cell Cancers. J. Clin Oncol, 1997, 15: pp 594 - 603.
7. J. Oldenburg, S. D. ![]() , J. Nuver, et al. Testicular seminoma and non-seminoma: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Annals of Oncology 24 (Supplement 6): vi125 - vi132, 2013.
, J. Nuver, et al. Testicular seminoma and non-seminoma: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Annals of Oncology 24 (Supplement 6): vi125 - vi132, 2013.
8. Трякин А.А., Федянин М.Ю., Буланов А.А., с соавт. Метастазы герминогенных опухолей в головной мозг. Опыт Российского онкологического центра. Онкоурология, 2013 (4): с. 5971.
9. Harland SJ, Cook PA, Fossa SD, et al. Intratubular germ cell neoplasia of the contralateral testis in testicular cancer: defining a high risk group. J Urol. 1998 Oct; 160(4): 1353-7.
10. C. Kollmannsberger, T. Tandstad, P. Bedard, et al. Characterization of relapse in patients with clinical stage I (CSI) nonseminoma (NS-TC) managed with active surveillance (AS): A large multicenter study. J Clin Oncol 31, 2013 (suppl; abstr 4503).
11. Tandstad T., Cavallin-Stahl E., Dahl O, et al. One course of adjuvant BEP in clinical stage I, nonseminoma: Mature and expanded results from the SWENOTECA group. J Clin Oncol 31, 2013 (suppl; abstr 4553).
12. Albers, P. Randomized phase III trial comparing retroperitoneal lymph node dissection with one course of bleomycin and etoposide plus cisplatin chemotherapy in the adjuvant treatment of clinical stage I NSGCT: AUO trial AH 01/94 by the German Testicular Cancer Study. J Clin Oncol. - 2008. - 26(18). - P. 2966-72.
13. de Wit, R, J.T. Roberts, P.M. Wilkinson et al. Equivalence of Three or Four Cycles of Bleomycin, Etoposide, and Cisplatin Chemotherapy and of a 3- or 5-Day Schedule in Good-Prognosis Germ Cell Cancer: A randomized trial of EORTC and MRC/.//J Clin Oncol. - 2001. - P. 1629 - 1640.
14. А.А., Трякин. Лекарственное и комбинированное лечение несеминомных герминогенных опухолей у мужчин. Диссертация ... доктора медицинских наук: 14.00.12.; [Место защиты: ФГБУ "НМИЦ онкологии им. Н.Н. Блохина" Минздрава России] - Москва, 2015. - 254 с.
15. Трякин А.А., Гладков О.А., Матвеев В.Б. с соавт. Практические рекомендации по лекарственному лечению герминогенных опухолей яичка. Злокачественные опухоли. - 2016. - N 4, спецвыпуск 2, - С. 353 - 366.
16. Feldman DR, Lorch A, Kramar A, et al. Brain Metastases in Patients With Germ Cell Tumors: Prognostic Factors and Treatment Options-An Analysis From the Global Germ Cell Cancer Group. J Clin Oncol. 2016 Feb 1; 34(4): 345-51.
17. De Santis M, Becherer A, Bokemeyer C et al. 2-18Fluoro-deoxy-d-glucose positron emission tomography is a reliable predictor for viable tumor in postchemotherapy seminoma: an update of the prospective multicentric SEMPET trial. J Clin Oncol 2004; 22: 1034 - 1039.
18. Motzer RJ, Sheinfeld J, Mazumdar M, et al. Paclitaxel, Ifosfamide, and Cisplatin Second-Line Therapy for Patients With Relapsed Testicular Germ Cell Cancer. J Clin Oncol, 2000, 18, (12): 2413 - 2418.
19. Mead GM, Cullen MH, Huddart R, et al. A phase II trial of TIP (paclitaxel, ifosfamide and cisplatin) given as second-line (post-BEP) salvage chemotherapy for patients with metastatic germ cell cancer: a medical research council trial. Br J Cancer 2005; 93: 178 - 184..
20. P.J. Loehrer, R. Gonin, C.R. Nichols, et al. Vinblastine plus ifosfamide plus cisplatin as initial salvage therapy in recurrent germ cell tumor. J Clin Oncol, 16 (1998), pp. 2500 - 2504.
Приложение А1
СОСТАВ РАБОЧЕЙ ГРУППЫ
1. Гладков О.А., профессор, д.м.н., ООО "ЭВИМЕД", г. Челябинск.
Конфликт интересов: отсутствует.
2. Матвеев В.Б., профессор, д.м.н., заведующий отделением урологии ФГБУ "НМИЦ онкологии им. Н.Н. Блохина" Минздрава России
Конфликт интересов: отсутствует.
3. Моисеенко Ф.В., д.м.н., заведующий отделением химиотерапии ГБУЗ "Санкт-Петербургский клинический научно-практический центр специализированных видов медицинской помощи (онкологический)", г. Санкт-Петербург
Конфликт интересов: отсутствует.
4. Полоцкий Б.Е., профессор, д.м.н., зам. главного врача по онкологии "Клиника МЕДСИ на Пятницком шоссе"
Конфликт интересов: отсутствует.
5. Проценко С.А., профессор, д.м.н., заведующая отделением химиотерапии ФГБУ "НИИ онкологии им. Н.Н. Петрова" Минздрава России, г. Санкт-Петербург.
Конфликт интересов: отсутствует.
6. Трякин А.А., д.м.н., главный научный сотрудник отделения клинической фармакологии и химиотерапии ФГБУ "НМИЦ онкологии им. Н.Н. Блохина" Минздрава России
Конфликт интересов: отсутствует.
7. Тюляндин С.А., профессор, д.м.н., заведующий отделением клинической фармакологии и химиотерапии ФГБУ "НМИЦ онкологии им. Н.Н. Блохина" Минздрава России;
Конфликт интересов: отсутствует.
8. Федянин М.Ю., д.м.н., старший научный сотрудник отделения клинической фармакологии и химиотерапии ФГБУ "НМИЦ онкологии им. Н.Н. Блохина" Минздрава России.
Конфликт интересов: отсутствует.
Приложение А2
МЕТОДОЛОГИЯ РАЗРАБОТКИ КЛИНИЧЕСКИХ РЕКОМЕНДАЦИЙ
Целевая аудитория данных клинических рекомендаций:
1. Врачи-онкологи;
2. Врачи-урологи;
3. Врачи-хирурги;
4. Врачи-радиологи;
5. Врачи-радиотерапевты;
6. Врачи-детские онкологи;
7. Врачи-генетики;
8. Студенты медицинских ВУЗов, ординаторы и аспиранты.
Методы, использованные для сбора/селекции доказательств: поиск в электронных базах данных; анализ современных научных разработок по проблеме герминогенных опухолей в РФ и за рубежом; обобщение практического опыта российских и зарубежных специалистов.
Таблица П1 - Уровни достоверности доказательств в соответствии с классификацией Агентства по политике медицинского обслуживания и исследований (AHCPR, 1992)
Уровни достоверности доказательств
Описание
Ia
Доказательность, основанная на мета-анализе рандомизированных контролируемых исследований
Ib
Доказательность, основанная как минимум на одном рандомизированном контролируемом исследовании с хорошим дизайном
IIa
Доказательность, основанная как минимум на одном крупном нерандомизированном контролируемом исследовании
IIb
Доказательность, основанная как минимум на одном квазиэкспериментальном исследовании с хорошим дизайном
III
Доказательность, основанная на неэкспериментальных описательных исследованиях с хорошим дизайном, типа сравнительных исследований, корреляционных исследований и исследований случай-контроль
IV
Доказательность, основанная на мнении экспертов, на опыте или мнении авторов
Таблица П2 - Уровни убедительности рекомендаций в соответствии с классификацией Агентства исследований и оценки качества медицинского обслуживания (AHRQ, 1994)
Уровень убедительности рекомендации
Уровни достоверности доказательств
Описание
A
Ia, Ib
Доказательность, основанная как минимум на одном рандомизированном контролируемом исследовании с хорошим дизайном
B
IIa, IIb, III
Доказательность, основанная на хорошо выполненных нерандомизированных клинических исследованиях
C
IV
Доказательность, основанная на мнении экспертов, на опыте или мнении авторов. Указывает на отсутствие исследований высокого качества
Методы, использованные для формулирования рекомендаций - консенсус экспертов.
Экономический анализ
Анализ стоимости не проводился и публикации по фармакоэкономике не анализировались.
Метод валидизации рекомендаций:
- Внешняя экспертная оценка;
- Внутренняя экспертная оценка
Описание метода валидизации рекомендаций:
Настоящие рекомендации в предварительной версии рецензированы независимыми экспертами, которые попросили прокомментировать, прежде всего, насколько интерпретация доказательств, лежащих в основе рекомендаций, доступна для понимания.
Получены комментарии со стороны врачей-онкологов и урологов первичного звена в отношении доходчивости изложения рекомендаций и их оценки важности рекомендаций как рабочего инструмента повседневной практики.
Комментарии, полученные от экспертов, тщательно систематизировались и обсуждались председателем и членами рабочей группы. Каждый пункт обсуждался и вносимые в результате этого изменения в рекомендации регистрировались. Если же изменения не вносились, то регистрировались причины отказа от внесения изменений.
Консультации и экспертная оценка: Проект рекомендаций рецензирован также независимыми экспертами, которых попросили прокомментировать, прежде всего, доходчивость и точность интерпретации доказательной базы, лежащей в основе рекомендаций.
Для окончательной редакции и контроля качества рекомендации повторно проанализированы членами рабочей группы, которые пришли к заключению, что все замечания и комментарии экспертов приняты во внимание, риск систематических ошибок при разработке рекомендаций сведен к минимуму.
Обновления клинических рекомендаций: актуализация проводится не реже чем один раз в три года с учетом появившейся новой информации о диагностике и тактике ведения мужчин с герминогенными опухолями. Решение об обновлении принимает МЗ РФ на основе предложений, представленных медицинскими профессиональными некоммерческими организациями. Сформированные предложения должны учитывать результаты комплексной оценки лекарственных препаратов, медицинских изделий, а также результаты клинической апробации.
При отборе публикаций, как потенциальных источников доказательств, использованная в каждом исследовании методология изучается для того, чтобы убедиться в ее достоверности. Результат изучения влияет на уровень доказательств, присваиваемый публикации, что в свою очередь влияет на силу, вытекающих из нее рекомендаций.
Приложение А3
СВЯЗАННЫЕ ДОКУМЕНТЫ
КР400. Хронический болевой синдром (ХБС) у взрослых пациентов, нуждающихся в паллиативной медицинской помощи (http://cr.rosminzdrav.ru/#!/schema/708)
Приложение Б
АЛГОРИТМЫ ВЕДЕНИЯ ПАЦИЕНТА
Алгоритм ведения пациента с подозрением на герминогенную опухоль (с образованием в яичке)
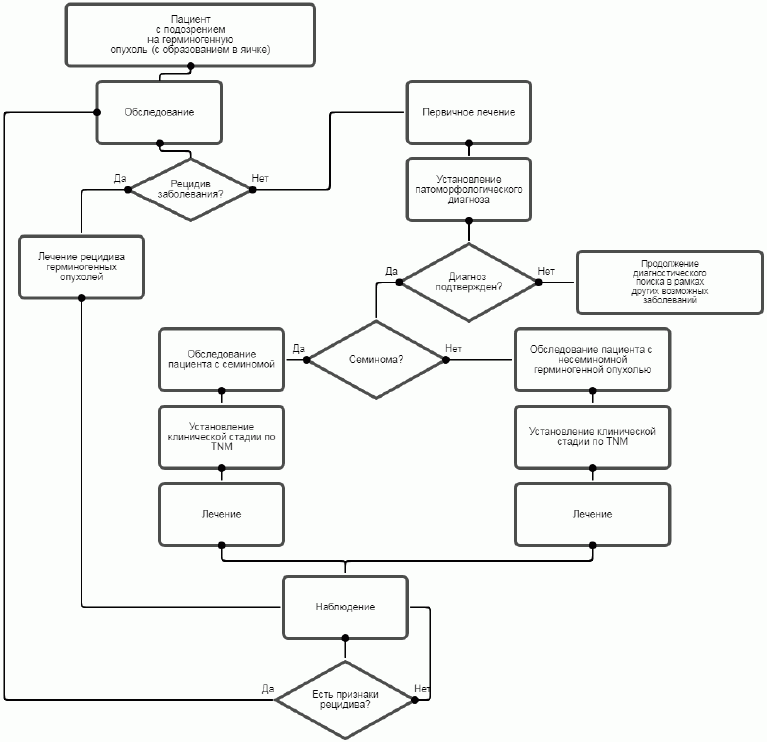
Приложение В
ИНФОРМАЦИЯ ДЛЯ ПАЦИЕНТОВ
Рекомендации при осложнениях химиотерапии - связаться с химиотерапевтом.
1) При повышении температуры тела 38 °C и выше:
- Рекомендовано применение прием противомикробной терапии по рекомендации химиотерапевта.
2) При стоматите:
- Диета - механическое, термическое щажение;
- Частое полоскание рта (каждый час) - ромашка, кора дуба, шалфей, смазывать рот облепиховым (персиковым) маслом;
- Обрабатывать полость рта по рекомендации химиотерапевта.
3) При диарее:
- Диета - исключить жирное, острое, копченое, сладкое, молочное, клетчатку. Можно нежирное мясо, мучное, кисломолочное, рисовый отвар. Обильное питье;
- Принимать препараты по рекомендации химиотерапевта.
4) При тошноте:
- Принимать препараты по рекомендации химиотерапевта.
Приложение Г
Режим
Препараты
Введение
Дни лечения
Показания
EP
Этопозид 100 мг/м2
в/в, 40 мин.
1 - 5 дни
4 курса - благоприятный прогноз (при противопоказаниях к блеомицину), длительность курса - 21 день
Цисплатин <**> 20 мг/м2
в/в, 1 час
1 - 5 дни
BEP
Блеомицин 30 мг
в/в, 2 - 20 мин.
1, 3, 5 дни
3 курса - благоприятный прогноз, 4 курса - промежуточный/неблагоприятный прогноз, длительность курса - 21 день
Этопозид 100 мг/м2
в/в, 40 мин.
1 - 5 дни
цисплатин <**> 20 мг/м2
в/в, 1 час
1 - 5 дни
PEI
этопозид 75 мг/м2
в/в, 40 мин.
1 - 5 дни
4 курса - промежуточный/неблагоприятный прогноз (при противопоказаниях к блеомицину как альтернатива ВЕР), длительность курса - 21 день
ифосфамид 1200 мг/м2
в/в, 1 - 2 часа
1 - 5 дни
цисплатин <**> 20 мг/м2
в/в, 1 час
1 - 5 дни
месна <*>
в/в,
струйно <*>
1 - 5 дни
Режимы второй линии химиотерапии
TIP
ифосфамид 1500 мг/ м2
в/в, 1 - 2 часа
2 - 5 дни
4 курса - предпочтительный режим второй линии, длительность курса - 21 день
цисплатин <**> 25 мг/м2
в/в, 1 час
2 - 5 дни
месна <*>
в/в,
струйно <*>
2 - 5 дни
паклитаксел# 175 мг/м2
в/в, 3 часа
1 день
филграстим 5 мкг/кг
п/к
6 - 15 дни
VeIP
ифосфамид 1200 мг/м2
месна
в/в, 1 - 2 часа
в/в,
струйно <*>
1 - 5 дни
1 - 5 дни
4 курса - стандартный режим второй линии, длительность курса - 21 день
цисплатин <**> 20 мг/м2
в/в, 1 час
1 - 5 дни
винбластин 0,11 мг/кг
в/в струйно
1, 2 дни
филграстим 5 мкг/кг
п/к
6 - 15 дни
Режимы третьей линии химиотерапии
TGO
паклитаксел# 80 мг/ м2
в/в, 1 час
1, 8 дни
4 курса, длительность курса - 21 день
гемцитабин# 800 мг/
в/в, 30 мин.
1, 8 дни
оксалиплатин# 130 мг/м2
в/в, 2 часа
1 день
GemOX
Гемцитабин# 1000 мг/м2
в/в, 30 мин
1, 8 дни
4 курса, длительность курса - 21 день
Оксалиплатин# 130 мг/м2
в/в, 2 часа
1 день
--------------------------------
<**> Введение цисплатина осуществляется на фоне внутривенной гидратации физиологическим раствором хлорида натрия (суммарный суточный объем 2,5 л), необходимой для поддержания диуреза > 100 мл/час в процессе введения цисплатина и в последующие 3 часа.
<*> Месна применяется в суточной дозе, составляющей 100% от дозы ифосфамида и разделенной на три введения в течение дня: непосредственно перед ифосфамидом и далее через 4 и 8 часов после начала его инфузии.
Алгоритм редукции доз химиопрепаратов в зависимости от гематологической токсичности <*> (15)
Число тромбоцитов, x 109/л
> 100
75 - 99
50 - 74
Число нейтрофилов, x 109/л
этопозид
цисплатин
этопозид
цисплатин
этопозид
цисплатин
>= 1,0
100%
100%
75%
100%
50%
100%
0,5 - 0,99
100%
100%
50%
100%
отсрочка на 4 дня
< 0,5
отсрочка на 4 дня
отсрочка на 4 дня
отсрочка на 4 дня
--------------------------------
<*> Определяется по анализам на день начала очередного курса химиотерапии, указан % дозы преп.
