<Письмо> Минздрава России от 07.11.2018 N 15-4/10/2-7235
МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ
ПИСЬМО
от 7 ноября 2018 г. N 15-4/10/2-7235
Министерство здравоохранения Российской Федерации направляет клинические рекомендации (протокол лечения) "Доброкачественная дисплазия молочной железы", разработанные в соответствии со статьей 76 Федерального закона от 21 ноября 2011 г. N 323-ФЗ "Об основах охраны здоровья граждан в Российской Федерации", для использования в работе руководителями органов исполнительной власти субъектов Российской Федерации в сфере здравоохранения при подготовке нормативных правовых актов, руководителями медицинских организаций акушерско-гинекологического профиля, а также для использования в учебном процессе.
С.А.КРАЕВОЙ
Приложение
Утверждаю
Президент Российского общества
акушеров-гинекологов
академик РАН, профессор
В.Н.СЕРОВ
2 ноября 2018 г.
Согласовано
Главный внештатный специалист
Министерства здравоохранения
Российской Федерации
По акушерству и гинекологии
Академик РАН профессор
Л.В.АДАМЯН
2 ноября 2018 г.
ДОБРОКАЧЕСТВЕННАЯ ДИСПЛАЗИЯ МОЛОЧНОЙ ЖЕЛЕЗЫ
КЛИНИЧЕСКИЕ РЕКОМЕНДАЦИИ (ПРОТОКОЛ ЛЕЧЕНИЯ)
Состав Рабочей группы
Адамян Лейла Владимировна - заместитель директора ФГБУ "Национальный медицинский исследовательский центр акушерства, гинекологии и перинатологии имени академика В.И. Кулакова" Минздрава России, главный внештатный акушер-гинеколог Минздрава России, заведующая кафедрой репродуктивной медицины и хирургии ФГБОУ ВО "Московский государственный медико-стоматологический университет им. А.И. Евдокимова" Минздрава России, заслуженный деятель науки России, академик РАН, д.м.н., профессор.
Андреева Елена Николаевна - заместитель директора ФГБУ "Национальный медицинский исследовательский центр эндокринологии" Минздрава России - директор института репродуктивной медицины, профессор кафедры эндокринологии Института высшего и постдипломного образования ФГБУ "Национальный медицинский исследовательский центр эндокринологии" Минздрава России, профессор кафедры репродуктивной медицины и хирургии ФГБОУ ВО "Московский государственный медико-стоматологический университет имени А.И. Евдокимова" Минздрава России, д.м.н.
Артымук Наталья Владимировна - заведующая кафедрой акушерства и гинекологии N 2 ФГБОУ ВО "Кемеровский государственный медицинский университет" Минздрава России, главный внештатный специалист Минздрава России по акушерству и гинекологии в Сибирском федеральном округе, д.м.н., профессор, член правления Российского общества акушеров-гинекологов, президент КРОО "Ассоциация акушеров-гинекологов Кузбасса".
Белокриницкая Татьяна Евгеньевна - заведующая кафедрой акушерства и гинекологии ФПК и ППС ФГБОУ ВО "Читинская государственная медицинская академия" Минздрава России, заслуженный врач Российской Федерации, д.м.н., профессор, член Правления Российского общества акушеров-гинекологов, Член совета Ассоциации акушерских анестезиологов-реаниматологов, президент Забайкальского общества акушеров-гинекологов.
Корженкова Галина Петровна - онколог-рентгенолог, старший научный сотрудник ФГБУ "Национальный медицинский исследовательский центр онкологии имени Н.Н. Блохина" Минздрава России, к.м.н.
Протасова Анна Эдуардовна - руководитель центра онкологии клиники Скандинавия, профессор кафедры онкологии ФГБОУ ВО "Санкт-Петербургский государственный университет", профессор кафедры онкологии ФГБОУ ВО "Северо-Западный государственный медицинский имени И.И. Мечникова" Минздрава России, профессор кафедры акушерства и гинекологии ФГБУ "Северо-Западный федеральный медицинский исследовательский центр имени В.А. Алмазова" Минздрава России, д.м.н.
Рожкова Надежда Ивановна - руководитель Национального центра онкологии репродуктивных органов ФГБУ "Московский научно-исследовательский онкологический институт имени П.А. Герцена" Минздрава России, профессор кафедры клинической маммологии, лучевой диагностики и лучевой терапии ФПК МР ФГАОУ ВО "Российский университет дружбы народов", президент Российской ассоциации радиологов, президент Российской ассоциации маммологов, д.м.н., профессор.
Сутурина Лариса Викторовна - руководитель отдела охраны репродуктивного здоровья ФГБНУ "Научный центр проблем здоровья семьи и репродукции человека", профессор кафедры эндокринологии Иркутской государственной медицинской академии последипломного образования - филиала ФГБОУ ДПО "Российская медицинская академия непрерывного профессионального образования" Минздрава России, д.м.н., профессор.
Филиппов Олег Семенович - заслуженный врач Российской Федерации, д.м.н., профессор, заместитель директора Департамента медицинской помощи детям и службы родовспоможения Минздрава России, профессор кафедры акушерства и гинекологии ФППОВ ФГБОУ ВО "Московский государственный медико-стоматологический университет имени А.И. Евдокимова" Минздрава России. Конфликт интересов отсутствует.
Список сокращений
ГК
- гормональные контрацептивы
ДДМЖ
- доброкачественная дисплазия молочной железы
ДЗМЖ
- доброкачественные заболевания молочных желез
МГТ
- менопаузальная гормональная терапия
МКБ-10
- международная классификация болезней десятого пересмотра
МРТ
- магнитно-резонансная томография
НПВС
- нестероидные противовоспалительные средства
РГ-ГТ
- гонадотропин рилизинг-гормон
РМЖ
- рак молочной железы
УЗИ
- ультразвуковое исследование
NB
- Nota Bene - обратить внимание
Введение
Доброкачественные заболевания молочных желез (ДЗМЖ) широко распространены в женской популяции и характеризуются спектром клинически значимых аномалий, выявляемых при использовании инструментальных методов, или в виде пальпируемых образований, которые определяются при физикальном обследовании. Точных данных о распространенности ДЗМЖ нет, однако, по некоторым оценкам, максимальная заболеваемость ДЗМЖ регистрируется в возрасте 40 - 44 лет, достигая 200-400:100 000/год с последующим медленным снижением к 65 годам (34, 37, 72). Некоторые формы ДЗМЖ ассоциированы с повышенным риском развития рака молочной железы РМЖ в будущем (24, 26). В связи с этим оптимизация диагностики и тактики ведения женщин с ДЗМЖ является частью стратегии снижения заболеваемости РМЖ.
В настоящее время в Российской Федерации оказание медицинской помощи при доброкачественных заболеваниях молочных желез и подходы к профилактике рака регламентированы рядом документов, в частности, приказами Минздравсоцразвития России от 15 марта 2006 г. N 154 "О мерах по совершенствованию оказания медицинской помощи при заболеваниях молочной железы" и от 19 августа 2008 г. N 597н "Об организации деятельности центров здоровья по формированию здорового образа жизни у граждан Российской Федерации, включая сокращение потребления алкоголя и табака", приказами Минздрава России от 3 декабря 2012 г. N 1006н "Об утверждении порядка проведения диспансеризации определенных групп взрослого населения", 3 февраля 2015 N 36ан "Об утверждении порядка проведения диспансеризации определенных групп взрослого населения" с изменениями, отраженными в приказе Минздрава России от 9 декабря 2016 г. N 946н "О внесении изменений в порядок проведения диспансеризации определенных групп взрослого населения, утвержденный приказом Министерства здравоохранения Российской Федерации от 3 февраля 2015 г. N 36ан".
К непосредственным обязанностям врача акушера-гинеколога относится оценка риска и раннее выявление как доброкачественных, так и злокачественных заболеваний молочных желез, а также оказание специализированной помощи при ДЗМЖ, включающей лечебные и профилактические подходы.
В данных клинических рекомендациях обобщены и представлены современные подходы к диагностике, дифференциальной диагностике, лечению и профилактике доброкачественной дисплазии молочной железы (ДДМЖ), представлены стратегии раннего выявления и оценки риска РМЖ, которые основаны на принципах доказательной медицины и являются ключевыми в организации своевременного оказания эффективной помощи пациенткам.
В пособии использованы градации достоверности рекомендаций и убедительности доказательств, представленные в приложении 1.
Целевая аудитория данных клинических рекомендаций: врачи акушеры-гинекологи, студенты, ординаторы, аспиранты, преподаватели, научные сотрудники.
1. Определение и классификации
Доброкачественная дисплазия молочной железы (ДДМЖ) характеризуется спектром пролиферативных и регрессивных изменений тканей молочных желез с формированием ненормальных соотношений эпителиального и соединительнотканного компонентов и образованием в молочной железе изменений фиброзного, кистозного, пролиферативного характера, которые часто, но не обязательно, сосуществуют (3).
Синонимы доброкачественной дисплазии молочной железы: "мастопатия", "фиброзно-кистозная мастопатия", "дисгормональная гиперплазия молочных желез", "фиброзно-кистозная болезнь", "доброкачественная болезнь молочной железы", "фиброаденоматоз".
Классы МКБ-10: Болезни молочной железы (N60 - N64)
Таблица 1
Доброкачественная дисплазия молочной железы (N60)
N 60.0
Солитарная киста молочной железы
N 60.1
Диффузная кистозная мастопатия
Исключена: с пролиферацией эпителия (N60.3)
N 60.2
Фиброаденоз молочной железы
Исключена: фиброаденома молочной железы (D24)
N 60.3
Фибросклероз молочной железы
Кистозная мастопатия с пролиферацией эпителия
N 60.4
Эктазия протоков молочной железы
N 60.8
Другие доброкачественные дисплазии молочной железы
N 60.9
Доброкачественная дисплазия молочной железы неуточненная
Гистологическая классификация ДЗМЖ базируется на основе оценки степени клеточной пролиферации и наличия/отсутствия атипии. В соответствии с этим подходом ДДМЖ могут быть классифицированы по трем категориям: непролиферативные, пролиферативные без атипии и с атипичной гиперплазией (36).
NB! Пролиферативная активность эпителия молочной железы варьирует в зависимости от степени дифференцировки долек. Высокий уровень пролиферативной активности наблюдается в недифференцированных дольках 1-го типа, присутствующей в груди молодых нерожавших женщин. В клетках, составляющих дольки типа 1, скорость клеточной пролиферации выше в 3 раза, чем в дольках 2-го типа и в 10 раз выше, чем в дольках 3-го типа (65, 66, 67).
2. Стратификация рисков заболеваний молочных желез
Факторы, которые ассоциированы с повышенным риском ДЗМЖ, представлены в таблице 2.
Таблица 2
Установленные факторы риска ДЗМЖ
Фактор
Характер воздействия
Опубликован о
Ранние факторы риска
Низкий объем массы жировой ткани в детстве и подростковом возрасте
Положительная ассоциация с риском ДЗМЖ
(10)
Высокорослость в 10 лет и быстрый линейный рост в 10 - 18 лет
Положительная ассоциация с риском ДЗМЖ
(14)
Прием алкоголя в возрасте от менархе до первых родов
Положительная ассоциация с риском ДЗМЖ
(12, 50)
Животный жир, мясо (![]() 3 порций в день) в подростковом возрасте
3 порций в день) в подростковом возрасте
Положительная ассоциация с риском ДЗМЖ
(9, 30)
Факторы риска в старшем возрасте
МГТ
Длительность МГТ (более 8 - 15 лет) ассоциирована с увеличением риска ДЗМЖ
(23, 62)
NB! Факторы, влияние которых на риск ДЗМЖ не доказано: вес при рождении, пребывание на грудном вскармливании, физическая активность в подростковом возрасте, менструальная и репродуктивная история, курение с подросткового возраста и гормональная контрацепция (10, 22, 30, 72)
Факторы, которые влияют на риск рака молочной железы, включают возраст, семейный анамнез, репродуктивные факторы и индивидуальные факторы, связанные с образом жизни (таблица 3).
Таблица 3
Установленные факторы риска рака молочной железы
Фактор
Характер воздействия
Опубликовано
Возраст
Риск РМЖ увеличивается с возрастом
(71)
Женский пол
Частота РМЖ в 100 раз чаще у женщин, чем у мужчин
Белая раса
Частота впервые выявленного РМЖ у белых выше, чем у представительниц негроидной расы
(18)
Вес
Увеличение ИМТ ассоциировано с возрастанием риска РМЖ в постменопаузе
(46)
Рост
Высокий рост ассоциирован с увеличением риска РМЖ как в пре-, так и в постменопаузе
(61)
Эстрогены
Высокие уровни эндогенных эстрогенов повышают риск РМЖ в пре- и постменопаузальном возрасте
(27)
ДЗМЖ, пролиферативные формы
Пролиферативные формы (особенно с атипией) ДЗМЖ ассоциированы с повышением риска РМЖ
(26)
Плотность ткани молочной железа при маммографии
Повышенная маммографическая плотность ассоциирована с увеличением риска РМЖ
(43)
Минеральная плотность костей
Повышенная плотность костей по данным денситометрии ассоциирована с увеличением риска РМЖ
(58)
Андрогены
Повышение уровня тестостерона ассоциировано с увеличением риска РМЖ
(42)
Инсулиноподобные факторы роста
IGF1 положительно ассоциирован с риском РМЖ
(28)
Инсулин
Гиперинсулинемия является независимым фактором риска РМЖ
(33)
Внутриутробное воздействие диэтилстильбэстрола
У женщин, подвергавшихся внутриутробно воздействию диэтилстильбэстрола повышен риск РМЖ в возрасте 40 лет и старше
(41)
Возраст менархе
Ранний возраст менархе (13 и менее лет) ассоциирован с увеличением риска рака РМЖ
(61)
Возраст менопаузы, длительность МГТ
Относительный риск РМЖ возрастает на 1,03% с каждым годом отсрочки менопаузы, что сопоставимо с влиянием длительности МГТ
(19)
Роды и возраст при рождении первого ребенка
У рожавших женщин риск РМЖ к 70 годам в целом ниже, чем у нерожавших. При рождении 1-го ребенка в 20 лет риск РМЖ в сравнении с нерожавшими ниже на 20%, в 25 лет - на 10%. Однако при рождении первого ребенка в 35 годам риск РМЖ на 5% выше, чем у нерожавших
(64)
Персональная история РМЖ
Протоковая карцинома in situ или инвазивный РМЖ повышает риск РМЖ контралатеральной МЖ
(5)
Семейная история РМЖ
Риск РМЖ существенно зависит от числа родственниц первой линии с РМЖ
(20)
Мутации генов BRCA1, BRCA2, p53, ATM, and PTEN
5 - 6% РМЖ непосредственно связаны с мутациями данных генов
(44)
Алкоголь
Употребление алкоголя связано с повышением риска РМЖ в сравнении с не употребляющими алкоголь.
(76)
Курение
Умеренное увеличение риска РМЖ у курильщиков
(32)
Воздействие ионизирующей радиации
Воздействие облучения с лечебной целью в раннем возрасте ассоциировано с риском РМЖ
(38)
NB! Факторы, которые НЕ ассоциированы с повышенным риском РМЖ: непролиферативные формы ДЗМЖ, аборт (самопроизвольный и медицинский), химические вещества (диоксины, хлорорганические пестициды), стерилизация маточных труб, кофеин, грудные импланты, электромагнитное поле, электрические одеяла, красители для волос. Также не подтверждена повышение риска РМЖ в связи с работой в ночные часы (15, 31, 39, 49, 60, 70, 74).
Факторы, влияние которых на риск РМЖ окончательно не установлен: бесплодие, диетические факторы (соя/фитоэстрогены, жир, красное и обработанное мясо), факторы окружающей среды (географический регион проживания, воздействие облучения при диагностических исследованиях, пассивное курение).
4. Диагностика заболеваний молочных желез
4.1. Расспрос пациентки и объективное обследование
молочных желез
NB! На данном этапе должны быть идентифицированы факторы риска рака молочной железы.
При анализе жалоб и анамнеза необходимо обращать внимание на наличие таких симптомов, как боль, наличие образований и уплотнений в молочной железе, их локализацию, продолжительность и динамику симптомов с течением времени, а также наличие и цвет самопроизвольных выделений из сосков, если они присутствуют.
Далее необходимо провести тщательный визуальный осмотр груди, в положении пациентки стоя или сидя, при этом руки пациентки должны располагаться на талии. Во время осмотра следует отмечать размер и симметричность молочных желез, наличие покраснений, отека или изменения кожи по типу "апельсиновой корки", выбуханий или смещения сосково-ареолярного комплекса. На следующем этапе проводится пальпация областей подмышечных и надключичных лимфатических узлов и, наконец, пальпация груди (рис. 1). В большинстве руководств рекомендуется исследовать молочную железу пациентки в положении лежа на спине, или сначала в положении сидя, а затем - в положении на спине.

Рис. 1. Варианты последовательной пальпации молочной железы.
В медицинской документации необходимо указывать расположение, размер и консистенцию выявленных образований и уплотнений, связь с кожей и окружающими тканями, расстояние от края ареолы. В ходе объективного обследования оценивается наличие признаков, характерных для РМЖ (таблица 4).
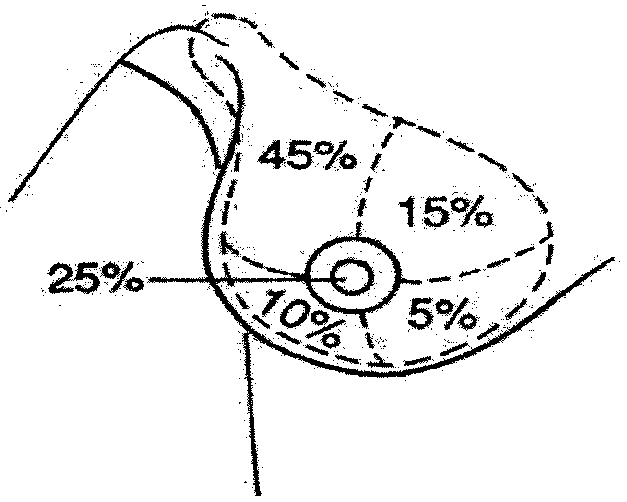
Рис. 2. Частота возникновения злокачественных новообразований в различных участках молочной железы (35).
Таблица 4.
Дифференциальная диагностика образований
в молочных железах (35)
Признак
Клинические особенности
ДЗМЖ
Злокачественная опухоль
Консистенция
Плотная или эластичная
Твердая
Болезненность
Часто
Нет (90%)
Края
Ровные, гладкие
Неровные
Подвижность
Подвижное, смещаемое, не фиксировано
Фиксировано к коже или грудной стенке
Кожа в виде "лимонной корки"
Маловероятно
Высокая вероятность
Выделения из сосков
Двусторонние, без примеси крови, зеленого или желтого цвета
С одной стороны, с кровью
Втянутость соска
Отсутствует
Может быть
В соответствии с рекомендациями NCCN (2017), при отсутствии клинических проявлений заболеваний молочных желез и отсутствии повышенного риска, объективное обследование молочных желез проводится с 25 лет, каждые 1 - 3 года, при этом женщина должна быть осведомлена о необходимости самоконтроля (см. приложение 3) и обращения к врачу при необходимости (54).
NB! Метод объективного обследования молочных желез имеет невысокую чувствительность (54%), но его специфичность составляет 94% (68, 73). Хотя объективное обследование молочных желез при проведении скрининга не обеспечивает снижения смертности от РМЖ, тем не менее, доказано, что его использование позволяет диагностировать РМЖ на более ранних стадиях (47).
4.2. Инструментальные методы диагностики
Основными методами инструментальной диагностики заболеваний молочных желез являются: маммография, ультразвуковое исследование и магнитно-резонансная томография.
Маммография
Диагностическая маммография является основным методом диагностики заболеваний молочной железы, чувствительность метода составляет 85 - 87%, специфичность 91 - 92% (48). В то же время чувствительность и специфичность маммографии существенно снижается при повышенной маммографической плотности ткани молочной железы (11, 53). Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1a).
NB! Цифровая маммография имеет преимущества перед обычной ("film screen") маммографией, благодаря лучшей контрастности изображения, особенно при повышенной маммографической плотности, лучшей визуализации кожи и периферических тканей, возможности хранения и динамической оценки результатов, более низкой дозе облучения (51, 69).
В ныне действующем приказе Минздрава России от 9 декабря 2016 г. N 946н "О внесении изменений в порядок проведения диспансеризации определенных групп взрослого населения, утвержденный приказом Министерства здравоохранения Российской Федерации от 3 февраля 2015 г. N 36ан" проведение маммографии рекомендуется у женщин в возрасте с 39 лет, 1 раз в 2 - 3 года. Целесообразность проведения маммографии в более раннем возрасте и ее кратность лучше определять коллегиально, совместно с онкологом, с учетом клинической ситуации. Согласно международным рекомендациям, при впервые обнаруженных пальпируемых образованиях в молочной железе проведение маммографии рекомендовано у женщин старше 30 лет, хотя в ряде случаев данное исследование может выполняться даже у женщин моложе 30 лет. Так в руководстве NCCN (2017) рассматривается возможность применения диагностической маммографии у женщин моложе 30 лет с впервые выявленными пальпируемыми образованиями в молочной железе при отсутствии изменений по данным ультразвукового исследования (54).
Современные международные рекомендации и алгоритмы скрининга РМЖ представлены в разделе "Скрининг РМЖ".
Дуктография
Введение контрастного препарата в млечные протоки под рентгенологическим контролем (дуктография) используется крайне редко, но полезен для выявления внутрипротоковый образований (68).
Метод ультразвуковой диагностики
УЗИ является незаменимым методом инструментальной диагностики в маммологии и дополняет как маммографию, так и магнитно-резонансное исследование. УЗИ рассматривается в качестве основного инструментального метода оценки состояния молочных желез у женщин молодого возраста, а также беременных и кормящих. Метод используется при дифференциальной диагностике кистозных и солидных образований в молочной железе, при неясной клинико-рентгенологической картине, при контролируемой биопсии/пункции визуализируемых образований, при контроле за эффективностью лечения (40). Дополнительное применение УЗИ при высокой маммографической плотности молочной железы повышает чувствительность маммографии с 50% до 75% (11). Уровень убедительности рекомендаций A (уровень достоверности доказательств 1a).
NB! Проведение УЗИ с допплерографией рекомендуется в качестве дополнительного метода при сомнительных результатах рентгенографии, стандартного УЗИ и пункционной биопсии (17). Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1b).
Магнитно-резонансная томография (МРТ)
МРТ, как правило, не является методом выбора на первом этапе диагностики заболеваний молочных желез, но позволяет получить дополнительную информацию в сложных клинико-диагностических ситуациях. В то же время МРТ является методом выбора при необходимости исследования молочных желез у девочек и молодых женщин, беременных и кормящих.
NB! Для дифференциальной диагностики ДЗМЖ и РМЖ проводится динамическая МРТ с введением контрастного средства. Чувствительность МРТ молочных желез с контрастированием выше, чем чувствительность маммографии, но специфичность ниже, что приводит к большему числу ложно-положительных результатов. Кроме того, микрокальцинаты при МРТ не выявляются.
NB! Вклад МРТ относительно снижения смертности от РМЖ в рандомизированных исследованиях не установлен, поэтому отбор пациентов для дополнительного проведения данного исследования должен проводиться взвешенно. Диагностические МРТ молочных желез целесообразно проводить в учреждениях, где есть условия проведения одновременной биопсии, поскольку поражения, наблюдаемые на МРТ, могут быть не видны при других методах визуализации (56).
Согласно Руководству NCCN (2017) МРТ в качестве скрининга проводится дополнительно к маммографии у следующих категорий женщин (Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1a): носительство мутаций BRCA и у родственниц носительниц BRCA первой линии, которые сами не тестировались, начиная с 25 - 29 лет; риск РМЖ в течение жизни ![]() 20% начиная с 25 - 29 лет (кумулятивный риск РМЖ определяется с использованием компьютерной программы, основанной на модели GAIL, в которой учитываются следующие факторы риска: возраст, возраст менархе, возраст первых родов или их отсутствие, число родственниц первой линии с РМЖ, чисто предшествующих биопсий по поводу ДЗМЖ, атипическая гиперплазия при предыдущей биопсии молочной железы, раса (54), (программа доступна на сайте https://www.cancer.gov/bcrisktool/Default.aspx).
20% начиная с 25 - 29 лет (кумулятивный риск РМЖ определяется с использованием компьютерной программы, основанной на модели GAIL, в которой учитываются следующие факторы риска: возраст, возраст менархе, возраст первых родов или их отсутствие, число родственниц первой линии с РМЖ, чисто предшествующих биопсий по поводу ДЗМЖ, атипическая гиперплазия при предыдущей биопсии молочной железы, раса (54), (программа доступна на сайте https://www.cancer.gov/bcrisktool/Default.aspx).
Кроме того, МРТ в качестве скрининга может проводиться дополнительно к маммографии у следующих категорий женщин (уровень убедительности доказательств C (мнение экспертов): облучение грудной клетки в возрасте от 10 до 30 лет, наследственные синдромы Li-Fraumeni, Bannayan-Riley-Ruvalcaba (или родственницы первой линии); риск РМЖ более 20%, связанный с генами и/или уровнем риска (ATM, CDH1, CHEK2, NF1, NBN, PALB2, PTEN, STK11, TP53).
МРТ молочных желез рассматривается также, как метод скрининга пациенток с дольковой карциномой in situ (LCIS) и атипической дольковой/протоковой гиперплазией (ALH/ADH), если риск РМЖ в течение жизни ![]() 20% (уровень убедительности доказательств C (мнение экспертов).
20% (уровень убедительности доказательств C (мнение экспертов).
При риске РМЖ в течение жизни менее 15% МРТ молочных желез с целью скрининга НЕ рекомендуется (Уровень убедительности доказательств C (мнение экспертов).
Для адекватной трактовки результатов методов инструментальной диагностики и выбора последующей маршрутизации пациенток рекомендуется применение системы BI-RADS (Breast Imaging Reporting and Data System).
NB! Категории оценки BI-RADS едины для всех методов обследования молочной железы (таблица 5).
Прочие методы инструментальной диагностики
Использование термографии или других методов визуализации, например, сцинтиграфии, в качестве альтернативы маммографии не рекомендуется (69).
Таблица 5.
Классификация результатов исследования в соответствии
с системой BI-RADS (Breast Imaging Reporting and Data
System) и рекомендуемая тактика ведения (25)
Классификационная категория
Вероятность РМЖ
Тактика ведения в зависимости от проведенного исследования
Маммография
УЗИ
МРТ
BI-RADS-0: результат неполный - необходимо дополнительное исследование (и/или сравнение с предыдущими маммограммами случае маммографического скрининга)
Не применимо
Повторный вызов для дополнительного исследования, сравнение с предыдущим результатом, или то и другое
Повторный вызов для дополнительного исследования
Рекомендуется дополнительное исследование: маммография или прицельное УЗИ
BI-RADS-1: результат отрицательный
Вероятность малигнизации практически 0%
Рутинный скрининг
Рутинный скрининг
Рутинный скрининг, если кумулятивный риск РМЖ в течение жизни ![]() 20% <*>
20% <*>
BI-RADS-2: доброкачественные изменения
Вероятность малигнизации практически 0%
Рутинный скрининг
Рутинный скрининг
Рутинный скрининг, если кумулятивный риск РМЖ в течение жизни ![]() 20% <*>
20% <*>
BI-RADS-3: вероятно, доброкачественные изменения
Вероятность малигнизации > 0%, но ![]() 2%
2%
Наблюдение с кратковременными (6 мес.) интервалами или последующая динамическая маммография
Наблюдение с кратковременными (6 мес.) интервалами
Кратковременный (6-мес.) интервал наблюдения
BI-RADS-4: подозрение на малигнизацию
Вероятность малигнизации > 2%, но < 95%
Диагноз ставится на основании результата биопсии
BI-RADS-5: высокая вероятность малигнизации
Вероятность малигнизации > 95%
BI-RADS-6: малигнизация, доказанная с помощью биопсии
Не применимо
Хирургическое лечение, если клинически оправдано
--------------------------------
<*> Кумулятивный риск РМЖ определяется с использованием компьютерной программы, основанной на модели GAIL (NCCN, 2017) (доступна на https://www.cancer.gov/bcrisktool/Default.aspx).
4.3. Тонкоигольная аспирационная биопсия
и прицельная трепанобиопсия
Тонкоигольная аспирационная биопсия позволяет получить материал, пригодный для цитологического исследования, тем не менее, при использовании данного метода процент диагностических ошибок РМЖ при непальпируемых злокачественных опухолях достигает 36%.
Трепанобиопсия с использованием радиографических или ультразвуковых методик позволяет получить достаточный образец ткани для решения вопроса о наличии или отсутствии малигнизации (68).
Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1a).
NB! Определение показаний/противопоказаний к процедуре и ее проведение является компетенцией врача-онколога.
4.4. Тактика обследования при выделениях из сосков
При наличии выделений из соска из нескольких протоков, которые не имеют спонтанного характера, пациенткам моложе 40 лет предлагают наблюдение и информируют их о необходимости обратиться к врачу при появлении спонтанных выделений; у пациенток 40 лет и старше производят также маммографию, если она не сделана ранее (54).
При персистирующих спонтанных выделениях, отмечающихся также при объективном обследовании, односторонних выделениях из одного протока, серозном, кровянистом или серозно-кровянистом характере отделяемого рекомендуется следующая тактика (54): у пациенток моложе 30 лет производится УЗИ +/- маммография, у пациенток 30 лет и старше - диагностическая маммография + УЗИ. Далее тактика зависит от результатов обследования и определяется онкологом. При категории BI-RADS 1 - 3 может быть применена МРТ или дуктография, далее, по показаниям, может производиться эксцизия протока, или проводится наблюдение. При категории BI-RADS 4 - 5 диагноз ставится на основании биопсии ткани молочной железы.
При галакторее рекомендуется выполнить тест на беременность, исследовать уровень пролактина и исключить прием препаратов, которые могут быть причиной галактореи (6).
NB! Цитологическое исследование отделяемого из сосков большого диагностического значения не имеет, так чувствительность метода относительно выявления РМЖ составляет 35 - 47% (68).
3.5. Гормональные исследования
Возможными, хотя и не обязательными, гормональными нарушениями, которые могут быть выявлены при ДЗМЖ, являются: умеренная гиперпролактинемия, дисбаланс гонадотропинов, недостаточность прогестерона, относительная или абсолютная гиперэстрогенемия, гиперандрогенемия, гипотиреоз. У части больных (чаще при ожирении) выявляется гиперинсулинизм.
В зависимости от клинических показаний при ДДМЖ рекомендуется исследовать концентрации ФСГ, ЛГ, ТТГ, свободного Т4, пролактина, эстрадиола, прогестерона, кортизола крови. При проявлениях, потенциально свидетельствующих о гиперандрогенемии (гирсутизм, угревая сыпь, алопеция), рекомендуется исследовать концентрации тестостерона, ДГЭАС и определять 17-OH-прогестерон для исключения неклассической формы врожденной дисфункции коры надпочечников.
Объем гормонального обследования может быть расширен при наличии дополнительных показаний.
NB! Исследование 17-кетостероидов в моче в настоящее время не рекомендуется, так как доступны более информативные методы исследования концентраций андрогенов (тестостерона, дегидроэпиандростерона и его сульфата) в сыворотке/плазме крови с помощью ИФА, РИА или хроматографии с масс-спектрометрией.
5. Лечение и профилактика
5.1. Лечение ДДМЖ
Методы хирургического лечения ДДМЖ
Определение показаний и противопоказаний к хирургических методов лечения при ДДМЖ является компетенцией онколога.
Методы консервативного лечения ДДМЖ
Немедикаментозные методы
Немедикаментозные подходы к коррекции масталгии включают методы психотерапии и использование правильно подобранного белья. Кроме того, 85% пациенток отмечают исчезновение боли, если в результате проведенного обследования МЖ патологических изменений не обнаруживается, и только 15% требуется лечение (68). (Уровень убедительности рекомендаций B).
Медикаментозная терапия
Характеристика лекарственных препаратов, с зарегистрированными показаниями к применению и доказанной эффективностью для лечения ДЗМЖ, представлена в таблице 6.
Имеются убедительные свидетельства эффективности использования при ДДМЖ лекарственных препаратов на основе Витекса священного и препаратов прогестерона (Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1a).
Для коррекции масталгии эффективно применение лекарственного препарата на основе индол-3-карбинола (Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1b).
Агонисты дофамина преимущественно используются при гиперпролактинемии (шифр МКБ E22.1), в соответствии с клиническими рекомендациями Российской ассоциации эндокринологов (2014) (1), однако ингибиторы пролактина могут эффективно применяться и при лечении ДДМЖ (16) (Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1b).
Среди медикаментозных средств для коррекции масталгии также эффективны тамоксифен (в дозе 10 мг ежедневно в течение 3 - 6 месяцев, а в случае его неэффективности - даназол в дозе 200 мг ежедневно или только в лютеиновой фазе менструального цикла (68) (уровень убедительности рекомендаций A (уровень достоверности доказательств - 1a), хотя их применение ограничено в связи с побочными эффектами. Кроме того, в РФ ДЗМЖ не являются официальным показанием для применения тамоксифена.
Доказана эффективность коррекции масталгии при использовании агонистов РГ-ГТ (68), однако длительность применения данных препаратов ограничена в связи с проявлениями эстрогенного дефицита и у женщин с ДДМЖ они, как правило, назначаются по другим показаниям. (Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1a).
Эффективными средствами для коррекции масталгии являются нестероидные противовоспалительные средства (НПВС) как системного, так и локального применения (68) (Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1b).
Эффективность зарегистрированных в РФ для лечения ДЗМЖ гомеопатических лекарственных препаратов (Мастопол и Маммосан, Россия), а также ферментного препарата Вобэнзим (Германия) менее убедительна (Уровень убедительности рекомендаций B, C).
NB! В связи с тем, что мастопатия часто ассоциирована с заболеваниями щитовидной железы, в том числе, с аутоиммунным тиреоидитом (7), использование йодида калия без соответствующего обследования не рекомендуется.
Таблица 6.
Лекарственные препараты,
с зарегистрированными показаниями к применению для лечения
ДЗМЖ с доказанной эффективностью (A)
(http://www.grls.rosminzdrav.ru).
N п/п
Состав, форма выпуска
Показания к применению при ДЗМЖ (из официальной инструкции)
Противопоказания и ограничения
Режим дозирования
Уровень убедительности рекомендаций и достоверности доказательств
1
Таблетки:
Vitex agnus castus (Agnus castus) 162 мг
Caulophyllum thalictroides D4 81 мг
Cyclamen europaeum (Cyclamen) D4 81 мг
Strychnos ignatii (Ignatia) D6 81 мг
Iris versicolor (Iris) D2 162 мг
Lilium lancifolium (Lilium tigrinum) D3 81 мг
Капли для приема внутрь:
Vitex agnus castus (Agnus castus) D1 20 г
Caulophyllum thalictroides D4 10 г
Cyclamen europaeum (Cyclamen) D4 10 г
Strychnos ignatii (Ignatia) D6 10 г
Iris versicolor (Iris) D2 20 г
Lilium lancifolium (Lilium tigrinum) D3 10 г
Фиброзно-кистозная мастопатия
(Из инструкции к препарату с рег номером П N 014026/01)
Повышенная чувствительность к компонентам препарата. Период беременности и грудного вскармливания. Злокачественные заболевания молочных желез. Наследованная непереносимость галактозы, генетический дефицит лактазы или нарушение всасывания глюкозы и галактозы. Возраст до 12 лет.
Таблетки:
Внутрь по 1-й таблетке 2 раза в день, с небольшим количеством жидкости не менее 3 месяцев
Капли:
По 30 капель 2 раза в день (утром и вечером), немного разбавляя их водой или другой жидкостью не менее 3 месяцев
A(1a), систематический обзор нескольких РКИ
2
Гель для наружного применения 1%,
1 доза аппликатора соответствует 2,5 г геля и содержит 0,025 г прогестерона.
Мастопатия, связанная с недостаточностью прогестерона;
Масталгия, связанная с:
Приемом пероральных контрацептивов;
Беременностью;
Пубертатным периодом;
Пременопаузой;
Предменструальным синдромом;
-
Мастопатией
(Из инструкции к препарату с рег номером П N 013765/01)
Повышенная чувствительность к компонентам препарата. Применение препарата в периоды беременности и грудного вскармливания возможно в тех случаях, когда польза от лечения превышает потенциальный риск для плода или младенца.
1 доза аппликатора или 2,5 г геля наносится на кожу молочных желез до полного всасывания 2 раза в день, в среднем 5 г ежедневно, в т.ч. в дни менструации.
A(1b)
РКИ
3
Капсулы:
Прогестерон микронизированный 100 и 200 мг
Прогестерондефицитные состояния у женщин:
фиброзно-кистозная мастопатия и др.
(Из инструкции к препарату с рег номером ЛС-000186)
Повышенная чувствительность к компонентам препарата;
тромбоз глубоких вен, тромбофлебит, тромбоэмболические нарушения (тромбоэмболия легочной артерии, инфаркт миокарда, инсульт), внутричерепное кровоизлияние или наличие данных состояний/заболеваний в анамнезе;
кровотечения из влагалища неясного генеза; неполный аборт;
порфирия; установленные или подозреваемые злокачественные новообразования молочных желез и половых органов; и др (см. офиц. инструкцию)
При фиброзно-кистозной мастопатии, суточная доза 200 или 400 мг в течение 10 дней (обычно с 17-го по 26-й день цикла).
A(1b)
РКИ
4
Капсулы:
Индолкарбинол 250 мг
Циклическая масталгия, в том числе на фоне доброкачественной гиперплазии молочной железы
(Из инструкции к препарату с рег номером ЛП-002010)
Повышенная чувствительность к компонентам препарата. Наследственная непереносимость галактозы, дефицит лактазы или глюкозо-галактозная мальабсорбция. Период беременности и грудного вскармливания. Детский возраст до 18 лет.
Внутрь, 2 раза в сутки по 200 мг. Суточная доза препарата 400 мг.
Капсулы принимают перед едой.
Длительность курса лечения 6 месяцев.
A(1b)
РКИ
5
Табл. бромокриптина мезилата <*> 2,5 или 10 мг;
Фиброзно-кистозная мастопатия и др.
(Из инструкции к препарату с рег номером П N 008603)
Гиперчувствительность (в т.ч. к алкалоидам спорыньи), неконтролируемая артериальная гипертензия, беременность.
Внутрь, во время еды - по 2,5 мг 2 - 3 раза в сутки в течение нескольких месяцев.
A(1b)
РКИ
6
Капсулы:
Даназол <**> 100 мг, 200 мг.
Доброкачественные новообразования молочной железы (фиброзно-кистозная мастопатия) и др.
(Из инструкции к препарату с рег номером П N 014488/01)
Повышенная чувствительность к даназолу или любым другим ингредиентам препарата, беременность, период грудного вскармливания, порфирия, рак молочной железы, карцинома, андрогензависимые опухоли, кровотечение из влагалища неясного генеза и др (см офиц инструкцию).
При фиброзно-кистозной мастопатии от 100 до 400 мг (обычно 300 мг) в течение 3 - 6 мес.
A(1b)
РКИ
--------------------------------
<*> Применяется преимущественно при гиперпролактинемии.
<**> Применение ограничено в связи с побочными эффектами.
Наряду с вышеизложенным, в обязанности акушера-гинеколога входит подбор заместительной гормональной терапии и комбинированных оральных контрацептивов.
Применение гормональных контрацептивов и средств МГТ при ДДМЖ.
Гормональная контрацепция
Медицинские критерии применения гормональных контрацептивов (ГК) в настоящее время регламентировано в 5-м издании руководства ВОЗ (52).
ДЗМЖ, в том числе с наличием семейной истории РМЖ и носительством BRCA1 и BRCA2, классифицируются в данном руководстве, как категория 1 (состояние, при котором нет ограничений для использования контрацептивного метода), как для комбинированных гормональных контрацептивов (КОК, пластыри, вагинальные кольца и инъекционные контрацептивы), так и для чисто прогестагенных ГК (чисто прогестагенных оральных ГК, ГК, содержащих левоноргестрел и этоногестрел, депо медроксипрогестерона ацетата, норэтистерона энантата). Это связано с тем, что применение ГК не усугубляет риск РМЖ, если он уже повышен. Данный подход относится как к началу, так и к продолжению использования метода контрацепции при выявлении ДЗМЖ (52) Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1b).
NB! Применение комбинированных КОК с низкой дозой этинилэстрадиола (20 мкг) ассоциировано со снижением выраженности масталгии (68)
Неуточненные образования в молочной железе рассматриваются, как категория 2 (состояние, при котором преимущества применения метода в основном превышают теоретический или доказанный риск) как для комбинированных гормональных контрацептивов (КОК, пластыри, вагинальные кольца и инъекционные контрацептивы), так и для чисто прогестагенных ГК (чисто прогестагенные оральные ГК; ГК, содержащие левоноргестрел и этоногестрел, депо медроксипрогестерона ацетат, норэтистерона энантат), но требуют незамедлительного уточнения диагноза. Этот подход относится как к начальному выбору, так и к продолжению использования метода контрацепции при выявлению неуточненного образования молочной железы. (52) Уровень убедительности рекомендаций A, уровень достоверности доказательств - 1a.
МГТ
В соответствии с национальными клиническими рекомендациями "Менопаузальная гормонотерапия и сохранение здоровья женщин в зрелом возрасте", утвержденными Минздравом России 02 октября 2015 г., ДДМЖ не являются противопоказанием для МГТ. Общие принципы стратегии снижения рисков включают применение МГТ по показаниям, начало МГТ в возрасте моложе 60 лет при длительности постменопаузы менее 10 лет и использование в препаратах МГТ минимальных эффективных доз эстрогенов: для препаратов, содержащих 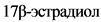 или эстрадиола валерат, 1 - 0,5 мг в сутки, для трансдермальных препаратов - 14 мкг в сутки (5). Уровень убедительности рекомендаций A, уровень достоверности доказательств - 1b.
или эстрадиола валерат, 1 - 0,5 мг в сутки, для трансдермальных препаратов - 14 мкг в сутки (5). Уровень убедительности рекомендаций A, уровень достоверности доказательств - 1b.
NB! Согласно последним данным, риск РМЖ повышается, начиная с 8 - 10 летней продолжительности использования МГТ (75). Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1b).
При возникновении РМЖ у женщин, получавших препараты эстрадиола и тиболон, опухоль имеет более благоприятные характеристики в сравнении с опухолями у женщин, которые вообще не использовали МГТ. Использование препаратов МГТ, содержащих эстрогены и норэтистерон, напротив, ассоциировано с менее благоприятными характеристиками опухоли (63) (Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1b).
Использование эстроген-гестагенной терапии у худых женщин ассоциировано с более благоприятным вариантом РМЖ, чем у женщин, никогда не применявших МГТ, тогда как у женщин с избыточной массой тела данная закономерность не прослеживается (45). (Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1b).
В целом, по мнению экспертов Международной ассоциации по менопаузе (IMS), риск рака молочной железы, связанный с МГТ, мал и постепенно снижается после прекращения лечения прекращается (Уровень убедительности рекомендаций B). Повышенный риск развития рака молочной железы связан с добавлением синтетического прогестагена МПА и продолжительностью использования (Уровень убедительности рекомендаций B). Риск может быть ниже при использовании микронизированного прогестерона или дидрогестерона (Уровень убедительности рекомендаций C). Вероятность риска РМЖ при применении МГТ может быть частично снижена путем отбора женщин с более низким индивидуальным исходным риском, включая низкую маммологическую плотность, превентивным изменением образа жизни (снижение массы тела, употребления алкоголя, повышением физической активности) (Уровень убедительности рекомендаций D) (8).
5.2. Профилактика ДДМЖ
Установленные протективные факторы относительно риска ДДМЖ:
- Поддержание оптимального ИМТ. К доказанным методам профилактики ДЗМЖ у потомства женского пола относится поддержание оптимальной (физиологической) массы тела матери в предгравидарный период во время беременности, так как ИМТ матерей до беременности в пределах 20 - 25 кг/м2 и адекватный набор веса при беременности ассоциированы с более низким риском ДЗМЖ у дочерей. Профилактическую значимость имеет поддержание оптимального веса в препубертате и в подростковом возрасте, так как ИМТ в возрасте 10 лет и в 18-летнем возрасте отрицательно коррелирует с риском ДЗМЖ в репродуктивном возрасте (13).
- Коррекция рациона. Профилактическое значение имеет отказ от приема алкоголя в возрасте от менархе до первых родов (12, 50), ограничение животный жира и мяса (не ![]() 3 порций в день) в рационе, особенно в молодом возрасте (9, 30).
3 порций в день) в рационе, особенно в молодом возрасте (9, 30).
- Оптимизация длительности МГТ. Длительность МГТ, не превышающая 8 - 15 лет, ассоциирована со снижением риска ДЗМЖ (23, 62). Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1a).
5.3. Профилактика РМЖ
Установленные протективные факторы относительно риска РМЖ Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1a)
- Физическая активность. Регулярные физические упражнения ассоциированы с умеренным снижением риска РМЖ и его рецидивов (57, 59).
- Диетические факторы. Использование в рационе растительных масел, орехов, витамина E и клетчатки, а также уменьшение потребления животных жиров, красного мяса и алкоголя ассоциировано со снижением риска ДЗМЖ (9, 30).
- Кормление грудью. Каждые 12 месяцев кормления грудью ассоциированы со снижением относительного риска РМЖ на 4,3% (21).
NB! Бисфосфонаты не оказывают протективного влияния относительно риска РМЖ (29)
Факторы, влияние которых на риск РМЖ окончательно не установлено: некоторые диетические факторы (средиземноморская диета, фрукты и овощи), прием лекарственных препаратов (кальций/витамин D, антиоксиданты, НПВС).
Профилактика РМЖ у женщин групп высокого риска
- Женщинам, у которых диагностирована атипичная гиперплазия, значительно повышающая риск последующего инвазивного рака в пораженной груди и контралатеральной груди, настоятельно рекомендуется профилактическая медикаментозная терапия, которая включает применение тамоксифена (для женщин в пременопаузе и постменопаузе), ралоксифена (для женщин в постменопаузе) и ингибиторов ароматазы (для женщин в постменопаузе) (6). Уровень убедительности рекомендаций A, (уровень достоверности доказательств - 1a.
- Женщинам-носительницам генетических мутаций гена BRCA после обсуждения соотношения протективной пользы и риска, а также возможностей реконструктивной хирургии, может быть предложена двухстороняя мастэктомия (54).
NB! Назначение профилактической медикаментозной терапии и определения показаний к риск-редуцирующим вмешательствам относится к компетенции онколога. Риск-редуцирующая сальпингоовариоэктомия в РФ юридически не легитимна и не проводится даже по желанию пациентки.
5.4. Скрининг РМЖ
Под скринингом подразумевается профилактическое обследование здоровых групп населения с целью выявления заболевания на ранней стадии. Основной целью скрининговых программ по раннему выявлению рака молочной железы является снижение показателей смертности от данного заболевания путем диагностики ранних стадий РМЖ.
NB! Маммографический скрининг женского населения является доказанным методом профилактики смертности от РМЖ (69) Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1a).
В рекомендациях по скринингу для выявления РМЖ, принятым в 2017 г. Европейским обществом заболеваний молочной железы (European Society of Breast Imaging, EUSOBI) указано, что проведение маммографического скрининга каждые 2 года позволяет снизить смертность от РМЖ, прежде всего женщин в возрасте 50 - 69 лет (1-й приоритет данного мероприятия), а также, в меньшей степени, в возрасте 73 - 75 лет (2-й приоритет), и, при ежегодном скрининге, в возрастной группе от 40 - 45 лет до 49 лет (3-й приоритет) (69).
N.B.! Для женщин 50 - 69 лет, с учетом 10-летнего латентного периода и дозы радиации, получаемой во время скрининга (2.5 mGy), риск смерти от РМЖ, связанного с проведением маммографии, составляет 1 на 100 000 скринированных женщин, при этом риск индуцированного РМЖ как минимум в 100 раз ниже вероятности избежать смерти от РМЖ, благодаря проведению маммографического скрининга (69).
Рекомендации по началу и окончанию скрининга РМЖ до настоящего времени не стандартизованы. В США, в соответствии с консенсусами различных сообществ, возраст начала скрининга варьирует от 40 до 50 лет с интервалом 1 - 2 года (ACOG, American Cancer Society; U.S. Preventive Services Task Force). В программе скрининга РМЖ, принятой в Великобритании ("The Breast Cancer Screening Programmes", UK), в настоящее время предусмотрено приглашение женщин в возрасте 50 - 70 лет для скрининговой маммографии каждые 3 года с целевым уровнем охвата таргетной популяции ![]() 80,0% (77).
80,0% (77).
В соответствии с клиническими рекомендациями Российского общества онкомаммологов, РООМ (2015), рекомендуемым (и желательным) возрастом начала скрининга РМЖ является 40 и более лет, а допустимым - возраст 50 - 69 лет, с интервалом 2 года (2). Однако до настоящего времени на систематической основе скрининг рака молочной железы, в частности маммографический, в РФ не проводится.
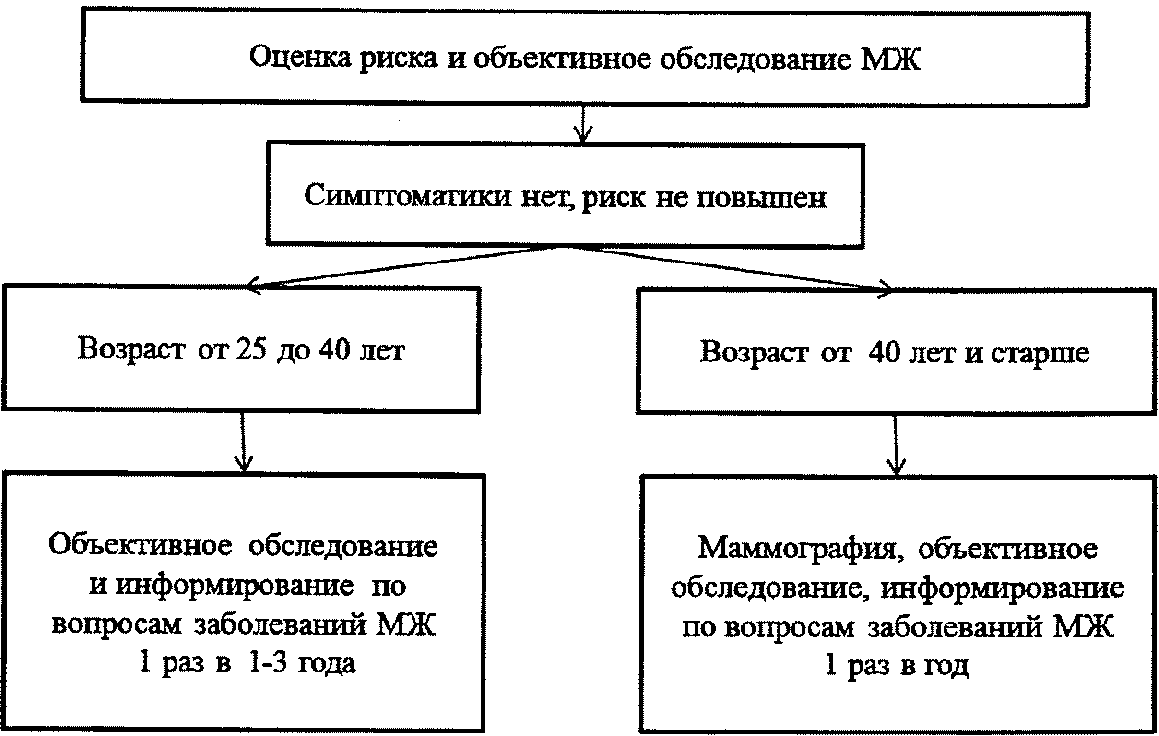
Алгоритмы скрининга РМЖ (адаптировано из NCCN, 2017) (54)
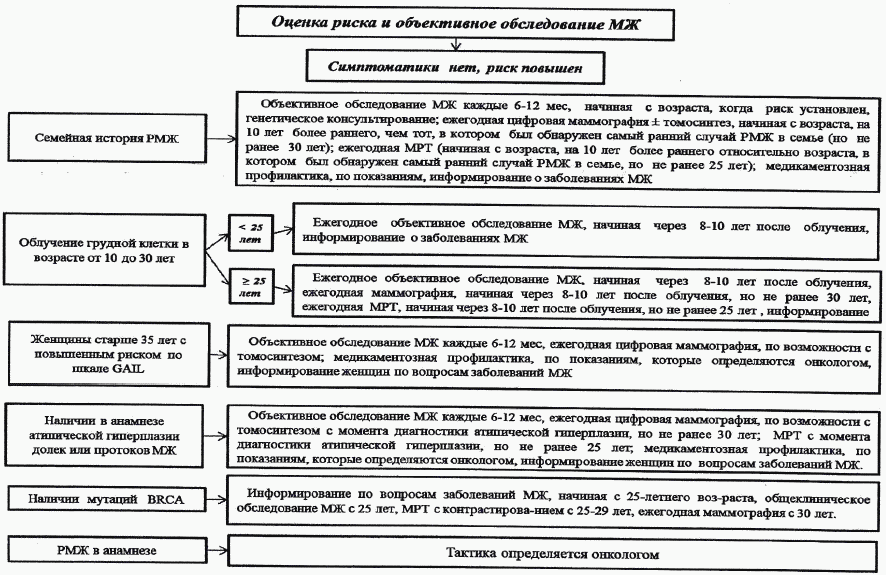
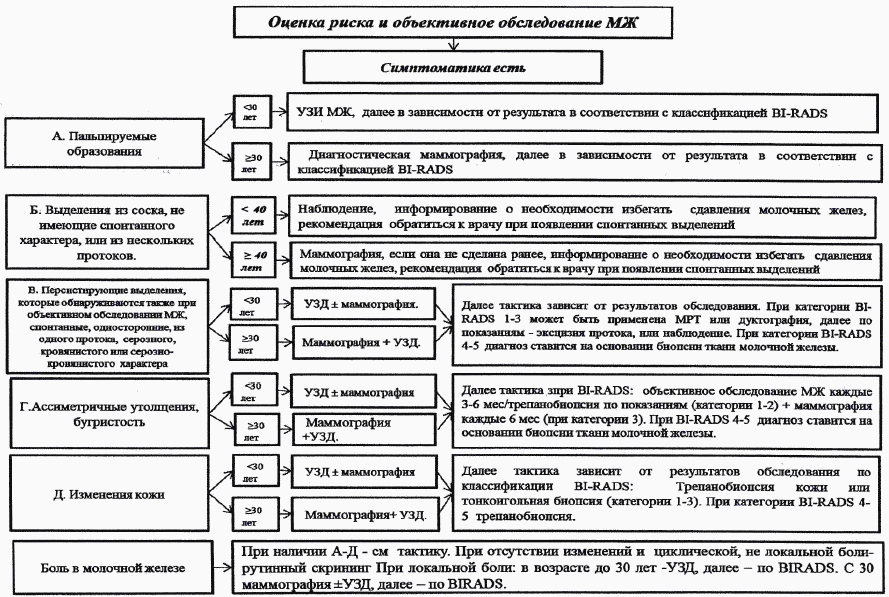
ЛИТЕРАТУРА
1. Клинические рекомендации по гиперпролактинемии: клиника, диагностика, дифференциальная диагностика и методы лечения/Российская ассоциация эндокринологов. - 2014. - 19 с. (https://www.endocrincentr.ru/specialists/science/nauchnye-publikacii/konsensusy-i-klinicheskie-rekomendacii).
2. Клинические рекомендации РООМ по скринингу РМЖ/Под ред Н.А. Захаровой, д.м.н. В.Ф. Семиглазова, Г.М. Манихас. - 2015. - 18 с.
3. Маммология: национальное руководство/под ред. А.Д. Каприна, Н.И. Рожковой. - 2-е изд., перераб. и доп. - М.,: ГЭОТАР-Медиа, 2016. - 496 с.
4. Медицина, основанная на доказательствах. Руководство для начинающих пользователей/Под ред Г.Т. Сухих. - М.: ООО "Верди". - 2011. - 179 с.
5. Менопаузальная гормонотерапия и сохранение здоровья женщин в зрелом возрасте: клинические рекомендации (протокол лечения), утв. Минздравом России 2 октября 2015. - М. - 2015, - 49 с.
6. The ACOG Practice Bulletin No. 164 Summary: Diagnosis and Management of Benign Breast Disorders (2016) Obstetrics and gynecology: 127 (6), pp 1181 - 1183
7. Anil C, Guney T, Gursoy A. The prevalence of benign breast diseases in patients with nodular goiter and Hashimoto's thyroiditis J Endocrinol Invest. 2015 Sep;38(9):971-5.
8. Baber RJ, Panay N, Fenton A; IMS Writing Group. 2016 IMS Recommendations on women's midlife health and menopause hormone therapy. Climacteric. 2016 Apr; 19(2): 109-50.
9. Baer HJ, Schnitt SJ, Connolly JL, Byrne C, Cho E, Willett WC, et al. Adolescent diet and incidence of proliferative benign breast disease. Cancer Epidemiol Biomarkers Prev. 2003; 12(11Pt 1):1159-1167.
10. Baer HJ, Schnitt SJ, Connolly JL, Byrne C, Willett WC, Rosner B, Colditz GA. Early life factors and incidence of proliferative benign breast disease.Cancer Epidemiol Biomarkers Prev. 2005 Dec; 14(12):2889-97.
11. Berg WA, Blume JD, Cormack JB, et al. Combined screening with ultrasound and mammography vs mammography alonein women at elevated risk of breast cancer. JAMA 2008; 299:2151-2163.
12. Berkey CS, Willett WC, Frazier AL et al. Prospective study of adolescent alcohol consumption and risk of benign breast disease in young women. Pediatrics. 2010 May; 125(5):e1081-7. doi: 10.1542/peds.2009-2347. Epub 2010 Apr 12.
13. Berkey CS, Rosner B, Willett WC et al. Prenatal factors and infant feeding in relation to risk of benign breast disease in young women. Breast Cancer Res Treat. 2015 Dec; 154(3):573-82.
14. Berkey CS, Rosner B, Tamimi RM et al. Body size from birth through adolescence in relation to risk of benign breast disease in young women. Breast Cancer Res Treat. 2017 Feb; 162(1):139-149.
15. Calle EE, Frumkin H, Henley SJ et al. Organochlorines and breast cancer risk.CA Cancer J Clin. 2002 Sep - Oct; 52(5):301-9.
16. Castillo-Huerta E, Garibay-Valencia M, 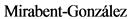 F. Clinical comparision of alpha dihidroergocriptina against cabergolina in the treatment of the fibrocystic mastopathy. Ginecol Obstet Mex. 2013 Jul; 81(7):370-6
F. Clinical comparision of alpha dihidroergocriptina against cabergolina in the treatment of the fibrocystic mastopathy. Ginecol Obstet Mex. 2013 Jul; 81(7):370-6
17. Catalano O, Raso MM, D'Aiuto M et al. Additional role of colour Doppler ultrasound imaging in intracystic breast tumours Radiol Med. 2009 Mar; 114(2):253-66.
18. Centers for Disease Control and Prevention (CDC) MMWR Morb Mortal Wkly Rep. 2012; 61(45):922.
19. Collaborative Group on Hormonal Factors in Breast Cancer. Breast cancer and hormone replacement therapy: collaborative reanalysis of data from 51 epidemiological studies of 52, 705 women with breast cancer and 108, 411 women without breast cancer. Lancet. 1997 Oct 11; 350(9084):1047-59.
20. Collaborative Group on Hormonal Factors in Breast Cancer. Familial breast cancer: collaborative reanalysis of inpidual data from 52 epidemiological studies including 58, 209 women with breast cancer and 101,986 women without the disease. Lancet. 2001 Oct 27; 358(9291): 1389-99.
21. Collaborative Group on Hormonal Factors in Breast Cancer. Breast cancer and breastfeeding: collaborative reanalysis of inpidual data from 47 epidemiological studies in 30 countries, including 50302 women with breast cancer and 96973 women without the disease. Lancet. 2002 Jul 20; 360(9328):187-95.
22. Cui Y, Page DL, Chlebowski RT et al. Cigarette smokingand risk of benign proliferative epithelial disorders of the breast in the Women's Health Initiative. Cancer Causes Control. 2007; 18(4):431-438.
23. Cui Y, Page DL, Lane DS, Rohan TE. Menstrual and reproductive history, postmenopausal hormone use, and risk of benign proliferative epithelial disorders of the breast: a cohort study. Breast Cancer Res Treat. 2009 Mar; 114(1):113-20.
24. Degnim AC, Dupont WD, Radisky DC et al Extent of atypical hyperplasia stratifies breast cancer risk in 2 independent cohorts of women. Cancer. 2016 Oct; 122(19):2971-8.
25. D'Orsi CJ, Sickles EA, Mendelson EB, et al. ACR BI-RADS Atlas(R), Breast Imaging Reporting and Data System, 5th ed. Reston, VA: American College of Radiology; 2013.
26. Dyrstad SW, Yan Y, Fowler AM, Colditz GA. Breast cancer risk associated with benign breast disease: systematic review and meta-analysis Breast Cancer Res Treat. 2015 Feb; 149(3):569-75.
27. Eliassen AH, Missmer SA, Tworoger SS et al.Endogenous steroid hormone concentrations and risk of breast cancer among premenopausal women. J Natl Cancer Inst. 2006 Oct 4; 98(19):1406-15.
28. Endogenous Hormones and Breast Cancer Collaborative Group, Key TJ, Appleby PN, Reeves GK, Roddam AW.Insulin-like growth factor 1 (IGF1), IGF binding protein 3 (IGFBP3), and breast cancer risk: pooled inpidual data analysis of 17 prospective studies. Lancet Oncol. 2010 Jun; 11(6):530-42.
29. Fournier A, Mesrine S, Gelot A et al. Use of Bisphosphonates and Risk of Breast Cancer in a French Cohort of Postmenopausal Women. Clin Oncol. 2017 Oct 1; 35(28):3230-3239.
30. Frazier AL1, Rosenberg SM. Preadolescent and adolescent risk factors for benign breast disease. J Adolesc Health. 2013 May; 52(5 Suppl):S36-40.
31. Gaudet MM, Patel AV, Sun J et al.Tubal sterilization and breast cancer incidence: results from the cancer prevention study II nutrition cohort and meta-analysis. Am J Epidemiol. 2013 Mar 15; 177(6):492-9
32. Gram IT, Park SY, Kolonel LN et al.Smoking and Risk of Breast Cancer in a Racially/Ethnically Diverse Population of Mainly Women Who Do Not Drink Alcohol: The MEC Study. Am J Epidemiol. 2015 Dec 1; 182(11):917-25.
33. Gunter MJ, Hoover DR, Yu H et al. Insulin, insulin-like growth factor-I, and risk of breast cancer in postmenopausal women. J Natl Cancer Inst. 2009 Jan 7; 101(1):48-60.
34. Guray M, Sahin AA. Benign breast diseases: classification, diagnosis, and management. Oncologist. 2006 May; 11(5):435-49.
35. https://patient.info/doctor/breast-lumps-and-breast-examination#ref-13
36. Harris JR. Diseases of the breast. 4th ed. Philadelphia: Lippincott Williams & Wilkins; 2010. p. 1174.
37. Heinemann K, Thiel C, Mohner S, Lewis MA, Raff T, Kuhl-Habich D, Heinemann LAJ (2003) Benign gynecological tumors: Estimate incidence results of the german gohort study on women's health. Eur J Obstet Gynecol Reprod Biol. 2003 Mar 26; 107(1):78-80.
38. Henderson TO, Amsterdam A, Bhatia S et al. Systematic review: surveillance for breast cancer in women treated with chest radiation for childhood, adolescent, or young adult cancer. Ann Intern Med. 2010 Apr 6; 152(7):444-55; W144-54. doi: 10.7326/0003-4819-152-7-201004060-00009.
39. Holmes MD1, Willett WC. Does diet affect breast cancer risk? Breast Cancer Res. 2004; 6(4): 170-8.
40. Hooley RJ1, Scoutt LM, Philpotts LE. Breast ultrasonography: state of the art. Radiology. 2013 Sep; 268(3):642-59.
41. Hoover RN1, Hyer M, Pfeiffer RM et al. Adverse health outcomes in women exposed in utero to diethylstilbestrol. N Engl J Med. 2011 Oct 6; 365(14):1304-14.
42. Kaaks R, Berrino F, Key T et al. Serum sex steroids in premenopausal women and breast cancer risk within the European Prospective Investigation into Cancer and Nutrition (EPIC). J Natl Cancer Inst. 2005 May 18; 97(10):755-65.
43. Kerlikowske K, Ichikawa L, Miglioretti DL et al. Longitudinal measurement of clinical mammographic breast density to improve estimation of breast cancer risk. J Natl Cancer Inst. 2007 Mar 7; 99(5):386-95.
44. Kuchenbaecker KB, Hopper JL, Barnes DR et al. Risks of Breast, Ovarian, and Contralateral Breast Cancer for BRCA1 and BRCA2 Mutation Carriers. JAMA. 2017 Jun 20; 317(23):2402-2416. doi: 10.1001/jama.2017.7112.
45. Kjartansdottir OJ, Sigurdardottir LG, Olafsdottir EJ et al.Estrogen-progestin use and breast cancer characteristics in lean and overweight postmenopausal women. Breast Cancer Res Treat. 2017 Jun; 163(2):363-373.
46. Lauby-Secretan B, Scoccianti C, Loomis D et al. Body Fatness and Cancer-Viewpoint of the IARC Working Group. N Engl J Med. 2016; 375(8):794-798
47. Lauby-Secretan B, Scoccianti C, Loomis D, International Agency for Research on Cancer Handbook Working Group et al (2015) Breast Cancer Screening - Viewpoint of the IARC Working Group. N Engl J Med 372(24):2353-2358
48. Lehman CD, Wellman RD, Buist DS, Kerlikowske K, Tosteson AN, Miglioretti DL; Breast Cancer Surveillance Consortium. Diagnostic Accuracy of Digital Screening Mammography With and Without Computer-Aided Detection. JAMA Intern Med. 2015 Nov; 175(11): 1828-37.
49. Lipworth L et al., 2009; Lipworth L, Tarone RE, Friis S, Ye W, Olsen JH, Nyren O, McLaughlin JK.Cancer among Scandinavian women with cosmetic breast implants: a pooled long-term follow-up study.Int J Cancer. 2009 Jan 15; 124(2):490-3.
50. Liu Y et al., 2012 Liu Y, Tamimi RM, Berkey CS, Willett WC, Collins LC, Schnitt SJ, Connolly JL, Colditz GA. Intakes of alcohol and folate during adolescence and risk of proliferative benign breast disease.Pediatrics. 2012 May; 129(5):el 192-8.
51. Mahesh M AAPM/RSNA physics tutorial for residents: digital mammography: an overview. Radiographics. 2004; 24(6):1747.
52. Medical eligibility criteria for contraceptive use. WHO, 2015. http://www.who.int/reproductivehealth/publications/family_planning/MEC-5/en/
53. Melnikow J, Fenton JJ, Whitlock EP et al. Supplemental Screening for Breast Cancer in Women With Dense Breasts: A Systematic Review for the U.S. Preventive Service Task Force [Internet]. Rockville (MD): Agency for Healthcare Research and Quality (US); 2016 Jan. Report No.: 14-05201-EF-3.
54. https://www.nccn.org/
55. Nichols HB, Berrington de 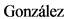 A, Lacey JV Jr et al. Declining incidence of contralateral breast cancer in the United States from 1975 to 2006. J Clin Oncol. 2011 Apr 20; 29(12): 1564-9.
A, Lacey JV Jr et al. Declining incidence of contralateral breast cancer in the United States from 1975 to 2006. J Clin Oncol. 2011 Apr 20; 29(12): 1564-9.
56. Lehman CD, Wellman RD, Buist DS, Kerlikowske K, Tosteson AN, Miglioretti DL; Breast Cancer Surveillance Consortium. Diagnostic Accuracy of Digital Screening Mammography With and Without Computer-Aided Detection. JAMA Intern Med. 2015 Nov; 175(11): 1828-37.
57. Pizot C, Boniol M, Mullie P et al.Physical activity, hormone replacement therapy and breast cancer risk: A meta-analysis of prospective studies Eur J Cancer. 2016 Jan; 52:138-54.
58. Qu X, Zhang X, Qin A et al.Bone mineral density and risk of breast cancer in postmenopausal women.Breast Cancer Res Treat. 2013 Feb; 138(1):261-71.
59. Ramirez K, Acevedo F, Herrera ME et al. Physical activity and breast cancer. Rev Med Chil. 2017 Jan; 145(1):75-84.
60. Reeves GK, Kan SW, Key T et al. Breast cancer risk in relation to abortion: Results from the EPIC study. Int J Cancer. 2006 Oct 1; 119(7):1741-5.
61. Ritte R, Lukanova A, 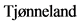 A et al Height, age at menarche and risk of hormone receptor-positive and -negative breast cancer: a cohort study. Int J Cancer. 2013 Jun 1; 132(11):2619-29.
A et al Height, age at menarche and risk of hormone receptor-positive and -negative breast cancer: a cohort study. Int J Cancer. 2013 Jun 1; 132(11):2619-29.
62. Rohan TE, Miller AB. Hormone replacement therapy and risk of benign proliferative epithelial disorders of the breast. Eur J Cancer Prev. 1999 Apr; 8(2): 123-130.
63.  M, Graff-Iversen S, Weiderpass E et al.Postmenopausal Hormone Therapy and Breast Cancer Prognostic Characteristics: A Linkage between Nationwide Registries. Cancer Epidemiol Biomarkers Prev. 2016 Nov; 25(11):1464-1473.
M, Graff-Iversen S, Weiderpass E et al.Postmenopausal Hormone Therapy and Breast Cancer Prognostic Characteristics: A Linkage between Nationwide Registries. Cancer Epidemiol Biomarkers Prev. 2016 Nov; 25(11):1464-1473.
64. Rosner B, Colditz GA, Willett WC. Reproductive risk factors in a prospective study of breast cancer: the Nurses' Health Study. Am J Epidemiol. 1994 Apr 15; 139(8):819-35.
65. Russo J, Rivera R, Russo IH Role of hormones in mammary cancer initiation and progression. Breast Cancer Res Treat. 1992;23(3):211.
66. Russo IH, Russo J J Mammary Gland Biol Neoplasia. 1998;3(1):49.
67. Russo J, Hu YF, Silva ID, Russo IH Cancer risk related to mammary gland structure and development Microsc Res Tech. 2001;52(2):204.
68. Santen RJ, Mansel R. Benign Breast Disorders N Engl J Med 2005;353:275-85.
69. Sardanelli F, Aase HS,  M et al. Position paper on screening for breast cancer by the European Society of Breast Imaging (EUSOBI) and 30 national breast radiology bodies from Austria, Belgium, Bosnia and Herzegovina, Bulgaria, Croatia, Czech Republic, Denmark, Estonia, Finland, France, Germany, Greece, Hungary, Iceland, Ireland, Italy, Israel, Lithuania, Moldova, The Netherlands, Norway, Poland, Portugal, Romania, Serbia, Slovakia, Spain, Sweden, Switzerland and Turkey. Eur Radiol. 2017 Jul; 27(7):2737-2743.
M et al. Position paper on screening for breast cancer by the European Society of Breast Imaging (EUSOBI) and 30 national breast radiology bodies from Austria, Belgium, Bosnia and Herzegovina, Bulgaria, Croatia, Czech Republic, Denmark, Estonia, Finland, France, Germany, Greece, Hungary, Iceland, Ireland, Italy, Israel, Lithuania, Moldova, The Netherlands, Norway, Poland, Portugal, Romania, Serbia, Slovakia, Spain, Sweden, Switzerland and Turkey. Eur Radiol. 2017 Jul; 27(7):2737-2743.
70. Schnitt SJ. Benign breast disease and breast cancer risk: morphology and beyond. Am J Surg Pathol. 2003 Jun; 27(6):836-41.
71. Siegel RL, Miller KD, Jemal A. Cancer Statistics, 2017. CA Cancer J Clin. 2017 Jan; 67(1):7-30.
72. Silvera SA, Rohan TE., 2008 Silvera SA, Rohan TE. Benign proliferative epithelial disorders of the breast: a review of the epidemiologic evidence. Breast Cancer Res Treat. 2008 Aug; 110(3):397-409.
73. Thistlethwaite J.Clinical breast examination for asymptomatic women Australian Family Physician Vol. 36, No. 3, March 2007:145-149
74. Travis RC, Balkwill A, Fensom GK et al. Night Shift Work and Breast Cancer Incidence: Three Prospective Studies and Meta-analysis of Published Studies. J Natl Cancer Inst. 2016 Oct 6; 108(12). https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5241898/
75. Wang K, Li F, Chen L, Lai YM, Zhang X, Li HY. Change in risk of breast cancer after receiving hormone replacement therapy by considering effect-modifiers: a systematic review and dose-response meta-analysis of prospective studies. Oncotarget. 2017 Aug 11; 8(46):81109-81124.
76. White AJ, DeRoo LA, Weinberg CR, Sandler DP.Lifetime Alcohol Intake, Binge Drinking Behaviors, and Breast Cancer Risk. Am J Epidemiol. 2017 Sep 1; 186(5):541-549.
77. https://www.gov.uk/guidance/breast-screening-programme-overview
Приложение 1
ГРАДАЦИИ
ДОСТОВЕРНОСТИ РЕКОМЕНДАЦИЙ И УБЕДИТЕЛЬНОСТИ ДОКАЗАТЕЛЬСТВ
В данных клинических рекомендациях все сведения ранжированы по уровню убедительности рекомендаций и достоверности доказательств в зависимости от количества и качества исследований по данной проблеме.
Уровни достоверности доказательств <*>
Уровень
Тип данных
1a
Мета анализ рандомизированных контролируемых исследований (РКИ)
1b
Хотя бы одно РКИ
2a
Хотя бы одно хорошо выполненное контролируемое исследование без рандомизации
2b
Хотя бы одно хорошо выполненное квазиэкспериментальное исследование
3
Хорошо выполненные неэкспериментальные исследования: сравнительные, корреляционные или "случай-контроль"
4
Экспертное консенсусное мнение либо клинический опыт признанного авторитета
Уровни убедительности рекомендаций <*>
Уровень
Основание рекомендации
A
Основана на клинических исследованиях хорошего качества, по своей тематике непосредственно применимых к данной специфической рекомендации, включающих по меньшей мере одно РКИ
B
Основана на результатах клинических исследований хорошего дизайна, но без рандомизации
C
Составлена при отсутствии клинических исследований хорошего качества, непосредственно применимых к данной рекомендации
--------------------------------
<*> Цит. по: "Медицина, основанная на доказательствах. Руководство для начинающих пользователей"/Под ред Г.Т. Сухих. - М.: ООО "Верди". - 2011. - 179 с. [адапт. из "Levels of Evidence", Oxford Centre for Evidence-based Medicine (2009)] (4).
Приложение 2
МЕТОДИКА
САМООБСЛЕДОВАНИЯ МОЛОЧНЫХ ЖЕЛЕЗ (ИНФОРМАЦИЯ ДЛЯ ПАЦИЕНТКИ)
- Если у вас приходят месячные (то есть вы находитесь в так называемом "репродуктивном" возрасте), самообследование следует проводить раз в месяц на 7 - 10 день от первого дня начала менструации, когда проходят болезненность и набухание груди.
- Если у вас менструальные циклы стали нерегулярными или уже наступила менопауза, делать это необходимо раз в месяц в любое, но фиксированное время вне нагрубания молочных желез.
- Самообследование молочной железы проводится при хорошем освещении. Перед началом самообследования рекомендуется расслабиться и успокоиться. Необходимо относиться к этому мероприятию как к обычной гигиенической процедуре. Большинство изменений, которые можно обнаружить в молочной железе, являются доброкачественными.
- Процедура самообследования молочной железы состоит из семи этапов, однако при правильном и последовательном выполнении она занимает немного времени.
Шаг 1: Осмотр белья
Одним из признаков того, что в молочной железе происходят изменения, могут быть выделения из соска. Незначительные выделения из соска могут остаться незамеченными на его поверхности, но оставлять следы на бюстгальтере. Поэтому необходимо тщательно его осмотреть: нет ли на нем следов выделения из соска в виде кровянистых, бурых, зеленоватых или желтоватых пятен, корочек.
Шаг 2: Общий вид молочных желез
Осмотр молочных желез надо начинать с осмотра сосков и ареол, чтобы убедиться, что нет втяжения, изъязвления, покраснений, высыпаний или других изменений этой зоны. Необходимо раздеться до пояса и встать перед зеркалом. Затем свободно опустить руки. Внимательно рассмотреть в зеркале каждую молочную железу. Проверить, не отмечаются ли какие-то изменения их величины, формы и контуров.
Обязательно следует обратить внимание на симметричность обеих молочных желез: расположены ли они на одном уровне, равномерно ли они перемещаются при поднятии и заведении рук за голову, наклонах туловища, поворотах налево и направо, не отмечается ли фиксация или смещение одной из молочных желез в сторону. Асимметрия размеров и формы груди не всегда является признаком заболевания. Очень часто форма и размеры двух молочных желез у женщин могут несколько отличаться, но если эти отличия появляются и нарастают - это следует учесть.
Далее осматривается надключичная, подключичная и подмышечная области, что позволяет установить сглаженность одной из них, что свидетельствует о наличии увеличенных лимфатических узлов. Медленно поднимите обе руки - это усилит и уточнит указанное зрительное впечатление. Особое внимание следует обратить на наличие отека верхней конечности, шеи, что может быть вызвано нарушением лимфооттока.
Необходимо обращать внимание на возможные изменение формы желез с образованием возвышений, западаний, втягивания кожи или области соска. Внимательно посмотрите, не выделяются ли при этих действиях из соска капли жидкости.
Шаг 3: Состояние кожи.
На этом этапе проверяется состояние кожи, покрывающей молочные железы. Необходимо проверить эластичность кожи, как хорошо она собирается в складку. Надо обращать внимание на изменения цвета кожи, наличие покраснения всей ее поверхности или отдельных участков, нет ли на ней опрелости, сыпи, изменений в виде "лимонной корки".
Кожа прощупывается на предмет ее уплотнений, набухания, наличия ямочек или бугорков на ее поверхности, втянутости, язвочек или сморщенности. При этом брать ткань молочной железы в складку между пальцами не следует, так как из-за ее дольчатого строения у женщины может создаться ошибочное впечатление наличия в ее толще опухолевого уплотнения.
Шаг 4: Самопальпация стоя
При пальпации молочных желез стоя рекомендуется использовать крем или лосьон. Обследование левой молочной железы проводится правой рукой, а правой - левой рукой. Ощупывание проводите подушечками пальцев, а не их кончиками. Для этого надо сомкнуть три или четыре пальца. Затем начать пальпацию круговыми проникающими движениями. Большой палец при этом не участвует. При больших размерах молочной железы ее надо поддерживать противоположной рукой. Имеются два метода самопальпации:
Метод спирали: когда прощупывание молочной железы проводится по спирали, начиная от подмышки и доходя до соска. Подушечками пальцев совершаются круговые движения, перемещаясь в направлении соска.
Метод сегментов: мысленно поделите всю поверхность передней грудной стенки от ключицы до реберного края и молочную железу на небольшие сегменты. Самообследование молочных желез проводится последовательно в каждом сегменте сверху вниз. Нужно выбрать один, наиболее удобный для вас способ и всегда придерживаться именно его - это позволит вам правильно сравнивать результаты пальпации.
Сначала проведите поверхностное прощупывание, при этом подушечки пальцев не проникают в толщу молочной железы. Очень важно делать это, не захватывая кончиками пальцев ткань молочной железы, а прикладывая пальцы плашмя (как минимум, средние и концевые фаланги II - V пальцев). Это дает возможность выявить небольшие неглубокие образования, расположенные непосредственно под кожей. После этого проводится глубокое ощупывание, когда подушечки пальцев последовательно постепенно достигают ребер. Такую пальпацию необходимо проводить от ключицы до нижнего края ребер, и от грудины до подмышечной линии, включая и область подмышек, где можно обнаружить увеличенные лимфоузлы.
Шаг 5: Самопальпация лежа
Техника и последовательность обследования лежа схожа с методикой обследования стоя. Данный этап является наиболее важной частью самообследования молочных желез, потому что только этим способом можно хорошо пропальпировать все их ткани. При этом определяют, каковы молочные железы на ощупь под пальцами и запоминают эти ощущения. Ощупывание проводится лежа на твердой, плоской поверхности. Под лопатку со стороны осматриваемой молочной железы подкладывается подушка в виде валика, чтоб грудная клетка была приподнята, а молочная железа более распластана на грудной клетке. Можно подложить какой-нибудь валик или жесткую подушечку. Руку следует вытянуть вдоль туловища или завести за голову.
Шаг 6: Самопальпация под душем
Можно провести дополнительное самообследование под душем. Мыльные пальцы, скользя по мокрой коже, иногда могут легче обнаружить патологию в молочных железах.
Шаг 7: Обследование соска молочной железы
Проводя осмотр сосков, необходимо определить: не изменены ли их форма и цвет, нет ли в их области втянутости, мокнутия, изъязвлений или трещин. Необходимо пропальпировать сосок и область под соском, так как в этой области может быть опухоль. В конце самообследования молочной железы необходимо осторожно взять сосок большим и указательным пальцами и надавить на него, обращая внимание на то, имеются ли из него выделения и оценить их характер, если они есть.
На что следует обратить внимание?
- Увеличение или уменьшение размеров желез, их формы, симметричности.
- Смещение вверх или в сторону, наличие подвижности или фиксация тканей.
- Нарушение конфигурации желез (втяжения, выпячивания).
- Состояние соска и ареолы (втяжение деформация, изъязвление).
- Состояние кожных покровов железы: локальная или разлитая гиперемия (покраснение) кожи железы, распространение ее на соседние участки.
- Наличие выделений из соска, их характер - молозивные, зеленовато-бурые, серозные, мазеобразные, кровянистые.
- Локальный или тотальный отек по типу "лимонной корки".
- Расширение кровеносных сосудов.
- Наличие узелковых уплотнений, изъязвлений кожи, корок, мокнущих поверхностей, свищей, распада тканей.
При наличии любых изменений в молочной железе, или при возникновении ощущений, не свойственных предыдущему самоосмотру, следует немедленно обратиться к врачу!
Кроме проведения регулярного самообследования, необходимо ежегодно посещать врача акушера-гинеколога для осмотра молочных желез.
