"МУ 1.2.4108-24. 1.2. Гигиена, токсикология, санитария. Оценка воздействия вредных химических соединений на кожные покровы и обоснование предельно допустимых уровней загрязнений кожи. Методические указания"
ГОСУДАРСТВЕННОЕ САНИТАРНО-ЭПИДЕМИОЛОГИЧЕСКОЕ НОРМИРОВАНИЕ
РОССИЙСКОЙ ФЕДЕРАЦИИ
Утверждаю
Руководитель
Федеральной службы по надзору
в сфере защиты прав потребителей
и благополучия человека,
Главный государственный
санитарный врач
Российской Федерации
А.Ю.ПОПОВА
25 декабря 2024 г.
1.2. ГИГИЕНА, ТОКСИКОЛОГИЯ, САНИТАРИЯ
ОЦЕНКА ВОЗДЕЙСТВИЯ ВРЕДНЫХ ХИМИЧЕСКИХ СОЕДИНЕНИЙ НА КОЖНЫЕ
ПОКРОВЫ И ОБОСНОВАНИЕ ПРЕДЕЛЬНО ДОПУСТИМЫХ УРОВНЕЙ
ЗАГРЯЗНЕНИЙ КОЖИ
МЕТОДИЧЕСКИЕ УКАЗАНИЯ
МУ 1.2.4108-24
1. Разработаны ФБУН "ФНЦГ им. Ф.Ф. Эрисмана" Роспотребнадзора (Кузьмин С.В., Ракитский В.Н., Березняк И.В., Федорова Н.Е., Синицкая Т.А., Ильницкая А.В., Федорова С.Г., Вещемова Т.Е., Заволокина Н.Г., Тарасова Л.С., Михеева Е.Н., Артемова О.В., Масальцев Г.В.).
2. Утверждены руководителем Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека, Главным государственным санитарным врачом Российской Федерации А.Ю. Поповой 25 декабря 2024 г.
3. МУ 1.2.4108-24 введены взамен Методических указаний по оценки воздействия вредных химических соединений на кожные покровы и обоснование предельно допустимых уровней загрязнения кожи, утвержденных заместителем Главного государственного санитарного врача СССР 01.11.1979 N 2102-79.
I. Область применения
1.1. Настоящие методические указания (далее - МУ) разработаны для оценки местно-раздражающего и кожно-резорбтивного действия вредных химических соединений разных классов на кожные покровы. Настоящие МУ могут быть применены самостоятельно, а также при оценке воздействия соединения при комплексном (кожным и ингаляционным путями) поступлении в организм.
1.2. МУ предназначены для Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека, а также могут быть использованы специалистами научно-исследовательских организаций, лабораторий и кафедр гигиенического профиля, занимающихся оценкой опасности химических соединений на всех этапах их обращения и их гигиеническим нормированием, проведением производственного контроля за условиями труда <1>.
--------------------------------
<1> Главы I, II СП 2.2.3670-20 "Санитарно-эпидемиологические требования к условиям труда", утвержденных постановлением Главного государственного санитарного врача Российской Федерации от 02.12.2020 N 40 (зарегистрировано Минюстом России 29.12.2020, регистрационный N 61893).
II. Общие положения
2.1. Основой безопасности при работе с химическими соединениями является минимизация непосредственного контакта с ними и предотвращение их поступления в организм ингаляционным и кожным путями. Кожный путь воздействия химических соединений, в том числе пестицидов, на человека в производственных условиях представляет потенциальную опасность для здоровья человека. При регистрационных испытаниях пестицидов, осуществляемых в соответствии с законодательством Российской Федерации <2>, опасность кожного пути воздействия оценивается наравне с ингаляционным.
--------------------------------
<2> Статья 10 Федерального закона от 19.07.1997 N 109-ФЗ "О безопасном обращении с пестицидами и агрохимикатами".
2.2. Настоящие МУ содержат унифицированные подходы к изучению местного раздражающего и кожно-резорбтивного действия химических соединений и установлению гигиенических нормативов их содержания на кожных покровах. Установление величины предельно допустимых уровней (далее - ПДУ) загрязнения кожи (мг/см2) или ориентировочных допустимых уровней (далее - ОДУ) загрязнения кожи (мг/см2) <3>, обоснованной с учетом возможного раздражающего и токсического действия, позволяет оценить риск возникновения острых и хронических проявлений воздействия химических соединений на кожные покровы, как изолировано, так и в комплексе с ингаляционным поступлением, обосновать необходимость технологических и специальных защитных мероприятий, направленных на исключение контакта кожных покровов человека при работе с вредными химическими соединениями.
--------------------------------
<3> Таблица 2.3 СанПиН 1.2.3685-21 "Гигиенические нормативы и требования к обеспечению безопасности и (или) безвредности для человека факторов среды обитания", утвержденных постановлением Главного государственного санитарного врача Российской Федерации от 28.01.2021 N 2 (зарегистрировано Минюстом России 29.01.2021, регистрационный N 62296), с изменениями, внесенными постановлением Главного государственного санитарного врача Российской Федерации от 30.12.2022 N 24 (зарегистрировано Минюстом России 09.03.2023, регистрационный N 72558).
III. Общие рекомендации к изучению местного раздражающего
и кожно-резорбтивного действия химических соединений
3.1. Изучение местного раздражающего/разъедающего действия и резорбции соединения через кожу проводится для новых, внедряемых в производство химических соединений, для химических соединений, широко применяемых в промышленности, но не изученных при воздействии на кожные покровы, и для соединений, при контакте с которыми у работающих выявляются признаки отклонений в состоянии здоровья по данным профилактических медицинских осмотров <4>. Изучению подлежат соединения, находящиеся в жидком или твердом агрегатном состоянии. Устанавливать ПДУ для газообразных соединений не целесообразно, так как соблюдение предельно допустимой концентрации (далее - ПДК) соединения в воздухе рабочей зоны предохраняет организм от токсического воздействия при проникновении его через кожные покровы.
--------------------------------
<4> Приказ Минздрава России от 28.01.2021 N 29н "Об утверждении Порядка проведения обязательных предварительных и периодических медицинских осмотров работников, предусмотренных частью четвертой статьи 213 Трудового кодекса Российской Федерации, перечня медицинских противопоказаний к осуществлению работ с вредными и (или) опасными производственными факторами, а также работам, при выполнении которых проводятся обязательные предварительные и периодические медицинские осмотры" (зарегистрирован Минюстом России 29.01.2021, регистрационный N 62277), с изменениями, внесенными приказом Минздрава России от 01.02.2022 N 668н (зарегистрирован Минюстом России 09.09.2022, регистрационный N 67206).
3.2. Перед проведением исследований проводится анализ физико-химических свойств соединения, параметров токсичности при других путях поступления, некоторых специальных параметров: липофильность, коэффициент распределения октанол/вода (масло/вода); кислотные или щелочные свойства (pH); особенности технологического процесса для построения рабочей гипотезы о наличии и степени раздражающего эффекта, возможности проникновения через кожу, особенностях распределения и прогнозирования токсичности.
3.3. Исследования проводят после сбора и анализа всех доступных данных о раздражающих, токсических свойствах соединения, в том числе уже известных исследований на человеке и (или) лабораторных животных, проверенных и верифицированных данных в исследованиях in vitro, информации о раздражающем воздействии одного или нескольких структурно схожих соединений, что позволяет снизить потребность в исследованиях in vivo с позиции защиты животных.
3.4. Изучение воздействия химических соединений на кожные покровы с последующим обоснованием гигиенических нормативов проводится в 4 этапа:
3.4.1. Исследование и оценка местного действия.
3.4.2. Ориентировочная оценка кожно-резорбтивного действия, в том числе сенсибилизирующего.
3.4.3. Количественная оценка кожной резорбции с установлением:
а) среднесмертельной дозы (далее - LD50) и среднеэффектного времени гибели животных (далее - TL50);
б) порога Limaccut и зоны Zaccut острого действия;
в) коэффициента кумуляции - Kcumcut;
г) порога Limchcut и зоны Zchcut хронического действия;
д) ПДУ загрязнения кожи или ОДУ загрязнения кожи.
3.4.4. Гигиенический контроль содержания вредных соединений на коже работающих с целью обоснования ПДУ загрязнения кожи и оценки риска кожно-резорбтивного действия.
3.5. Выбор животных.
3.5.1. В качестве подопытных животных используются белые крыс с исходной массой 200 - 220 г, мыши (18 - 22 г), морские свинки (300 - 350 г), кролики (2,0 - 3,0 кг). Эксперимент рекомендуется проводить на двух видах животных, включая белых крыс. Для изучения местного раздражающего действия в острых опытах используются кролики породы "Шиншилла", морские свинки - светлой масти.
3.5.2. Количество животных в группе - не менее 10 особей для морских свинок, крыс и мышей, и не менее 3 животных для кроликов. Допустимые различия в массе тела животных - +/- 10% от средней массы.
3.5.3. При наличии информации о возможном выраженном раздражающем/разъедающем (коррозионном) действии соединения проводится предварительное испытание in vitro. Если на основании анализа имеющихся данных принимается решение проводить испытания in vivo, то исследования проводятся на одном животном. Если на одном животном выраженное раздражающее действие не подтвердилось, повторяется эксперимент на двух животных с экспозицией 4 часа. В зависимости от степени выраженности раздражения/повреждения принимается решение о признании разъедающего действия и о целесообразности дальнейшего изучение соединения. При отсутствии необратимых повреждений кожи (язвы, кровотечение, некроз) исследования раздражающего действия продолжаются.
3.6. Подготовка животных к эксперименту.
3.6.1. Участок аппликации составляет не менее 5% от общей поверхности кожи животных, что соответствует 2/3 хвоста у крыс и мышей, или участку кожи на спине крыс 4 x 4 см, кроликов 7 x 8 см, морских свинок 5 x 5 см.
3.6.2. За 1 - 2 дня до эксперимента выстригают ножницами или электробритвой шерсть на спине, обеспечивая доступ к коже животного. В опыте целесообразно использовать животных с чистой, здоровой кожей без механических повреждений. Для изучения местного действия шерсть выстригают на симметричных участках спины по обе стороны от позвоночника, оставляя шерстяной покров между ними в 2 см. Правый бок служит для аппликации изучаемого соединения, левый - для контроля.
3.6.3. Для изучения кожной резорбции исследуют один бок животного, при этом контролем служит другая группа животных.
3.6.4. На время экспозиции для исключения слизывания соединения с кожи и поступления его через органы дыхания животные фиксируются наиболее физиологичным способом. С этой целью применяются специальные станки, либо полужесткие воротники (из резины, пластика); морских свинок, мыши и белые крысы помещаются в индивидуальные домики (рестрейнеры).
3.6.5. Время экспозиции - 4 часа для всех видов животных кроме мышей, контакт для которых составляет 2 часа. Время наблюдения после однократной аппликации: 1 час, 24, 48, 72 часа, 14 дней.
3.7. Способ нанесения.
3.7.1. Исследуемое соединение наносится на 5% участок кожи животного в дозированных количествах из расчета на 1 кг массы тела и на 1 см2 поверхности кожного покрова и равномерно распределяется.
3.7.2. Рекомендуется, чтобы проба исследуемого соединения соответствовала чистому соединению или смеси соединений, которые потенциально могут воздействовать на человека в реальных производственных условиях. Допустимо проводить исследование с использованием радиоактивных меток.
3.7.3. Изучаемое соединение наносят, преимущественно, в чистом виде. В случае невозможности нанесения соединения в чистом виде, а также при наличии выраженного раздражающего либо токсического эффекта, исследуют разведения изучаемых соединений. В качестве растворителей и разбавителей допустимо использовать дистиллированную воду, физиологический раствор, модельную среду, имитирующую потовую жидкость (таблица 1). При невозможности разведения соединения в перечисленных выше растворителях допускается применение растительного и вазелинового масла, ланолина, этилового спирта или ацетона.
Таблица 1
Модель "потовой жидкости"
N
Соединение
Количество (мг, мл)
1
Натрий хлористый
2000 мг
2
Калий хлористый
300 мг
3
Кальций хлористый
40 мг
4
Молочная кислота
1000 мг
5
Мочевина
400 мг
6
Аммоний сернокислый
350 мг
7
Нашатырный спирт (водный раствор аммиака 10%)
1 мл
8
Аспарагиновая кислота
200 мг
9
Фенол х/ч
80 мг
10
Ацетон
30 мг
Примечание: перечисленные компоненты растворяют в 1 л дистиллированной воды, доводя pH до 4,5 (с помощью 1 М раствора соляной кислоты). Водородный показатель (pH) контролируют с применением pH-метра.
3.7.4. Нанесение соединения осуществляется открытым способом или под негерметичной повязкой, например, нейлоновой, марлевой. В случае если прямое наложение невозможно (например, с жидкостями или некоторыми пастами), соединение наносят на марлевую повязку, а затем прикладывают к коже таким образом, чтобы соединение было равномерно распределено по повязке, повязка не сдавливала животное, но удерживалась посредством подходящего материала на протяжении всего периода воздействия, плотно контактируя с кожей животного.
Для высоколетучих соединений (температура кипения до плюс 100 °C) используют закрытый способ нанесения: метод наклейки капсул и часовых стекол. После нанесения соединения на кожу, обработанное место может быть защищено специальным стандартным устройством (рисунок).
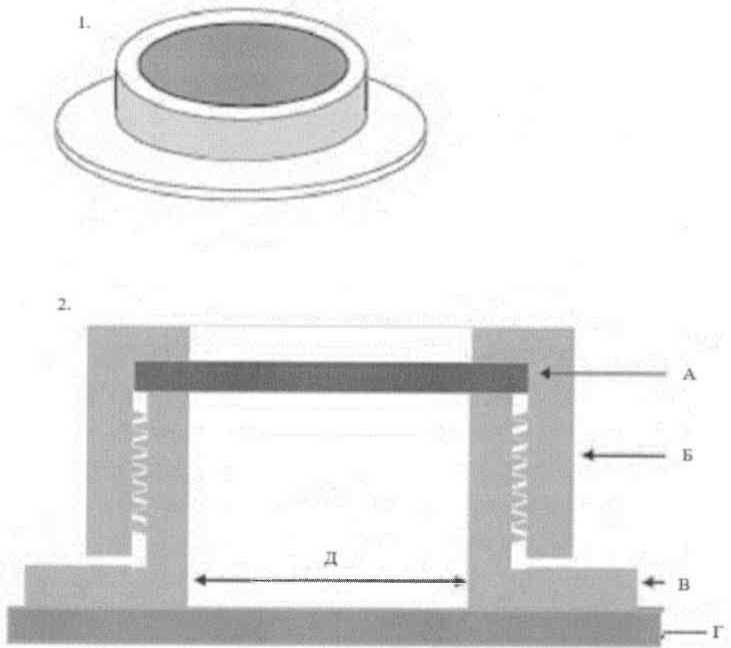
Рисунок. Пример стандартного устройства, используемого
для ограничения и защиты места нанесения соединения
во время исследований перкутанной абсорбции in vivo.
Примечания: 1 - вид стандартного устройства снаружи;
2 - схема стандартного устройства изнутри; А - фильтр
из активированного угля или марлевая повязка; Б - насадка
с резьбой; В - основа с резьбой; Г - кожа;
Д - цианоакрилатный клей
В случае возможного испарения соединение допустимо улавливать угольными фильтрами устройства. После нанесения на выстриженную кожу спины животного, зафиксированного в станке, точного количества изучаемого соединения, этот участок кожи покрывается раструбом обычной стеклянной воронки, имеющей по бокам специально сделанные 4 отверстия диаметром 2 - 3 мм. Воронка плотно фиксируется на теле животного цианоакрилатным клеем. Затем воронка соединяется с поглотителем Рихтера (или какими-либо другими поглотителями) при помощи изогнутой под прямым углом стеклянной трубки, концы которой соединены резиновыми муфтами с одной стороны с горловиной воронки, а с другой с входным концом трубки поглотителя. После этого при помощи аспиратора начинается отсос воздуха с парами исследуемого соединения из-под воронки при объемной скорости 10 - 50 мл воздуха в минуту и так далее. В зависимости от целей эксперимента и летучести соединения продолжительность отсасывания воздуха из-под воронки может составлять до 4 часов. В течение опыта поглотители можно несколько раз заменить на новые, если стоит задача изучить динамику испарения соединения с поверхности кожи. Количество испарившегося соединения определяется в поглотительном растворе химико-аналитическими или другими подходящими для этой задачи методами. После окончания опыта производятся смывы с данного участка кожи, чтобы определить остаточное количество соединения. Из общей дозы, нанесенной на кожу, производится вычитание количества испарившегося соединения и оставшегося на коже. В итоге устанавливается количество соединения, поступившее в организм через кожу.
При изучении кожно-резорбтивного действия в длительном (подострый, хронический) эксперименте, испытуемое соединение наносится на кожу 2/3 поверхности хвоста мышей или крыс, который для этого помещается в стеклянную коническую пробирку на время экспозиции. Используемые лабораторные животные фиксируются путем помещения в специальные индивидуальные домики (рестрейнеры).
3.7.5. Эксперимент проводят при контролируемых параметрах микроклимата: температуре воздуха в помещении плюс (22 +/- 3) °C (для грызунов) и (20 +/- 3) °C (для кроликов); относительной влажности воздуха 30 - 70% (оптимально 50 - 60%).
В местах содержания и проведения манипуляций с животными обеспечивается искусственное освещение: 12 часов - свет, 12 часов - темнота. При кормлении может быть использована обычная лабораторная диета с неограниченным количеством питьевой воды.
3.7.6. Контрольные животные содержатся в одинаковых условиях. На соответствующие участки кожи им наносится растворитель или разбавитель, используемый в опыте. При изучении местного действия контролем служит противоположный участок кожи того же животного.
3.8. Способ смыва.
3.8.1. После окончания экспозиции остатки соединения удаляются теплой водой с мылом, избегая грубых приемов и манипуляций, способных вызывать повреждение кожи.
3.8.2. Установление количественных параметров токсичности при резорбции соединения возможно при условии получения сведений о количестве соединения, проникшего в организм. С этой целью определяют остаточные количества соединения на коже. Определение соединения в смывах проводится сразу после экспозиции при установлении LD50, Limaccut и Limchcut (не менее 8 раз в течение хронического эксперимента).
3.8.3. Как для проведения смыва, так и для его анализа рекомендуется применять специфический избирательный химический метод. При выборе жидкости, применяемой для смыва, учитывают:
а) способность жидкости растворять искомые соединения;
б) безвредность ее как для кожи, так и для целостного организма (например, этиловый спирт, слабая кислота, слабая щелочь).
3.8.4. Специально обработанной хлопчатобумажной салфеткой, смоченной в жидкости, с помощью пинцета проводят смыв с участка кожи, на котором проводили аппликацию соединения (таблица 2). Манипуляция повторяется не менее 3 раз. После каждого контакта с кожей салфетка промывается в смывающей жидкости. Пробу смыва (емкость со смывающей жидкостью и салфетка) помещают в емкость с крышкой, маркируют и помещают в контейнер для транспортировки в аналитическую лабораторию.
Таблица 2
Средства для проведения смыва
N
Наименование
1
Пинцет медицинский нержавеющий, ГОСТ 21241-2023 <5>
2
Стеклянные емкости вместимостью 100 см3 с герметичной крышкой, содержащие 20 см3 смывающей жидкости
3
Салфетки из белой хлопчатобумажной вязи, подготовленные по следующей схеме:
- вырезать салфетки размером 10 x 10 см;
- кипятить в 5% растворе углекислого кислого натрия (навеска 50 +/- 0,1 г натрия углекислого кислого растворить в дистиллированной воде в мерной колбе вместимостью 1000 см3) салфетки (на 10 салфеток 1 л раствора) в течение 5 - 10 минут и оставить в растворе на 8 - 14 часов;
- промыть в холодной проточной водопроводной воде не менее 30 минут;
- промыть салфетки последовательно в 3 емкостях с дистиллированной водой, контролировать pH промывных вод с помощью индикаторной бумаги (целевое значение - pH 6 - 7);
- Двухкратно салфетки промыть в емкости с 96% этиловым спиртом ректификованным (из расчета 100 мл на 10 салфеток), отжать с помощью пинцета, после чего разложить салфетки на фильтровальной бумаге. Закрыть сверху вторым листом бумаги. Сушить при комнатной температуре в течение 24 часов.
Просушенные салфетки упаковать в фольгу. Хранить упакованные салфетки в сухом помещении в лабораторном шкафу (срок хранения не ограничен).
Примечание: допускается использование средств для проведения смыва с аналогичными или лучшими характеристиками.
--------------------------------
<5> ГОСТ 21241-2023 "Пинцеты медицинские. Общие технические требования и методы испытаний", введенный приказом Росстандарта от 22.09.2023 N 929-ст.
3.8.5. Для малолетучих соединений количество соединений, проникшее в организм, рассчитывают по формуле (1) или по формуле (2):
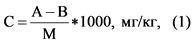
где: C - количество соединения, проникшее в организм в мг/кг;
A - количество соединения, нанесенное на кожу в мг;
B - количество соединения в смыве в мг;
M - масса тела в г.
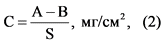
где: C - количество соединения, проникшее в организм в мг/см2;
A - количество соединения, нанесенное на кожу в мг;
B - количество соединения в смывах в мг;
S - участок аппликации соединения на коже в см2.
Для летучих соединений в формулы 1 и 2 вносят поправку на испарение (п. 3.7.4).
3.8.6. При наличии возможности определения соединения или его метаболитов в биосредах расчет проникшего в организм соединения производят, исходя из определяемых количеств.
IV. Оценка местного действия химического соединения на кожу
4.1. Исследования проводят в острых (однократных) опытах. В качестве подопытных животных используются морские свинки (300 - 350 г), кролики (2,0 - 3,0 кг). Для изучения местного действия в острых опытах используются кролики породы "Шиншилла", морские свинки - светлой масти. Использование животных других видов возможно при предоставлении достаточного обоснования. Количество животных в группе составляет не менее 10 особей для морских свинок и не менее 3 животных для кроликов.
На кожу первоначально наносится 20 мг/см2 соединения. Реакция кожи регистрируется по окончании экспозиции, через 1 и 24, 72 часа и 14 дней после однократной аппликации.
Продолжительность периода наблюдений выбирают таким образом, чтобы в полной мере можно было оценить обратимость наблюдаемых эффектов. Однако эксперимент прекращается, если у животного наблюдаются продолжительные признаки сильной боли или дистресса. Для определения обратимости реакций животные находятся под наблюдением в течение 14 дней после удаления пробы. Эксперимент целесообразно закончить досрочно в случае наблюдения обратимости реакций до окончания 14 дней наблюдений.
4.2. Функциональные нарушения кожи характеризуются появлением различной степени выраженности эритемы, отека, трещин, изъязвлений, изменением температуры и скорости проницаемости эпидермиса, снижением сопротивления кожи постоянному электрическому току, уменьшением ее нейтрализующей способности. Оценку воздействия изучаемого соединения на кожный покров рекомендуется проводить по критериям, приведенным в таблицах 3 - 5 <6>.
--------------------------------
<6> Методические указания к постановке исследований по изучению раздражающих свойств и обоснованию предельно допустимых концентраций избирательно действующих раздражающих веществ в воздухе рабочей зоны, утвержденные заместителем Главного государственного санитарного врача СССР 11.08.1980 N 2196-80 (далее - МУ N 2196-80).
Оценка степени эритемы (таблица 3) и отека (таблица 4) суммируются для каждого подопытного животного, после чего вычисляется средняя оценка выраженности раздражающего свойства соединения для группы экспериментальных животных, позволяющая проводить межгрупповое сравнение (таблица 5).
Таблица 3
Оценка степени эритемы
N
Интенсивность эритемы (визуальная оценка)
Оценка эритемы, в баллах
1
Отсутствие эритемы
0
2
Слабая эритема (едва заметная, розовый тон)
1
3
Умеренно-выраженная эритема (розово-красный тон)
2
4
Выраженная эритема (красный тон)
3
5
Резко выраженная эритема (говяжья краснота) - образование ожога, препятствующего классификации эритемы (ярко-красный тон)
4
Примечание: выраженность эритемы измеряется визуально.
Таблица 4
Оценка отека кожи животных
Интенсивность отека (увеличение толщины кожной складки, мм)
Оценка отека (в баллах)
Кролики
Морские свинки
Отсутствие
0
0
0
Слабый
до 0,5
до 0,3
1
Умеренный
0,6 - 1,0
0,4 - 0,6
2
Выраженный
1,1 - 2,0
0,7 - 1,0
3
Резко выраженный
> 2,0
> 1,0
4
Примечание: величина отека определяется путем измерения толщины кожной складки (мм), например, при помощи микрометра типа МК (МК - гладкие для измерений наружных размеров изделий) 1 - 2 класса точности с отсчетом показаний по шкалам стебля и барабана 0,01 мм, с диапазоном измерений 0 - 25 мм, произведенного в соответствии с документами по стандартизации <7>.
--------------------------------
<7> ГОСТ 6507-90 "Микрометры. Технические условия", введенный постановлением Госстандарта СССР от 25.01.1990 N 86.
Таблица 5
Классификация раздражающего действия
Классы
Средний суммарный балл выраженности эритемы и величины отека
Выраженность раздражающего действия
0
0
Отсутствие раздражающего действия
1
0,1 - 2,0
Слабораздражающее действие
2
2,1 - 4,0
Умеренное раздражающее действие
3
4,1 - 6,0
Выраженное раздражающее действие
4
6,1 - 8,0
Резко выраженное раздражающее действие;
чрезвычайно сильное раздражающее действие
5
Неразбавленное соединение вызывает некроз
6
50% раствор вызывает некроз
7
25% раствор вызывает некроз
8
10% раствор вызывает некроз
9
5% раствор вызывает некроз
10
Растворы менее 5% вызывают некроз
4.3. Раздражающее действие оценивается с учетом тяжести поражения и обратимости. Обратимость кожных поражений рассматривается, исходя из оценки реакции раздражения. Если реакции кожи, такие как алопеция, гиперкератоз, гиперплазия и шелушение, сохраняются до конца 14-дневного срока наблюдения, исследуемое соединение признают раздражающим. Реакция кожи, проходящая до 14 дней, оценивается в соответствии с классификацией (таблица 5).
4.4. При необходимости, для соединений, относящихся к 1 - 4 классам по степени выраженности раздражающего действия на кожу, целесообразно устанавливать величину минимального разбавления, вызывающего раздражающий эффект у 50% животных (порог однократного действия соединения), и минимального разбавления, не вызывающего раздражения кожи.
4.5. Для соединений, относящихся к 5 - 10 классам по степени выраженности раздражающего действия на кожу, изучение кожно-резорбтивного действия не проводят в связи с тем, что в дополнении к высокому групповому показателю эритемы и отека (более 6,1 балла), неразбавленное соединение, или его растворы (содержание от 50% до менее 5%) способны вызывать некроз.
4.6. Для соединений, относящихся к 4 - 10 классам по раздражающему действию на кожу, ставится пометка "местное действие" (м. д.), т.е. опасны при попадании на кожу и слизистые оболочки глаз.
4.7. Оценка сенсибилизирующего действия химического соединения на кожу.
4.7.1. Кожная сенсибилизация изучается путем подкожной инъекции и (или) накожного нанесения соединения. Используют не менее 10 опытных и 5 контрольных морских свинок.
4.7.2. Оптимальным является использование максимизационного теста или теста Бюхлера, при которых провокационная проба наносится на участок кожи противоположный боку, на котором проводили индукционные аппликации. Кожная реакция оценивается в соответствии с классификацией по шкале Магнуссона-Клигмана <8> (таблица 6).
--------------------------------
<8> Приложение 6.5 Р 1.2.3156-13 "Оценка токсичности и опасности химических веществ и их смесей для здоровья человека", утвержденного врио руководителя Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека, Главного государственного санитарного врача Российской Федерации 27.12.2013.
Таблица 6
Классификация кожной реакции при оценке
N
Реакция в провокационном тесте
Баллы
1
Отсутствие видимых изменений
0
2
Разрозненная или неоднородная эритема
1
3
Умеренная или сплошная эритема
2
4
Интенсивная эритема и отек
3
4.7.3. Максимизационный тест на морских свинках проводится следующим образом. Рекомендуется, чтобы группа, подвергающаяся воздействию, содержала не менее 20 животных, контрольная группа - не менее 10.
Концентрация исследуемого соединения для индукционной экспозиции выбирается таким образом, чтобы она была хорошо физиологически переносима и вызывала легкое или умеренное раздражение кожи. Концентрация в провокационной экспозиции подбирается таким образом, чтобы она не вызывала раздражение. Подходящие концентрации определяются в предварительном испытании на 2 - 3 животных, если другая информация отсутствует. Для этой цели предпочтение отдается ПАФ-обработанным (полный адьювант Фрейнда) животным.
Индукционная экспозиция: подкожные инъекции.
День 0 - исследуемая группа. Три пары подкожных инъекций объемом 0,1 мл вводятся в плечевую область, очищенную от шерсти таким образом, чтобы инъекции были по обе стороны срединной линии: инъекция 1 - смесь 1:1 (по объему) ПАФ/вода или физиологический раствор; инъекция 2 - исследуемое соединение в подходящем растворителе в выбранной концентрации; инъекция 3 - исследуемое соединение в выбранной концентрации в смеси 1:1 (по объему) ПАФ/вода или физиологический раствор.
В инъекции 3 растворимые в воде соединения до смешивания с ПАФ растворяются в воде. Жирорастворимые или нерастворимые соединения до перемешивания с водой растворяются в ПАФ. Конечная концентрация исследуемого соединения равняется концентрации в инъекции 2.
Инъекции 1 и 2 вводятся близко друг другу и к голове животного, в то время как инъекция 3 вводится ближе к хвостовой части тестовой области.
День 0 - контрольная группа. Три пары подкожных инъекций объемом 0,1 мл вводятся в одно и то же место животным, не подвергшимся обработке: инъекция 1 - смесь 1:1 (по объему) ПАФ/вода или физиологический раствор; инъекция 2 - неразбавленный растворитель; инъекция 3 - 50% растворителя в смеси 1:1 (по объему) ПАФ/вода или физиологический раствор.
Индукционная экспозиция: местное нанесение.
День 5 - 7 - тестовая и контрольная группы. За 24 часа до нанесения соединения, если соединение не является раздражающим для кожи, тестовая область после стрижки или бритья обрабатывается 0,5 мл 50% лаурилсульфатом натрия в вазелине для того, чтобы вызвать местное раздражение.
День 6 - 8 - тестовая группа. С тестовой области снова удаляется шерсть. Фильтровальная бумага (2 x 4 см) полностью заполняется исследуемым соединением в подходящем растворителе (с приведением обоснования выбора растворителя) и накладывается на тестовую область под герметичную повязку на 48 часов. Твердые соединения измельчаются и помещаются в подходящий растворитель. Жидкости допускается наносить неразбавленными.
День 6 - 8 - контрольная группа. С тестовой области снова удаляют шерсть. На тестовую область наносится только растворитель. Фильтровальная бумага (2 x 4 см) полностью заполняется исследуемым растворителем в количестве, равном тому, что наносится в тестовой группе, и накладывается на тестовую область под герметичную повязку на 48 часов.
Провокационная экспозиция: местное нанесение.
День 20 - 22 - тестовая и контрольная группы. С боков тестовых и контрольных животных удаляется шерсть. Пластырь, заполненный тестовым соединением, накладывается на один бок животного. Допускается накладывать пластырь, заполненный растворителем, на другой бок того же животного. Пластырь удерживается на коже под герметичной повязкой в течение 24 часов.
Наблюдения: тестовая и контрольная группы. Через 21 час после удаления пластыря контрольная область очищается, шерсть коротко остригается, бреется или депилируется. Через 3 часа (через 48 часов с начала контрольного нанесения) наблюдается кожная реакция и регистрируется в соответствии с классификацией (таблица 6).
Через 24 часа после данного наблюдения (72 часа) проводится второе наблюдение, и снова регистрируется реакция.
4.7.4. Тест Бюхлера проводится следующим образом. В тестовой группе рекомендуется использовать не менее 20 животных, в контрольной - 10.
Концентрации исследуемого соединения для каждой индукционной экспозиции подбираются таким образом, чтобы она была максимально возможной (при слабом раздражающем действии). Концентрация, используемая в провокационной экспозиции, подбирается таким образом, чтобы она была максимальной, не вызывающей раздражение. Подходящие концентрации определяют в предварительном тесте с использованием 2 - 3 животных, если другая информация отсутствует.
Для растворимых соединений рекомендуется использовать воду или не вызывающий раздражение раствор поверхностно-активных веществ (ПАВ) в качестве растворителя. Для других исследуемых соединений используется 80% смесь этанола/воды, подходящая для индукционной экспозиции, ацетон - для провокационной пробы.
Индукционная экспозиция: местное нанесение.
День 0 (до экспозиции) - тестовая группа. С одного бока животного удаляется (коротко остригается) шерсть. Тестовый пластырь полностью заполняется исследуемым соединением в подходящем растворителе (жидкие исследуемые соединения допускается наносить не разбавленными). Исследуемое соединение накладывается на тестовую область и удерживается на коже под герметичной повязкой или пластырем в течение 6 часов.
Обеспечивают герметичность тестовой системы. Подходит ватный диск, круглый или квадратный, размером примерно 4 - 6 см. Для гарантии герметичности предпочтительно использовать фиксацию подходящей повязкой.
День 0 (до экспозиции) - контрольная группа. На одном боку животного удаляется (коротко остригается) шерсть. На кожу тем же путем, что и для тестовой группы, наносится только растворитель. Тестовая система удерживается на коже герметичным пластырем или подходящей повязкой в течение 6 часов.
День 6 - 8 и 13 - 15 - тестовая и контрольная группы. На 6 - 8, а потом на 13 - 15 дни та же тестовая область того же бока животного (шерсть удаляют, если необходимо) обрабатывается тем же способом, что и в 0 день.
Провокационная экспозиция.
День 27 - 29 - тестовая и контрольная группы. С необработанного бока животных тестовой и контрольной групп удаляется (коротко остригается) шерсть. На заднюю часть остриженного бока животных тестовой и контрольной групп накладывается повязка, содержащая необходимое количество исследуемого соединения в максимально возможной концентрации, не вызывающей раздражение. Если необходимо, то повязку или пластырь с растворителем также накладывают на переднюю часть бока животных тестовой и контрольной групп. Пластырь удерживают герметичной повязкой на коже в течение 6 часов.
Наблюдения: тестовая и контрольная группы. Через 21 час после удаления пластыря с контрольной области удаляется шерсть.
Через 3 часа (через 30 часов после наложения контрольного пластыря) наблюдаются кожные реакции и регистрируются в соответствии с классификацией, приведенной для максимизационного теста (см. п. 4.7.2, таблицу 6).
Через 24 часа после осмотра (через 54 часа после наложения контрольного пластыря) кожные реакции вновь наблюдаются и регистрируются.
4.7.5. При необходимости, для получения информации о сенсибилизации, можно применять другие методы <9>. Так, при изучении простых химических соединений рекомендуется применение метода сенсибилизации морских свинок внутрикожно в зону уха и (или) воспроизведение гиперчувствительности замедленного типа (далее - ГЗТ) на мышах.
--------------------------------
<9> МУ 1.1.578-96 "Требования к постановке экспериментальных исследований по обоснованию предельно допустимых концентраций промышленных химических аллергенов в воздухе рабочей зоны и атмосферы", утвержденные Первым заместителем Председателя Госкомсанэпиднадзора, заместителем Главного государственного санитарного врача 21.10.1996.
При изучении сложных по составу соединений целесообразно осуществлять комбинированную сенсибилизацию морских свинок (в кожу уха и дополнительно на кожу). Так же могут быть использованы и другие способы сенсибилизации животных. Например, при исследовании химических соединений, особенно пастообразных и вязких, загрязняющих кожные покровы рабочих, целесообразна проверка возможности развития контактной аллергии методом многократных накожных аппликаций на морских свинках.
Для оценки иммунологической реактивности в крови у морских свинок через 48 часов после провокационной пробы проводится определение реакции специфического лизиса лейкоцитов (РСЛЛ), лейкоцитарной формулы крови. Кожную сенсибилизацию позволительно оценивать по реакции региональных лимфатических узлов в сочетании с другими методами.
V. Оценка кожно-резорбтивного действия химических соединений
5.1. Ориентировочная оценка кожно-резорбтивного действия. Ориентировочная оценка кожно-резорбтивного действия может осуществляться "пробирочным методом" и нанесением соединения на кожу спины лабораторного животного.
5.1.1. Для того, чтобы установить возможность развития интоксикации при однократном воздействии, погружают хвосты мышей или крыс в исследуемый продукт в пробирке ("пробирочный" метод) на 2 часа (мыши) или на 4 часа (крысы), так как это дает возможность оценить воздействие на кожу максимально возможных количеств соединения. Принимают меры для исключения попадания паров соединения из пробирки в дыхательные пути животного, например, путем герметизации пробирки с соединением.
5.1.2. Нанесение соединения на кожу спины начинается с 20 мг/см2 (максимально наносимое количество соединения на кожу кроликов) при отсутствии местного раздражающего действия (класс 0). Для соединений 1 - 4 классов используется минимальное разбавление соединения, не вызывающее раздражающего эффекта в острых опытах. Соединения, имеющие экстремальные значения pH менее 2.0 и более 11.5 (щелочи и кислоты) наносятся только в разведении, не вызывающем раздражающего эффекта.
5.1.3. Для установления видовой чувствительности рекомендуется использовать не менее 2 видов лабораторных животных (самки крысы обязательны).
5.1.4. Учет реакции ведется по гибели животных или по развитию клинических признаков интоксикации.
5.1.5. В случаях отсутствия клинических признаков воздействия после однократной аппликации изучение кожной резорбции проводится в подостром эксперименте (20 аппликаций) в течение 4 недель по 5 раз в неделю.
5.1.6. Изучение состояния подопытных животных проводится через 5, 10, 20 аппликаций с привлечением интегральных и специфических показателей. Целесообразно использовать показатели, оказавшиеся чувствительными при ингаляционном и пероральном путях поступления <10>. При необходимости допустимо проводить определение исследуемого соединения и его метаболитов в биосредах (кровь, моча) при помощи поверенных автоматических анализаторов. Один из интегральных показателей, рекомендуемых к исследованию - вес тела, который измеряют у всех животных один раз в неделю при помощи поверенных прецизионных весов с функцией взвешивания нестабильных грузов.
--------------------------------
<10> Методические указания к постановке исследований для обоснования санитарных стандартов вредных веществ в воздухе рабочей зоны, утвержденные Главным государственным санитарным врачом СССР 04.04.1980 N 2163-80.
5.1.7. Если на данном этапе не выявлено резорбтивного действия соединения, дальнейшие исследования по изучению кожного воздействия прекращаются.
5.1.8. Если при воздействии самой высокой возможной дозы (2500 мг/кг) смертельный исход маловероятен, проводится исследование по определению пороговой дозы. Порогом вредного действия соединения (острого и хронического) называется <11> минимальная доза нанесенного на кожу соединения, которая вызвала в адекватной статистической группе животных изменения, выходящие за пределы физиологических приспособительных реакций, или возникновение скрытой (временно компенсированной) патологии. Порог вредного действия характеризуется следующими признаками:
--------------------------------
<11> МУ N 2196-80.
а) изменения достоверно (p <= 0,05) отличаются от контроля и выходят за пределы физиологических колебаний показателя для данного вида животных и данного времени года;
б) достоверных (p <= 0,05) изменений по сравнению с контролем нет, но наблюдаются скрытые нарушения равновесия с внешней средой, выявляемые, в частности, при помощи функциональных нагрузок;
в) изменения достоверно (p <= 0,05) отличаются от контроля, находятся в пределах физиологической нормы, однако стойко сохраняются в хроническом эксперименте на животных (более 1 месяца).
г) проведение параллелей между результатами биохимических, физиологических и морфологических исследований. Если функциональные изменения выходят за пределы гомеостатических колебаний и сопровождаются изменениями структуры тканей и органов, то найденные сдвиги следует рассматривать как патологические, вредные для организма. Если обнаруженные функциональные изменения прогрессируют во времени и тем более, если они не исчезают в восстановительный период, тогда они расцениваются как вредные, патологические.
5.1.9. В случае гибели животных при однократном воздействии или при наличии изменений показателей, используемых в подостром эксперименте, выходящих за порог вредного действия, к ПДК соединения в воздухе рабочей зоны вносится пометка "+" - соединение, при работе с которым требуется специальная защита кожи и глаз". Для указанной группы соединений устанавливаются ПДУ загрязнения кожи. С этой целью приступают к следующему этапу исследований - количественной оценке кожно-резорбтивного поступления вредных химических соединений в организм.
5.2. Количественная оценка кожно-резорбтивного поступления вредных химических соединений в организм при однократном воздействии.
5.2.1. Установление LD50cut и TL50cut.
Для выбора начальных доз с целью определения LD50 используют уравнения, учитывающие корреляционную связь между параметрами токсичности органических соединений при различных путях (формулы 3 - 5):
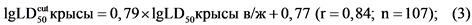
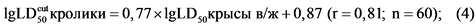
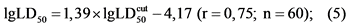
Расчетные значения TL50 могут быть получены из формулы (6):
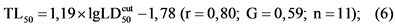
Наиболее часто определяется зависимость между LD50cut и TL50cut, представленная в таблице 7.
Таблица 7
Зависимость среднесмертельной дозы от среднеэффективного
времени гибели животных
LD50cut, мг/кг
TL50cut, мин
50
5
51 - 300
3 - 15
301 - 2000
15 - 120
2000
120
5.2.2. Кроме смертельных эффектов учитываются клинические признаки интоксикации, время их появления, выраженность и другие объективные показатели, аналогичные проявлениям при других путях воздействия соединений (изменение массы тела, поведенческие реакции, биохимические, гематологические показатели).
5.2.3. Расчет LD50 проводится в мг/кг, а также в мг/см2, методом пробит-анализа.
5.2.4. Степень опасности химического соединения при кожном пути поступления по величинам LD50cut устанавливается в соответствии со следующими диапазонами (таблица 8).
Таблица 8
Классификация кожно-резорбтивного действия по LD50cut
Класс опасности
LD50cut, мг/кг
1
< 100
2
100 - 500
3
501 - 2500
4
> 2500
5.2.5. Определение порога Limaccut острого действия. В эксперименте для определения Limaccut исследуют не менее 3 уровней. Разрыв между ними определяет степень токсичности соединения и его кумулятивные свойства. Выбор показателей для определения воздействия соединения проводится с учетом изменений, выявленных при ингаляционном и других путях поступления соединения. Порог вредного действия устанавливается по интегральным и специфическим показателям.
5.2.6. Зона острого действия (Zaccut) при дермальном поступлении вычисляется по отношению средней смертельной концентрации (дозы) к пороговой концентрации (дозе) при однократном воздействии по формуле (7):
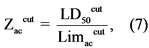
где: LD50cut - средняя смертельная концентрация (доза) при однократном накожном нанесении в мг/кг;
Limaccut - пороговая концентрация (доза) при однократном накожном нанесении в мг/кг.
5.3. Исследование кумулятивных свойств.
5.3.1. В качестве подопытных животных используются белые крысы с исходной массой 200 - 220 г. Количество животных в группе не менее 10 особей. Изучение кумуляции соединения проводится при 20 кратном нанесении на кожу 1/5, 1/10, или 1/20 LD50cut в течение месяца. Дозу, вводимую животным, выбирают экспериментально исходя из LD50cut, установленной в однократном опыте.
5.3.2. В качестве показателя кумулятивного действия соединения при поступлении его через кожу позволительно использовать дозы, вызывающие не только гибель (ее может не быть), а и небольшие, но статистически достоверные сдвиги каких-либо чувствительных показателей (пороговые дозы), а также промежуток времени, в течение которого развился определенный объективно регистрируемый эффект (ET50).
5.3.3. В случае, когда животные погибают, кумулятивные свойства соединения характеризуются коэффициентом кумуляции: отношением LD50cut при многократном нанесении к LD50cut при однократной аппликации на кожу по формуле (8):
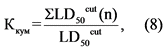
где: 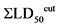 - средняя смертельная концентрация (доза) при многократном накожном нанесении в мг/кг;
- средняя смертельная концентрация (доза) при многократном накожном нанесении в мг/кг;
LD50cut - средняя смертельная концентрация (доза) при однократном накожном нанесении в мг/кг.
5.4. Определение порога Limch хронического действия.
5.4.1. Опыты проводятся на белых крысах по 4 часа в день 5 раз в неделю на протяжении 4 месяцев.
5.4.2. Выбор уровней воздействия основывается на знании свойств соединения (например, быстрое обезвреживание, метаболизирование, способность к кумуляции). Исследования проводятся на двух - трех уровнях воздействия ниже Limaccut.
5.4.3. Рекомендуется, чтобы самый высокий уровень дозы вызывал токсический эффект, без смертельного исхода, самый низкий уровень дозы не вызывал никаких признаков интоксикации.
Для изучения проявлений воздействия применяется комплекс функциональных, биохимических и морфологических показателей, связанных с характером биологического действия соединения. Исследования проводятся с использованием методов и методик, применяемых для оценки токсических свойств соединений при пероральном поступлении. Наряду с применением интегральных и специфических показателей, характеризующих действие вредного соединения на организм, проводится изучение скорости всасывания соединения через кожу, кинетики и метаболизма его в организме.
5.4.4. Исследование состояния животного проводят в динамике. В течение всего эксперимента наблюдают за состоянием животных, еженедельно взвешивают, ежемесячно проводят клинические биохимические анализы, регистрируются изменение поведенческих реакций и т.д.
После окончания эксперимента половина животных в каждой группе умерщвляется, вторая половина оставляется на 28 дней после эксперимента, для выявления способности к восстановлению или необратимости токсических эффектов.
Все животные в исследовании подвергаются макроскопической аутопсии. Рекомендуется все макроскопические поражения, кожу, органы-мишени подвергать гистологическому изучению.
5.4.5. Зона хронического действия вычисляется по отношению пороговой концентрации (дозы) при однократном воздействии к пороговой концентрации (дозе) при хроническом воздействии по формуле (9):
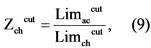
где: Limaccut - пороговая концентрация (доза) при однократном накожном нанесении в мг/кг;
Limchcut - пороговая концентрация (доза) при хроническом накожном воздействии в мг/кг;
5.5. Обоснование ПДУ загрязнения кожи.
5.5.1. ПДУ загрязнений кожных покровов в мг/см2 рассчитывается с учетом величины экспериментального порога хронического действия и коэффициента запаса (от 3 до 20).
5.5.2. Обоснование коэффициента запаса производится с учетом:
- среднесмертельной дермальной дозы LD50cut;
- времени контакта с кожей, приводящей к 50% гибели TL50cut;
- порога (Limaccut) и зоны (Limaccut) острого действия;
- коэффициента кумуляции Kcumcut;
- порога (Limchcut) и зоны (Limchcut) хронического действия.
5.5.3. Коэффициент запаса возрастает:
- с увеличением абсолютной токсичности;
- с уменьшением величины TL50 и увеличением скорости всасывания соединения через кожу;
- с уменьшением зоны острого действия;
- с увеличением кумулятивных свойств соединения;
- с увеличением зоны хронического действия.
5.5.4. При наличии сенсибилизирующего, канцерогенного и других проявлений отдаленных последствий действия соединения обосновывается установление коэффициента запаса, превышающего 20. Решение в каждом конкретном случае зависит от особенностей действия соединения, от адекватности и чувствительности показателей, избранных для определения минимально действующей дозы. В обычных случаях коэффициент запаса находится в диапазоне от 3 до 20.
5.5.5. Определение величины ПДУ проводится путем пересчета дозы соединения (мг/кг) в плотность загрязнения кожных покровов (мг/см2) по формуле (10):
ПДУ = Limchcut x M : Kз x S, мг/см2, (10)
где: Limchcut - пороговая доза, установленная экспериментально в хроническом эксперименте с учетом определения остаточного количества соединения на коже (п. 3.8);
M - масса тела человека, в среднем принята за 70 кг;
Kз - коэффициент запаса (п.п. 5.5.2 - 5.5.4);
S - площадь кожного покрова человека, в среднем равна 16120 см2.
5.6. Обоснование ОДУ загрязнения кожных покровов.
5.6.1. Для оперативной оценки риска кожно-резорбтивного действия соединений допустим расчет ОДУ загрязнения кожных покровов.
5.6.2. Расчет ОДУ (мг/см2) проводится с применением величины Limchcut (мг/кг), экспериментальной или рассчитанной на основе показателя острой дермальной токсичности - LD50cut (мг/кг) соединения, по формуле (11):
ОДУ = (Limchcut x M x Kост x Kотн.прон.) : S x Kз, мг/см2, (11)
где: Limchcut - пороговая доза, установленная экспериментально в хроническом опыте или рассчитанная на основании LD50cut в мг/кг;
M - масса тела человека, в среднем принята за 70 кг;
Kост. - коэффициент остаточный, выражающий экспозиционное соотношение количества соединения, оставшегося на коже после определенного времени, и первоначально нанесенное, в среднем равен 0,25;
Kотн.прон. - коэффициент относительной проницаемости кожи человека и крысы или кролика для данного соединения (экспериментально установленный), ориентировочно равен 2;
S - площадь кожного покрова человека, в среднем равна 16120 см2;
Kз - коэффициент запаса определяется классом опасности соединения при острой дермальной экспозиции в соответствии с пунктом 5.2.4.
5.6.3. Коэффициент запаса для соединений 1 - 2 класса опасности по острой кожной токсичности равен от 20 до 10, для соединений 3 - 4 класса - от 10 до 3.
Для соединений, обладающих выраженными отдаленными и (или) специфическими эффектами, включая сенсибилизацию, коэффициент запаса может приниматься на уровне 20 и более. Для соединений, обладающих канцерогенным действием (2 класс опасности), коэффициент запаса равен 50.
5.6.4. Величина Limchcut (мг/кг) устанавливается экспериментально или рассчитывается по следующей формуле (12):
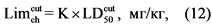
где: LD50cut - средняя смертельная концентрация (доза) при однократном накожном нанесении, мг/кг;
К - коэффициент для соединений 1 - 2 класса опасности по острой кожной токсичности, составляет 0,0002; для соединений 3 - 4 класса опасности - 0,001.
VI. Гигиенический контроль содержания вредных соединений
на коже работающих
6.1. Для изучения степени загрязнения кожи отбирают лиц профессий, подвергающихся по условиям производства наибольшему контакту с химическими соединениями, например, в химической и нефтехимической промышленности - аппаратчики и слесари; в машиностроительной и металлообрабатывающей промышленности - станочники, работающие с растворителями; в сельском хозяйстве - операторы техники, используемой для обработки почвы и растений пестицидами <12>.
--------------------------------
<12> МУК 4.1.3220-14 "Гигиенический и аналитический контроль за загрязнениями кожных покровов лиц, работающих с пестицидами", утвержденные руководителем Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека, Главным государственным санитарным врачом 02.09.2014 (далее - МУК 4.1.3220-14).
6.2. Смывы с фиксированных участков кожи работающих отбираются способом обмыва с использованием пинцета и специально подготовленных хлопчатобумажных салфеток (п. 3.8). В качестве растворителей применяется холодная или нагретая вода, этиловый спирт, разбавленные растворы кислот, растворы соды, поверхностно-активные соединения и другие сравнительно безопасные для здоровья человека соединения.
6.3. Смывы проводят с различных участков кожи: открытых (полностью или частично): лицо, шея, кисти рук, предплечья; закрытых спецодеждой: грудь, спина, голени. Смывы с кистей проводятся обязательно.
6.4. Оптимальные размеры участков кожи для проведения смывов:
- 2 кисти рук, включая межпальцевые промежутки, площадь около 720 см2;
- лицо + передняя часть шеи, площадь около 700 см2;
- 2 предплечья, с внутренней стороны примерно по 100 см2, всего - 200 см2;
- 2 голени, с передней стороны примерно по 100 см2, всего - 200 см2;
- грудь, под одеждой, около 200 см2.
Размеры и смываемые участки выбраны опытным путем, как наиболее загрязняемые части тела в процессе выполнения различных работ. Участки для смывов могут дополняться смывами со спины или живота (площадь около 200 см2).
Минимальная площадь участков смыва составляет 5% поверхности кожного покрова, которая для среднего взрослого человека составляет около 800 см2, что соответствует площади кистей рук.
Допускается проведение смывов только с кистей рук при соблюдении защиты других участков кожи, осуществляемой в соответствии с методическими документами <13>.
--------------------------------
<13> Глава 3 МУК 4.1.3220-14.
6.5. До начала работы участки кожи очищают от возможных загрязнений, промывая их водой с мылом, затем протирают 70% раствором этилового спирта. Используют чистую спецодежду, перчатки, респиратор.
6.6. Смывы проводят в течение всей смены: в начале, перед обедом и в конце. Наиболее полные сведения о загрязнении кожи можно получить при проведении смывов после выполнения вспомогательных и основных производственных операций, наиболее типичных для данного производственного процесса.
6.7. Выбор смывающей жидкости осуществляется с учетом физико-химических свойств соединений, а также их стабильности в используемом для смыва растворе. Отбор, хранение и транспортирование смывов с кожных покровов осуществляется в соответствии с аттестованными методами и методиками определения. При отсутствии метода (методики) определения соединения в смывах с кожных покровов для количественной идентификации можно использовать валидированные методики определения данного соединения в объектах окружающей среды.
При использовании в качестве смывающей жидкости этилового спирта или его водных растворов в примерный перечень вспомогательного оборудования, используемый при выполнении процедуры пробоподготовки, включается <14>:
--------------------------------
<14> Примечание: допускается использовать вспомогательное оборудование с аналогичными или лучшими характеристиками.
- встряхиватель (шейкер) лабораторный;
- ротационный вакуумный испаритель;
- посуда стеклянная лабораторная (колбы круглодонные на шлифе, воронки химические, стеклянные палочки), ГОСТ 25336-82.
При валидации методики с целью оценки полноты извлечения (смыва) соединения в качестве биологической модели для создания экспонированного смыва возможно использование подготовленной изолированной свиной кожи, которая близка по анатомо-физиологическим свойствам коже человека.
Процедуру предварительной подготовки образцов свиной кожи фиксированной площади (100 - 200 см2) выполняется в соответствии с методическими документами <15>.
--------------------------------
<15> Приложение 4 МУК 4.1.3220-14.
6.8. Количественные уровни действующего соединения идентифицируются в натурных пробах, смывов с различных участков кожных покровов работающих. Результаты выражаются в виде мкг/смыв.
Для дальнейшей статистической обработки аналитические результаты, полученные в размерности мкг/смыв, переводят в мг/см2, для чего количество соединения в мг (мкг · 10-3) относятся к величине площади смыва с фиксированного участка в соответствии с методическими документами <16>.
--------------------------------
<16> МУК 4.1.3220-14.
Значение отрицательных проб (не обнаружено) при расчете средней пробы трактуется как ![]() предела аналитического обнаружения.
предела аналитического обнаружения.
6.9. Для малолетучих соединений из полученных результатов вычисляется среднее за смену значение загрязнения исследуемого участка кожи по формуле (13):
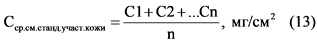
где: C - среднесменное количество соединения на стандартном участке кожи в мг/см2;
C1, C2, Cn - количество соединения, определяемое в течение смены в смывах со стандартного участка в мг/см2;
n - количество смывов.
6.10. Полученные результаты загрязнений кожных покровов с учетом площади исследуемых участков позволяют определить загрязнение всей поверхности кожных покровов по формуле (14):

где: Cср.см.общ. - среднесменное количество соединения на всей поверхности кожного покрова в мг/см2;
Cср.см.1,2,..n - среднесменное количество соединения на исследуемых участках (например, кисти рук, спина, грудь) в мг;
S1, S2, ...Sn - площадь исследуемого участка в см2;
S общая - площадь всей поверхности кожного покрова, в среднем равная 16120 см2 (таблица 9).
Таблица 9
Данные размеров общей поверхности тела человека <17>
--------------------------------
<17> МУК 4.1.3220-14.
Область
Площадь в см2
Процентное соотношение к общей поверхности тела, %
Голова:
Лицо
500
3,12
Волосистая часть головы
478
2,99
Туловище:
Шея спереди
240
1,50
Грудь и живот
2900
18,00
Шея сзади
200
1,25
Спина
2560
16,00
Верхняя конечность:
Плечо
625
3,90
Предплечье
450
2,80
Кисть
360
2,25
Нижняя конечность:
Ягодица
400
Бедро с ягодичной областью
1625
10,15
Голень
1000
6,25
Стопа
515
3,22
Общая площадь поверхности
Кожи взрослого человека
16120
100
6.11. Для малолетучих и водонерастворимых соединений учитывается возможность воздействия соединения после смены. С этой целью дополнительно проводятся смывы соединения после душа.
6.12. Для определения реальной опасности кожно-резорбтивного действия соединения в условиях производства сопоставляются среднесменные величины соединения на коже с экспериментально установленным ПДУ (мг/см2) или, рассчитанной на основании острых и подострых экспериментов, величиной ОДУ (мг/см2).
НОРМАТИВНЫЕ И МЕТОДИЧЕСКИЕ ДОКУМЕНТЫ
1. Федеральный закон от 30.03.1999 N 52-ФЗ "О санитарно-эпидемиологическом благополучии населения".
2. Федеральный закон от 19.07.1997 N 109-ФЗ "О безопасном обращении с пестицидами и агрохимикатами".
3. СанПиН 1.2.3685-21 "Гигиенические нормативы и требования к обеспечению безопасности и (или) безвредности для человека факторов среды обитания".
4. СП 2.2.3670-20 "Санитарно-эпидемиологические требования к условиям труда".
5. Приказ Минздрава России от 28.01.2021 N 29н "Об утверждении Порядка проведения обязательных предварительных и периодических медицинских осмотров работников, предусмотренных частью четвертой статьи 213 Трудового кодекса Российской Федерации, перечня медицинских противопоказаний к осуществлению работ с вредными и (или) опасными производственными факторами, а также работам, при выполнении которых проводятся обязательные предварительные и периодические медицинские осмотры".
6. Р 1.2.3156-13 "Оценка токсичности и опасности химических веществ и их смесей для здоровья человека".
7. МУ 1.1.578-96 "Требования к постановке экспериментальных исследований по обоснованию предельно допустимых концентраций промышленных химических аллергенов в воздухе рабочей зоны и атмосферы".
8. Методические указания к постановке исследований для обоснования санитарных стандартов вредных соединений в воздухе рабочей зоны.
9. Методические указания к постановке исследований по изучению раздражающих свойств и обоснованию предельно допустимых концентраций избирательно действующих раздражающих веществ в воздухе рабочей зоны.
10. МУ 1.2.3017-12 "Оценка риска воздействия пестицидов на работающих".
11. МУК 4.1.3220-14 "Гигиенический и аналитический контроль за загрязнениями кожных покровов лиц, работающих с пестицидами".
12. МР 3056-84 "Разработка методов определения вредных соединений на коже".
13. ГОСТ 25336-82 "Посуда и оборудование лабораторные стеклянные. Типы, основные параметры и размеры".
14. ГОСТ 32519-2013 "Методы испытаний по воздействию химической продукции на организм человека. Изучение хронической токсичности при внутрижелудочном поступлении".
15. ГОСТ 32639-2014 "Методы испытаний по воздействию химической продукции на организм человека. Субхроническая кожная токсичность: 90-дневное исследование".
16. ГОСТ 32371-2013 "Методы испытаний по воздействию химической продукции на организм человека. Кожно-резорбтивное действие: метод in vivo".
17. ГОСТ 32375-2013 "Методы испытаний по воздействию химической продукции на организм человека. Испытания по оценке кожной сенсибилизации".
18. ГОСТ 32435-2013 "Методы испытания по воздействию химической продукции на организм человека. Кожно-резорбтивное действие: метод in vitro".
19. ГОСТ 32436-2013 "Методы испытания по воздействию химической продукции на организм человека. Испытания по оценке острого раздражающего/разъедающего (коррозионного) действия на кожу".
20. ГОСТ 34556-2019 "Методы испытаний по воздействию химической продукции на организм человека, испытания по оценке кожной сенсибилизации методом изучения реакции региональных лимфатических узлов".
21. ГОСТ 21241-2023 "Пинцеты медицинские. Общие технические требования и методы испытаний".
22. ГОСТ 6507-90 "Микрометры. Технические условия".
