"МР 1.2.0344-24 1.2. Общие вопросы. Гигиена, токсикология, санитария. Методические рекомендации по идентификации и количественному определению метаболитов как биомаркеров вредного воздействия. Методические рекомендации"
ГОСУДАРСТВЕННОЕ САНИТАРНО-ЭПИДЕМИОЛОГИЧЕСКОЕ НОРМИРОВАНИЕ
РОССИЙСКОЙ ФЕДЕРАЦИИ
Утверждаю
Руководитель Федеральной службы
по надзору в сфере защиты прав
потребителей и благополучия человека,
Главный государственный санитарный
врач Российской Федерации
А.Ю.ПОПОВА
29 марта 2024 г.
1.2. ОБЩИЕ ВОПРОСЫ. ГИГИЕНА, ТОКСИКОЛОГИЯ, САНИТАРИЯ
МЕТОДИЧЕСКИЕ РЕКОМЕНДАЦИИ
ПО ИДЕНТИФИКАЦИИ И КОЛИЧЕСТВЕННОМУ ОПРЕДЕЛЕНИЮ МЕТАБОЛИТОВ
КАК БИОМАРКЕРОВ ВРЕДНОГО ВОЗДЕЙСТВИЯ
МЕТОДИЧЕСКИЕ РЕКОМЕНДАЦИИ
МР 1.2.0344-24
Методические рекомендации по идентификации и количественному определению метаболитов как биомаркеров вредного воздействия. МР 1.2.0344-24
1. Разработаны ФБУН ЕМНЦ ПОЗРПП Роспотребнадзора (д.м.н. Сутункова М.П., Чемезов А.И., Унесихина М.С.).
2. Утверждены руководителем Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека, Главным государственным санитарным врачом Российской Федерации А.Ю. Поповой 29 марта 2024 г.
3. Введены впервые.
I. Область применения
1.1. Настоящие методические рекомендации (далее - МР) описывают унифицированный подход к поиску биомаркеров, основанный на применении методов метаболомики, заключающихся в изучении комплексных биохимических изменений, происходящих в организме в ответ на исследуемое воздействие с использованием лабораторных животных, с целью дальнейшей валидации выявленных биомаркеров в условиях реальной экспозиции к вредным факторам.
II. Общие положения
2.1. Метаболомика наука, занимающаяся изучением низкомолекулярных веществ в организме посредством целостного рассмотрения изменений совокупности метаболитов, обозначаемой как "метаболомный профиль", при протекании внутренних процессов и действии внешних факторов окружающей среды.
2.2. Количественное и полуколичественное определение содержания метаболитов в биологическом материале (далее - биоматериал) проводят с использованием методов масс-спектрометрии в сочетании с газовой или жидкостной хроматографией.
2.3. Оценку изменения содержания совокупности метаболитов в биоматериале проводят с применением методов однофакторного дисперсионного и многомерного статистического анализа [6, 7]. Оценку изменения отдельно взятых веществ проводят методами однофакторного статистического анализа [8].
2.4. Алгоритм проведения исследования включает в себя: эксперимент по моделированию вредного воздействия с использованием лабораторных животных, масс-спектрометрический анализ биоматериала с предварительным жидкостно-хроматографическим разделением (далее - УВЭЖХ-МС), статистическую обработку результатов анализа с целью выявления изменений содержания веществ с последующей их идентификацией. В результате получают ряд метаболитов, изменение содержания которых в организме лабораторных животных связано с воздействием изучаемого вредного фактора. Общая схема проведения исследования приведена на рис. 1. Схема алгоритма проведения подготовки, жидкостного хроматомасс-спектрометрического анализа и первичной обработки результатов анализа проб биоматериала экспериментальных животных представлена в приложении 1 к настоящим МР. Схема алгоритма проведения статистической обработки результатов анализа проб биоматериалов экспериментальных животных представлена в приложении 2 к настоящим МР.
2.5. Настоящие МР могут быть использованы в рамках выполнения задач социально-гигиенического мониторинга при изучении влияния факторов среды обитания человека на состояние здоровья населения, посредством моделирования вредного воздействия с использованием лабораторных животных.
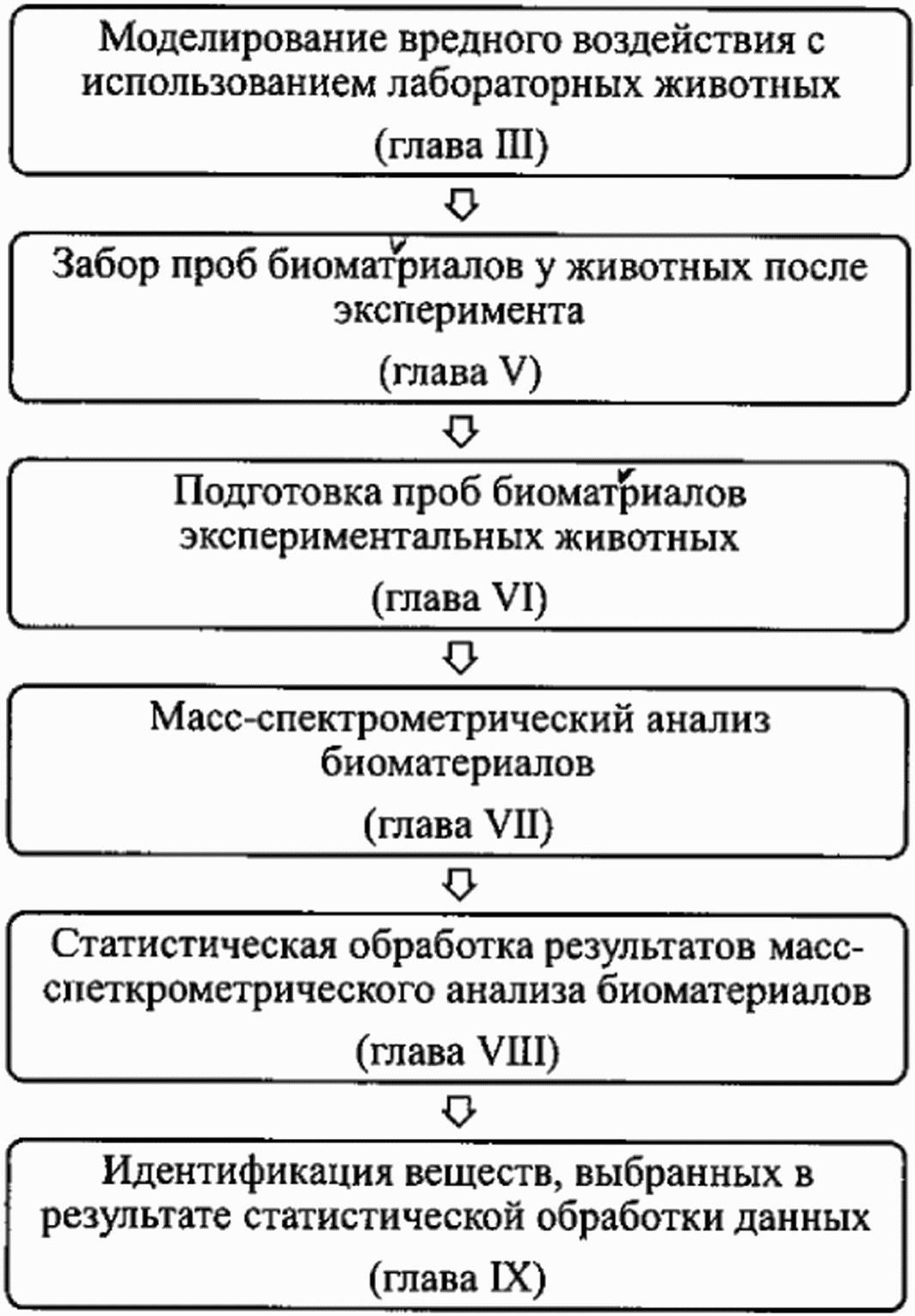
Рис. 1 - схема проведения исследования по идентификации
биомаркеров вредного воздействия
2.6. Настоящие МР содержат описание процесса получения специфического метаболомного отклика организма на вредное воздействие с применением тест-объекта мелких лабораторных грызунов (крыс).
III. Планирование эксперимента
по моделированию вредного воздействия
3.1. Этап моделирования вредного воздействия с использованием лабораторных животных начинают с поиска имеющихся литературных данных об эффектах действия такового на организм.
IV. Оборудование, необходимое для проведения исследования
по идентификации биомаркеров вредного воздействия
4.1. В табл. 1 - 2 приведен перечень оборудования для проведения исследования по идентификации биомаркеров вредного воздействия <1>.
--------------------------------
<1> Примечание: допускается использование оборудования с аналогичными или лучшими метрологическими и техническими характеристиками.
Таблица 1
Перечень оборудования, необходимого для подготовки
и хранения проб сыворотки и плазмы крови, тканей и органов
лабораторных животных
Наименование оборудования
Обозначение и наименование документов, технические характеристики
Низкотемпературный морозильник с возможностью поддержания температуры минус 80 °C и ниже
-
Весы лабораторные специального класса точности
ГОСТ Р 53228
Центрифуга настольная с возможностью поддержания температуры образцов от 0 до плюс 25 °C и частотой вращения ротора 14000 об/мин
-
Дозаторы автоматические переменного объема с диапазонами вместимости 20 - 200, 100 - 1000
ГОСТ 28311
Посуда мерная лабораторная II класса точности: цилиндры, колбы
ГОСТ 1770
Таблица 2
Перечень оборудования, необходимого для проведения
масс-спектрометрического анализа проб сыворотки и плазмы
крови, органов лабораторных животных, с предварительным
жидкостно-хроматографическим разделением веществ
Наименование оборудования
Обозначение и наименование документов, технические характеристики
Жидкостный хроматомасс-спектрометр, включающий нижеперечисленные блоки и программное обеспечение
Градиентный насос для хроматографии
Предел рабочего давления 1300 бар
Термостатируемый отсек для хранения проб, с возможностью автоматического ввода жидких проб
Возможность поддержания температуры плюс 4 °C
Термостат для хроматографических колонок
-
Тандемный масс-спектрометр высокого разрешения типа Q-TOF, TOF-TOF, Orbitrap, FT/ICR
Диапазон массовых чисел, а.е.м 50 - 1500
Точность измерения массы, ppm, не более 10
Чувствительность (отношение сигнал/шум) в режиме ионизации электроспреем в режиме MS при вводе 1,0 пг левомицетина, не менее 50
Чувствительность (отношение сигнал/шум) в режиме ионизации электроспреем в режиме MS при вводе 1,0 пг резепина, не менее 100
Программное обеспечение, контролирующее работу всего прибора, обеспечивающее сбор и хранение всех масс-спектров в процессе проведения хромато-масс-спектрометрического анализа, обеспечивающее обработку результатов измерений, вывод и расчет хроматограмм, вывод и вычитание фона масс-спектров
-
V. Забор проб биологического материала
у лабораторных животных
5.1. При сборе биоматериала для метаболомного исследования необходимо максимально быстро остановить метаболические процессы в тканях и жидкостях лабораторных животных, для того чтобы минимизировать изменения химического состава, не относящиеся к изучаемому воздействию [9].
5.2. В качестве материала для анализа крови лабораторных животных может использоваться как сыворотка, так и плазма. Забор крови осуществляется единообразно: из одного кровеносного сосуда, в одинаковом количестве (от 100 мм3 до 1 см3) и в однотипные емкости - пробирки типа "Эппендорф" соответствующей вместимости [10, 11]. Место пункции очищают, не допуская попадания в пробу посторонних веществ. В качестве антикоагулянта для получения плазмы применяют гепарин, т.к. данное вещество оказывает наименьшее влияние на состав пробы. Отделение сыворотки и плазмы проводят при температуре плюс 4 °C, полученный материал разделяют на порции объемом по 100 мм3 в отдельные пластиковые пробирки. Одновременно с этим создают образец контроля (далее - ОК) - смесь равных объемов биоматериала, взятых от всех проб из эксперимента. ОК также разделяют на порции по 100 мм3. Отобранный материал замораживают в жидком азоте и хранят до момента анализа при температуре минус 80 °C.
5.3. Органы и ткани сразу после извлечения промывают в изотоническом растворе 0,09% хлорида натрия и замораживают в жидком азоте с последующим хранением при температуре минус 80 °C. Описание приготовления ОК для образцов тканей представлено в п. 6.8.
VI. Подготовка проб биологического материала
лабораторных животных к жидкостному
хроматомасс-спектрометрическому анализу
6.1. Подготовка биоматериала лабораторных животных из эксперимента по моделированию вредного воздействия производится единообразно, в короткий промежуток времени. Перед проведением подготовки пробы размораживают на льду или в холодильнике при температуре не выше плюс 4 °C.
6.2. Алгоритм пробоподготовки биологических образцов сыворотки и плазмы крови включает одновременное фракционирование, удаление высокомолекулярных веществ и устранение влияния солей. При этом процедуру составляют таким образом, чтобы минимизировать количество этапов и обеспечить сохранность как можно большего количества содержащихся в пробе низкомолекулярных веществ: фракционирование, депротеинизация и обессоливание проводятся в один этап.
6.3. Биологические образцы тканей перед подготовкой измельчают в ступке при температуре жидкого азота или автоматическом гомогенизаторе с охлаждением. Таким образом пробы тканей переводят в жидкое состояние для обеспечения возможности дальнейшей обработки аналогично пробам сыворотки и плазмы крови.
6.4. Фракционирование - этап подготовки проб биологических образцов, на котором осуществляется разделение веществ пробы на две фракции, одна из которых содержит относительно полярные, вторая - неполярные вещества. Это необходимо для дальнейшего жидкостно-хроматографического разделения компонентов пробы перед масс-спектрометрическим детектированием веществ.
6.5. Высокомолекулярные вещества подлежат удалению из биологических проб во избежание контаминации и закупорки колонки хроматографической системы, обладающей малым диаметром пор. Высокомолекулярные вещества в биологических пробах представлены белками и пептидами.
6.6. Удаление или уменьшение концентрации солей в пробах биоматериала необходимо для повышения интенсивности аналитических сигналов компонентов проб. Соли подавляют процессы ионизации органических молекул аналитов, происходящие в источнике ионов электрораспылительного типа. Это может привести к снижению интенсивности или исчезновению аналитического сигнала вещества.
6.7. Фракционирование, депротеинизация и удаление солей осуществляется с помощью двух вариантов:
1) добавлением композиций растворителей в процессе жидкостной экстракции низкомолекулярных метаболитов. Так, смесь ацетон-метанол используют для извлечения полярной фракции веществ пробы, пригодной для дальнейшего хроматографического разделения на сорбенте гидрофильных взаимодействий. Смесью хлороформ-метанол извлекают вещества липидной природы, хорошо разделяющиеся на обращенно-фазовой хроматографической колонке. Белки при этом выпадают в осадок вместе с неорганическими солями, обладающими худшей растворимостью в водных растворах органических растворителей. Влияние остаточного количества солей нивелируется за счет разбавления пробы;
2) использованием сорбентов различной полярности в процессе твердофазной экстракции метаболитов. Пробу пропускают через патрон, содержащий сорбент с диаметром пор до 120 ангстрем, удерживающий низкомолекулярные и пропускающий высокомолекулярные вещества и соли. Так, патроны с сорбентом с привитой фазой C18 извлекают вещества липидной природы, тогда как ионообменные картриджи удерживают на себе вещества, молекулы которых содержат полярные функциональные группы. Далее, промывочным растворителем очищают сорбент от высокомолекулярных веществ и солей, а сорбат смывают с патрона элюирующим растворителем. Из собранной фракции веществ пробы удаляют излишки растворителя и далее используют для анализа.
6.8. Подготовку проб ОК для сыворотки и плазмы крови, созданных во время пробоотбора (см. п. 5.2), проводят аналогично рабочим пробам (далее - РП). ОК для проб тканей составляют после проведения пробоподготовки, объединяя равные порции материала в одной емкости.
6.9. Для оперативного контроля процедуры анализа проб (см. п. 7.16) и учета возможных погрешностей в процессе пробоподготовки в пробы вводят известное количество вещества-стандарта (далее - ВС), удовлетворяющего следующим требованиям: стабильная ионизация в режиме генерации ионов методом электрораспыления, приемлемое удерживание на хроматографической колонке, изначальное отсутствие в анализируемых образцах. Результаты измерений аналитического сигнала ВС используют для нормализации аналитических сигналов веществ в пробах в процессе обработки данных (см. п. 8.5).
6.10. Пример подготовки биологических проб тканей, сыворотки и плазмы крови представлен в приложении 2 к настоящим МР.
VII. Жидкостный хроматомасс-спектрометрический анализ
проб сыворотки и плазмы крови, гомогенатов тканей
лабораторных животных из эксперимента по моделированию
вредного воздействия
7.1. УВЭЖХ-МС анализ - метод исследования, включающий хроматографическое разделение веществ пробы с последующим масс-спектрометрическим детектированием их аналитических сигналов. Хроматографическое разделение уменьшает взаимное влияние компонентов пробы в ионизационной камере масс-спектрометра: в результате последовательного элюирования снижается вероятность занижения или полного подавления аналитического сигнала веществ.
7.2. В течение всего времени проведения анализа пробы биоматериала хранят при температуре плюс 4 °C во избежание деградации проб.
7.3. Измерение проб биоматериала при проведении метаболомного исследования проводят в виде серии проб, включающей холостой анализ (далее - ХА, см. п. 7.5), уравновешивающие образцы контроля (далее - УОК, см. п. 7.6), холостые пробы (далее - ХП, см. п. 7.7), образцы контроля (см. п. 7.8), образцы контроля стабильности сигналов (далее - ОКС, см. п. 7.9), РП (см. п. 7.10).
7.4. Последовательность проведения серии измерений 20 проб представлена в табл. 3 [12]. При большем количестве РП серию измерений составляют в соответствии с пунктами 7.3, 7.5 - 7.10.
Таблица 3
Схема последовательности проведения серии измерений,
включающей 20 рабочих проб биологического материала
Порядковый номер пробы в серии
1
2
3
4
5
6
7
8
9
Тип пробы
ХА
УОК
УОК
ХП 1
ОКС 1
ОКС 2
ОКС 3
ОК 1
ОК 2
Порядковый номер пробы в серии
10
11
12
13
14
15
16
17
18
Тип пробы
РП 1
РП 2
РП 3
РП 4
РП 5
ОК 3
РП 6
РП 7
РП 8
Порядковый номер пробы в серии
19
20
21
22
23
24
25
26
27
Тип пробы
РП 9
РП 10
ОК 4
РП 11
РП 12
РП 13
РП 14
РП 15
ОК 5
Порядковый номер пробы в серии
28
29
30
31
32
33
34
35
-
Тип пробы
РП 16
РП 17
РП 18
РП 19
РП 20
ОК 6
ОК 7
ХП 2
-
Примечание: ХА - холостой анализ; УОК - уравновешивающий образец контроля; ОК - образец контроля анализа; ХП - холостая проба; ОКС - образец контроля стабильности сигналов; РП - рабочая проба.
7.5. Включение ХА в процедуру анализа необходимо для выявления примесей веществ, содержащихся в подвижной фазе хроматографа, и которые не могут быть устранены заменой растворителей и промывкой хроматографической системы. Соответствующие данным веществам аналитические сигналы исключают из анализа при обработке данных РП и ОК на этапе поиска веществ (см. п. 7.19). ХА проводят без ввода пробы, с использованием хроматографического метода, применяемого для анализа РП (см. п.п. 7.11 и 7.12).
7.6. УОК представляет собой образец контроля, однако полученные при его анализе аналитические сигналы веществ в обработке данных результатов эксперимента не используют. УОК включают в процедуру анализа для фиксации матрицы пробы на хроматографической колонке и стабилизации времени удерживания компонентов проб при анализе.
7.7. Анализ ХП проводится для выявления веществ, вносимых в пробу в процессе пробоподготовки, и, таким образом, не несущих полезной информации о биоматериале. Кроме того, анализ ХП в конце серии проб необходим для обнаружения явления переноса - контаминации системы хроматографа. ХП приготавливается аналогично рабочим пробам (см. гл. VI), однако, вместо биоматериала добавляют равный объем воды, используемой при подготовке хроматографического элюента. Аналитические сигналы, найденные при анализе холостой пробы, исключаются при обработке данных РП и ОК на этапе поиска веществ (см. п. 7.19).
7.8. Результаты анализа ОК используют на этапе обработки данных: с их помощью производится отбор сигналов веществ, включаемых в дальнейший анализ (см. п. 7.19). Одна серия измерений включает минимум пять ОК, при этом два из них анализируют до и два после серии проб. Кроме того, ОК включают в аналитическую серию через каждые пять рабочих проб.
7.9. ОКС представляют собой ОК, по которым оценивается стабильность аналитической системы. По результатам расчета среднеквадратического отклонения (далее - СКО) значений величины сигналов и времени удержания веществ в данных пробах принимается решение о готовности хроматомасс-спектрометрической системы к анализу. В случае, когда СКО вышеупомянутых параметров превышают допустимую величину погрешности аналитической системы, проводят повторный анализ ОКС и повторяют процедуру проверки. В случае повторного превышения - проводят поиск и устранение причины.
7.10. В серии измерений РП анализируют в случайном порядке. Максимальное количество проб в серии определяется общим временем проведения анализа - оно не должно превышать 48 часов, при условии стабильности сигнала ВС (п. 7.16) и поддержании температуры проб не более плюс 4 °C [13].
7.11. Хроматографическое разделение метаболитов как полярной, так и неполярной фракций, осуществляют в градиентном режиме, начиная с подвижной фазы, обладающей наименьшей элюирующей способностью, и, с течением времени, увеличивая долю фазы с наибольшей элюирующей способностью.
7.12. Программа хроматографического градиента строится на основе объема применяемой аналитической колонки и скорости потока элюента и включает в себя следующие этапы:
- предварительное кондиционирование - промывка хроматографической системы 10 колоночными объемами стартового элюента, обладающего наименьшей элюирующей способностью;
- ввод пробы;
- градиентное элюирование - непрерывное изменение состава подвижной фазы с линейным увеличением содержания растворителя с сильной элюирующей способностью до концентрации, обеспечивающей выход всех веществ с колонки. Время градиентного элюирования подбирают таким образом, чтобы обеспечить прохождение через хроматографическую систему от 10 до 20 колоночных объемов элюента;
- промывка - элюирование из хроматографической колонки сильноудерживаемых веществ. Этап осуществляют пропусканием через хроматографическую систему 5 колоночных объемов растворителя с сильной элюирующей способностью;
- возврат к стартовым условиям - изменение состава элюента до стартовых значений, осуществляемое пропусканием через хроматографическую систему от 2 до 3 колоночных объемов подвижной фазы;
- конечное кондиционирование - промывка хроматографической системы 10 колоночными объемами стартового элюента.
7.13. При анализе серии проб предварительное кондиционирование колонки проводят только для первой пробы, конечное кондиционирование осуществляют после анализа каждой пробы.
7.14. Пример программ градиентного элюирования для предварительного хроматографического разделения фракций полярных и неполярных веществ проб биоматериала представлен в приложении 3 к настоящим МР.
7.15. Масс-спектрометрическое детектирование аналитических сигналов веществ в пробах биоматериалов осуществляют в режиме сканирования положительных и отрицательных ионов в диапазоне массово-зарядовых чисел (далее - m/z) от 50 до 1500.
7.16. Оперативный контроль процедуры анализа осуществляют посредством оценки стабильности сигнала ВС. Если в серии проб имеют место тенденции к увеличению или снижению сигнала более чем на 25% от среднего значения из всех предыдущих проб, то процедуру анализа останавливают до устранения причины возникновения отклонений. Если в отдельных РП или ОК наблюдают завышенные или заниженные значения сигнала ВС, не формирующие каких-либо закономерностей, то такие пробы исключают из дальнейшей обработки данных.
7.17. Обработку масс-хроматограмм полного ионного тока ХП, ОК и РП проводят в программном обеспечении производителя оборудования. Анализ масс-хроматограмм заключается в поиске и интегрировании сигналов квазимолекулярных ионов, соответствующих индивидуальным веществам. Результатом обработки масс-хроматограмм является перечень значений m/z ионов веществ, для которых указывают максимальное значение интенсивности аналитического сигнала, площадь и время удерживания его пика на хроматограмме.
7.18. В результаты анализа не включают вещества, обладающие интенсивностью аналитического сигнала менее, чем трехкратный уровень шума детектора и включающие менее двух изотопных пиков, а также обнаруживаемые в диапазонах пика ввода пробы и возврата хроматографического градиента к стартовым условиям.
7.19. С целью исключения из результатов анализа веществ, не относящихся к изучаемому в эксперименте воздействию, из данных, полученных при обработке ОК, отбрасывают все сигналы веществ, найденные в ХП. Оставшиеся вещества, присутствующие более чем в 70% проб ОК, включают в поиск при обработке данных анализа РП.
7.20. Для последующего анализа данных РП из эксперимента по моделированию вредного воздействия используют значения m/z ионов веществ, соответствующие им площади пиков аналитических сигналов и их время удерживания.
VIII. Статистическая обработка результатов анализа проб
биологического материала животных из эксперимента
по моделированию вредного воздействия
8.1. Обработка результатов анализа проб биоматериала включает в себя следующие этапы: выравнивание данных, импутация пропущенных значений, фильтрация, нормализация и статистический анализ. Пример обработки результатов анализа проб с использованием программного обеспечения MetaboAnalyst <2> представлен в приложении 5 к настоящим МР.
--------------------------------
<2> Официальный сайт программного обеспечения MetaboAnalyst: www.metaboanalyst.ca (в свободном доступе).
8.2. Выравнивание данных - процедура поиска сигналов идентичных веществ среди всех проб в эксперименте. Для процедуры используют данные, содержащие значения m/z с соответствующими им временем удерживания и площадью пика аналитического сигнала. Выравнивание проводят по точно заданному диапазону времени удерживания и m/z, соответствующее погрешности прибора. После сопоставления сигналов по заданным критериям между всеми пробами будет получена информация о наличии или отсутствии каждого вещества по всем пробам и о количестве пропущенных значений.
8.3. Импутация пропущенных значений - замена отсутствующего сигнала значением, рассчитанным по выбранному алгоритму. Значительное количество пропущенных значений может исказить результаты статистической обработки. Предполагается, что большинство пропущенных значений вызваны их низким содержанием в анализируемой пробе, т.е. сигнал вещества ниже предела обнаружения прибора, либо случайностью, поэтому импутацию пропущенных значений в результатах анализа проб проводят одним из следующих способов:
- присвоение значения сигнала, соответствующего теоретическому пределу обнаружения вещества;
- импутация среднего, медианного или минимального значения сигнала вещества среди всех проб.
Рекомендуется исключить из обработки вещества, имеющие более половины пропущенных значений аналитического сигнала среди всех проб, а в случае полного отсутствия сигналов вещества в одной из групп, в целях корректной статистической обработки, полностью исключить вещество из рассмотрения. По результатам данного этапа пробы, в которых отсутствовали некоторые сигналы, будут дополнены значениями, рассчитанными выбранным алгоритмом импутации данных.
8.4. Фильтрация данных представляет собой удаление шума и (или) неинформативных значений аналитических сигналов веществ:
- вещества с одинаковой величиной аналитического сигнала во всех РП исключают, если стандартное отклонение или межквартильный размах величины сигнала в РП меньше, чем в ОК;
- вещества с величиной аналитического сигнала, близкой к пределу обнаружения оборудования, исключают, если среднее или медиана значений в РП меньше, чем в ОК.
8.5. Нормализация данных - приведение уровня сигналов всех обнаруженных значений m/z в РП к величине сигнала ВС, т.к. во всех пробах его содержание одинаково (см. п. 6.9). Нормализация исключает вариации по величине сигнала, вносимые на стадиях пробоподготовки и анализа. По завершению этапа площади пиков сигналов всех веществ во всех образцах будут сглажены относительно сигнала ВС.
8.6. Статистическая обработка данных представляет собой процесс сравнения аналитического сигнала веществ в пробах для определения статистически значимых отличий между экспериментальными группами. Метод статистического анализа выбирают исходя из дизайна эксперимента по моделированию определенного воздействия на животных.
8.6.1. Классический статистический анализ используют для поиска статистической значимости отличий величины сигналов веществ между двумя экспериментальными группами. Для проведения межгрупповых сравнений данных, удовлетворяющих критериям нормального распределения, используют t-критерий Стьюдента и дисперсионный анализ (англ. Analysis of Variance, далее - ANOVA), в остальных - U-критерий Манна-Уитни. При наличии более чем двух экспериментальных групп используют однофакторный ANOVA. По результатам анализа каждому m/z будет присвоено p-значение, описывающее наличие или отсутствие различий между экспериментальными группами в зависимости от заданного уровня значимости.
8.6.2. Многомерный статистический анализ данных результатов измерений РП выполняют методами главных компонент и частичных наименьших квадратов (англ. Partial least squares regression, далее - PLS-DA):
- методом главных компонент проецирует значения сигналов всех веществ от всех проб на двухкоординатную плоскость, максимизируя общую выборочную дисперсию, уменьшая таким образом размерность данных. В результате этого преобразования становится возможным оценить схожесть проб в эксперименте, тенденции изменений в экспериментальных группах и выявить выбросы. Однако, данный метод не позволяет определить, сигналы каких именно веществ обусловили наблюдаемые тенденции.
- PLS-DA выделяет переменные, между которыми есть ковариационная связь, на основании чего строит модель регрессии. В отличие от методов однофакторного анализа, метод PLS-DA выявляет одновременное изменение нескольких переменных. Предсказательную способность модели, полученной методом PLS-DA для образцов из эксперимента, можно оценить по (Q2-критерию через кросс-валидацию и p-значению, полученному из специального алгоритма перестановки данных. Отрицательные значения Q2-критерия и p > 0,05 указывают на недостаточное количество образцов для применения метода и недостаточную прогностическую способность модели. В этом случае необходимо использовать данные однофакторного анализа и метода главных компонент. В результате анализа можно визуально оценить тенденции в изменениях между экспериментальными группами, а также получить данные о веществах в пробах, содержащие m/z, время удерживания веществ, величины значимости изменений сигналов в проекции на компоненты регрессионной модели (англ. variable importance in projection, далее - VIP) или суммарные коэффициенты регрессии.
IX. Процедура идентификации веществ, данные о которых
получены в результате статистической обработки результатов
хроматомасс-спектрометрического анализа биологических проб
9.1. Результаты статистической обработки представляют собой список веществ, для каждого из которых установлено m/z ионного аддукта и время удерживания. Количество данных веществ статистически значимо отличается в группах животных из эксперимента по моделированию вредного воздействия. С использованием m/z и времени удерживания веществ проводят их идентификацию.
9.2. Идентификация - установление молекулярной и структурной формул вещества. Идентификация может быть осуществлена с различной степенью достоверности: от низшей (V) до высшей (I) (см. табл. 4) [14]. Степени достоверности с IV по I, помимо обозначенного для них в таблице критерия, включают критерии низших степеней.
Таблица 4
Степени достоверности идентификации веществ
Степень достоверности
Сведения о веществе
Критерий присвоения степени достоверности идентификации
I
Однозначно подтвержденная структурная формула
Совпадение спектра фрагментации вещества и времени удерживания с таковыми для стандартного образца
II
Установлена наиболее вероятная структурная формула
Совпадение спектра фрагментации вещества с библиотечным спектром
III
Определены функциональные группы, класс вещества, варианты структурной формулы
Наличие характерных для выбранной структурной формулы ионов в спектре фрагментации вещества
IV
Однозначная молекулярная формула
Совпадение изотопного распределения, аддуктов
V
Точная моноизотопная масса
Отсутствие данного сигнала в холостой пробе, полученной в той же серии
9.3. Для идентификации вещества с достоверностью IV степени необходимо установить молекулярную формулу, соответствующую рассматриваемому значению m/z. Подбор молекулярной формулы осуществляется посредством выполнения следующих этапов [15]:
- определение вида квазимолекулярного иона, установление моноизотопной массы нейтральной молекулы вещества (достижение V степени достоверности идентификации вещества);
- конструирование расчетным образом всех возможных молекулярных формул, масса которых лежит в пределах погрешности детектора масс-спектрометра;
- выбор наиболее вероятных молекулярных формул (например, оценка возможности существования структурной формулы, применение "азотного правила");
- сопоставление расчетного изотопного распределения для оставшихся молекулярных формул с полученным экспериментально - наиболее близкий вариант считают окончательным.
Приведенные этапы выполняют с помощью программного обеспечения, поставляемого с масс-спектрометром, либо общедоступных сервисов, например, ChemCalc <3>.
--------------------------------
<3> Официальный сайт программного обеспечения ChemCalc: www.chemcalc.org (в свободном доступе); примечание: допускается использование аналогичных или с лучшими характеристиками программных средств для подбора молекулярной формулы химического вещества.
9.4. При идентификации вещества с достоверностью I, II и III степени необходимо получить спектры фрагментации иона с соответствующим ему в пробе значением m/z. Для этого проводят повторный анализ проб в тандемном режиме масс-спектрометра, извлекая только интересующие ионы. Подвергая их фрагментации, регистрируют спектры осколочных ионов. Для генерации молекулярных формул фрагментов по алгоритму используют m/z осколочных ионов (см. п. 9.3). Состав и интенсивность сигнала осколочных ионов позволяет выдвинуть предположение о наличии тех или иных функциональных групп в веществе (степень достоверности идентификации III) [16]. Предположение о наиболее вероятной структурной формуле вещества (степень достоверности идентификации II) формируют, сравнивая фрагментационную картину молекулы вещества в РП с данными библиотек тандемных спектров HMDB <4>, MoNA <5>, MassBank <6>, METLIN <7>. Также учитывают биологический контекст, к примеру, особенности химического состава анализируемой пробы, и хроматографическое время удерживание - при различении возможных изомеров. В дополнение к спектрам фрагментации, для ограничения количества возможных кандидатов, может оказаться полезным поиск веществ по точной моноизотопной массе или молекулярной формуле в метаболомных базах данных: HMDB, LipidMaps <8>, KEGG <9>. Спектры фрагментации получают на разных уровнях энергии, сообщаемой квазимолекулярным ионам.
--------------------------------
<4> Официальный сайт базы данных Human Metabolome Database: hmdb.ca (в свободном доступе).
<5> Официальный сайт библиотеки масс-спектров MassBank of North America: mona.fiehnlab.ucdavis.edu (в свободном доступе).
<6> Официальный сайт библиотеки масс-спектров MassBank Europemassbank.eu/MassBank (в свободном доступе).
<7> Официальный сайт библиотеки масс-спектров METLIN:https://metlin.scripps.edu/ (в свободном доступе).
<8> Официальный сайт базы данных LIPID MAPS: www.lipidmaps.org (в свободном доступе).
<9> Официальный сайт Киотской энциклопедии генов и геномов: www.genome.jp/kegg (в свободном доступе).
9.5. Для достижения I степени достоверности идентификации вещества, необходимо иметь в распоряжении стандартный образец вещества, для сравнения с экспериментально полученными: m/z, хроматографическим временем удерживания и спектром фрагментации. Вещество из РП считают однозначно идентифицированным только при условии совпадения всех трех перечисленных характеристик.
9.6. По наличию или отсутствию критериев достоверности для каждого вещества (или значения m/z) присваивают уровень идентификации. Вещества со степенью достоверности идентификации I, II и III используют для интерпретации результатов эксперимента по моделированию вредного воздействия.
Приложение 1
к МР 1.2.0344-24
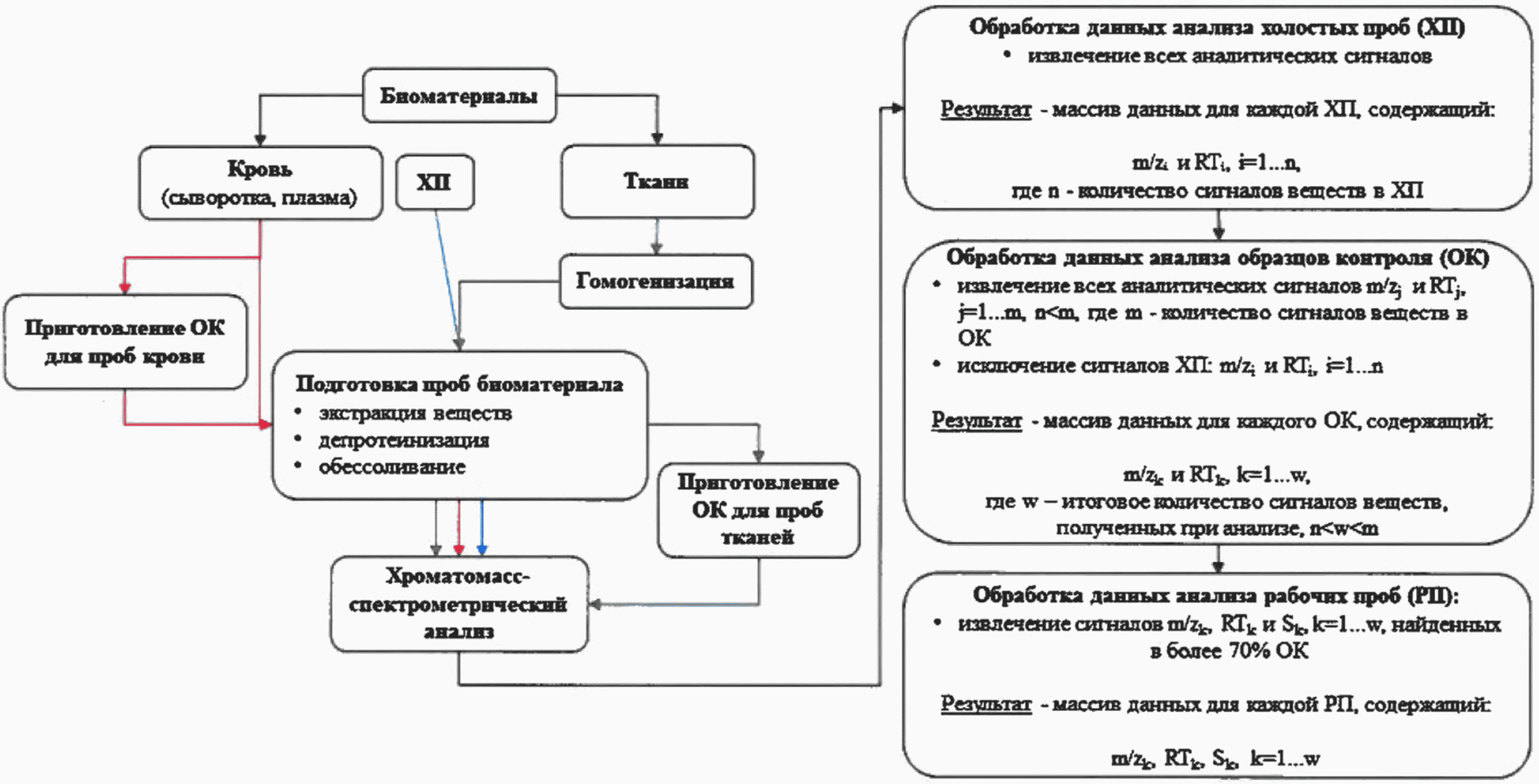
АЛГОРИТМ
ПОДГОТОВКИ И МАСС-СПЕКТРОМЕТРИЧЕСКОГО АНАЛИЗА ПРОБ
БИОМАТЕРИАЛА ЭКСПЕРИМЕНТАЛЬНЫХ ЖИВОТНЫХ <11>
--------------------------------
<11> Примечание: ХП - холостая проба; ОК - образец контроля; РП - рабочая проба; m/z - массово-зарядовое число аналитического сигнала вещества; RT - время удерживания вещества на хроматографической колонке; Sk - площадь пика сигнала вещества; -> - алгоритм подготовки проб крови; -> - алгоритм подготовки проб тканей; -> - алгоритм подготовки холостых проб.
Приложение 2
к МР 1.2.0344-24
ПРИМЕР
ПРОЦЕДУРЫ ПОДГОТОВКИ БИОЛОГИЧЕСКИХ ПРОБ
ДЛЯ ХРОМАТОГРАФИЧЕСКОГО ИССЛЕДОВАНИЯ
С МАСС-СПЕКТРОМЕТРИЧЕСКИМ ДЕТЕКТИРОВАНИЕМ
2.1. Подготовка фракции полярных метаболитов веществ крови: 100 мм3 сыворотки или плазмы, отогретой при температуре плюс 4 °C, смешивают с 300 мм3 предварительно охлажденной до минус 20 °C смеси ацетон-метанол, взятых в объемном соотношении 3:7. Смесь перемешивают и выдерживают в течение 30 минут при температуре 0 °C. После этого центрифугируют при 14000 об/мин в течение 10 минут при температуре плюс 4 °C, надосадок собирают и переносят в предварительно охлажденную на льду хроматографическую виалу.
2.2. Подготовка фракции неполярных метаболитов веществ крови: к 100 мм3 сыворотки или плазмы крови, отогретой при температуре плюс 4 °C, добавляют 100 мм3 предварительно охлажденного до плюс 4 °C 0,09% раствора хлорида натрия и 1 см3 предварительно охлажденной до минус 20 °C смеси хлороформ-метанол, взятых в объемном соотношении 2:1. Смесь перемешивают и выдерживают в течение 30 минут при температуре 0 °C. После этого пробу центрифугируют при 7800 об/мин в течение 3 минут при температуре плюс 4 °C. Отделившийся нижний слой пробы отбирают и переносят в предварительно охлажденную на льду хроматографическую виалу.
2.3. Тканевый материал перед анализом предварительно измельчают: навеску замороженной ткани перетирают в предварительно охлажденной жидким азотом ступке до порошкообразного состояния, после чего добавляют: для получения фракции полярных метаболитов веществ - смесь ацетон-метанол (см. п. 6.4) в соотношении 300 мм3 смеси на 100 мг ткани; для получения фракции неполярных метаболитов веществ - раствор хлорида натрия 0,09% и смесь хлороформ-метанол в соотношении на 100 мг ткани 100 мм3 0,09% NaCl и 1 см3 смеси хлороформ/метанол на 100 мг ткани. После добавления смеси экстрагентов подготовка проб ведется в соответствии с п.п. 2.1 и 2.2.
Приложение 3
к МР 1.2.0344-24
ПРИМЕР
ПРОГРАММ ГРАДИЕНТНОГО ЭЛЮИРОВАНИЯ ДЛЯ ПРЕДВАРИТЕЛЬНОГО
ХРОМАТОГРАФИЧЕСКОГО РАЗДЕЛЕНИЯ ФРАКЦИЙ ПОЛЯРНЫХ И НЕПОЛЯРНЫХ
ВЕЩЕСТВ ПРОБ БИОЛОГИЧЕСКОГО МАТЕРИАЛА
3.1 Хроматографическое разделение фракций полярных веществ осуществляют в градиентном режиме с использованием колонки с гидрофильным сорбентом. Состав подвижных фаз: A - раствор уксусной кислоты 5 ммоль/л в воде; B - раствор уксусной кислоты 5 ммоль/л в ацетонитриле. Для колонки с размерами 150 x 2,1 мм и зернением частиц сорбента 1,8 микрон программу градиента устанавливают: 0 - 2.5 мин - 90% B; 2,5 - 10 мин - снижение до 50% B; 10 - 15 мин - удержание 50% B; 15 - 20 мин - возврат к 90% B. Скорость потока элюента - 0,4 см3/мин, вводимый объем пробы 5 мм3 [17].
3.2 Хроматографическое разделение фракций неполярных веществ осуществляют в градиентном режиме с использованием колонки, наполненной сорбентом с привитой фазой C18. Состав подвижных фаз: A - раствор муравьиной кислоты 0,1% в воде; B - раствор муравьиной кислоты 0.1% в ацетонитриле. Для колонки с размерами 100 x 2,1 мм и зернением частиц сорбента 1,7 микрон, программу градиента устанавливают следующей: 0 - 5 мин - удержание 5% B; 5 - 25 мин - повышение до 35% B; 25 - 35 мин - повышение до 70% B; 35 - 36 мин - повышение до 100% B; 36 - 39 мин - удержание 100% B; 39 - 42 мин - возврат к 5% B. Скорость потока элюента - 0,4 см3/мин, вводимый объем пробы 5 мм3 [17].
Приложение 4
к МР 1.2.0344-24
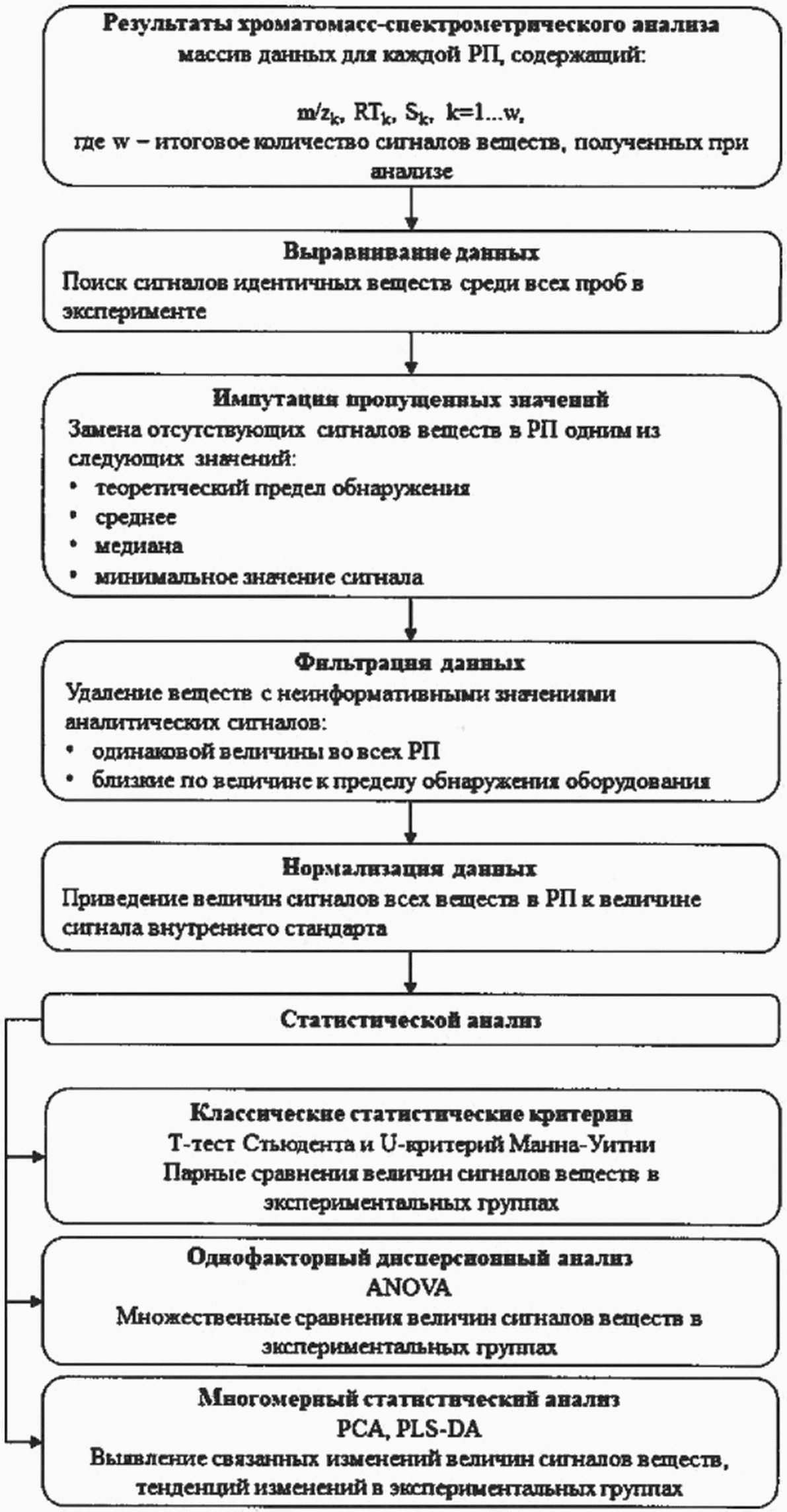
АЛГОРИТМ
СТАТИСТИЧЕСКОГО АНАЛИЗА ДАННЫХ МАСС-СПЕКТРОМЕТРИЧЕСКОГО
АНАЛИЗА ПРОБ БИОМАТЕРИАЛА ЭКСПЕРИМЕНТАЛЬНЫХ ЖИВОТНЫХ <12>
--------------------------------
<12> Примечание:
РП рабочая проба;
m/z - массово-зарядовое число аналитического сигнала вещества;
RT - время удерживания вещества на хроматографической.
Приложение 5
к МР 1.2.0344-24
ПРИМЕР
ОБРАБОТКИ РЕЗУЛЬТАТОВ АНАЛИЗА ПРОБ БИОЛОГИЧЕСКОГО МАТЕРИАЛА
С ИСПОЛЬЗОВАНИЕМ ПРОГРАММНОГО ОБЕСПЕЧЕНИЯ METABOANALYST 5.0
5.1. Данные, полученные при обработке файлов РП, преобразуют в таблицу формата ".csv" для каждой пробы в отдельности, содержащую результаты анализа как в положительном, так и в отрицательном режимах ионизации, со следующими наименованиями колонок:
- "mz" - массово-зарядовое число квазимолекулярного иона вещества;
- "rt" - время удерживания соответствующего вещества, мин;
- "into" - площадь аналитического сигнала.
Для каждой экспериментальной группы создают папку, в которую размещают результаты анализа РП. Из папок, содержащих сгруппированные файлы, формируют архив формата ".zip". Для корректной обработки в программном обеспечении, наименования всех файлов, папок и общего архива не должны содержать символы кириллицы.
5.2. Данные загружают в разделе "Статистический анализ" (англ. Statistical analysis), расположенном в окне обзора модулей анализа (англ. Module overview) (рис. П5.1 и П5.2).

Рис. П5.1 - интерфейс программного обеспечения
"MetaboAnalyst"

Рис. П5.2 - окно выбора метода анализа
5.3. В окне выбора формата данных, в разделе "Сжатый файл" (англ. A compressed file), посредством нажатия кнопки "Выбрать" (англ. Choose) выбирают и загружают архив с файлами эксперимента, далее выбирают тип данных "Список масс-спектрометрических пиков" (англ. MS peak list) и подтверждают операцию нажатием на кнопку "Подтвердить" (англ. Submit) (рис. П5.3).
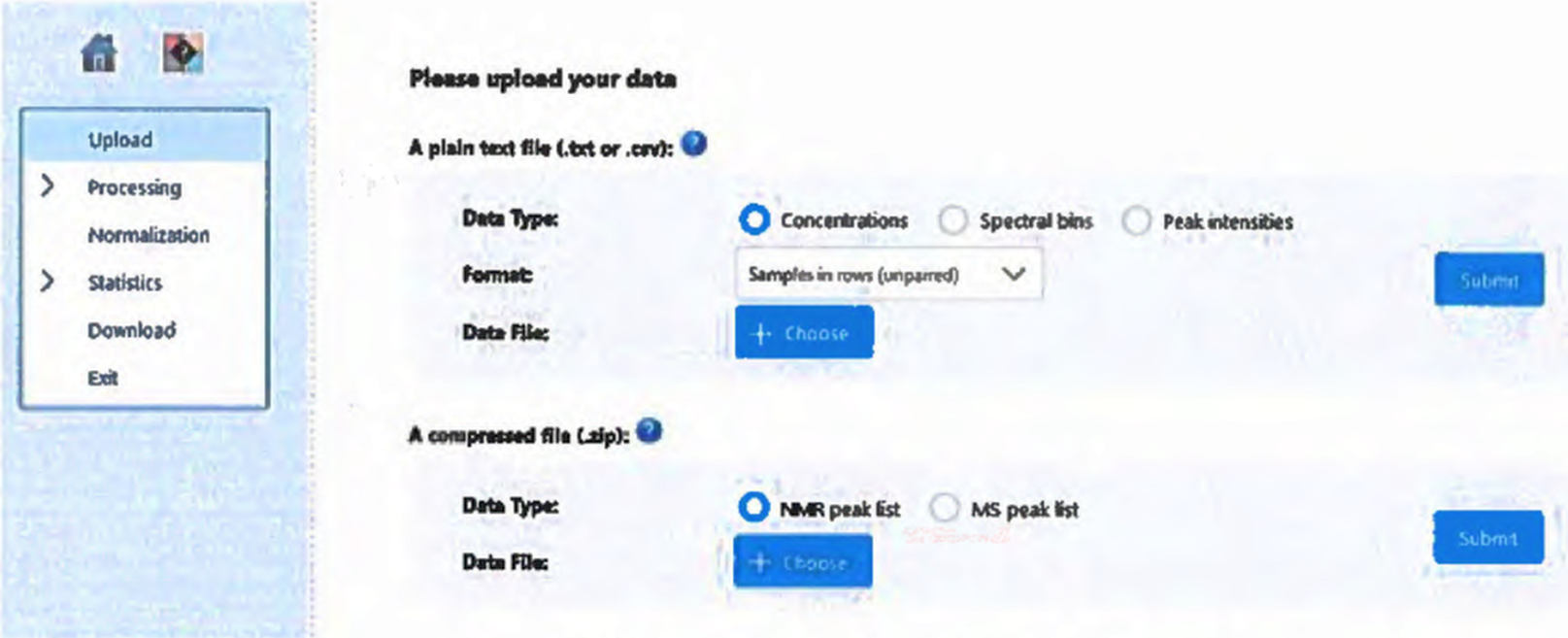
Рис. П5.3 - окно выбора формата данных
5.4. В появившемся окне задают точность определения времени удержания в секундах и m/z. После подтверждения параметров выравнивания, система отобразит информацию о количестве загруженных файлов (англ. Data integrity check), содержащих результаты анализа проб аналитических сигналов веществ, о количестве экспериментальных групп и пропущенных значениях (рис. П5.4).

Рис. П5.4 - окно, содержащее информацию о загруженных данных
5.5. Для выполнения импутации пропущенных значений переходят во вкладку "Пропущенные значения" (англ. Missing Values). Данный процесс в результатах анализа проб проводят посредством присвоения значения сигнала, соответствующего теоретическому пределу обнаружения вещества. Из обработки исключают вещества, имеющие более половины пропущенных значений аналитического сигнала среди всех проб (рис. П5.5).
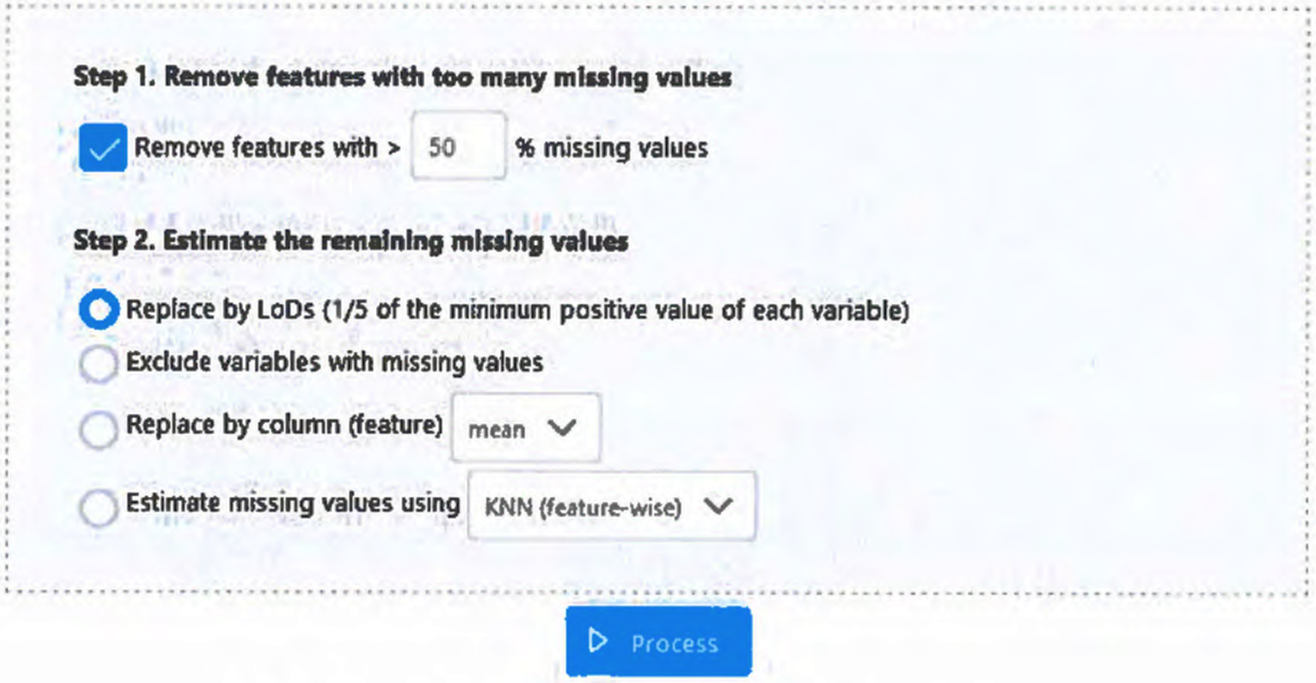
Рис. П5.5 - окно выбора параметров импутации
5.6. Удаление неинформативных значений аналитических сигналов проводят посредством оценки стандартного отклонения или межквартильного размаха величины сигнала фильтры "Стандартное отклонение" (англ. Standard deviation) и "Межквартильный размах" (англ. Interquartile range), соответственно, и по среднему или медиане значений сигнала фильтры "Среднее значение интенсивности" (англ. Mean intensity value) и "Медианное значение интенсивности" (англ. Median intensity value), соответственно (рис. П5.6). В окне "Статистические фильтры" (англ. Statistical filters) необходимо выбрать соответствующий фильтр, и применить его нажатием кнопки "Подтвердить" (англ. Submit) после каждого выбранного фильтра, т.к. их действие является аддитивным. По окончании отбора данных переходят к этапу нормализации нажатием кнопки "Продолжить" (англ. Proceed).
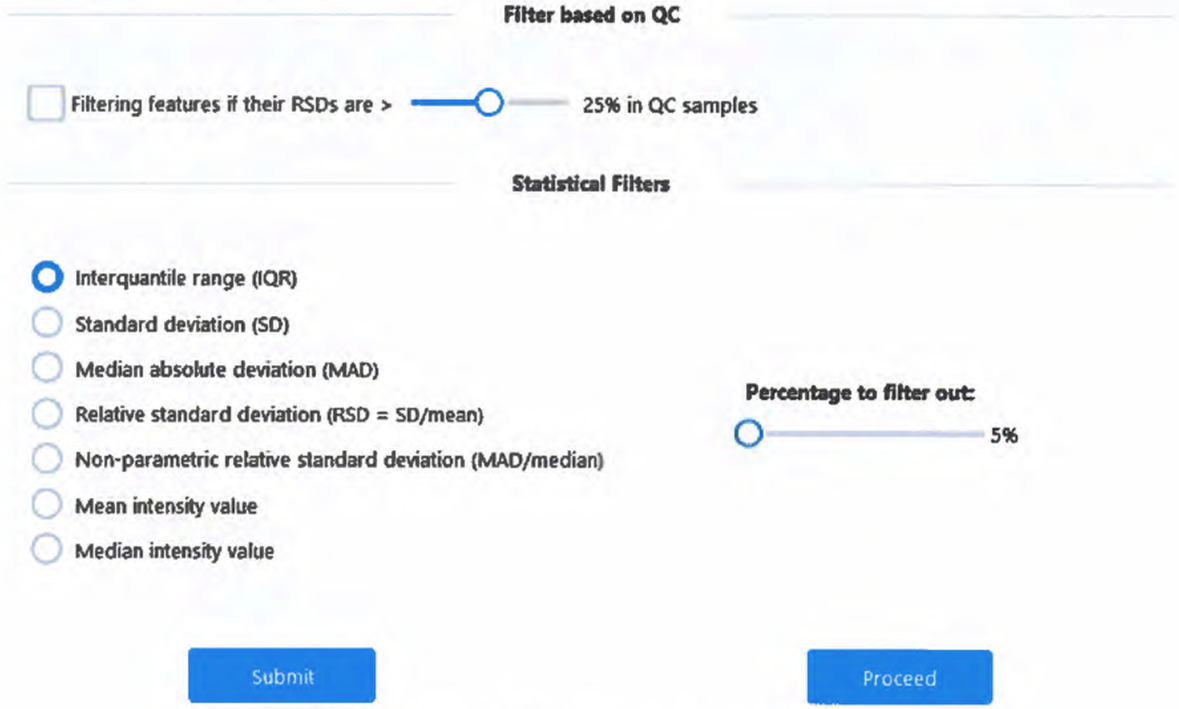
Рис. П5.6 - окно выбора параметров отбора данных
5.7. Нормализация сигналов веществ в РП проводят с использованием вещества-стандарта. Для этого в окне "Нормализация проб" (англ. Sample normalization) выбирают пункт "Нормализация по референсному сигналу" (англ. Normalisation by reference feature) и в выпадающем списке отмечают сигнал, соответствующий ВС (рис. П5.7).
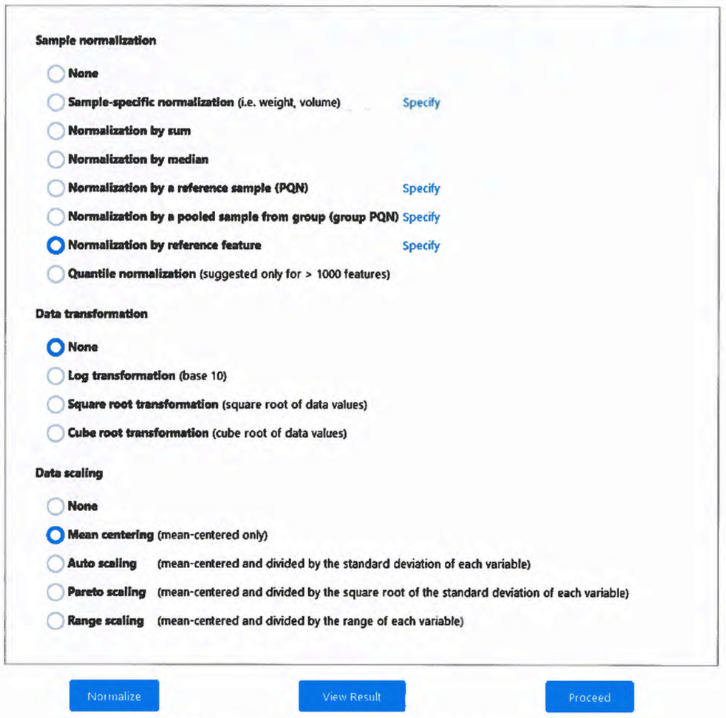
Рис. П5.7 - окно выбора параметров нормализации данных
5.8. В окне "Статистические методы" (англ. Statistics) представлены методы получения информации о сигналах, величины которых значимо отличаются в экспериментальных группах (рис. П5.8).

Рис. П5.8 - окно выбора методов статистического анализа
5.9. Классический статистический анализ представлен в виде "вулканообразной" диаграммы (англ. Volcano plot, далее - Volcano plot), учитывающим статистическую значимость отличий с поправкой на множественные сравнения или без (пункты "Коррекция с учетом оценкой ложноположительных результатов" (англ. false discovery rate, FDR) и "Данные без обработки" (англ. Raw), соответственно) и кратность изменения сигнала (англ. Fold change) (рис. П5.9). Пороговые значения данных параметров задают в соответствующих полях. По умолчанию, для проведения межгрупповых сравнений используется t-критерий Стьюдента (использование U-критерия Манна-Уитни выбирают отметкой пункта "Непараметрический критерий" (англ. Non-parametric tests). Результат анализа выгружают в виде изображения или таблицы формата Excel, содержащей m/z выбранных веществ, время удержания, p-значение и кратность изменения сигнала (рис. П5.10).
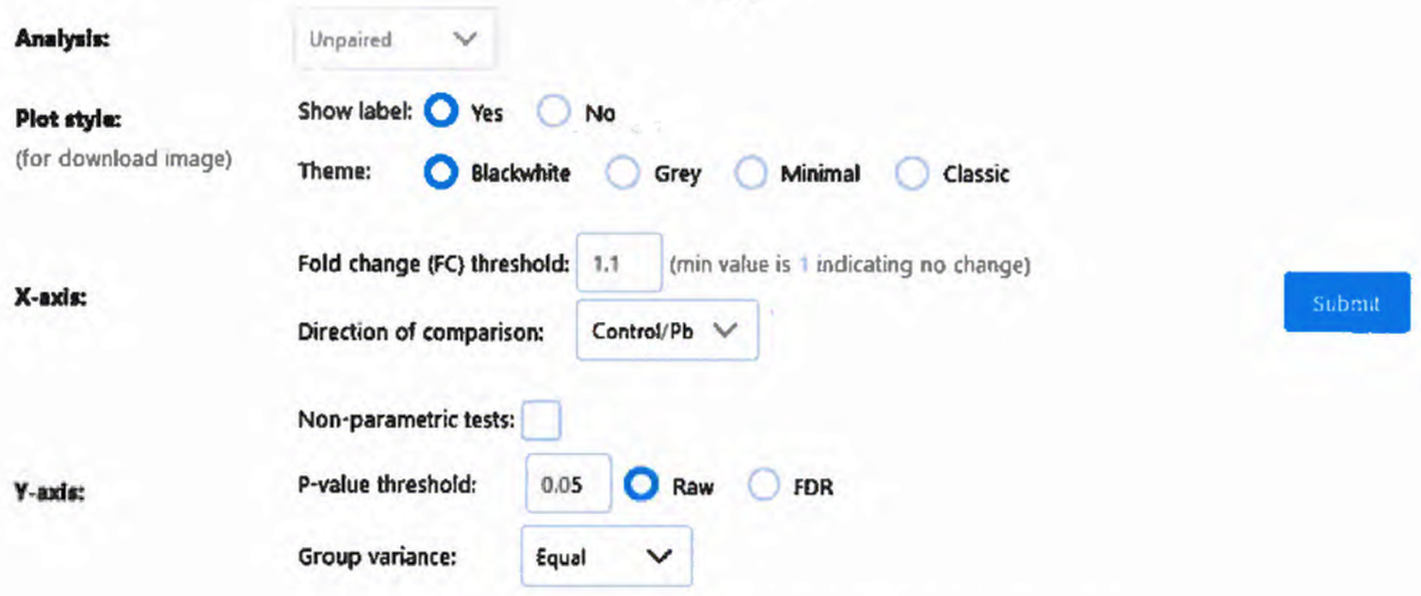
Рис. П5.9 - параметры статистического анализа
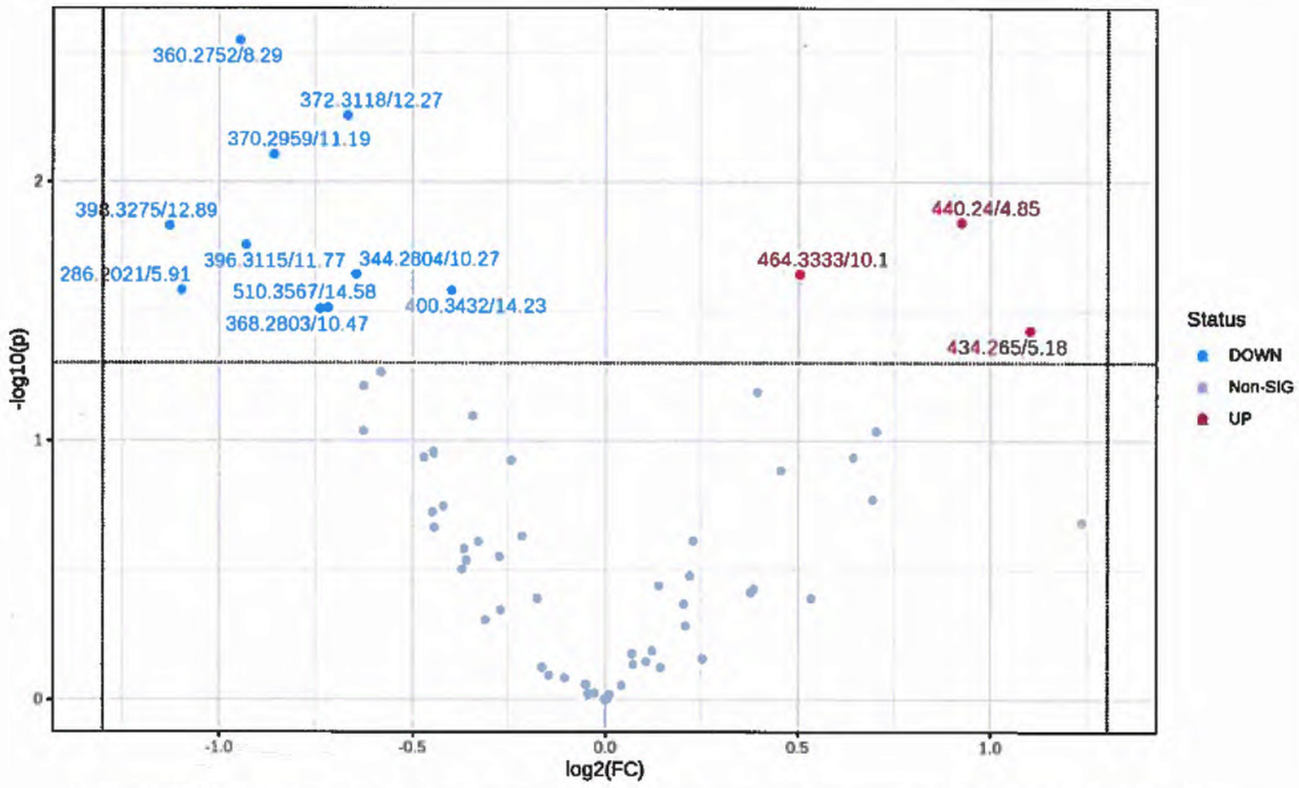
Рис. П5.10 - пример статистической обработки данных
с построением Volcano plot: по вертикальной оси отложено
значение отрицательного логарифма значения p (пороговое
значение отмечено горизонтальной пунктирной линией),
по горизонтальной - кратность изменения сигнала;
вещества, отмеченные серыми точками, не показали
значимого изменения сигнала, синими - показали
статистически значимое уменьшение, красными - увеличение
сигнала в направлении сравнения
5.10. Многомерный статистический анализ данных результатов измерений РП выполняют методами главных компонент, который проецирует значения сигналов всех веществ от всех проб на двухкоординатную плоскость, уменьшая таким образом размерность данных и демонстрируя тенденцию в изменении сигналов между двумя экспериментальными группами и их выбросы (рис. П5.11).
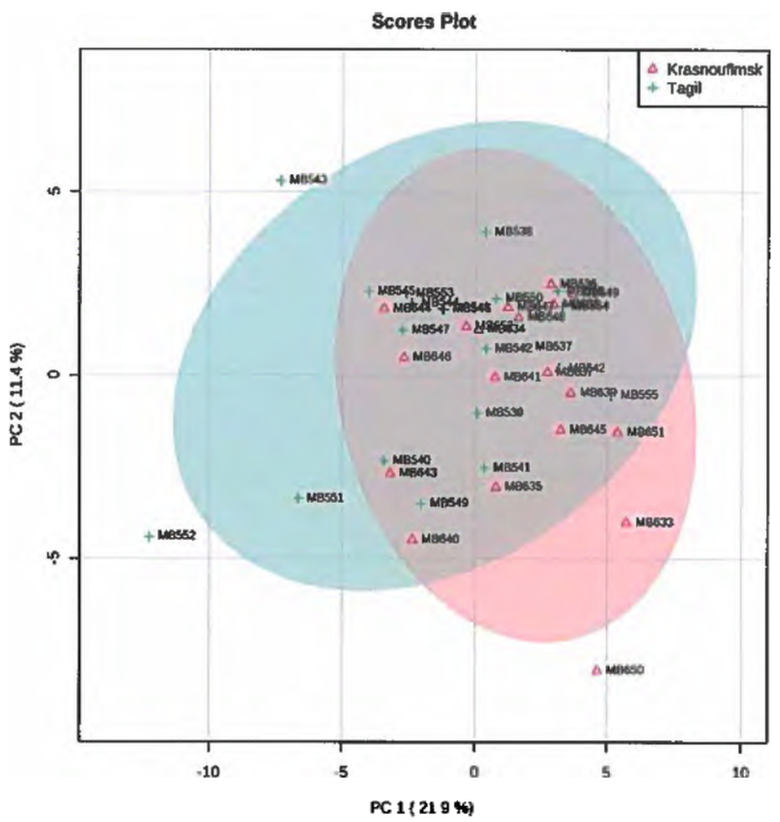
Рис. П5.11 - пример результата обработки
данных методом главных компонент. Расхождение областей
(красный и зеленый эллипсы), относящихся к пробам
из различных экспериментальных групп, свидетельствует
об отличиях между ними
5.11. Метод PLS-DA позволяет с определенной достоверностью установить вещества, сигналы которых привели к наибольшим межгрупповым различиям (рис. П5.12). При удовлетворительных значениях Q2-критерия и p-значения для интерпретации метаболомного эксперимента используют вещества, представленные на вкладке "Значимые вещества" (англ. Important features), отсортированные по величине значимости изменений сигналов в проекции на компоненты регрессионной модели или коэффициенту регрессии. Данные выгружают в виде таблицы, содержащей m/z и время удерживания вещества, значения проекций на компоненты или суммарные коэффициенты регрессии.
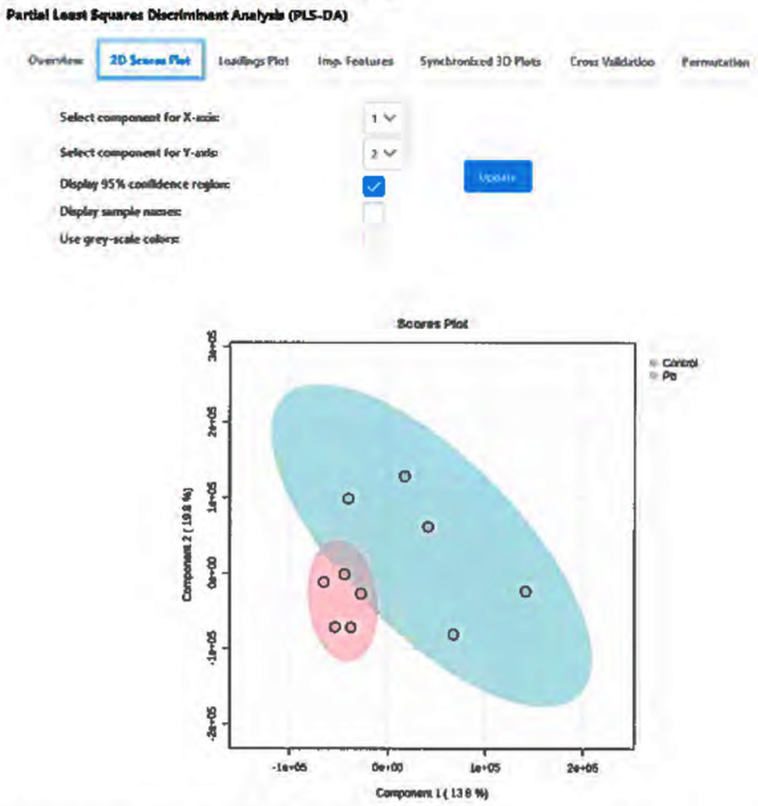
Рис. П5.12 - пример результата обработки данных методом
частично-наименьших квадратов
БИБЛИОГРАФИЧЕСКИЕ ССЫЛКИ
1. Федеральный закон от 30.03.1999 N 52-ФЗ "О санитарно-эпидемиологическом благополучии населения".
2. ГОСТ Р 53228 "Весы неавтоматического действия. Часть 1. Метрологические и технические требования".
3. ГОСТ 28311 "Дозаторы медицинские лабораторные. Общие технические требования и методы испытаний".
4. ГОСТ 1770 "Посуда мерная лабораторная стеклянная. Цилиндры, мензурки, колбы, пробирки. Общие технические условия".
5. Rudaz S. Identification and data processing methods in metabolomics. London: Future Science Limited, 2015. 187 c.
6. Gromski P. S. et al. A tutorial review: Metabolomics and partial least squares-discriminant analysis-a marriage of convenience or a shotgun wedding//Analytica chimica acta. - 2015. - T. 879. - C. 10 - 23.
7. Харькова О.А., Соловьев А.Г. Статистические методы и математическое моделирование. Архангельск: СГМУ, 2017. 125 с.
8. Metz T.O. Metabolic profiling. Totowa, NJ: Humana Press, 2011. 391 c.
9. Патент N 2719912 С1 России, МПК G09B 23/28. Способ забора крови у крыс из периферических вен хвоста: N 2019121113: заявл. 03.04.2020/П.Д. Тимкин, М.Е. Кропотова, Н.И. Петренко; заявитель ФГБОУ ВО "Амурская государственная медицинская академия" Министерства здравоохранения России.
10. Грачева О.А., Пахомов Г.А., Елдашев А.В. Методы взятия крови у разных видов животных, птиц и рыб: Учебно-методическое пособие//Казань: ФГОУ ВПО КГАВМ. - 2008.
11. Broadhurst D. Goodacre R., Reinke S.N. et al. Guidelines and considerations for the use of system suitability and quality control samples in mass spectrometry assays applied in untargeted clinical metabolomic studies//Metabolomics. - 2018. - T. 14. - C. 1 - 17.
12. Chetwynd A. J., Dunn W. B., Rodriguez-Blanco G. Collection and preparation of clinical samples for metabolomics//Metabolomics: from fundamentals to clinical applications. - 2017. - T. 965. - C. 19 - 44.
13. Schymanski E. L. et al. Identifying small molecules via high resolution mass spectrometry: communicating confidence//Environ. Sci. Technol - 2014. - T. 48:4. - C. 2097 - 2098.
14. Лебедев А. Масс-спектрометрия в органической химии. - Litres, 2022.
15. Demarque D. P. et al. Fragmentation reactions using electrospray ionization mass spectrometry: an important tool for the structural elucidation and characterization of synthetic and natural products//Natural Product Reports. - 2016. - T. 33. - N. 3. - C. 432 - 455.
16. Venter L. et al. Untargeted urine metabolomics reveals a biosignature for muscle respiratory chain deficiencies//Metabolomics. - 2015. - T. 11. - C. 111 - 121.
