"МР 4.2.0357-24. 4.2. Методы контроля. Биологические и микробиологические факторы. Реконструкция полных геномов штаммов из фондов государственных коллекций патогенных микроорганизмов. Методические рекомендации"
ГОСУДАРСТВЕННОЕ САНИТАРНО-ЭПИДЕМИОЛОГИЧЕСКОЕ НОРМИРОВАНИЕ
РОССИЙСКОЙ ФЕДЕРАЦИИ
Утверждаю
Руководитель Федеральной службы
по надзору в сфере защиты прав
потребителей и благополучия человека,
Главный государственный санитарный
врач Российской Федерации
А.Ю.ПОПОВА
23 декабря 2024 г.
Дата введения 23 марта 2025 г.
4.2. МЕТОДЫ КОНТРОЛЯ.
БИОЛОГИЧЕСКИЕ И МИКРОБИОЛОГИЧЕСКИЕ ФАКТОРЫ
РЕКОНСТРУКЦИЯ
ПОЛНЫХ ГЕНОМОВ ШТАММОВ ИЗ ФОНДОВ ГОСУДАРСТВЕННЫХ КОЛЛЕКЦИЙ
ПАТОГЕННЫХ МИКРООРГАНИЗМОВ
МЕТОДИЧЕСКИЕ РЕКОМЕНДАЦИИ
МР 4.2.0357-24
1. Разработаны ФБУН "Государственный научный центр прикладной микробиологии и биотехнологии" (М.В. Фурсов, А.А. Кисличкина, Л.А. Шишкина, Ю.П. Скрябин, А.А. Сизова, В.И. Соломенцев).
2. Утверждены руководителем Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека, Главным государственным санитарным врачом Российской Федерации А.Ю. Поповой 23 декабря 2024 г.
3. Введены впервые.
I. Общие положения и область применения
1.1. Настоящие методические рекомендации (далее - МР) описывают процесс реконструкции полных геномов штаммов патогенных микроорганизмов.
1.2. Процесс реконструкции полных геномов представляет собой de novo сборку с использованием данных секвенирования на платформах, генерирующих длинные и короткие прочтения.
II. Описание метода
2.1. Метод полногеномного секвенирования позволяет получить информацию о структуре всего генома исследуемого объекта, провести сравнение с уже известными геномами, изучить мутационную вариабельность, микроэволюцию в популяции и глобальные эволюционные процессы, происходящие на уровне первичной структуры дезоксирибонуклеиновой кислоты (далее-ДНК).
2.2. Полногеномные секвенаторы, производящие большие объемы данных коротких прочтений геномов предоставляют для анализа почти весь геном. Появившиеся в дальнейшем технологии секвенирования, генерирующие длинные прочтения, определяют положения повторяющихся элементов и осуществляют реконструкцию полного генома используя гибридный подход. Для этого используются данные, полученные с использованием длинных и коротких прочтений одновременно. Стандартная процедура полногеномного секвенирования включает в себя фрагментацию ДНК, приготовление библиотеки из случайных фрагментов ДНК и определение их нуклеотидной последовательности на секвенаторе. В результате секвенирования получается большой объем последовательностей ДНК (прочтений), длина которых зависит от используемой технологии. С помощью специализированных программ-ассемблеров (приложение 2 к настоящим МР) проводится сборка прочтений в более крупные фрагменты - контиги, которые являются фрагментами хромосомы и плазмид. При использовании гибридного подхода уменьшается количество контигов, что при достаточном объеме данных позволяет получить сборку, состоящую из хромосомы и плазмид, собранных в кольцо.
2.3. В зависимости от количества и размеров повторов выделяются три группы сложности геномов:
- геномы первой группы сложности имеют малое количество повторов, кроме рибосомного оперона размером от 5 до 7 тыс. пар нуклеотидов;
- геномы второй группы сложности имеют большое количество коротких повторов, размером не превышающих 7 тыс. пар нуклеотидов;
- геномы третьей группы сложности содержат протяженные повторы, превышающие 7 тыс. пар нуклеотидов.
Методом мономолекулярного нанопорового секвенирования получают непрерывные прочтения длиной несколько сотен тысяч оснований, что дает возможность определить сложные структуры генома.
Существуют различные сборщики геномов, основанные на разных принципах анализа, и получаемые результаты могут различаться между друг другом, как при использовании в качестве входных данных только коротких прочтений, так и комбинации коротких прочтений и протяженных.
2.4. Процесс подготовки ДНК-библиотек (набор фрагментов ДНК полного генома, фланкированных адаптерами) различается для наиболее распространенных подходов к полногеномному секвенированию:
- секвенирование на молекулярных кластерах с использованием флуоресцентно меченых нуклеотидов (рассмотрено на примере секвенатора Illumina MiSeq и набора для приготовления ДНК-библиотек Nextera DNA Library Preparation Kit <1>);
--------------------------------
<1> Примечание (и далее по тексту): при проведении секвенирования на молекулярных кластерах с использованием флуоресцентно меченых нуклеотидов допускается использование секвенаторов и наборов для приготовления ДНК-библиотек с аналогичными или лучшими характеристиками.
- технология комбинаторного синтеза зонд-якорь (англ. Combinatorial Probe-Anchor Synthesis, далее-cPAS) (рассмотрена на примере секвенатора MGISEQ-2000RS и и набора для приготовления ДНК-библиотек Universal DNA Library Preparation Kit <2>);
--------------------------------
<2> Примечание (и далее по тексту): при проведении массированного параллельного секвенирования по технологии cPAS допускается использование секвенаторов и наборов для приготовления ДНК-библиотек с аналогичными или лучшими характеристиками.
- полногеномное секвенирование ДНК с использованием метода реверсивной терминации (рассмотрено на примере секвенатора Genolab M и и набора для приготовления ДНК-библиотек Raissol Bio "SG GM" <3>);
--------------------------------
<3> Примечание (и далее по тексту): при проведении полногеномного секвенирования ДНК с использованием метода реверсивной терминации допускается использование секвенаторов и наборов для приготовления ДНК-библиотек с аналогичными или лучшими характеристиками.
- технология нанопорового мономолекулярного секвенирования (рассмотрено на примере секвенатора Oxford Nanopore MinlON и и набора для приготовления ДНК-библиотек RBK004 <4>).
--------------------------------
<4> Примечание (и далее по тексту): при получении данных секвенирования методом мономолекулярного нанопорового секвенирования допускается использование секвенаторов и наборов для приготовления ДНК-библиотек с аналогичными или лучшими характеристиками.
2.4.1. Технология секвенирования на молекулярных кластерах с использованием флуоресцентно меченых нуклеотидов является частным случаем секвенирования на основе синтеза. Принцип этой технологии заключается в следующем: адаптеры, необходимые для ПЦР и последующего секвенирования на молекулярных кластерах лигируют к предварительно фрагментированной ДНК. Полученные ДНК-библиотеки фиксируются на поверхности проточной ячейки. Для синтеза комплементарной ДНК на поверхность проточной ячейки подается реакционная смесь, содержащая ферменты, олигонуклеотиды и четыре типа меченых флуорисцентными метками разных цветов дезоксинуклеозидтрифосфатов. Нуклеотид-терминатор включается в синтезируемую цепь ДНК и идентифицируется, затем цикл синтеза повторяется. Количество циклов зависит от используемых реактивов и задается пользователем.
2.4.2. Технология полногеномного секвенирования ДНК с использованием метода реверсивной терминации имеет сходные принципы с методом секвенирования на молекулярных кластерах с использованием флуоресцентно меченых нуклеотидов. В основе метода лежит синтез комплементарной цепи к одноцепочечным фрагментам ДНК, закрепленным на твердой подложке. ДНК-зависимая ДНК-полимераза синтезирует комплементарную цепь. Встраивание каждого нового флуоресцентно-меченного нуклеотида регистрируется при помощи специального детектора.
2.4.3. Принцип секвенирования по технологии cPAS заключается в использовании ДНК-наношариков (структур, полученных путем амплификации ДНК-библиотек с помощью репликации по типу катящегося кольца). ДНК-наношарики наносят на проточную ячейку, далее к наношарикам добавляют "якорную последовательность", которая является праймером для секвенирования. Затем в реакцию добавляют четыре типа меченых флуорисцентными метками дезоксинуклеозидтрифосфатов. Встраивание каждого нового флуоресцентно-меченного нуклеотида регистрируется при помощи специального детектора.
2.4.4. Мономолекулярное нанопоровое секвенирование проходит в реакционной камере секвенатора, разделенной двухслойной мембраной с порой. В камеру подается электрическое напряжение, под действием которого молекула ДНК проходит через пору. При прохождении различных нуклеотидов через пору электрическое напряжение изменяется, что позволяет определять последовательность ДНК.
2.5. В случае проведения полногеномного секвенирования на иных типах оборудования необходимо использовать наборы для приготовления ДНК-библиотек и реактивы для процесса секвенирования в соответствии с инструкцией производителей приборов.
III. Биологический материал для исследования
3.1. Рекомендуется, чтобы штаммы микроорганизмов перед процедурой полногеномного секвенирования были предварительно охарактеризованы и идентифицированы до определенного таксономического уровня, с описанием основных фенотипических признаков, таких как характер роста на питательной среде, время культивирования, форма, размер и цвет колоний, размер и форма клеток, наличие жгутиков и капсулы, подвижность. Отмечаются атипичные свойства исследуемой культуры.
Исходные суспензии клеток сохраняются (при необходимости проведения повторной процедуры секвенирования). Перед выделением ДНК рекомендуется проводить рассев до единичных колоний и наращивание бактериальной массы проводить из одной колонии.
3.2. В качестве материала для проведения исследования используется ДНК микроорганизмов. Для выделения ДНК используется стандартный метод фенол-хлороформной экстракции, а также готовые наборы реагентов, разрешенные к применению на территории Российской Федерации, имеющие действующий срок годности. Применение готовых наборов реагентов осуществляется в соответствие с инструкциями производителей.
3.3. Концентрацию ДНК измеряют по уровню флуоресценции интер-калирующего красителя. При измерении концентрации ДНК использование спектрофотомерии не рекомендуется, поскольку этот метод крайне чувствителен к примесям в образце. Помимо концентрации в ряде случаев рекомендуется проведение оценки целостности ДНК, что проверяется путем гель-электрофореза с определенными маркерами длин ДНК.
3.4. Выделение ДНК осуществляется с запасом для проведения повторного секвенирования или дополнительного секвенирования на других платформах, если планируется получения гибридной сборки.
3.5. Аликвота ДНК сохраняется не только до завершения всех процедур секвенирования, а также для будущих исследований, если будет необходимо подтверждать наличие или отсутствие каких-либо ДНК участков или для процедуры сборки полного генома.
IV. Оборудование и материалы
4.1. Полногеномное секвенирование проводится с использованием оборудования, расходных материалов и программного обеспечения согласно приложениям 1, 2 к настоящим МР и рекомендациям производителя.
4.2. Полногеномное секвенирование проводится в лаборатории, в которой используются методы амплификации нуклеиновых кислот.
V. Массированное параллельное секвенирование
с использованием флуоресцентно-меченых нуклеотидов
на молекулярных кластерах
5.1. Технология секвенирования на молекулярных кластерах подразумевает синтез новой молекулы ДНК на матрице. Приготовление ДНК-библиотек для секвенирования на оборудовании Illumina MiSeq с использованием набора Nextera DNA Library Preparation Kit проходит в несколько этапов: тагментация, амплификация тагментированной ДНК, очистка библиотек.
5.2. Для тагментации концентрацию ДНК нормализуют до 0,2 нг/мкл. В ПЦР-планшет к 5 мкл нормализованной ДНК добавляют 10 мкл тагмен-тирующего буфера, затем 5 мкл амплифицирующей смеси (англ. Amplicon Tagment Mix, ATM), помещают ПЦР-планшет в термоциклер, при температуре плюс 55 °C на 5 мин, после чего охлаждают до температуры плюс 10 °C. Затем добавляют 5 мкл нейтрализующего буфера (англ. Neutralize Tagment Buffer, далее - NT), центрифугируют для осаждения (1 мин при 1700 об/мин), далее инкубируют при комнатной температуре 5 мин.
Далее к тагментированной ДНК добавляют по 5 мкл индекса 1 и индекса 2 (в горизонтальные ряды ПЦР-планшета добавляют индекс 2-пробирки с белыми крышками, в вертикальные ряды индекс 1 - пробирки с оранжевыми крышками). Далее добавляют 15 мкл ПЦР-смеси (англ. PCR Master Mix, NPM), центрифугируют для осаждения (1 мин при 1700 об/мин) и помещают в термоциклер с предварительно нагретой крышкой с программой: при температуре плюс 72 °C - 3 мин, плюс 95 °C - 30 секунд; далее 12 циклов: при температуре плюс 95 °C - 10 секунд, плюс 55 °C 30 секунд, плюс 72 °C - 30 секунд; и заключительная элонгация при температуре плюс 72 °C 5 мин; охлаждение до плюс 10 °C.
После амплификации образцы очищают на магнитных частицах. ПЦР-планшет центрифугируют для осаждения (1 мин при 1700 об/мин), индексированные фрагменты ДНК (50 мкл) переносят в микроцентрифужную пробирку объемом 1,5 мл и добавляют 30 мкл магнитных частиц. Встряхивают в течение 2 мин, затем инкубируют при комнатной температуре 5 мин, после чего помещают пробирки в магнитный штатив, пока жидкость не станет прозрачной. Супернатант удаляют, дважды промывают образец 80% этанолом (свежеприготовленным), далее удаляют оставшийся спирт. Высушивают в магнитном штативе в течение 15 мин, затем извлекают пробирки из магнитного штатива, добавляют 52,5 мкл ресуспендирующего буфера (англ. Resuspension Buffer, далее - RSB), встряхивают в течение 2 мин, затем инкубируют при комнатной температуре 2 мин. Помещают пробирки в магнитный штатив, пока жидкость не станет прозрачной и отбирают 50 мкл супернатанта, содержащего библиотеки ДНК. Концентрацию очищенных библиотек проверяют на флуориметре.
Картридж для секвенирования не позднее, чем за 2 часа до запуска помещают в водяную баню при комнатной температуре. Размораживают буфер для гибридизации (англ. HT1) при комнатной температуре, после чего оставляют при температуре от плюс 2 до плюс 8 °C.
Производят перерасчет концентрации библиотек и нормализуют их, разбавляя RSB до 4 нмоль в 10 мкл. Библиотеки объединяют.
В отдельную микроцентрифужную пробирку вносят 800 мкл воды и 200 мкл 1н NaOH. В результате получают 1 мл 0,2 н NaOH. Раствор перемешивают, перевернув несколько раз. Полученный раствор используют в течение 12 часов.
В микроцентрифужной пробирке смешивают 5 мкл 4 нмоль объединенных библиотек и 5 мкл 0,2 н NaOH, полученную смесь перемешивают на вортексе, после чего центрифугируют при 280 об/мин в течение 1 мин и инкубируют при комнатной температуре в течение 5 мин. Полученную смесь добавляют к 990 мкл реактива NT1, получая 1 мл библиотеки с концентрацией 20 пмоль. 600 мкл 20 пмоль библиотек вносят в ячейку для образца в картридже для секвенирования.
Далее проводят подготовку секвенатора Illumina MiSeq к запуску:
- запускают программу для проведения процесса секвенирования;
- создают панель образцов;
- выбирают набор для подготовки библиотек;
- вводят название запуска;
- в открывшийся таблице указывают названия образцов в ячейках, соответствующих лункам ПЦР-планшета;
- сохраняют данные;
- создают таблицу с информацией по запуску: секвенатор, формат выходных данных ".fastq only", вводят номер картриджа, название набора для подготовки библиотек, название эксперимента и количество циклов. После чего сохраняют таблицу и приступают к секвенированию;
- в главном меню прибора выбирают "Секвенирование" и следуют инструкциям на экране прибора.
VI. Полногеномное секвенирование ДНК с использованием метода
реверсивной терминации
6.1. Подготовка ДНК-библиотеки для секвенирования методом реверсивной терминации на оборудовании Genolab М с использованием набора Raissol Bio "SG GM" происходит в несколько этапов: фрагментация ДНК, лигирование адаптеров, очистка после лигирования, постановка индексной ПЦР, очистка после индексной ПЦР, измерение концентрации.
6.2. Для фрагментации ДНК необходимо внести 10 мкл ДНК с концентрацией 20 нг/мкл в стрипы или пробирки объемом 0,2 мл. Приготовить мастер-микс для фрагментации: буфер (3 в 1) - 13,4 мкл, 3-фермент - 1,6 мкл и ДНК-нуклеаза - 1 мкл. Мастер-микс добавить в образцы ДНК и поместить в амплификатор после выхода прибора в рабочее состояние после первого этапа. Программа для фрагментации: плюс 4 °C - ![]() , плюс 65 °C - 25 мин, плюс 75 °C - 10 мин и охлаждение образцов до плюс 4 °C.
, плюс 65 °C - 25 мин, плюс 75 °C - 10 мин и охлаждение образцов до плюс 4 °C.
6.3. Для лигирования адаптеров необходимо приготовить мастер-микс на необходимое количество реакций: лигазный буфер - 20,5 мкл, адаптеры - 3,5 мкл, лигаза - 1 мкл. Перемешать, сбросить капли с помощью кратковременного центрифугирования. После завершения программы фрагментации внести по 25 мкл получившегося мастер-микса к образцам. Поместить в амплификатор с установленной программой для лигирования: при температуре плюс 4 °C-![]() , плюс 22 °C - 30 мин, плюс 4 °C -
, плюс 22 °C - 30 мин, плюс 4 °C - ![]() . После установки пробирок в амплификатор необходимо пропустить первый шаг.
. После установки пробирок в амплификатор необходимо пропустить первый шаг.
6.4. После проведения лигирования необходимо провести очистку на магнитных частицах, для этого добавить 45 мкл магнитных частиц к каждому образцу и перемешать на вортексе до гомогенного состояния. Инкубировать 5 мин при комнатной температуре. Далее поместить образцы на магнитный штатив, инкубировать 3 - 5 мин до прозрачного раствора. После этого удалить супернатант. Дважды промыть 200 мкл 80% этанолом (свежеприготовленным). Удалить спирт. Далее необходимо высушить образцы с открытыми крышками при комнатной температуре в течение 10 мин до полного испарения остатков спирта. Добавить 24 мкл деионизированной, свободной от нуклеаз воды к магнитным частицам. Интенсивно перемешать пробирки на вортексе, сбросить капли с помощью кратковременного центрифугирования. Поместить образцы на магнитный штатив, инкубировать в течение 2 - 3 мин до прозрачного раствора. Перенести 22 мкл элюата в новые пробирки или стрипы, не захватывая магнитные частицы.
6.5. На этапе проведения индексной ПЦР к каждому образцу необходимо добавить по 2 мкл индивидуальных праймерных миксов. Далее необходимо приготовить мастер-микс на необходимое количество реакций: ПЦР буфер - 25 мкл, ПЦР фермент 1 - 0,5 мкл, ПЦР фермент 2 - 0,75 мкл. Перемешать мастер-микс, осадить. Внести по 26,25 мкл к каждому образцу. Поместить пробирки в амплификатор. Запустить программу для индексной ПЦР: при температуре плюс 95 °C - 2 мин, плюс 95 °C - 15 сек, плюс 56 °C - 30 сек, плюс 72 °C - 17 сек, плюс 72 °C - 2 мин, плюс 4 °C - ![]() .
.
6.6. После ПЦР-реакции необходимо провести очистку на магнитных частицах, для этого добавить 50 мкл магнитных частиц к каждому образцу, перемешать на вортексе до гомогенного состояния. Инкубировать 5 мин при комнатной температуре. Далее поместить образцы на магнитный штатив, инкубировать 3 - 5 мин до просветления раствора. После удалить супернатант. Дважды промыть 200 мкл 80% этанолом (свежеприготовленным). Спирт удалить. Далее необходимо высушить образцы с открытыми крышками при комнатной температуре в течение 10 мин до полного испарения остатков спирта. Добавить 22 мкл ТЕ буфера к осадку частиц. Интенсивно перемешать пробирки на вортексе, сбросить капли с помощью кратковременного центрифугирования. Поместить образцы на магнитный штатив, инкубировать в течение 2 - 3 мин до просветления раствора. Перенести 20 мкл элюата в новые пробирки или стрипы, не захватывая магнитные частицы. Концентрацию очищенных библиотек проверить на флуориметре.
6.7. Получившийся ПЦР-продукт нужно нормализовать до 4 нмоль в 20 мкл, разбавив водой лабораторного качества. Нормализованные библиотеки объединяют по 5 мкл каждого образца в пробирке на 1,5 мл - 2 мл. Картридж для секвенирования хранится при температуре минус 25 - минус 15 °C. Не позднее, чем за 2 часа до запуска, картридж помещают в водяную баню комнатной температуры. Заранее (минимум за 30 мин до запуска) нужно достать загрузочную проточную ячейку, которая хранится при температуре плюс 2 - 8 °C.
6.8. Полученный пул библиотек нужно денатурировать 0,2 н NaOH. В отдельную микроцентрифужную пробирку вносят 800 мкл воды и 200 мкл 1 н NaOH. В результате получают 1 мл 0,2 н NaOH. Раствор перемешивают, перевернув несколько раз. Полученный раствор используют в течение 12 часов. В микроцентрифужной пробирке смешивают 5 мкл 4 нмоль объединенных библиотек и 5 мкл 0,2 н NaOH, полученную смесь перемешивают на вортексе, после чего центрифугируют при 1700 об/мин в течение 1 мин и инкубируют при комнатной температуре в течение 5 мин.
Для остановки реакции денатурации добавляют 5 мкл нейтрализующего реагента. Далее вносят 985 мкл гибридизующего реагента. 20 пмоль смесь библиотек готова. Для получения загрузочной концентрации (2,5 пмоль) в пробирку на 2 мл нужно внести 187,5 мкл смеси библиотек (концентрация 20 пмоль) и 1312,5 мкл гибридизующего реагента. Полученную пробирку с 2,5 пмоль библиотекой нужно поместить в загрузочный порт для образца в картридже.
6.9. Для подготовки секвенатора Genolab M к запуску необходимо включить прибор и запустить сопряженный с прибором системный блок. Перед тем, как начать процесс секвенирования, нужно осуществить промывку прибора. Зайти в программу, выбрать вкладку "Регулярная промывка". Для промывки используют промывочную ячейку и три промывочные картриджи, которые заполняются растворами: первый-Твин 20 0,05% (в 999,5 мл деионизованной воды растворить 500 мкл Твин 20); второй - 0,1 н NaOH (в 1 литре деионизованной воды растворить 4 г гидроксида натрия); третий - деионизованная вода. Суммарное время промывки - 50 мин. На сенсорной панели прибора необходимо проверить показатели температуры охлаждаемого контейнера для реагентов, она не должна превышать плюс 5 °C.
6.10. После промывки прибора в программе нужно выбрать вкладку "Секвенирование". Следующим этапом подгружается файл со всей информацией о запуске в формате ".csv". Нужно внести необходимую информацию в следующие ячейки: B2 - название эксперимента, A7 - количество циклов для первой нити ДНК, A8 - количество циклов для второй нити ДНК, B14 - необходимость демультиплексирования, начиная с ячейки A18 - название образцов, с ячейки F18 - последовательность индекса 1, с ячейки H18 - последовательность индекса 2.
6.11. Перед загрузкой необходимо сканировать штрих-код ячейки, который отображается на сенсорной панели. Перед загрузкой в прибор ячейку необходимо предварительно протереть в одном направлении безворсовой салфеткой, пропитанной 96% этанолом. В отсек для реагентов загружается картридж (блок A или блок B). Картридж предварительно необходимо встряхнуть, чтобы перемешать реагенты, и удалить крышку с пробирки исследуемого образца. Отсканировать штрих-код картриджа. После нажатия кнопки "начало" запустится процесс секвенирования. На сенсорной панели прибора будет отображаться время секвенирования, количество пройденных циклов, загрузка ячейки кластерами, шкала с качеством секвенируемых данных Q30. По окончанию процесса секвенирования прибор промывается.
VII. Получение данных массированного параллельного
секвенирования по технологии комбинаторного синтеза
зонд-якорь (cPAS)
7.1. Подготовка библиотек для секвенирования на оборудовании MGISEQ-2000RS по технологии cPAS с использованием набора Universal DNA Library Preparation Kit происходит в несколько этапов: фрагментация молекул ДНК; отбор фрагментов нужной длинны; восстановление концов ДНК; лигирование адаптеров; амплификация библиотек; циркуляризация; создание ДНК-наношариков.
7.2. Для приготовления ДНК-библиотек исходную ДНК необходимо фрагментировать. Размер фрагментов должен быть в диапазоне 100 - 700 пар оснований, с пиком в 250 - 300 пар оснований. ДНК фрагментируют с помощью ультразвука в ультразвуковой бане в течение 7 мин с рабочим циклом: 15 сек работы и 1 мин отдыха. В работу берут 1000 нг ДНК в 100 мкл ТЕ-буфера. Контроль за качеством проведенной фрагментации осуществляют с помощью электрофореза в агарозном геле.
7.3. На следующем этапе отбирают фрагменты нужной длины. Отбор фрагмента осуществляется с помощью магнитных частиц: 50 мкл ДНК осаждают на магнитных частицах (30 мкл), после чего супернатант переносят в чистые пробирки, а магнитные частицы сбрасывают. К полученному супернатанту вносят 10 мкл магнитных частиц, супернатант удаляют, дважды промывают образец 200 мкл 80% этанолом (свежеприготовленным), далее удаляют оставшийся спирт. Высушивают в магнитном штативе в течение 10 мин, затем извлекают пробирки из магнитного штатива, эллюируют 42 мкл ТЕ буфера. После отбора фрагмента нужной длины производят количественную оценку с помощью флуориметрии.
7.4. После получения фрагментов нужной длины осуществляется восстановление концов молекул ДНК после фрагментации и наращивание добавление липких 3' - А концов ДНК. На первом этапе образцы после отбора фрагмента нужной длины нормализуют, в последующую работу берут 100 нг ДНК в 40 мкл ТЕ буфера. Затем готовят смесь реактивов для восстановления концов из расчета 7,1 мкл буфера (англ. ERAT Buffer) и 2,9 мкл фермента (англ. ERAT Enzyme) на один образец. 10 мкл полученной смеси вносят в каждый образец, после чего тщательно перемешивают и ставят в термоциклер с предварительно нагретой крышкой и установленной программой: плюс 37 °C - 15 мин, плюс 65 °C - 30 мин, охлаждение до плюс 4 °C.
7.5. На следующем этапе проводят лигирование адаптерных последовательностей. Для проведения реакции к каждому образцу добавляют 5 мкл уникальных для каждого образца адаптеров и заранее приготовленную смесь ДНК-лигазы и буфера для лигирования. Полученную смесь инкубируют в термоциклере при температуре плюс 23 °C в течение 30 мин, затем охлаждают до плюс 4 °C. После инкубирования образцы коротко осаждают на микроцентрифуге и вносят 20 мкл ТЕ-буфера в каждый образец, доводя конечный объем до 100 мкл.
Продукт лигирования очищают на магнитных частицах, добавляя 50 мкл магнитных частиц к образцам, интенсивно перемешивают их и инкубируют в течение 5 мин при комнатной температуре, после чего помещают на магнитный штатив до просветления, удаляют супернатант и дважды промывают 200 мкл 80% этанолом (свежеприготовленным). Этанол отбирают, образцы коротко центрифугируют и снова помещают на магнитный штатив с целью удалить оставшийся этанол. После чего образцы высушивают на магнитном штативе, снимают с магнитного штатива и вносят 21 мкл ТЕ-буфера в каждый образец, инкубируют 5 мин при комнатной температуре, коротко центрифугируют и помещают на магнитный штатив до полного просветления. В чистые пробирки отбирают 19 мкл супернатанта, который используют для последующей амплификации.
7.6. Для проведения амплификации готовят мастер-микс, из расчета 25 мкл смеси реактивов (англ. PCR Enzyme Mix) и 6 мкл смеси праймеров (англ. PCR Primer Mix). К образцам добавляют 31 мкл полученного мастер-микса, тщательно перемешивают, осаждают и помещают их в термоциклер с нагретой крышкой и установленной программой: при температуре плюс 95 °C - 3 мин, далее 7 циклов: плюс 98 °C - 20 сек, плюс 60 °C - 15 сек, плюс 72 °C - 30 сек, после чего заключительная элонгация плюс 72 °C - 10 мин и охлаждение до плюс 4 °C.
7.7. Продукт амплификации очищают на магнитных частицах, добавляя 50 мкл магнитных частиц к образцам, интенсивно перемешивают их и инкубируют в течение 5 мин при комнатной температуре, после чего помещают на магнитный штатив до просветления, удаляют супернатант и дважды промывают 200 мкл 80% этанолом (свежеприготовленным). Этанол отбирают, образцы коротко центрифугируют и снова помещают на магнитный штатив с целью удалить оставшийся этанол. После чего образцы высушивают на магнитном штативе, снимают с штатива и вносят 32 мкл ТЕ-буфера в каждый образец, инкубируют 5 мин при комнатной температуре, коротко центрифугируют и помещают на магнитный штатив до полного просветления. В чистые пробирки отбирают 30 мкл супернатанта, который используют для циркуляризации. После очистки измеряют концентрацию нуклеиновой кислоты. Далее образцы объединяют в зависимости от их концентрации, размера генома и дорожки на проточной ячейке.
7.8. Для циркуляризации используют 1 пкмоль объединенных библиотек, объем доводят до 48 мкл ТЕ-буфером. Из объединенных библиотек получают кольцевую ДНК (процесс включает денатурацию при температуре плюс 95 °C, циркуляризацию одноцепочечной ДНК, ферментативное разрушение оставшейся двуцепочечной ДНК и очистку на магнитных частицах). Концентрацию полученных кольцевых фрагментов ДНК учитывают и рассчитывают необходимое количество для получения наношариков.
7.9. Для получения наношариков в реакцию берут 60 фмоль кольцевой ДНК-библиотеки для каждого наношарика. Объем доводят до 20 мкл с помощью буферного раствора (англ. Low ТЕ Buffer), к полученной смеси добавляют 20 мкл буфера для создания наношариков, аккуратно перемешивают и ставят в термоциклер с установленной программой: при температуре плюс 95 °C - 1 мин, плюс 65 °C - 1 мин, плюс 40 °C - 1 мин, после чего охлаждение до плюс 4 °C. Полученную смесь осаждают и помещают на лед. После чего к ней добавляют смесь ферментов для формирования наношариков. Полученную смесь аккуратно перемешивают, осаждают и инкубируют при температуре плюс 35 °C 35 мин в термоциклере с заранее нагретой до плюс 35 °C крышкой. После реакции вносят 20 мкл буфера для остановки реакции и осторожно перемешивают пипеткой 5 - 8 раз. Эту и последующие манипуляции необходимо осуществлять наконечниками с широким отверстием с целью предотвращения механического повреждение наношариков. После получения наношариков проводят их квантификацию, концентрация должна превышать 8 нг/мкл.
7.10. В связи с малыми размерами большинства геномов патогенных микроорганизмов рекомендуется осуществлять независимую загрузку образцов на каждую дорожку проточной ячейки. Для этого используют специализированный загрузчик. Готовят загрузочную смесь: 16 мкл буфера для загрузки наношариков и 0,5 мкл смеси ферментов для создания наношариков на каждый образец, 25 мкл наношариков. 30 мкл загрузочной смеси наносят на ячейку с помощью загрузчика и инкубируют проточную ячейку 30 мин при комнатной температуре.
7.11. Картридж с реагентами для секвенирования заранее помещают в водяную баню при комнатной температуре для оттаивания. Затем его необходимо перемешать. В фольге ячеек N 1 и N 2 картриджа проделывают отверстия. Готовят смесь дезоксинуклеотидов и смесь ферментов для секвенирования и вносят в соответствующие ячейки. После чего отверстия заклеивают пленкой и интенсивно перемешивают картридж. Пленку удаляют после перемешивания. Затем 500 мкл смеси ферментов для множественной амплификации смещения (англ. MDA Enzyme mix) вносят в реагент для множественной амплификации смещения (англ. MDA Reagent), проделывают отверстие в фольге ячейки картриджа и вносят всю смесь в соответствующее отверстие.
7.12. Для запуска секвенирования выбирают ярлык, соответствующий секвенированию на главном экране секвенатора MGISEQ-2000RS в блоке A или B. Ячейку и картридж устанавливают в прибор, считывают их бар-коды, указывают тип загрузки и длину прочтений.
VIII. Получение данных секвенирования методом
мономолекулярного нанопорового секвенирования
8.1. Библиотеки для секвенирования на оборудовании Oxford Nanopore MinlON готовят с использованием набора для быстрого баркодирования RBK004. Все компоненты набора размораживают при комнатной температуре, затем осторожно перемешивают на вортексе или пипетируют.
8.2. В ПЦР-пробирки объемом 0,2 мл вносят 7,5 мкл ДНК с концентрацией 800 нг и 2,5 мкл смеси для фрагментации RB01-12, осторожно перемешивают, затем инкубируют при температуре плюс 30 °C - 1 мин, плюс 80 °C - 1 мин и охлаждают на льду в течение 5 мин. Библиотеки объединяют и смешивают с эквивалентным объемом магнитных частиц, инкубируют 5 мин при комнатной температуре. Далее пробирки помещают на магнитный штатив. После осветления раствора отбирают супернатант и промывают осадок дважды 200 мкл свежеприготовленным 80% спиртом. После просушивания осадка снимают пробирку с магнитного штатива и суспендируют осадок в 10 мкл буфера (Tris-HCl pH 7.5 - 8.0 с 50 нмоль NaCl). Инкубируют пробирку 2 мин при комнатной температуре, затем помещают в магнитный штатив и после осветления раствора отбирают супернатант в чистую пробирку. Затем добавляют 1 мкл реактива RAR Осторожно перемешивают и инкубируют 5 мин при комнатной температуре. Приготовленная библиотека до загрузки хранится на льду.
8.3. Загрузка проточной ячейки:
- буферы SQB, FLT и FLB, а также загрузочные частицы LB размораживают при комнатной температуре, а после разморозки помещают на лед;
- крышку секвенатора открывают, крышку загрузочного порта сдвигают по часовой стрелке, чтобы было видно отверстие для загрузки;
- после открытия загрузочного порта, удаляют небольшой объем воздуха, находящийся в нем, для этого устанавливают 1000 мкл-пипетку на 200 мкл, вставляют наконечник пипетки в загрузочный порт и поворачивают колесо пипетки, пока не будет установлен объем 220 - 230 мкл или не будет виден небольшой объем буфера, при этом необходимо избегать образования пузырей в области пор;
- готовят смесь буферов для проточной ячейки: 30 мкл FLT добавляют во флакон FLB и перемешивают пипеткой;
- 800 мкл полученной загрузочной смеси буферов вносят в проточную ячейку через загрузочный порт, избегая внесения воздуха и инкубируют 5 мин;
- тщательно перемешивают пипетированием реактивы SQB и LB;
- в новой пробирке готовят библиотеку для загрузки: к 34 мкл SQB добавляют 25.5 мкл LB, 4.5 мкл свободной от нуклеаз воды и 11 мкл ДНК-библиотеки (конечный объем - 75 мкл);
- завершают загрузку проточной ячейки: осторожно поднимают крышку порта для образцов, вносят 200 мкл оставшейся загрузочной смеси буферов в проточную ячейку через порт для загрузки, избегая попадания пузырей воздуха в систему;
- аккуратно перемешивают подготовленную библиотеку пипетированием непосредственно перед загрузкой;
- медленно по каплям вносят 75 мкл библиотеки на мембрану;
- аккуратно закрывают крышку загрузочного порта;
Подготовка к секвенированию:
- запускают программу секвенирования на компьютере;
- отмечают устройство из списка подключенных секвенаторов, выбирают вкладку и задают его параметры;
- далее указывают название эксперимента и набор реактивов;
- запускают процесс секвенирования с параллельным процессом осуществления бейсколлинга и демультиплексирования.
Приложение 1
к МР 4.2.0357-24
ПЕРЕЧЕНЬ
РЕКОМЕНДОВАННОГО ОБОРУДОВАНИЯ И РАСХОДНЫХ МАТЕРИАЛОВ <5>
--------------------------------
<5> Примечание: допускается использование оборудования и расходных материалов с аналогичными или лучшими метрологическими и (или) техническими характеристиками. При использовании других наборов для приготовления ДНК-библиотек, необходимо следовать руководствам изготовителей. В случае проведения полногеномного секвенирования на иных типах оборудования, необходимо следовать рекомендациям изготовителей приборов.
1. Программируемый термоциклер с функцией амплификации.
2. ПЦР-бокс.
3. Холодильник с камерами, поддерживающими температуру от плюс 2 до плюс 8 °C и от минус 18 до минус 25 °C.
4. Набор автоматических пипеток переменного объема (1 - 10 мкл, 10 - 100 мкл, 100 - 1000 мкл);
5. Одноразовые наконечники с аэрозольным барьером для пипеток переменного объема в штативах: до 10 мкл, до 200 мкл и до 1000 мкл, свободные от РНКаз и ДНКаз, стерильные.
6. Емкость для сброса отработанных расходных материалов.
7. Комплект рабочей защитной одежды.
8. Резиновые (латексные, нитриловые, виниловые) неопудренные перчатки одноразового применения.
9. Пробирки, стрипы или планшеты (в зависимости от количества проб, анализируемых в ходе одного эксперимента), совместимые с моделью термоциклера, из оптически прозрачного пластика для ПЦР.
10. Пробирки типа "эппендорф" объемом 1,5 и 2 мл.
11. Штативы для микропробирок объемом 0,6 - 1,5 мл.
14. Миницентрифуга-вортекс со сменными роторами.
15. Ротор для ПЦР-стрипов.
16. Роторы для микропробирок объемом 0,2 - 1,5 мл.
17. Раствор для деконтаминации 0,2%-ный раствор ДП-2Т, хлорацида или аналогичный (в случае контаминации).
18. Флуориметр для определения количественного анализа ДНК.
19. Магнитный штатив на 96 мест для работы с глубоколуночными планшетами и планшетами для ПЦР с адаптером для для работы с одиночными пробирками и стрипами объемом 0,2 мл.
20. Вода деионизированная, свободная от нуклеаз.
21. 1 ![]() ТЕ буфер (pH 8.0).
ТЕ буфер (pH 8.0).
22. Полисорбат 20 (Твин 20).
23. Натрия гидроксид.
24. Tris-HCl буфер.
25. Этанол абсолютный, для молекулярной биологии.
26. Набор для измерения концентрации ДНК с помощью флуори-метра.
27. Набор для приготовления ДНК-библиотек для секвенирования на молекулярных кластерах Nextera DNA Library Preparation Kit.
28. Набор для приготовления ДНК-библиотек для секвенирования методом реверсивной терминации Raissol Bio "SG GM".
29. Набор для приготовления ДНК-библиотек для секвенирования по технологии cPAS Universal DNA Library Preparation Kit.
30. Набор для приготовления ДНК-библиотек методом нанопорового мономолекулярного секвенирования RBK004.
31. Секвенатор Illumina MiSeq (технология массированного параллельного секвенирования с использованием флуоресцентно-меченых нуклеотидов на молекулярных кластерах).
32. Секвенатор Genolab M (технология реверсивной терминации, например).
33. Секвенатор MGISeq-2000 (технология cPAS).
34. Секвенатор Oxford Nanopore MinlON (технология нанопорового мономолекулярного секвенирования).
35. Компьютер для подключения платформы мономолекулярного нанопорового секвенирования (для Oxford Nanopore MinlON необходим процессор i7, не менее 4 ядер, с оперативной памятью не менее 16 Гб, твердотельным накопителем (SSD) объемом не менее 1 Тб и USB-портом 3.0).
36. Компьютер для обработки данных, с характеристиками: не менее четырех ядер, видеокарта с объемом оперативной памяти не менее 8 Гб, оперативная память не менее 16 Гб, жесткий диск объемом не менее 1 Тб и установленной операционной системой Linux.
Приложение 2
к МР 4.2.0357-24
ПРИМЕР
ИСПОЛЬЗОВАНИЯ ПРОГРАММНОГО ОБЕСПЕЧЕНИЯ
ДЛЯ МОЛЕКУЛЯРНОГО СЕКВЕНИРОВАНИЯ <6>
--------------------------------
<6> Примечание: допускается использование другого программного обеспечения с аналогичными или лучшими характеристиками.
Общие сведения
1. Для обработки полученных по результатам секвенирования данных используется программное обеспечение <7>.
--------------------------------
<7> Ассемблер, осуществляющий сборку геномов с использованием гибридного подхода (например, Unicycler, официальный сайт - github.com/rrwick/Unicycler (в свободном доступе); программа, осуществляющая вычисление метрических показателей прочтений (например, pauvre, официальный сайт - github.com/conchoecia/pauvre (в свободном доступе); универсальная программа для оценки качества прочтений (например, FastQC, официальный сайт - www.bioinformatics.babraham.ac.uk/projects/fastqc (в свободном доступе); программа для определения качества сборки геномов (например, Quast, официальный сайт - bioinf.spbau.ru/ ru/quast (в свободном доступе).
Оценка качества полученных данных
2. Для оценки качества файлов в формате ".fastq", полученных в результате массированного параллельного секвенирования методом синтеза якоря комбинаторного зонда, с использованием флуоресцентно-меченых нуклеотидов на молекулярных кластерах или методом реверсивной терминации используется программное обеспечение (например, программа "FastQC").
На примере программы "FastQC" для оценки качества полученных прочтений используется значение Phred, которое в файлах формата ".fastq" находится в четвертой строке каждого прочтения. Значение рассчитывается по формуле (1):
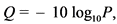
(1)
где: Q - значение Phred;
P - вероятность ошибки.
Например, Q = 10 означает, что вероятность ошибки составляет 10%, Q = 20 соответствует 1%, Q = 30 - 0,1% ошибочно идентифицированных нуклеотидов.
Для оценки качества полученных данных мономолекулярного секвенирования используется программное обеспечение (например, программа pauvre <8>).
--------------------------------
<8> Примечание: с помощью команды pauvre получают статистические данные по анализируемому файлу в формате ".fastq": - pauvre stats-finput_reads.fastq.
Реконструкция геномов с использованием гибридного подхода
3. Для отдельной сборки данных, коротких единичных прочтений, полученных в результате массированного параллельного секвенирования методом синтеза якоря комбинаторного зонда или с использованием флуоресцентно-меченых нуклеотидов на молекулярных кластерах или методом реверсивной терминации, а также сборки длинных прочтений, полученных в результате мономолекулярного секвенирования, используется программное обеспечение (например, программа Unicycler).
Например, программа Unicycler также может осуществить гибридную сборку данных объединив короткие и длинные прочтения. В результате получается реконструкция полного генома.
Для осуществления гибридной сборки используется команда со следующими параметрами (табл. 1): - unicycler-1 short_reads_l.fastq.gz-2 short_reads_2.fastq.gz-1 long_reads.fastq.gz-о outputdir.
Таблица 1
Параметры, которые используются для гибридной сборки
(на примере программы Unicycler)
Параметр
Переменная в примере
Описание
-1
long_reads.fastq.gz
Архив длинных прочтений мономолекулярного секвенирования
-0
output_dir
Название выходной директории, в которой будут сохранены полученные данные
-1
short_reads_1.fastq.gz
Архив коротких прямых прочтений
-2
short_reads_2.fastq.gz
Архив коротких обратных прочтений
Оценку качества полученных сборок проводят с использованием программного обеспечения (например, программа Quast) <9>.
--------------------------------
<9> Примечание: для запуска Quast используют команду: - quast.py fasta_files.
БИБЛИОГРАФИЧЕСКИЕ ССЫЛКИ
1. Федеральный закон от 30.03.1999 N 52-ФЗ "О санитарно-эпидемиологическом благополучии населения".
2. Постановление Правительства Российской Федерации от 01.06.2021 N 852 "О лицензировании медицинской деятельности (за исключением указанной деятельности, осуществляемой медицинскими организациями и другими организациями, входящими в частную систему здравоохранения, на территории инновационного центра "Сколково") и признании утратившими силу некоторых актов Правительства Российской Федерации".
3. СанПиН 3.3686-21 "Санитарно-эпидемиологические требования по профилактике инфекционных болезней".
4. СанПиН 2.1.3684-21 "Санитарно-эпидемиологические требования к содержанию территорий городских и сельских поселений, к водным объектам, питьевой воде и питьевому водоснабжению, атмосферному воздуху, почвам, жилым помещениям, эксплуатации производственных, общественных помещений, организации и проведению санитарно-противоэпидемических (профилактических) мероприятий".
5. МУ 1.3.2569-09 "Организация работы лабораторий, использующих методы амплификации нуклеиновых кислот при работе с материалом, содержащим микроорганизмы I - IV групп патогенности".
6. МР 3.1.0272-22 "Молекулярно-генетический мониторинг штаммов возбудителя новой коронавирусной инфекции".
7. Koren S. et al. Hybrid error correction and de novo assembly of singlemolecule sequencing reads//Nature biotechnology. - 2012. - T. 30. - N. 7. - C. 693.
8. Koren S. et al. Reducing assembly complexity of microbial genomes with single-gecule sequencing//Genome biology. - 2013.- T. 14. - N. 9. - C. R101.
9. Wick R. R. et al. Unicycler: resolving bacterial genome assemblies from short and long sequencing reads//PLoS computational biology. - 017. - T. 13. - N. 6. - C. el005595.
СПРАВОЧНАЯ ИНФОРМАЦИЯ
В настоящих МР используются следующие термины и определения:
Секвенатор - устройство, с помощью которого выполняется автоматизированное определение последовательности нуклеотидов в цепи ДНК - секвенирования.
Массированное параллельное секвенирование - группа методов определения нуклеотидной последовательности ДНК и РНК для получения формального описания ее первичной структуры.
Полногеномное секвенирование - исследование всей последовательности ДНК и РНК.
Короткие прочтения (примерно до 300 пар оснований) и длинные прочтения (до 1 млн. пар оснований)-участки ДНК, считываемые с генома при помощи специальной машины-секвенатора в процессе полногеномного секвенирования.
Контиг - консенсусная область ДНК, представляющая набор перекрывающихся сегментов ДНК.
Черновой геном-геном, состоящий из набора контигов.
Полный (завершенный) геном-реконструкция полной последовательности генома.
Сборка генома - процесс объединения большого количества коротких фрагментов ДНК в одну или несколько длинных последовательностей (контигов) в целях восстановления последовательностей ДНК хромосом, из которых возникли эти фрагменты в процессе секвенирования.
Сборка de novo-метод сборки последовательностей ДНК, который осуществляется без картирования на референсный геном.
Гибридная сборка-метод сборки последовательностей ДНК, компилирующий короткие и длинные прочтения, сгенерированные на разных секвенаторах.
Бейсколлинг-конвертация сырого сигнала от секвенатора в последовательность ДНК.
Демультиплексирование - распределение прочтений, полученных в результате секвенирования по сигнальным последовательностям, соответствующим исследуемым образцам.
