"Клинические рекомендации "Предсердно-желудочковая блокада"
МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ
КЛИНИЧЕСКИЕ РЕКОМЕНДАЦИИ
ПРЕДСЕРДНО-ЖЕЛУДОЧКОВАЯ БЛОКАДА
Кодирование по Международной статистической классификации болезней и проблем, связанных со здоровьем: I44.0, I44.1, I44.2, I44.3
Год утверждения (частота пересмотра): 2025
Пересмотр не позднее: 2027
ID: 568_2
Возрастная категория: Дети
Специальность:
Разработчик клинической рекомендации Ассоциация сердечно-сосудистых хирургов России, Общероссийская общественная организация "Российское кардиологическое общество", Всероссийская общественная организация "Ассоциация детских кардиологов России", Всероссийское научное общество специалистов по клинической электрофизиологии, аритмологии и кардиостимуляции
Одобрено Научно-практическим Советом Минздрава России
Список сокращений
АВ - атриовентрикулярный(ая)
ВПС - врожденные пороки сердца
ПЖБ - предсердно-желудочковая блокада
ПЖС - предсердно-желудочковое соединение
ПЖУ - предсердно-желудочковый узел
ЧЖС - частота желудочковых сокращений
ЧСС - частота сердечных сокращений
ЭКГ - электрокардиограмма
ЭКС - электрокардиостимулятор (Электрокардиостимулятор имплантируемый двухкамерный, частотно-адаптивный***, Электрокардиостимулятор имплантируемый однокамерный, частотно-адаптивный***)
ЭхоКГ - эхокардиография
** - препарат включен в перечень жизненно необходимых и важнейших лекарственных препаратов для медицинского применения
*** - медицинское изделие, имплантируемое при оказании медицинской помощи в рамках программы государственных гарантий бесплатного оказания гражданам медицинской помощи
# - при использовании препарата возможны отклонения от официальной инструкции по его применению
Термины и определения
Доказательная медицина - надлежащее, последовательное и осмысленное использование современных наилучших доказательств (результатов клинических исследований) в процессе принятия решений о состоянии здоровья и лечении пациента [1, 2].
Заболевание - возникающее в связи с воздействием патогенных факторов нарушение деятельности организма, работоспособности, способности адаптироваться к изменяющимся условиям внешней и внутренней среды при одновременном изменении защитно-компенсаторных и защитно-приспособительных реакций и механизмов организма [3].
Инструментальная диагностика - диагностика с использованием для обследования пациента различных приборов, аппаратов и инструментов.
Конфликт интересов - ситуация, при которой у медицинского или фармацевтического работника при осуществлении ими профессиональной деятельности возникает личная заинтересованность в получении лично либо через представителя компании материальной выгоды или иного преимущества, которое влияет или может повлиять на надлежащее исполнение ими профессиональных обязанностей вследствие противоречия между личной заинтересованностью медицинского работника или фармацевтического работника и интересами пациента [3].
Лабораторная диагностика - совокупность методов, направленных на анализ исследуемого материала с помощью различного специализированного оборудования.
Пациент - физическое лицо, которому оказывается медицинская помощь или которое обратилось за оказанием медицинской помощи независимо от наличия у него заболевания и от его состояния [3].
Рабочая группа по разработке/актуализации клинических рекомендаций - коллектив специалистов, работающих совместно и согласованно в целях разработки/актуализации клинических рекомендаций и несущих общую ответственность за результаты данной работы.
Уровень достоверности доказательств (УДД) - степень уверенности в том, что найденный эффект от применения медицинского вмешательства является истинным [4].
Уровень убедительности рекомендаций (УУР) - степень уверенности в достоверности эффекта вмешательства и в том, что следование рекомендациям принесет больше пользы, чем вреда в конкретной ситуации [4].
Холтеровское мониторирование электрокардиограммы - метод непрерывной записи электрокардиограммы на цифровой носитель с последующей дешифровкой и анализом ЭКГ [5].
Электрокардиостимуляция - это метод лечения, при котором роль естественного водителя ритма (синусового узла) выполняет искусственный водитель ритма. Этот водитель ритма вырабатывает электрические импульсы определенной силы и частоты. В качестве искусственного водителя ритма используют специальные аппараты - электрокардиостимуляторы.
1. Краткая информация по заболеванию или состоянию (группы заболеваний или состояний)
1.1 Определение заболевания или состояния (группы заболеваний или состояний)
Предсердно-желудочковая блокада (ПЖБ) - замедление, частичное или полное прекращением проведения возбуждения от предсердий к желудочкам. Замедление проведения импульса может происходить в предсердиях, АВ узле, системе Гиса-Пуркинье. Все варианты ПЖБ блокад могут быть преходящими и персистирующими, врожденными и приобретенными [6 - 8].
1.2 Этиология и патогенез заболевания или состояния (группы заболеваний или состояний)
Изменение АВ проведения может быть связано как с нарушением регуляции его деятельности со стороны вегетативной нервной системы, так и с органическим и/или структурными изменениями проводящей системы сердца [6 - 27].
Таблица 1. Причины развития атриовентрикулярной блокады
Хирургическая коррекция врожденных пороков сердца
- дефект межжелудочковой перегородки,
- атриовентрикулярная коммуникация,
- тетрада Фалло,
- обструкция выходного отдела левого желудочка,
- корригированная транспозиция магистральных сосудов,
- дискордантное АВ соединение
Изолированная врожденная ПЖБ
- повреждение ткани АВ-узла плода материнскими антителами класса анти-SSA/Ro анти-SSB/La, направленными к внутриклеточным растворимым рибонуклеопротеидным комплексам 48-KD SSB/La, 52-KD SSA/Ro, и 60-KD SSA/Ro
ПЖБ, ассоциированная со структурными аномалиями развития сердца
- аномалии развития межпредсердной и межжелудочковой перегородки,
- общий артериальный ствол,
- корригированная транспозиция магистральных сосудов,
- гетеротаксия (левопредсердный изомеризм)
Воспалительные инфекционные заболевания
- бактериальные и вирусные инфекции в том числе и внутриутробные (семейства герпесвирусов и энтеровирусов),
- острая ревматическая лихорадка,
- болезнь Лайма,
- болезнь Чагаса,
- ВИЧ-инфекция,
- бактериальный эндокардия с перевальвулярным абсцессом
Нейромышечные заболевания
- мышечная дистрофия Эмери-Дрейфуса (Emery-Dreifuss),
- мышечная дистрофия Дюшена (Duchenne),
- миотоническая дистрофия
Хромосомные и генетические заболевания
- синдром Холта-Орама (Holt-Oram),
- 18-p синдром,
- синдром Кернса-Сейра (Kearns-Sayre),
- болезнь Фабри,
- Гликогеноз II и V типа,
- Мукополисахаридоз I H, I H/S и II типа,
- синдром удлиненного интервала QT
Дегенеративные заболевания миокарда
- болезнь Лева,
- болезнь Ленегра
Другие причины
- повреждение проводящей системы сердца при катетерных процедурах (эндоваскулярное закрытие дефекта межжелудочковой перегородки, радиочастотная абляция наджелудочковых тахикардий),
- метаболические и эндокринные (карнитиновая недостаточность, гипер- и гипотиреоидизм, феохромоцитома, гипоальдостеронизм),
- гипертрофическая кардиомиопатия,
- инфильтративные заболевания (амилоидоз, саркоидоз, гемохроматоз, опухоли сердца),
- фармакотерапия (бета-адреноблокаторы, блокаторы кальциевых каналов, сердечные гликозиды, антиаритмические препараты, классы I и III, др.),
- электролитные нарушения (гиперкалиемия, гиперкальциемия),
- вагус-ассоциированные ПЖБ (спорт высоких достижений, нейрокардиогенные, обструктивное апное сна)
Появление ПЖБ I степени на фоне брадикардии может быть связано с повышением тонуса парасимпатического отдела вегетативной нервной системы. Тахизависимые ПЖБ I степени, возникающие при учащении ритма сердца, очевидно, связаны с блокадой проведения по быстрому ![]() каналу АВ узла. Данная блокада может сохраняться в ортостатическом положении пациента, но может проходить после подкожного введения атропина. Такая ответная реакция дает основание считать, что при тахизависимой ПЖБ I степени характер влияния вегетативной регуляции АВ проведения является не главным. ПЖБ I степени может возникать у пациентов после применения таких лекарственных средств как: блокаторы кальциевых каналов, бета-адреноблокаторы, сердечные гликозиды и др. Причиной развития ПЖБ I степени могут быть воспалительные заболевания миокарда различной этиологии; инфильтративные и дегенеративные заболевания. ПЖБ I степени может возникать также после перенесенной хирургической или эндоваскулярной коррекции врожденных пороков сердца (ВПС) или в результате катетеризации правых отделов сердца.
каналу АВ узла. Данная блокада может сохраняться в ортостатическом положении пациента, но может проходить после подкожного введения атропина. Такая ответная реакция дает основание считать, что при тахизависимой ПЖБ I степени характер влияния вегетативной регуляции АВ проведения является не главным. ПЖБ I степени может возникать у пациентов после применения таких лекарственных средств как: блокаторы кальциевых каналов, бета-адреноблокаторы, сердечные гликозиды и др. Причиной развития ПЖБ I степени могут быть воспалительные заболевания миокарда различной этиологии; инфильтративные и дегенеративные заболевания. ПЖБ I степени может возникать также после перенесенной хирургической или эндоваскулярной коррекции врожденных пороков сердца (ВПС) или в результате катетеризации правых отделов сердца.
ПЖБ II степени нередко наблюдается при патологической ваготонии, при токсических поражениях сердца, связанных с гликозидами наперстянки, бета-адреноблокаторами и блокаторами кальциевых каналов, а также при аутоиммунных поражениях проводящей системы с последующим развитием кардиосклероза и дегенеративных заболеваниях. проводящей системы сердца. ПЖБ II степени наблюдается у детей после операций на сердце, иногда ПЖБ как I, так и II степени может быть следствием аномалии развития проводящей системы сердца при ВПС. Следует иметь в виду, что ПЖБ I - II степени могут трансформироваться в полную ПЖБ у детей с органической или структурной патологией сердца.
Полная ПЖБ (ПЖБ III степени) может быть, как врожденной (изолированной и на фоне структурной патологии сердца), так и приобретенной. Врожденная изолированная ПЖБ ассоциирована с заболеваниями соединительной ткани у матери (33 - 64%) и вызвана поражением ткани АВ узла циркулирующими в крови антителами класса анти-48 kD SS-B/La, анти-52 kD SS-A/Ro, и анти-60 kD SS-A/Ro у матерей генетически предрасположенных индивидуумов. После прохождения через плаценту материнские аутоантитела класса анти-SSA/Ro и анти-SSB/La, перекрестно реагируют с L типами кальциевых каналов в клетках сердца у плода, вследствие чего возникает замедление атриовентрикулярной проводимости (ПЖБ I степени). Длительные нарушения гомеостаза кальция в клетках сердца у плода под влиянием продолжающего воздействия материнских аутоантител класса анти-SSA/Ro и анти-SSB/La могут привести к активации апоптоза клеток. Апоптоз не ассоциируется с воспалением, так как клетки при апоптозе не набухают и не разрушаются до поглощения их макрофагами. Опсонизированный фагоцитоз клеток приводит к синтезу цитокинов (интерлейкинов - 1, 6, 8, фактора некроза опухолей и др.), которые вместе с антителами класса анти-SSA/Ro и анти-SSB/La и активацией системы комплемента генерируют устойчивую воспалительную реакцию в сердце плода. В конечном итоге это, приводит к необратимому повреждению и развитию полной ПЖБ. Развитие врожденной полной ПЖБ документируется не ранее 16 - 18 недели гестации [24]. Антитела продолжают обнаруживаться в крови новорожденного до 6 месяца жизни. "Скрытое" носительство антител встречается в среднем у 1% женщин, а предсказуемый уровень рождения ребенка с полной ПЖБ во много раз ниже. Вероятно, на возникновение аутоиммунного поражения атриовентрикулярного соединения влияет величина титра антител (1:16 и выше). При наличии антител класса анти-48 kD SS-B/La, анти-52 kD SS-A/Ro, и анти-60 kD SS-A/Ro у матери врожденной полной ПЖБ блокада у ребенка установлена ассоциация со следующими HLA гаплотипами: A1, B8, DR3, MB2 и MT2. Такие HLA гаплотипы как DR2, MB1/MT1 - характерны для матерей с положительным титром антител и детей без врожденной полной ПЖБ. Другими факторами риска, которые могут оказывать влияние на развитие изолированной врожденной полной ПЖБ у плода являются возраст матери, зимний сезон, повышенная инфицированность матери во время беременности, низкий уровень витамина D [6 - 8, 10, 12, 13, 19].
Возникновение врожденной полной ПЖБ удается установить внутриутробно только в 32% случаев. Примерно у 28% детей наблюдается прогрессирующее течение врожденной ПЖБ от I до III степени.
Установлено, что нарушения АВ проводимости также ассоциированы с мутациями в гене SCN5A, кодирующем функцию натриевых каналов. Мутации в данном гене имеют широкий спектр фенотипических проявления в виде каналопатий/кардиомиопатий: - синдром удлиненного интервала QT типа 3, - синдром типа Бругада, дилатационная кардиомиопатия, - изолированная кардиомиопатия предсердий. Наблюдается высокая степень наследования в патогенезе врожденной неиммунной изролированной ПЖБ [25, 26].
Около 25% случаев врожденных ПЖБ III степени сочетаются со структурными аномалиями сердца, наиболее часто с дефектами развития межпредсердной и межжелудочковой перегородок, левопредсердным изомеризмом, а также L-транспозицией магистральных сосудов [18 - 21]. Одной из наиболее частых причин, приобретенной ПЖБ III степени является воспалительное поражение миокарда [22].
В ряде случаев приобретенная ПЖБ III степени возникает после операции по коррекции ВПС [27]. Наиболее часто ПЖБ развивается при хирургической коррекции атриовентрикулярной коммуникации, дефекта межжелудочковой перегородки, пороков развития аортального и митрального клапанов). Развитием ПЖБ могут сопровождаться ряд наследственных и нейромышечных заболеваний.
ПЖБ I степени может быть результатом замедленного проведения в предсердии, АВ узле, пучке Гиса или в его ножках. Доминирующим местом задержки импульса является АВ-узел (у 83% больных). Задержка проведения в предсердиях или АВ узле при ПЖБ I степени носит транзиторный или стабильный характер и может медленно прогрессировать в сторону высоких степеней ПЖБ.
ПЖБ II степени тип Мобитц I (с периодикой Самойлова-Венкебаха), вызывается замедлением проводимости в АВ узле в 72% случаев и в системе пучка Гиса - в 28%. Циклы Венкебаха могут видоизменяться и под влиянием других явлений (например, супернормального проведения или зависимых от брадикардии задержек и блокад проведения). В редких случаях в цикле Венкебаха отмечается блокирование двух последовательных Р-волн. При ПЖБ II степени типа Мобитц II интервалы PQ (R), предшествующие выпавшему сокращению, всегда постоянны и не меняются даже после выпавшего сокращения. В случаях, соответствующих последнему критерию, ПЖБ II степени тип Мобитц II ограничивается системой Гиса-Пуркинье (35% случаев на уровне пучка Гиса и 65% - в дистальной части системы Гиса-Пуркинье). ПЖБ II степени в АВ узле имеет относительно благоприятное течение и не ведет к внезапной асистолии. Согласно общепринятому мнению, ПЖБ II степени в системе Гис-Пуркинье часто прогрессирует до полной ПЖБ и приступов Морганьи-Адамса-Стокса.
1.3 Эпидемиология заболевания или состояния (группы заболеваний или состояний)
ПЖБ I степени может встречаться на электрокардиограмме (ЭКГ) у здоровых детей от 0,6 до 8% случаев. У детей с нормальным синусовым ритмом транзиторное увеличение интервала PQ встречается у младших детей в 5% случаев и в 15% у старших детей, в основном в ночное время. Более высокая частота выявления ПЖБ I степени отмечается у тренированных спортсменов - 8,7%. Частота выявления ПЖБ I степени у детей при проведении холтеровского мониторирования сердечного ритма гораздо выше - до 10 - 22%. Частота ПЖБ II степени составляет 0,003% в популяции. Достаточно высокая распространенность (2,4%) ПЖБ II степени тип Мобитц I отмечается у тренированных спортсменов, проходящих рутинную ЭКГ. Средняя частота врожденной полной ПЖБ составляет 1 на 22 000 новорожденных и колеблется в пределах от 1 на 25000 до 1 на 15000. Частота развития ПЖБ после хирургической коррекции врожденных пороков сердца составляет от 1 до 17%, что зависит от анатомии порока и вида выполненного кардиохирургического вмешательства [7, 8, 17].
1.4 Особенности кодирования заболевания или состояния (группы заболеваний или состояний) по Международной статистической классификации болезней и проблем, связанных со здоровьем
I44.0 Предсердно-желудочковая блокада первой степени
I44.1 Предсердно-желудочковая блокада второй степени
I44.2 Предсердно-желудочковая блокада полная
I44.3 Другая и неуточненная предсердно-желудочковая блокада
1.5 Классификация заболевания или состояния (группы заболеваний или состояний)
В зависимости от степени нарушения АВ проводимости выделяют три степени АВ-блокады:
- Предсердно-желудочковая блокада I степени.
- Предсердно-желудочковая блокада II степени - атриовентрикулярная блокада, тип I и II; блокада Мобитца, тип I и II; блокада второй степени, тип I и II; блокада Венкебаха.
- Предсердно-желудочковая блокада III степени - полная блокада сердца, блокада третьей степени [8].
1.6 Клиническая картина заболевания или состояния (группы заболеваний или состояний)
Спектр клинических проявлений ПЖБ широк и варьирует от полного отсутствия симптомов до развития сердечной недостаточности, синкопальных состояний и внезапной смерти. ПЖБ I степени может встречаться у здоровых детей и протекает бессимптомно. Дети с ПЖБ I степени, у которых длительность интервала PQ (R) от 240 мс и более, нуждаются в наблюдении с целью контроля над возможным прогрессированием степени блокады.
Клинические проявления заболевания у детей с ПЖБ II - III степени зависят от величины пауз ритма, исходной частоты сердечных сокращений или активности замещающего ритма. При внезапно возникающих паузах ритма велик риск развития синкопальных состояний. Появление симптомов сердечной недостаточности зависит от возможности обеспечить адекватный метаболическим потребностям минутный объем кровообращения, величина которого зависит от частоты сердечных сокращений и ударного объема левого желудочка. У детей старшего возраста, несмотря на снижение ЧСС, минутный объем кровообращения поддерживается увеличением ударного объема, в основе чего лежит нарастание при брадикардии конечного диастолического размера левого желудочка. Таким образом, появлением симптомов сердечной недостаточности будет зависеть либо от уровня исходной брадикардии и/или отсутствия адекватного прироста ЧСС при нагрузке, а также от сократительной функции левого желудочка.
Особого внимания в этой связи заслуживают плоды с диагностированной ПЖБ. Предикторами развития водянки плода и его гибели являются частота сокращения желудочков менее 55 в минуту, а предсердий менее 120 в минуту. Плоды с полной ПЖБ и структурной аномалией сердца имеют как минимум 50% риск внутриутробной или перинатальной гибели. Среди новорожденных с изолированной ПЖБ почти 90% асимптомны и имеют нормальную функцию левого желудочка. К факторам риска неблагоприятного исхода ПЖБ у новорожденных и детей раннего возраста следует отнести: частота сокращений желудочков менее 55 ударов в минуту, замещающий ритм с широкими желудочковыми комплексами, наличие желудочковой эктопии, или высокая частота сокращения предсердий (более 140 в минуту).
Приступы потери сознания (синдром Морганьи-Адамса-Стокса) являются наиболее ярким клиническим проявлением ПЖБ II - III степени. Причиной потери сознания являются длительные периоды асистолии желудочков, т.е. периоды отсутствия эффективных сокращений желудочков, возникающие в результате перехода ПЖБ II степени в полную ПЖБ, когда еще не начал функционировать замещающий водитель ритма желудочков, расположенный ниже уровня блокады. Асистолия желудочков может развиться и при резком угнетении автоматизма эктопических центров II и III порядка при ПЖБ III степени. Таким образом, развитие синдрома связано с гипоксией мозга в результате редкого ритма сокращения желудочков или его отсутствия.
Врожденная изолированная ПЖБ непосредственно связана с неонатальная волчанкой - симптомокомплексом, диагностируемым у новорожденных, матери которых часто страдают аутоиммунными ревматическими заболеваниями), и проявляющимся двумя основными признаками - поражением кожи и сердца. Приблизительно в половине всех описанных случаев неонатальная волчанка представлена в виде изолированного кожного заболевания, а в другой половине наблюдений - в виде изолированной АВ-блокады. В 10% случаев имеется сочетание этих синдромов. Редко неонатальная волчанка сопровождается другими проявлениями, чаще преходящего характера [28].
Таким образом, при прогнозировании течения полной ПЖБ и рисков, связанных с ней, имеет значение: определение генеза блокады, выявление времени возникновения и степени прогрессирования ПЖБ, наличие клинических проявлений, включая синдром Морганьи-Адамса-Стокса. Наличие приступов потери сознания у пациентов с ПЖБ является предиктором внезапной сердечной смерти [7, 8, 14 - 17].
2. Диагностика заболевания или состояния (группы заболеваний или состояний) медицинские показания и противопоказания к применению методов диагностики
Диагноз ПЖБ устанавливается в соответствии с классификациями, представленными в разделе 1.5. на основании документированного подтверждения любым из инструментальных методов исследования в сочетании с клинической симптоматикой.
Критерии установления диагноза ПЖБ включает следующие этапы:
- выяснение жалоб и сбор анамнеза;
- объективное обследование;
- выполнение ЭКГ, холтеровского мониторирования сердечного ритма, эхокардиографии;
- другие дополнительные методы исследования - на втором этапе обследования (по показаниям);
- исключение обратимых причин ПЖБ.
2.1 Жалобы и анамнез
При анализе анамнеза основное значение придается выяснению обстоятельств обнаружения ПЖБ: случайно при проведении профилактического осмотра или диспансеризации, на фоне развития острого воспалительного процесса, при обследовании по поводу хронической патологии и т.д. Тщательный анализ анамнестических данных имеет одно из первостепенных значений в определении причины развития ПЖБ [7, 28].
Среди наиболее часто встречающихся жалоб:
- снижение толерантности к физическим нагрузкам (одышка при нагрузке);
- головокружение;
- потеря сознания (синкопальные состояния);
- кожные проявления в случае если ПЖБ входит в симптомокомплекс неонатальной волчанки.
2.2 Физикальное обследование
- Рекомендуется проведение физикального обследования пациента для диагностики основного заболевания/состояния, ставшего причиной развития ПЖБ. При проведении стандартного клинического осмотра следует обратить особое внимание на термометрию общую, измерение роста и массы тела, измерение частоты дыхания и частоты сердцебиения, артериального давления на периферических артериях [7, 29].
(УУР C, УДД 5)
- Рекомендуется при обследовании проводить выявление и диагностику сопутствующих нарушений ритма сердца и аритмогенных электрокардиографических синдромов [30 - 33].
(УУР C, УДД 5)
2.3 Лабораторные диагностические исследования
- Рекомендуется при выявлении у ребенка ПЖБ до рождения или после рождения в течение первых шести - восьми месяцев жизни, обследовать ребенка и его мать на носительство антител класса anti-SSA/Ro и anti-SSB/La для подтверждения врожденного характера АВ-блокады [10].
(УУР C, УДД 5)
Комментарии: В настоящее время для выявления материнских антител к растворимым ядерным антигенам 48-KD SSB/La, 52-KD SSA/Ro, и 60-KD SSA/Ro используется метод количественного анализа радиолиганд. Учитывая то, что обнаруженные во время исследования материнские аутоантитела класса anti-SSA/Ro и anti-SSB/La остаются пожизненно, то их определение, вне зависимости от сроков выявления полной атриовентрикулярной блокады, позволяет определить прогноз заболевания и подтвердить врожденный характер данного нарушения сердечного ритма.
- Рекомендуется общий (клинический) анализ крови развернутый, анализ крови биохимический общетерапевтический, исследование уровня натрия в крови, исследование уровня калия в крови, исследование уровня общего кальция в крови, исследование уровня/активности изоферментов креатинкиназы в крови, исследование уровня тропонинов I, T в крови, определение активности лактатдегидрогеназы в крови при выявлении у ребенка ПЖБ с целью исключения электролитных нарушений (гиперкалиемия и гиперкальциемия) и воспалительных/ишемических повреждений миокарда [7, 8, 14 - 16, 29].
(УУР C, УДД 5)
- Рекомендуются другие методы диагностики, направленные на выявление потенциальной причины развития ПЖБ (табл. 1) [7, 8, 14 - 17, 29, 34, 35, 36].
(УУР C, УДД 5)
Комментарии: Специфической лабораторной диагностики ПЖБ не существует, за исключением изолированной врожденной ПЖБ. Изменения в лабораторных показателях неспецифичны и являются проявлениями других сопутствующих заболеваний. Генетическое исследование проводится в семьях с подозрением на наследственный характер нарушений проводимости, либо при наличии других фенотипических признаков наследственных синдромов у пациента. Проводятся исследования с целью верификации возбудителя текущего инфекционного процесса (определение антител классов M, G (IgM, IgG) к аденовирусу (Adenovirus) в крови; Молекулярно-биологическое исследование периферической и пуповинной крови на парвовирус B19 (Parvovirus B19); Определение антител к парвовирусу B19 (Parvovirus B19) в крови; Определение антител классов M, G (IgM, IgG) к вирусу Эпштейна-Барра (Epstein - Barr virus) в крови; Определение антител к вирусу кори в крови; Определение антител к вирусу краснухи (Rubella virus) в крови; Определение антител к цитомегаловирусу (Cytomegalovirus) в крови; Определение антител к стафилококкам (Staphylococcus spp.) в крови; Бактериологическое исследование отделяемого из зева на стрептококк группы A (Streptococcus gr. A); Молекулярно-биологическое исследование мазков со слизистой оболочки носоглотки на возбудитель дифтерии (Corynebacterium diphtheriae); Определение антител к вирусу клещевого энцефалита в крови; Определение антител к возбудителям иксодовых клещевых боррелиозов группы Borrelia burgdorferi sensu lato в крови; Определение антител к вирусу простого герпеса (Herpes simplex virus) в крови; Молекулярно-биологическое исследование крови на вирус герпеса человека 7 типа (Herpes-virus 7); Определение антител к вирусу герпеса человека 6 типа (Herpesvirus 6) в крови; Определение антител классов M, G (IgM, IgG) к вирусу иммунодефицита человека ВИЧ-1 (Human immunodeficiency virus HIV 1) в крови; Определение антител классов M, G (IgM, IgG) к вирусу иммунодефицита человека ВИЧ-2 (Human immunodeficiency virus HIV 2) в крови; Исследование уровня антител классов M, G (IgM, IgG) к вирусу иммунодефицита человека ВИЧ-1/2 и антигена p24 (Human immunodeficiency virus HIV 1/2 + Agp24) в крови; Молекулярно-биологическое исследование крови на вирус Эпштейна-Барра (Epstein - Barr virus); Молекулярно-биологическое исследование мазков со слизистой оболочки носоглотки на аденовирус (Human Adenovirus); Молекулярно-биологическое исследование периферической и пуповинной крови на вирус краснухи (Rubella virus); Определение токсинов золотистого стафилококка (Staphylococcus aureus) в образцах фекалий; Иммунохроматографическое экспресс-исследование мазка из зева на стрептококки группы A; Микробиологическое (культуральное) исследование слизи и пленок с миндалин на палочку дифтерии (Corinebacterium diphtheriae); Определение суммарных антител к вирусу клещевого энцефалита в крови; Определение суммарных антител к возбудителям иксодовых клещевых боррелиозов группы Borrelia burgdorferi sensu lato в крови; Определение антигенов вируса простого герпеса 1 и 2 типов (Herpes simplex virus types 1, 2) в крови.
2.4 Инструментальные диагностические исследования
- Пациентам с подозрением на нарушение АВ проводимости рекомендуется регистрация ЭКГ в 12 отведениях для документации характера ритма, частоты сокращений, нарушения проводимости. При постоянном нарушении АВ проведения стандартная поверхностная ЭКГ достаточно информативна [8, 14, 15, 17, 29] (Приложение А3.3).
(УУР C, УДД 5)
Комментарии: ПЖБ I степени диагностируется при увеличении интервала PQ (R) свыше: у детей от 0 до 2 лет - 0,15 сек; у детей от 3 до 10 лет - 0,16 сек; у детей от 11 до 15 лет - 0,18 сек; у детей старшего возраста и взрослых - 0,19 - 0,20 сек. При ПЖБ I степени все зубцы P "проводятся" к желудочкам при постоянном, но пролонгированном интервале PQ (R).
Существует несколько электрокардиографических вариантов ПЖБ II степени: тип Мобитц I, тип Мобитц II. АВ блокада II степени тип Мобитц I, или блокада Самойлова-Венкебаха, характеризируется прогрессирующим удлинением интервала PQ (R) на ЭКГ с последующим выпадением желудочкового комплекса. При этом складывается закономерность: интервал PQ (R) перед выпадением (перед длинной паузой) оказывается продолжительнее интервала PQ (R) после выпадения комплекса QRS (сразу после длинной паузы). Желудочковые комплексы, как правило, имеют нормальную форму, так как синхронность возбуждения желудочков не нарушается. При ПЖБ II степени тип Мобитц II выпадение отдельных желудочковых сокращений не сопровождается постепенным удлинением интервала PQ (R), который остается постоянным, т.е. не изменяющимся от цикла к циклу (нормальным или удлиненным). Выпадение желудочковых комплексов может иметь определенную закономерность, но чаще всего бывает беспорядочным. Данный тип нарушения проведения в АВ соединении обусловлен дистальным поражением проводящей системы. Один из вариантов ПЖБ II степени получил название ПЖБ высокой степени, так как, степень нарушения атриовентрикулярной проводимости при этой блокаде значительно выше, что приводит к частому выпадению комплексов или выпадению подряд нескольких желудочковых комплексов. При высокой степени ПЖБ выпадают два и более желудочковых комплексов подряд (блокада 3:1; 4:1 и т.д.). При данном варианте блокады развивается резкая брадикардия, что может быть причиной развития синдрома Морганьи-Адамса-Стокса.
При ПЖБ III степени (полная ПЖБ) импульсы из предсердия полностью не проводятся к желудочкам. Поэтому предсердия и желудочки сокращаются независимо друг от друга, каждые в своем ритме: предсердия в более частом, синусовом ритме, а желудочки - в ритме АВ соединения. При этом определяется довольно выраженная желудочковая брадикардия, и ритм желудочков, как правило, ригидный. Если частота предсердных и желудочковых сокращений одинакова, то диагностировать полную АВ блокаду можно при длительной регистрации ЭКГ, когда возникает период несоответствия предсердных и желудочковых сокращений.
- Рекомендуется проведение холтеровского мониторирования сердечного ритма при интермиттирующем течении нарушения АВ проводимости и при определении показаний к имплантации электрокардиостимулятора [8, 14, 15, 17, 29].
(УУР C, УДД 5)
Комментарии: Холтеровское мониторирование сердечного ритма позволяет проводить наблюдение за ритмом сердца на протяжении 24 и более часов. Данный метод исследования используется при диагностике преходящих форм ПЖБ. Результаты холтеровского мониторирования сердечного ритма учитываются при определении показаний к имплантации электрокардиостимулятора при ПЖБ: наличие желудочковой эктопии, замещающего ритма с широкими желудочковыми комплексами, пауз ритма более чем в 3 раза превышающие базовый ритм.
- Рекомендуется проведение электрокардиографии с физической нагрузкой при выявлении у ребенка ПЖБ с целью диагностики хронотропной недостаточности [29, 37].
(УУР C, УДД 5)
Комментарии: Рекомендуется использовать тесты с дозированной физической нагрузкой (велоэргометрия и др.). Следует учитывать, что данные тесты имеют ограничения по возрасту и росту пациента.
- Рекомендуется проведение эхокардиографии при выявлении у ребенка ПЖБ с целью диагностики структурной патологии сердца, органической патологии миокарда (кардиомиопатии), признаков аритмогенной дисфункции миокарда, оценки гемодинамической значимости аритмии [8, 14, 15, 17, 29].
(УУР C, УДД 5)
Комментарии: Под аритмогенной дисфункцией миокарда подразумевают вторичную обратимую дисфункцию миокарда, проявляющуюся дилатацией всех полостей, начиная с предсердных камер, с последующим снижением сократительной способности миокарда желудочков, возникновением относительной митральной регургитации и развитием застойной сердечной недостаточности.
2.5 Иные диагностические исследования
Дифференциальная диагностика.
Дифференциальный диагноз ПЖБ I степени нужно проводить с эктопической предсердной тахикардией с удлинением АВ проводимости. Залпы эктопической тахикардии начинаются через экстрасистолию, ЧСС выше, чем частота основного ритма, морфология зубца Р эктопической тахикардии отличается от морфологии синусового ритма, залпы заканчиваются, как правило, через паузу ритма или через блокирование суправентрикулярной экстрасистолии.
Дифференциальный диагноз ПЖБ с блокированной суправентрикулярной экстрасистолии. Наличие блокированной суправентрикулярной экстрасистолии иногда может создавать впечатление, что у пациента имеется нарушение АВ проводимости и может быть ошибочно могут поставить диагноз АВ блокада II степени тип Мобитц II (2:1). На ЭКГ и на суточном мониторировании ЭКГ у таких больных отмечаются частые суправентрикулярные экстрасистолы, морфология зубца Р отличается от синусового зубца Р. Суправентрикулярная экстрасистолия может быть с аберрацией (с уширением комплекса QRS) в виде залпов (3-х и более экстрасистол подряд) эктопической тахикардии.
Дифференциальный диагноз ПЖБ с АВ диссоциацией. Характерный признак АВ-диссоциации - частота желудочковых сокращений выше, чем предсердных либо частота желудочковых сокращений совпадает с ритмом сокращения предсердий. АВ диссоциация наблюдается при выраженной синусовой (предсердной) брадикардии или ускоренном узловом ритме [7].
3. Лечение, включая медикаментозную и немедикаментозную терапии, диетотерапию, обезболивание, медицинские показания и противопоказания к применению методов лечения
Лечение пациентов с бессимптомной ПЖБ не требуется. Исключение составляют случаи проведения этиотропной, патогенетической и симптоматической терапии заболеваний, ставших причиной развития ПЖБ. Но независимо от причины АВ блокады, при появлении симптомов, связанных с брадикардией, проводится хирургическое лечение - имплантация кардиостимулятора
3.1 Консервативное лечение
- Рекомендуется назначение препарата из группы алкалоиды белладонны, третичные амины (#Атропин**), с целью купирования критической (симптомной) брадикардии при ПЖБ II - III степени в неотложных ситуациях после рождения в любом возрасте [15, 16, 29, 39, 40].
(УУР C, УДД 5)
Комментарии: Препарат #Атропина** вводится в экстренных случаях внутривенно в дозе 0,01 мг/кг.
- Рекомендуется назначение адренергических и дофаминергических средств (#Эпинефрин**, #Допамин**) с целью купирования критической брадикардии при ПЖБ II - III степени в неотложных ситуациях [29, 39, 41] (Приложение А3.2).
(УУР C, УДД 5)
Комментарии: Препарат #Эпинефрин** применяется в экстренных случаях при гемодинамически значимой брадикардии на фоне ПЖБ. Вводится внутривенно (инфузия) со скоростью 0,05 - 0,5 мкг/кг/мин. Препарат #Допамин** применяется в экстренных случаях при гемодинамически значимой брадикардии на фоне ПЖБ при условии низкой вероятности развития ишемии миокарда. Вводится внутривенной (инфузия) со скоростью от 5 до 15 мкг/кг/мин. Стартовая доза 5 мкг/кг/мин с последующим увеличением.
- Рекомендуется этиотропная, патогенетическая и симптоматическая терапия заболеваний, ставших причиной развития ПЖБ (табл. 1) [7, 8, 14 - 17, 29, 34, 35, 36].
(УДД 5, УУР C)
3.2 Хирургическое лечение
3.2.1 Временная электрокардиостимуляция для лечения неотложных состояний при ПЖБ
- Рекомендуется установка временного однокамерного не частотно-адаптивного электрокардиостимулятора.
- У детей с ПЖБ II - III степени в случае отсутствия эффекта от использования #атропина** и адренергических и дофаминергических средств (#эпинефрин**, #допамин**) при наличии симптомной брадикардии (синкопе, признаки застойной сердечной недостаточности, у новорожденных при частоте сердечных сокращений менее 55 ударов в минуту в отсутствии симптомов) [38, 42 - 45].
(УУР C, УДД 4)
Комментарии: Временная электрокардиостимуляция может быть осуществлена чрескожно, чреспищеводно или путем введения трансвенозного электрода для электрокардиостимуляции. Использование временной трансвенозной электрокардиостимуляции при брадикардиях у детей встречается редко, поскольку риск возникновения острого неблагоприятного сердечно-сосудистого события, связанного с ПЖБ, низкий, а временная трансвенозная стимуляция связана с осложнениями. Сообщается о частоте нежелательных явлений, связанных с временной трансвенозной доступом от 14 до 40%. Риск инфекционных осложнений при имплантации кардиостимулятора увеличивается у пациентов, у которых есть временный кардиостимулятор до постоянной имплантации. Однако в ряде случаев временная стимуляция считается клинически необходимой.
3.2.2 Постоянная электрокардиостимуляция
Постоянная электрокардиостимуляция проводится с помощью имплантированных электрокардиостимуляторов.
ИЗОЛИРОВАННАЯ ВРОЖДЕННАЯ ПЖБ
- Пациентам с изолированной врожденной ПЖБ III степени имплантация кардиостимулятора рекомендуется при наличии симптомов, связанных с брадикардией (синкопе, сердечная недостаточность) [46, 47, 48, 49, 50].
(УДД 4, УУР C)
- Пациентам с врожденной ПЖБ III степени имплантация кардиостимулятора рекомендуется при наличии систолической дисфункции системного желудочка [17, 48, 50, 51, 52, 53].
(УДД 5, УУР C)
- Пациентам с врожденной ПЖБ III степени имплантация кардиостимулятора рекомендуется при наличии ширококомплексного замещающего ритма, сложных желудочковых нарушений ритма сердца (полиморфная экстрасистолия, групповая экстрасистолия, желудочковая тахикардия) [17, 48, 50, 51, 52, 53].
(УДД 5, УУР C)
- Асимптомным пациентам первого года жизни с врожденной ПЖБ III степени имплантация кардиостимулятора рекомендуется при средней частоте сокращений желудочков <= 50 ударов минуту [48, 50, 54].
(УДД 5, УУР C)
- Асимптомным пациентам в возрасте старше 1 года с врожденной ПЖБ III степени имплантация кардиостимулятора рекомендуется при средней частоте сокращений желудочков < 50 ударов минуту или при наличии внезапных пауз ритма по продолжительности, превышающих базовый ритм более чем в три раза [17, 50, 51, 53, 54, 52].
(УДД 5, УУР C)
- Имплантация кардиостимулятора рекомендуется пациента с врожденной ПЖБ III степени сопровождающейся дилатацией системного желудочка (показатель z >= 3) [50, 53].
(УДД 5, УУР C)
ПЖБ ПРИ ВРОЖДЕННЫХ ПОРОКАХ СЕРДЦА
- Имплантация кардиостимулятора рекомендуется при врожденной ПЖБ III степени у новорожденных и детей первого года жизни со сложными врожденными пороками сердца, когда брадикардия связана с нарушением гемодинамики или когда средняя частота сокращения желудочков < 60 - 70 ударов в минуту [50, 52].
(УДД 5, УУР C)
ПОСЛЕОПЕРАЦИОННАЯ ПЖБ
- Пациентам с ПЖБ II - III степени возникшей после кардиохирургического вмешательства имплантация кардиостимулятора рекомендуется при сохранении ПЖБ на протяжении более 7 - 10 дней [17, 50, 52, 53, 57].
(УДД 5, УУР C)
- Имплантация кардиостимулятора рекомендуется при прогрессирующей ПЖБ II - III степени в отдаленном послеоперационном периоде особенно когда кардиохирургическое вмешательство было осложнено ПЖБ III степени с последующей трансформацией в синусовый ритм [50, 58].
(УДД 5, УУР C)
- Пациентам с необъяснимыми обмороками перенесших кардиохирургическое вмешательство осложненное ПЖБ III степени с последующей трансформацией в синусовый ритм имплантация кардиостимулятора рекомендуется при наличии остаточной бифасцикулярной блокады [47].
(УУР C, УДД 5)
ПРИОБРЕТЕННАЯ ПЖБ, СВЯЗАННАЯ С ДРУГИМИ ПРИЧИНАМИ
- Пациентам с приобретенной ПЖБ II - III степени имплантация кардиостимулятора рекомендуется при симптомной брадикардии, систолической дисфункцией системного желудочка в отсутствии обратимых причин [17, 50].
(УУР C, УДД 5)
- Имплантация кардиостимулятора рекомендуется пациентам с нейромышечным заболеванием при наличии симптомной брадикардии на фоне ПЖБ любой степени [17, 50, 51, 59].
(УУР C, УДД 5)
- Пациентам с ПЖБ любой степени и/или другими нарушениями проводимости при синдроме Кернса-Сейра имплантация кардиостимулятора рекомендуется из-за высокой вероятности прогрессирования ПЖБ [50, 60].
(УДД 4, УУР C)
- Имплантация кардиостимулятора рекомендуется пациентам с миотонической дистрофией 1 типа при ПЖБ I степени (PR > 240 мсек) или замедлении внутрижелудочковой проводимости (продолжительность комплекса QRS > 120 мсек) [50, 61].
(УУР C, УДД 5)
- Имплантация кардиостимулятора рекомендуется пациентам с заболеваниями, вызванными мутациями гена LMNA, кодирующего синтез белка ламин А/С (мышечная дистрофия Эмери-Дрейфуса, поясно-конечностная мышечная дистрофия) при ПЖБ I степени (PR > 240 мсек) и/или блокаде левой ножки пучка Гиса [50, 62].
(УУР C, УДД 5)
Комментарии: При наличии потенциально обратимых причин ПЖБ нет необходимости в постоянной электрокардиостимуляции. У пациентов с ПЖБ при миотонической дистрофии 1 типа, а также на фоне заболеваний, вызванных мутациями одного, кодирующего синтез белка ламин А/С (мышечная дистрофия Эмери-Дрейфуса, поясно-конечностная мышечная дистрофия), в качестве альтернативы имплантации электрокардиостимулятора, следует рассматривать имплантацию кардиовертера-дефибриллятора. До достижения веса 15 кг проводится имплантация электрокардиостимулятора с использованием только эпикардиальных электродов. У младенцев и детей раннего возраста со структурно нормальным сердцем, изолированной АВ блокадой и нормальной функцией желудочков в качестве исходного режима кардиостимуляции предпочтительно применение постоянного электрокардиостимулятора имплантируемого однокамерного, частотно-адаптивного ***. Эндокардиальная имплантация электродов допустима по достижении ребенком массы тела равной 15 кг. При массе тела от 15 до 19 кг имплантируется электрокардиостимулятор имплантируемый однокамерный, частотно-адаптивный***. При массе тела 20 кг и более имплантируется электрокардиостимулятор имплантируемый двухкамерный, частотно-адаптивный***. Противопоказания к эндокардиальной имплантации электродов: протезированный трехстворчатый клапан, право-левый внутрисердечный шунт, ВПС и корригированные ВПС препятствующие трансвенозному доступу к камерам сердца (наличие анатомических барьеров), повторные дислокации электродов [63 - 65].
При эпикардиальной стимуляции имплантация электродов на верхушку и боковую стенку левого желудочка имеет наибольший потенциал для предотвращения диссинхронии и снижения сократительной функции, стимуляция выходного отдела и боковой стенки ПЖ связана с высоким риском дисфункции левого желудочка [17, 64, 67, 68].
4. Медицинская реабилитация и санаторно-курортное лечение, медицинские показания и противопоказания к применению методов медицинской реабилитации, в том числе основанных на использовании природных лечебных факторов
Услуги по медицинской реабилитации пациента с заболеваниями сердечно-сосудистой системы осуществляются при необходимости в соответствии с основным заболеванием, ставшем причиной развития ПЖБ.
Специальной реабилитации пациенты после имплантации кардиостимулятора не требуют. В отдельных случаях предполагается щадящий режим физической активности с ограничением движений конечности большой амплитуды на стороне имплантации электрокардиостимулятора*** в подключичной области в течение 1 месяца.
5. Профилактика и диспансерное наблюдение, медицинские показания и противопоказания к применению методов профилактики
5.1. Профилактика
Профилактику развития ПЖБ возможно рассматривать в случае развития патологического процесса при повреждение ткани АВ-узла плода материнскими антителами класса анти-SSA/Ro анти-SSB/La, направленными к внутриклеточным растворимым рибонуклеопротеидным комплексам 48-KD SSB/La, 52-KD SSA/Ro, и 60-KD SSA/Ro. Рассматриваются варианты назначения женщинам носителям антител класса anti-SSA/Ro и anti-SSB/La #дексаметазона**, еженедельное применение плазмафереза для удаления циркулирующих антител, внутривенное введение иммуноглобулина (#иммуноглобулин человека нормальный**). #Дексаметазон** внутривенно или перорально назначается в дозе 4 мг/сутки с 16 по 24 недели беременности, внутривенное введение #иммуноглобулины, нормальные человеческие** в дозе 0,4 г/кг однократно на 12, 15, 18, 21 и 24 неделе беременности. В отдельных публикациях показано, что данное лечение способствует восстановлению АВ-проводимости, а результаты катамнестического наблюдения свидетельствуют об отсутствии рецидивов возникновения ПЖБ после завершения курса медикаментозной терапии. Эхокардиография плода выполняются каждые 1 - 2 недели [10, 11, 40, 41, 45, 68, 69].
5.2. Диспансерное наблюдение
Рекомендации по диспансерному наблюдению с предсердно-желудочковой блокадой:
- Рекомендуется пациентам с ПЖБ I - III степени диспансерное наблюдение у врача - детского кардиолога не реже одного раза в год [70, 71, 72].
(УУР C, УДД 5)
Комментарий: Диспансерное наблюдение включает диспансерный прием (осмотр, консультацию) врача - детского кардиолога, регистрацию ЭКГ, холтеровское мониторирование сердечного ритма и эхокардиографию. При прогрессировании ПЖБ в ходе динамического наблюдения и/или появлении симптомов, связанных с брадикардией (утомляемость, головокружение, обмороки) выполняется внеплановое обследование в условиях стационара. При лечении сопутствующих заболеваний следует избегать назначения лекарственных препаратов, угнетающих предсердно-желудочковое проведение. Возможность выполнения вакцинации определяется заболеванием, ставшим причиной развития ПЖБ. Факт наличия электрокардиостимулятора имплантируемого у пациента не является противопоказанием к вакцинации.
Рекомендации по диспансерному наблюдению пациентов с имплантированным электрокардиостимулятором***.
- Через 2 - 4 недели, через 6 месяцев, а затем не реже 1 раза в год после имплантации ЭКС*** рекомендуется диспансерный прием (осмотр, консультация) врача - детского кардиолога тестирование состояния, при необходимости программирование постоянного имплантируемого антиаритмического устройства [70, 71, 72].
(УУР C, УДД 5)
- Пациентам после имплантации кардиостимулятора*** для оценки функции желудочков рекомендуется выполнение эхокардиографии не реже 1 раза в год [50, 73].
(УДД 5, УУР C)
- Пациентам после имплантации кардиостимулятора*** с целью оценки смещения и целостности отведений электрокардиостимулятора рекомендуется прицельная рентгенография органов грудной клетки в двух проекциях каждые 1 - 3 года в зависимости от роста темпов роста ребенка и клинической ситуации [74, 75].
(УУР C, УДД 5)
Комментарии: В комплекс регулярного обследования входит: тестирование состояния, при необходимости программирование постоянного имплантируемого антиаритмического устройства; регистрация ЭКГ; холтеровское мониторирование сердечного ритма; эхокардиография; велоэргометрия (при наличии показаний). Сроки наблюдения и объем необходимого обследования могут варьировать от характера заболевания, ставшего причиной развития ПЖБ. Особое внимание следует уделять детям, кому имплантация ЭКС*** выполнялась в возрасте до 6 месяцев, вследствие более интенсивного физического развития и высокой вероятности формирования сердечной странгуляции из-за наличия избыточной длины электродов в средостении. Оценка прицельной рентгенографии органов грудной клетки в 2-х проекциях - передней и левой боковой - эффективный способ подтвердить или опровергнуть наличие сердечной странгуляции. Данный метод исследования у асимптомного пациента должен выполняется последовательно каждые 1 - 3 года после эпикардиальной имплантации до тех пор, пока в перикарде находится электрод избыточной длины [74, 75].
Рекомендации о допуске к занятиям спортом и допуске к соревнованиям пациентов с предсердно-желудочковой блокадой:
- При ПЖБ I степени [PQ (R) < 0,3 сек] и структурно нормальном сердце рекомендуются все состязательные виды спорта без ограничений в отсутствие риска развития ПЖБ более высокой степени, на что может указывать прогрессирование ПЖБ при физической нагрузке [77].
(УУР C, УДД 5)
- При наличии асимптомной ПЖБ II степени, тип Мобитц I, и структурно нормального сердца с улучшением АВ-проводимости или ее полным восстановлением при физической нагрузке рекомендуется допуск ко всем состязательным виды спорта без ограничений [77].
(УУР C, УДД 5)
- При наличии у спортсмена асимптомной ПЖБ II степени, тип Мобитц I, при которой не отмечается улучшения АВ-проводимости на фоне физической нагрузки, рекомендуется выполнить внутрисердечное электрофизиологическое исследование для выявления дистальной блокады ствола Гиса [77].
(УУР C, УДД 5)
- Бессимптомные пациенты с ПЖБ высокой степени или полной ПЖБ в отсутствии показаний в имплантации к электрокардиостимулятора а также с реакцией на нагрузку, приближенной к таковой при соответствующем виде спорта, рекомендуется допуск к занятиям спортом и участиям в спортивных соревнованиях [77].
(УУР C, УДД 5)
Комментарий: В данном случае рекомендуются виды спорта с низкими или средними динамическими и статическими нагрузками: боулинг, гольф, стрельба, автогонки, конный спорт, мотоспорт, гимнастика, каратэ, дзюдо, парусный спорт, стрельба из лука, фехтование, настольный теннис, теннис (парный разряд), волейбол, легкая атлетика (прыжки).
Рекомендации о допуске к занятиям спортом и допуске к соревнованиям пациентов имплантированным электрокардиостимулятором:
- Пациенты с постоянными имплантируемым электрокардиостимулятором рекомендуется допуск к занятиям спортом при отсутствии ограничивающих структурных и органических заболеваний сердца или симптомов [77].
(УУР C, УДД 5)
Комментарии: Могут быть рекомендованы виды спорта с низкими или средними динамическими и низкими статическими нагрузками, исключая травматичные - боулинг, гольф, стрельбу, фехтование, настольный теннис, теннис (парный разряд), волейбол.
- Пациентам, полностью зависящим от имплантируемого электрокардиостимулятора, не рекомендуется заниматься видами спорта, в которых существует риск столкновения, которое может привести к повреждению системы кардиостимулятора [77].
(УУР C, УДД 5)
Пациенты могут иметь дополнительные ограничения, связанные с заболеваниями, ставшими причиной развития ПЖБ.
6. Организация оказания медицинской помощи
Показания для плановой госпитализации (стационар).
1. Впервые выявленная стойкая ПЖБ I степени, ПЖБ II - III степени.
2. Появление симптоматики, потенциально ассоциированной с ПЖБ (предобморочное состояние, слабость, головокружение).
3. Плановая имплантация постоянного имплантируемого электрокардиостимулятора.
4. Плановая замена имплантированного электрокардиостимулятора.
5. Дисфункция имплантированного электрокардиостимулятора, требующая хирургического вмешательства.
6. Инфекционные осложнения, связанные с системой стимуляции.
Комментарии: Первичная госпитализация в специализированное детское кардиологическое отделение связана с диагностикой причины развития атриовентрикулярной блокады и проведением возможного этиотропного и патогенетического лечения. Госпитализация осуществляется в специализированное детское кардиологическое отделение медицинских организаций III уровня. При наличии показаний к имплантации кардиостимулятора при первичной госпитализации и отсутствии технической возможности, пациент направляется в учреждение, имеющим опыт имплантации кардистимулятора детям.
Показания для экстренной госпитализации (стационар).
1. Появление симптоматики, потенциально ассоциированной с ПЖБ (обморок, остановки кровообращения и восстановления нормальной сердечной деятельности).
2. Остро возникшая ПЖБ, требующая неотложной помощи.
2. Состояния, требующие временной стимуляции сердца.
3. Нарушения гемодинамики связанные с электрокардиостимулятором имплантируемым.
4. Острая дисфункция электрокардиостимулятора имплантируемого, требующая хирургической коррекции.
Комментарии: При обмороке или остановке кровообращения экстренные лечебные мероприятия должны быть начаты бригадой скорой медицинской помощи. Госпитализация пациента должна быть осуществлена в лечебное учреждение, которое имеет возможность оказания реаниматологической помощи. Оптимальна госпитализация в стационар, располагающий возможностями и опытом установки временной и постоянной кардиостимуляции.
Показания для выписки пациента из стационара.
1. Установление диагноза и/или отсутствие показаний к имплантации кардиостимулятора.
2. Пациенты с электрокардиостимулятором имплантируемым, которым дальнейшее стационарное лечение не требуется.
7. Дополнительная информация (в том числе факторы, влияющие на исход заболевания или состояния)
7.1. Осложнения:
Наиболее частые осложнения предсердно-желудочковых блокад - различные аритмии. Сердце пытается возместить выпавшее ритмичное сокращение. Могут развиваться замещающие ритмы, в том числе, желудочковая тахикардия. Эта аритмия опасна переходом в фибрилляцию желудочков и развитием внезапной смерти.
7.2. Исходы и прогноз
Для детей с транзиторной ПЖБ I степени прогноз заболевания благоприятный. На фоне лечения основного заболевания, как правило, происходит восстановление АВ-проведения. Стойкая АВ-блокада I степени (аутоиммунного, постмиокардитического или травматического характера) может прогрессировать в АВ-блокаду II - III степени за счет нарастания фиброза либо вследствие апоптоза клеток проводящей системы сердца. Для детей с АВ-блокадой III степени без имплантации кардиостимулятора прогноз заболевания в целом неблагоприятный.
Критерии оценки качества медицинской помощи
N
Критерии качества
Оценка выполнения (да/нет)
1.
Проведено физикальное обследование пациента для диагностики основного заболевания/состояния, вызвавшего ПЖБ
Да/нет
2.
Проведена регистрация электрокардиограммы в 12 отведениях для документирования характера ритма, частоты сокращений, типа нарушений проводимости
Да/нет
3.
Выполнено холтеровское мониторирование сердечного ритма при интермиттирующем течении нарушения АВ проводимости и при определении показаний к имплантации электрокардиостимулятора
Да/нет
4.
Выполнена эхокардиография
Да/нет
5.
Выполнен общий (клинический) анализ крови развернутый, анализ крови биохимический общетерапевтический, исследование уровня/активности изоферментов креатинкиназы в крови, исследование уровня тропонинов I, T в крови, определение активности лактатдегидрогеназы в крови, исследование уровня натрия в крови, исследование уровня калия в крови, исследование уровня общего кальция в крови.
Да/нет
6.
Выполнено обследование ребенка и матери на носительство антител класса anti-SSA/Ro и anti-SSB/La в случае диагностики изолированной ПЖБ в течение первых шести - восьми месяцев жизни.
Да/нет
7.
Выполнено назначение препарата из группы алкалоиды белладонны, третичные амины (атропина**) у пациентов с критической (симптомной) брадикардией при ПЖБ II - III степени в неотложных ситуациях после рождения в любом возрасте
Да/нет
8.
Выполнено назначение препарата из группы адренергические и дофаминергические средства (#допамин**, #эпинефрин**) у пациентов с критической (симптомной) брадикардией при ПЖБ II - III степени в неотложных ситуациях после рождения в любом возрасте
Да/нет
9.
Выполнена установка временного однокамерного не частотно-адаптивного электрокардиостимулятора при наличии показания в случае отсутствия эффекта от использования атропина** и адренергических и дофаминергических средства (#допамин**, #эпинефрин**) при наличии симптомной брадикардии (синкопе, признаки застойной сердечной недостаточности, у новорожденных при частоте сердечных сокращений менее 55 ударов в минуту в отсутствии симптомов)
Да/нет
10.
Выполнена имплантация постоянного электрокардиостимулятора пациентам с изолированной врожденной ПЖБ III степени при наличии симптомов, связанных с брадикардией (синкопе, сердечная недостаточность);
Да/нет
11.
Выполнена имплантация постоянного электрокардиостимулятора пациентам с изолированной врожденной ПЖБ III степени при наличии систолической дисфункции системного желудочка;
Да/нет
12.
Выполнена имплантация кардиостимулятора пациентам с изолированной врожденной ПЖБ III степени при наличии ширококомплексного замещающего ритма, сложных желудочковых нарушений ритма сердца (полиморфная экстрасистолия, групповая экстрасистолия, желудочковая тахикардия);
Да/нет
13.
Выполнена имплантация кардиостимулятора *** асимптомным пациентам первого года жизни с врожденной ПЖБ III степени при средней частоте сокращений желудочков <= 50 ударов в минуту
Да/нет
14.
Выполнена имплантация кардиостимулятора *** асимптомным пациентам в возрасте старше года с врожденной ПЖБ III степени при средней частоте сокращений желудочков < 50 ударов в минуту или при наличии внезапных пауз ритма превышающих базовый ритм более чем в три раза;
Да/нет
15.
Выполнена имплантация кардиостимулятора*** при врожденной ПЖБ III степени сопровождающейся дилатацией левого желудочка (показатель z >= 3);
Да/нет
16.
Выполнена имплантация кардиостимулятора*** при врожденной ПЖБ III степени у новорожденных и детей первого года жизни со сложными врожденными пороками сердца когда брадикардия связана с нарушением гемодинамики или когда средняя частота сокращений желудочков < 60 - 70 ударов в минуту;
Да/нет
17.
Выполнена имплантация кардиостимулятора пациентам с ПЖБ II - III степени возникшей после кардиохирургического вмешательства при сохранении ПЖБ на протяжении более 7 - 10 дней
Да/нет
18.
Выполнена имплантация кардиостимулятора при прогрессирующей ПЖБ II - III степени в отдаленном послеоперационном периоде, особенно в случае когда кардиохирургическое вмешательство было осложнено ПЖБ III степени с последующей трансформацией в синусовый ритм
Да/нет
19.
Выполнена имплантация кардиостимулятора пациентам с необъяснимыми обмороками перенесших кардиохирургическое вмешательство осложненное ПЖБ III степени с последующей трансформацией в синусовый ритм при наличии остаточной бифасцикулярной блокады
Да/нет
20.
Выполнена имплантация кардиостимулятора пациентам с приобретенной ПЖБ II - III степени при симптомной брадикардии, систолической дисфункцией системного желудочка в отсутствии обратимых причин
Да/нет
21.
Выполнена имплантация кардиостимулятора пациентам с нейромышечными заболевании при наличии симптомной брадикардии на фоне ПЖБ любой степени
Да/нет
22.
Выполнена имплантация кардиостимулятора пациентам с ПЖБ любой степени и/или других нарушениях проводимости при синдроме Кернса-Сейра из-за высокой вероятности прогрессирования ПЖБ;
Да/нет
23.
Выполнена имплантация кардиостимулятора пациентам с миотонической дистрофией 1 типа при ПЖБ I степени (PR > 240 мсек) или замедлении внутрижелудочковой проводимости (продолжительность комплекса QRS > 120 мсек);
Да/нет
24.
Выполнена имплантация кардиостимулятора:
пациентам с заболеваниями, вызванными мутациями гена LMNA, кодирующего синтез белка ламин A/C (мышечная дистрофия Эмери-Дрейфуса, поясно-конечностная мышечная дистрофия) при ПЖБ I степени (PR > 240 мсек) и/или блокаде левой ножки пучка Гиса
Да/нет
25.
Выполнен осмотр/консультация врача и тестирование состояния, при необходимости программирование, постоянного имплантируемого антиаритмического устройства через 2 - 4 недели, через 6 месяцев, а затем не реже 1 раза в год после имплантации электрокардиостимулятора.
Да/нет
26.
Выполнена эхокардиография после имплантации кардиостимулятора не реже 1 раза в год.
Да/нет
27.
Выполнена прицельная рентгенография органов грудной клетки в двух проекциях после имплантации кардиостимулятора каждые 1 - 3 года.
Да/нет
Список литературы
1. Howick JH. The Philosophy of Evidence-based Medicine. Wiley. p. 15.
2. Sackett DL, Rosenberg WM, Gray JA, et al. Evidence based medicine: what it is and what it isn't. BMJ. 1996; 312: 71 - 72.
3. Федеральный закон от 21.11.2011 N 323-ФЗ (ред. от 03.04.2017) "Об основах охраны здоровья граждан в Российской Федерации".
4. Андреева Н.С., Реброва О.Ю., Зорин Н.А. Системы оценки достоверности научных доказательств и убедительности рекомендаций: сравнительная характеристика и перспективы унификации.//Медицинские технологии. Оценка и выбор. - 2012. - N 4. - С. 10 - 24.
5. Макаров Л.М. Холтеровское мониторирование. 4-е изд. - М.: ИЖ "Медпрактика-М" - 2017. - 504 с.
6. Аритмии сердца: Механизмы, диагностика, лечение: Монография: В 3 т (под ред. Мандела В. Дж./пер. с англ. - М.: Медицина, 1996. - Т. 2. - 464 с.
7. Белозеров Ю.М. Детская кардиология. - МЕДпрес-информ, 2004. - 525c
8. Егоров Д.Ф., Адрианов А.В. Диагностика и лечение брадикардии у детей. - СПб.: "Человек", 2008. - 320 с.
9. Fetal Cardiology: Embryology, Genetics, Physiology, Echocardiographic Evaluation, Diagnosis and Perinatal Management of Cardiac Diseases. Third Edition. Simcha Yagel, Norman H. Silverman, Ulrich Gembruch - Taylor & Francis Group, LLC, 2019. - 860 p.
10. Melim C, Pimenta J, Areias JC. Congenital atrioventricular heart block: From diagnosis to treatment. Rev Port Cardiol. 2022 Mar; 41(3): 231 - 240. English, Portuguese. doi: 10.1016/j.repc.2019.09.021. Epub 2022 Feb 24. PMID: 36062654
11. Knight CL, Nelson-Piercy C. Management of systemic lupus erythematosus during pregnancy: challenges and solutions. Open Access Rheumatol. 2017 Mar 10; 9: 37 - 53. doi: 10.2147/OARRR.S87828. PMID: 28331377; PMCID: PMC5354538.
12.  P, Izmirly PM, Ramos-Casals M, Buyon JP, Khamashta MA. The clinical spectrum of autoimmune congenital heart block. Nat Rev Rheumatol. 2015 May; 11(5): 301 - 12. doi: 10.1038/nrrheum.2015.29. Epub 2015 Mar 24. PMID: 25800217; PMCID: PMC5551504.
P, Izmirly PM, Ramos-Casals M, Buyon JP, Khamashta MA. The clinical spectrum of autoimmune congenital heart block. Nat Rev Rheumatol. 2015 May; 11(5): 301 - 12. doi: 10.1038/nrrheum.2015.29. Epub 2015 Mar 24. PMID: 25800217; PMCID: PMC5551504.
13. Edward P., Walsh J., Philip Saul et al. Cardiac arrhythmias in children and young adults with congenital heart disease. - Lippricont Williams&Wilkins, 2001. - 516 p.
14. Hung D. Allen et al. Moss and Adams. Heart disease in infants, children, and adolescents: including the fetus and young adult. 7th ed. - Lippricont Williams&Wilkins, 2008. - Vol. 1. - 760 p.
15. Park Myung K. Pediatric Cardiology for Practitioners. 7 th ed. - Elsevier, 2021. - 487 p.
16. Baruteau, A.E.; Pass, R.H.; Thambo, J.B.; Behaghel, A.; Le Pennec, S.; Perdreau, E.; Combes, N.; Liberman, L.; McLeod, C.J. Congenital and childhood atrioventricular blocks: Pathophysiology and contemporary management. Eur. J. Pediatr. 2016, 175, 1235 - 1248.
17. Pharmacological and non-pharmacological therapy for arrhythmias in the pediatric population: EHRA and AEPC-Arrhythmia Working Group joint consensus statement. Brugada J, Blom N, Sarquella-Brugada G, Blomstrom-Lundqvist C, Deanfield J, Janousek J, Abrams D, Bauersfeld U, Brugada R, Drago F, de Groot N, Happonen JM, Hebe J, Yen Ho S, Marijon E, Paul T, Pfammatter JP, Rosenthal E; European Heart Rhythm Association; Association for European Paediatric and Congenital Cardiology. Europace. 2013 Sep; 15(9): 1337 - 82.
18. Alboni P, Anna Holz, Michele Brignole. Vagally mediated atrioventricular block: pathophysiology and diagnosis. Heart. 2013; 99: 904 - 908.
19. Ambrosi A, Wahren-Herlenius M Congenital heart block: evidence for a pathogenic role of maternal autoantibodies. Arthritis Res Ther. 2012; 14: 208.
20. Perinatal Outcome in Fetuses with Heterotaxy Syndrome and Atrioventricular Block or Bradycardia Maria C. Escobar-Diaz, Wayne Tworetzky, Kevin Friedman, Terra Lafranchi, Francis Fynn-Thompson, Mark E. Alexander, and Douglas Y. Mah Pediatr Cardiol. 2014 Aug; 35(6): 906 - 913.
21. Andrea W Wan, Alexandra Jevremovic, Elif Seda Selamet Tierney, Brian W McCrindle, Elizabeth Dunn, Cedric Manlhiot, Rachel M Wald, John P Kingdom, Edgar T Jaeggi, Lynne E Nield. Comparison of impact of prenatal versus postnatal diagnosis of congenitally corrected transposition of the great arteries. Am J Cardiol. 2009 Nov 1; 104(9): 1276 - 9.
22. Antoon F M Moorman, Vincent M Christoffels, Robert H Anderson. Anatomic substrates for cardiac conduction. Heart Rhythm. 2005 Aug; 2(8): 875 - 86.
23. Susan P Etheridge, Hitoshi Horigome, Denver Sallee, Anita Moon-Grady, Hsin-Yi Weng, Michael J Ackerman, D Woodrow Benson. Arrhythmia phenotype during fetal life suggests long-QT syndrome genotype: risk stratification of perinatal long-QT syndrome. Circ Arrhythm Electrophysiol. 2013 Oct; 6(5): 946 - 51
24. J P Buyon, R Hiebert, J Copel, J Craft, D Friedman, M Katholi, L A Lee, T T Provost, M Reichlin, L Rider, A Rupel, S Saleeb, W L Weston, M L Skovron. Autoimmune-associated congenital heart block: demographics, mortality, morbidity and recurrence rates obtained from a national neonatal lupus registry. Am Coll Cardiol. 1998; 31: 1658 - 66
25. Baruteau AE, Fouchard S, Behaghel A, Mabo P, Villain E, Thambo JB,  F, Gournay V, Rouault F, Chantepie A, Guillaumont S, Godart F, Bonnet C, Fraisse A, Schleich JM, Lusson JR, Dulac Y, Leclercq C, Daubert JC, Schott JJ, Le Marec H, Probst V Characteristics and long-term outcome of nonimmune isolated atrioventricular block diagnosed in utero or early childhood: amulticentre study. Eur Heart J. 2012; 33: 622 - 629;
F, Gournay V, Rouault F, Chantepie A, Guillaumont S, Godart F, Bonnet C, Fraisse A, Schleich JM, Lusson JR, Dulac Y, Leclercq C, Daubert JC, Schott JJ, Le Marec H, Probst V Characteristics and long-term outcome of nonimmune isolated atrioventricular block diagnosed in utero or early childhood: amulticentre study. Eur Heart J. 2012; 33: 622 - 629;
26. Bettina F Cuneo, Susan P Etheridge, Hitoshi Horigome, Denver Sallee, Anita Moon-Grady, Hsin-Yi Weng, Michael J Ackerman, D Woodrow Benson. Arrhythmia phenotype during fetal life suggests long-QT syndrome genotype: risk stratification of perinatal long-QT syndrome. Circ Arrhythm Electrophysiol. 2013 Oct; 6(5): 946 - 51
27. Liberman L, Silver ES, Chai P, Anderson BR (2016) Incidence and characteristics of heart block after heart surgery in pediatric patients: a multicenter study. J Thorac Cardiovasc Surg. 2016 Jul; 152(1): 197 - 202.
28. Кошелева Н.М., Алекберова З.С. Неонатальная волчанка//Современная ревматология. - 2015. - Т. 9. - N 4 - С. 92 - 97.
29. Topjian AA, Raymond TT, Atkins D, Chan M, Duff JP, Joyner BL Jr, Lasa JJ, Lavonas EJ, Levy A, Mahgoub M, Meckler GD, Roberts KE, Sutton RM, Schexnayder SM; Pediatric Basic and Advanced Life Support Collaborators. Part 4: Pediatric Basic and Advanced Life Support: 2020 American Heart Association Guidelines for Cardiopulmonary Resuscitation and Emergency Cardiovascular Care. Circulation. 2020 Oct 20; 142(16_suppl_2): S469 - S523
30. Brignole M, Auricchio A, Baron-Esquivias G, et al. 2013 ESC Guidelines on cardiac pacing and cardiac resynchronization therapy. The Task Force on cardiac pacing and resynchronization therapy of the European Society of Cardiology (ESC). Developed in collaboration with the European Heart Rhythm Association (EHRA). European Heart Journal. 2013; 34: 2281 - 2329;
31. Del Rosso A, Ungar A, Maggi R, et al. Clinical predictors of cardiac syncope at initial evaluation in patients referred urgently to a general hospital: the EGSYS score. Heart. 2008; 94: 1620 - 6;
32. Perez-Rodon J, Martinez-Alday J, Baron-Esquivias G, et al. Prognostic value of the electrocardiogram in patients with syncope: data from the group for syncope study in the emergency room (GESINUR). Heart Rhythm. 2014; 11: 2035 - 44;
33. Shen WK, Sheldon RS, Benditt DG, et al. 2017 ACC/AHA/HRS guideline for the evaluation and management of patients with syncope: a report of the American College of Cardiology/American Heart Association Task Force on Clinical Practice Guidelines and the Heart Rhythm Society. Circulation. 2017; 136: 60 - 122
34. Wan, D, Blakely, C, Branscombe, P, et al. Lyme carditis and high-degree atrioventricular block. Am J Cardiol. 2018; 121: 1102 - 4
35. Mandell, BF. Cardiovascular involvement in systemic lupus erythematosus. Semin Arthritis Rheum. 1987; 17: 126 - 41.
36. Nakayama, Y, Ohno, M, Yonemura, S, et al. A case of transient 2:1 atrioventricular block, resolved by thyroxine supplementation for subclinical hypothyroidism. Pacing Clin Electrophysiol. 2006; 29: 106 - 8
37. Brubaker, PH, Kitzman, DW. Chronotropic incompetence: causes, consequences, and management. Circulation. 2011; 123: 1010 - 20
38. Ricardo Munoz, Eduardo M. da Cruz Carol G. Vetterly, David S. Cooper, Donald Berry Editors Handbook of Pediatric Cardiovascular Drugs. Second Edition. Springer-Verlag, London, 2014 - 636 p
39. Нарушения ритма сердца у детей: основные принципы диагностики и лечения/И.А. Ковалев, С.В. Попов, И.А. Антонченко., Мурзина О.Ю., Свинцова Л.И., Николишин А.Н. - Томск: СТТ (Издательство "STT"), 2006. - 272 с. - ISBN 5-93629-240-1. - EDN VWTQYR.
40. Kukla, P.; Podlejska, B.;  , J. Congenital Complete Heart Block-To Stimulate (When?) or Not to Stimulate? Healthcare 2024, 12, 1158. https://doi.org/10.3390/healthcare12121158
, J. Congenital Complete Heart Block-To Stimulate (When?) or Not to Stimulate? Healthcare 2024, 12, 1158. https://doi.org/10.3390/healthcare12121158
41. Saleh F, Greene EA, Mathison D. Evaluation and management of atrioventricular block in children. Curr Opin Pediatr. 2014 Jun; 26(3): 279 - 85.
42. LotfyW, Hegazy R, Abdelaziz O, Sobhy R, Hasanein H, Shaltout F Permanent cardiac pacing in pediatric patients. Pediatr Cardiol. 2013; 34: 273 - 280.
43. Henry M. Spotnitz, MD. Transvenous Pacing in Infants and Children With Congenital Heart Disease. Ann Thorac Surg 1990; 49: 495 - 6;
44. Robert Whitehill, Peter Fischbach, Jessica Posey, ![]() Fawwaz Shaw, and Chad Mao, Temporary transvenous atrioventricular synchronous pacing using a single lead in a pediatric patient. HeartRhythm Case Rep. 2019 Dec; 5(12): 593 - 596;
Fawwaz Shaw, and Chad Mao, Temporary transvenous atrioventricular synchronous pacing using a single lead in a pediatric patient. HeartRhythm Case Rep. 2019 Dec; 5(12): 593 - 596;
45. Murphy JJ. Current practice and complications of temporary transvenous cardiac pacing. BMJ. 1996; 312: 1134
46. Michele Brignole, Angelo Auricchio, Gonzalo Baron-Esquivias, PierreBordachar, Giuseppe Boriani, Ole-A Breithardt, John Cleland, Jean-Claude Deharo, Victoria Delgado, Perry M.Elliott, Bulent Gorenek, CarstenW. Israel, Christophe Leclercq, Cecilia Linde, ![]() 'sMont, Luigi Padeletti, Richard Sutton, PanosE. Vardas/2013 ESC Guidelines cardiac pacing and cardiac resynchronization therapy//European Heart Journal. 2013. - Vol. 34 - P. 2281 - 2329.
'sMont, Luigi Padeletti, Richard Sutton, PanosE. Vardas/2013 ESC Guidelines cardiac pacing and cardiac resynchronization therapy//European Heart Journal. 2013. - Vol. 34 - P. 2281 - 2329.
47. Epstein AE, DiMarco JP, Ellenbogen KA, Estes NA 3rd, Freedman RA, Gettes LS, Gillinov AM, Gregoratos G, Hammill SC, Hayes DL, Hlatky MA, Newby LK, Page RL, Schoenfeld MH, Silka MJ, Stevenson LW, Sweeney MO, Tracy CM, Epstein AE, Darbar D, DiMarco JP, Dunbar SB, Estes NA 3rd, Ferguson TB Jr, Hammill SC, Karasik PE, Link MS, Marine JE, Schoenfeld MH, Shanker AJ, Silka MJ, Stevenson LW, Stevenson WG, Varosy PD ACCF/AHA/HRS focused update incorporated into the ACCF/AHA/HRS 2008 guidelines for device-based therapy of cardiac rhythm abnormalities: a report of the American College of Cardiology Foundation/American Heart Association Task Force on Practice Guidelines and the HeartRhythm Society. JAmCollCardiol. 2013 Jan 22; 61(3): e6-75.
48. Jaeggi ET, Hamilton RM, Silverman ED, et al. Outcome of children with fetal, neonatal or childhood diagnosis of isolated congenital atrioventricular block. J Am Coll Cardiol 2002; 39: 130 - 137.
49. Baruteau AE, Fouchard S, Behaghel A, et al. Characteristics and long-term outcome of non-immune isolated atrioventricular block diagnosed in utero or early childhood: a multicentre study. Eur Heart J 2012; 33: 622 - 629.
50. Michael J. Silka1, Maully J. Shah, Jennifer N. Avari Silva et al. 2021 PACES expert consensus statement on the indications and management of cardiovascular implantable electronic devices in pediatric patients: executive summary. Heart Rhythm. 2021 Nov; 18(11): 1925 - 1950.
51. Kusumoto FM, Schoenfeld MH, Barrett C, et al. 2018 ACC/AHA/HRS guideline on the evaluation and management of patients with bradycardia and cardiac conduction delay: a report of the American College of Cardiology/American Heart Association Task Force on Clinical Practice Guidelines, and the Heart Rhythm Society. J Am Coll Cardiol 2019; 74: 932 - 987.
52. Jaeggi ET, Hornberger LK, Smallhorn JF, et al. Prenatal diagnosis of complete atrioventricular block associated with structural heart disease: combined experience of two tertiary care centers and review of the literature. Ultrasound Obstet Gynecol 2005; 26: 16 - 21.
53. Udink ten Cate F, Breur JM, Cohen MI, et al. Dilated cardiomyopathy in isolated congenital complete atrioventricular block: early and long term risk in children. J Am Coll Cardiol 2001; 7: 1129 - 1134.
54. Karpawich PP, Gillette PC, Garson Jr. A, et al. Congenital complete atrioventricular block: clinical and electrophysiologic predictors of need for pacemaker insertion. Am J Cardiol 1981; 48: 1098 - 1102.
55. Epstein AE, Dimarco JP, Ellenbogen KA, et al. ACC/AHA/HRS 2008 guidelines for device-based therapy of cardiac rhythm abnormalities. Heart Rhythm 2008; 5: 934 - 955.
56. Dewey RC, Capeless MA, Levy AM. Use of ambulatory electrocardiographic monitoring to identify high-risk patients with congenital complete heart block. N Engl J Med 1987; 316: 835 - 839.
57. Weindling SN, Saul PJ, Gamble WJ, et al. Duration of complete atrioventricular block after congenital heart disease surgery. Am J Cardiol 1998; 82: 525 - 527; 21. Romer AJ, Tabbutt S, Etheridge SP, et al. Atrioventricular block after congenital heart surgery: analysis from the Pediatric Cardiac Critical Care Consortium. J Thorac Cardiovasc Surg 2019; 157: 1168 - 1177;
58. Villain E, Ouarda F, Beyler C, et al. Predictive factors for late complete atrio-ventricular block after surgical treatment for congenital cardiomyopathy. Arch Mal Coeur Vaiss 2003; 96: 495 - 498.
59. Feingold B, Mahle WT, Auerbach S, et al. Management of cardiac involvement associated with neuromuscular diseases: a scientific statement from the American heart association. Circulation 2017; 136: e200 - e231
60. Di Mambro C, Tamborrino PP, Silvetti MS, et al. Progressive involvement of cardiac conduction system in paediatric patients with Kearns-Sayre syndrome: how to predict occurrence of complete heart block and sudden cardiac death? Europace 2021; 6: 948 - 957.
61. Wahbi K, Meune C, Porcher R, et al. Electrophysiological study with prophylactic pacing and survival in adults with myotonic dystrophy and conduction system disease. JAMA 2012; 307: 1292 - 1301.
62. Hasselberg NE, Edvardsen T, Petri H, et al. Risk prediction of ventricular arrhythmias and myocardial function in Lamin A/C mutation positive subjects. Europace 2014; 16: 563 - 571.
63. Minimally Invasive Epicardial Pacemaker Implantation in Neonates with Congenital Heart Block. R. Costa, K. R da Silva, M. M.i Filho, R. Carrillo. Arq Bras Cardiol. 2017; 109(4): 331 - 339.
64. Alban-Elouen Baruteau, R H. Pass, JB Thambo, A Behaghe, S Le Pennec, E Perdreau, N Combes, L Liberman, C J. McLeod. Congenital and childhood atrioventricular blocks: pathophysiology and contemporary management Eur J Pediatr. 2016; 175: 1235 - 1248
65. M S Horenstein, P P Karpawich, M V Tantengco. Single versus dual chamber pacing in the young: noninvasive comparative evaluation of cardiac function. Pacing Clin Electrophysiol. 2003 May; 26(5): 1208 - 11
66.  J., van Geldorp I.E.,
J., van Geldorp I.E.,  S., Rosenthal E., Nugent K., Tomaske M.,
S., Rosenthal E., Nugent K., Tomaske M., ![]() A., Elders J., Hiippala A., Kerst G., Gebauer R.A.,
A., Elders J., Hiippala A., Kerst G., Gebauer R.A., ![]() P., Frias P., Gabbarini F., Clur S-A., Nagel B., Ganame J., Papagiannis J., Marek J., Tisma-Dupanovic S., Tsao S.,
P., Frias P., Gabbarini F., Clur S-A., Nagel B., Ganame J., Papagiannis J., Marek J., Tisma-Dupanovic S., Tsao S.,  J-H., Wren Ch., Friedberg M., de Guillebon M., Volaufova J., Prinzen F.W., Delhaas T. Permanent cardiac pacing in children: choosing the optimal pacing site: a multicenter study. Circ. 2013; 127(5): 613 - 623.
J-H., Wren Ch., Friedberg M., de Guillebon M., Volaufova J., Prinzen F.W., Delhaas T. Permanent cardiac pacing in children: choosing the optimal pacing site: a multicenter study. Circ. 2013; 127(5): 613 - 623.
67. (61) Left ventricular apical pacing in children: feasibility and long-termeffect on ventricular function. J Kovanda, M. Lozek, S Ono, P. Kubus, V Tomek, J Janousek. Europace 2020; 22: 306 - 313
68. Ruffatti A, Milanesi O, Chiandetti L, Cerutti A, Gervasi MT, De Silvestro G, Pengo V, Punzi L. A combination therapy to treat second-degree anti-Ro/La-related congenital heart block: a strategy to avoid stable third-degree heart block?//Lupus. 2012 May; 21(6): 666 - 71.
69. Amit Saxena, Peter M. Izmirly, Barbara Mendez, Jill P. Buyon, Deborah M. Friedman. Prevention and treatment in utero of autoimmune associated congenital heart block//Cardiol Rev. 2014; 22(6): 263 - 267.
70. Ковалев И.А., Белозеров Ю.М., Садыкова Д.И., Сабирова Д.Р., Яковлева Л.В., Хабибрахманова З.Р., Сакерин А.С. Атриовентрикулярная (предсердно-желудочковая) блокада у детей. Педиатрическая фармакология. 2018; 15 (5): 365 - 375.
71. Slotwiner D, Varma N, Akar J, et al. HRS expert consensus statement on remote interrogation and monitoring for cardiovascular implantable electronic devices. Heart Rhythm 2015; 12: E69 - E100.
72. Wilkoff BL, Auricchio A, Brugada J, et al. HRS/EHRA expert consensus on the monitoring of cardiovascular implantable electronic devices (CIEDs): description of techniques, indications, personnel, frequency and ethical considerations. Heart Rhythm 2008; 5: 907 - 925].
73. Tantengco MV, Thomas RL, Karpawich PP. Left ventricular dysfunction after long-term right ventricular apical pacing in the young. J Am Coll Cardiol 2001; 37: 2093 - 2100.
74. (62) Carreras EM, Duncan WJ, Djurdjev O, Campbell AI. Cardiac strangulation following epicardial pacemaker implantation: a rare pediatric complication. J Thorac Cardiovasc Surg. 2015; 149(2): 522 - 27.
75. Takeuchi D, Tomizawa Y. Cardiac strangulation from epicardial pacemaker leads: diagnosis, treatment, and prevention. Gen Thorac Cardiovasc Surg. 2015; 63(1): 22 - 9.
76. Slotwiner D, Varma N, Akar JG, et al. Совместное экспертное заключение Американского общества сердечного ритма (HRS) по удаленной телеметрии и мониторингу сердечно-сосудистых имплантируемых электронных устройств.//Вестник аритмологии. - 2015. - N 82. - С. 43 - 72.
77. Eligibility and disqualification recommendations for competitive athletes with cardiovascular abnormalities: task force 9: arrhythmias and conduction defects: a scientific statement from the American Heart Association and American College of Cardiology. Zipes DP, Link MS, Ackerman MJ, et al. J Am Coll Cardiol. 2015; 66(21):2412 - 2423.
Приложение А1
СОСТАВ
РАБОЧЕЙ ГРУППЫ ПО РАЗРАБОТКЕ И ПЕРЕСМОТРУ
КЛИНИЧЕСКИХ РЕКОМЕНДАЦИЙ
1. Ковалев И.А., д.м.н., профессор (Москва) - председатель рабочей группы, член АДКР
2. Джаффарова О.Ю. к.м.н. (Томск) - секретарь рабочей группы, член АДКР
3. Попов С.В., д.м.н., профессор (Томск) - член ВНОА, член РКО
4. Криволапов С.Н. (Томск) - член ВНОА, член РКО
5. Соловьев В.М. (Москва) - член АДКР
6. Термосесов С.А. (Москва) - член ВНОА
7. Садыкова Д.И., д.м.н. (Казань) - член АДКР
Члены Рабочей группы подтвердили отсутствие финансовой поддержки/конфликта интересов. В случае сообщения о наличии конфликта интересов член(ы) рабочей группы был(и) исключен(ы) из обсуждения разделов, связанных с областью конфликта интересов.
Приложение А2
МЕТОДОЛОГИЯ РАЗРАБОТКИ КЛИНИЧЕСКИХ РЕКОМЕНДАЦИЙ
Клинические рекомендации разработаны специалистами-экспертами Всероссийская общественная организация "Ассоциация детских кардиологов России" и Всероссийского научного общества специалистов по клинической электрофизиологии, аритмологии и кардиостимуляции - на основе достижений доказательной медицины, отечественного и зарубежного клинического опыта в области нарушений ритма сердца у детей. Основой настоящей версии клинических рекомендаций стали российские и зарубежные фундаментальные руководства и монографии по детской кардиологии, кардиологии, результаты исследований, последние версии европейских и американских методических руководств. Источниками современных обновлений были журнальные публикации в авторитетных рецензируемых журналах, входящих в российские и зарубежные индексы научного цитирования.
Целевая аудитория данных клинических рекомендаций:
1. Врач - детский кардиолог.
2. Врач - педиатр.
3. Врач - сердечно-сосудистый хирург.
4. Врач общей практики (семейный врач).
В ходе разработки использованы система шкал УДД и УУР для лечебных, реабилитационных, профилактических вмешательств и диагностических вмешательств (Таблицы ПА2-1, ПА2-4 и ПА2-2), введенная в 2018 г. ФГБУ ЦЭККМП Минздрава РФ.
Таблица ПА2-1. Шкала оценки уровней достоверности доказательств (УДД) для методов диагностики (диагностических вмешательств)
УДД
Расшифровка
1
Систематические обзоры исследований с контролем референсным методом или систематический обзор рандомизированных клинических исследований с применением метаанализа
2
Отдельные исследования с контролем референсным методом или отдельные рандомизированные клинические исследования и систематические обзоры исследований любого дизайна, за исключением рандомизированных клинических исследований, с применением метаанализа
3
Исследования без последовательного контроля референсным методом или исследования с референсным методом, не являющимся независимым от исследуемого метода или нерандомизированные сравнительные исследования, в том числе когортные исследования
4
Несравнительные исследования, описание клинического случая
5
Имеется лишь обоснование механизма действия или мнение экспертов
Таблица ПА2-1. Шкала оценки уровней достоверности доказательств (УДД) для методов профилактики, лечения, медицинской реабилитации, в том числе основанных на использовании природных лечебных факторов (профилактических, лечебных, реабилитационных вмешательств)
УДД
Расшифровка
1
Систематический обзор рандомизированных клинических исследований с применением метаанализа
2
Отдельные рандомизированные клинические исследования и систематические обзоры исследований любого дизайна, за исключением рандомизированных клинических исследований, с применением метаанализа
3
Нерандомизированные сравнительные исследования, в том числе когортные исследования
4
Несравнительные исследования, описание клинического случая или серии случаев, исследования "случай-контроль"
5
Имеется лишь обоснование механизма действия вмешательства (доклинические исследования) или мнение экспертов
Таблица ПА2-1. Шкала оценки уровней убедительности рекомендаций (УУР) для методов профилактики, диагностики, лечения, медицинской реабилитации, в том числе основанных на использовании природных лечебных факторов (профилактических, диагностических, лечебных, реабилитационных вмешательств)
УУР
Расшифровка
A
Сильная рекомендация (все рассматриваемые критерии эффективности (исходы) являются важными, все исследования имеют высокое или удовлетворительное методологическое качество, их выводы по интересующим исходам являются согласованными)
B
Условная рекомендация (не все рассматриваемые критерии эффективности (исходы) являются важными, не все исследования имеют высокое или удовлетворительное методологическое качество и/или их выводы по интересующим исходам не являются согласованными)
C
Слабая рекомендация (отсутствие доказательств надлежащего качества (все рассматриваемые критерии эффективности (исходы) являются неважными, все исследования имеют низкое методологическое качество и их выводы по интересующим исходам не являются согласованными)
Порядок обновления клинических рекомендаций.
Механизм обновления клинических рекомендаций предусматривает их систематическую актуализацию - не реже чем один раз в три года, а также при появлении новых данных с позиции доказательной медицины по вопросам диагностики, лечения, профилактики и реабилитации конкретных заболеваний, наличии обоснованных дополнений/замечаний к ранее утвержденным КР, но не чаще 1 раза в 6 месяцев.
Приложение А3
СПРАВОЧНЫЕ МАТЕРИАЛЫ,
ВКЛЮЧАЯ СООТВЕТСТВИЕ ПОКАЗАНИЙ К ПРИМЕНЕНИЮ
И ПРОТИВОПОКАЗАНИЙ, СПОСОБОВ ПРИМЕНЕНИЯ И ДОЗ
ЛЕКАРСТВЕННЫХ ПРЕПАРАТОВ, ИНСТРУКЦИИ ПО ПРИМЕНЕНИЮ
ЛЕКАРСТВЕННОГО ПРЕПАРАТА
Приложение А3.1
НОРМАТИВНЫЕ ДОКУМЕНТЫ
И РЕСУРСЫ, НА ОСНОВАНИИ КОТОРЫХ РАЗРАБОТАНЫ
КЛИНИЧЕСКИЕ РЕКОМЕНДАЦИИ
1. Приказ Министерства здравоохранения Российской Федерации от 28.02.2019 N 103н "Об утверждении порядка и сроков разработки клинических рекомендаций, их пересмотра, типовой формы клинических рекомендаций и требований к их структуре, составу и научной обоснованности, включаемой в клинические рекомендации информации".
2. Приказ Министерства здравоохранения Российской Федерации от 25 октября 2012 г. N 440н "Об утверждении Порядка оказания медицинской помощи по профилю "детская кардиология".
3. Приказ Министерства здравоохранения Российской Федерации от 10 мая 2017 г. N 203н "Об утверждении критериев оценки качества медицинской помощи".
4. Методические рекомендации по оценке достоверности доказательств и убедительности рекомендаций. ФГБУ ЦЭККМП Минздрава России, 2018.
5. Распоряжение Правительства РФ от 31 декабря 2018 г. N 3053-р "Об утверждении перечня медицинских изделий, имплантируемых в организм человека при оказании медицинской помощи в рамках программы государственных гарантий бесплатного оказания гражданам медицинской помощи, а также перечня медицинских изделий, отпускаемых по рецептам на медицинские изделия при предоставлении набора социальных услуг".
6. Распоряжение Правительства РФ от 12 октября 2019 г. N 2406-р "Об утверждении перечня жизненно необходимых и важнейших лекарственных препаратов, а также перечней лекарственных препаратов для медицинского применения и минимального ассортимента лекарственных препаратов, необходимых для оказания медицинской помощи" (в ред. распоряжений Правительства РФ от 26.04.2020 N 1142-р, от 12.10.2020 N 2626-р, от 23.11.2020 N 3073-р).
Приложение А3.2
СПОСОБ
ПРИМЕНЕНИЯ И ДОЗЫ ЛЕКАРСТВЕННЫХ ПРЕПАРАТОВ,
ИСПОЛЬЗУЕМЫХ ПРИ ЛЕЧЕНИИ ПЖБ
Препарат
(класс)
Дозы и схемы
Механизм действия
Параметры, требующие внимания
Нежелательные побочные эффекты
Межлекарственные взаимодействия
#Атропина сульфат**
[29, 39, 41]
Внутривенно 0.01 мг/кг (минимальная доза 0.1 мг)
Блокатор м-холинорецепторов. Фармакологический эффект быстрый.
Исследование пульса.
Регистрация электрокардиограммы
Сухость во рту, покраснение и сухость кожи, беспокойство, усталость, болезненные позывы на мочеиспускание, замедление моторики желудочно-кишечного тракта, сердцебиение, расстройство сознания, головная боль, тремор
При одновременном применении с антихолинергическими средствами и средствами, обладающими антихолинергической активностью, усиливается антихолинергическое действие
#Допамин**
[29, 39, 41]
Вводится внутривенно (инфузия) со скоростью от 5 до 15 мкг/кг/мин. Стартовая доза 5 мкг/кг/мин с последующим увеличением.
Стимулятор адренергических и допаминэргических рецепторов, селективная ренальная вазодилатация.
Фармакологический эффект быстрый
Исследование пульса.
Регистрация электрокардиограммы
Тахиаритмия, экстрасистолия, повышение или снижение артериального давления, головная боль, тошнота
При одновременном применении с диуретиками усиливается мочегонное действие.
При одновременном применении с сердечными гликозидами возможно повышение риска развития нарушений сердечного ритма, аддитивный положительный инотропный эффект
#Эпинефрин**
[29, 39, 41]
Вводится внутривенно (инфузия) со скоростью 0,01 - 1 мкг/кг/мин
Адреномиметик, оказывает прямое стимулирующее действие на - и -адренорецепторы.
Исследование пульса.
Регистрация электрокардиограммы
Тахиаритмия, экстрасистолия, повышение или снижение артериального давления, головная боль, тошнота
При одновременном применении с антигипертензивными средствами (в т.ч. с диуретиками) - снижение их эффективности.
При одновременном применении с сердечными гликозидами возможно повышение риска развития нарушений сердечного ритма, аддитивный положительный инотропный эффект
Приложение А3.3
ЭЛЕКТРОКАРДИОГРАФИЧЕСКИЕ КРИТЕРИИ ПЖБ
Вид нарушений ритма сердца
Признак
Атриовентрикулярная блокада
I степень
II степень
Мобиц I
II степень
Мобиц II
III степень
Частота ритма
Предсердий: регулярный и соответствует возрасту.
Желудочков: регулярный, соответствует частоте предсердий.
Предсердий: регулярный и соответствует возрасту.
Предсердий: регулярный и соответствует возрасту.
Предсердий: регулярный и соответствует возрасту в случае отсутствия сердечной недостаточности.
Желудочков: регулярный, но значительно меньше, чем частота предсердий.
Желудочков: нерегулярный, меньше, чем частота предсердий, из-за периодического "выпадения" QRS.
Желудочков: нерегулярный, меньше, чем частота предсердий, из-за периодического "выпадения" QRS
Регулярность ритма
Регулярный
Не регулярный
Не регулярный
Регулярный
Зубец P
Нормальный
Нормальный
Нормальный
Нормальный
PQ (R) интервал
Увеличен
Прогрессивное увеличение с последующим "выпадением" QRS.
Нормальный и слегка увеличенный фиксированный размер. Периодически за P волной отсутствует QRS.
Не определяется из-за АВ-диссоциации.
QRS комплекс
Узкий в случае отсутствия блокады ножек пучка Гиса.
Узкий в случае отсутствия блокады ножек пучка Гиса.
Узкий в случае отсутствия блокады ножек пучка Гиса.
Узкий в случае отсутствия блокады ножек пучка Гиса.
Приложение А3.3
ВИДЫ
ЭЛЕКТРОКАРДИОСТИМУЛЯТОРОВ ИМПЛАНТИРУЕМЫХ,
ИСПОЛЬЗУЕМЫХ ПРИ ЛЕЧЕНИИ ПЖБ У ДЕТЕЙ
Код вида в номенклатурной классификации медицинских изделий
Наименование вида медицинского изделия
139070
Электрокардиостимулятор имплантируемый двухкамерный, частотно-адаптивный***
210180
Электрокардиостимулятор имплантируемый однокамерный, частотно-адаптивный***
Приложение Б
АЛГОРИТМЫ ДЕЙСТВИЙ ВРАЧА
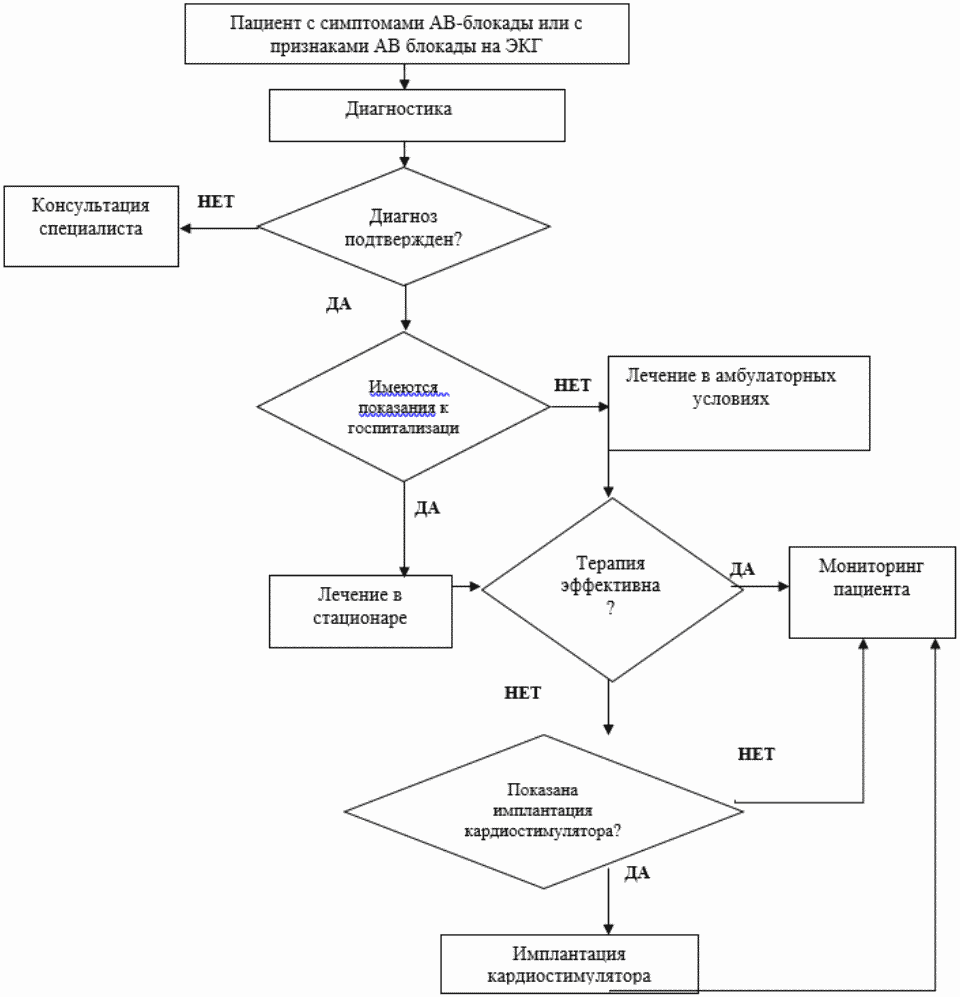
Приложение В
ИНФОРМАЦИЯ ДЛЯ ПАЦИЕНТА
Предсердно-желудочковая (атриовентрикулярная) блокада - разновидность блокады сердца, обозначающая нарушение проведения электрического импульса из предсердий в желудочки (атриовентрикулярная проводимость), нередко приводящее к нарушению ритма сердца и гемодинамики. Выделяют три степени атриовентрикулярной блокады в зависимости от тяжести нарушения проведения.
В основе нарушения проводимости могут лежать как функциональные причины: интенсивные занятия спортом, употребление некоторых лекарств (бета-адреноблокаторы, антиаритмических препаратов I и III классов, сердечные гликозиды, и др.); органические заболевания: инфаркт миокарда, миокардиты, кардиомиопатии, дегенеративные и инфильтративные заболевания миокарда, врожденные пороки сердца и др.; хирургическая травма при коррекции пороков сердца. ПЖБ может носить изолированный врожденный характер. Это приводит к поражению наиболее слабого звена проводящей системы сердца: атриовентрикулярного соединения. В результате электрический импульс или достигает желудочков с задержкой или проведение его частично или полностью блокируется.
ПЖБ I степени требует только наблюдения. Если блокада II или III степени связана с употреблением лекарственных препаратов, необходима корректировка их дозы вплоть до полной отмены. При врожденной или приобретенной ПЖБ в краткосрочной перспективе при наличии показаний проводится лечение, направленное на основное заболевание, ставшего причиной развития ПЖБ, и учащение ритма сердца (медикаменты, установка временной системы электрокардиостимуляции). В долгосрочной перспективе жизнеспасающим методом лечения является имплантация постоянного имплантируемого электрокардиостимулятора.
Для детей с транзиторной ПЖБ I степени прогноз заболевания благоприятный. На фоне лечения основного заболевания, как правило, происходит восстановление АВ проведения. Стойкая АВ блокада I степени (аутоиммунного, постмиокардитического или травматического характера) может прогрессировать в АВ блокаду II - III степени. Для детей с АВ блокадой III степени без имплантации кардиостимулятора прогноз заболевания в целом неблагоприятный.
Многие дети с кардиостимулятором продолжают обычную повседневную деятельность, включая занятия физкультурой и спортом. Обсудите с врачом вашу активность и образ жизни.
Приложение Г1 - ГN
ШКАЛЫ ОЦЕНКИ, ВОПРОСНИКИ И ДРУГИЕ ОЦЕНОЧНЫЕ ИНСТРУМЕНТЫ
СОСТОЯНИЯ ПАЦИЕНТА, ПРИВЕДЕННЫЕ В КЛИНИЧЕСКИХ РЕКОМЕНДАЦИЯХ
Не применяются.
