"Клинические рекомендации "Лимфомы из клеток мантии у взрослых"
МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ
КЛИНИЧЕСКИЕ РЕКОМЕНДАЦИИ
ЛИМФОМЫ ИЗ КЛЕТОК МАНТИИ У ВЗРОСЛЫХ
МКБ 10: C85.7
Год утверждения (частота пересмотра): 2017 (пересмотр каждые 2 года)
ID: КР136
URL
Профессиональные ассоциации
- Национальное гематологическое общество
Ключевые слова
лимфома из клеток мантийной зоны;
диагностика;
терапия 1-й, 2-й линий;
высокодозная химиотерапия;
аутологичная трансплантация гемопоэтических клеток крови;
высокие дозы цитозара;
продолжительная ремиссия;
Список сокращений
ЛКМ - лимфома из клеток мантии
ЕВМТ - Европейского общества трансплантации костного мозга
аутоТГСК - аутологичная трансплантация гемопоэтических стволовых клеток
ОО - общий ответ
ПР - полная ремиссия
БСВ - бессобытийная выживаемость
MIPIb (Mantle cell lymphoma International Prognostic Index) - международный прогностический индекс лимфомы из клеток мантийной зоны биологический
ЛДГ - лактатдегидрогеназа
ЖКТ - желудочно-кишечный тракт
ЦНС - центральная нервная система
ИФТ - иммунофенотипирование
Термины и определения
Доказательная медицина - подход к медицинской практике, при котором решения о применении профилактических, диагностических и лечебных мероприятий принимаются исходя из имеющихся доказательств их эффективности и безопасности, а такие доказательства подвергаются поиску, сравнению, обобщению и широкому распространению для использования в интересах пациентов.
Заболевание - возникающее в связи с воздействием патогенных факторов нарушение деятельности организма, работоспособности, способности адаптироваться к изменяющимся условиям внешней и внутренней среды при одновременном изменении защитно-компенсаторных и защитно-приспособительных реакций и механизмов организма.
Инструментальная диагностика - диагностика с использованием для обследования больного различных приборов, аппаратов и инструментов.
Лабораторная диагностика - совокупность методов, направленных на анализ исследуемого материала с помощью различного специализированного оборудования.
Уровень достоверности доказательств - положение, истинность которого должна быть доказана аргументом, или опровергнута антитезисом.
Хирургическое вмешательство - инвазивная процедура, может использоваться в целях диагностики и\или как метод лечения заболевания.
Терапия 1-й, 2-й и 3-й линии - очередность схем лечения ЛКМ.
1. Краткая информация
1.1 Определение
Лимфома из клеток мантии (син.: из мантийных клеток) - это B-клеточная лимфома из мелких клеток с, как правило, агрессивным течением [1].
1.2 Этиология и патогенез
Одним из ключевых событий в патогенезе ЛКМ считается транслокация t(11; 14)(q13; q32). Ген CCND1, находящийся в 13 локусе длинного плеча 11 хромосомы, переносится в область энхансера конституционально гиперэкспрессированных в B-лимфоцитах генов IgVH. В результате развивается гиперэкспрессия белка-регулятора клеточного цикла циклина D1. Установление факта избыточной экспрессии циклина D1 является одним из основных молекулярных и иммунологических маркеров ЛКМ. Анализ точек разрыва в 11q13 и 14q32 показал, что транслокация происходит во время первичной перестройки генов иммуноглобулинов в костномозговой клетке-предшественнице B-лимфопоэза между одним из D- и J-сегментов генов иммуноглобулинов. Около 50% перестроек в 11q13 происходят в регионе, обозначенным как главный кластер транслокации. Оптимальным способом определения t(11; 14)(q13; q32) является флуоресцентная гибридизация in situ (FISH): частота выявления транслокации этим методом при ЛКМ достигает 99%. Партнером для гена, кодирующего циклин D1, могут стать и локусы легких цепей иммуноглобулинов: t(2; 11) (p11; q13) и t(11; 22) (q13; q11). Вариантные транслокации встречаются менее чем в 1% случаев ЛКМ. Циклин D1 в комплексе с циклин-зависимыми киназами 4 и 6 (CDK4/6) является регулятором перехода клеток из G1 в S-фазу клеточного цикла. Активный комплекс циклин D1/CDK4(6) фосфорилирует ретинобластомный протеин (RB), белок-блокатор транскрипционного фактора E2F. Комплекс циклин D1/CDK4 имеет и киназанезависимые функции, связываясь, в частности, с белком-блокатором клеточного цикла p27kip, который, в свою очередь, титрует из ядра комплекс циклина E/CDK2. Это дополнительно способствует ускорению клеточного цикла. При ЛКМ циклин-зависимые киназы CDK4 и CDK6, необходимые для реализации циклина D1a, часто гиперэкспрессированы. В случае CDK4 это достигается за счет амплификации гена CDK4, а в случае CDK6 отмечается снижение экспрессии микроPHK-29. Это ведет к стабилизации транскрипта CDK6 и способствует гиперэкспрессии белка, что ассоциируется с более короткой выживаемостью больных. В цитоплазме циклин D1 полиубиквитинируется через E3 лигазу SKpl-Cul1-F (SCF; FBX4-![]() Crystallin) и деградируется через протеасому. Мутации T268A и мутации в E3 убиквитино-лигазном комплексе увеличивают ядерную экспрессию циклина D1. Несмотря на отсутствие описаний таких мутаций при ЛКМ, PI3K/Akt-зависимое ингибирование
Crystallin) и деградируется через протеасому. Мутации T268A и мутации в E3 убиквитино-лигазном комплексе увеличивают ядерную экспрессию циклина D1. Несмотря на отсутствие описаний таких мутаций при ЛКМ, PI3K/Akt-зависимое ингибирование  имеет схожий эффект и создает вклад в дисрегуляцию циклина D1 при ЛКМ. [7]
имеет схожий эффект и создает вклад в дисрегуляцию циклина D1 при ЛКМ. [7]
Таким образом, транскрипция, трансляция, включение в комплексы, расположение в клетке и деградация циклина D1a подвергаются очень тонкой регулировке. Сама по себе гиперэкспрессия циклина D1a не способствуют развитию опухоли у мышей с удаленным тимусом и отсутствием T-лимфоцитов. Только наличие дополнительных событий, способствующих увеличению внутриядерной концентрации и времени экспозиции циклина D1, а также, что важно, и циклинзависимых киназ 4 и 6 позволяет реализоваться их онкогенному потенциалу.
ЛКМ характеризуется нестабильностью кариотипа и значительным количеством вторичных хромосомных аберраций. В последнее время описано большое количество случаев ЛКМ, сопровождающихся наличием однородительских дисомий, способствующих инактивации генов-супрессоров опухоли. Например, одна из наиболее часто обнаруживаемых однородительских дисомий, включает участок короткого плеча 17 хромосомы и способствует инактивации гена TP53. Приобретенные хромосомные аберрации в генах контроля повреждений ДНК и в генах, относящихся к контролю динамики микротрубочек, могут дополнительно увеличить генетическую нестабильность. Вторичные генетические нарушения, которые затрагивают пути восстановления поврежденной ДНК находятся под особым интересом, так как могут быть причиной рефрактерности к химиотерапии. Мутации, ведущие к инактивации гена ATM (ataxia-telangiectasia mutated) встречается при ЛКМ в 40 - 75% случаев. ATM-киназа в норме играет ключевую роль в ответе на повреждения ДНК, являясь геном-супрессором опухоли и входит в состав ATM-p53 пути. Повреждение ДНК индуцирует активацию киназ ATM и ATR, которые вместе с белками p53 и p14/ARF могут индуцировать арест клеточного цикла, восстановление ДНК или апоптоз. E3-убиквитин-лигаза MDM2, нацеленная на p53 для его протеасомной деградации ингибируется ARF, который в свою очередь ингибируется BMI1. CHK1 и CHK2 активируются ATR и ATM, соответственно. Это ведет к фосфорилированию ключевых субстратов p53, CDC25A, CDC25B и аресту клеточного цикла. Подавление экспрессии CHK1 (cell checkpoint kinase 1), CHK2 и 2-серин-треонин киназы, участвующих в ответе на повреждение ДНК вместе с белками ATM и p53, снижает контроль за S-фазой клеточного цикла и выявляется в случаях ЛКМ с высокой генетической нестабильностью. [14, 17, 18]
1.3 Эпидемиология
Лимфома из клеток мантии (ЛКМ) составляет около 6% от всех вновь диагностированных случаев неходжкинских лимфом. В Западной Европе, Скандинавии и США ее частота варьирует от 0,5 до 0,7 на 100.000 населения, причем у людей старше 65 лет заболеваемость возрастает до 3,9 на 100.000. Болеют преимущественно мужчины старше 60 лет (медиана возраста 65 - 75 лет, М:Ж - 2-4:1). В США ежегодно заболевают от 5.000 до 6.000 человек, что косвенным образом свидетельствует о том, что в РФ ежегодно должно выявляться не менее 2.500 новых случаев. [1]
1.4 Кодирование по МКБ 10
C85.7 - другие неуточненные типы неходжкинской лимфомы
1.5 Классификация
Стадирование ЛКМ по Ann-Arbor
Стадия I Вовлечение одной группы лимфатических узлов (ЛУ) - I или локализованное поражение одного экстралимфатического органа или ткани - I E
Стадия II Вовлечение >= 2 групп ЛУ по одну сторону диафрагмы - II
или локализованное поражение одного экстралимфатического органа
или ткани с вовлечением >= 1 группы ЛУ по ту же сторону диафрагмы - II E
Стадия III Вовлечение групп ЛУ по обе стороны диафрагмы с/без локализованного поражения экстралимфатического органа или ткани - III E, селезенки - III S, или того и другого - III S + E
Стадия IV Диффузное или диссеминированное поражение экстралимфатического органа или ткани с/без вовлечения ЛУ
Для стадировании ЛКМ используется такая же модифицированная классификация по стадиям Ann Arbor, как при лимфоме Ходжкина и большинстве других лимфопролиферативных заболеваний. Принимая во внимание вовлечение периферической крови и костного мозга в большинстве случаев, стадирование по Ann Arbor не имеет прогностического значения. [2]
1.6 Клинические признаки
В 90% случаев диагноз устанавливается в III или IV стадии. Часто имеются B-симптомы - лихорадка (гипертермию), ночные поты, потерю массы тела более 10% за последние полгода. Спленомегалия (увеличение размеров селезенки наблюдается более чем у 50% пациентов. Часто выявляется лейкоцитоз с наличием клеток МКЛ в крови. Наиболее распространенной экстранодальной локализацией при МКЛ является поражение желудочно-кишечного тракта: лимфоматозные полипы толстой кишки или желудка. Следует помнить, что даже при отсутствии явных полипов или видимых изменений слизистой оболочки при гистологическом исследовании биоптатов могут выявляться участки опухолевой инфильтрации. Может наблюдаться также поражение мочеполовой системы, легких и мягких тканей, в том числе мягких тканей головы и шеи, периорбитальных тканей глаза. Поражение центральной нервной системы может развиться у больных с ЛКМ, в связи с прогрессированием заболевания. Также у небольшой части больных, особенно с бластоидным вариантом МКЛ, встречаются изолированные ЦНС-рецидивы после первоначально успешного лечения. Частота возникновения ЦНС-рецидивов увеличилась в последнее время в связи с появлением более эффективной системной терапии и увеличением продолжительности выживания больных с МКЛ. [3, 4, 5]
2. Диагностика
2.1 Жалобы и анамнез
Жалобы пациентов при ЛКМ не отличаются от таковых при других видах лимфом. Пациенты отмечают увеличение размеров лимфоузлов, чувство тяжести в левом подреберье, нарастающую слабость, частые инфекционные заболевания.
- Рекомендуется при сборе анамнеза заболевания и семейного анамнеза выяснять следующее: установление предшествующих развитию заболевания факторов: (бактериальная или вирусная инфекция, стресс, сопутствующие заболевания, пересадка органов в анамнезе); семейный анамнез: болезни системы кроветворения у кровных родственников. [3, 4]
Уровень убедительности рекомендаций B (уровень достоверности доказательств - 2++)
Комментарии: сбор жалоб и анамнеза позволит определить объем обследования больного.
2.2 Физикальное обследование
- Рекомендуется обращать внимание на следующие факторы: гипертермия, снижение массы тела и симптомы интоксикации, гепато- и спленомегалия, лимфаденопатия, патология молочных желез, сердца, вен нижних конечностей, врожденные аномалии. [3, 4].
Уровень убедительности рекомендаций B (уровень достоверности доказательств - 2++)
Комментарии: позволяет отдифференцировать реактивную лимфаденопатию от системного заболевания крови.
2.3 Лабораторная диагностика
- Рекомендуется для диагностики ЛКМ проведение обязательных лабораторных тестов. [3, 4]
Уровень убедительности рекомендаций B (уровень достоверности доказательств - 1+)
Комментарии: список обязательных лабораторных тестов включает общий анализ крови (ОАК), мазок периферической крови, биохимический анализ крови, ВИЧ, вирусы гепатитов B и C, количественный иммунохимический анализ крови, исследование костного мозга (цитологическое и гистологическое), иммуногистохимическое исследование костного мозга, биопсия опухолевого лимфоузла или образования (цитологическое и гистологическое), иммуногистохимическое исследование опухолевого образца.
- Рекомендуется выполнить развернутый клинический анализ крови с определением гемоглобина, эритроцитов, тромбоцитов, лейкоцитов, подсчетом лейкоцитарной формулы. [3, 4]
Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1++).
Комментарии: объем исследования включает в себя дифференциальный подсчет клеток крови с использованием автоматического анализатора; обязателен оптический подсчет количества тромбоцитов (по Фонио), исследование морфологии эритроцитов, тромбоцитов, нейтрофилов по мазку, СОЭ;
- Рекомендуется выполнить биохимический анализ крови [3, 4]
Комментарий: включает обязательное определение следующих параметров - ЛДГ, мочевая кислота, мочевина, креатинин, общий белок, альбумин, билирубин, АСТ, АЛТ, щелочная фосфатаза, электролиты, кальций
Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1++).
Комментарии: для оценки функционального состояния внутренних органов и выявления сопутствующей патологии.
- Рекомендуется выполнить общий анализ мочи [3, 4]
Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1++).
- Рекомендуется выполнить коагулограмму [3, 4]
Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1++).
Комментарии: для оценки функционального состояния тромбоцитов и свертывающей системы, в том числе для исключения синдрома диссеминированного внутрисосудистого свертывания крови (ДВС).
- Рекомендуется исследование крови на вирус иммунодефицита человека (ВИЧ), антител к вирусам гепатитов B и C и проведение полимеразной цепной реакции (ПЦР) на эти вирусы. [3, 4]
Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1++).
Комментарии: для исключения ВИЧ и гепатит ассоциированных лимфатических заболеваний; определения степени активности инфекционного процесса при его наличии
- Рекомендуется количественный иммунохимический анализ крови. [3, 4]
Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1++).
Комментарии: для исключения иммунодефицитных состояний, наличия моноклональной секреции патологических белков.
- Рекомендуется выполнить определение группы крови, резус-фактора [3, 4]
Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1++).
Комментарии: определение группы крови обязательно всем больным для подбора компонентов крови для переливания при развитии панцитопении.
- Рекомендуется выполнить (у женщин детородного возраста) тест на беременность [3, 4]
Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1++).
- Рекомендуется обязательное выполнение биопсии лимфоузла или любого другого очага поражения с морфологическим (цитологическим и гистологическим) исследованием, при необходимости с использованием инвазивных методов диагностики. [3, 4]
Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1++).
Комментарии: диагноз лимфомы устанавливают только на основании морфологического исследования биоптата. Морфологическое исследование проводится с помощью гистологического и иммуногистохимического методов. В части случаев необходимо проведение цитологического, молекулярно-биологических и генетических тестов. Одно цитологическое исследование пунктатов или мазков-отпечатков лимфатических узлов или других опухолевых очагов не является достаточным основанием для нозологической верификации лимфом. В исключительных случаях (локализация опухоли в труднодоступных анатомических зонах) объектом исследования может быть тканевой материал, полученный с помощью "пистолетной" ("кор"-) биопсии.
- Рекомендуется обязательное выполнение иммуногистохимического [3, 4]
исследования биоптата опухоли с обязательным определением экспрессии следующих антигенов: CD3, CD5, CD10, CD20, CD23, cyclinD1 и Ki67, при возможности SOX11.
Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1++).
- Рекомендуется при наличии лимфоцитоза выполнение иммунофенотипирования (ИФТ) методом проточной цитометрии. [3, 4]
Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1++).
Комментарии: выполнение ИФТ обязательно при наличии лимфоцитоза в общем анализе крови (независимо от числа лейкоцитов), или в миелограмме, а также при преобладании лимфоидных клеток, атипичных лимфоцитов или клеток с бластной морфологией в плевральной, асцитической или других биологических жидкостях. Выполнение ИФТ позволяет быстро провести дифференциальную диагностику опухолевого и реактивного лимфоцитоза, что важно для определения дальнейшей тактики обследования пациента. Материалом для ИФТ могут служить клетки крови, костного мозга, выпотных жидкостей, бронхоальвеолярного смыва, ликвора, гомогенизированные образцы тканей (селезенка, лимфатические узлы и т.д.), клеточная суспензия, полученная при аспирационной тонкоигольной пункции лимфатических узлов.
- Рекомендуется выполнять цитогенетическое исследование для определения t(11; 14)(q13; q32). При невозможности выполнения стандартного цитогенетического исследования или его отрицательном результате желательно определение t(11; 14)(q13; q32) методом FISH на отпечатках лимфоузла, срезах с парафиновых блоков, в клетках крови или костного мозга. [3, 4]
Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1++).
Комментарии: Во всех иммунологически сомнительных случаях (например, отсутствие CD5, наличие CD23 или слабая экспрессия CD20) проведение цитогенетического исследования особо целесообразно.
- Рекомендуется цитологическое и гистологическое исследование костного мозга. [3, 4]
Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1++).
Комментарии: миелограмма и трепанобиопсия костного мозга обязательна всем больным для определения объема поражения.
- Рекомендуется при отсутствии гистологических признаков определение вовлечения костного мозга с использованием метода FISH, проточной цитофлюориметрии или определение B-клеточной клональности методом ПЦР на основании анализа реарранжировок генов тяжелых цепей иммуноглобулинов. [3, 4]
Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1++).
Комментарии: Морфологическое исследование пунктата костного мозга (стернального или др.) не заменяет гистологическое исследование трепанобиоптата. Отсутствие морфологических признаков поражения костного мозга не исключает наличие минимального поражения костного мозга, что выявляется с помощью ПЦР метода.
- Рекомендуется во всех ситуациях и обязательно при наличии показаний (бластоидный вариант +/- гиперлейкоцитоз, общемозговая симптоматика) выполнение люмбальной пункции с цитологическим исследованием ликвора для исключения нейролейкемии. Профилактическое интратекальное введение цитостатиков на усмотрение лечащего врача. [3, 4]
Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1++).
Рекомендуется выполнение эзофагогастродуоденоскопии и фиброколоноскопии с обязательными биопсиями слизистых желудка, двенадцатиперстной кишки, сигмовидной кишки, поперечной ободочной и слепой кишки, даже при отсутствии визуальных признаков вовлечения органа ("слепые" биопсии). Эндоскопическое исследование является обязательным для больных с локальными стадиями. [3, 4]
- Рекомендуется иммунохимическое исследование белков сыворотки крови и мочи с определением концентрации ![]() -микроглобулина.
-микроглобулина.
Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1++).
- Рекомендуется рассмотрение вопроса об использовании антипневмококковой вакцины, особенно у пациентов старше 60 лет, кому планируется длительная поддерживающая терапия ритуксимабом. [3, 4]
Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1++).
- Рекомендуется проведение биопсии дополнительных очагов поражения. [3, 4]
Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1++).
Комментарии: при определении стадии опухолевого процесса может потребоваться биопсия других очагов поражения, если нельзя исключить их опухолевую природу другими способами.
- Рекомендуется обязательное выполнение повторной биопсии и морфологического исследования пораженных лимфатических узлов или очагов, расположенных экстранодально при рецидиве или прогрессировании заболевания. [3, 4]
Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1++).
Комментарии: повторная биопсия позволит уточнить морологический вариант рецидива/прогрессии, исключить неопухолевое поражение (например, туберкулез, грибковая инвазия, вторая опухоль). Повторная биопсия также показана при наличии резидуальных очагов для подтверждения ремиссии.
- Рекомендуется повторная аспирация и трепанобиопсия костного мозга для плановой оценки результатов лечения (при исходном поражении костного мозга) и при появлении клинически немотивированных цитопении и лихорадки (вне зависимости от наличия исходного поражения). [3, 4]
Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1++).
Комментарии: аспират костного мозга может быть информативен для оценки регенерации и диспластических изменений миелопоэза. У больных с поражением костного мозга цитологическое исследование пунктата для оценки изменений объема опухолевой инфильтрации не всегда информативно.
2.4 Инструментальная диагностика
Рекомендуется выполнить КТ шеи, грудной клетки, органов брюшной полости и малого таза (по возможности с внутривенным контрастированием). [3, 4]
Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1++).
Комментарии: позволяют выявить очаги опухолевого поражения. [3, 4]
- Рекомендуется выполнить рентгенографию органов грудной клетки в двух проекциях (при невозможности выполнения КТ) [3, 4]
Уровень убедительности рекомендаций D (уровень достоверности доказательств - 3).
- Рекомендуется выполнение УЗИ периферических лимфатических, внутрибрюшных и забрюшинных узлов и органов брюшной полости [3, 4]
Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1++).
Комментарий: УЗИ может использоваться для определения исходного объема поражения и контроля за лечением.
- Рекомендуется выполнение эндоскопического исследования желудка [3, 4]
Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1++).
- Рекомендуется выполнения ПЭТ при сохранении остаточных образований после завершения высокодозной терапии и аутоТГСК с целью решения вопроса о проведении локальной лучевой терапии. [37]
Уровень убедительности рекомендаций D (уровень достоверности доказательств - 3).
Комментарии: Роль ПЭТ недостаточно определена из-за большой вероятности получения ложноотрицательных результатов у больных ЛКМ. Это связанно с тем, что уровень пролиферативной активности опухолевых клеток в значительной части случаев близок к нормальному и повышенного накопления радиофармпрепарата не происходит. Исходная чувствительность метода достигает только 67%, особенно много ложноотрицательных результатов при вовлечении ЖКТ.
2.5 Дополнительные исследования, консультации специалистов
При наличии показаний могут выполняться дополнительные методы исследования:
- Рекомендуется исследование прямой пробы Кумбса [3, 4]
Комментарий: выполняется при наличии клинических или лабораторных признаках гемолиза
Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1++).
- Рекомендуется выполнение рентгенографии костей скелета, сцинтиграфия костей скелета [3, 4]
Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1++).
Комментарии: при необходимости исключения поражения костей
- Рекомендуется консультация гинеколога (у женщин) [3, 4]
Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1++).
- Рекомендуется консультация смежных специалистов при показаниях (исключение туберкулеза, оказание ЛОР-пособия и т.п.) [3, 4]
Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1++).
2.6. Стадирование. Формулирование диагноза
Для стадировании ЛКМ используется такая же модифицированная классификация по стадиям Ann Arbor, как при лимфоме Ходжкина и большинстве других лимфопролиферативных заболеваний. Принимая во внимание вовлечение периферической крови и костного мозга в абсолютном большинстве случаев, стадирование по Ann Arbor не имеет прогностического значения. [2]
Клинической системой прогноза ЛКМ является международный прогностический индекс лимфомы из клеток мантии - MIPI (Mantle cell lymphoma International Prognostic Index). Его модификациями являются упрощенный индекс (sMIPI) и комбинированный биологический индекс (MIPIb), учитывающий количество клеток экспрессирующих Ki-67. [26]
![]() Низкий риск по шкале MIPI - 5-летняя общая выживаемость (ОВ) составляет 60%.
Низкий риск по шкале MIPI - 5-летняя общая выживаемость (ОВ) составляет 60%.
![]() Промежуточный риск по шкале MIPI - медиана ОВ составляет 51 месяц.
Промежуточный риск по шкале MIPI - медиана ОВ составляет 51 месяц.
![]() Высокий риск по шкале MIPI - медиана ОВ составляет 29 месяцев.
Высокий риск по шкале MIPI - медиана ОВ составляет 29 месяцев.
Расчет упрощенного варианта международного прогностического индекса лимфомы из клеток мантии sMIPI.
Баллы Возраст ECOG ЛДГ/ВН ЛДГ Лейкоциты 109/л
0 < 50 0 - 1 < 0,67 < 6,700
1 50 - 59 - 0,67 - 0,99 6,700 - 9,999
2 60 - 69 2 - 4 1,000 - 1,49 10,000 - 14,999
3 >= 70 - >= 1,5000 >= 15,000
Каждый прогностический фактор оценивается от 0 до 3 баллов, которые потом суммируются (максимально 11 баллов). Пациенты, набравшие от 0 до 3 баллов, относятся в группу низкого риска; 4 - 5 баллов - в группу промежуточного риска; 6 - 11 баллов - в группу высокого риска. При статусе по шкале ECOG >= 2 больному присваивается 2 балла. Влияние концентрации ЛДГ оценивалось путем деления концентрации ЛДГ сыворотки больного на значение верхней нормы лаборатории (например, у больного концентрация ЛДГ на момент установления диагноза 390 Е/л, а лабораторные нормы составляют 250 - 480 Е/л; тогда проводится деление 390 / 480 = 0,81, что соответствует 1 баллу).
Расчет комбинированного биологического варианта международного прогностического индекса лимфомы из клеток мантии MIPIb: [48]
MIPIb = 0,03535 x возраст (годы)
+ 0,6978 (если ECOG > 1)
+ 1,367 x log 10 (ЛДГ/ВГН ЛДГ)
+ 0,9393 x log 10 (число лейкоцитов)
+ 0,02142 x Ki-67 (%)
Группы риска при расчете MIPIb:
1. Низкий: MIPIb < 5,7
2. Промежуточный: 5,7 < MIPIb < 6,5
3. Высокий: MIPIb > 6,5
Применение индекса MIPIb позволяет избежать случаи включения молодых больных с бластоидным вариантом заболевания в группу низкого риска. Для расчета MIPI и MIPIb возможно использование одного из специализированных медицинских калькуляторов, например QxMD Calculate (http://www.qxmd.com (http://www.qxmd.com)).
Другими, наиболее часто выделяемыми факторами неблагоприятного прогноза являются бластоидный вариант заболевания и высокий (Ki-67 > 30%) пролиферативный индекс, а также высокий уровень ![]() микроглобулина.
микроглобулина.
3. Лечение
Особенностью заболевания является рецидивирующее течение, несмотря на различные режимы терапии. Применение (R) CHOP-подобных курсов эффективно только в достижении общего ответа (ОО): полные ремиссии (ПР) достигаются в трети случаев, а медиана бессобытийной выживаемости (БСВ) составляет 16 - 20 месяцев. [6]
Основными тенденциями в терапии ЛКМ за последнее десятилетие являются:
1. интенсификация индукционной терапии высокими дозами цитарабина** (3 - 4 курса по 12 г/м2/курс) для пациентов моложе 60 лет; [7]
2. широкое распространении аутоТГСК в качестве консолидации первой ремиссии у пациентов моложе 60 - 65 лет; [12, 14, 16]
3. применение комбинаций средних доз цитарабина** с бендамустином**, платиносодержащими препаратами, бортезомибом**; [17]
4. постепенное исключение из протоколов интенсивной терапии высоких доз метотрексата**, в первую очередь из-за отсутствия убедительных данных о его эффективности и высокой токсичности у пациентов старшей возрастной группы; [46]
5. добавление бортезомиба** к CHOP-подобным режимам для пациентов старше 60 - 65 лет; [29]
6. использование поддерживающей терапии, в первую очередь моноклональными антителами, после среднедозной индукционной терапии (R-CHOP/R-B); [28, 54]
7. внедрение ингибиторов тирозинкиназы Брутона и иммуномодуляторов в клиническую практику. [55]
Основываясь на результатах различных исследований использование терапевтических моноклональных антител, высокодозной индукционной терапии и аутологичной трансплантации стволовых кроветворных клеток (аутоТГСК) превратились в наиболее эффективный способ достижения полных ремиссий, длительной бессобытийной и общей выживаемости у больных моложе 65 лет. [12, 14, 16]
Введение высоких доз цитарабина в схемы индукционной терапии позволяет достигать ОО в 90 - 95%, а ПР не менее чем в половине случаев. Целью высокодозной консолидации с поддержкой аутоТСКК является достижение молекулярной ремиссии, что коррелирует с более длительной безрецидивной выживаемостью (БРВ). Плато на кривой БСВ не регистрируется, но около половины больных после высокодозной терапии переживают 10-летний рубеж. [46]
Использование высоких доз цитарабина** и метотрексата** сопряжено с развитием гематологической токсичности IV степени, высоким риском тяжелых инфекционных осложнений и острой почечной недостаточности. Медиана возраста больных ЛКМ, которым предполагается проведение интенсивной индукционной полихимиотерапии (ПХТ), колеблется от 50 до 60 лет, что приводит к невыполнению высокодозной ПХТ в полном объеме у 30 - 50% больных. В результате редукции объема терапии у меньшего числа больных достигаются ПР, укорачивается БСВ и ОВ.
Снижение дозы цитарабина** в индукционной ПХТ с 12 до 4 г/м2 ведет к уменьшению сроков медианы БСВ с 5 до 3 лет, хотя ПР достигаются в 89 и 84% случаев, соответственно. Это подталкивает на поиск оптимальной по переносимости и эффективности индукционной ПХТ у больных с сопутствующей патологией в возрасте 55 - 65 лет. Альтернативой высоким дозам цитарабина** и метотрексата** могут быть курсы ПХТ, включающие средние дозы цитарабина** с цисплатином** (R-DHAP), бендамустином (R-BAC) и/или бортезомибом (R-HAD+B); различные комбинации гемцитабина** и оксалиплатина**. Их высокая эффективность продемонстрирована не только в терапии рецидивов и резистентных форм, но и у первичных больных. [54]
Медиана возраста больных ЛКМ колеблется около 65 лет, что ограничивает проведение интенсивной терапии не менее чем в половине случаев. Постоянный поиск новых схем иммунополихимиотерапии не позволяет выделить "золотой" стандарт, однако любая интенсификация сопряжена с токсичностью. Например, добавление средних доз цитарабина к схеме ритуксимаб-бендамустин (R-BAC) позволяет значительно улучшить результаты индукционной терапии, но только у соматически сохранных больных в возрасте до 75 лет. При невозможности применения среднедозных режимов терапии (R-CHOP или R-B) у пациентов с неудовлетворительным соматическим статусом возможно использование кладрибина с ритуксимабом или метрономной терапии, такой как R-PEPC. В ряде случаев возможно использование лучевой терапии, особенно при I - II стадиях заболевания. Неудовлетворительные результаты среднедозной терапии подталкивают к активному внедрению в клиническую практику новых таргетных препаратов, таких как ингибиторы тирозинкинзы Брутона (ибрутиниб) и ингибиторы PI3K, механизм действия которых направлен на блокирование передачи сигнала от B-клеточного рецептора к ядру клетки. [65]
Высокая токсичность флударабина**, связанная в первую очередь с развитием гипоплазии и аплазии костномозгового кроветворения, привела к исключению данного препарата из терапии первой линии как у молодых пациентов, так и у больных старшей возрастной группы.
Важной особенностью терапии ЛКМ является медленное достижение ответа и, как следствие, необходимость в проведении от 6 до 8 курсов индукционной терапии. Таким образом, выбор терапии, в первую очередь, зависит от возраста больного и его соматического статуса.
3.1 Локальные (I - II) стадии
С появлением высокочувствительных методов диагностики I - II стадия у пациентов с ЛКМ устанавливается исключительно редко (в 1 - 3% случаев). Стандартная терапия не разработана. В ретроспективных исследованиях показано преимущество комбинированного химиолучевого лечения над химиотерапией, ремиссии достигаются у 95% больных. Медианы ОВ и выживаемости без прогрессирования составили 6,4 и 3,2 года, соответственно.
- Рекомендуется в качестве варианта терапии может явиться применение 4 - 6 курсов ПХТ по схеме R-CHOP и локальной лучевой терапии в СОД 30 Гр при достижении полной ремиссии или СОД 36 - 40 Гр при частичном ответе.
Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1++).
- Рекомендуется у пациентов моложе 60 лет при вовлечении более одного лимфатического узла/локуса целесообразно проводить интенсивную индукционную терапию. При определении стадии заболевания обязательно исключение вовлечения ЖКТ и костного мозга, желательно выполнение ПЭТ.
Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1++).
- Рекомендуется у пациентов с бессимптомным индолентным течением ЛКМ возможно использование тактики "watch and wait" - "наблюдай и жди".
Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1++).
3.2 Больные моложе 60 - 65 лет с сохранным соматическим статусом, являющиеся кандидатами для проведения высокодозной терапии и аутоТСКК.
3.2.1 Первая линия терапии.
Целью терапии является достижение полной ремиссии, в т.ч. молекулярной, что соотносится с длительными БСВ и ОВ.
- Рекомендуется проведение индукционной терапии с использованием высоких доз цитарабина.
Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1++).
Комментарии: Принимая во внимание медиану возраста больных старше 50 лет, необходимость в проведении 6 - 8 циклов терапии длительностью 21 - 28 дней, высокодозные режимы чередуются (альтернируются) с CHOP-подобными схемами: R-HyperCVAD/R-HMA, R-MaxiCHOP/R-HD-AraC, R-CHOP/R-DHAP. Однако, принимая во внимание отсутствие значимой эффективности курсов HyperCVAD и MaxiCHOP над курсом CHOP в терапии ЛКМ, а также превышающую токсичность над эффективностью метотрексата, схемой выбора в терапии молодых и соматически сохранных пациентов может служить R-CHOP/R-HAD (6 - 8 курсов, в зависимости от времени достижения ремиссии). [38, 43]
При высоком риске развития синдрома лизиса опухоли, особенно при гиперлейкоцитозе более 50,0 x 109/л, возможно исключение из первого курса терапии ритуксимаба или проведение предфазы циклофосфамидом** и дексаметазоном**. Ряд европейских исследователей придерживаются схем индукционной терапии, включающих средние дозы цитарабина** в комбинации с цисплатином** (R-CHOP/R-DHAP). Однако снижение дозы в индукционной терапии нивелируются добавлением цитарабина** к тотальному облучению тела (ТОТ) во время предтранслплантационного кондиционирования. К настоящему времени большинство исследователей склоняется к исключению из схем ПХТ высокодозного метотрексата** из-за его высокой токсичности и отсутствия значимой эффективности.
- Рекомендуется при достижении ЧР или ПР выполняется сбор аутологичных стволовых кроветворных клеток с очисткой трансплантата in vivo от возможной контаминации CD20+ клетками ритуксимабом**. [46]
Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1++).
В качестве кондиционирования (высокодозной консолидации) при ЛКМ в используются ТОТ в дозе 12 - 14 Гр со снижением дозы над легкими до 8 Гр в комбинации с цитостатическими препаратами (циклофосфамид**, этопозид**, мелфалан**, цитарабин**) или высокодозные схемы ПХТ, например, BEAM. [21, 46, 61]
Рандомизированных исследований различных режимов кондиционирования не существует. При анализе регистра EBMT (Европейского общества трансплантации костного мозга) преимущество ТОТ продемонстрировано только у пациентов с частичной ремиссией заболевания. При достижении полной ремиссии лучшей эффективностью и безопасностью обладает кондиционирование по схеме BEAM +/- R. В реальной клинической практике в России тотальное облучение тела на сегодняшний день практически не используется. В связи с нерегулярностью поставок кармустина** в режиме кондиционирования возможно использование ломустина** или бендамустина** 140 - 200 мг/м2 однократно. [43]
Необходимость в применении поддерживающей терапии ритуксимабом** после выполнения интенсивной индукционной терапии и аутоТГСК на сегодняшний день не определена. [28] В рандомизированном исследовании Le Gouill с соавт. в группе больных, получавших поддерживающую терапию ритуксимабом** после аутоТГСК, отмечено статистически достоверное улучшение БСВ по сравнению с больными без поддерживающей терапии. Однако при анализе ОВ в обеих группах различий при медиане наблюдения 2 года не получено. Кроме того, длительное использование антиCD20 антител после интенсивной индукционной терапии приводит к необходимости массивной заместительной терапии иммуноглобулинами.
- Рекомендуется контрольные обследования в течение первого года после аутоТГСК выполняются каждые 3 месяца и включают КТ (при необходимости УЗИ), желателен контроль минимальной остаточной болезни в костном мозге.
Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1++).
Комментарии: молекулярный рецидив может быть купирован монотерапией ритуксимабом**. Эндоскопические методы исследования, особенно фиброколоноскопию, целесообразно выполнять у больных с вовлечением ЖКТ 1 раз в 6 месяцев. Большинство рецидивов возникают в течение первых трех лет после аутоТГСК. Динамическое наблюдение после аутоТГСК проводится не менее 5 лет с интервалом 3 - 6 месяцев.
Сочетание высокого риска, определяемого по шкале MIPIb, гиперлейкоцитоза более 40 - 50 x 109/л и бластоидного варианта является фактором крайне неблагоприятного прогноза, даже при выполнении интенсивной индукционной терапии и аутоТГСК. Это делает возможным рассмотрения вопроса о выполнении трансплантации аллогенного костного мозга в первой ремиссии болезни ("тандемная" трансплантация). [61]
- Рекомендуется выполнять люмбальную пункцию у больных с бластоидным вариантом заболевания и наличием опухолевого гиперлейкоцитоза.
Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1++).
Комментарии: Четких рекомендаций по профилактике нейролейкемии нет
3.2.2. Терапия рецидивов.
Противорецидивная терапия определяется схемой индукционной терапии и продолжительностью ремиссии.
- Рекомендуется: при использовании в качестве первой линии терапии только CHOP-подобных или флударабин** содержащих схем возможно применение высоких/средних доз цитарабин** a (R-HAD +/- бортезомиб, доза цитарабина** -2 г/м2, 2 - 4 введения каждые 12 часов) или платиносодержащих курсов терапии (R-DHAP, R-GemOx +/- ифосфамид** и дексаметазон**), различных комбинаций бендамутстина** с цитарабином** и/или бортезомибом. Учитывая химиорезистентность, возможно включение новых таргетных препаратов. В клинических исследованиях показана эффективность ибрутиниба - использование этого препарата как в монорежиме, так и в различных комбинациях включено в американские, европейские и российские рекомендации. [32, 42, 45]
Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1++).
Комментарии: среди нецитостатических препаратов наибольшей эффективностью обладает ибрутиниб. Назначение ибрутиниба возможно у пожилых и соматически ослабленных больных уже в первом рецидиве при невозможности проведения адекватной ПХТ. При развитии раннего рецидива также целесообразно рассмотреть возможность назначения ибрутиниба.
- Рекомендуется аутоТГСК может рассматриваться в качестве консолидации второй линии терапии при химиочувствительном рецидиве после длительной (более 3 - 5 лет) ремиссии у пациентов моложе 65 лет, ранее не получавших высокодозную терапию.
Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1++).
- Рекомендуется при развитии рецидива после интенсивной индукционной терапии включающей высокодозный цитарабин и аутоТГСК возможно применение платиносодержащих режимов и бендамустина** (в т.ч. с повторным использованием цитарабина** - схема R-BAC).
Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1++).
- Рекомендуется у больных моложе 50 - 55 лет рассмотрение вопроса о выполнении аллоТКМ с немиелоаблативным режимом кондиционирования.
Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1++).
Комментарии: аллоТКМ является единственным методом, позволяющим вылечить больного ЛКМ. Возможность ее проведения определяется химиочувствительностью опухоли, возрастом и коморбидностью пациента, а также наличием донора. Длительная ОВ после аллоТКМ достигает 40 - 50%. Ранние рецидивы после интенсивной индукционной терапии и аутоТгсК фактически некурабельны. Выполнение аллоТКМ в этой группе больных не позволяет достигнуть ремиссии, в первую очередь, из-за отсутствия достаточного времени для развития реакции трансплантат против опухоли. Возможно эффект будет достигнут после включения в схемы противорецидивной терапии новых препаратов, например, ибрутиниба.
3.3. Распространенные стадии у больных старше 60 - 65 лет и пациентов, не являющихся кандидатами для проведения интенсивной терапии.
3.3.1. Первая линия терапии.
Целью терапии в этой группе является достижение ремиссии и ее поддержание нехимиотерапевтическими агентами. Выбор тактики, в первую очередь, определяется соматическим статусом пациента, наличием сопутствующей патологии и признаков почечной недостаточности. Проводится 6 - 8 курсов индукционной ПХТ с последующей поддержкой ритуксимабом**. В ряде случаев, у соматически сохранных больных в возрасте до 70 лет возможно выполнение аутоТГСК (режим кондиционирования BEAM-R). [29]
- Рекомендуется: в настоящее время базовыми режимами терапии соматически сохранных больных старше 65 лет являются комбинации R - B** и R-CHOP. [47]
Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1++).
Комментарии: в проспективном рандомизированном исследовании эффективность режима R-B оказалась выше R-CHOP при более благоприятном профиле токсичности - медиана беспрогрессивной выживаемости составила 35,4 месяцев против 22,1 месяцев, соответственно. Однако при более длительном наблюдении эффективность обоих режимов оказалась схожей. Применение флударабина** в первой линии терапии нецелесообразно из-за высокой токсичности. К более интенсивным вариантам индукции можно отнести схему R-BAC (ритуксимаб** 375 мг/м2 в 0 или 1 дни, бендамустин** 70 мг/м2 в 1 - 2 дни и цитарабин** 500 мг/м2 в 1 - 3 дни 1 р/д). Применение более интенсивных режимов терапии сопряжено с высокой токсичностью и невыполнимостью плана терапии, что негативно сказывается на возможности достижения ЧР и ПР. Другим, довольно интенсивно применяемым в Европе режимом терапии является комбинация RiBVD - ритуксимаб** 375 мг/м2 в 1 день, бендамустин** 90 мг/м2 в 1 - 2 дни, бортезомиб** 1,3 мг/м2 в 1, 4, 8 и 11 дни и дексаметазон** 40 мг во 2 день однократно, шесть 28-дневных циклов. Частота достижения полных ремиссий составляет 75%, а беспрогрессивная выживаемость достигает 70% в течение 2 лет. Менее интенсивные схемы для больных с наличием тяжелой сопутствующей патологии: R-CVP, комбинации аналогов пуринов (кладрибин**) с ритуксимабом** и алкилирующими препаратами, метрономная терапия R-PEPC. Возможно участие в клинических исследованиях первой линии терапии, т.к. применение новых малотоксичных таргетных препаратов позволит, по всей видимости, увеличить общую выживаемость в этой группе больных.
- Рекомендуется: поддерживающая терапия ритуксимабом достоверно увеличивает безрецидивную выживаемость пожилых пациентов ЛКМ, достигших ремиссию после среднедозной индукционной терапии. Проводится каждые 2 месяца в дозе 375 мг/м2 в течение 2 лет или до прогрессирования болезни. Профилактика нейролейкемии проводится пациентам с бластоидным вариантом заболевания, гиперлейкоцитозом и при наличии симптомов вовлечения ЦНС.
Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1++).
3.3.2. Терапия рецидивов.
- Рекомендуется: применение средних доз цитарабина (R-HAD +/- B), платиносодержащих курсов (R-DHAP(Ox), R-GIDOX) различных комбинаций бендамутстина с цитарабином и/или бортезомибом**, кладрибином** после использования в первой линии терапии CHOP-подобных или флударабин** содержащих схем. [50, 61]
Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1++).
- Рекомендуется: у пациентов с наличием сопутствующей патологии или при втором рецидиве возможно применение таких схем как R-бортезомиб, R-PEPC, ибрутиниб +/- ритуксимаб**.
Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1++).
Комментарии: использование ибрутиниба целесообразно начинать на более ранних этапах противорецидивной терапии. При их неэффективности во втором рецидиве выполняются альтернативные противорецидивные схемы лечения или рассматривается возможность участия в клинических исследованиях. [55, 62, 67, 65, 64]
Терапия больных с ЛКМ в зависимости от возраста и соматического статуса
< 60 - 65 лет, кандидаты для ВДХТ и аутоТСКК
> 60 - 65 лет, не кандидаты для ВДХТ и аутоТСКК
1 линия терапии
1. Интенсивная индукция:
R-(Maxi) CHOP/R-HD-AraC
R-HyperCVAD/R-HMA
R-CHOP/R-DHAP
1. Консолидация: аутоТГСК (BEAM-R, ТОТ + ПХТ)
1. +/- R-поддержка 375 мг/м2 1 раз в 2 - 3 месяца 2 - 3 года (всего 12 введений)
1. Среднедозная индукция:
R-BAC, R-B
R-CHOP, R-CVP
R-VcrCAP
Кладрибин+R или R-PEPC при тяжелом соматическим статусе
Клинические исследования
1. R-поддержка 375 мг/м2 1 раз в 2 - 3 месяца 2 - 3 года (всего 1<...> введений)
Рецидив/прогрессия
1. R-DHAP(Ox), R-GIDOX
R-BAC
R-HAD +/- B (AraC 1 - 2 г/м2 x 4 +/- бортезомиб)
Ибрутиниб
АллоТКМ (при достижении ответа)
АутоТГСК (при отсутствии на более раннем этапе и достижении ответа)
R-B (после R-CHOP)
Бортезомиб (лучше в комбинации)
Клинические исследования R-FC(M), R-PEPC
Лучевая терапия (особенно при локальном рецидиве)
R-HAD +/- B (AraC 1 г/м2 x 4 <...> бортезомиб)
R-DHAP(Ox), R-GIDOX
R-B, R-BAC (после CHOP)
Ибрутиниб
Бортезомиб +/- ритуксимаб R-FC(M)
R-PEPC
Клинические исследования
Лучевая терапия (особенно при локальном рецидиве)
4. Реабилитация
Специальных методов реабилитации при ЛМЗ не существует. Реабилитация при возникновении осложнений в течение заболевания и лечения проводится в рамках соответствующих нозологий. Рекомендуется вести здоровый образ жизни, исключить избыточную инсоляцию и тепловые физиопроцедуры.
5. Профилактика
- Рекомендуется: соблюдать предписания гематолога по лечению и не заниматься самолечением, избегать провоцирующих заболевание факторов, изменить виды и условия труда на невредные и облегченные, ограничить инсоляции и физиотерапевтические методы лечения, планировать беременность.
Уровень убедительности рекомендаций D (уровень достоверности доказательств - 4).
Комментарии: Методов профилактики ЛМЗ в настоящее время не существует, поскольку неизвестен этиологический факторы, ведущие к развитию заболевания. Диспансерное наблюдение гематологом или онкологом осуществляется в период лечения и после достижения ремиссии лимфомы.
6. Дополнительная информация, влияющая на течение и исход заболевания
6.1 Ошибки и необоснованные назначения
- Не рекомендуется выполнение пункции лимфоузла (очага поражения)
Уровень убедительности рекомендаций D (уровень достоверности доказательств - 4).
Комментарии: диагноз лимфомы не может быть установлен по пунктату, без полноценного гистологического и гистохимического исследования
6.2 Лимфомы и беременность
- Рекомендуется со всеми больными детородного возраста обоих полов обсуждать вопрос о возможности криоконсервации спермы или ткани яичника перед началом терапии.
Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1++).
Комментарии: химиотерапия и облучение области таза могут привести к необратимой стерильности пациента
- Рекомендуется с женщинами детородного возраста обсуждать вопрос о необходимости гормональной защиты от беременности, а также о методах возможной гормональной защиты яичников при проведении интенсивных программ лечения.
Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1++).
6.3 Прогноз
Прогноз определяется в соответствии со шкалой MIPI. Прогноз также напрямую зависит от полноценной и своевременной диагностики, и применения адекватной тактики лечения.
Критерии оценки качества медицинской помощи
N
Критерии качества
Оценка выполнения
Уровень достоверности доказательств
Уровень убедительности рекомендаций
1
Выполнена биопсия лимфоузла (очага поражения) с цитологическим, морфологическим, иммуногистохимическим исследованиями
Да/Нет
1+
A
2
Выполнен клинический анализ крови (гемоглобин, эритроциты, тромбоциты, лейкоциты, лейкоцитарная формула)
Да/Нет
1+
A
3
Выполнен Биохимический анализ крови (общий белок, альбумин, мочевина, креатинин, мочевая кислота, АЛТ, АСТ, общий и прямой билирубин, холестерин, ЛДГ, щелочная фосфатаза, электролиты, кальций)
Да/Нет
1+
A
4
Выполнено КТ/УЗИ/МРТ грудной полости, брюшной полости, малого таза, дополнительных очагов поражения
Да/Нет
2
A
2
Выполнена трепанобиопсия с гистологическим исследованием костного мозга
Да/Нет
1+
A
6
Выполнено ЭКГ
Да/Нет
2
B
Выполнена Коагулограмма
Да/Нет
2
B
Список литературы
1. Swerdlow S.H., Campo E., Harris N.L., et al., editors. WHO classification of tumours of haematopoietic and lymphoid tissues. IARC: Lyon 2008.
2. Carbone PP, Kaplan HS, Musshoff K, et al. Report of the committee on Hodgkin's disease staging classification. Cancer Res 1971; 31: 1860 - 1861.
3. Воробьев В.И., Кравченко С.К., Гемджян Э.Г. и др. Программное лечение первичных больных мантийноклеточной лимфомой в возрасте до 65 лет. Клиническая онкогематология. 2013. Том 6, N 3. С. 274 - 281.
4. Воробьев В.И., Лорие Ю.Ю., Мангасарова Я.К., Кравченко С.К., Кременецкая А.М. Возможности терапии рецидивов и резистентного течения лимфомы из клеток мантийной зоны. Гематология и трансфузиология. 2011. N 1: 34 - 37.
5. Поддубная И.В. Терапевтические проблемы при лимфоме зоны мантии. Современная онкология. 2010; 2: 48 - 53
6. Argatoff LH, Connors JM, Klasa RJ, et al. Mantle cell lymphoma: a clinicopathologic study of 80 cases. Blood. 1997; 89: 2067 - 78.
7. Bernstein SH, Epner E, Unger JM, et al. A phase II multicenter trial of HyperCVAD MTX/Ara-C and rituximab in patients with previously untreated mantle cell lymphoma; SWOG 0213. Ann Oncol. 2013; 24(6): 1587 - 93
8. Codet R, Mrhalova M, Krskova L, et al. Mantle cell lymphoma: improved diagnostics using a combined approach of immunohistochemistry and identification of t(11; 14)(q13: q32) by polymerase chain reaction and fluorescence in situ hybridization. Virchows Arch. 2003; 442: 538 - 47.
9. Coleman M, Martin P, Ruan J, et al. Prednisone, etoposide, procarbazine, and cyclophosphamide (PEP-C) oral combination chemotherapy regimen for recurring/refractory lymphoma: low-dose metronomic, multidrug therapy. Cancer. 2008; 112: 2228 - 2232.
10. Corazzelli G, Capobianco G, Arcamone M, et al. Long-term results of gemcitabine plus oxaliplatin with and without rituximab as salvage treatment for transplant-ineligible patients with refractory/relapsing B-cell lymphoma. Cancer Chemother Pharmacol. 2009; 64: 907 - 16.
11. Corazzelli G, Russo F, Capobianco G, et al. Gemcitabine, ifosfamide, oxaliplatin and rituximab (R-GIFOX), a new effective cytoreductive/mobilizing salvage regimen for relapsed and refractory aggressive non-Hodgkin"s lymphoma: results of a pilot study. Ann Oncol. 2006; 17 (Suppl 4): iv18 - 24.
12. Damon LE, Johnson JL, Niedzwiecki D, et al. Immunochemotherapy and autologous stem-cell transplantation for untreated patients with mantle-cell lymphoma: CALGB 59909. J Clin Oncol. 2009; 27(36): 6101 - 08.
13. Dietrich S, Tielesch B, Rieger M, et al. Patterns and Outcome of Relapse After Autologous Stem Cell Transplantation for Mantle Cell Lymphoma. Cancer. 2010; 117(9): 1901 - 10
14. Dreyling MH, Hoster E, Van Hoof A, et al. Early Consolidation with Myeloablative Radio chemotherapy Followed by Autologous Stem Cell Transplantation in First Remission in Mantle Cell Lymphoma: Long Term Follow up of a Randomized Trial of the European MCL Network. Blood. 2008; 112: 769
15. Dreyling M, Kluin-Nelemans HC, Bea S, et al. Update on the Molecular Pathogenesis and Clinical Treatment of Mantle Cell Lymphoma: Report of the 11th Annual Conference of the European Mantle Cell Lymphoma Network. Leuk Lymphoma. 2013; 54(4): 699 - 707
16. Fenske TS, Carreras J, Zhang M, et al. Outcome of patients with mantle-cell lymphoma undergoing autologous versus reduced-intensity allogenic transplantation. Ann Oncol. 2011; 22 (Suppl. 4) Abstract 018
17. Friedberg JW, Vose JM, Kelly JL, et al. The Combination of bendamustine, bortezomib, and rituximab for patients with relapsed/refractory indolent and mantle cell non-Hodgkin lymphoma. Blood. 2011; 117(10): 2807 - 12
18. Fu K, Weisenburger DD, Greiner TC, et al. Cyclin D1-negative mantle cell lymphoma: a clinicopathologic study based on gene expression profiling. Blood. 2005; 106: 4315 - 21
19. Furtado M, Rule S. Indolent mantle cell lymphoma. Haematologica. 2011; 96(8): 1086 - 8
20. Geisler C. Front-line therapy of MCL. Hematologica. 2010; 95: 1241 - 43
21. Geisler CH, Kolstad A, Laurell A, et al. Nordic MCL2 trial update: six-year follow-up after intensive immunochemotherapy for untreated mantle cell lymphoma followed by BEAM or BEAC + autologous stem-cell support: still very long survival but late relapses do occur. Br J Haematol. 2012; 158(3): 355 - 62
22. Gill S, Herbert KE, Prince HM, et al. Mantle cell lymphoma with central nervous system involvement: frequency and clinical features. Br J Haematol. 2009; 147: 83 - 88
23. Gill S, Wolf M, Prince H, et al. [18F]fluorodeoxyglucose positron emission tomography scanning for staging, response assessment and disease surveillance in patients with mantle cell lymphoma. Clin Lymphoma Myeloma. 2008; 8(3): 159 - 65
24. Gironella M, L-pez A, Pau A, et al. Rituximab plus gemcitabine and oxaliplatin as salvage therapy in patients with relapsed/refractory mantle-cell lymphoma ASH 54th Annual Meeting. 2012. Vol.: 120, Issue 21. Abstract # 2825.
25. Hermine O, Hoster E, Walewski J, et al. Alternating courses of 3x CHOP and 3x DHAP Plus rituximab followed by a high dose ARA-C containing myeloablative regimen and autologous stem cell transplantation (ASCT) increases overall survival when compared to 6 courses of CHOP plus rituximab followed by myeloablative radiochemotherapy and ASCT in mantle cell lymphoma: final analysis of the MCL Younger Trial of the European Mantle Cell Lymphoma Network (MCL net). Blood (ASH Annual Meeting Abstracts). 2012; 120(21): Abstract 151
26. Hoster E, Dreyling M, Klapper W, et al. A new prognostic index (MIPI) for patients with advanced-stage mantle cell lymphoma. Blood. 2008; 111: 558 - 65
27. Hoster E, et al. A new prognostic index (MIPI) for patients with advanced mantle cell lymphoma. Blood. 2008; 111: 558 - 65.
28. Howard OM, Gribben JG, Neuberg DS, et al. Rituximab and CHOP induction therapy for newly diagnosed mantle cell lymphoma: molecular complete responses are not predictive of progression-free survival. J Clin Oncol. 2002; 20: 1288 - 94
29. Kahl BS, Long WL, Eickhoff JC, et al. Maintenance rituximab following induction chemoimmunotherapy may prolong progression-free survival in mantle cell lymphoma: A pilot study from the Wisconsin Oncology Network. Ann Oncol. 2006; 17: 1418 - 1423
30. Kluin-Nelemans JC, Hoster E, Hermine O, et al. Treatment of older patients with mantle-cell lymphoma. N Engl J Med. 2012; 367(6): 520 - 31
31. Komatsu H, Iida S, Yamamoto K, et al. A variant chromosome translocation at 11q13 identifying PRADl/Cyclin D1 as the BCL-1 gene. Blood. 1994; 84: 1226 - 31
32. LaCasce AS, Vandergrift JL, Rodriguez MA, et al. Comparative outcome of initial therapy for younger patients with mantle cell lymphoma: an analysis from the NCCN NHL Database. Blood. 2012; 119(9): 2093 - 9
33. Le Gouill S,  N, Dhedin N, et al. Reduced-intensity conditioning allogeneic stem cell transplantation for relapsed/refractory mantle cell lymphoma: a multicenter experience. Ann Oncol. 2012; 23(10): 2695 - 2703
N, Dhedin N, et al. Reduced-intensity conditioning allogeneic stem cell transplantation for relapsed/refractory mantle cell lymphoma: a multicenter experience. Ann Oncol. 2012; 23(10): 2695 - 2703
34. Leitch HA, Gascoyne RD, Chhanabhai M, et al. Limited stage mantle cell lymphoma: Clinical outcome in patients from British Columbia. Ann Oncol. 2003; 14(10): 1555 - 61
35. Lenz G, Dreyling M, Hoster E, et al. Immunochemotherapy with rituximab and cyclophosphamide, doxorubicin, vincristine, and prednisone significantly improves response and time to treatment failure, but not long-term outcome in patients with previously untreated mantle cell lymphoma: results of a prospective randomized trial of the German Low Grade Lymphoma Study Group (GLSG). J Clin Oncol. 2005; 23: 1984 - 92
36. Liu Z, Dong HY, Gorczyca W, et al. CD5-mantle cell lymphoma. American Journal of Clinical Pathology. 2002; 118(2): 216 - 24
37. Martin P, Chadburn A, Christos P, et al. Outcome of deferred initial therapy in mantle-cell lymphoma. J Clin Oncol. 2009; 27(8): 1209 - 13
38. Mato AR, Svoboda J, Feldman T, et al. Post-treatment (not interim) positron emission tomography-computed tomography scan status is highly predictive of outcome in mantle cell lymphoma patients treated with R-HyperCVAD. Cancer. 2012; 118(14): 3565 - 70
39. Merli F, Luminari S, Ilariucci F, et al. Rituximab plus HyperCVAD alternating with high dose cytarabine and methotrexate for the initial treatment of patients with mantle cell lymphoma, a multicentre trial from Gruppo Italiano Studio Linfomi. Br J Haematol. 2012; 156(3): 346 - 53
40. Mozos A, Royo A, Hartmann E, et al. SOX11 expression is highly specific for mantle cell lymphoma and identifies the cyclinDl-negative subtype. Haematologica. 2009; 94(11): 1555 - 62
41. Ondrejka SL, Lai R, Kumar N, et al. Indolent mantle cell leukemia: clinicopathological variant characterized by isolated lymphocytosis, interstitial bone marrow involvement, к light chain restriction, and good prognosis. Haematologica. 2011; 96: 1221 - 27
42. Orchard J, Garand R, Davis Z, et al. A subset of t(11; 14) lymphoma with mantle cell features displays mutated IgVH genes and includes patients with good prognosis, nonnodal disease. Blood. 2003; 101(12): 4975 - 81
43. Park BB, Kim WS, Eom HS, et al. Salvage therapy with gemcitabine, ifosfamide, dexamethasone, and oxaliplatin (GIDOX) for B-cell non-Hodgkin"s lymphoma: a consortium for improving survival of lymphoma (CISL) trial. Invest New Drugs. 2011; 29: 154 - 60
44. Pott C, Hoster E, Beldjord K, et al. R-CHOP/R-DHAP compared to R-CHOP induction followed by high dose therapy with autologous stem cell transplantation induces higher rates of molecular remission in MCL: results of the MCL Younger Intergroup Trial of the European MCL Network. Blood. 2010 (ASH Annual Meeting Abstracts); 116: Abstract 965
45. Rodriguez J, Gutierrez A, Obrador-Hevia A, et al. Therapeutic concepts in mantle cell lymphoma. Eur J Haematol. 2010; 85(5): 371 - 86
46. Rodriguez J, Gutierrez A, Palacios A, et al. Rituximab, gemcitabine and oxaliplatin: An effective regimen in patients with refractory and relapsing mantle cell lymphoma. Leuk. Lymphoma. 2007; 48: 2172 - 78
47. Romaguera J, Fayad L, Feng L, et al. Ten-year follow-up after intense chemoimmunotherapy with rituximab-HyperCVAD alternating with rituximab-high dose methotrexate/cytarabine (R-MA) and without stem cell transplantation in patients with untreated aggressive mantle cell lymphoma. Br J Haematol. 2010; 150(2): 200 - 08
48. Rummel MJ, Niederle N, Maschmeyer G, et al. Bendamustine plus rituximab versus CHOP plus rituximab as first-line treatment for patients with indolent and mantle-cell lymphomas: an open-label, multicentre, randomised, Phase 3 non-inferiority Trial. Lancet. 2013; 381(9873): 1203 - 10
49. Schaffel R, Hedvat CV, Teruya-Feldstein J, et al. Prognostic impact of proliferative index determined by quantitative image analysis and the International Prognostic Index in patients with mantle cell lymphoma Annals of Oncology. 2010; 21: 133 - 39
50. Smithers DW. Summary of papers delivered at the Conference on Staging in Hodgkin"s Disease (Ann Arbor). Cancer Res. 1971; 31(11): 1869 - 70
51. Spurgeon SE, PindyckT, Okada C, et al. Cladribine plus rituximab is an effective therapy for newly diagnosed mantle cell lymphoma. Leuk Lymphoma. 2011; 52: 1488 - 1494
52. Sun T, Nordberg M, Cotelingam J, et al. Fluorescence in situ hybridization: method of choice for a definitive diagnosis of mantle cell lymphoma. Am J Hematol. 2003; 74(1): 78 - 84
53. Swerdlow S, Campo E, Harris NL, et al. WHO Classification of Tumours of Haematopoietic and Lymphoid Tissues (International Agency for Research on Cancer (IARC)) 4th ed., 2008.
54. Tam C, Bassett R, Ledesma C, et al. Mature results of the M. D. Anderson Cancer Center risk-adapted transplantation strategy in mantle cell lymphoma. Blood. 2009; 113(18): 4144 - 52
55. Tiemann M, Schrader C, Klapper W, et al. Histopathology, cell proliferation indices and clinical outcome in 304 patients with mantle cell lymphoma (MCL): a clinicopathological study from the European MCL Network. Br J Haematol. 2005; 131(1): 29 - 38
56. Visco C, Finotto S, Zambello R, et al. Combination of rituximab, bendamustine, and cytarabine for patients with mantle-cell non-Hodgkin lymphoma ineligible for intensive regimens or autologous transplantation. J Clin Oncol. 2013; 31(11): 1442 - 49
57. Wang M, Rule SA, Martin P, et al. Targeting BTK with ibrutinib in relapsed or refractory mantle-cell lymphoma. N Engl J Med. 2013; 369(6): 507 - 16
58. Wlodarska I, Meeus P, Stul M, et al. Variant t(2; 11)(p11; q13) associated with the IgK-CCND1 rearrangement is a recurrent translocation in leukemic small-cell B-non-Hodgkin lymphoma. Leukemia. 2004; 18: 1705 - 10
59. Yatabe Y, Suzuki R, Matsuno Y, et al. Morphological spectrum of cyclin D1-positive mantle cell lymphoma: Study of 168 cases. Pathology International. 2001; 51: 747 - 61
60. Yatabe Y, Suzuki R, Tobinai K, et al. Significance of cyclin D1 overexpression for the diagnosis of mantle cell lymphoma: a clinicopathologic comparison of cyclin D1-positive MCL and cyclin D1-negative MCL-like B-cell lymphoma. Blood. 2000; 95: 2253 - 61
61. Zhou Y, Wang H, Fang W, et al. Incidence Trends of Mantle Cell Lymphoma in the United States Between 1992 and 2004. Cancer. 2008; 113: 791 - 8.
62. Spurgeon SE, Pindyck T, Okada C, et al. Cladribine plus rituximab is an effective therapy for newly diagnosed mantle cell lymphoma. Leuk Lymphoma. 2011; 52: 1488 - 1494
63. Visani G, Malerba L, Stefani PM, et al. BeEAM (bendamustine, etoposide, cytarabine, melphalan) before autologous stem cell transplantation is safe and effective for resistant/relapsed lymphoma patients. Blood. 2011; 118: 3419 - 25
64. Ruan J, Martin P, Coleman M, et al. Durable Responses with the Metronomic Regimen RT-PEPC in Elderly Patients with Recurrent Mantle Cell Lymphoma. Cancer. 2010; 116(11): 2655 - 64.
65. Eskelund CW, Kolstad A, Jerkeman M, et al. 15-year follow-up of the Second Nordic Mantle Cell Lymphoma trial (MCL2): prolonged remissions without survival plateau. Br J Haematol. 2016 Jul 5. [Epub ahead of print].
66. Dreyling M, Jurczak W, Jerkeman M, et al. Ibrutinib versus temsirolimus in patients with relapsed or refractory mantle-cell lymphoma: an international, randomised, open-label, phase 3 study. Lancet. 2016; 387(10020): 770 - 8
67. Wang ML, Lee H, Chuang H, et al. Ibrutinib in combination with rituximab in relapsed or refractory mantle cell lymphoma: a single-centre, open-label, phase 2 trial. Lancet Oncol. 2016; 17(1): 48 - 56
68. Mato R, Svoboda J, Feldman T, et al. Post-Treatment (Not Interim) Positron Emission Tomography-Computed Tomography Scan Status Is Highly Predictive of Outcome in Mantle Cell Lymphoma Patients Treated With R-HyperCVAD. Cancer. Volume 118, Issue 14.
69. Wang ML, Blum KA, Martin P, et al. Long-term follow-up of MCL patients treated with single-agent ibrutinib: updated safety and efficacy results. Blood. 2015; 126: 739 - 45
70. Chihara D, Cheah CY, Westin JR, et al. Rituximab plus hyper-CVAD alternating with MTX/Ara-C in patients with newly diagnosed mantle cell lymphoma: 15-year follow-up of a phase II study from the MD Anderson Cancer Center. Br J Haematol. 2016; 172(1): 80 - 8
Приложение А1
СОСТАВ РАБОЧЕЙ ГРУППЫ
Коллектив авторов
Авторы клинических разделов:
Воробьев Владимир Иванович. Кандидат медицинских наук, врач-гематолог, заведующий блоком интенсивной терапии гематологического отделения ГБУЗ Городская клиническая больница им. С.П. Боткина" Департамента здравоохранения города Москвы
Тумян Гаяне Сергеевна. Доктор медицинских наук, врач-онколог, ведущий научный сотрудник отделения химиотерапии гемобластозов ФГБУ "РОНЦ им. Н.Н. Блохина", профессор кафедры онкологии Российской медицинской академии последипломного образования, Москва
Поддубная Ирина Владимировна. Член-корреспондент РАН, заслуженный деятель образования РФ, доктор медицинских наук, профессор, заведующая кафедрой онкологии, проректор по учебной работе и международному сотрудничеству ГБОУ ДПО "Российская медицинская академия последипломного образования" (РМАПО) МЗ РФ, г. Москва
Приложение А2
МЕТОДОЛОГИЯ РАЗРАБОТКИ КЛИНИЧЕСКИХ РЕКОМЕНДАЦИЙ
На протяжении многих лет врачи и организаторы здравоохранения всего мира стараются облегчить и оптимизировать свою работу посредством разработок рекомендаций по лечению отдельных заболеваний, которые составлены ведущими специалистами данной области медицины и учитывают, как все последние достижения медицинской науки, так и практические особенности здравоохранения данного региона. Подобные рекомендации создаются на различных уровнях, начиная от международных рекомендаций, написанных объединенными группами экспертов разных стран, заканчивая локальными, действующими в отдельных клиниках. Наличие подобных рекомендаций способствует облегчению выбора тактики лечения практическими врачами, обеспечивает их полной и современной информацией о преимуществах и ограничениях различных методов лечения, а также позволяет организаторам здравоохранения лучше оценивать возможные объемы необходимого лечения.
В 2007 г. была создана первая в России рабочая группа по написанию клинических рекомендаций по лечению больных хроническим лимфолейкозом. Впервые эти рекомендации были изданы в 2008 г., в 2010 - 2011 гг. они были модернизированы и переизданы. На этом этапе к работе над их написанием был приглашен международный эксперт, профессор M. Hallek (Германия).
Учитывая этот успешный опыт создания клинических рекомендаций, а также нарастающую потребность практикующих врачей в аналогичном документе, касающемся других нозологий, Российское профессиональное общество онкогематологов под руководством проф. И.В. Поддубной и Национальное гематологическое общество под руководством проф. В.Г. Савченко выступили с инициативой написания Российских клинических рекомендаций по диагностике и лечению злокачественных лимфопролиферативных заболеваний. Данное начинание было поддержано проф. F. Cavalli (Швейцария), который согласился стать третьим руководителем проекта.
Первая версия Российских клинических рекомендаций по диагностике и лечению лимфопролиферативных заболеваний была подготовлена в 2012 - 2013 гг., и в 2013 г. была опубликована в журнале "Современная онкология", а также на ряде профессиональных медицинских сайтов, в том числе на сайтах обоих обществ, и незамедлительно получила широкое распространение среди практических врачей-онкологов и гематологов страны.
Динамичное развитие современной онкогематологии требует от специалистов постоянного обновления своих знаний и внедрения новых методов диагностики и лечения в практику. В этой связи клинические рекомендации должны постоянно совершенствоваться, развиваться и обновляться в соответствии с научными открытиями и новыми требованиями специалистов, непосредственно занимающихся лечением больных. Учитывая эти требования, рабочая группа по подготовке рекомендаций приняла решение о регулярном обновлении данного документа 1 раз в 2 года.
Вторая версия Российских клинических рекомендаций по диагностике и лечению злокачественных лимфопролиферативных заболеваний была опубликована в 2014 г. Были добавлены последние данные о возможностях диагностики и лечения лимфом, хронического лимфолейкоза и множественной миеломы, а также добавлены новые разделы и приложения. Обсуждение обновлений состоялось в рамках II Конгресса гематологов России.
В данное издание вошла третья версия рекомендаций, подготовленная специалистами в 2015 - 2016 гг. Все основные разделы рекомендаций были обновлены с учетом последних научных достижений в данной области, а также пожеланий практических онкологов и гематологов, имевших возможность использовать первые издания рекомендаций начиная с 2013 г. В рекомендации добавлены новые классификации и прогностические системы, разработанные в последние годы, а также лекарственные препараты, зарегистрированные или планируемые к регистрации в Российской Федерации в 2015 - 2016 гг. Значительно расширен круг специалистов смежных областей, участвовавших в написании разделов рекомендаций по диагностике и лечению пациентов, у которых помимо лимфопролиферативной патологии диагностируются иные тяжелые заболевания, влияющие на терапевтическую тактику.
Обновления рекомендаций были широко и подробно обсуждены специалистами в рамках трех крупнейших мероприятий, проводимых в данной области: Форума экспертов по вопросам диагностики и лечения злокачественных лимфопролиферативных заболеваний "Лимфорум", ежегодной Российской конференции с международным участием "Злокачественные лимфомы", а также III Конгресса гематологов России.
Целевая аудитория данных клинических рекомендаций:
1. Гематология (31.08.29)
2. Онкология (31.08.57)
Методология сбора доказательств
Методы, использованные для сбора/селекции доказательств:
Поиск публикаций в специализированных периодических печатных изданиях с импакт-фактором > 0.3;
Поиск в электронных базах данных.
Базы данных, использованных для сбора/селекции доказательств:
Доказательной базой для рекомендаций являются публикации, вошедшие в Кохрайновскую библиотеку, базы данных PUBMED и MEDLINE. Глубина поиска составляла 30 лет.
Методы, использованные для анализа доказательств:
- Обзоры опубликованных мета-анализов;
- Систематические обзоры с таблицами доказательств.
Методы, использованные для качества и силы доказательств:
- Консенсус экспертов;
- Оценка значимости доказательств в соответствии с рейтинговой схемой доказательств (табл. 4, 5).
В настоящих клинических рекомендациях в квадратных скобках приведены уровни доказательности рекомендаций, в соответствии со шкалами, разработанными Американским обществом клинической онкологии (ASCO) и Европейским обществом медицинской онкологии (ESMO).
Таблица П1 - Рейтинговая схема для оценки уровня достоверности доказательств
Уровни достоверности доказательств
Описание
1++
Мета-анализы высокого качества, систематические обзоры рандомизированных контролируемых исследований (РКИ), или РКИ с очень низким риском систематических ошибок
1+
Качественно проведенные мета-анализы, систематические обзоры или РКИ
1-
Мета-анализы, систематические обзоры или РКИ с высоким риском систематических ошибок
2++
Высококачественные систематические обзоры исследований случай-контроль или когортных исследований с отсутствием или очень низким риском эффектов смешивания или систематических ошибок и высокой вероятностью причинной взаимосвязи
2+
Хорошо проведенные исследования случай-контроль или когортные исследования со средним риском эффектов смешивания или систематических ошибок и средней вероятностью причинной взаимосвязи
2-
Исследования случай-контроль или когортные исследования с высоким риском эффектов смешивания или систематических ошибок и средней вероятностью причинной взаимосвязи
3
Не аналитические исследования (описания случаев, серий случаев)
4
Мнение экспертов
Таблица П2 - Рейтинговая схема для оценки убедительности рекомендаций
Уровни убедительности рекомендаций
Описание
A
Рекомендации основаны:
по меньшей мере, на одном мета-анализе, систематическом обзоре или РКИ, оцененных как 1++, напрямую применимых к целевой популяции и демонстрирующих устойчивость результатов
или
группе доказательств, включающих результаты исследований, оцененных как 1+, напрямую применимых к целевой популяции и демонстрирующих общую устойчивость результатов
B
Рекомендации основаны:
на группе доказательств, включающих результаты исследований, оцененных как 2++, напрямую применимых к целевой популяции и демонстрирующих общую устойчивость результатов
или
экстраполированных доказательств из исследований, оцененных как 1++ или 1+
C
Рекомендации основаны:
на группе доказательств, включающих результаты исследований, оцененных как 2+, напрямую применимых к целевой популяции и демонстрирующих общую устойчивость результатов
или
экстраполированных доказательств из исследований, оцененных как 2++
D
Рекомендации основаны на доказательствах уровня 3 или 4
или
экстраполированных доказательств из исследовании, оцененных как 2+
Индикаторы доброкачественной клинической практики (Good Practice Points - GPPs):
Доброкачественная практика рекомендаций основывается на квалификации и клиническом опыте авторского коллектива.
Методология валидизации рекомендаций
Методы валидизации рекомендаций:
- Внешняя экспертная оценка;
- Внутренняя экспертная оценка.
Описание методики валидизации рекомендаций:
Настоящие рекомендации в предварительной версии были рецензированы независимыми экспертами, которых попросили прокомментировать, насколько качественно интерпретированы доказательства и разработаны рекомендации. Также была проведена экспертная оценка изложения рекомендаций и их доступности для понимания.
Рекомендации обсуждены и одобрены ведущими специалистами профильных Федеральных центров РФ и практическими врачами. Проект клинических рекомендаций был рассмотрен на совещаниях рабочей группы в 2015 - 2016 гг., на Форуме экспертов по вопросам диагностики и лечения злокачественных лимфопролиферативных заболеваний "Лимфорум", ежегодной Российской конференции с международным участием "Злокачественные лимфомы", а также III Конгресса гематологов России.
Окончательная редакция:
Для окончательной редакции и контроля качества рекомендации были повторно проанализированы членами авторского коллектива, которые пришли к заключению, что все существенные замечания и комментарии экспертов приняты во внимание, риск систематических ошибок при разработке сведен к минимуму.
Клинические рекомендации утверждены на XIII Российской конференции с международным участием "Злокачественные лимфомы" в 2016.
Приложение А3
СВЯЗАННЫЕ ДОКУМЕНТЫ
Рисунок N 1 Инициальная терапия больных с ЛКМ в зависимости от возраста и соматического статуса
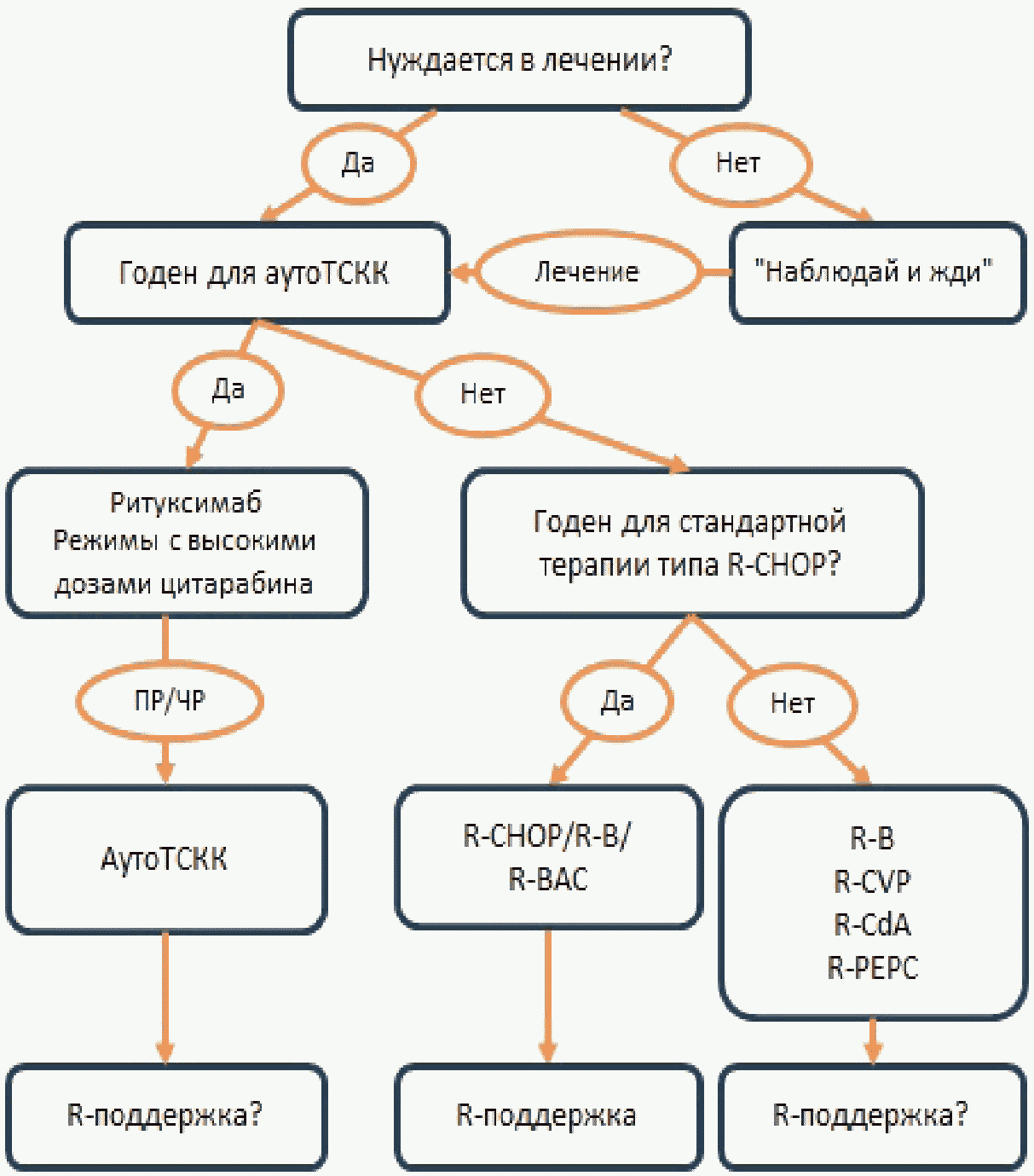
Рисунок N 2. Терапия больных с ЛКМ в рецидиве\резистентности в зависимости от возраста и соматического статуса
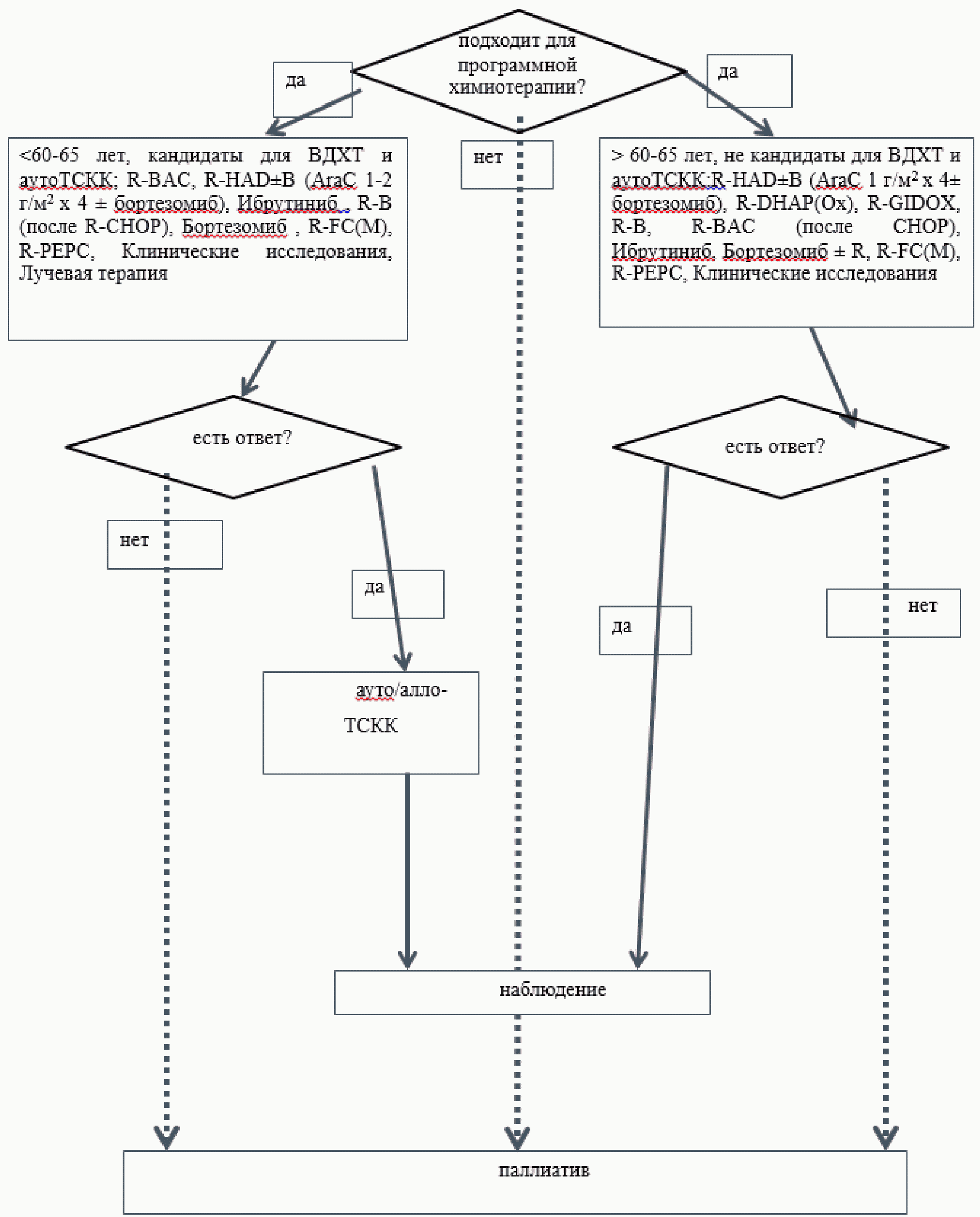
КР400. Хронический болевой синдром (ХБС) у взрослых пациентов, нуждающихся в паллиативной медицинской помощи (http://cr.rosminzdrav.ru/#!/schema/708)
Приложение Б
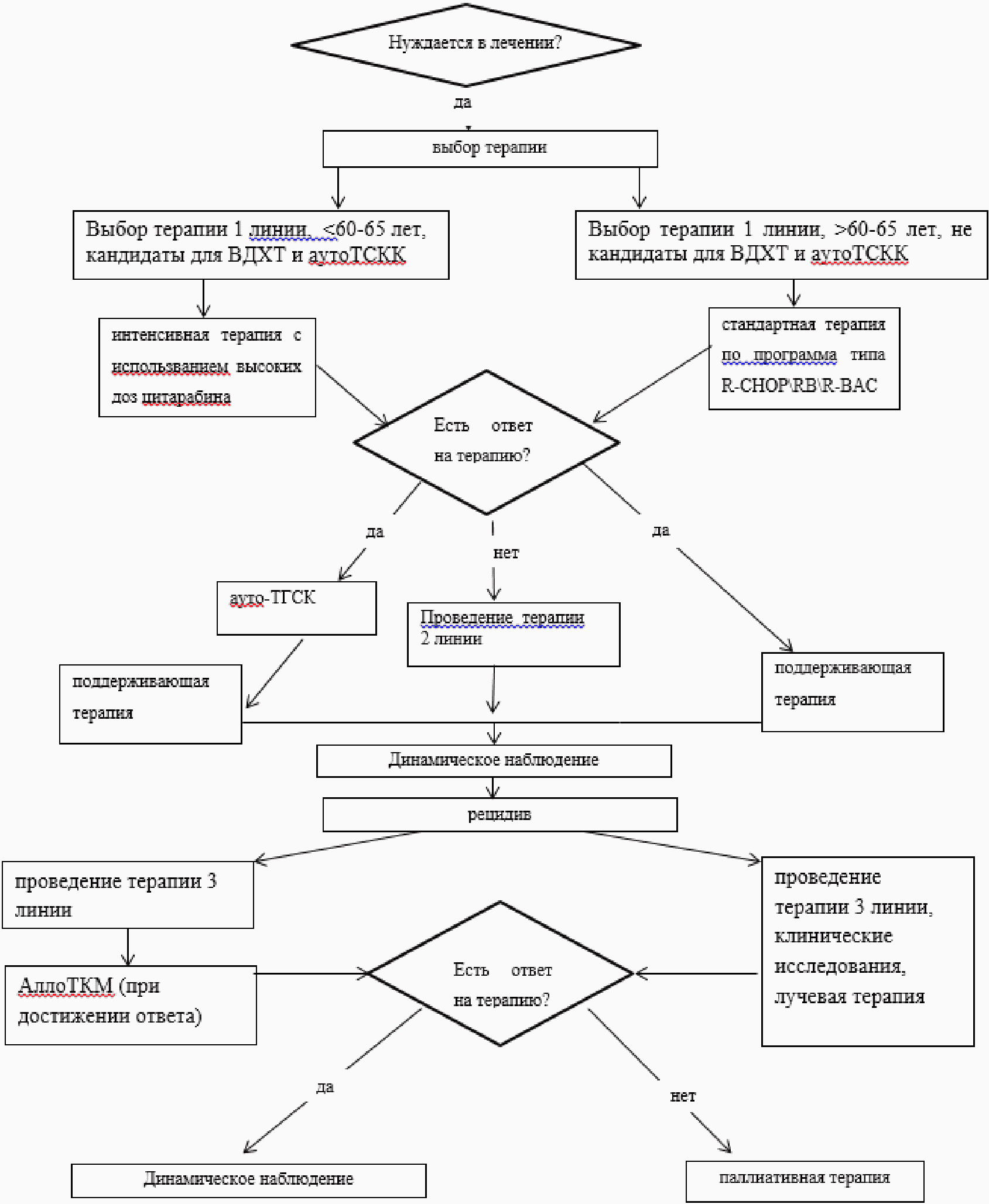
АЛГОРИТМЫ ВЕДЕНИЯ ПАЦИЕНТА
Приложение Б
АЛГОРИТМЫ ВЕДЕНИЯ ПАЦИЕНТА С ЛИМФОМОЙ ИЗ КЛЕТОК МАНТИИ
Приложение В
ИНФОРМАЦИЯ ДЛЯ ПАЦИЕНТОВ
Что такое лимфома из клеток мантийной зоны?
Это опухолевое заболевание лимфатической ткани. Клетки опухоли происходят из B-клеток, которые располагаются в мантийной зоне лимфатических узлов. Как правило, первым симптомом лимфомы является значительное увеличение размеров лимфатических узлов на шее, в подмышечных впадинах или в паху. При этом, в отличие от инфекционных заболеваний, увеличенные лимфатические узлы безболезненны, их размеры не уменьшаются со временем и при лечении антибиотиками. Иногда, вследствие давления со стороны увеличенных печени, селезенки и лимфатических узлов, возникает чувство переполнения в животе, затруднения дыхания, распирающие боли в нижней части спины, ощущение давления в лице или на шее
Как подтвердить, что у Вас ЛМЗ?
Основным анализом, позволяющим подтвердить диагноз лимфомы, является микроскопическое исследование образца лимфоидной ткани, полученной при биопсии (хирургическом удалении лимфатического узла или кусочка ткани пораженного органа). Эта ткань направляется на морфологическое исследование к врачу-патоморфологу, главной задачей которого является определить: "Есть ли в изучаемой ткани опухолевые (лимфомные) клетки?" Если врач находит опухолевые клетки в изучаемом гистологическом препарате, то следующий вопрос, который он должен решить: "С каким видом лимфомы мы имеем дело?" Для этого проводится иммуногистохимическое и цитогенетическое исследования.
Какое медицинское обследование необходимо перед началом лечения?
Подробный рассказ о том, какие симптомы заболевания появились и когда.
Развернутый клинический, биохимический и ииммунохимический анализ крови.
Если у Вас повышено содержание лейкоцитов - иммунофенотипирование лимфоцитов периферической крови.
КТ или ПЭТ\КТ, УЗИ для определения всех очагов опухолевого поражения.
Исследование костного мозга и люмбальной жидкости.
ЭКГ, ЭХО кардиография для выявления заболеваний сердца.
Тест на беременность.
Консультация репродуктолога если вы хотите иметь детей после окончания терапии.
Нуждаетесь ли вы сейчас в лечении?
Очень редко ЛМЗ не требует немедленного начала терапии, когда объем поражения очень мал, нет признаков быстрого роста опухоли, отсутствуют симптомы интоксикации.
Приложение Г
