Постановление Правительства РФ от 01.10.2015 N 1046
ПРАВИТЕЛЬСТВО РОССИЙСКОЙ ФЕДЕРАЦИИ
ПОСТАНОВЛЕНИЕ
от 1 октября 2015 г. N 1046
ОБ УТВЕРЖДЕНИИ ПРАВИЛ
ПРЕДОСТАВЛЕНИЯ СУБСИДИЙ ИЗ ФЕДЕРАЛЬНОГО БЮДЖЕТА РОССИЙСКИМ
ОРГАНИЗАЦИЯМ НА КОМПЕНСАЦИЮ ЧАСТИ ЗАТРАТ НА РЕАЛИЗАЦИЮ
ПРОЕКТОВ ПО ОРГАНИЗАЦИИ И ПРОВЕДЕНИЮ КЛИНИЧЕСКИХ ИСПЫТАНИЙ
ИМПЛАНТИРУЕМЫХ МЕДИЦИНСКИХ ИЗДЕЛИЙ В РАМКАХ ПОДПРОГРАММЫ
"РАЗВИТИЕ ПРОИЗВОДСТВА МЕДИЦИНСКИХ ИЗДЕЛИЙ" ГОСУДАРСТВЕННОЙ
ПРОГРАММЫ РОССИЙСКОЙ ФЕДЕРАЦИИ "РАЗВИТИЕ ФАРМАЦЕВТИЧЕСКОЙ
И МЕДИЦИНСКОЙ ПРОМЫШЛЕННОСТИ" НА 2013 - 2020 ГОДЫ
Правительство Российской Федерации постановляет:
Утвердить прилагаемые Правила предоставления субсидий из федерального бюджета российским организациям на компенсацию части затрат на реализацию проектов по организации и проведению клинических испытаний имплантируемых медицинских изделий в рамках подпрограммы "Развитие производства медицинских изделий" государственной программы Российской Федерации "Развитие фармацевтической и медицинской промышленности" на 2013 - 2020 годы.
Председатель Правительства
Российской Федерации
Д.МЕДВЕДЕВ
Утверждены
постановлением Правительства
Российской Федерации
от 1 октября 2015 г. N 1046
ПРАВИЛА
ПРЕДОСТАВЛЕНИЯ СУБСИДИЙ ИЗ ФЕДЕРАЛЬНОГО БЮДЖЕТА РОССИЙСКИМ
ОРГАНИЗАЦИЯМ НА КОМПЕНСАЦИЮ ЧАСТИ ЗАТРАТ НА РЕАЛИЗАЦИЮ
ПРОЕКТОВ ПО ОРГАНИЗАЦИИ И ПРОВЕДЕНИЮ КЛИНИЧЕСКИХ ИСПЫТАНИЙ
ИМПЛАНТИРУЕМЫХ МЕДИЦИНСКИХ ИЗДЕЛИЙ В РАМКАХ ПОДПРОГРАММЫ
"РАЗВИТИЕ ПРОИЗВОДСТВА МЕДИЦИНСКИХ ИЗДЕЛИЙ" ГОСУДАРСТВЕННОЙ
ПРОГРАММЫ РОССИЙСКОЙ ФЕДЕРАЦИИ "РАЗВИТИЕ ФАРМАЦЕВТИЧЕСКОЙ
И МЕДИЦИНСКОЙ ПРОМЫШЛЕННОСТИ" НА 2013 - 2020 ГОДЫ
1. Настоящие Правила устанавливают цели, порядок и условия предоставления субсидий из федерального бюджета российским организациям на компенсацию части затрат на реализацию проектов по организации и проведению клинических испытаний имплантируемых медицинских изделий, включая проекты по их разработке, в рамках подпрограммы "Развитие производства медицинских изделий" государственной программы Российской Федерации "Развитие фармацевтической и медицинской промышленности" на 2013 - 2020 годы (далее соответственно - проект, субсидия).
2. Субсидии предоставляются в целях достижения значений следующих целевых показателей подпрограммы "Развитие производства медицинских изделий" государственной программы Российской Федерации "Развитие фармацевтической и медицинской промышленности" на 2013 - 2020 годы:
а) доля медицинских изделий отечественного производства в общем объеме потребления в денежном выражении;
б) объем инвестиций в научные исследования, разработки, технологические инновации и перевооружение производства медицинских изделий;
в) реализация отраслевого плана мероприятий по импортозамещению в отрасли медицинской промышленности Российской Федерации.
3. Под проектом понимается комплекс взаимосвязанных мероприятий и процессов, включающий в себя:
а) выполнение научно-исследовательских, опытно-конструкторских и технологических работ (при необходимости) медицинских изделий;
б) организацию и проведение клинических испытаний медицинских изделий;
в) организацию производства медицинских изделий, в том числе создание инфраструктуры;
г) последующую коммерциализацию произведенных медицинских изделий.
4. Субсидии предоставляются в пределах бюджетных ассигнований, предусмотренных федеральным законом о федеральном бюджете на соответствующий финансовый год и плановый период, и лимитов бюджетных обязательств, утвержденных в установленном порядке Министерству промышленности и торговли Российской Федерации на цели, указанные в пункте 1 настоящих Правил.
5. Субсидия предоставляется российской организации, зарегистрированной в Российской Федерации и имеющей действующую лицензию на производство и техническое обслуживание медицинской техники в соответствии с законодательством Российской Федерации с указанием выполняемых работ в части производства медицинской техники.
6. Субсидии предоставляются российским организациям на следующих условиях:
а) бизнес-план проекта предусматривает начало выпуска и реализации медицинских изделий, прошедших клинические испытания в рамках проекта, не позднее 3 лет с даты заключения договора о предоставлении субсидии;
б) бизнес-план проекта предусматривает получение выручки от реализации медицинских изделий, прошедших клинические испытания в рамках проекта, суммарно за 3 года со дня начала выпуска и реализации этих изделий в размере, не менее чем в 3 раза превышающем размер предоставленной субсидии;
в) утратил силу. - Постановление Правительства РФ от 20.01.2017 N 37;
г) проект предусматривает разработку медицинских изделий, включенных в перечень медицинских изделий, имплантируемых в организм человека при оказании медицинской помощи в рамках программы государственных гарантий бесплатного оказания гражданам медицинской помощи, утверждаемый Правительством Российской Федерации, организацию и проведение клинических испытаний этих медицинских изделий, а также организацию их производства;
д) проект не предполагает финансирования из бюджетов бюджетной системы Российской Федерации в соответствии с иными нормативными правовыми актами;
е) проект направлен на достижение целей, предусмотренных пунктом 2 настоящих Правил.
7. Субсидии предоставляются на возмещение фактически осуществленных не ранее 1 января 2015 г. и документально подтвержденных следующих затрат российской организации, связанных с реализацией проекта, предусмотренных бизнес-планом проекта:
а) на приобретение медицинских изделий сравнения;
б) на договоры с медицинскими учреждениями, принимающими участие в реализации проекта;
в) на страховые взносы по страхованию жизни и здоровья пациентов, участвующих в клинических испытаниях медицинского изделия;
г) на заработную плату работников российской организации, непосредственно участвующих в реализации проекта, имеющих высшее фармацевтическое, медицинское, биологическое, химическое или техническое образование и (или) ученую степень кандидата или доктора наук, включая компенсационные выплаты и стимулирующие выплаты, а также на вознаграждение по договорам гражданско-правового характера, заключенным с физическими лицами и индивидуальными предпринимателями, непосредственно участвующими в реализации проекта, включая уплату страховых взносов на обязательное пенсионное страхование, обязательное медицинское страхование, обязательное социальное страхование на случай временной нетрудоспособности и в связи с материнством, обязательное социальное страхование от несчастных случаев на производстве и профессиональных заболеваний. При этом для расчета размера возмещения соответствующих затрат учитывается размер средней заработной платы и (или) указанного вознаграждения, не превышающий размера среднемесячной номинальной начисленной заработной платы работников в целом по экономике субъекта Российской Федерации, в котором осуществляет свою деятельность российская организация;
д) на работы по договорам на выполнение опытно-конструкторских и технологических работ, непосредственно связанных с реализацией проекта;
е) на работы по договорам на изготовление макетов и опытных партий медицинских изделий, а также проведение их клинических испытаний в рамках проекта.
8. Субсидии предоставляются на основании договора о предоставлении субсидии, заключенного между Министерством промышленности и торговли Российской Федерации и российской организацией. Договор о предоставлении субсидии предусматривает:
а) цели, условия и порядок предоставления субсидии;
б) сроки перечисления субсидии;
в) обязанность Министерства промышленности и торговли Российской Федерации и органов государственного финансового контроля проводить проверки соблюдения российской организацией условий, целей и порядка предоставления субсидии, которые установлены договором о предоставлении субсидии и настоящими Правилами, и согласие российской организации на проведение таких проверок;
г) ответственность российской организации за неисполнение или ненадлежащее исполнение принятых обязательств, в том числе по достижению количественных значений показателей (индикаторов) эффективности реализации проекта;
д) порядок возврата сумм, использованных российской организацией, в случае установления по итогам проверок, проведенных Министерством промышленности и торговли Российской Федерации и органами государственного финансового контроля, факта нарушения условий, целей и порядка предоставления субсидии, которые определены настоящими Правилами и договором о предоставлении субсидии, а также порядок применения в случае недостижения установленных количественных значений показателей (индикаторов) эффективности реализации проекта, предусмотренных подпунктом "и" настоящего пункта, штрафных санкций, расчет размера которых осуществляется согласно приложению N 1;
е) условия расторжения договора о предоставлении субсидии, включая условие одностороннего расторжения Министерством промышленности и торговли Российской Федерации указанного договора в случае неисполнения организацией в течение 12 месяцев реализации проекта контрольных событий, предусмотренных планом-графиком реализации проекта;
ж) порядок, форма и сроки представления отчетности о достижении значений целевых показателей реализации проекта, предусмотренных договором о предоставлении субсидии, и об осуществлении затрат, источником финансового обеспечения которых является субсидия, в том числе порядок осуществления фактической проверки достижения заявленных значений показателей (индикаторов) эффективности реализации проектов после их завершения;
з) сведения о целевых показателях реализации проекта, в том числе:
план-график реализации проекта, включая контрольные события и динамику достижения значений целевых показателей по годам его реализации;
график движения денежных средств в рамках реализации проекта;
итоги реализации проекта;
и) количественные значения следующих показателей (индикаторов) эффективности реализации проекта по годам в течение срока реализации проекта:
объем реализации медицинских изделий, клинические испытания которых осуществляются в рамках реализации проекта (нарастающим итогом за весь срок реализации проекта, в денежном выражении);
доля разработанных новых медицинских изделий в общем объеме продукции, выпускаемой российской организацией;
объем инвестиций в научные исследования, разработки, технологические инновации и перевооружение производства медицинских изделий;
количество патентов и (или) секретов производства (ноу-хау), которые предполагается получить в рамках реализации проекта;
количество высокотехнологичных рабочих мест, создаваемых и модернизируемых в рамках реализации проекта;
начало выпуска и реализации медицинских изделий, прошедших клинические испытания в рамках проекта, не позднее 3 лет со дня заключения договора о предоставлении субсидии;
объем экспорта медицинских изделий, которые созданы в ходе реализации проекта (нарастающим итогом за весь срок реализации проекта, в денежном выражении);
к) требование ведения российской организацией раздельного учета затрат, источником финансового обеспечения которых является субсидия;
л) порядок и случаи возврата в текущем финансовом году российской организацией остатков субсидии, не использованных в отчетном финансовом году;
м) запрет конвертации в иностранную валюту полученных средств федерального бюджета.
9. Для заключения договора о предоставлении субсидии российская организация представляет в Министерство промышленности и торговли Российской Федерации следующие документы:
а) сопроводительное письмо с указанием реквизитов российской организации;
б) копии учредительных документов, заверенные руководителем российской организации;
в) копия бизнес-плана проекта, включающего в себя:
маркетинговый анализ с обоснованием спроса на медицинские изделия, которые будут созданы в ходе реализации проекта;
показатели (индикаторы) эффективности реализации проекта по итогам каждого полугодия его реализации;
план-график реализации проекта, содержащий контрольные события и динамику достижения целевых показателей по годам его реализации;
структуру затрат, связанных с реализацией проекта;
объем инвестиций, привлекаемых в виде собственных средств российской организации, заемных средств или средств соинвесторов;
размер субсидии, запрашиваемой на реализацию проекта;
объем реализации медицинских изделий, клинические испытания которых осуществлялись в рамках реализации проекта (нарастающим итогом за весь срок реализации проекта, в денежном выражении);
сведения о доле разработанных новых медицинских изделий в общем объеме продукции, выпускаемой российской организацией;
количество патентов и (или) секретов производства (ноу-хау), которые предполагается получить в рамках реализации проекта;
количество высокотехнологичных рабочих мест, создаваемых и модернизируемых в рамках реализации проекта;
срок реализации проекта;
объем экспорта медицинских изделий, которые будут созданы в ходе реализации проекта;
г) копия выписки из Единого государственного реестра юридических лиц, выданной не ранее 2 месяцев до дня подачи документов, заверенная в установленном порядке (в случае непредставления российской организацией этого документа Министерство промышленности и торговли Российской Федерации запрашивает его самостоятельно);
д) гарантийные письма инвесторов (соинвесторов) и (или) кредитных организаций либо государственной корпорации "Банк развития и внешнеэкономической деятельности (Внешэкономбанк)" о готовности предоставить финансовое обеспечение расходов, связанных с реализацией проекта, в случае если бизнес-план проекта предусматривает привлечение таких средств. Указанные письма должны содержать сведения об эффективности планируемых инвестиций в проект, подготовленные на основе анализа бизнес-плана проекта.
10. Министерство промышленности и торговли Российской Федерации регистрирует документы, указанные в пункте 9 настоящих Правил, в порядке их поступления.
11. Министерство промышленности и торговли Российской Федерации рассматривает в порядке поступления документы, указанные в пункте 9 настоящих Правил, и в течение 20 календарных дней со дня их поступления заключает с российской организацией договор о предоставлении субсидии либо отказывает ей (в письменной форме) в заключении такого договора в случае несоответствия представленных документов положениям пункта 9 настоящих Правил.
12. Субсидия предоставляется на возмещение не более 80 процентов указанных в пункте 7 настоящих Правил затрат российской организации, фактически осуществленных до заключения договора о предоставлении субсидии, но не ранее 1 января 2015 г. Максимальный размер субсидии не может превышать 200 млн. рублей на весь срок реализации проекта.
13. Для получения субсидии российская организация, с которой заключен договор о предоставлении субсидии, не чаще одного раза в месяц и не позднее 5 декабря представляет в Министерство промышленности и торговли Российской Федерации заявление о предоставлении субсидии, составленное в произвольной форме и подписанное руководителем этой организации, с приложением следующих документов:
а) копии договоров и первичных учетных документов (счетов-фактур, актов сдачи-приемки выполненных работ, товарных накладных, платежных ведомостей), подтверждающих осуществление затрат по направлениям, указанным в пункте 7 настоящих Правил, заверенные в установленном порядке;
б) справка, подписанная руководителем и главным бухгалтером российской организации, о том, что эта организация не находится в стадии реорганизации, банкротства, ликвидации и не имеет ограничений на осуществление хозяйственной деятельности;
в) справка налогового органа, подтверждающая отсутствие у российской организации просроченной задолженности по уплате налогов, сборов и иных обязательных платежей, подлежащих уплате в бюджеты бюджетной системы Российской Федерации в соответствии с законодательством Российской Федерации, заверенная в установленном порядке (в случае непредставления организацией такого документа Министерство промышленности и торговли Российской Федерации запрашивает его самостоятельно);
г) справка, подписанная руководителем и главным бухгалтером и скрепленная печатью российской организации (при наличии), с указанием банковских реквизитов расчетных счетов этой организации, на которые в случае принятия положительного решения будет перечислена субсидия;
д) справка, подписанная руководителем и главным бухгалтером и скрепленная печатью российской организации (при наличии), подтверждающая неполучение этой организацией из бюджетов бюджетной системы Российской Федерации компенсации затрат по заявленным согласно настоящим Правилам направлениям в соответствии с иными актами Правительства Российской Федерации за один и тот же период;
е) отчеты, предусмотренные договором о предоставлении субсидии;
ж) расчет субсидии на возмещение затрат российской организации на приобретение медицинских изделий сравнения в рамках реализации проекта по форме согласно приложению N 2, и (или) расчет субсидии на возмещение затрат российской организации на договоры с медицинскими организациями, принимающими участие в реализации проекта, по форме согласно приложению N 3, и (или) расчет субсидии на возмещение затрат российской организации на страховые взносы по страхованию жизни и здоровья пациентов, участвующих в клинических испытаниях медицинского изделия в рамках реализации проекта, по форме согласно приложению N 4, и (или) расчет субсидии на возмещение затрат российской организации на оплату труда работников, непосредственно участвующих в реализации проекта, а также на вознаграждение по договорам гражданско-правового характера, заключенным с физическими лицами и индивидуальными предпринимателями, непосредственно участвующими в реализации проекта, включая уплату страховых взносов на обязательное пенсионное страхование, обязательное медицинское страхование, обязательное социальное страхование на случай временной нетрудоспособности и в связи с материнством, обязательное социальное страхование от несчастных случаев на производстве и профессиональных заболеваний, по форме согласно приложению N 5, и (или) расчет субсидии на возмещение затрат российской организации на осуществление работ по договорам на выполнение опытно-конструкторских и технологических работ, непосредственно связанных с реализацией проекта, по форме согласно приложению N 6, и (или) расчет субсидии на возмещение затрат российской организации на осуществление работ по договорам на изготовление макетов и опытных партий медицинских изделий, а также проведение их клинических испытаний в рамках проекта по форме согласно приложению N 7;
з) справка, подписанная руководителем организации, о ходе достижения плановых значений показателей (индикаторов) эффективности реализации проекта, в том числе по итогам завершения реализации проекта.
14. Министерство промышленности и торговли Российской Федерации регистрирует заявление о предоставлении субсидии и документы, представленные в соответствии с пунктом 13 настоящих Правил, в порядке их поступления.
Заявления о предоставлении субсидии рассматриваются в порядке поступления.
15. Министерство промышленности и торговли Российской Федерации проверяет полноту и достоверность сведений, содержащихся в представленных российской организацией документах, их соответствие положениям пункта 13 настоящих Правил и условиям договора о предоставлении субсидии и в течение 10 календарных дней принимает решение о предоставлении субсидии либо об отказе в предоставлении субсидии.
16. Основаниями для отказа в предоставлении субсидии являются:
а) несоответствие представленных документов положениям пункта 13 настоящих Правил и условиям договора о предоставлении субсидии;
б) наличие в документах неполных и недостоверных сведений;
в) недостаток лимитов бюджетных обязательств, утвержденных в установленном порядке Министерству промышленности и торговли Российской Федерации на цели, предусмотренные пунктом 2 настоящих Правил;
г) превышение максимального размера субсидии, выдаваемой одной российской организации, предусмотренного пунктом 12 настоящих Правил;
д) установление факта неисполнения российской организацией бизнес-плана и (или) нарушение сроков исполнения плана-графика реализации проекта, включая ключевые события его реализации, более чем на 45 календарных дней.
17. Министерство промышленности и торговли Российской Федерации в течение 10 календарных дней со дня принятия решения о предоставлении субсидии или об отказе в предоставлении субсидии уведомляет (в письменной форме) о принятом решении российскую организацию, подавшую заявление о предоставлении субсидии.
18. Перечисление субсидии осуществляется в установленном порядке на расчетный счет российской организации, открытый в российской кредитной организации.
19. В случае установления фактов нарушения условий предоставления субсидии российская организация обязана возвратить соответствующие средства в доход федерального бюджета в течение 10 рабочих дней со дня получения требования Министерства промышленности и торговли Российской Федерации, направленного заказным почтовым отправлением с уведомлением о вручении.
В случае если по итогам реализации проекта хотя бы одно из значений целевых показателей реализации проекта, указанных в договоре о предоставлении субсидии, составляет менее 100 процентов значения, заявленного в проекте и определенного договором о предоставлении субсидии, к российской организации применяются штрафные санкции, расчет размера которых осуществляется согласно приложению N 1 к настоящим Правилам.
20. Информация о размерах и сроках перечисления субсидий учитывается Министерством промышленности и торговли Российской Федерации при формировании прогноза кассовых выплат из федерального бюджета, необходимого для составления в установленном порядке кассового плана исполнения федерального бюджета.
21. Утратил силу. - Постановление Правительства РФ от 20.01.2017 N 37.
22. Министерство промышленности и торговли Российской Федерации и федеральный орган исполнительной власти, осуществляющий функции по контролю и надзору в финансово-бюджетной сфере, осуществляют контроль за соблюдением российскими организациями условий, целей и порядка предоставления субсидий.
Приложение N 1
к Правилам предоставления
субсидий из федерального
бюджета российским организациям
на компенсацию части затрат
на реализацию проектов по организации
и проведению клинических испытаний
имплантируемых медицинских изделий
в рамках подпрограммы "Развитие
производства медицинских изделий"
государственной программы
Российской Федерации
"Развитие фармацевтической
и медицинской промышленности"
на 2013 - 2020 годы
РАСЧЕТ РАЗМЕРА ШТРАФНЫХ САНКЦИЙ
Размер штрафных санкций (тыс. рублей) (A) определяется по формуле:
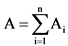 ,
,
для ![]()
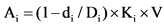 при
при ![]()
![]() при
при ![]() ,
,
для ![]()
(или если не предусмотрено значение индикатора на отчетный период)
![]() ,
,
где:
A - общая сумма штрафных санкций за отчетный период (тыс. рублей);
![]() - вклад i-го индикатора в общую сумму штрафных санкций за отчетный период (тыс. рублей);
- вклад i-го индикатора в общую сумму штрафных санкций за отчетный период (тыс. рублей);
![]() - достигнутое значение i-го целевого показателя, указанного в договоре о предоставлении субсидии, на дату окончания срока реализации проекта;
- достигнутое значение i-го целевого показателя, указанного в договоре о предоставлении субсидии, на дату окончания срока реализации проекта;
![]() - плановое значение i-го показателя, указанного в договоре о предоставлении субсидии;
- плановое значение i-го показателя, указанного в договоре о предоставлении субсидии;
V - объем средств федерального бюджета, использованных организацией - получателем субсидии в рамках реализации проекта на дату окончания срока реализации проекта (тыс. рублей);
![]() - весовой коэффициент значения i-го показателя, указанный в договоре о предоставлении субсидии;
- весовой коэффициент значения i-го показателя, указанный в договоре о предоставлении субсидии;
n - количество индикаторов, указанное в договоре о предоставлении субсидии.
Приложение N 2
к Правилам предоставления
субсидий из федерального
бюджета российским организациям
на компенсацию части затрат
на реализацию проектов по организации
и проведению клинических испытаний
имплантируемых медицинских изделий
в рамках подпрограммы "Развитие
производства медицинских изделий"
государственной программы
Российской Федерации
"Развитие фармацевтической
и медицинской промышленности"
на 2013 - 2020 годы
(форма)
Номер и дата договора
Сумма договора
Предмет договора
Наименование медицинского изделия
Сумма платежей по договору за расчетный период
Размер субсидии (гр. 5 x 0,5)
1
2
3
4
5
6
ИТОГО
Приложение N 3
к Правилам предоставления
субсидий из федерального
бюджета российским организациям
на компенсацию части затрат
на реализацию проектов по организации
и проведению клинических испытаний
имплантируемых медицинских изделий
в рамках подпрограммы "Развитие
производства медицинских изделий"
государственной программы
Российской Федерации
"Развитие фармацевтической
и медицинской промышленности"
на 2013 - 2020 годы
(форма)
Номер и дата договора
Сумма договора
Предмет договора
Целевое назначение услуги
Сумма платежей по договору за расчетный период
Размер субсидии (гр. 5 x 0,5)
1
2
3
4
5
6
ИТОГО
Приложение N 4
к Правилам предоставления
субсидий из федерального
бюджета российским организациям
на компенсацию части затрат
на реализацию проектов по организации
и проведению клинических испытаний
имплантируемых медицинских изделий
в рамках подпрограммы "Развитие
производства медицинских изделий"
государственной программы
Российской Федерации
"Развитие фармацевтической
и медицинской промышленности"
на 2013 - 2020 годы
(форма)
Номер и дата договора
Наименование страховой компании
Сумма договора
Предмет договора
Размер страховой премии по договору
Размер субсидии (гр. 5 x 0,5)
1
2
3
4
5
6
ИТОГО
Приложение N 5
к Правилам предоставления
субсидий из федерального
бюджета российским организациям
на компенсацию части затрат
на реализацию проектов по организации
и проведению клинических испытаний
имплантируемых медицинских изделий
в рамках подпрограммы "Развитие
производства медицинских изделий"
государственной программы
Российской Федерации
"Развитие фармацевтической
и медицинской промышленности"
на 2013 - 2020 годы
(форма)
Номер и дата расчетно-платежной ведомости
Начисленная сумма
Расчетная ведомость по налогам на ФОТ за _______ 20__ г.
Сумма начислений
Общие затраты на ФОТ и страховые взносы
Размер субсидии (гр. 5 x 0,8)
1
2
3
4
5
6
Приложение N 6
к Правилам предоставления
субсидий из федерального
бюджета российским организациям
на компенсацию части затрат
на реализацию проектов по организации
и проведению клинических испытаний
имплантируемых медицинских изделий
в рамках подпрограммы "Развитие
производства медицинских изделий"
государственной программы
Российской Федерации
"Развитие фармацевтической
и медицинской промышленности"
на 2013 - 2020 годы
(форма)
Номер и дата договора
Сумма договора
Предмет договора
Результат (подтверждающие документы)
Сумма платежей по договору за расчетный период
Размер субсидии (гр. 5 x 0,8)
1
2
3
4
5
6
Приложение N 7
к Правилам предоставления
субсидий из федерального
бюджета российским организациям
на компенсацию части затрат
на реализацию проектов по организации
и проведению клинических испытаний
имплантируемых медицинских изделий
в рамках подпрограммы "Развитие
производства медицинских изделий"
государственной программы
Российской Федерации
"Развитие фармацевтической
и медицинской промышленности"
на 2013 - 2020 годы
(форма)
Номер и дата договора
Сумма договора
Предмет договора
Целевое назначение договора
Сумма платежей по договору за расчетный период
Размер субсидии (гр. 5 x 0,8)
1
2
3
4
5
6
