"Методика расчета показателя "Доля исследований и разработок в интересах медицины и здравоохранения, по которым организован учет и мониторинг их дальнейшего применения"
Утверждаю
Заместитель министра здравоохранения
Российской Федерации
17.04.2025 г.
МЕТОДИКА
РАСЧЕТА ПОКАЗАТЕЛЯ "ДОЛЯ ИССЛЕДОВАНИЙ И РАЗРАБОТОК
В ИНТЕРЕСАХ МЕДИЦИНЫ И ЗДРАВООХРАНЕНИЯ, ПО КОТОРЫМ
ОРГАНИЗОВАН УЧЕТ И МОНИТОРИНГ
ИХ ДАЛЬНЕЙШЕГО ПРИМЕНЕНИЯ"
1. Настоящая методика разработана в соответствии с приказом Министерства экономического развития Российской Федерации от 1 июля 2024 г. N 399 "Об утверждении Порядка разработки (корректировки) и утверждения методик расчета показателей национальных проектов (программ), государственных программ Российской Федерации и их структурных элементов" и национальным стандартом Российской Федерации ГОСТ Р 71136-2023 "Национальные цели развития, национальные проекты (программы) и государственные программы Российской Федерации. Методики расчета показателей. Общие положения и требования к применяемым при расчетах данным" в целях обеспечения реализации национального проекта "Новые технологии сбережения здоровья", утвержденным приказом Федерального агентства по техническому регулированию и метрологии от 6 декабря 2023 г. N 1521-ст.
2. Настоящая методика применяется для расчета показателя "Доля исследований и разработок в интересах медицины и здравоохранения, по которым организован учет и мониторинг их дальнейшего применения" (П02930-С1) (далее - Показатель), включенного в перечень показателей федерального проекта "Управление медицинской наукой" национального проекта "Новые технологии сбережения здоровья", в целях мониторинга достижения национальной цели "Технологическое лидерство", определенной Указом Президента Российской Федерации от 7 мая 2024 г. N 309 "О национальных целях развития Российской Федерации на период до 2030 года и на перспективу до 2036 года".
3. Показатель характеризует долю проектов тематик научных исследований, выполняемых за счет средств федерального бюджета, сведения о которых размещены в отраслевом сегменте медицинской науки единой государственной информационной системе учета научно-исследовательских, опытно-конструкторских и технологических работ гражданского назначения (далее - ЕГИСУ НИОКТР, отраслевой сегмент медицинской науки ЕГИСУ НИОКТР) и в отношении которых идентифицирован отраслевой тип разрабатываемого результата, являющийся лекарственным препаратом, медицинским изделием, методом профилактики, диагностики, лечения или профилактики, доведенных в соответствии с уровнем готовности технологии по итогам выполнения прикладного научного исследования (этапов прикладного научного исследования) до готовности к допуску к применению для лекарственных препаратов и медицинских изделий или ко включению в клинические рекомендации для методов профилактики, диагностики, лечения и реабилитации (далее - проекты тематик научных исследований, подлежащие мониторингу), для которых осуществляется мониторинг их дальнейшего применения, в общем количестве тематик прикладных научных исследований, подлежащих мониторингу.
Для целей настоящей методики определено следующее.
Для расчета Показателя используются сведения о проектах тематик научных исследований, сведения о которых содержатся в отраслевом сегменте медицинской науки ЕГИСУ НИОКТР начиная с года начала реализации федерального проекта "Управление медицинской наукой".
Под мониторингом дальнейшего применения исследований и разработок в интересах медицины и здравоохранения понимается ежегодный сбор информации о допуске к применению лекарственных препаратов и медицинских изделий, разработка которых осуществлялась в рамках проектов тематик научных исследований, подлежащих мониторингу, и информации о включении в клинические рекомендации методов профилактики, диагностики, лечения, реабилитации, разработка которых осуществлялась в рамках проектов тематик научных исследований, подлежащих мониторингу.
Для целей настоящей методики лекарственный препарат считается допущенным к применению если он включен в государственный реестр лекарственных средств <1> и (или) в единый реестр зарегистрированных лекарственных средств Евразийского экономического союза <2> (далее - Реестры лекарственных средств).
--------------------------------
<1> Статья 33 Федерального закона от 12 апреля 2010 г. N 61-ФЗ "Об обращении лекарственных средств" (Собрание законодательства Российской Федерации, 2010, N 16, ст. 1815; 2019. N 52, ст. 7793).
<2> Решение Совета Евразийской экономической комиссии от 3 ноября 2016 г. N 84 "О порядках формирования и ведения единого реестра зарегистрированных лекарственных средств Евразийского экономического союза и информационных баз данных в сфере обращения лекарственных средств".
Для целей настоящей методики медицинское изделие считается допущенным к применению в если оно включено в государственный реестр медицинских изделий и организаций (индивидуальных предпринимателей), осуществляющих производство и изготовление медицинских изделий <3>, и (или) в единый реестр медицинских изделий, зарегистрированных в рамках Евразийского экономического союза <4>, либо если в реестр разрешений на применение незарегистрированных медицинских изделий для диагностики in vitro внесена запись о предоставлении разрешения на применение незарегистрированных медицинских изделий для диагностики in vitro <5> (далее - Реестры медицинских изделий).
--------------------------------
<3> Статья 38 Федерального закона от 21 ноября 2011 г. N 323-ФЗ "Об основах охраны здоровья граждан в Российской Федерации" (Собрание законодательства Российской Федерации, 2011, N 48, ст. 6724; 2022, N 13, ст. 1953).
<4> Решение Совета Евразийской экономической комиссии от 12 февраля 2016 г. N 46 "О Правилах регистрации и экспертизы безопасности, качества и эффективности медицинских изделий".
<5> Постановление Правительства Российской Федерации от 24 ноября 2021 г. N 2026 "О незарегистрированных медицинских изделиях для диагностики in vitro" (Собрание законодательства Российской Федерации, 2021. N 49, ст. 8219).
4. Федеральным органом исполнительной власти, ответственным за формирование (расчет) и предоставление (распространение) информации по Показателю, является Министерство здравоохранения Российской Федерации.
5. Расчет показателя осуществляется Министерством здравоохранения Российской Федерации посредством использования государственной информационной системы "Цифровая аналитическая платформа предоставления статистических данных" (далее - Информационная система) в соответствии с алгоритмом расчета, приведенным в настоящей Методике, и на основе значений компонентов Показателя, представленных в соответствии с настоящей Методикой. В случае непредставления для расчета Показателя в информационную систему значений компонентов Показателя в порядке и в сроки, установленные настоящей Методикой, при расчете значения Показателя используются данные прошлого периода.
6. Показатель рассчитывается в Информационной системе в целом по Российской Федерации, с годовой периодичностью, нарастающим итогом начиная с периода за 2025 год.
7. Тип Показателя - возрастающий. Предельное значение Показателя стремится к 1 или 100%.
8. Сроки расчета Показателя в Информационной системе, представления (распространения) информации по Показателю: ежегодно - не позднее 1 марта года, следующего за отчетным годом.
9. Единица измерения Показателя - процент (код по Общероссийскому классификатору единиц измерения - 744).
10. Показатель Nj рассчитывают по формуле:
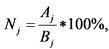
где
Aj - число подлежащих мониторингу проектов тематик научных исследований на конец j-того года с начала реализации федерального проекта "Управление медицинской наукой", для которых осуществлен мониторинг, единица;
Bj - общее число тематик научных исследований, подлежащих мониторингу на конец j-того года с начала реализации федерального проекта "Управление медицинской наукой", единица;
j - отчетный год (j = 2025 для первого года реализации федерального проекта "Управление медицинской наукой" (2025 год)), год.
11. Источником информации для компонента Aj при расчете Показателя являются административные данные, собираемые Министерством здравоохранения Российской Федерации с использованием системы межведомственного электронного взаимодействия. Сроки предоставления информации для компонента Aj - ежегодно, не позднее 1 марта года, следующего за отчетным годом.
Форма сбора административных данных для компонента Aj приведена в приложении.
12. Источником информации для компонента Bj при расчете Показателя являются данные ЕГИСУ НИОКТР <6>. Сроки предоставления информации для компонента Bj - ежегодно, не позднее 1 марта года, следующего за отчетным годом.
--------------------------------
<6> Формирование и ведение ЕГИСУ НИОКТР осуществляет Министерство науки и высшего образования Российской Федерации (постановление Правительства Российской Федерации от 12 апреля 2013 г. N 327 "О единой государственной информационной системе учета научно-исследовательских, опытно-конструкторских и технологических работ гражданского назначения").
13. Верификация информации для компонента Aj обеспечивается Министерством здравоохранения Российской Федерации посредством сверки сведений о допущенных к применению лекарственных препаратах, медицинских изделиях со сведениями Реестров лекарственных препаратов и Реестров медицинских изделий, соответственно, и сведений о включенных в клинические рекомендации методов профилактики, диагностики, лечения и реабилитации с содержанием клинических рекомендаций.
14. Верификация информации для компонента Bj обеспечивается Министерством здравоохранения Российской Федерации посредством сверки полученных административных данных со сведениями, опубликованными в ЕГИСУ НИОКТР.
Приложение
к методике расчета показателя
"Доля исследований и разработок
в интересах медицины и здравоохранения,
по которым организован учет и мониторинг
их дальнейшего применения"
Форма сбора
административных данных для компонента Aj, используемого
в расчете показателя "Доля исследований и разработок
в интересах медицины и здравоохранения, по которым
организован учет и мониторинг
их дальнейшего применения"
N п/п <1>
Регистрационный номер проекта тематики научного исследования в ЕГИСУ НИОКТР <1>, <2>
Наименование проекта тематики научного исследования <1>
Организация-исполнитель проекта тематики научного исследования <1>
Тип разрабатываемого результата <1>, <3>
Наименование разрабатываемого результата <1>
Год начала мониторинга <1>
Год допуска к применению результата исследований (разработки) <4>
Сведения о допуске результата исследований (разработки) <5>
--------------------------------
<1> - сведения заполняются при направлении формы сбора административных данных.
<2> - единая государственная информационная система учета научно-исследовательских, опытно-конструкторских и технологических работ гражданского назначения.
<3> - лекарственный препарат, медицинское изделие, метод профилактики, метод диагностики, метод лечения, метод реабилитации.
<4> - в случае отсутствия допуска вместо года указывается "нет".
<5> - для лекарственного препарата указывается наименование реестра (государственный реестр лекарственных средств или единый реестр зарегистрированных лекарственных средств Евразийского экономического союза, номер регистрационного удостоверения и его дату. Для медицинского изделия указывается наименование реестра (государственный реестр медицинских изделий и организаций (индивидуальных предпринимателей), осуществляющих производство и изготовление медицинских изделий, единый реестр медицинских изделий, зарегистрированных в рамках Евразийского экономического союза или реестр разрешений на применение незарегистрированных медицинских изделий для диагностики in vitro), номер регистрационного удостоверения (номер реестровой записи) и его дату. Для метода профилактики, метода диагностики, метода лечения, метода реабилитации (далее - метод) указывается название клинических рекомендаций, дату ее утверждения или последней актуализации, реквизиты структурной единицы клинических рекомендаций, в которой содержатся сведения о методе, и выдержку из клинических рекомендаций, содержащую сведения о методе.
