"Методика расчета показателя "Количество лекарственных препаратов, разработанных и выведенных на рынок, на каждые 5 млрд рублей, направленных на финансирование прикладных научных исследований"
Утверждаю
Заместитель Министра здравоохранения
Российской Федерации
Т.В.СЕМЕНОВА
4 декабря 2024 г.
МЕТОДИКА
РАСЧЕТА ПОКАЗАТЕЛЯ "КОЛИЧЕСТВО ЛЕКАРСТВЕННЫХ ПРЕПАРАТОВ,
РАЗРАБОТАННЫХ И ВЫВЕДЕННЫХ НА РЫНОК, НА КАЖДЫЕ 5 МЛРД
РУБЛЕЙ, НАПРАВЛЕННЫХ НА ФИНАНСИРОВАНИЕ ПРИКЛАДНЫХ
НАУЧНЫХ ИССЛЕДОВАНИЙ"
1. Настоящая методика разработана в соответствии с приказом Министерства экономического развития Российской Федерации от 1 июля 2024 г. N 399 "Об утверждении Порядка разработки (корректировки) и утверждения методик расчета показателей национальных проектов (программ), государственных программ Российской Федерации и их структурных элементов" и национальным стандартом Российской Федерации ГОСТ Р 71136-2023 "Национальные цели развития, национальные проекты (программы) и государственные программы Российской Федерации. Методики расчета показателей. Общие положения и требования к применяемым при расчетах данным" в целях обеспечения реализации национального проекта "Новые технологии сбережения здоровья", утвержденным приказом Федерального агентства по техническому регулированию и метрологии от 6 декабря 2023 г. N 1521-ст.
2. Настоящая методика применяется для расчета показателя "Количество лекарственных препаратов, разработанных и выведенных на рынок на каждые 5 млрд рублей, направленных на финансирование прикладных научных исследований" (далее - Показатель), включенного в перечень показателей федерального проекта "Управление медицинской наукой". Федеральный проект "Управление медицинской наукой" входит в состав национального проекта "Новые технологии сбережения здоровья".
3. Показатель характеризует количество лекарственных препаратов и биомедицинских клеточных продуктов, предназначенных для исполнения индивидуального медицинского назначения биомедицинского клеточного продукта, специально произведенного для отдельного пациента непосредственно в медицинской организации, в которой применяется данный биомедицинский клеточный продукт (далее - индивидуальный биомедицинский клеточный продукт), разработанных федеральными бюджетными учреждениями и выведенных на рынок, в расчете на каждые 5 млрд рублей, направленных на финансирование прикладных научных исследований в области медицины и здравоохранения, проводимых федеральными государственными учреждениями.
Для целей настоящей методики выведение на рынок лекарственного препарата в i-ом году означает регистрацию лекарственного препарата в установленном порядке в i-ом году или предоставление в i-ом году разрешения на производство и применение индивидуального биомедицинского клеточного продукта в соответствии с датой предоставления указанного разрешения в соответствии с реестровой записью реестра разрешений на производство и применение индивидуальных биомедицинских клеточных продуктов <1>. Лекарственный препарат считается зарегистрированным в i-ом году, если он включен в i-ом году в государственный реестр лекарственных средств <2> и (или) в единый реестр зарегистрированных лекарственных средств Евразийского экономического союза <3> (далее - Реестры).
--------------------------------
<1> Пункт 75 Правил предоставления, подтверждения и отмены разрешения на производство и применение биомедицинских клеточных продуктов, предназначенных для исполнения индивидуального медицинского назначения, утвержденных постановлением Правительства Российской Федерации от 28 марта 2024 г. N 385 (Собрание законодательства Российской Федерации, 2024, N 14, ст. 1916).
<2> Статья 33 Федерального закона от 12 апреля 2010 г. N 61-ФЗ "Об обращении лекарственных средств" (Собрание законодательства Российской Федерации, 2010, N 16, ст. 1815; 2019, N 52, ст. 7793).
<3> Решение Совета Евразийской экономической комиссии от 3 ноября 2016 г. N 84 "О порядках формирования и ведения единого реестра зарегистрированных лекарственных средств Евразийского экономического союза и информационных баз данных в сфере обращения лекарственных средств".
Для целей настоящей методики лекарственный препарат считается разработанным федеральным государственным учреждением в случае, если в соответствии со сведениями в Реестрах указанное учреждение является держателем или владельцем регистрационного удостоверения лекарственного препарата, либо если указанное учреждение передало права третьему лицу, заключив с ним соответствующий договор, на основании которых третье лицо является держателем или владельцем регистрационного удостоверения лекарственного препарата.
Для целей настоящей методики индивидуальный биомедицинский клеточный продукт считается разработанным федеральным государственным учреждением в случае, если разрешение на его производство и применение предоставлено указанному учреждению.
4. Федеральным органом исполнительной власти, ответственным за расчет Показателя в государственной информационной системе "Цифровая аналитическая платформа предоставления статистических данных" (далее - Информационная система), является Министерство здравоохранения Российской Федерации.
5. Расчет Показателя осуществляется посредством использования Информационной системы в соответствии с алгоритмом расчета, приведенным в настоящей Методике, и на основе значений компонентов Показателя, представленных в соответствии с настоящей Методикой. В случае непредставления для расчета Показателя в информационную систему значений компонентов Показателя в порядке и в сроки, установленные настоящей Методикой, при расчете значения Показателя используются данные прошлого периода.
6. Показатель рассчитывается в Информационной системе в целом по Российской Федерации, с годовой периодичностью, начиная с периода за 2025 год.
7. Предельное значение Показателя стремится к бесконечности.
8. Сроки представления (распространения) информации по Показателю: ежегодно - не позднее 1 марта года, следующего за отчетным.
9. Единица измерения Показателя - единица (код по Общероссийскому классификатору единиц измерения - 642).
10. Показатель Nj рассчитывают по формуле:
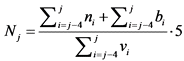 ,
,
где
ni - количество зарегистрированных в установленном порядке в i-ом году лекарственных препаратов, разработанных федеральными государственными учреждениями, для которых указанными учреждения представлены сведения об их разработке, в том числе об осуществлении отдельных этапов разработки, в рамках государственного задания учреждению на выполнение прикладных научных исследований в области медицины и здравоохранения, единица;
bi - количество индивидуальных биомедицинских клеточных продуктов, разрешения на производство и применение которых предоставлено федеральным государственным учреждениям в i-ом году, единица;
vi - объем средств федерального бюджета в i-ом году по коду подраздела классификации расходов бюджетов 0908 "Прикладные научные исследования в области здравоохранения" по кодам вида расходов "611 Субсидии бюджетным учреждениям на финансовое обеспечение государственного (муниципального) задания на оказание государственных (муниципальных) услуг (выполнение работ)" и "621 Субсидии автономным учреждениям на финансовое обеспечение государственного (муниципального) задания на оказание государственных (муниципальных) услуг (выполнение работ)" <4>, направленных на выполнение научных тем научных исследований с видом научной (научно-технической) деятельности "прикладные исследования", миллиард рублей;
--------------------------------
<4> Приказ Министерства финансов Российской Федерации от 24 мая 2022 г. N 82н "О порядке формирования и применения кодов бюджетной классификации Российской Федерации, их структуре и принципах назначения" (зарегистрирован в Министерстве юстиции Российской Федерации 30.06.2022 г., регистрационный N 69085).
J - отчетный год (J = 1 для первого года реализации федерального проекта "Управление медицинской наукой" (2025 год)), год.
Примечание.
В формуле расчета Показателя умножение на число "пять" обусловлено расчетом числа лекарственных препаратов, разработанных и выведенных на рынок, на каждые 5 млрд рублей, направленных на финансирование прикладных научных исследований.
11. Источником информации для компонента ni и bi при расчете Показателя являются собираемые Министерством здравоохранения Российской Федерации с использованием системы межведомственного электронного взаимодействия административные данные федеральных государственных учреждений, выполняющих в i-ом году государственное задание в сфере науки за счет средств федерального бюджета по коду подраздела классификации расходов бюджетов 0908 "Прикладные научные исследования в области здравоохранения" по кодам вида расходов "611 Субсидии бюджетным учреждениям на финансовое обеспечение государственного (муниципального) задания на оказание государственных (муниципальных) услуг (выполнение работ)" и "621 Субсидии автономным учреждениям на финансовое обеспечение государственного (муниципального) задания на оказание государственных (муниципальных) услуг (выполнение работ)".
Сроки предоставления информации для компонентов ni и bi - ежегодно, не позднее 1 марта года, следующего за отчетным годом.
Форма сбора административных данных для компонента ni и bi приведена в приложении к настоящей методике.
12. Источником информации для компонента vi при расчете Показателя являются данные единой государственной информационной системы учета научно-исследовательских, опытно-конструкторских и технологических работ гражданского назначения <5>.
--------------------------------
<5> Постановление Правительства Российской Федерации от 12 апреля 2013 г. N 327 (Собрание законодательства Российской Федерации, 2013, N 16, ст. 1956).
Сроки предоставления информации для компонента vi - ежегодно, не позднее 1 марта года, следующего за отчетным годом.
13. Верификация информации для компонента ni обеспечивается Министерством здравоохранения Российской Федерации посредством сверки полученных административных данных со сведениями, опубликованными в Реестрах.
14. Верификация информации для компонента bi обеспечивается Министерством здравоохранения Российской Федерации посредством сверки полученных административных данных со сведениями реестра разрешений на производство и применение индивидуальных биомедицинских клеточных продуктов <6>.
--------------------------------
<6> Ведение реестра осуществляет Министерство здравоохранения Российской Федерации (пункт 75 Правил предоставления, подтверждения и отмены разрешения на производство и применение биомедицинских клеточных продуктов, предназначенных для исполнения индивидуального медицинского назначения, утвержденных постановлением Правительства Российской Федерации от 28 марта 2024 г. N 385 (Собрание законодательства Российской Федерации, 2024, N 14, ст. 1916)).
15. Верификация информации для компонента vi обеспечивается Министерством здравоохранения Российской Федерации посредством сверки полученных административных данных со сведениями государственной интегрированной информационной системы "Электронный бюджет" <7>.
--------------------------------
<7> Ведение системы осуществляет Министерство финансов Российской Федерации, Федеральное казначейство (постановление Правительства Российской Федерации от 30 июня 2015 г. N 658 "О государственной интегрированной информационной системе управления общественными финансами "Электронный бюджет").
Приложение
Форма
сбора административных данных для компонентов ni и bi,
используемых в расчете показателя "Количество лекарственных
препаратов, разработанных и выведенных на рынок, на каждые 5
млрд рублей, направленных на финансирование прикладных
научных исследований"
N
Номер регистрационного удостоверения лекарственного препарата
Дата регистрационного удостоверения лекарственного препарата
Название лекарственного препарата
Номер записи в реестре разрешений на производство и применение индивидуальных биомедицинских клеточных продуктов
Название индивидуального биомедицинского клеточного продукта
Название и регистрационный номер темы научного исследования, результатом которого является лекарственный препарат (индивидуальный биомедицинский клеточный продукт), по данным ЕГИСУ НИОКТР <*>
Наименование организации-исполнителя темы научного исследования
Период выполнения темы научного исследования (год начала - год окончания)
1
2
N
--------------------------------
<*> - единая государственная информационная система учета научно-исследовательских, опытно-конструкторских и технологических работ гражданского назначения.
