"Клинические рекомендации "Геморрагический инсульт"
МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ
КЛИНИЧЕСКИЕ РЕКОМЕНДАЦИИ
ГЕМОРРАГИЧЕСКИЙ ИНСУЛЬТ
Кодирование по Международной статистической классификации болезней и проблем, связанных со здоровьем: I60, I61, I62, Q28.2
Год утверждения (частота пересмотра): 2025
Пересмотр не позднее: 2027
ID: 523_3
Возрастная категория: Взрослые
Специальность:
Разработчик клинической рекомендации
Ассоциация нейрохирургов России, Всероссийское общество неврологов, Общероссийская общественная организация "Союз реабилитологов России", Общероссийская общественная организация "Федерация анестезиологов и реаниматологов", Национальное общество нейрорадиологов, Ассоциация эндоваскулярных нейрохирургов имени академика Ф.А. Сербиненко
Одобрено Научно-практическим Советом Минздрава России
Список сокращений
АГМ - аневризма головного мозга
АВМ - артериовенозная мальформация
АД - артериальное давление
АКБМ - артериальный круг большого мозга
АЧТВ - активированное частичное тромбопластиновое время
БКК - блокаторы кальциевых каналов
аСАК - аневризматическое САК
ВМГ - внутримозговая гематома
ВЖК - внутрижелудочковое кровоизлияние
ВСА - внутренняя сонная артерия
ВЧГ - внутричерепная гипертензия
ВЧД - внутричерепное давление
ГИ - геморрагический инсульт
ДТЧ - декомпрессивная трепанация черепа
ЗНМА - задняя нижняя мозжечковая артерия
ИВЛ - искусственная вентиляция легких
ИПМР - индивидуальная программа медицинской реабилитации
КТ - компьютерная томография
КТА - компьютерно-томографическая ангиография
ЛСК - линейная скорость кровотока
МЕ - международные единицы
МНО - международное нормализованное отношение
МРА - магнитно-резонансная ангиография
МРТ - магнитно-резонансная томография
НВД - наружный вентрикулярный дренаж
нВЧК - нетравматическое внутричерепное кровоизлияние
НМГ - низкомолекулярный гепарин (АТХ B01AB Группа гепарина)
НФГ - нефракционированный гепарин (гепарин натрия**)
ОНМК - острое нарушение мозгового кровообращения
ОРИТ - отделение реанимации и интенсивной терапии
ПИТ - палата интенсивной терапии
ПИТС - синдром последствий интенсивной терапии
ПМА - передняя мозговая артерия
ПСА - передняя соединительная артерия
САК - субарахноидальное кровоизлияние
САД - систолическое артериальное давление
СМА - средняя мозговая артерия
СРХ - стереотаксическая радиохирургия
СДГ - субдуральная гематома
ТКДГ - ультразвуковая допплерография транскраниальная артерий методом мониторирования
ТМО - твердая мозговая оболочка
ЦАГ - церебральная ангиография
ЦВ - церебральный вазоспазм
ЦПД - церебральное перфузионное давление
ЧМН - черепно-мозговые нервы
ЧСС - частота сердечных сокращений
ШКГ - шкала комы Глазго
ЭКГ - электрокардиография
CBF - cerebral blood flow - скорость мозгового кровотока
CBV - cerebral blood volume - объем мозгового кровотока
MTT - mean transit time - среднее время прохождения
S-M - классификация Spetzler-Martin
Термины и определения
Геморрагический инсульт - полиэтиологическое заболевание, характеризующееся внутричерепным кровоизлиянием нетравматического генеза.
Аневризма головного мозга - локальное выпячивание стенки интракраниальной артерии [1].
Артериовенозная мальформация - врожденное патологическое образование головного мозга, состоящее из клубка сосудов, в котором приводящие артерии и отводящие вены соединены между собой, при отсутствии капиллярного русла (артериовенозные фистулы) [2, 3].
Внутрижелудочковое кровоизлияние - кровоизлияние в желудочки головного мозга (в том числе вследствие прорыва крови в желудочки в процессе формирования внутримозговой гематомы) [4].
Внутримозговое кровоизлияние (паренхиматозное, внутримозговая гематома) - локальное кровотечение из кровеносных сосудов в паренхиму головного мозга [5].
Субарахноидальное кровоизлияние - скопление крови под паутинной (арахноидальной) оболочкой головного мозга [6].
Субдуральное кровоизлияние (субдуральная гематома) - скопление излившейся крови или ее сгустков между паутинной (арахноидальной) оболочкой и внутренней поверхностью твердой мозговой оболочки [7].
Рабочая группа - двое или более людей одинаковых или различных профессий, работающих совместно и согласованно в целях создания клинических рекомендаций и несущих общую ответственность за результаты данной работы.
Уровень достоверности доказательств - отражает степень уверенности в том, что найденный эффект от применения медицинского вмешательства является истинным.
Уровень убедительности рекомендаций - отражает не только степень уверенности в достоверности эффекта вмешательства, но и степень уверенности в том, что следование рекомендациям принесет больше пользы, чем вреда, в конкретной ситуации.
1. Краткая информация по заболеванию или состоянию (группы заболеваний или состояний)
1.1 Определение заболевания или состояния (группы заболеваний или состояний)
Геморрагический инсульт - полиэтиологическое заболевание, характеризующееся внутричерепным кровоизлиянием нетравматического генеза (нВЧК).
В зависимости от типа распространения крови в полости черепа выделяют следующие формы нВЧК:
субдуральное кровоизлияние (субдуральная гематома),
субарахноидальное кровоизлияние (САК),
внутримозговое кровоизлияние (паренхиматозное, внутримозговая гематома (ВМГ)),
внутрижелудочковое кровоизлияние (ВЖК).
В ряде случаев нВЧК может быть смешанным (субарахноидально-паренхиматозным, паренхиматозно-вентрикулярным и др.) [8].
1.2 Этиология и патогенез заболевания или состояния (группы заболеваний или состояний)
Причины нВЧК включают различные заболевания и патологические состояния сосудистой системы головного мозга, при которых может произойти разрыв артериального сосуда.
Наиболее частой причиной так называемых "спонтанных" нВЧК является артериальная гипертония (гипертензивное ВЧК), при которой формируется гипертоническая ангиопатия - изменения сосудистой стенки в виде перерастяжения, истончения, фибриноидного некроза, образования милиарных аневризм и диссекции [9]. При этом чаще всего поражаются артерии, кровоснабжающие глубинные отделы больших полушарий, и кровоизлияния приводят к формированию глубинных ВМГ. Второй по частоте причиной разрыва артерий мозга служит амилоидная ангиопатия, при которой поражаются преимущественно корковые артерии и ВМГ локализуются в субкортикальных и корковых отделах полушарий.
нВЧК могут развиваться при различных сосудистых заболеваниях мозга:
аневризмах головного мозга (АГМ),
артериовенозных мальформациях (АВМ),
кавернозных мальформациях (КМ),
дуральных артериовенозных фистулах (ДАВФ),
болезни мойямойя.
АГМ представляют собой ограниченные расширения артерий головного мозга. Они относятся к мультифакториальным заболеваниям. Среди этиологических факторов выделяют генетические факторы, приводящие к изменению сосудистой стенки, и факторы внешнего воздействия в виде артериальной гипертензии, атеросклероза, курения, инфекции (эмбологенные аневризмы) и др. [10 - 18]. Роль генетических факторов особенно четко проявляется при семейной форме заболевания (7 - 20%) и сочетании АГМ с генетически обусловленными соединительно-тканными заболеваниями (аутосомно-доминантный поликистоз почек; синдром Элерса-Данло IV типа и др.). Для АГМ наиболее характерны САК - аневризматическое САК (аСАК) (90%), но возможны также ВМГ (до 40%) и ВЖК (до 20%). Механизм кровоизлияния - разрыв патологически измененной стенки аневризмы.
АВМ - врожденное патологическое образование, состоящее из клубка сосудов, в котором приводящие артерии и отводящие вены соединены между собой, при отсутствии капиллярного русла (артериовенозные фистулы). АВМ формируются вследствие нарушения ангиогенеза. В крайне редких случаях возможно формирование АВМ после рождения, на фоне существующих артериовенозных фистул или тромбоза вен [2, 3]. В последние годы установлена связь развития АВМ с генными мутациями в различных генах, однако они неспецифичны [19, 20]. АВМ ассоциированы с наследственной геморрагической телеангиэктазией (болезнь Рендю-Ослера), при которой они выявляются в 10 раз чаще, чем в популяции в целом [21, 22]. Для АВМ наиболее типичны кровоизлияния с образованием ВМГ, которые в 50% случаев сочетаются с САК и в 50% - с ВЖК (смешанные кровоизлияния). Основной механизм кровоизлияния - разрыв артерий на фоне высокого давления в артериовенозных шунтах мальформации.
Причиной нВЧК могут быть тромбозы венозных синусов и вен, тромбофилии, коагулопатии, васкулиты и васкулопатии. Кровоизлияние может возникнуть на фоне приема антикоагулянтов (АТХ B01A Антитромботические средства), проведения тромболизиса, при эклампсии. Особыми формами формирования ВМГ являются кровоизлияние в опухоль и геморрагическая трансформация ишемического инсульта путем диапедезного пропитывания.
1.3 Эпидемиология заболевания или состояния (группы заболеваний или состояний)
Гипертензивное внутримозговое кровоизлияние (гипертензивные ВМГ) составляет 10 - 15% от всех видов нарушения мозгового кровообращения. В Российской Федерации (РФ) диагностируют около 40 000 гипертензивных ВМГ в год. Средний возраст пациентов составляет 60 - 65 лет, соотношение мужчин и женщин - 1,6:1. Риск развития значительно повышается после 55 лет и удваивается с каждым последующим десятилетием. Летальность достигает 40 - 50%, а инвалидность развивается у 70 - 75% выживших. Факторами риска являются высокое артериальное давление, злоупотребление алкоголем, наличие в анамнезе предыдущих нарушений мозгового кровообращения, а также нарушения функции печени, сопровождающиеся тромбоцитопенией, гиперфибринолизом и уменьшением факторов свертывания крови [8, 23, 24].
Аневризматическое субарахноидальное кровоизлияние (аСАК) составляет 2 - 5% от всех видов инсульта, что для РФ соответствует 10 000 - 15 000 пациентов в год. Следует различать это количество и значительно более высокую распространенность АГМ в популяции - в среднем 2,8%. Наиболее часто аСАК происходит в возрасте 30 - 50 лет. Дети составляют около 3%, пациенты пожилого и старческого возраста - 8%. АГМ в 1,5 раза чаще встречаются у женщин. аСАК сопряжены с высоким риском летального исхода (до 60% при отсутствии лечения) и инвалидности (до 30% выживших) [25 - 27].
Кровоизлияния из АВМ составляют 1 - 2% от всех видов инсульта, при распространенности АВМ в популяции - 0,015% - 0,14% [28, 29]. Заболевание чаще манифестирует в возрасте 20 - 40 лет [30]. Ежегодный риск кровоизлияния составляет 2 - 4% [31]. У перенесших кровоизлияние этот риск кумулятивно нарастает, достигая 45% через 20 лет. Риск кровоизлияния повышается при глубинной локализации АВМ, ее дренировании в глубокие вены мозга и кровоизлиянии в анамнезе. При отсутствии указанных факторов риск разрыва мальформации составляет 0,9%, при их комбинации - до 34% [32]. Частота летального исхода после кровоизлияния из АВМ в среднем составляет около 20%. У 14% пациентов с АВМ выявляются аневризмы, связанные с АВМ - интранидальные и афферентных сосудов (проксимальные и дистальные) [33, 34]. Такие аневризмы являются установленной причиной кровоизлияния при АВМ в 16% случаев [35]. Риск кровоизлияния повышается по мере увеличения размеров ассоциированных аневризм [36].
1.4 Особенности кодирования заболевания или состояния (группы заболеваний или состояний) по Международной статистической классификации болезней и проблем, связанных со здоровьем
I60 - Субарахноидальное кровоизлияние
I60.0 - Субарахноидальное кровоизлияние из ствола внутренней сонной артерии синуса и бифуркации
I60.1 - Субарахноидальное кровоизлияние из средней мозговой артерии
I60.2 - Субарахноидальное кровоизлияние из передней соединительной артерии
I60.3 - Субарахноидальное кровоизлияние из задней соединительной артерии
I60.4 - Субарахноидальное кровоизлияние из базилярной артерии
I60.5 - Субарахноидальное кровоизлияние из позвоночной артерии
I60.6 - Субарахноидальное кровоизлияние из других внутричерепных артерий
I60.7 - Субарахноидальное кровоизлияние из внутричерепной артерии неуточненной
I60.8 - Другое субарахноидальное кровоизлияние.
I60.9 - Субарахноидальное кровоизлияние с неуточненной причиной
I61 - Внутримозговое кровоизлияние
I61.0 - Внутримозговое кровоизлияние в полушарие субкортикальное
I61.1 - Внутримозговое кровоизлияние в полушарие кортикальное
I61.2 - Внутримозговое кровоизлияние в полушарие неуточненное
I61.3 - Внутримозговое кровоизлияние в ствол мозга
I61.4 - Внутримозговое кровоизлияние в мозжечок
I61.5 - Внутримозговое кровоизлияние внутрижелудочковое
I61.6 - Внутримозговое кровоизлияние множественной локализации
I61.8 - Другое внутримозговое кровоизлияние
I61.9 - Внутримозговое кровоизлияние неуточненное
I62 - Другое нетравматическое внутричерепное кровоизлияние
I62.0 - Субдуральное кровоизлияние (острое) (нетравматическое)
I62.1 - Нетравматическое экстрадуральное кровоизлияние
Нетравматическое эпидуральное кровоизлияние
I62.9 - Внутричерепное кровоизлияние (нетравматическое) неуточненное
Q28.2 - Артериовенозный порок развития церебральных сосудов
1.5 Классификация заболевания или состояния (группы заболеваний или состояний)
Классификация гипертензивных ВМГ
- по локализации (5 вариантов) [37]:
1. Лобарные - локализованные в одной доле мозга.
2. Латеральные, или путаменальные - кровоизлияния в подкорковые образования полушария большого мозга, латерально от внутренней капсулы. Это самый частый вариант кровоизлияния.
3. Медиальные, или таламические - гематома расположена кнутри от внутренней капсулы.
4. Смешанные - как правило, массивные кровоизлияния, при которых гематома распространяется на несколько анатомических структур.
5. Кровоизлияния в заднюю черепную ямку. ВМГ могут формироваться в полушариях мозжечка и в стволе мозга, где наиболее типична локализация на уровне моста.
До 90% кровоизлияний локализуются в больших полушариях головного мозга, с примерно равным распределением частоты вариантов 1 - 4. В задней черепной ямке ВМГ чаще образуются в полушариях мозжечка.
- по объему [38, 39]:
небольшие до 20 - 30 мл,
средние - от 30 до 50 - 60 мл,
большие - свыше 60 мл.
Объем ВМГ имеет принципиально важное значение для выработки тактики лечения и прогнозирования исхода.
Классификация САК
- по периодам (три основных) [40]:
1. Острый период - 14 дней с момента последнего САК (период, в течение которого чаще всего происходит ухудшение пациентов на фоне отека, вазоспазма и ишемии головного мозга). В этом периоде выделяют острейший период (0 - 72 часа), когда у пациента клинические проявления обусловлены именно кровоизлиянием (до возникновения вазоспазма).
2. Подострый период - 15 - 31 дней с момента последнего САК (период, в течение которого регрессируют основные осложнения САК).
3. Холодный период - 1 месяц и более с момента САК (период, когда могут наблюдаться остаточные нарушения, связанные с перенесенным САК).
Классификация аневризм [41 - 43]:
- по месту возникновения: бифуркационные и стволовые АГМ.
- по форме: мешотчатые (около 90% АГМ, одно- или многокамерные) и фузиформные.
- по количеству АГМ: одиночные (80%) и множественные (20%).
- по размеру: милиарные аневризмы (до 2 мм включительно), среднего размера (3 - 14 мм), большого размера (15 - 24 мм) и гигантские АГМ (25 и более мм).
90% АГМ располагаются в передних отделах АКБМ, 10% - в задних отделах (вертебробазилярном бассейне) АКБМ.
Классификации артериовенозных мальформаций
Для оценки АВМ было предложено около 2-х десятков классификаций. Наибольшую популярность приобрела шкала, названная по имени предложивших ее в 1986 г авторов шкалой Spetzler-Martin (S-M) [44]. В основе шкалы лежит оценка трех характеристик АВМ по данным ангиографии и КТ/МРТ головы: 1) размера, 2) локализации относительно функционально значимой области (ФЗО): сенсомоторная, речевая и зрительная кора, таламус и гипоталамус, ствол, ядра мозжечка и 3) характера дренирования крови в венозную систему мозга (приложение Г10). В соответствии с количеством баллов, выделено пять степеней риска хирургического вмешательства.
I - II степень (1 - 2 балла) - риск неврологического дефицита низкий, рекомендуется операция;
III степень (3 балла) - риск умеренный, операция по индивидуальным показаниям;
IV - V (4 - 5 баллов) - риск высокий, целесообразно консервативное ведение.
Предложены также две модификации этой шкалы - шкала Spetzler-Ponce (приложение Г11), которая делит больных на три категории риска [45], и шкала Lawton-Young, которую M. Lawton разработал на основе исходной шкалы S-M, добавив еще три фактора, влияющих на исход лечения: возраст, факт кровоизлияния из АВМ в анамнезе и компактность структуры АВМ [46, 47] (приложение Г13). Эта шкала имеет наиболее высокую прогностическую точность. При значении 6 баллов и выше риск инвалидизирующего дефицита или летального исхода операции составляет 39 - 63% [48].
При радиохирургическом лечении АВМ применяют шкалы Radiosurgery Based AVM Score [49, 50] (приложение Г15) и Virginia Radiosurgery AVM [51] Scale (приложение Г14).
1.6 Клиническая картина заболевания или состояния (группы заболеваний или состояний)
1.6.1 Клинические проявления гипертензионной внутримозговой гематомы
Клинические проявления и течение гипертензивной ВМГ разнятся в зависимости от ее локализации, размера и скорости развития [52]. Симптоматика развивается, как правило, внезапно, обычно днем, во время физической нагрузки, эмоционального стресса, но чаще на фоне обычной повседневной деятельности. Неврологические симптомы обычно усиливаются в течение нескольких минут или часов до и во время госпитализации, что отражает раннее увеличение объема гематомы или нарастание отека мозга [53]. Более частый вариант дебюта - постепенное плавное прогрессирование симптомов в течение минут, а иногда и часов, менее частый - резкое развитие симптомов со снижением уровня сознания в течение нескольких секунд. Общемозговые расстройства являются ведущими, однако у лиц старшего возраста и/или при небольших, ограниченных белым веществом головного мозга, гематомах общемозговые и менингеальные симптомы могут быть мало выражены или отсутствовать.
Снижение уровня сознания (около 50% случаев)
При обширных кровоизлияниях часто снижается уровень сознания из-за повышенного внутричерепного давления и сдавления таламуса и ствола мозга. При увеличении объема гематомы уровень сознания снижается до комы и смерти из-за повышения внутричерепного давления (ВЧД) и сдавления центров ствола мозга.
Тошнота и рвота (40 - 50%)
Рвота является типичным признаком ВМГ, вызванным повышением внутричерепного давления и деформацией структур мозга. Рвота наблюдается примерно у 50% пациентов с полушарными ВМГ, и еще более часто встречается у пациентов с кровоизлияниями в мозжечок. У пациентов с гематомами мозжечка рвота почти всегда возникает на ранних стадиях клинического течения.
Головная боль (около 40%)
Кровоизлияние непосредственно в паренхиме мозга, не затрагивающее пространство спинномозговой жидкости (СМЖ), безболезненно. Таким образом, головная боль не является обязательным симптомом ВМГ. Головная боль чаще встречается у пациентов с большими гематомами и связана с натяжением мозговых оболочек, повышенным внутричерепным давлением, появлением крови в спинномозговой жидкости. Пациенты с небольшими глубокими гематомами часто не испытывают головной боли в течение всего периода болезни. Головная боль может быть единственным проявлением кровоизлияния в области хвостатого ядра, которое обычно сопровождается внутрижелудочковым кровоизлиянием.
Судорожные приступы (до 10%)
Судорожные приступы наблюдаются примерно у 10% пациентов с ВМГ и примерно у 50% пациентов с лобарными гематомами. Приступы обычно возникают в дебюте ВМК или в течение первых 24 часов [54].
Очаговые неврологические симптомы
Около 40% гипертензивных ВМГ возникают в базальных ганглиях, 30% в таламусе, 20% в долевых и около 10% возникают в мозжечке и мосту [55]. Полосатое тело (хвостатое ядро и скорлупа) является наиболее распространенным местом возникновения гипертензивной ВМГ. При этой локализации формирование гематомы вызывает глубокий контралатеральный гемипарез и нарушение чувствительности по гемитипу, тогда как кровоизлияние в таламус сопровождается более выраженными нарушениями чувствительности, чем двигательными расстройствами. Лобарные кровоизлияния могут сопровождаться нарушениями корковых функций, такими как афазия, игнорирование, нарушения "схемы тела", анозогнозия, гемианопсия. При увеличении гематомы в размерах могут присоединяться содружественное отклонение глазных яблок в сторону ВМГ (парез произвольного взора в сторону, противоположную гематоме). Глазодвигательные нарушения, такие как парез взора вверх, паралич конвергенции, ареактивные суженные зрачки, другие нарушения черепно-мозговой иннервации, альтернирующие синдромы предполагают кровоизлияние стволовой локализации. В части случаев ВМГ ствола сразу приводят к развитию комы и нарушений витальных функций. Для кровоизлияний в мозжечок характерны выраженное головокружение, нистагм, резкая боль в затылке, атаксия. При ВМГ мозжечка значительного объема возникает прямое сдавление ствола мозга с поражением нервов и проводящих путей ствола, нарушением функции дыхания и гемодинамики, или окклюзионная гидроцефалия, с развитием окклюзионно-дислокационного синдрома.
Менингеальная симптоматика в первые часы представлена преимущественно светобоязнью, скуловым симптомом Бехтерева. В дальнейшем появляется ригидность мышц затылка, симптомы Кернига, Брудзинского. У пожилых пациентов в 1/3 случаев раздражение мозговых оболочек не выявляют.
Прорыв крови в желудочковую систему (изолированное ВЖК или прорыв ВМГ) возникает у половины пациентов. Для ВЖК характерны гипертермия, гиперсаливация. Окклюзия ликворопроводящих путей сопровождается развитием окклюзионно-гипертензионного синдрома, при массивном ВЖК возникает нарушение бодрствования, горметония, мышечная гипотония, расстройства дыхания и гемодинамики.
Дислокационный синдром развивается при ВМГ значительного объема, чаще височной локализации и сопровождается нарушением бодрствования, анизокорией с мидриазом на стороне поражения, сменой полушарного пареза взора на стволовой, расстройствами дыхания и сердечно-сосудистой деятельности [56].
1.6.2 Клинические проявления субарахноидального кровоизлияния
Выделяют типичные (70%) и атипичные (30%) проявления САК.
При типичном начале заболевания основным клиническим симптомом САК является внезапная, сильная головная боль (по типу "удара в голову"), которую пациенты описывают как "худшую головную боль в моей жизни". Часто головная боль сопровождается рвотой, светобоязнью, кратковременной или длительной утратой сознания. Артериальное давление чаще повышено. В первое время менингеальные симптомы связаны с распространением крови в желудочковую систему. По мере распространения излившейся крови на уровень спинного мозга возникает боль в шее и ее ригидность.
Общемозговые и/или очаговые неврологические нарушения обнаруживаются более чем у 25% пациентов. Может отмечаться угнетение сознания и спутанность сознания; пациенты с субарахноидальным кровоизлиянием тяжелой степени часто поступают в состоянии комы. Двигательные неврологические дефициты возникают у 10 - 15% пациентов, обычно из-за аневризм средней мозговой артерии. Характерным признаком аневризмы супраклиноидного отдела ВСА является недостаточность III черепного нерва (птоз, мидриаз). Повышенное внутричерепное давление после разрыва может вызвать недостаточность отводящего нерва из-за его сдавления. У части пациентов дебют САК сопровождается судорожным приступом [57].
У 30% пациентов с разрывами АГМ наблюдается стертая или атипичная клиническая картина САК (ложномигренозная форма, ложногипертоническая форма, ложновоспалительная форма, ложнопсихотическая форма, ложнотоксическая форма, ложнорадикулярная форма). У 40% пациентов при осмотре не наблюдается никаких неврологических симптомов.
Примерно у половины пациентов отмечается легкое или умеренное повышение артериального давления.
1.6.3 Клинические проявления разрыва АВМ
Разрыв АВМ в 97% пациентов сопровождается развитием общемозгового синдрома. Менингеальный синдром наблюдают в 88%: в 60% он умеренно выражен, в 28% - грубый. У 42% пациентов при разрыве АВМ сознание ясное, у 44% происходит нарушение уровня бодрствования до оглушения, у 14% - до сопора и комы. Парезы мышц конечностей наблюдают в 53%, плегию - в 21% [58].
Очаговые неврологические нарушения и угнетение сознания при кровоизлиянии из АВМ возникают реже, чем при кровоизлиянии из аневризм или ГИ. Это связано с тем, что ВМГ при разрыве мальформации обычно не распространяются на внутреннюю капсулу, не всегда имеют большие размеры, течение заболевания редко осложняется развитием ангиоспазма, а разрыв глубинных эфферентов часто приводит к изолированным вентрикулярным кровоизлияниям. Кроме того, гематома рядом с ядром АВМ часто раздвигает паренхиму мозга и не повреждает его проводящие пути. Пациенты с разрывом АВМ наиболее молодые, что способствует их восстановлению [31, 59].
Очаговые неврологические нарушения развиваются чаще при наличии ВМГ (52%), реже - при изолированном САК (41%), еще реже - при изолированном ВЖК (28%) [31].
В 28% кровоизлияние из АВМ клинически проявляет себя лишь общемозговым и менингеальным синдромом без очаговых неврологических нарушений. Такая клиническая картина требует дифференцировки с разрывом аневризмы головного мозга. В пользу разрыва мальформации у таких пациентов свидетельствует меньшая выраженность менингеального синдрома (в 65% он умеренно выражен), а у 20% пациентов можно выявить изменения мышечного тонуса, анизорефлексию и наличие патологических рефлексов [58].
2. Диагностика заболевания или состояния (группы заболеваний или состояний) медицинские показания и противопоказания к применению методов диагностики
Критериями установки диагноза геморрагического инсульта являются:
1) клинические данные (острое развитие общемозговых/очаговых симптомов),
2) данные КТ/МРТ (выявление крови).
На основании результатов обследования принимается решения о тактике дальнейшего ведения [60].
Основными диагностическими задачами у пациентов с геморрагическим инсультом являются: установка причины кровоизлияния, определение локализации и объема кровоизлияния и сопутствующего состояния мозга (отек, дислокация, вторичные очаги повреждения), определение тяжести состояния пациента.
Диагностический алгоритм включает:
1) сбор жалоб и анамнеза,
2) физикальное обследование,
3) лабораторные исследования,
4) инструментальные исследования.
- Рекомендуется провести прием (осмотр, консультацию) первичный врача-невролога всем пациентам с геморрагическим инсультом с целью определения уровня нарушения сознания и выявления очаговых неврологических симптомов [60].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
- Рекомендуется выполнить прием (осмотр, консультацию) врачом-нейрохирургом в срок не позднее 60 минут с момента получения результатов компьютерной томографии больному, у которого по заключению компьютерной томографии или магнитно-резонансной томографии установлены признаки геморрагического инсульта с целью определения показаний к операции и выбора метода операции [60].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
Комментарий: консультация проводится в срок не позднее 60 минут <1> с момента получения результатов компьютерной томографии больному, у которого по заключению компьютерной томографии или магнитно-резонансной томографии установлены признаки геморрагического инсульта.
--------------------------------
<1> Приказ Министерства здравоохранения Российской Федерации от 14 апреля 2025 г. N 203н "Об утверждении критериев оценки качества медицинской помощи"; (Зарегистрировано в Минюсте России 28 мая 2025 г. N 82382);(http://publication.pravo.gov.ru/document/0001202505290045); вступил в силу с 01.09.2025
2.1 Жалобы и анамнез
Жалобы и анамнез описаны в разделе "Клиническая картина".
Пациенты с геморрагическим инсультом при возможности речевого контакта обычно предъявляют жалобы на головную боль, тошноту, рвоту, головокружение, а также на нарушение ряда функций, соответствующее очагу поражения мозга (слабость в конечностях, нарушение речи, чувствительности, двоение, нарушение зрения и др.) Анамнестически удается установить, что заболевание развилось остро, на фоне подъема артериального давления. У большинства пациентов кровоизлиянию предшествует длительно существующая, "не леченая" артериальная гипертензия, мочекаменная болезнь, ожирение, сахарный диабет.
- Рекомендуется провести сбор анамнеза и жалоб при патологии центральной нервной системы и головного мозга с внесением результатов оценки в медицинскую документацию всем пациентам с геморрагическим инсультом для проведения дифференциальной диагностики [60].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
Комментарии: при сборе анамнеза и жалоб необходимо обратить внимание на сроки и остроту появления симптомов;
у пациента с неясным анамнезом и нарушением сознания - исключать черепно-мозговую и сочетанную травму [60].
2.2 Физикальное обследование
Данные физикального обследования описаны в разделе "Клиническая картина".
При общем осмотре оценивают уровень сознания, тяжесть состояния, функции жизненно важных органов и систем.
При неврологическом осмотре оценивают наличие менингеальных симптомов и очаговых симптомов (поражения черепных нервов, полушарий и ствола головного мозга).
- Рекомендуется провести общий осмотр, стандартную оценку тяжести состояния и уровня сознания всем пациентам с геморрагическим инсультом для проведения дифференциальной диагностики и установления этиологии заболевания [61].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
- Рекомендуется провести визуальное исследование при патологии центральной нервной системы и головного мозга, пальпацию при патологии центральной нервной системы и головного мозга, исследование чувствительной и двигательной сферы при патологии центральной нервной системы и головного мозга (оценка неврологического статуса) с внесением результатов оценки в медицинскую документацию всем пациентам с геморрагическим инсультом для проведения дифференциальной диагностики и установления этиологии заболевания [60].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
- Рекомендуется провести оценку по шкалам: шкала комы Глазго, шкала инсульта Национального института здоровья, Канадская неврологическая шкала, шкала Hunt-Hess, шкала WFNS, модифицированная шкала Рэнкина пациентам с геморрагическим инсультом в зависимости от его этиологии для оценки тяжести состояния [62 - 67].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 3)
Комментарии: шкала комы Глазго (ШКГ) - см. приложение Г4,
шкала инсульта Национального института здоровья (NIHSS) - см. приложение Г17,
Канадская неврологическая шкала - см. приложение Г18,
шкала Hunt-Hess - см. приложение Г1,
шкала WFNS - см. приложение Г5,
модифицированная шкала Рэнкина - см. приложение Г9.
- Рекомендуется выполнить оценку состоятельности глотания при помощи теста оценки глотания ("трехглотковая проба" с использованием пульсоксиметра) в течение первых 3 часов пребывания пациента в стационаре для выявления ранних признаков дисфагии с целью снижения риска аспирации [68].
Уровень убедительности рекомендаций B (уровень достоверности доказательств - 2)
Комментарии: Дисфагия - частое проявление инсульта, которое является фактором риска аспирационной пневмонии и ассоциировано с более высокой смертностью [69, 70]. Ранний скрининг дисфагии у взрослых пациентов, поступивших с острым инсультом, снижает у них риски пневмонии, летального исхода, зависимости от посторонней помощи и продолжительного пребывания в стационаре [68, 70].
Оценку дисфагии следует проводить пациенту до приема пищи или пероральных лекарственных средств в ПИТ/ОРИТ.
Скрининговое тестирование глотания (см. приложение Г20).
При невозможности тестирования функции глотания или выявлении дисфагии показана установка назогастрального зонда для осуществления нутритивной поддержки.
2.3 Лабораторные диагностические исследования
Пациенту с геморрагическим инсультом необходимо выполнить ряд лабораторных исследований, включающий общий (клинический) анализ крови [71, 72] и общий (клинический) анализ мочи [73], анализ крови биохимический общетерапевтический [74], коагулограмму (ориентировочное исследование системы гемостаза) [75], исследование агрегации тромбоцитов (при наличии анамнеза приема антиагрегантов, кроме гепарина) [76, 77].
- Рекомендуется провести исследование общего (клинического) анализа крови развернутого всем пациентам с геморрагическим инсультом для оценки тяжести состояния [71, 72].
Уровень убедительности рекомендаций B (уровень достоверности доказательств - 3)
Комментарии: оценка количества и среднего объема тромбоцитов имеет прогностическое значение.
- Рекомендуется провести исследование общего (клинического) анализа мочи всем пациентам с геморрагическим инсультом в рамках общетерапевтического скрининга с целью выявления признаков нарушения функции почек и мочевыводящих путей [73].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
- Рекомендуется провести анализ крови биохимический общетерапевтический всем пациентам с геморрагическим инсультом в рамках общетерапевтического скрининга с целью выявления признаков электролитных и метаболических нарушений, а также маркеров воспаления [74].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
- Рекомендуется провести анализ коагулограммы (ориентировочное исследование системы гемостаза) всем пациентам с геморрагическим инсультом с целью профилактики вторичных геморрагических осложнений [75].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
Комментарии: изменение свертывающей системы крови в сторону гипокоагуляции может быть обусловлено как заболеванием (патология крови, печени и т.д.), так и приемом медикаментов.
- Рекомендуется провести исследование агрегации тромбоцитов пациентам с геморрагическим инсультом при наличии анамнеза приема ангиагрегантов, кроме гепарина [76, 77].
Уровень убедительности рекомендаций B (уровень достоверности доказательств - 3)
2.4 Инструментальные диагностические исследования
- Рекомендуется выполнить компьютерную томографию головного мозга или магнитно-резонансную томографию головного мозга не позднее 40 минут от момента поступления в стационар всем пациентам с геморрагическим инсультом для уточнения расположения и объема внутричерепного кровоизлияния [78 - 81].
Уровень убедительности рекомендаций B (уровень достоверности доказательств - 2)
Комментарии:
Исследование необходимо выполнить в течение первых 40 минут от момента госпитализации <2>.
--------------------------------
<2> Приказ Министерства здравоохранения Российской Федерации от 14 апреля 2025 г. N 203н "Об утверждении критериев оценки качества медицинской помощи"; (Зарегистрировано в Минюсте России 28 мая 2025 г. N 82382);(http://publication.pravo.gov.ru/document/0001202505290045); вступил в силу с 01.09.2025
Объем кровоизлияния определяют либо с помощью программы, поставляемой производителем томографа, либо по формуле ABC/2, где A - наибольший диаметр, B - перпендикулярный диаметр по отношению к A, C - количество срезов x толщину среза. Пациентам, у которых во время хирургического вмешательства планируется использовать нейронавигацию, также производят сканирование в том режиме, который необходим для последующей передачи изображения на конкретную навигационную станцию [82, 83].
При выполнении КТ (МРТ) следует определить:
наличие и топическое расположение патологического очага (очагов);
объем каждого вида очага (гипо-, гиперденсивной части);
положение срединных структур мозга и степень их смещения в мм;
состояние ликворосодержащей системы мозга (величина, форма, положение, деформация желудочков) с определением вентрикуло-краниальных коэффициентов;
состояние цистерн мозга;
состояние борозд и щелей мозга.
Степень выраженности САК оценивается по классификации Fisher (см. приложение Г2) и/или Hijdra (см. приложение Г6). При наличии сопутствующего ВЖК используется шкала Graeb (см. приложение Г3).
- Рекомендуется выполнить осмотр кожных покровов головы на наличие повреждений и провести оценку уже имеющейся компьютерной томографии головного мозга в костном режиме пациентам с угнетением уровня сознания, отсутствием данных анамнеза, выявленной изолированной субдуральной гематомой для исключения переломов костей черепа [84].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
Комментарии: СДГ может быть обусловлена травмой головы, о которой нет информации
- Рекомендуется выполнить спинномозговую пункцию (люмбальную, поясничную) пациенту с симптомами геморрагического инсульта при отсутствии возможности проведения компьютерной или магнитно-резонансной томографии головного мозга для определения крови в спинномозговой (цереброспинальной) жидкости [85].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
Комментарии: при наличии клинических и/или инструментальных признаков дислокации проведение спинномозговой пункции противопоказано.
- Рекомендуется выполнить компьютерно-томографическую ангиографию, или магнитно-резонансную ангиографию, или церебральную ангиографию для выявления источника кровоизлияния при подозрении на разрыв аневризмы или артериовенозной мальформации по данным компьютерной томографии головного мозга и (или) магнитно-резонансной томографии головного мозга с целью выявления источника кровотечения [86 - 89].
Уровень убедительности рекомендаций B (уровень достоверности доказательств - 1)
Комментарии: выполняют один из перечисленных видов ангиографии. КТ-ангиографию при подозрении на нетравматический характер кровоизлияния следует выполнять от дуги аорты, включая магистральные артерии головы и шеи, в артериальной венозной фазе, для исключения всех видов сосудистых мальформаций и оценки доступа к ним. Чувствительность КТА в выявлении АВМ и аневризмы на фоне кровоизлияния составляет 84 - 100% при специфичности 77 - 100% [90]. При проведении КТА у пациентов с ГИ часто наблюдают "симптом пятна" (spot sign), обусловленный экстравазацией контрастного средства. При проведении КТА в первые 3 часа от начала заболевания вероятность этого симптома составляет 66%, через 6 часов снижается до 13% [23]. "Симптом пятна" является признаком нарастания объема ВМГ и ухудшает исход заболевания [91].
- Рекомендуется выполнить компьютерно-томографическую ангиографию, или магнитно-резонансную ангиографию, или церебральную ангиографию для выявления источника кровоизлияния пациентам с ГИ моложе 45 лет при отсутствии гипертонического анамнеза - для выявления источника кровоизлияния [86 - 89].
Уровень убедительности рекомендаций B (уровень достоверности доказательств - 1)
Комментарии: выполняют один из перечисленных видов ангиографии.
- Рекомендуется выполнить отсроченную компьютерно-томографическую ангиографию сосудов головного мозга через несколько минут после введения контрастного средства пациентам с "симптомом пятна" по данным компьютерно-томографической ангиографии сосудов головного мозга для отличия артериовенозной мальформации и аневризмы [23].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
Комментарии: при "симптоме пятна" происходит изменение его конфигурации и плотности из-за смешивания контрастного средства с гематомой при повторном исследовании. При АВМ и аневризме этого не происходит, их плотность соответствует плотности рядом расположенных нормальных артерий при обоих исследованиях.
- Рекомендуется выполнить церебральную ангиографию тотальную селективную при недостаточной информативности данных компьютерной или магнитно-резонансной томографии головного мозга с целью уточнения анатомо-топографических характеристик аневризмы и выявления источника кровоизлияния [92].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
- Рекомендуется провести оценку кровоизлияния по шкале SICH всем пациентам с гипертензивными ВМГ для решения вопроса о необходимости выполнения исследования сосудов головного мозга с контрастированием (компьютерно-томографическая ангиография сосудов головного мозга, церебральная ангиография тотальная селективная) [93].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
Комментарии:
Оценку кровоизлияния по шкале SICH (secondary intracerebral hemorrhage score) предложил Almandoz J.E.D. с соавт. в 2010 году (см. приложение Г12) [93].
Факторами риска выявления сосудистой патологии у пациентов с ВМГ являются: анатомическая форма кровоизлияния по данным нативной КТ, молодой возраст пациента, женский пол, отсутствие артериальной гипертензии и нарушений коагуляции (см. приложение Г12). При оценке по шкале SICH в 0 - 2 балла вероятность сосудистой патологии составляет 3%, в 3 балла и более - 34%.
Мальформации могут быть не обнаружены при ангиографии из-за небольших размеров и сдавления гематомой [94, 95].
При отсутствии АВМ при первичной КТА или ЦАГ целесообразно выполнение повторной КТА или ЦАГ после резорбции ВМГ для обнаружения мальформации.
Ангиографическими факторами риска разрыва АВМ являются стеноз и варикоз эфферентов, исключительно глубинное венозное дренирование, единственный эфферент, венозный рефлюкс, экстра- и интранидальные аневризмы [32, 96 - 98].
2.5 Иные диагностические исследования
- Рекомендуется провести ультразвуковую допплерографию транскраниальную артерий методом мониторирования (ТКДГ) с измерением линейной скорости кровотока в М1 сегменте СМА и вычислением индекса Линдегаарда всем пациентам с аневризматическим субарахноидальным кровоизлиянием для оценки выраженности церебрального вазоспазма [16, 99, 100].
Уровень убедительности рекомендаций B (уровень достоверности доказательств - 2)
Комментарии:
Преимуществами ТКДГ является ее неинвазивный характер, быстрота и простота выполнения исследования, возможность динамически исследований с отслеживанием динамики скоростных показателей кровотока при наличии церебрального вазоспазма (ЦВ). В случае принятия решения по инвазивному лечению ЦВ требуется проведение ЦАГ.
Индекс Линдегаарда - соотношение ЛСК в М1 сегменте СМА к ЛСК в экстракраниальном отделе ипсилатеральной ВСА.
Для характеристики наличия и выраженности ЦВ по данным ТКДГ желательно вычислять среднюю линейную скорость кровотока (ЛСК) по М1 сегменту СМА [27, 101]. В то же время в отечественной нейрохирургической школе допустим расчет ИЛ с использованием систолических скоростей. Степени выраженности ЦВ по данным ИЛ и систолической (средней) скоростям кровотока представлены в таблице 1.
Таблица 1. Степени выраженности церебрального вазоспазма на основании ТКДГ [27, 101]
Средняя (систолическая) скорость по СМА, см/сек
Индекс Линдегаарда (соотношение скоростей СМА/ВСА шея)
Интерпретация
100 - 120 (120 - 160)
2 - 3
Нет спазма
120 - 200 (160 - 240)
3 - 6
Умеренный
> 200 (240)
> 6
Тяжелый
- Рекомендуется при наличии в лечебном учреждении технической возможности провести компьютерно-томографическую перфузию головного мозга пациентам с аневризматическим субарахноидальным кровоизлиянием с интенсивностью Fisher III - IV вследствие разрыва аневризмы средней мозговой артерии или внутренней сонной артерии перед операцией для выявления очагов скрытой ишемии [102 - 106].
Уровень убедительности рекомендаций B (уровень достоверности доказательств - 1)
Комментарии: шкала Fisher см. приложение Г2.
- Рекомендуется при наличии в лечебном учреждении технической возможности провести компьютерно-томографическую перфузию головного мозга при клинически обоснованном подозрении на церебральный вазоспазм и увеличении средней скорости кровотока по М1 сегменту при ультразвуковой допплерографии транскраниальной артерий методом мониторирования (ТКДГ) выше 200 см/с для оценки риска развития массивной ишемии [107 - 109].
Уровень убедительности рекомендаций B (уровень достоверности доказательств - 1)
Комментарии: при КТ-перфузии критическим считается снижение скорости церебрального кровотока (CBF) в бассейне спазмированной артерии ниже 10 - 15 мл/100г/мин, объема кровотока (CBV) ниже 1 - 1,5 мл/100г, и повышение среднего время прохождения (МТТ) выше 6 секунд [27, 108].
3. Лечение, включая медикаментозную и немедикаментозную терапии, диетотерапию, обезболивание, медицинские показания и противопоказания к применению методов лечения
3.1 Лечение пациентов с гипертензивной внутримозговой гематомой
Вопросы лечения геморрагического инсульта являются сложными и не до конца решенными. Существующие опубликованные результаты клинических исследований не позволяют сделать однозначные выводы о превосходстве консервативного или нейрохирургического лечения в отношении функционального восстановления пациентов во время лечения в стационаре или в дальнейшем на амбулаторном этапе. Результаты клинических исследований нейрохирургического лечения свидетельствуют о том, что оно позволяет у некоторых пациентов избежать летального исхода, но его положительное влияние на степень инвалидизации в дальнейшем однозначно не установлено. Результаты клинических исследований консервативных методов лечения также не являются полностью однозначными, что зачастую затрудняет их практическое применение. Определенным является то, что пациент должен проходить лечение и реабилитацию в медицинской организации, имеющей в своем составе отделения нейрохирургии, реанимации и интенсивной терапии, и отделение ранней реабилитации.
3.1.1 Интенсивная терапия пациентов с гипертензивной внутримозговой гематомой
Коррекция артериального давления при гипертензивной внутримозговой гематоме
Безопасность и эффективность снижения цифр систолического АД (САД) в периоде заболевания до 7 дней от начала симптомов была изучена в рандомизированных клинических исследованиях ATACH [110], INTERACT [111], INTERACT2 [112], ATACH-II, INTERACT3 [113], а также дополнительно в анализе данных пациентов исследований INTERACT2 и ATACH-II [114].
- Рекомендуется снижение систолического артериального давления ниже 140 мм рт. ст. с использованием внутривенных антигипертензивных препаратов (селективные блокаторы кальциевых каналов с преимущественным действием на сосуды (С08С), ингибиторы АПФ (C09AA), бета-адреноблокаторы (C07A) и альфа-адреноблокаторы (C02CA) в условиях его непрерывного мониторирования (необходимо стремиться к минимальной вариабельности цифр артериального давления) при подтвержденном геморрагическом инсульте в течение первых 6 ч после появления симптомов с целью уменьшения окончательного объема гематомы [113, 115].
Уровень убедительности рекомендаций B (уровень достоверности доказательств - 2)
Комментарии: Снижение АД в течение 6 часов от начала симптомов у пациентов с внутримозговым кровоизлиянием ассоциируется с меньшим риском увеличения гематомы. Метаанализ четырех рандомизированных контролируемых исследований, включивших 2919 участников, показал отношение шансов 0,76 (95% ДИ 0,60 - 0,95) в отношении роста гематомы. Это указывает на то, что раннее снижение артериального давления является эффективной стратегией профилактики увеличения гематомы при внутримозговом кровоизлиянии [115]. Результаты объединенного анализа INTERACT2 и ATACH-II показали, что снижение цифр АД было линейно связано с повышением вероятности более благоприятного 90-дневного исхода заболевания (оценка по модифицированной шкале Рэнкина 0 - 2 балла). У пациентов с цифрами САД более 220 мм рт. ст. может быть обоснованным более активное снижение цифр АД [37, 114, 115]. По данным INTERACT3, желательно достигать целевого уровня САД ниже 140 мм рт. ст. в течение 1 часа от начала лечения [113], но не быстрее чем на 60 мм рт. ст. в час [115]. Не рекомендуется снижение САД ниже 130 мм рт. ст. [113].
- Рекомендуется раннее начало антигипертензивной терапии у пациентов с небольшими гематомами (объемом < 30 мл), в идеале - в течение первых 2 часов после появления симптомов [115].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
- Рекомендуется поддержание систолического артериального давления ниже 140 мм рт. ст. в течение 7 дней от начала заболевания [113, 115].
Уровень убедительности рекомендаций B (уровень достоверности доказательств - 2)
Контроль температуры тела
- Рекомендуется пациенту с гипертензивной внутримозговой гематомой после госпитализации снижение температуры тела физическими методами охлаждения и/или жаропонижающими средствами (АТХ M01A Нестероидные противовоспалительные и противоревматические препараты) до целевого значения ![]() 37,5 °C [113].
37,5 °C [113].
Уровень убедительности рекомендаций B (уровень достоверности доказательств - 2)
Комментарии: желательно достигать целевого уровня температуры тела ![]() 37,5 °C в течение 1 часа от начала лечения и поддерживать в течение 7 дней [113].
37,5 °C в течение 1 часа от начала лечения и поддерживать в течение 7 дней [113].
Контроль гликемии
- Рекомендуется пациенту с гипертензивной внутримозговой гематомой в течение госпитализации достижение уровня глюкозы сахароснижающими препаратами (АТХ A10 Препараты для лечения сахарного диабета) до целевых значений 6,1 - 7,8 ммоль/л у пациентов без сахарного диабета и 7,8 - 10,0 ммоль/л у пациентов с сахарным диабетом [113].
Уровень убедительности рекомендаций А (уровень достоверности доказательств - 2)
Комментарии: желательно достигать целевого уровня гликемии в течение 7 дней [113].
Коррекция изменений системы гемостаза при гипертензивной внутримозговой гематоме
В настоящее время в связи с все более активным применением антикоагулянтной терапии, в частности, для профилактики ишемического инсульта, увеличивается число геморрагических инсультов, возникших на фоне приема данных препаратов. Кроме того, гипертензивная ВМГ может возникать и на фоне антиагрегантной терапии, а также у пациентов с имеющимися заболеваниями системы гемостаза. Схема инактивации антитромботических средств у пациентов с возникшей гипертензивной ВМГ представлена см. приложение Б2.
- Рекомендуется отмена антагонистов витамина K (B01AA: варфарин** и т.д.) и внутривенное назначение 20 мг фитоменадиона (B02BA01) в сочетании с факторами свертывания крови II, VII, IX и X в комбинации** (B02BD01) или свежезамороженной плазмы у пациентов с гипертензивной внутримозговой гематомой в течение 7 дней от начала симптомов при повышенном МНО на фоне приема антагонистов витамина K (B01AA: варфарин** и т.д.) до целевого уровня МНО < 1,5 [37, 113, 116].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
Комментарии: желательно достигать целевого уровня МНО < 1,5 в течение 1 часа от начала лечения и поддерживать в течение 7 дней [113].
В 2024 г. в России появилась зарегистрированная для применения у пациентов парентеральная форма витамина К1 (фитоменадиона; B02BA01) в виде эмульсии для внутривенного введения. В отличии от пероральной формы, внутривенное введение фитоменадиона (витамина К1) увеличивает выработку факторов свертывания в пределах 1 - 2 часов и достигает максимального эффекта уже через 12 часов. В случае стойкого повышения МНО введение фитоменадиона (витамина К) можно повторять каждые 12 часов. У большинства пациентов с кровотечениями на фоне АВК, введение фитоменадиона (витамина К1) рекомендуется начинать, не дожидаясь лабораторных анализов и данных визуализации, поскольку риски, связанные с введением витамина К1 низки [37].
В сравнении со свежезамороженной плазмой (СЗП), у факторов свертывания крови II, VII, IX и X в комбинации [Протромбиновый комплекс]** (B02BD01) может возникать меньше осложнений, при их назначении возможна более быстрая коррекция МНО [37, 116].
Введение СЗП требует не только временных затрат на подготовку к гемотрансфузии (разморозку, пробу на индивидуальную совместимость и т.д.), но и введения значительно большего объема (20 мл/кг), что часто задерживает время нормализации МНО и может занять в среднем до 30 часов. Кроме того, большой объем вводимой СЗП увеличивает риски перегрузки жидкостью (особенно на фоне сопутствующей кардиологической патологии, исходно требовавшей терапии антагонистами витамина К) и развития посттрансфузионных реакций. Частота тромботических осложнений сходна как на фоне терапии концентратом протромбинового комплекса, так и при применении СЗП [117].
- Не рекомендуется применять рекомбинантный активированный фактор свертывания крови VII (Эптаког альфа [активированный])** (B02BD08) для коррекции цифр МНО, увеличенных на фоне приема антагонистов витамина K у пациентов с гипертензивной внутримозговой гематомой [37, 116].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
Комментарии: не рекомендуется назначение рекомбинантного активированного фактора свертывания крови VII**, который может приводить к снижению МНО, но не замещает все необходимые факторы свертывания. Кроме того, он характеризуется быстрым периодом полувыведения (2 - 3 часа), после которого потребуется введение повторной дозы или другого препарата [117].
- Не рекомендуется использование менадиона натрия бисульфита** для коррекции эффекта антагонистов витамина К в связи с низкой эффективностью [118].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
- Рекомендуется отмена дабигатрана этексилата** (B01AE07) и назначение специфического антидота идаруцизумаба или #факторов свертывания крови II, VII, IX и X в комбинации [Протромбиновый комплекс]** в первые 6 часов после верификации гипертензивной внутримозговой гематомы у пациентов, получающих дабигатрана этексилат (B01AE07)**. У пациентов с ВМГ на фоне ривароксабана** (B01AF01) или апиксабана** (B01AF02) рекомендуется применение #факторов свертывания крови II, VII, IX и X в комбинации [Протромбиновый комплекс]** в связи с недоступностью специфического антидота [37, 119, 120]
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
Комментарии: Кратность и дозы введения рассчитываются индивидуально на основании массы тела пациента и показателя МНО. Целесообразно рассмотреть введение 25 - 50 ЕД/кг в зависимости от показателя МНО с его дальнейшей повторной оценкой [37, 119, 120] При этом, высшая разовая доза не должна превышать рекомендованную для каждого отдельного препарата внутри группы факторов свертывания крови II, VII, IX и X в комбинации [Протромбиновый комплекс]** (B02BD01).
- Рекомендуется для ингибирования эффекта гепарина натрия** (B01AB01) (нефракционированного гепарина, НФГ) у пациентов в первые 6 часов после верификации гипертензивной внутримозговой гематомы назначение протамина сульфата** (V03AB14) [37, 116].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
Комментарии: на фоне терапевтических доз гепарина натрия** (B01AB01) показано внутривенное введение протамина сульфата** (V03AB14), который струйно вводят со скоростью 1 мл (10 мг) раствора в течение 2 минут. В случае необходимости инъекции повторяют с интервалами 15 - 30 мин, общая доза обычно составляет 5 мл (50 мг) раствора - вводят в течение 10 мин. Не следует вводить более 150 мг в течение 1 часа. Альтернативным способом расчета необходимой дозы является введение 1 мг протамина сульфата** на 100 единиц НФГ с учетом периода полувыведения гепарина натрия** (от 1 до 2 часов). Протамина сульфат** следует вводить путем медленной внутривенной инфузии, не превышающей 20 мг/мин (из-за риска анафилактических реакций). Нейтрализация гепарина натрия** (НФГ), введенного внутривенно, наступает в среднем через 5 минут после введения и сохраняется в течение 2 часов. При подкожном введении гепарин натрия** (НФГ) характеризуется более продолжительным эффектом из-за длительного всасывания из подкожно-жировой клетчатки [119]. Реверсия профилактической дозы гепарина натрия** (НФГ), введенной подкожно, не показана [116].
- Рекомендуется применение #протамина сульфата** (V03AB14) в первые 6 часов после верификации гипертензивной внутримозговой гематомы у пациентов, получающих низкомолекулярные гепарины (НМГ) (АТХ B01AB Группа гепарина): далтепарин натрия (B01AB04), эноксапарин натрия** (B01AB05), надропарин кальция (B01AB06), для частичной инактивации НМГ [116].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
Комментарии: В отличие от НФГ (гепарин натрия**), протамина сульфат** менее эффективен в устранении эффекта НМГ, поскольку он не связывается с короткими углеводными цепями НМГ, однако может нейтрализовать более высокомолекулярные фракции, которые, как считается, чаще ассоциированы с кровотечениями [104]. Таким образом, протамина сульфат** (V03AB14) эффективно ингибирует влияние НМГ на FII, но лишь частично ингибирует его влияние на FX. Рекомендована следующая схема дозирования #протамина сульфата**: для эноксапарина натрия** (B01AB05), введенного в течение предыдущих 8 часов - 1 мг #протамина сульфата** на 1 мг эноксапарина натрия**; введенного более 8 часов назад - 0,5 мг #протамина сульфата** на 1 мг эноксапарина натрия**. Для далтепарина натрия** (B01AB04) и надропарина кальция (B01AB06) - 1 мг #протамина сульфата**на 100 анти-Ха МЕ [116].
Показана реверсия только терапевтической, но не профилактической дозы НМГ [116]. Однако в ряде клинических ситуаций, связанных с нарушением элиминации НМГ и кумуляции его эффекта, выявлен терапевтический эффект на фоне профилактических дозировок [117]. Поэтому в последнее время все большее место занимает персонифицированный подход к дозированию НМГ, основанный, в том числе, на лабораторном мониторинге.
Определить наличие и выраженность антикоагулянтного эффекта на фоне НМГ можно по анти-Ха. Реверсия НМГ на фоне ГИ показана при анти-Ха ![]() 0,3 и/или возникновении ВМГ менее чем 12 часов с момента последнего введения НМГ.
0,3 и/или возникновении ВМГ менее чем 12 часов с момента последнего введения НМГ.
- Не рекомендуется у пациентов с гипертензивной внутримозговой гематомой, получавших препараты группы "антиагреганты, кроме гепарина" (B01AC), проводить трансфузию тромбоцитарной массы с целью ингибирования эффекта этих препаратов [37, 116].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
Комментарии: возможный положительный эффект трансфузии тромбоцитарной массы при гипертензивной ВМГ не установлен. Важным вопросом в коррекции эффекта антиагрегантов, кроме гепарина, является лабораторная оценка их эффективности, поскольку, по разным данным, у части пациентов есть резистентность к ацетилсалициловой кислоте** и клопидогрелу**. Необратимая инактивация циклооксигеназы ацетилсалициловой кислотой** означает, что он оказывает длительный фармакодинамический эффект и ингибирует тромбоциты на оставшуюся часть их жизни (до 10 суток). Однако у ацетилсалициловой кислоты** очень короткий фармакокинетический период полувыведения, поэтому препарат сохраняется в кровообращении всего несколько минут. Следовательно, переливание тромбоцитов может быть целесообразным в терапии кровотечений, связанных с приемом ацетилсалициловой кислоты**, поскольку новые тромбоциты не будут подвергаться действию ацетилсалициловой кислоты**. В рекомендациях 2016 г. предлагается осуществлять трансфузию тромбоцитов пациентам с ВМГ на фоне ацетилсалициловой кислоты**, которым планируется выполнение нейрохирургической операции. На фоне прекращения приема необратимых ингибиторов P2Y12 (клопидогрела** (B01AC Антиагреганты, кроме гепарина), прасугрела (B01AC Антиагреганты, кроме гепарина)), восстановление нормальной функции тромбоцитов будет происходить только с синтезом и поступлением в кровоток новых тромбоцитов. При трансфузии тромбоцитов в период менее 3 - 5 периодов полувыведения препаратов-ингибиторов P2Y12 (клопидогрела** (B01AC Антиагреганты, кроме гепарина), прасугрела (B01AC Антиагреганты, кроме гепарина)), будет наблюдаться фармакологическое ингибирование перелитых тромбоцитов, а присутствие активных метаболитов препарата может привести к еще более длительному ингибированию тромбоцитов. Таким образом, при ВМГ на фоне ингибиторов P2Y12 (клопидогрела** (B01AC Антиагреганты, кроме гепарина), прасугрела (B01AC Антиагреганты, кроме гепарина)), рекомендовано воздержаться от переливания тромбоцитов даже в контексте предстоящего нейрохирургического вмешательства [117].
- Не рекомендуется назначение рекомбинантного активированного фактора свертывания крови VII (Эптаког альфа [активированный])** (B02BD08) пациентам с гипертензивной внутримозговой гематомой без нарушения свертывания крови в связи с повышением риска тромбоэмболических осложнений [115].
Уровень убедительности рекомендаций А (уровень достоверности доказательств - 1)
- Не рекомендуется рутинное применение транексамовой кислоты** (B02AA02) из-за отсутствия определенности между балансом клинических преимуществ (улучшением функционального исхода, летальностью) и побочными эффектами транексамовой кислоты** (B02AA02) [115].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
Комментарии:
Возможно назначение #транексамовой кислоты** (B02AA02) (1 г в/в болюсно + 1 г в/в инфузия за 8 ч) у пациентов с гипертензивной ВМГ в сроки до 4,5 часов от начала симптомов и высоким риском роста гематомы с целью уменьшения окончательного объема ВМГ [121]. Высокий риск роста гематомы в дополнении к сроку до 4,5 часов от начала симптомов ассоциирован со следующими нейровизуализационными признаками КТ/КТА:
1. Лобарные кровоизлияния (особенно связанные с амилоидной ангиопатией)
2. Объем гематомы > 30 мл или с быстрым увеличением (> 33% или > 6 мл за 24 часа)
3. Особые признаки:
- "Spot sign" (признак "пятна") - экстравазация контрастного средства в виде точечных очагов внутри гематомы на КТА.
- "Black hole sign" ("черная дыра") - гиподенсный участок внутри гиперденсной гематомы на нативной КТ.
- "Blend sign" ("признак смешения") - сочетание участков разной плотности в гематоме.
- "Island sign" ("островковый признак") - мелкие отдельные очаги кровоизлияния вокруг основной гематомы.
Транексамовая кислота** (B02AA02) при спонтанном внутримозговом кровоизлиянии по сравнению с плацебо или открытым контролем не оказывала статистически значимого влияния на смертность или зависимость от посторонней помощи на 90-й день, а также на смертность к 90-му дню; однако транексамовая кислота** (B02AA02) в некоторой степени предотвращала рост гематомы через 24 часа по сравнению с плацебо или открытым контролем [121].
Коррекция отека головного мозга и повышенного внутричерепного давления у пациентов с гипертензивной внутримозговой гематомой
На течение гипертензивной ВМГ значимое влияние оказывает формирование отека мозга, которое может сопровождаться и повышением ВЧД. Это требует принятия мер по их коррекции.
- Рекомендуется у пациентов с гипертензивной внутримозговой гематомой при ее объеме ![]() 15 мл, наличии признаков повышения внутричерепного давления > 16 - 18 мм рт. ст. и отека головного мозга назначение растворов с осмодиуретическим действием (15% #маннитол** ((B05BC) 1,5 - 2,0 г/кг массы тела, который вводят инфузионно в течение 30 минут или 10% раствор натрия хлорида (Стерильные лекарственные препараты аптечного изготовления, ОФС.1.8.0006), разовая доза 20 - 50 мл в центральную вену [122 - 125]. Необходимо контролировать осмолярность плазмы крови, при осмолярности более 320 мОсм/л проведение терапии неэффективно [126].
15 мл, наличии признаков повышения внутричерепного давления > 16 - 18 мм рт. ст. и отека головного мозга назначение растворов с осмодиуретическим действием (15% #маннитол** ((B05BC) 1,5 - 2,0 г/кг массы тела, который вводят инфузионно в течение 30 минут или 10% раствор натрия хлорида (Стерильные лекарственные препараты аптечного изготовления, ОФС.1.8.0006), разовая доза 20 - 50 мл в центральную вену [122 - 125]. Необходимо контролировать осмолярность плазмы крови, при осмолярности более 320 мОсм/л проведение терапии неэффективно [126].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
Комментарии: влияние #маннитола** (B05BC) изучено в субанализе когорты пациентов INTERACT2, включившей 2839 пациентов [124]. Его назначение было безопасным, и частота возникновения нежелательных явлений в подгруппе пациентов, получавших #маннитол** (B05BC), не превышала их частоту у пациентов, не получавших #маннитол** (B05BC).
- Не рекомендуется назначение дексаметазона** (H02AB02) при ВМГ в связи с отсутствием доказанного эффекта и повышением риска летального исхода [127].
Уровень убедительности рекомендаций B (уровень достоверности доказательств - 2)
Профилактика тромбоза вен нижних конечностей и тромбоэмболических осложнений
Одним из важных факторов, влияющих на течение острого периода гипертензивной ВМГ, является риск развития тромбоза глубоких вен нижних конечностей и тромбоэмболических осложнений (ВТЭО), который особенно высок у пациентов с выраженными двигательными нарушениями или не являющихся мобильными вследствие иных причин. Особую сложность представляет профилактика ВТЭО при гипертензивной ВМГ, что требует оценки не только непосредственно риска ВТЭО, но и риска повторного кровотечения [128].
- Рекомендуется у пациентов с гипертензивной внутримозговой гематомой, которые имеют риск развития ВТЭО, профилактика тромбоза глубоких вен нижних конечностей, начиная со дня поступления методом перемежающейся пневмокомпрессии и/или использование компрессионных изделий медицинского назначения (чулков) при отсутствии противопоказаний для их применения [129].
Уровень убедительности рекомендаций B (уровень достоверности доказательств - 2)
Комментарии: применение только эластической компрессии нижних конечностей не уменьшает риски тромбоза глубоких вен нижних конечностей и не улучшает исходы заболевания [129]. Проспективное рандомизированное исследование, сравнивающее перемежающуюся пневмокомпрессию в комбинации с компрессионными изделиями медицинского назначения (чулками) и использование только последних, показало значительное снижение риска тромбоза глубоких вен [130]. Однако использование компрессионных изделий медицинского назначения (чулков) может вызывать повреждение кожи [131].
Перед началом перемежающейся пневмокомпрессии обоснованным является проведение дуплексного сканирования вен нижних конечностей для исключения уже имеющегося тромбоза глубоких вен нижних конечностей.
- Рекомендуется профилактическое назначение низкомолекулярных гепаринов (B01AB Группа гепарина) или #нефракционированного гепарина натрия** (B01AB01) подкожно (5000 анти-Ха МЕ каждые 8 часов или 2500 - 5000 анти-Ха МЕ каждые 12 часов) в период не ранее 48 часов после появления клиники гипертензивной внутримозговой гематомы при отсутствии признаков продолжающегося роста гематомы и коагулопатии [126, 130, 132, 133].
Уровень убедительности рекомендаций B (уровень достоверности доказательств - 1)
Комментарии: Рекомендованная доза #эноксапарина натрия** (B01AB05) 40 мг однократно в сутки подкожно. Дозы введения рассчитываются индивидуально на основании массы тела пациента. Согласно данным метаанализа, включившего 1000 пациентов ГИ из 4 исследований, рандомизированными из которых были 2 [133], раннее применение препаратов #эноксапарина натрия** (B01AB05) или #гепарина натрия** (B01AB01) (спустя 1 - 6 дней после поступления) было связано со статистически значимым снижением частоты тромбоэмболии легочной артерии и незначительным увеличением объема гематомы. Требуется индивидуальный подход с учетом хирургического вмешательства и клинического состояния пациента с обязательным мониторингом гемостаза и динамики неврологического статуса.
Возобновление приема антитромботических средств пациентам с развившейся гипертензивной внутримозговой гематомой
У пациентов, перенесших гипертензивную ВМГ, получавших антиагрегантную/антикоагулянтную терапию по поводу других заболеваний или для профилактики сердечно-сосудистой, цереброваскулярной патологии и имеющих показания для назначения соответствующей терапии, следует рассматривать в качестве кандидатов для возобновления соответствующей терапии [134].
- Рекомендуется возобновление антиагрегантной терапии (B01AC) у пациентов, перенесших гипертензивную внутримозговую гематому, при сохранении показаний к данной терапии на фоне сопутствующих заболеваний [134, 135].
Уровень убедительности рекомендаций B (уровень достоверности доказательств - 2)
Комментарии: срок возобновления должен определяться индивидуально в каждом случае [134]. Существующих данных недостаточно, чтобы однозначно определить оптимальные сроки возобновления антиагрегантной терапии. При их приеме риск возникновения повторных кровоизлияний был значительно меньше, чем положительный эффект от вторичной профилактики острых нарушений мозгового кровообращения.
- Рекомендуется у пациентов, перенесших гипертензивную внутримозговую гематому и имеющих в долгосрочной перспективе очень высокий риск ВТЭО, проводить возобновление приема антагонистов витамина К (B01AA) на индивидуальной основе с учетом оценки потенциальной пользы и риска повторного кровотечения [136 - 140].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
Комментарии: оптимальные сроки возобновления приема антитромботических средств не известны. В настоящее время проводятся клинические исследования, направленные на установление групп пациентов, у которых будет возможно возобновление приема антитромботических средств.
3.1.2 Хирургическое лечение пациентов с гипертензивной внутримозговой гематомой
Хирургическое лечение направлено на удаление ВМГ, устранение компрессии, дислокации головного мозга, разрешение обструктивной гидроцефалии [139, 141 - 145].
- Рекомендуется хирургическое лечение по поводу удаления внутримозговой гематомы с учетом условий для хирургического лечения, наличия показаний и отсутствии противопоказаний, сроков и методов [139, 141 - 145].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
Условия для хирургического лечения геморрагического инсульта
Для выполнения хирургических вмешательств операционная должна быть укомплектована в соответствие с действующими Приказами. Минимально инвазивные операции, такие как:
пункционная аспирация (A16.23.015 Пункция гематомы головного мозга, A16.23.017 Удаление гематомы головного мозга),
локальный фибринолиз (A16.23.017.001 Закрытое дренирование гематомы головного мозга при помощи фибринолитических препаратов),
эндоскопическая аспирация (A16.23.015 Пункция гематомы головного мозга, A16.23.017 Удаление гематомы головного мозга)
могут быть выполнены под локорегионарной анестезией (B01.003.004.002 Проводниковая анестезия).
Факторами риска неблагоприятного исхода при хирургическом лечении являются [8, 142, 143]:
- снижение бодрствования до сопора и ниже;
- объем внутримозговой гематомы более 50 см3;
- массивное вентрикулярное кровоизлияние;
- поперечная дислокация 10 мм и более;
- деформация цистерн ствола мозга;
- рецидив кровоизлияния.
Показания и противопоказания к хирургическому лечению
- Рекомендуется удаление путаменальных и субкортикальных гематом (A16.23.017.009 Удаление гематом глубинных структур головного мозга, A16.23.017.007 Удаление гематом больших полушарий головного мозга) объемом более 30 см3, вызывающих выраженный неврологический дефицит и/или дислокацию мозга (смещению срединных структур более 5 мм или деформации цистерн ствола мозга) [8, 147 - 151]
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
- Рекомендуется удаление гематомы мозжечка (A16.23.017.008 Удаление гематом мозжечка) объемом более 10 - 15 см3, диаметром более 3 см, вызывающей компрессию ствола мозга и/или окклюзионную гидроцефалию [8, 147 - 151]
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
- Не рекомендуется выполнять только наружное вентрикулярное дренирование без удаления гематомы мозжечка ввиду возможного увеличения аксиальной дислокации мозга [8, 143 - 145].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
- Рекомендуется хирургическое лечение при кровоизлиянии в таламус, сопровождающимся гемотампонадой желудочков и/или окклюзионной гидроцефалией [8, 148, 149].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
Комментарии: Целесообразность хирургического удаления гипертензивных гематом таламуса объемом более 10 см3 и ствола, сопровождающихся грубым неврологическим дефицитом, обсуждается, и устоявшегося мнения на этот счет среди врачей-нейрохирургов пока нет [141].
- Не рекомендуется хирургическое вмешательство при угнетении бодрствования до комы (по шкале комы Глазго - 7 баллов и менее) [8, 147 - 151]
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
Комментарии: У больных в коме исходы не зависят от метода лечения (интенсивной терапии или хирургического вмешательства) [146].
- Не рекомендуется проведение операции на фоне выраженной артериальной гипертензии (систолическом АД более 200 мм рт. ст.) [142, 144].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
Комментарии: Относительным противопоказанием к операции является наличие тяжелой соматической патологии (сахарный диабет, почечная, печеночная, сердечно-сосудистая и легочная патология в стадии суб- и декомпенсации, коагулопатии, сепсис) [8].
Выбор сроков хирургического лечения
- Рекомендуется проводить экстренные операции пациентам с внутримозговой гематомой мозжечка объемом более 15 см3, учитывая опасность компрессии ствола мозга и окклюзионной гидроцефалии [147, 148].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
- Рекомендуется проводить экстренные операции пациентам с внутримозговой гематомой больших полушарий (субкортикальной и путаменальной локализации) при угнетении сознания до глубокого оглушения и сопора (по шкале комы Глазго - 9 - 12 баллов) ввиду развития дислокационного синдрома [147, 148].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
- Рекомендуется проведение операции в срочном порядке (в течение 72 часов от момента поступления в стационар) пациентам с внутримозговой гематомой больших полушарий при уровне сознания 13 - 14 баллов по шкале комы Глазго [146, 147, 156, 157].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
Комментарии: При компенсированном состоянии пациента, нормальном бодрствовании или его снижении не глубже оглушения, отсутствии признаков нарастания компрессии мозга, но высоких цифрах артериального давления (систолическое более 200 мм рт. ст.) во избежание трудностей с интраоперационным гемостазом и послеоперационного рецидива гематомы операцию целесообразно отложить до снижения и стабилизации АД. В ряде случаев на протяжении первых суток гематома может продолжать формироваться и склонна к рецидивам, поэтому проведение хирургического удаления гематом в первые 24 часа связано с повышенным риском рецидива кровоизлияния [144, 151, 152].
Методы хирургического лечения
Некоторые операции могут быть дополнены локальным фибринолизом (A16.23.017.001 Закрытое дренирование гематомы головного мозга при помощи фибринолитических препаратов). В случае его использования с учетом применения препаратов офф-лейбл необходимо проведение врачебной комиссии с указанием о необходимости данного вида лечения по жизненным показаниям. Наиболее изученным в РФ препаратом для локального фибринолиза является - рекомбинантная #проурокиназа**. Средняя доза на однократное введение - 50 000 МЕ, время экспозиции - 6 - 12 часов [160, 161].
- Рекомендуется миниинвазивное удаление путаменальных и мозжечковых гематом (A16.23.017.009 Удаление гематом глубинных структур головного мозга, A16.23.017.008 Удаление гематом мозжечка) (с использованием методов эндоскопической аспирации - A16.23.015 Удаление гематомы головного мозга, локального фибринолиза - A16.23.017.001 Закрытое дренирование гематомы головного мозга при помощи фибринолитических препаратов, с использованием стереотаксической навигации - A16.23.023 Стереотаксические операции на головном мозге в случае отсутствия выраженного дислокационного синдрома, угрожающей жизни дислокации головного мозга по данным компьютерной томографии головного мозга [8, 147 - 151, 161].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
Комментарии:
При ВМГ базальных ядер объемом более 25 - 30 см3 хирургическое вмешательство позволяет уменьшить летальность и улучшить функциональные исход [143, 155, 156].
Операция может быть дополнена локальным фибринолизом (A16.23.017.001 Закрытое дренирование гематомы головного мозга при помощи фибринолитических препаратов) [8, 147, 161].
- Рекомендуется при выполнении экстренного хирургического вмешательства микрохирургическое удаление внутримозговой гематомы у пациентов с субкортикальными, путаменальными и мозжечковыми внутримозговыми гематомами с клиникой быстрого нарастания дислокационного синдрома ввиду наибольшего риска рецидива кровоизлияния в первые 24 часа и в необходимости достижения надежного хирургического гемостаза [149, 150, 157].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
Комментарии: При субкортикальных кровоизлияниях необходима микрохирургическая ревизия полости гематомы для удаления возможной ангиографически негативной мальформации, частота встречаемости которых может достигать 30% [157, 158].
- Рекомендуется миниинвазивное удаление субкортикальных гематом (A16.23.017.007 Удаление гематом больших полушарий головного мозга) с использованием методов эндоскопической аспирации - A16.23.015 Удаление гематомы головного мозга, локального фибринолиза - A16.23.017.001 Закрытое дренирование гематомы головного мозга при помощи фибринолитических препаратов, с использованием стереотаксической навигации - A16.23.023 Стереотаксические операции на головном мозге при наличии у пациента тяжелой соматической патологии [8, 148, 149, 161].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
Комментарии: Обязательным условием в этом случае является проведение церебральной ангиографии тотальной селективной и исключение сосудистой мальформации.
При ВМГ субкортикальной локализации более 25 - 30 см3 хирургическое вмешательство позволяет уменьшить летальность и улучшить функциональные исходы [142, 153, 159].
Операция может быть дополнена локальным фибринолизом (A16.23.017.001 Закрытое дренирование гематомы головного мозга при помощи фибринолитических препаратов).
- Рекомендуется проведение наружного дренирования желудочков или эндоскопической тривентрикулостомии пациентам с гематомой мозжечка малого размера (менее 10 см3), сопровождающейся смещением и/или окклюзией IV желудочка или сильвиева водопровода с развитием окклюзионной гидроцефалии [8, 148, 149, 161, 168]
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
- Рекомендуется мини-инвазивное удаление внутримозговой гематомы путем эндоскопической или пункционной аспирации, при необходимости (при признаках окклюзионной гидроцефалии) дополненные ликворошунтирующей операцией (эндоскопическая вентрикулостомия III желудочка (тривентрикулостомия) или установка наружного вентрикулярного дренажа) при объеме внутримозговой гематомы мозжечка 10 - 20 см3, уровне сознания пациента 13 - 14 баллов по шкале комы Глазго [8, 147 - 149].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
- Рекомендуется микрохирургическое удаление внутримозговой гематомы и декомпрессивная краниэктомия задней черепной ямки, дополненные ликворошунтирующей операцией (эндоскопическая вентрикулостомия III желудочка (тривентрикулостомия) или установка наружного вентрикулярного дренажа) при объеме внутримозговой гематомы мозжечка более 20 см3, уровне сознания пациента 8 - 12 баллов по шкале комы Глазго [8, 147 - 149].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
- Рекомендуется использование нейронавигации при проведении пункционной аспирации гематомы при удалении путаменальных, мозжечковых, вентрикулярных кровоизлияний [14, 145, 153, 154, 160 - 164].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
- Рекомендуется проведение пункционной аспирации и локального фибринолиза при путаменальных, таламических или смешанных внутримозговых гематом объемом 30 - 45 см3 сопровождающихся выраженной очаговой неврологической симптоматикой [159, 160].
Уровень убедительности рекомендаций B (уровень достоверности доказательств - 4)
- Не рекомендуется проведение локального фибринолиза при позиционировании конца катетера вне центра внутримозговой гематомы [160, 161].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
- Рекомендуется наружное дренирование боковых желудочков с проведением локального фибринолиза сгустков крови или их эндоскопическое удаление (при условии исключения сосудистой аномалии) при массивном кровоизлиянии в боковые желудочки [146, 159, 160, 165].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
Комментарии: При полной тампонаде обоих боковых желудочков рекомендуется установка двух наружный вентрикулярных дренажей в передние рога и введение в каждый из желудочков дозы 50 000 ME рекомбинантной #проурокиназы**.
- Рекомендуется у пациентов с окклюзионной гидроцефалией проводить эндоскопическую тривентрикулостомию и/или наружное дренирование до регресса окклюзионной гидроцефалии и восстановления проходимости желудочковой системы [4, 160].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
- Рекомендуется дополнять установкой датчика внутричерепного давления пациентам с тяжелым состоянием (снижение бодрствования до сопора, выраженная соматическая патология), которое может потребовать длительной интенсивной терапии в послеоперационном периоде, вмешательство на гематоме [148, 149].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
- Не рекомендуется проведение открытого удаления путаменальных гематом в сочетании с первичной декомпрессивной трепанацией черепа, так как это сопряжено с высокими рисками плохих исходов [173].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
- Рекомендуется отсроченная (вторичная) декомпрессивная трепанация черепа при субкортикальных и путаменальных гематомах у больных при нарастании отека и поперечной дислокации головного мозга без рецидива кровоизлияния [173].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
3.1.3 Послеоперационное ведение пациентов с гипертензивной внутримозговой гематомой
После операции пациент находится в отделении нейрореанимации/ПИТ/ОРИТ (см. раздел 3.1.1. Интенсивная терапия пациентов с гипертензивной внутримозговой гематомой)
- Рекомендуется выполнение компьютерной томографии головного мозга в течение 24 часов после хирургического лечение (контрольное исследование); каждые 24 часа в период проведения локального фибринолиза (A16.23.017.001 Закрытое дренирование гематомы головного мозга при помощи фибринолитических препаратов); на 7 и 21 сутки после удаления дренажа, а также экстренно при ухудшении неврологического статуса [160, 161].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
- Рекомендуется проведение мониторирования внутричерепного давления до его стойкой нормализации (менее 15 мм рт. ст.) для ВЧД-ориентированной интенсивной терапии [8, 37].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
3.2 Лечение пациентов с аневризматическим субарахноидальным кровоизлиянием
3.2.1 Интенсивная терапия пациентов с аневризматическим субарахноидальным кровоизлиянием
Ведение и лечение пациентов с субарахноидальным кровоизлиянием до операции
Задачами консервативного лечения пациентов с САК в предоперационном периоде являются стабилизация состояния пациентов, профилактика рецидива САК, профилактика и лечение сосудистого спазма и ишемии мозга.
Общие рекомендации
- Рекомендуется всем пациентам в остром периоде аСАК постельный режим с целью минимизации колебаний системного артериального давления и снижения риска рецидива САК [174].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
- Рекомендуется всем пациентам в остром периоде аСАК анальгезия и/или седация при проведении всех манипуляций (НПВС (M01A), парацетамол** (N02BE01) или трамадол** (N02AX02) для снижения выраженности головной боли и болей другой локализации [17, 168].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
- Рекомендуется всем пациентам в остром периоде аСАК поддержание нормотермии < 38,0 [175].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
Комментарии: При упорной лихорадке необходимо исключить инфекционный генез. Лихорадка должна купироваться фармакологически или с применением систем внешнего охлаждения.
- Рекомендуется всем пациентам в остром периоде аСАК, находящимся в состоянии оглушения, сопора или комы, установка желудочного зонда из-за угрозы возможной аспирации и мочевого катетера для контроля темпа диуреза [174].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
- Рекомендуется всем пациентам в остром периоде аСАК назначение слабительных средств в клизмах для профилактики подъема внутричерепного давления и рецидива САК [174].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
- Рекомендуется всем пациентам в остром периоде аСАК, отмена антитромботических средств [116].
Уровень убедительности рекомендаций B (уровень достоверности доказательств - 3)
- Рекомендуется с момента поступления пациентов в остром периоде аСАК в стационар проведение перемежающейся пневмокомпрессии или использование компрессионных изделий медицинского назначения (чулков) для профилактики тромбоза глубоких вен и тромбоэмболических осложнений [128].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
- Рекомендуется всем пациентам в остром периоде аСАК поддержание уровня гликемии <10 ммоль/л [17, 168].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
- Рекомендуется рассмотреть необходимость профилактического применения противоэпилептических препаратов (#леветирацетама** (N03AX14) в/в 500 мг 2 раза в сутки; или #вальпроевой кислоты** (N03AG01) в/в 3 - 41,5 мг/кг/сут) у пациентов с одним из следующих признаков: субарахноидальное кровоизлияние из аневризмы средней мозговой артерии; тяжесть состояния по шкале Hunt-Hess 3 - 5; рентгенологическая степень по шкале Fisher III-IV; очаг кровоизлияния, прилежащий к корковым структурам; гидроцефалия [177, 178].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4) - для #вальпроевой кислоты**
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5) - для #леветирацетама**
Комментарии: длительность применения не более 7 суток.
- Рекомендуется назначение противоэпилептических препаратов пациентов с развившимися эпиприступами в остром периоде (леветирацетам** (N03AX14) в/в 500 - 1000 мг х 2 р/сут; или вальпроевая кислота** (N03AG01) в/в 20 - 30 мг/кг/сут) [178].
Уровень убедительности рекомендаций А (уровень достоверности доказательств - 1)
Комментарии: Режим дозирования:
низкоинтенсивная терапия: монотерапия: леветирацетам** в дозе <2000 мг/сут (<1000 мг/сут при нарушении функции почек), вальпроевая кислота** в дозе ![]() 15 мг/кг/сут или средний уровень <75 мкг/мл;
15 мг/кг/сут или средний уровень <75 мкг/мл;
высокоинтенсивная терапия: более 48 часов леветирацетама** в дозе ![]() 2000 мг/сут (
2000 мг/сут (![]() 1000 мг/сут при нарушении функции почек), вальпроевая кислота** в дозе > 15 мг/кг/сут или средний уровень
1000 мг/сут при нарушении функции почек), вальпроевая кислота** в дозе > 15 мг/кг/сут или средний уровень ![]() 75 мкг/мл;
75 мкг/мл;
длительность применения не более 7 суток.
- Рекомендуется провести электроэнцефалографию с видеомониторингом в течение 24 - 48 часов пациентам с устойчивым снижением уровня бодрствования или нарушением сознания для исключения бессудорожных приступов, если появление общемозговой симптоматики нельзя объяснить другими причинами [27].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
Профилактика повторного кровоизлияния
- Рекомендуется хирургическое выключение аневризмы из кровотока как основной метод профилактики повторного кровоизлияния [16, 17, 168].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
- Не рекомендуется применение антифибринолитической терапии (B02AA) для рутинного лечения пациентов с субарахноидальным кровоизлиянием [27].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
Профилактика дыхательных нарушений
- Рекомендуется обеспечение SpO2 ![]() 92 с дополнительной кислородной поддержкой при необходимости [27] [173].
92 с дополнительной кислородной поддержкой при необходимости [27] [173].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
- Рекомендуется интубация трахеи и перевод пациента на ИВЛ при нарастании дыхательной недостаточности на фоне инсуфляции О2 или развития неврологического ухудшения, требующего протекции дыхательных путей [123, 174].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
Нормализация и стабилизации показателей системной гемодинамики.
- Рекомендуется поддерживать уровень систолического артериального давления (САД) в пределах < 160 мм рт. ст. [16, 27].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
- Рекомендуется для купирования эпизодов артериальной гипертензии использовать нимодипин** (C08CA06) или урапидил** (C02CA06) в дозировках, соответствующих инструкции к применению; решение об одновременном назначении пероральных гипотензивных препаратов принимается индивидуально. [16, 17, 136] [181].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
- Рекомендуется при возникновении артериальной гипотензии проведение инфузионной терапии (B05BB). При неэффективности - инфузия коллоидных растворов (B05AA), симпатомиметических препаратов (C01CA) (норэпинефрин**) [27, 182, 183].
Уровень убедительности рекомендаций B (уровень достоверности доказательств - 2)
Профилактика церебрального вазоспазма и ишемии мозга
- Рекомендуется применение блокаторов кальциевых каналов: нимодипин** (C08CA06) в таблетированной форме по 60 мг 6 раз в сутки каждые 4 ч (максимальная доза 360 мг) per os или через назогастральный зонд в течение 21 дня [16, 17].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
Комментарии: При развитии у пациента артериальной гипотензии рассмотреть вопрос об отмене препарата.
Применение других блокаторов кальциевых каналов, как и иных способов их введения (в/в) не рекомендуется [27, 177].
3.2.2 Хирургическое лечение пациентов с аневризматическим субарахноидальным кровоизлиянием
Показания к операции (влияние состояния пациента)
- Рекомендуется хирургическое лечение по поводу разорвавшейся аневризмы в остром периоде кровоизлияния независимо от срока кровоизлияния пациентам с субарахноидальным кровоизлиянием при тяжести I - IV по Hunt-Hess [17, 178 - 181].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
- Рекомендуется проведение операции на аневризме головного мозга пациентам с субарахноидальным кровоизлиянием в остром периоде в течение первых суток после кровоизлияния при тяжести V по Hunt-Hess, при уровне сознания 8 баллов и более по Шкале комы Глазго, при наличии внутримозговой гематомы объемом 30 см3 и более [17, 178 - 181].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
- Не рекомендуется проведение операции на аневризме головного мозга у пациентов с субарахноидальным кровоизлиянием в остром периоде при крайне тяжелом состоянии и уровне сознания 7 баллов и менее по шкале комы Глазго [178 - 180, 182 - 185].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
Комментарии: в отдельных случаях решение о проведении операции у тяжелых пациентов принимается на основании врачебной комиссии.
Сроки операции
- Рекомендуется проводить операции в течение 72 часов с момента выявления разорвавшейся аневризмы головного мозга и/или в течение 24 часов с момента поступления пациента в стационар с наличием нейрохирургической службы при отсутствии противопоказаний [17, 168, 178 - 181].
Уровень убедительности рекомендаций B (уровень достоверности доказательств - 2)
Комментарии: у пациентов со сложными аневризмами (гигантскими, фузиформными, вертебробазилярной и параклиноидной локализации) на предоперационную подготовку может потребоваться более длительное время. При невозможности оказаний хирургической помощи на месте верификации диагноза показана транспортировка пациента в медицинские центры третьего уровня с возможностью нейрохирургической и эндоваскулярной помощью по неотложным показаниям.
Выбор метода хирургического лечения
Существуют 2 альтернативных метода лечения аневризм головного мозга - микрохирургический и эндоваскулярный. Выбор метода лечения зависит от технической оснащенности центра и степени развития каждой методики в нем [27, 186, 192 - 200].
- Рекомендуется проведение микрохирургической операции пациентам с аневризмами супраклиноидного отдела внутренней сонной артерии, перикаллезной артерии, передней соединительной артерии, средней мозговой артерии, задней нижней мозжечковой артерии [14, 16, 168, 194, 196].
Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1)
Комментарии: при невозможности по каким-либо причинам провести микрохирургическую операцию, следует рассмотреть возможность проведения эндоваскулярной операции.
- Рекомендуется проведение эндоваскулярной операции пациентам с аневризмами развилки и ствола базилярной артерии, устья верхней мозжечковой артерии, устья передней нижней мозжечковой артерии, задней нижней мозжечковой артерии, офтальмического и коммуникантного сегментов внутренней сонной артерии, интракраниального сегмента позвоночной артерии [14, 16, 168, 196].
Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1)
Комментарии: при невозможности по каким-либо причинам провести эндоваскулярную операцию, следует рассмотреть возможность проведения микрохирургической операции.
Операции у пациентов с множественными аневризмами
- Рекомендуется первоочередное выключение разорвавшейся аневризмы наиболее приемлемым (микрохирургическим или эндовазальным) способом [14, 16, 168].
Уровень убедительности рекомендаций B (уровень достоверности доказательств - 2)
Комментарии: Возможность выключения всех аневризм из кровотока за одно хирургическое вмешательство или в несколько этапов, в том числе, с комбинацией микрохирургических и эндовазальных вмешательств, решается индивидуально в каждом конкретном случае.
Прямые микрохирургические вмешательства на аневризме в остром периоде
- Рекомендуется микрохирургическое выключение аневризмы путем клипирования ее шейки или выключения несущей аневризму артерии при адекватном коллатеральном кровотоке [16, 168, 181, 197].
Уровень убедительности рекомендаций B (уровень достоверности доказательств - 2)
Комментарии: при выключении вместе с аневризмой несущей артерии решение о необходимости дополнительной реваскуляризирующей операции или вынужденной декомпрессивной трепанации черепа принимается оперирующим врачом в зависимости от конкретной ситуации.
- Рекомендуется все микрохирургические операции по поводу аневризмы головного мозга в остром периоде проводить под общим многокомпонентным эндотрахеальным наркозом [16, 197, 199].
Уровень убедительности рекомендаций B (уровень достоверности доказательств - 2)
- Рекомендуется в первую очередь выключать из кровотока аневризму головного мозга, ставшую источником кровоизлияния [14, 16, 168].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
- Рекомендуется по возможности также одномоментно выключать из кровотока все доступные из одного хирургического доступа сопутствующие аневризмы [14, 16, 168].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
Комментарии: возможность одномоментного микрохирургического выключения аневризм в остром периоде кровоизлияния определяется врачом-хирургом во время операции, принимая во внимание состояние головного мозга, выраженность кровоизлияния и т.д.
- Рекомендуется широкая латеральная супраорбитальная краниотомия при типичных аневризмах передних отделов вилизиева круга или другой доступ в зависимости от локализации аневризмы (передний межполушарный, срединный субокципитальный, ретросигмовидный) [16, 181] [173].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
- Не рекомендуется рутинное вскрытие конечной пластинки (lamina terminalis) как меры профилактики гидроцефалии при микрохирургической операции по поводу аневризмы головного мозга [206].
Уровень убедительности рекомендаций B (уровень достоверности доказательств - 3)
Контроль эффективности микрохирургической операции
- Рекомендуется после окончательного наложения клипсов вскрыть купол аневризмы [167, 181] [173].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
Комментарии: Отсутствие кровотечения будет свидетельствовать о полном выключении дна аневризмы.
- Рекомендуется интраоперационный контроль проходимости несущих аневризму артерий и функционально значимых ветвей посредством визуальной оценки области клипирования (через микроскоп и/или эндоскоп), ультразвукового исследования кровотока в артериях головного мозга или с помощью флюоресцентной видеоангиографии [168, 181, 200].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
Комментарии: в послеоперационном периоде после микрохирургического выключения аневризмы из кровотока для оценки состояния пришеечной части и подтверждения радикальности ее клипирования проводят контрольные ангиографические исследования (КТА или ЦАГ) [16, 181, 201]. КТА - малоинвазивный метод исследования, с меньшей лучевой нагрузкой, для ее выполнения необходимо оснащение учреждения компьютерным томографом не менее 64 срезов. ЦАГ - более инвазивный метод - показан в случае невозможности выполнить КТ-ангиографию [209]. При технической возможности рекомендуется выполнять КТА с опцией подавления артефактов от металла для минимизации артефактов от клипса с целью точной визуализации артерий в зоне клипса [210].
Интраоперационная санация базальных цистерн
- Рекомендуется проведение комбинированной санации базальных цистерн от крови с использованием цистернального дренирования в сочетании с интратекальным введением фибринолитического препарата (АТХ "B01AD Ферментные препараты") у пациентов с массивными формами кровоизлияния (III - IV ст. по модифицированной шкале Fisher, более 20 б. по Шкале Hijdra), оперированных микрохирургическим способом в первые 72 часа с момента кровоизлияния из аневризмы [211 - 214]
Уровень убедительности рекомендаций B (уровень достоверности доказательств - 1)
Комментарии:
модифицированная шкала Fisher - см. приложение Г2;
шкала Hijdra - см. приложение Г6;
с учетом применения препаратов офф-лейбл необходимо проведение врачебной комиссии с указанием о необходимости данного вида лечения по жизненным показаниям!
- Не рекомендуется интратекальное введение фибринолитика (АТХ B01AD Ферментные препараты) при неполном выключении разорвавшейся аневризмы, наличии других не выключенных из кровотока аневризм, индивидуальной непереносимости (гиперчувствительность) к фибринолитическим препаратам (АТХ B01AD Ферментные препараты) [211].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
Комментарии: при интраоперационном введении фибринолитика (АТХ B01AD Ферментные препараты) процедуру следует выполнять после выключения разорвавшейся аневризмы из кровотока. Следует осуществлять визуальный контроль состоятельности гемостаза в конце микрохирургического этапа.
- Рекомендуется при интратекальном применении фибринолитика (АТХ B01AD Ферментные препараты) введение #алтеплазы** в дозировке 1 - 5 мг [212].
Уровень убедительности рекомендаций B (уровень достоверности доказательств - 2)
- Рекомендуется при интратекальном применении фибринолитика (АТХ B01AD Ферментные препараты) введение #рекомбинантного белка, содержащего аминокислотную последовательность стафилокиназы** в дозировке 1 - 2 мг [211].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
Комментарии: при интраоперационном орошении базальных цистерн фибринолитический препарат (АТХ B01AD Ферментные препараты) следует развести физиологическим раствором натрия хлорида** в объеме 10 мл. При послеоперационном введении фибринолитика (АТХ B01AD Ферментные препараты) в цистернальный дренаж следует развести физиологическим раствором натрия хлорида** в объеме 5 мл.
- Рекомендуется следить за герметичностью и стерильностью цистернальной дренажной системы [211].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
- Рекомендуется ежедневный контроль анализа СМЖ из цистернального дренажа [211].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
Комментарии: цистернальное дренирование целесообразно прекратить при снижении показателя эритроцитов в клиническом анализе СМЖ ниже 10000 кл в 1 мкл
Эндоваскулярная операция
- Рекомендуется в первую очередь окклюзировать аневризму, ставшую источником кровоизлияния [180, 208, 209].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
- Рекомендуется по возможности также одномоментно окклюзировать сопутствующие аневризмы с высоким риском разрыва (неровные формы аневризматического мешка, дочерние расширения - дивертикулы) [216 - 218].
Уровень убедительности рекомендаций B (уровень достоверности доказательств - 2)
- Рекомендуется проводить все эндоваскулярные операции по поводу аневризмы головного мозга в остром периоде под общим многокомпонентным эндотрахеальным наркозом [16, 197, 198].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
- Рекомендуется стремиться к полному выключению аневризмы из кровотока (I степень по классификации Raymond Roy). В случае невозможности тотальной окклюзии без риска закрытия несущей артерии следует остановиться на субтотальном выключении аневризмы из кровотока (II степень по классификации Raymond Roy) с последующим радикальным лечением в холодном периоде [212, 213, 222].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
Комментарии:
Оценка проводится по классификации Raymond Roy (см. приложение 19) [221].
Неполное выключение аневризмы из кровотока (II-III степень по классификации Raymond Roy) считается достаточным при отсутствии контрастирования предполагаемого места разрыва аневризмы (купол аневризмы, дивертикулы) и допустимым при отсутствии необходимых расходных материалов в медицинском учреждении, куда был госпитализирован пациент. Повторная более полная эмболизация проводится в холодном периоде. При сохранении высокого риска повторного разрыва пациенту показан перевод в специализированный федеральный центр.
- Рекомендуется окклюзия полости аневризмы микроспиралями эндоваскулярными для эмболизации в остром периоде кровоизлияния - (A16.12.041.002) [16, 179, 196, 223].
Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1)
Комментарии: Баллон-ассистенцию (или поддерживающую эндоваскулярную окклюзию сосуда с помощью баллона - A16.12.041.003 согласно номенклатуре МУ) следует использовать при невозможности добиться устойчивого положения микрокатетера сосудистого в аневризме, сложности формирования плотного комплекса микроспиралей эндоваскулярных для эмболизацции в аневризме, необходимости проведения ангиопластики церебральных сосудов, высоком риске интраоперационного разрыва аневризмы. Возможно использование альтернативных методик, позволяющих сформировать устойчивый комплекс микроспиралей эндоваскулярных для эмболизацции в аневризме: двухкатетерная техника и использование временных ремоделирующих устройств. Возможна деконструкция несущей артерии при условии адекватного коллатерального кровотока [194, 222 - 224].
- Не рекомендуется рутинное использование стент-ассистенции (или трансартериальной окклюзии полости аневризмы с помощью микроспиралей эндоваскулярных для эмболизации при поддержке стента (A16.12.041.004) (стент для сосудов головного мозга металлический непокрытый***) в остром периоде разрыва аневризмы [225 - 227].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
Комментарии: использование ассистирующего стента для сосудов головного мозга металлического непокрытого*** в остром периоде разрыва аневризмы в медицинских центрах третьего уровня при условии полного устранения всех возможных источников интракраниального кровоизлияния и отсутствии необходимости открытого вмешательства. Имплантация при этом должна проводится на фоне в/в введения ингибиторов гликопротеиновых IIb/IIIа-рецепторов (АТХ B01AC Антиагреганты, кроме гепарина) с последующим переводом на пероральные антиагреганты, кроме гепарина, после операции. Отмена IIb/IIIа блокаторов (АТХ B01AC Антиагреганты, кроме гепарина) допускается не ранее чем через 2 - 4 часа после приема двойной антиагрегантной терапии [225 - 227].
Контроль эффективности эндоваскулярной операции
- Рекомендуется проведение ангиографического исследования (магнитно-резонансная ангиография интракраниальных сосудов или церебральная ангиография тотальная селективная) через 3 - 6 месяцев после операции для исключения реканализации аневризмы [16, 188, 201].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
Комментарии: в случае наличия предпосылок ранней жизнеугрожающей реканализации пролеченной аневризмы возможно проведение контрольного обследования в ближайшее время.
МРА интракраниальных артерий - неинвазивный метод исследования, не требующий введения контрастного средства, для его выполнения необходимо оснащение учреждения магнитно-резонансным томографом не менее 1,5 Тесла.
ЦАГ - более инвазивный метод - показан в случае невозможности выполнить МРА [228].
Другие хирургические вмешательства в остром периоде субарахноидального кровоизлияния
Установка наружного вентрикулярного дренажа
- Рекомендуется установка наружного вентрикулярного дренажа (А16.23.001 Пункция желудочка головного мозга, A16.23.047 Дренирование боковых желудочков головного мозга наружное) (Система нейрохирургическая для наружного дренирования, дренирования и мониторинга спинномозговой жидкости) всем пациентам с острой гидроцефалией и при наличии показаний (контроль внутричерепного давления, купирование внутричерепной гипертензии) у других пациентов с субарахноидальным кровоизлиянием [16, 222 - 226].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
Комментарии: Наружный вентрикулярный дренаж (НВД) (Система нейрохирургическая для наружного дренирования, дренирования и мониторинга спинномозговой жидкости) устанавливается из стандартной точки Кохера в контралатеральное по отношению к основному хирургическому доступу полушарие. Желательно устанавливать НВД (Система нейрохирургическая для наружного дренирования, дренирования и мониторинга спинномозговой жидкости) в одну операцию, как первый этап перед краниотомией и клипированием аневризмы.
В случае эндоваскулярного вмешательства НВД (Система нейрохирургическая для наружного дренирования, дренирования и мониторинга спинномозговой жидкости) устанавливают в операционной сразу после окклюзии аневризмы до пробуждения пациента после наркоза.
Если при эндоваскулярной операции планируется стентирование и введение пациенту антиагрегантов, кроме гепарина, НВД (Система нейрохирургическая для наружного дренирования, дренирования и мониторинга спинномозговой жидкости) следует устанавливать перед вмешательством после вводного наркоза.
- Рекомендуется установка наружных вентрикулярных дренажей (A16.23.001 Пункция желудочка головного мозга, A16.23.047 Дренирование боковых желудочков головного мозга наружное) (Система нейрохирургическая для наружного дренирования, дренирования и мониторинга спинномозговой жидкости) в оба боковых желудочка пациентам с выраженным внутрижелудочковым кровоизлиянием (10 - 12 баллов по шкале Graeb) [164, 223, 225].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
- Рекомендуется однократное внутривенное введение антибактериального препарата системного действия перед установкой наружного вентрикулярного дренажа (A16.23.001 Пункция желудочка головного мозга, A16.23.047 Дренирование боковых желудочков головного мозга наружное) (Система нейрохирургическая для наружного дренирования, дренирования и мониторинга спинномозговой жидкости), если пациент не находится на системной терапии инфекционных осложнений другой локализации [233].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
Комментарии: антибактериальный препарат системного действия и доза устанавливаются внутренними протоколами, утвержденными в стационаре.
- Не рекомендуется использование антибактериальных препаратов системного действия с профилактической целью на весь период наружного вентрикулярного дренирования [233].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
- Рекомендуется следить за герметичностью и стерильностью дренажной системы [227, 228].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
- Рекомендуется производить манипуляции с системой для сбора спинномозговой жидкости как можно реже [233].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
- Не рекомендуется гипердренирование спинномозговой жидкости: верхняя точка дренажной трубки должна быть на 10 - 15 см выше наружного слухового прохода [222, 227, 230].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
- Рекомендуется местная обработка области установки НВД спиртсодержащими антисептическими растворами (D08AX Другие антисептики и дезинфицирующие средства) с одновременной заменой фиксирующей стерильной повязки не реже 1 раза в 2 - 3 дня [233].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
- Не рекомендуется проводить профилактических введений антисептиков (D08AX), антибактериальных препаратов системного действия (J01) в наружный вентрикулярный дренаж [227, 228, 230, 231].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
- Рекомендуется всем пациентам с установленным наружным вентрикулярным дренажем (Система нейрохирургическая для наружного дренирования, дренирования и мониторинга спинномозговой жидкости) проводить микробиологическое (культуральное) исследование спинномозговой жидкости на аэробные и факультативно-анаэробные микроорганизмы и/или молекулярно-биологическое исследование на условно-патогенные микроорганизмы, исследование уровня глюкозы, лактата в спинномозговой жидкости, общий (клинический) анализ спинномозговой жидкости не реже 1 раза в 3 дня или при наличии клинических показаний (гипертермии, повышения воспалительных маркеров в крови, появления менингеальных симптомов, развития раневой ликвореи и т.д.) [227, 229] [239].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
- Рекомендуется произвести одномоментное (без предварительного перекрытия на сутки) удаление наружного вентрикулярного дренажа (Система нейрохирургическая для наружного дренирования, дренирования и мониторинга спинномозговой жидкости) с герметичным ушиванием раневого канала [222, 227].
Уровень убедительности рекомендаций B (уровень достоверности доказательств - 4)
- Рекомендуется вентрикулоперитонеальное шунтирование у пациентов с выраженной хронической постгеморрагической гидроцефалией аневризматического генеза [240].
Уровень убедительности рекомендаций B (уровень достоверности доказательств - 2)
Декомпрессивная трепанация черепа
Выделяют первичную (выполняется в ходе операции клипирования аневризмы) и вторичную (выполняется отсрочено) декомпрессивную трепанацию черепа (ДТЧ).
- Рекомендуется первичная декомпрессивная трепанация черепа пациентам в остром периоде субарахноидального кровоизлияния при наличии одного из факторов: 1) Hunt-Hess V, 2) дислокация срединных структур более 5 мм, 3) внутримозговая гематома более 30 мл, 4) признаки острой ишемии у пациентов с массивным базальным субарахноидальным кровоизлиянием (Fisher III) на 4 - 8 сутки после кровоизлияния [15, 242, 244].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
Комментарии: при проведении декомпрессивной трепанации черепа соблюдать следующие хирургические параметры [15,242 - 244]:
ДТЧ выполняется со стороны полушария с наиболее выраженным отеком;
оптимальной является лобно-теменно-височная краниоэктомия;
размеры ДТЧ должны быть 12 - 15 см в переднезаднем направлении;
обязательна резекция чешуи височной кости до основания средней черепной ямки;
важным условием ДТЧ является пластика твердой мозговой оболочки (ТМО) с увеличением подоболочечного пространства для отекающего мозга, что достигается за счет вшивание фрагмента надкостницы или искусственных заменителей ТМО;
герметичное ушивание ТМО при ее пластике снижает риск послеоперационной ликвореи;
в ходе операции желательно не вскрывать лобную пазуху и воздухоносные ячейки височной кости и обеспечить надежный этапный и окончательный гемостаз.
Установка датчика для контроля внутричерепного давления
- Рекомендуется мониторирование внутричерепного давления всем пациентам после операции находящимся на продолженной мед. седации или в коме [120, 121, 181, 237].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
Анестезиологическое обеспечение операций в остром периоде аневризматического субарахноидального кровоизлияния
Цели наркоза при операциях на аневризмах головного мозга в остром периоде:
А. анестезия и анальгезия пациента во время операции;
Б. предотвращение повторного разрыва аневризмы на всех этапах операции до момента выключения аневризмы;
В. обеспечение релаксации мозга для облегчения хирургического вмешательства и уменьшения тракционного повреждения мозгового вещества;
Г. поддержание адекватной мозговой перфузии для профилактики ишемии мозга;
Д. профилактика послеоперационной боли, тошноты и рвоты.
Общие рекомендации
- Рекомендуется использование внутривенных препаратов для общей анестезии (пропофол** (N01AX10) 1 - 1,5 мг/кг для индукции и 4 - 5 мг/кг для поддержания анестезии) в комбинации с опиоидными анальгетиками (фентанил** (N01AH01) в соответствии с инструкцией) для индукции и поддержания анестезии [246 - 248] [249].
Уровень убедительности рекомендаций B (уровень достоверности доказательств - 2)
Комментарии: Внутривенные препараты для общей анестезии, в частности пропофол** (N01AX10), обеспечивают более низкий уровень ВЧД, что может реализоваться в меньшем напряжении ткани мозга и создании более благоприятных условий для работы врача-нейрохирурга. Кроме того, пропофол** (N01AX10) обладает противоэпилептической и противорвотной активностью [246 - 248].
- Рекомендуется поддержание интраоперационной нормотермии (с применением согревающих устройств) для обеспечения нормокоагуляции [241, 242, 250].
Уровень убедительности рекомендаций B (уровень достоверности доказательств - 2)
- Рекомендуется регионарная анестезия скальпа (в точках выхода чувствительной корешков тройничного нерва на поверхность черепа; по линии кожного разреза; в местах установки шипов фиксирующей скобы) с помощью длительно действующих местных анестетиков (N01B) для обеспечения стабильности периоперационной гемодинамики [240, 243, 244].
Уровень убедительности рекомендаций 4 (уровень достоверности доказательств - C)
- Рекомендуется периоперационная фармакологическая профилактика послеоперационной тошноты и рвоты [254].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
- Рекомендуется установка мочевого катетера всем пациентам при проведении операции в остром периоде аневризматического субарахноидального кровоизлияния для измерения почасового диуреза после индукции [246, 247, 256].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
- Рекомендуется для коррекции повышенного внутричерепного давления в/в введение гиперосмолярных препаратов (АТХ B05BC Растворы с осмодиуретическим действием) (15% маннитол** (B05BC01) в соответствии с инструкцией) [257]
Уровень убедительности рекомендаций B (уровень достоверности доказательств - 1)
Комментарии: предпочтительно вводить препараты в центральную вену, с высоким темпом (в течение 10 - 15 мин). Инфузию следует начинать в момент кожного разреза.
- Рекомендуется интраоперационное проведение ИВЛ, направленное на поддержание нормовентиляции, при обязательном капнографическом контроле (PaCO2 = 33 - 35 мм рт. ст.) [250, 251, 258].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
Комментарии: стабильный уровень PaCO2 обеспечивает стабильное кровенаполнение мозга и стабильное ВЧД, нормовентиляция оставляет резерв для возможного снижения ВЧД на основе гипервентиляции. Важно учитывать, что при нарушенной ауторегуляции мозгового кровотока в условиях вазоспазма у пациентов с тяжелым САК, даже незначительный подъем PaCO2 влечет за собой скачок ВЧД. По этой причине безвентялиционные периоды (при интубации или пробуждении) должны быть как можно короче.
- Рекомендуется интраоперационный гликемический контроль для предотвращения тяжелых гипергликемии и гипогликемии, ассоциированных с ухудшением клинического исхода [252, 253, 260].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
- Рекомендуется использование тромбоэластографии (при возможности ее выполнения) при подозрении на интраоперационные системные нарушения гемостаза [262].
Уровень убедительности рекомендаций B (уровень достоверности доказательств - 2)
Комментарии: Комментарии: при отсутствии возможности оценки тромбоэластографии (ТЭГ, РОТЕМ), состояние системы гемостаза может быть оценено по результатам определения активированного частичного тромбопластинового времени (АЧТВ), протромбинового времени, исследования уровня фибриногена в крови
- Рекомендуется пробуждение всех пациентов в остром периоде САК в отделении реанимации [255, 256, 264].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
- Рекомендуется раннее пробуждение и экстубация пациентам с Hunt-Hess I-II, у которых не было осложнений во время операции, для своевременной оценки неврологического статуса [246, 255, 263].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
Управление системной гемодинамикой
- Рекомендуется установка катетера венозного центрального (МУ 260000) пациентам с Hunt-Hess III - V, признаками вазоспазма (вне зависимости от тяжести состояния по Hunt-Hess), оперированным в 1 - 3 сутки субарахноидального кровоизлияния (вне зависимости от тяжести состояния по Hunt-Hess) [246, 255].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
- Рекомендуется прямое инвазивное непрерывное измерение АД в интраоперационном периоде, начатое до индукции анестезии (либо частое неинвазивное измерение АД на периферических артериях при невозможности установки артериальной линии), для профилактики и своевременной коррекции нестабильной гемодинамики [266].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
- Рекомендуется поддержание эуволемии (Hct > 30%) в течение всей операции [258, 260].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
Комментарии: Учитывая высокую частоту гиповолемии, может потребоваться форсированная инфузионная терапия уже в начале операции.
- Рекомендуется коррекция интраоперационной гипотензии для профилактики вторичного повреждения мозга [261, 263, 270].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
Комментарии: начало инфузии кардиотонических препаратов (АТХ C01CA Адренергические и дофаминергические средства) (например, норэпинефрин** (C01CA03)) при устойчивом снижении среднего АД ниже 60 - 65 мм рт. ст. позволяет снизить риск повреждения органов, чувствительных к ишемическому повреждению (мозг, сердце, почки). Особенно важно не допускать гипотонии на этапах временного клипирования артерий. При проведении интраоперационного мониторинга ВЧД следует ориентироваться на уровень ЦПД не менее 60 мм рт. ст.
- Рекомендуется коррекция устойчивой гипертензии для профилактики повторного кровоизлияния [263, 264].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
Комментарии: целесообразно избегать устойчивого повышения систолического АД выше 160 - 180 мм рт. ст. в интраоперационном периоде, корректируя гипертензию с помощью блокаторов кальциевых каналов (например, нимодипин**) (C08CA), альфа-адреноблокаторов (например, урапидил**) ((C02CA), органических нитратов (C01DA) и др., с учетом необходимости поддержания ЦПД, достаточного для перфузии мозга.
3.2.3 Послеоперационное ведение пациентов с аневризматическим субарахноидальным кровоизлиянием после выключения аневризмы из кровотока
Основные задачи интенсивной терапии пациентов после выключения аневризмы - коррекция послеоперационных осложнений (церебральных и соматических). Наиболее частыми церебральными причинами тяжелого послеоперационного течения являются: прогрессирующий ЦВ, отсроченная церебральная ишемия и отек головного мозга, развитие арезорбтивной гидроцефалии. Ведение и лечение пациентов после операции осуществляется по тем же принципам, что и до операции, однако имеются особенности.
Базовые принципы интенсивной терапии
- Рекомендуется поднятие головного конца кровати на 30° [123, 265, 266].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
- Рекомендуется раннее начало энтерального питания (в течение 24 - 48 часов) после операции [123, 275].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
- Рекомендуется профилактика пролежней для маломобильных пациентов (повороты пациентов в кровати, матрас противопролежневый, гигиена) [123, 276].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
Профилактика тромбоза вен нижних конечностей и венозной тромбоэмболии
- Рекомендуется профилактическое назначение низкомолекулярных гепаринов (НМГ) (B01AB Группа гепарина) подкожно в период не ранее 24 часов после микрохирургического или эндоваскулярного выключения аневризмы [128].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
Комментарии: Решение о конкретном сроке начала антикоагулянтной профилактики и выбор дозы определяется индивидуально, с учетом особенностей нейрохирургического вмешательства.
- Рекомендуется перемежающаяся пневмокомпрессия или компрессионные чулки при наличии у пациентов противопоказаний к назначению НМГ (B01AB Группа гепарина) [17, 129, 131].
Уровень убедительности рекомендаций B (уровень достоверности доказательств - 2)
Управление параметрами системной гемодинамики и волемией после выключения аневризмы из кровотока
- Рекомендуется незамедлительная коррекция артериальной гипотензии на любом этапе лечения [17, 32].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
- Рекомендуется введение жидкости для достижения и поддержания эуволемии, определяемой как положительный ежедневный водный баланс в 500 - 750 мл [273], предпочтение следует отдавать сбалансированным кристаллоидным растворам (B05BB Растворы, влияющие на водно-электролитный баланс) [17, 27].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
Коррекция анемии
- Рекомендуется проведение трансфузии эритроцитарной массы (B05AX) при показателях гемоглобина 7 г/дл и ниже [127, 175, 265].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
Респираторная поддержка
- Рекомендуется поддерживать SpO2 ![]() 92% [123, 176].
92% [123, 176].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
- Рекомендуется достигать целевых параметров ИВЛ: PaCO2 = 35 - 45 мм рт. ст., PaO2 ![]() 80 мм рт. ст. [123, 181].
80 мм рт. ст. [123, 181].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
- Рекомендуется ранее выполнении трахеостомии при прогнозируемой длительной ИВЛ [123, 181].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
Контроль концентрации натрия крови
- Рекомендуется пациентам с аневризматическим САК поддержание значений натрия плазмы в нормальных пределах (135 - 145 ммоль/л). Рекомендуется коррекция гипонатриемии при концентрации натрия плазмы < 135 ммоль/л [123, 181].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
Комментарии: Гипонатриемия может развиваться как в результате синдрома неадекватной секреции вазопрессина (SIADH), так и при мозговом сольтеряющем синдроме (CSW) [279]. Пациенты с SIADH эуволемичны, гипонатриемия развивается на фоне задержки воды. Ограничение жидкости нежелательны у пациентов с аневризматическим САК. При CSW гипонатриемия вызвана потерями Na на фоне избыточной секреции натрийуретических пептидов. Для CSW характерен повышенный темп диуреза. Основным отличием SIADH и CSW является повышенный темп диуреза при CSW.
- Рекомендуется пациентам с SIADH осуществлять внутривенную инфузию 3% натрия хлорида (Стерильные лекарственные препараты аптечного изготовления, ОФС.1.8.0006) со скоростью 1 - 3 мл/кг, до достижения нормальных значений натрия плазмы (контроль натрия через 2 часа после начала инфузии, затем каждые 2 часа до достижения целевых значений) [16, 270].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
- Рекомендуется пациентам с CSW для коррекции гиповолемии и поддержания эуволемии проводить инфузионную терапию 0,9% натрия хлорида** (B05BB01). При выраженной гипонатриемии 0,9% натрия хлорида** (B05BB01) комбинируется с 3% натрия хлорида (Стерильные лекарственные препараты аптечного изготовления, ОФС.1.8.0006), и назначается #флудрокортизон** (H02AA02) 0,3 мг/сут. [16, 184, 280].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
Осуществление наружного вентрикулярного дренирования
- Рекомендуется контролировать адекватное функционирование НВД (Система нейрохирургическая для наружного дренирования, дренирования и мониторинга спинномозговой жидкости) [188].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
- Рекомендуется перекрывать НВД (Система нейрохирургическая для наружного дренирования, дренирования и мониторинга спинномозговой жидкости) во время любых позиционных изменений, транспортировки пациента и т.д. [181, 228, 229].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 3)
- Рекомендуется использовать комплекс мер, направленных на стандартизацию установки, использования, ухода за НВД (Система нейрохирургическая для наружного дренирования, дренирования и мониторинга спинномозговой жидкости) для снижения частоты развития дренаж-ассоциированных вентрикулитов [236].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
Комментарии: установка НВД (Система нейрохирургическая для наружного дренирования, дренирования и мониторинга спинномозговой жидкости) проводится в стерильных условиях операционной, накладывают фрезевое отверстие в стандартных точках (точка Кохера, точка Денди), проводят пункцию переднего или заднего рога бокового желудочка, вентрикулярный конец дренажа погружается на глубину 5 - 7 см, наружный конец дренажа выводится через контрапертуру, фиксируется к коже швами, присоединяется к стерильному ликвороприемнику (резервуар люмбальный) [283]. См. раздел "Установка наружного вентрикулярного дренажа".
Профилактика и терапия церебрального вазоспазма и ишемии головного мозга
Тактика у пациентов в сознании, при стабильном неврологическом статусе
- Рекомендуется провести ультразвуковую допплерографию транскраниальную артерий методом мониторирования (ТКДГ) пациентам с аневризматическим субарахноидальным кровоизлиянием не реже одного раза в сутки до начала стабилизации ЛСК (примерно 10 - 14 сутки после САК) [17, 181, 2288].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
- Рекомендуется динамическое наблюдение состояния пациента при показателях средней ЛСК в СМА 120 - 200 см/сек и индексе Линдегаарда 3 - 6) [27].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
- Рекомендуется проведение гипердинамической терапии церебрального вазоспазма при показателях средней ЛСК в СМА > 200 см/сек и/или индексе Линдегаарда > 6 [17].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
Тактика при ухудшении неврологического статуса у пациентов в сознании
- Рекомендуется дифференциальная диагностика причин нарастания неврологической симптоматики [17, 181, 273].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
Комментарии: Дифференциальная диагностика ЦВ и развития отсроченной церебральной ишемии проводится на основании:
а. Клинической картины: отсроченная церебральная ишемия определяется как возникновение новых очаговых неврологических нарушений или снижение не менее чем на 2 балла по шкале комы Глазго (либо по общему баллу, либо по одному из его отдельных компонентов, таких как открывание глаз, речь или двигательный ответ с любой стороны). Это должно длиться не менее 1 часа, не проявляться сразу после выключения аневризмы и не объясняться другими причинами [273, 274].
б. Методов нейровизуализации: КТ головного мозга, КТА, КТ-перфузия головного мозга, ЦАГ. Проявления ЦВ и ишемии будут подтверждаться очагами пониженной плотности, соответствующих определенным сосудистым бассейнам на КТ, зонами гипоперфузии по данным КТ-перфузии головного мозга (снижение церебрального кровотока менее 25 мл/100 г/мин, снижение церебрального объема крови менее 1,5мл/100г и/или повышение среднего времени прохождения более 6,5 секунд), визуализацией церебрального спазма при КТА (ЦАГ). Тяжелый ангиоспазм - сужение не менее 70% от исходного уровня по ангиограммам при ЦАГ или КТА [106, 274, 275]. Также исключаются другие причины ухудшения: интракраниальная гематома, гидроцефалия и др.
в. Экстренной ТКДГ: увеличение средней скорости кровотока по СМА более чем на 50 см/сек за 24 ч, или средняя ЛСК превышает 200 см/сек в СМА или индекс Линдегаарда >6 [287].
- Рекомендуется начало гипердинамической терапии церебрального вазоспазма и отсроченной церебральной ишемии, если вышеуказанные методы диагностики не могут быть доступны в течение 1 - 2 ч [17].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
Тактика у пациентов без сознания и/или в условиях медикаментозной седации
- Рекомендуется проводить ультразвуковую допплерографию транскраниальную артерий методом мониторирования (ТКДГ) не реже одного раза в сутки [17, 181, 275].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
- Рекомендуется провести экстренную ультразвуковую допплерографию транскраниальную артерий методом мониторирования (ТКДГ) при появлении признаков, указывающих на нарастание церебрального вазоспазма и отсроченной церебральной ишемии [17, 272, 276].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
Комментарии: косвенными признаками нарастания ЦВ и отсроченной церебральной ишемии у пациента в бессознательном (седатированном) состоянии являются: снижение оценки неврологического статуса по ШКГ на 1 или более баллов, появление асимметрии зрачков, любого дополнительного очагового неврологического дефицита, триады Кушинга, повышение ВЧД при наличии мониторинга.
ЦВ и развитие отсроченной церебральной ишемии подтверждается:
А. ТКДГ
Б. Методами нейровизуализации: КТ головного мозга, СКТ АГ, СКТ перфузии, ЦАГ.
Гипердинамическая терапия церебрального вазоспазма и отсроченной церебральной ишемии
Рассматривается как первый этап терапии ЦВ и отсроченной церебральной ишемии [288]. Заключается в повышении среднего АД для улучшения церебральной перфузии. Терапия включает применение вазопрессорных препаратов (АТХ C01CA Адренергические и дофаминергические средства) (норэпинефрина**(C01CA)), на фоне поддержания эуволемии комбинацией кристаллоидных (B05BB Растворы, влияющие на водно-электролитный баланс) или коллоидных (B05AA Кровезаменители и препараты плазмы крови) растворов (р-р #альбумина человека** (B05AA)) [17, 184].
При снижении сердечного выброса рекомендовано использовать препараты с инотропным действием (добутамин** (C01CA))), при отсутствии эффекта от изолированного применения вазопрессоров (АТХ C01CA Адренергические и дофаминергические средства) или снижении сердечного выброса. При проведении гипердинамической терапии возможно развитие легочной гипертензии, отека легких, гипергидратации пациента, нарушения сократимости миокарда и сердечного ритма. Необходимо проведение эхокардиографии при подозрении на кардиальные осложнения. Увеличение показателя тропонина, а также электрокардиографические признаки ишемического повреждения являются поводом незамедлительной коррекции целевых параметров среднего АД, консультации врачом-кардиологом.
Рекомендованный алгоритм гипердинамической терапии:
- Рекомендуется внутривенное непрерывное введение 0,9% натрия хлорида** (или сбалансированного кристаллоидного раствора**) (B05BB Растворы, влияющие на водно-электролитный баланс) внутривенно непрерывно 30 мл/кг в сутки [182].
Уровень убедительности рекомендаций B (уровень достоверности доказательств - 2)
- Рекомендуется достижение систолического АД 160 - 200 мм рт. ст. [289]
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
- Рекомендуется назначение #альбумина человека** (B05AA) при снижении альбумина в крови менее 30 г/л [290].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
Комментарий: рекомендуемые дозы для 25% #альбумина человека**: 0.625 г/кг в сутки в течение 7 дней; 1.25 г/кг в сутки в течение 7 дней; 1.875 г/кг в сутки в течение 7 дней; 2.5 г/кг в сутки в течение 7 дней
- Рекомендуется применение адренергических и дофаминергических средств (C01CA) для повышения АД [17]. [275] [276]
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
- Рекомендуется для быстрого восстановления и поддержания АД при остром его снижении применение норэпинефрина** (C01CA) в дозировках, соответствующих инструкции к применению [17]. [275] [276]
Уровень убедительности рекомендаций B (уровень достоверности доказательств - 2)
- Рекомендуется при острой сердечной недостаточности и декомпенсации хронической сердечной недостаточности (сниженной сократительной способности миокарда) использование добутамина** (C01CA) в дозировках, соответствующих инструкции к применению [17]. [275] [276]
Уровень убедительности рекомендаций B (уровень достоверности доказательств - 2)
Эндоваскулярное лечение церебрального вазоспазма методом интраартериального введения блокаторов кальциевых каналов после выключения аневризмы
- Рекомендуется прямая церебральная ангиография при выявлении тяжелого церебрального вазоспазма на основании клиники и по данным ультразвуковой допплерографии транскраниальных артерий методом мониторирования (ТКДГ) [292 - 294].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
Комментарии: Признаки тяжелого ЦВ: средняя линейная ЛСК в М1 СМА по данным ТКДГ более 200 см/сек или индекс Линдегаарда > 6; появление очагового неврологического дефицита и снижение уровня бодрствования.
- Рекомендуется интраартериальное (эндоваскулярное) введение блокаторов кальциевых каналов (БКК) в бассейн ВСА при признаках тяжелого ЦВ и неэффективности медикаментозных методов лечения при наличии технической возможности [293 - 295].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
Комментарии: С учетом применения препаратов офф-лейбл необходимо проведение врачебной комиссии с указанием о необходимости данного вида лечения по жизненным показаниям!
- Не рекомендуется интраартериальное введение БКК при неполном выключении разорвавшейся аневризмы, обширном (распространяющемся на несколько долей) ишемическом очаге в бассейне спазмированной артерии, выраженном инфекционно-воспалительном процессе (менингит, пневмония, сепсис и др.), остром повреждении почек или выраженной хронической болезни почек, выраженных кардиологических нарушениях (острый или недавно перенесенный инфаркт миокарда, A-V блокада 2 - 3 степени, выраженная брадикардия (ЧСС менее 50 уд/мин), трепетание предсердий или мерцательная аритмия), индивидуальной непереносимости (гиперчувствительность) к препаратам из группы БКК или к контрастному веществу [293 - 295].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
- Рекомендуется введение в один каротидный бассейн дозы 50 - 100 мг #верапамила** или 1 - 2 мг #нимодипина** пациентам при проведении интраартериального введения БКК [294, 295].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
Комментарии: Для терапии используются: #верапамил** (C08DA01) 0,25 мг/мл (5 мг на 25 мл 0,9% натрия хлорида** (B05BB01)) со средней скоростью 10 мл/мин или #нимодипин** (C08CA06) 0,01 мг/мл (после разведения 0,9% натрия хлорида** (B05BB01)). Инфузия проводится в ВСА медленно. Скорость введения зависит от показателей гемодинамики и ВЧД.
Процедура интраартериального введения блокаторов кальциевых каналов может выполняться многократно, в соответствии с показаниями и в зависимости от состояния больного, с интервалом не менее 8 часов.
- Не рекомендуется интраартериальное введение БКК при повышении ВЧД более 18 - 20 мм рт. ст. [293 - 295].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
Комментарии: Интраартериальное введение БКК сопровождается временным (на 10 - 30 мин) подъемом ВЧД, которое снижается до исходного уровня самостоятельно. У больных с ВЧД выше 18 мм. рт. ст. процедура несет риск аксиального смещения (вклинения). Если больной на момент процедуры находится в условиях медикаментозной седации, показан интраоперационный мониторинг ВЧД. При повышении ВЧД выше 18 - 20 мм рт. ст. может потребоваться осмотерапия и/или установка/открытие наружного вентрикулярного дренажа (Система нейрохирургическая для наружного дренирования, дренирования и мониторинга спинномозговой жидкости). При невозможности купирования высокого ВЧД, процедуру интраартериального введения блокаторов кальциевых каналов прекращают.
- Рекомендуется воздержаться от повторного интраартериального введения БКК при клиническом и ангиографическом улучшении состояния пациента [293 - 295].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
Комментарии: Критериями прекращения интраартериального введение БКК являются наличие не менее двух факторов из нижеперечисленных:
А. Улучшение неврологического статуса пациента.
Б. Снижение средней ЛСК по данным ТКДГ (менее 200 см/сек)
В. Отсутствие прогрессирования ЦВ, отмеченное при сопоставлении как минимум двух последовательных ангиографических исследований.
Внутричерепная гипертензия у пациентов с аневризматическим субарахноидальным кровоизлиянием
Мониторинг внутричерепного давления
Причинами внутричерепной гипертензии у пациентов с аневризматическим САК являются: масс эффект, оказываемый излившейся при кровоизлиянии кровью, гидроцефалия, отсроченная церебральная ишемия [296].
Незамедлительная установка НВД и дренирование спинномозговой жидкости (A16.23.001 Пункция желудочка головного мозга, A16.23.047 Дренирование боковых желудочков головного мозга наружное) (Система нейрохирургическая для наружного дренирования, дренирования и мониторинга спинномозговой жидкости) необходимо у пациентов с аневризматическим САК, у которых отмечается снижение уровня бодрствования или нарушения сознания и признаки гидроцефалии и/или ВЧГ при проведении КТ исследования [297].
- Рекомендуется мониторинг внутричерепного давления тензометрическим методом через НВД (Система нейрохирургическая для наружного дренирования, дренирования и мониторинга спинномозговой жидкости) при условии его адекватного функционирования [164, 283].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
- Рекомендуется при наличии технической возможности установка паренхиматозного датчика ВЧД (Система нейрохирургическая для наружного дренирования, дренирования и мониторинга спинномозговой жидкости) пациентам с тяжестью состояния до операции по шкале Hunt-Hess 4 - 5 (ШКГ <9 баллов) или требующих продолженной медикаментозной седации с высоким риском развития церебрального вазоспазма и отсроченной церебральной ишемии [122, 123, 298].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
Общие принципы терапии внутричерепной гипертензии у пациентов с аневризматическим субарахноидальным кровоизлиянием
- Рекомендуется начинать терапию внутричерепной гипертензии при внутричерепном давлении более 18 - 20 мм рт. ст. [122, 123, 298].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
- Рекомендуется возвышенное на 30 - 40° положение головного конца кровати [274].
Уровень убедительности рекомендаций B (уровень достоверности доказательств - 3)
- Рекомендуется выведение ликвора по НВД (Система нейрохирургическая для наружного дренирования, дренирования и мониторинга спинномозговой жидкости) у пациентов с НВД и повышением внутричерепного давления [16, 227, 229].
Уровень убедительности рекомендаций B (уровень достоверности доказательств - 3)
- Рекомендуется проведение седации пациентам, получающим интенсивную терапию, (пропофол** (N01AX10) в дозировках, соответствующих инструкции к применению, при необходимости - #дексмедетомидин (N05CM18) внутривенная инфузия со скоростью 0,2 - 0,7 мкг/кг/ч с титром по эффекту), аналгезии (фентанил** (N01AH01) в дозировках, соответствующих инструкции к применению) [300] [121, 123].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4) - для #дексмедетомидина
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5) - для пропофола** и фентанила**
- Рекомендуется у пациентов с отеком мозга (и повышением ВЧД) проведение осмотерапии с использованием осмотических диуретиков (15% маннитол** ((B05BC Растворы с осмодиуретическим действием) в соответствии с инструкцией, или 10% раствор натрия хлорида (Стерильные лекарственные препараты аптечного изготовления, ОФС.1.8.0006), разовая доза 20 - 50 мл в центральную вену [120, 124, 126].
Уровень убедительности рекомендаций B (уровень достоверности доказательств - 2)
- Не рекомендуется проведение гипервентиляции у пациентов с повышением ВЧД и аневризматическим САК [121, 123].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
- Рекомендуется поддержание ЦПД ![]() 60 мм рт. cт [121, 123].
60 мм рт. cт [121, 123].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
- Рекомендуется при проведении осмотерапии контролировать волемический статус, темп диуреза и регулярно оценивать концентрацию натрия крови и осмолярность плазмы крови [17, 121].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
- Рекомендуется прекращение мониторинга ВЧД через 48 - 72 часа с момента нормализации ВЧД и прекращения интенсивной терапии, направленной на коррекцию ВЧГ [123, 285].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
- Рекомендуется вторичная ДТЧ при наличии признаков рефрактерной ВЧГ [3, 5, 117].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
Комментарии: Рефрактерной считается ВЧГ, которая не поддается коррекции при консервативной терапии, и ВЧД остается выше 18 - 20 мм рт. ст. [122, 123, 243, 299].
Оценка исходов лечения пациентов
- Рекомендуется у пациентов, перенесших САК, проводить оценку исходов лечения по шкале исходов Глазго или модифицированной шкале Ренкина (Приложение Г) в сроки не ранее 6 мес после САК [16, 174, 175, 299].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
Комментарии: более ранняя оценка (при выписке пациента или в другие выбранные сроки) возможна как промежуточный этап.
3.3 Лечение пациентов с артериовенозной мальформацией
3.3.1 Общие рекомендации
Существуют три метода лечения АВМ: микрохирургическое удаление, эндоваскулярная эмболизация и радиохирургия. Каждый из них имеет свои преимущества и недостатки. При этом все они направлены на предотвращение кровоизлияний, для чего необходимо полное выключение мальформации из кровотока [95].
В остром периоде разрыва АВМ зачастую не требуется проводить хирургическое лечение самой мальформации ввиду невысокого риска повторного разрыва, тактика строится в основном исходя из объема интракраниального кровоизлияния, степени дислокации головного мозга и компрессии ликворопроводящих путей [31, 288].
- Рекомендуется при разрыве артериовенозной мальформации и супратенториальной внутримозговой гематоме объемом менее 30 мл, субтенториальной внутримозговой гематоме объемом менее 15 мл, отсутствии окклюзионной гидроцефалии и выраженного мозгового отека проводить плановое лечение артериовенозной мальформации в специализированных нейрохирургических центрах, где возможен мультимодальный подход [95, 289]
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
- Рекомендуется плановое лечение неразорвавшихся артериовенозных мальформаций в специализированных нейрохирургических центрах, где возможен мультимодальный подход [95].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
3.3.2 Хирургическое лечение пациентов с артериовенозной мальформацией
- Рекомендуется выполнение экстренной нейрохирургической операции при разрыве супратенториальной артериовенозной мальформации с формированием внутримозговой гематомы объемом более 30 мл [290, 291, 305].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
Комментарии: Экстренное хирургическое лечение возможно при ВМГ объемом менее 30 мл при наличии массивного перифокального отека с развитием поперечной дислокации более 5 мм или аксиальной дислокации.
У пациентов старше 80 лет, при наличии грубой соматической патологии или при нарушении сознания до комы (3 - 8 балла по ШКГ) принимать решение о проведении экстренной нейрохирургической операции следует на основании врачебной комиссии с учетом рисков естественного течения заболевания и периоперационных осложнений [305].
- Рекомендуется выполнение экстренной операции при кровоизлиянии из субтенториальной артериовенозной мальформации при наличии внутримозговой гематомы мозжечка объемом более 15 мл [306].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
Комментарии: У пациентов старше 80 лет, при наличии грубой соматической патологии или при нарушении сознания до комы (3 - 8 балла по ШКГ) принимать решение о проведении экстренной нейрохирургической операции следует на основании врачебной комиссии с учетом рисков естественного течения заболевания и периоперационных осложнений [306].
- Рекомендуется экстренная установка наружного вентрикулярного дренажа (A16.23.001 Пункция желудочка головного мозга, A16.23.047 Дренирование боковых желудочков головного мозга наружное) (Система нейрохирургическая для наружного дренирования, дренирования и мониторинга спинномозговой жидкости) при разрыве артериовенозной мальформации и развитии окклюзионной гидроцефалии [305].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
- Рекомендуется при выполнении экстренной операции удалять внутримозговую гематому вместе с артериовенозной мальформацией при небольших размерах мальформации, ее компактном строении, доступной локализации и высоком риске повторного разрыва [291, 306, 307].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
- Рекомендуется при проведении экстренного вмешательства удаление только внутримозговой гематомы без иссечения артериовенозной мальформации при мальформациях более 3 баллов по S-M [305].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
- Рекомендуется при выраженной внутричерепной гипертензии совместно с удалением внутримозговой гематомы выполнять декомпрессивную трепанацию черепа [291, 306, 307].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
- Рекомендуется выполнение отсроченной резекции или эмболизации артериовенозной мальформации (спустя 2 - 6 недель от кровоизлияния) при супратенториальной внутримозговой гематоме объемом менее 30 мл, субтенториальной внутримозговой гематоме менее 15 мл и отсутствии окклюзионной гидроцефалии [291, 295 - 297].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
Комментарии: В специализированных нейрохирургических центрах с большим опытом экстренной сосудистой нейрохирургии возможно удаление АВМ в раннем периоде кровоизлияния [307].
- Рекомендуется при наличии гемодинамических или интранидальных аневризм, локального варикоза или стеноза дренирующей вены и высокопоточных фистул проводить эмболизацию или резекцию разорвавшейся артериовенозной мальформации в ускоренном порядке из-за более высокого риска повторного разрыва таких мальформаций [297, 298, 309, 310].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
Эмболизация артериовенозных мальформаций
- Рекомендуется выполнять предоперационную эндоваскулярную окклюзию сосудов артериовенозной мальформации (A16.12.053.001 согласно номенклатуре МУ) перед резекцией артериовенозной мальформации при ее полиафферентном кровоснабжении, наличии высокопоточных фистул и труднодоступном расположении [298, 299, 310, 311].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
- Рекомендуется при церебральной ангиографии тотальной селективной по поводу артериовенозной мальформации контрастирование всех сосудистых бассейнов [313].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 2)
Комментарии: Необходимо исследование обоих каротидных бассейнов (раздельно ВСА и НСА), а также ВББ из обеих ПА. Особое внимание следует уделить визуализации возможных источников кровоизлияния: потоковые и интранидальные аневризмы, артериовенозные фистулы в структуре АВМ, варикозно измененные дренирующие вены.
- Рекомендуется при эндоваскулярной окклюзии сосудов артериовенозной мальформации (A16.12.053.001 Эндоваскулярная окклюзия сосудов артерио-венозной мальформации) 1 - 2 балла по S-M выполнять тотальную эмболизацию за один этап [314].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
Комментарий: при наличии в структуре АВМ прямой высокопотоковой фистулы возможно разбитие лечения на несколько этапов.
- Рекомендуется эндоваскулярной окклюзии сосудов артериовенозной мальформации (A16.12.053.001 Эндоваскулярная окклюзия сосудов артерио-венозной мальформации) 3 балла и более по S-M проводить эмболизацию в несколько этапов [315].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
Комментарии: Следует воздержаться от эмболизации более 60% крупных АВМ за один этап.
- Рекомендуется использование адгезивных (клей медицинский тканевой синтетический, клей хирургический Glubran 2) и неадгезивных (система жидкая эмболизирующая) эмболизирующих агентов при эндоваскулярном лечении артериовенозных мальформаций [315].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
Радиохирургическое лечение артериовенозных мальформаций
- Рекомендуется дистанционное лучевое лечение (A07.23.001 Дистанционная лучевая терапия при поражении центральной нервной системы и головного мозга) разорвавшейся артериовенозной мальформации только при невозможности проведения микрохирургического и эндоваскулярного лечения [95].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
- Рекомендуется дистанционное лучевое лечение (A07.23.001 Дистанционная лучевая терапия при поражении центральной нервной системы и головного мозга) в случае неполной резекции или эмболизации артериовенозной мальформации [289, 302, 303].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
- Рекомендуется выполнение дистанционного лучевого лечения (A07.23.001 Дистанционная лучевая терапия при поражении центральной нервной системы и головного мозга) артериовенозной мальформации не ранее 6 - 12 недель после кровоизлияния [292, 302].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
- Рекомендуется выполнение динамических магнитно-резонансных томографий головного мозга для оценки степени облитерации артериовенозной мальформации после радиохирургии [317].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
Комментарии: При невозможности выполнения МРТ для динамической оценки радикальности закрытия мальформации допустимо проведение КТ-ангиографии.
- Рекомендуется при тотальной окклюзии мальформации при магнитно-резонансной томографии головного мозга после радиохирургии выполнение церебральной ангиографии тотальной селективной для подтверждения радикальности ее облитерации [95, 305].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
- Рекомендуется повторное облучение артериовенозной мальформации при ее неполной облитерации через 3 - 5 лет после радиохирургии [315].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
3.3.3 Послеоперационное ведение пациентов
- Рекомендуется ранее пробуждение и экстубация пациентов при небольших и средних артериовенозных мальформациях, а также при отсутствии хирургических осложнений [319].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
- Рекомендуется пробуждение пациента после выполнения контрольной компьютерной томографии головного мозга при артериовенозной мальформации большого размера, а также при артериовенозной мальформации с интраоперационными осложнениями [319].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
- Рекомендуется мониторировать артериальное давление в послеоперационном периоде после выключения артериовенозной мальформации [25, 306].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
- Рекомендуется поддерживать систолическое артериальное давление менее 140 мм рт. ст. пациентам в послеоперационном периоде после выключения из кровотока артериовенозной мальформации [25, 306, 307]
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
- Рекомендуется выполнять контрольную компьютерную томографию головного мозга в течение 24 часов после операции по поводу артериовенозной мальформации [25].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
- Рекомендуется для исключения остаточной артериовенозной мальформации после ее резекции выполнять компьютерно-томографическую ангиографию сосудов головного мозга или церебральная ангиография тотальная селективная в течение 7 суток после операции [95].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
- Рекомендуется при выявлении остаточной артериовенозной мальформации при послеоперационной церебральной ангиографии тотальной селективной выполнять дальнейшее ее выключение из кровотока при помощи резекции (A16.12.053 Удаление артерио-венозной мальформации), эмболизации (A16.12.053.001 Эндоваскулярная окклюзия сосудов артерио-венозной мальформации) или радиохирургии (A07.23.001 Дистанционная лучевая терапия при поражении центральной нервной системы и головного мозга) [95, 303, 304, 308].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
- Не рекомендуется рутинное назначение антиконвульсантов после удаления артериовенозной мальформации [25].
Уровень убедительности рекомендаций B (уровень достоверности доказательств - 4)
- Рекомендуется назначение противоэпилептических препаратов в послеоперационном периоде пациентам с вновь развившимися эпиприступами [323].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
Комментарии: Длительность терапии определяется индивидуально.
- Рекомендуется продолжение противосудорожной терапии в послеоперационном периоде у пациентов с эпиприступами в анамнезе [324] [323]
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
4. Медицинская реабилитация и санаторно-курортное лечение, медицинские показания и противопоказания к применению методов медицинской реабилитации, в том числе основанных на использовании природных лечебных факторов
- Рекомендуется проведение услуг по медицинской реабилитации пациента с заболеваниями центральной нервной системы при геморрагическом инсульте на всех этапах лечения с целью улучшения исхода заболевания при консервативном и хирургическом лечении, выполнение лечебной физкультуры при заболеваниях центральной нервной системы и головного мозга, и (или) лечебной физкультуры с использованием аппаратов и тренажеров при заболеваниях центральной нервной системы и головного мозга, и (или) постуральной коррекции, и (или) эрготерапии, и (или) медико-логопедического исследования при дисфагии, и (или) медико-логопедической процедуры при афазии, и (или) медико-логопедической процедуры при дизартрии не позднее 48 часов от момента поступления в стационар [325].
Уровень убедительности рекомендаций B (уровень достоверности доказательств - 2)
Комментарии: реабилитация начинается не позднее 48 часов пребывания в палате интенсивной терапии (ПИТ) или в отделении реанимации и интенсивной терапии (ОРИТ) и продолжается в госпитальном отделении неврологии или нейрохирургии до выписки из ЛПУ [326 - 329]. После этого пациент маршрутизируется на последующие этапы реабилитационного лечения в зависимости от степени восстановления жизнедеятельности и независимости в повседневной жизни, установленной в соответствии с градациями моделей Шкалы реабилитационной маршрутизации.
В раннем восстановительном периоде (до 6 месяцев) пациенту предоставляется 1 - 3 курса реабилитационного лечения в отделениях медицинской реабилитации для пациентов с заболеваниями ЦНС в условиях круглосуточного, дневного пребывания или в амбулаторных условиях, в том числе с применением телемедицинских технологий.
В позднем восстановительном периоде (после 6 месяцев) решение о продолжении реабилитационной программы принимается в рамках региональных стандартов формирования индивидуальной программы медицинской реабилитации (ИПМР) [329].
4.1 Реабилитация пациентов в остром периоде ГИ (3 - 28 сутки)
Помимо основного неврологического дефицита, формирующегося в результате первичного повреждении головного мозга в результате ГИ пациенты имеют высокий риск развития синдрома последствий интенсивной терапии (ПИТС) как побочного эффекта специфической интенсивной терапии, в частности длительной иммобилизации, седации и искусственной вентиляции легких [326, 327].
Основными синдромами, формирующими картину ПИТС, являются:
- полимионейропатия критических состояний: диффузное снижение силы в конечностях;
- респираторная полимионейропатия, приводящая к удлинению сроков респираторной поддержки из-за слабости дыхательной мускулатуры и диафрагмы;
- снижение толерантности к нагрузкам (слабость);
- осложнения вынужденного позиционирования (bedrest и пронпозиция): травма плечевого сплетения, "свисающие" стопы и ранние подошвенные сгибательные контрактуры, пролежни;
- ортостатическая недостаточность при высаживании;
- нарушение пассажа мочи и склонность к уролитиазу;
- нарушению работы кишечника (констипация);
- осложнения наученного неиспользования (learned non-use): дисфагия из-за трахеопищеводного разобщения;
- делирий;
- хронизирующийся болевой синдром (мышечно-суставной, нейропатический);
- эмоционально-когнитивные нарушения (депрессия; снижение памяти);
- диссомния.
Это определяет необходимость профилактики ПИТС как базовой первичной технологии ранней реабилитации. Для этого используется технология "РеабИТ" [332], реализуемая силами мультидисциплинарной реабилитационной команды (МДРК) отделения ранней медицинской реабилитации и первичного сосудистого отделения (ПИТ ПСО). В рамках данных рекомендация приводим основные тезисы и комментарии по особенностям их применения у пациентов с САК и ВМК.
- Рекомендуется оценка тяжести синдрома последствий интенсивной терапии каждые 24 часа с использованием индекса тяжести ПИТС членами мультидисциплинарной реабилитационной команды пациентам с геморрагическим инсультом в период пребывания в ОРИТ для его диагностики и динамики в ходе реабилитационного лечения [326, 329, 330].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
Комментарии: Полный перечень клиниметрических шкал, нормативы значений и специальности членов МДРК, ответственных за контроль и интерпретацию данных по соответствующей шкале, представлены в соответствующих методических рекомендациях [332]. Расчет ПИТС индекса производится на основании суммирования ранжированных симптомов, установленных членами МДРК по своему профилю (приложение Г16). Сумма баллов в диапазоне от 0 до 10 отражает как факт наличия ПИТС, так и степень тяжести, и эффективность реабилитационных мероприятий. При интерпретации проявлений ПИТС следует учитывать, что такие модальности ПИТС, как двигательный дефицит, нарушение глотания, когнитивные нарушения, снижение гравитационного градиента, являются проявлением первичного поражения головного и спинного мозга. В этом случае их не следует включать в расчет. При дифференциальной диагностике двигательных нарушений фиксируются значимые симптомы на непораженной стороне, например, наличие полимионейропатии критических состояний подтверждайся, если на здоровой стороне сумма оценок силы не превышала 8 баллов. Преимущества других методов оценки тяжести ПИТС не доказано [335 - 338].
- Рекомендуется осуществлять профилактику развития синдрома последствий интенсивной терапии пациентам с геморрагическим инсультом, получающим помощь в условиях ОРИТ более 48 ч, вне зависимости от вида оперативного вмешательства, тяжести состояния и респираторного статуса для профилактики ПИТ-синдрома [326, 330].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
Комментарии: действующие руководства по лечению ГИ уклончивы [5, 27] в предложениях о сроках видах начала реабилитации, но настаивают на раннем начале. С позиции общей физиологии острой церебральной недостаточности профилактика синдрома наученного неиспользования обоснована как для ПИТС, так и острого очагового дефицита [332].
- Рекомендуется проводить индивидуальную программу реабилитации в ОРИТ ежедневно, начиная с 3 суток от дебюта заболевания продолжительностью не менее 1 ч, но не более 3 ч c учетом статуса сознания и уровня мобильности пациента с геморрагическим инсультом для профилактики развития синдрома последствий интенсивной терапии [339].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
Комментарии: в зависимости от возможности участия пациента в реабилитационных мероприятиях (тяжесть состояния, уровень сознания) реабилитация проводится в активном, пассивном и активно-пассивном режиме. Программа реабилитации должна включать комбинацию методик кинезиологических маневров (позиционирования, вертикализации и мобильности, велокинетические нагрузки и электронейромиостимуляцию), а также практики медицинских психологов, специалистов по эргореабилитации (эргоспециалистов) и медицинских логопедов [326, 327].
- Не рекомендуется начинать реабилитационные мероприятия по мобилизации и вертикализирующему позиционированию в ОРИТ ранее 24 часов от дебюта заболевания или послеоперационного периода пациентам с геморрагическим инсультом, а также при наличии абсолютных и без учета относительных противопоказаний из-за риска нарушений церебральной гемодинамики и прогрессирования ангиоспазма [341, 342].
Уровень убедительности рекомендаций B (уровень достоверности доказательств - 2)
- Рекомендуется прекратить реабилитационные процедуры при отклонении мониторируемых показателей от нормативных значений - развитии СТОП-сигналов пациентам с геморрагическим инсультом на любом этапе реабилитационного лечения с целью профилактики осложнений [330, 344].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
Комментарии: при появлении противопоказаний СТОП-сигналов (приложение Б3) в момент вертикализации, мобилизации или любой другой реабилитационной процедуры, данную процедуру следует немедленно остановить. Если стоп-сигналы развились в момент вертикализации, ее следует прекратить и вернуть пациента к предшествующей позиции (опустить на 20°) или опустить до 0° без остановок на углах подъема. Контактным пациентам следует тщательно объяснять суть и ожидаемые ощущения от планируемой процедуры, чтобы не спровоцировать нежелательные вегетативные реакции, обусловленные страхом и неопределенность, с особенно у детей. Уровень доказательности приведенных признаков не превышает уровня С, но получение более качественных аргументов в данном контексте сложно из-за соображений неэтичности формирования контрольной группы в таких исследованиях.
- Рекомендуется пациентам с геморрагическим инсультом в ОРИТ проводить "тест поднятых ног" перед началом каждой сессии маневров мобилизации и вертикализирующего позиционирования для определения риска гемодинамических СТОП-сигналов при мобилизации и вертикализирующем позиционировании [318, 332, 333].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
Комментарии: с одной стороны, положительный "тест поднятых ног" (passive leg raising test) указывает на гиповолемию, которая при маневре вертикализации приведет к развитию ортостатической недостаточности, что при любом неотложном состоянии крайне нежелательно. С другой стороны, эту ситуацию не следует считать окончательным противопоказанием для мобилизации. Следует оценить причины и план восстановления эуволемии, после чего, получив отрицательный результат при повторном тестировании, возобновить реализацию реабилитационного плана.
- Рекомендуется пациентам с геморрагическим инсультом в первые сутки пребывания в ОРИТ проводить невертикализирующее позиционирование посредством изменения положения конечностей и туловища пациента по отношению к горизонтальной плоскости, в зависимости от статуса вертикализированности, не реже чем каждые 2 часа c перерывом на ночной сон для профилактики осложнений лечебной иммобилизации [333, 334].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
Комментарии: в отличие от мобилизации, невертикализирующее [332] позиционирование не имеет абсолютных противопоказаний и должно использоваться с 1-х суток независимо от объема прочих модальностей ранней реабилитации дежурным медицинским персоналом. Позиционирование используется для гравитационной стимуляции при подъеме головного конца, поэтому головной конец всегда должен быть приподнят не ниже 30°. Пациентам помогают последовательно принимать позы лежа (на правом и/или левом боку или на спине), на приподнятом изголовье или сидя. При позиционировании следует непременно предусмотреть повороты на парализованные конечности для проприоцептивной стимуляции и профилактики синдрома "наученного неиспользования".
- Рекомендуется пациентам с геморрагическим инсультом в ОРИТ ежедневно проводить маневры вертикализации с последующим вертикализирующим позиционированием, начиная от высокого изголовья (30 - 60°) до положения сидя с опущенными ногами и стояния около постели, с целью пошагового восстановления гравитационного градиента [349].
Уровень убедительности рекомендаций B (уровень достоверности доказательств - 1)
Комментарии: Стояние - это лучшее положение тела для эффективного дыхания пациента и поддержания объема легких [334, 336]. Чем выше гравитационный градиент и продолжительность пребывания в нем пациента, тем ниже риск аспирации, пролежней, полимионейропатии, контрактур, патологической (болевой) сенситизации и прочих факторов ПИТС. Пациентам на спонтанном дыхании и ИВЛ в любых режимах следует стремиться к поддержанию максимально длительного вертикализирующего антигравитацию позиционирования на уровне гравитационного градиента, достигнутого при пассивной вертикализации. У контактных пациентов гравитационный градиент определяется по индивидуальному запросу пациента. Таких пациентов следует обучить наклонам вперед - в этом положении благодаря силе тяжести улучшается дренирование экскреции из задненижних сегментов легких. Процедуры вертикализации следует проводить 3 раза в день по 30 мин. Продолжительность процедуры зависит от переносимости, но должна составлять не менее 15 мин. В любой позиции голова должна быть в положении по средней линии для предотвращения затруднения венозного оттока, вторичного повышения внутричерепного и внутриглазного давления, а также нарастания патологического мышечного тонуса в паретичных конечностях [351].
- Рекомендуется пациентам с геморрагическим инсультом в ОРИТ начать активно-пассивную мобилизацию, в том числе вертикализацию и вертикализирующее позиционирование, не ранее 24 часов, но не позже 72 часов от начала неотложного состояния либо непосредственно после установления факта отсутствия противопоказаний к началу или продолжению мобилизации с целью профилактики осложнений иммобилизации [327, 328, 341].
Уровень убедительности рекомендаций B (уровень достоверности доказательств - 4)
Комментарии: ранняя мобилизация - элемент реабилитационного процесса для пациентов с инсультом в ОРИТ [343]. Мета-анализ данных показал шестнадцати исследований с участием 1757 пациентов с САК показала, что ранняя мобилизация улучшила показатель mRS при выписке (средняя разница -1,39, 95% ДИ от -2,51 до -0,28, I2 = 86%) и через 3 месяца (средняя разница -1,10, 95% ДИ от -1,54 до -0,66, I2 = 7%). Ранняя мобилизация была связана со снижением частоты церебральных вазопатий, как рентгенологических (ОШ 0,66, 95% ДИ от 0,45 до 0,96, I2 = 7%), так и клинических (ОШ 0,44, 95% ДИ от 0,27 до 0,72, I2 = 8%); 6% сеансов мобилизации включали нежелательные явления, в основном изменения гемодинамики. Продолжительность мобилизации рекомендуется составлять от 15 до 45 минут, разделенных на один, два или три раза в день. Основное внимание при ранней мобилизации должно быть уделено сидячей, стоячей и ходячей активности.
- Рекомендуется пациентам с ГИ, начиная с 72 часов от начала заболевания, в зависимости от тяжести состояния проводить кинезиотерапевтические маневры мобилизации: активно-пассивные движения во всех суставах с растяжением, активно-пассивный велокинез, переходы в сидячее положение с поддержкой, баланс сидя, переходы в кресло, баланс стоя, шаги на месте для инициации процессов нейрорепарации и профилактики ПИТС [326, 329, 349].
Уровень убедительности рекомендаций B (уровень достоверности доказательств - 1)
Комментарии: Мобилизация является одним из видов вмешательства в рамках реабилитации, которая облегчает передвижение пациентов и увеличивает расход энергии с целью улучшения исходов [353].
Пассивная мобилизация [349] для неконтактных пациентов представляет собой серию из 10 повторных пассивных движений (пассивная суставная гимнастика) в каждом из основных суставах с легчайшим растяжением (стретчингом) в крайних точках физиологического объема движений не менее 2-х раз в день. Также пассивная кинезиотерапия может выполняться с использованием велокинез с использованием прикроватного велоэргометра (9140790) для нижних /верхних конечностей с возможностью реверсивного движения и иных механотренажеров (140790), обеспечивающих циклические тренировки для отдельных суставов и имеющих сенсоры на определение вклада пациента при активно-пассивном режиме. Активная мобилизация предполагает обучение пациента и контроль за выполнением доступных самостоятельных движений во всех суставах (активная суставная гимнастика) в режиме 10 повторов 3 - 6 раз в день [325, 340].
- Рекомендуется при проведении маневров вертикализации и мобилизации у пациентов с ГИ использовать дополнительные методы мониторинга состояния церебрального статуса: измерение регионального насыщения кислородом головного мозга (rSO2), своевременной фиксации стоп-сигналов в виде снижения скорости мозгового в результате нарастания ангиоспазма или внутричерепной гипертензии [355].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
Комментарии: в отличие от других нозологических форм острой церебральной недостаточности при ГИ выше риск развития кортикальной ишемии и дислокационного синдрома, спровоцированными вертикализацией и двигательной активностью. Анализ наблюдений 148 пациентов с САК перед и во время мобилизации выявил критическое значение rSO, равное 57%, при котором есть риск осложнений, при этом изменения rSO2 во время мобилизации не были связаны с изменениями жизненно важных показателей, что позволяет предположить, что rSO2 является независимым стоп-сигналом.
- Рекомендуется использовать методики избирательной респираторной тренировки основных и вспомогательных мышц вдоха, в том числе специальные статические и динамические дыхательные упражнения, включая применение маневров мануальной или аппаратной (VEST) перкуссионной терапии, пациентам с ГИ на ИВЛ для профилактики респираторной полимионейропатии [342, 343].
Уровень убедительности рекомендаций B (уровень достоверности доказательств - 2)
Комментарии: процедуры, направленные на снижение одышки, улучшение трахеобронхиального клиренса, тренировку скелетных мышц и поддержание уровня самообслуживания, показаны в период перевода пациента на самостоятельное дыхание или непосредственно после него, можно использовать выдох с применением положительного давления. Для этого целесообразно применение тренажеров стимулирующей спирометрии, устройств с высокочастотными интра-/экстрапульмональными колебаниями, электростимуляции диафрагмы и межреберных мышц. Использование респираторных практик реабилитации у нейрореанимационных пациентов не оказывает негативного влияния на уровень внутричерепного давления [357]. Для восстановления голосового дыхания и возможности вербальной коммуникации эффективно использование клапана голосового для трахеостомической трубки [358], который создает полезное сопротивление выдоху и способствует улучшению эмоционального статуса пациента [345, 346].
- Рекомендуется включать в программу мобилизации дополнительный цикл кинезиотерапевтических процедур (велокинез, пассивная суставная гимнастика, стретчинг и пр.) на паретичную сторону продолжительностью на менее 20 минут не реже 2 раза в сутки пациентам с ГИ и гемипарезом любой степени выраженности, начиная с 72 часов после развития заболевания или послеоперационного периода, для профилактики развития синдрома наученного неиспользования [361] [362].
Уровень убедительности рекомендаций C (уровень достоверности доказательств 5)
- Рекомендуется включать упражнения с индивидуально подобранным нарастающим уровнем градуированных отягощений: простой подъем конечностей, подъем конечностей с утяжелителями, преодоление сопротивления эластичных жгутов доступных контакту пациентам с ГИ для профилактики потери мышечной массы и снижения толерантности к нагрузкам [363].
Уровень убедительности рекомендаций B (уровень достоверности доказательств 2)
Комментарии: включение упражнений на сопротивление при условии адекватного белкового обеспечения не ниже 1,3 г/кг/сут [364], позволяет сохранить мышечную массу в условиях вынужденной иммобилизации пациента в критическом состоянии. Без мышечной активности профилактика ПНМКС даже при достаточном белково-энергетическом балансе менее эффективна. Раннее начало энтерального питания снижает риск дальнейшего дефицита питания и поддерживает анаболические процессы. Одновременно необходимо планировать раннюю мобилизацию и физическую реабилитацию, Прогрессивный режим упражнений, от пассивной мобилизации до активных силовых тренировок, должен быть адаптирован к текущей функциональной способности пациента. Эта реабилитационная стратегия направлена на сохранение целостности скелетных мышц, улучшение нервно-мышечной функции и ускорение функционального восстановлен.
- Рекомендуется рассмотреть проведение инъекций ботулинического токсина типа А** в мышцы руки и/или ноги пациентам с ГИ при повышении тонуса более чем на 2 балла по шкале Эшворта, начиная с 72 часов после развития заболевания, с целью уменьшения спастичности и риска развития контрактур [364, 365].
Уровень убедительности рекомендаций C (уровень достоверности доказательств 5)
- Рекомендуется использование электростимуляции мышц пациентам с ГИ, находящимся в ОРИТ более 72 часов, в том числе в условиях искусственной вентиляции легких, для профилактики ближайших и долгосрочных осложнений ПИТС [367].
Уровень убедительности рекомендаций B (уровень достоверности доказательств - 2)
Комментарии: электростимуляция мышц была исследована в качестве лечения для профилактики полимионейропатии критических состояний. Лечение включает минимальное движение суставов и не требует взаимодействия с пациентом. Лечение с помощью электростимуляции мышц, проводимое в ходе исследований, длилось 30 - 60 мин ежедневно в течение не менее 4 дней. В метаанализе [368] с включением 11 рандомизированных контролируемых исследований с участием 576 пациентов, показали, что раннее использование электростимуляции мышц у пациентов в отделении интенсивной терапии позволило сократить время искусственной вентиляции легких, продолжительность пребывания в отделении интенсивной терапии и общий койко-день в клинике.
- Рекомендуется проводить логопедические занятия (A 21.23.006) пациентам с геморрагическим инсультом, начиная с 72 часов пребывания в ОРИТ для профилактики связанных с постэкстубационной дисфагией аспирационных осложнений и подготовки к восстановлению нормативного трансорального питания [368, 375].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
Комментарии: частота постэкстубационной дисфагии у пациентов ОРИТ составляет 18,3% до выписки из ОРИТ, из которых до 80% сохраняют признаки дисфагии при выписке из стационара [356, 357]. При этом у 36% отмечена "тихая" аспирация. При наличии постэкстубационной дисфагии следует проводить мероприятия по восстановлению глотания под контролем медицинского логопеда МДРК [358, 359]. Сущность ранних занятий медицинского логопеда состоит в поддержании глотательного рефлекса в условиях, когда оно невозможно из-за эндотрахеальной интубации [375].
- Рекомендуется проведение многокомпонентного нефармакологического вмешательства, включающего мобилизацию, оптимизацию анальгоседации, нормализацию сна, поддержание когнитивного статуса и уровня бытовой адаптации пациентам с ГИ в ОРИТ для снижения риска делирия [376 - 380].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
Комментарии: многокомпонентные вмешательства, осуществляемые МДРК ОРИТ, способны минимизировать риски когнитивных нарушений и делирия [361, 364].
Основу профилактики делирия и прочих эмоционально-когнитивных нарушений составляет выполнение основных требований рекомендательных протоколов анальгоседации как основного приоритета в профилактике ПИТС [380] [381] [382, 383].
Многокомпонентная реабилитационная программа профилактики содержит простые комплексы движений конечностями, циклы спонтанного дыхания, поддержание у пациента актуального уровня ориентированности в месте и времени, меры по обеспечению ночного сна, выполнение элементарных действий по самообслуживанию [384], использование индивидуально подобранных музыкальных произведений не более 45 минут в сутки [367, 370].
- Рекомендуется проводить программу гигиены сна, включающую использование глазных масок и беруш пациентам с геморрагическим инсультом, начиная с периода пребывания в ОРИТ, для сохранения циркадных ритмов и профилактики делирия [386 - 388].
Уровень убедительности рекомендаций B (уровень достоверности доказательств - 1)
Комментарии: режим пребывания в ОРИТ, постоянный свет, разговор персонала, тревоги мониторов, звуки респираторов - все эти раздражители неизбежно влияют на качество сна. Между тем обеспечение сна в период пребывания в ОРИТ является способом снижения риска когнитивных нарушений, в том числе психомоторного возбуждения и делирия. Помимо этого, сохранение структуры сна позволяет поддержать позитивное эмоциональное состояние пациента, его мотивированность в участии в лечебно-реабилитационной программе, а также повышает толерантность к мышечной активности. Объединенный анализ исследований продемонстрировал общее снижение распространенности делирия по протоколу, способствующему сну [389]. Обязательным компонентом протоколов является создание оптимальной среды пребывания пациента для обеспечения нормального сна (естественные маркеры для сна - окно или регулировка свет/темнота, отказ от ночных процедур, регулярные перерывы в уходе на 60 - 90 мин). Не исключено применение медикаментозных модуляций сна [387]
- Рекомендуется пациентам с ГИ при длительном пребывании в ОРИТ проводить занятия по восстановлению навыков самообслуживания в соответствии с возрастом и когнитивным статусом для профилактики бытовой дезадаптации [389, 390].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
Комментарии: отдельным разделом эмоционально-когнитивной реабилитации является эрготерапия. В условиях ОРИТ специалист по эргореабилитации (эргоспециалист) [392] обучает пациента простым повседневным бытовым действиям, обеспечивающим уход за своим телом (персональная гигиена, одевание, еда, пользование судном, альтернативная и дополнительная коммуникация). Значение эрготерапии в структуре РеабИТ состоит в том, что она способствует ускорению восстановления преморбидного паттерна жизнедеятельности (performance patterns) пациента, т.е. возврату к привычкам, режиму жизни, социальному статусу. Включение эрготерапии в реабилитационный комплекс позволяет сократить длительность пребывания в ОРИТ, у пациентов с хроническим критическим состоянием - время адаптации к спонтанному дыханию, предупредить развитие делирия.
4.2 Реабилитация пациентов в раннем восстановительном периоде геморрагического инсульта (до 180 суток)
- Рекомендуется пациентам с геморрагическим инсультом с выявленным на 1-м этапе лечения продленным нарушением сознания в срок от 14 и не позднее 28 дней от начала заболевания или послеоперационного периода провести плановую очную или телеконсультацию со специалистами по хроническим нарушениям сознания реабилитационного центра 3 - 4 уровня для оценки статуса, корректировки лечения и определения маршрутизации [329, 393, 394].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
- Рекомендуется пациентам с геморрагическим инсультом использовать шкалу реабилитационной маршрутизации (https://rehabrus.ru/materialyi/professionalnyie-standartyi/) для обеспечения этапности реабилитационного лечения [393].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
- Рекомендуется пациентам с геморрагическим инсультом на 2 - 3 этапах реабилитационного лечения включать в индивидуальную реабилитационную программу все модальности нейрореабилитации, доказавшие эффективность при других формах очагового поражения головного мозга [395 - 398].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
Комментарии: основу ИПМР пациентов с ГИ должны составлять базовые процедуры, включающие занятия со специалистами по физической реабилитации (кинезиоспециалистами) [380, 384, 385], медицинскими логопедами [401], специалистами по эргореабилитации (эргоспециалистами) [402] и медицинскими психологами. Структура программы зависит от преобладающего домена нарушений жизнедеятельности, определяющего причину снижения независимости в повседневной жизни [403]. На начальном этапе реабилитационные тренировки длятся не менее 45 минут в день, а соответствующее увеличение интенсивности тренировок помогает улучшить функциональные возможности пациента [404]. Занятия в соответствии с личными потребностями и целями пациента следует проводить 2 - 5 раз в неделю, не менее 45 минут в день и не менее 8 недель. Интенсивность реабилитационных тренировок должна подбираться индивидуально, при этом следует в полной мере учитывать физическую силу, выносливость и сердечно-легочную функцию пациента. Рекомендуется персонализировать значения параметров интенсивности упражнений на основе процента резерва частоты сердечных сокращений, процента максимальной частоты сердечных сокращений и воспринимаемой человеком силы.
- Рекомендуется пациентам с ГИ при реабилитации на 3 этапе реабилитации использовать дистанционные занятия в телережиме для сокращения сроков адаптации к повседневной активности [390, 407].
Уровень убедительности рекомендаций B (уровень достоверности доказательств - 1)
Комментарии: пациенты после инсульта должны иметь возможность получать регулярное и непрерывное медицинское наблюдение, а также возможность продолжения реабилитационного лечения в случае отсутствия транспортных возможностей для регулярного посещения отделений реабилитации. Занятия в домашних условиях создают у пациента ощущение комфорта и повышают приверженность пациентов к проводимым процедурам [407]. Кроме этого, телереабилитация способствует закреплению навыков, приобретенных пациентами во время пребывания в стационарных отделениях.
- Рекомендуется пациентам с геморрагическим инсультом, проходящим 2 - 3 этапы медицинской реабилитации, проводить диагностику ПИТ-синдрома и включать его коррекцию в реабилитационные задачи для достижения преморбидного или максимально возможного уровня показателей активности, участия и качества жизни [408].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
Комментарии: более 75% пациентов, выписанных от ОРиТ имеют проявление синдрома последствий интенсивной терапии как барьера в структуре реабилитационного цикла, что предполагает необходимость обязательной диагностики этого состояния и включение в ИПМР специфического модуля основных и вспомогательных реабилитационных практик, ориентированных на его устранение и профилактику дальнейшего прогрессирования.
- Рекомендуется взрослым пациентам с ПИТ-синдромом пациентам на 2 - 3 этапах реабилитационного лечения с преобладанием нейромышечного домена проводить курс специфической адъювантной фармакологической модуляции #(Инозин+Никотинамид+Рибофлавин+Янтарная кислота** (N07N6E)) для повышения эффективности реабилитационного лечения двигательных нарушений [409] [410 - 412].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 3)
Комментарии: режим дозирования 10,0 внутривенно капельно 1 раз в сутки в течение 10 суток.
- Рекомендуется взрослым пациентам с ПИТ-синдромом пациентам на 2 - 3 этапах реабилитационного лечения с преобладанием домена эмоционально-когнитивных нарушений (легкими/умеренными когнитивными нарушениями) проводить курс адъювантной фармакологической модуляции (Этилметилгидроксипиридина сукцинат** (N07N6E)) для повышения эффективности реабилитационного лечения [410 - 412].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 3)
Комментарии: немногочисленные исследования фармакотерапии последствий ГИ не выявили значимых результатов. Длительной время изучалось применение флуоксетина** для профилактики депрессии и улучшения двигательной функции, но польза не доказана [397, 398]. Между тем, серия исследований, посвященной лекарственной терапии ПИТС в разные периоды реабилитации при ОЦН без субпопуляционного выделения ГИ показала, что дополнение реабилитационной программы медикаментами с направленным эффектом на двигательные нарушения (#Инозин+Никотинамид+Рибофлавин+Янтарная кислота** (N07N6E)) [411] и на легкие/умеренные когнитивные нарушения (Этилметилгидроксипиридина сукцинат** (N002161/01)) [394, 396], обусловленные феноменом наученного неиспользования при ПИТ-синдроме, ускоряет их восстановление.
- Не рекомендуется ограничивать пациентам, перенесших геморрагический инсульт, привычный образ жизни в части сексуальной и иной физической активности с целью сохранения качества жизни [415].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
Комментарии: у специалистов существует пробел в знаниях о сексуальной жизни после перенесенного инсульта, что приводит к тому, что эта тема редко затрагивается в беседах с пациентами. Многие люди боятся возвращаться к сексуальной активности после инсульта. Однако, по-видимому, при половом акте АД повышается лишь незначительно (до = 140 мм рт. ст.) на короткое время, а затем оно восстанавливается до исходного уровня вскоре после начала половой жизни у здоровых взрослых. Не хватает знаний о физической подготовке после ICH. Например, неясно, как направлять людей после ICH в плане поднятия тяжестей (подъемы с использованием больших групп мышц по сравнению с малыми, тяжелые подъемы по сравнению с повторяющимися) и насколько и на какое время следует повышать артериальное давление. Кроме того, неясно, что следует посоветовать в отношении потенциального риска кровотечения, связанного с физической нагрузкой, когда артериальное давление достигает > 300 мм рт. ст.
5. Профилактика и диспансерное наблюдение, медицинские показания и противопоказания к применению методов профилактики
5.1 Профилактика геморрагического инсульта
- Рекомендуется контроль артериального давления, повышение физической активности, контроль веса тела, правильное питание, отказ от курения пациентам с заболеваниями сердечно-сосудистой системы с целью профилактики развития мозговых сосудистых катастроф [16, 305].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
- Рекомендуется провести магнитно-резонансную ангиографию интракраниальных сосудов каждые 6 месяцев в течение 2 лет пациентам после радиохирургии [416].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
- Рекомендуется провести церебральную ангиографию тотальную селективную через 3 - 5 лет пациентам после радиохирургии для верификации облитерации АВМ [417 - 419]
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 2)
Комментарии: При отсутствии полной облитерации решается вопрос о повторной радиохирургии или микрохирургическом удалении АВМ.
Исследование является ключевым элементом стандартного наблюдения, поскольку оно:
1. Достоверно подтверждает или исключает полную облитерацию (цель лечения).
2. Определяет дальнейшую тактику (наблюдение или повторное вмешательство).
3. Позволяет провести повторное лечение максимально эффективно и безопасно.
4. Соответствует международным клиническим рекомендациям.
Лечение артериальной гипертензии
- Рекомендуется контроль и управление артериальным давлением пациентам с геморрагическим инсультом с целью предотвращения повторных кровоизлияний [402, 420].
Уровень убедительности рекомендаций B (уровень достоверности доказательств - 2)
Комментарии: В исследовании Biffi A. И соавт. [421] со средним периодам наблюдения 36,8 месяцев было определено, что повторные кровоизлияния чаще случаются при лобарном расположении гематомы (102 из 505 случаев), чем при нелобарном (44 из 640 случаев). Частота гематом у пациентов с недостаточным контролем АД составила 84 случая на 1000 человеко-лет, а при успешном контроле АД - 49 случаев на 1000 человеко-лет. Риск рецидива внутримозгового кровоизлияния составил 3,53 (95% ДИ 1,65 - 7,54), невнутримозгового - 4,23 (95% ДИ 1,02 - 17,52). Систолическое АД было ассоциировано с повышенным риском развития рецидива как лобарного кровоизлияния (ОР 1,21, 95% ДИ 1,02 - 1,76 при повышении АД на 10 мм рт. ст.), так и нелобарного кровоизлияния (ОР 1,54, 95% ДИ 1,03 - 2,30).
- Рекомендуется снижение АД до 130 и 80 мм рт. ст. в долгосрочной перспективе пациентам с геморрагическим инсультом для предотвращения повторных кровоизлияний [309, 420].
Уровень убедительности рекомендаций B (уровень достоверности доказательств - 2)
Комментарии: В крупном проспективном когортном исследовании с участием 1145 пациентов с внутричерепной гематомой риск рецидива кровоизлияния был значительно выше у пациентов с САД ![]() 120 мм рт. ст. и ДАД
120 мм рт. ст. и ДАД ![]() 80 мм рт. ст. по сравнению с пациентами, у которых САД < 120 мм рт. ст. и ДАД <80 мм рт. ст. [420]. В исследовании PRoFESS (режим профилактики для эффективного предотвращения повторного инсульта) риск развития ВМГ во время наблюдения был выше у пациентов с САД
80 мм рт. ст. по сравнению с пациентами, у которых САД < 120 мм рт. ст. и ДАД <80 мм рт. ст. [420]. В исследовании PRoFESS (режим профилактики для эффективного предотвращения повторного инсульта) риск развития ВМГ во время наблюдения был выше у пациентов с САД ![]() 160 мм рт. ст. по сравнению с пациентами с САД от 130 до 139 мм рт. ст. (ОР 2,07 [95% ДИ 1,22 - 3,51]), при этом обнаружена статистически незначимая тенденция к снижению частоты внутричерепной гематомы при САД < 130 мм рт. ст. [422].
160 мм рт. ст. по сравнению с пациентами с САД от 130 до 139 мм рт. ст. (ОР 2,07 [95% ДИ 1,22 - 3,51]), при этом обнаружена статистически незначимая тенденция к снижению частоты внутричерепной гематомы при САД < 130 мм рт. ст. [422].
Антикоагулянтная терапия
- Рекомендуется возобновление терапии оральными антикоагулянтами (В01АА Антагонисты витамина К) в сроки 4 - 8 недель после развития гематомы пациентам с гипертензивной внутримозговой гематомой и неклапанной фибрилляцией предсердий с целью профилактики тромбоэмболических событий [136, 401, 404, 422, 423].
Уровень убедительности рекомендаций B (уровень достоверности доказательств - 2)
Комментарии: До настоящего времени нет четкого понимания времени назначения оральных антикоагулянтов (B01AA Антагонисты витамина К) у пациентов со гипертензивной ВМГ и фибрилляцией предсердий [424]. Исследования, в которых пациентам назначали #варфарин**, ориентированы на срок старта терапии 4 - 8 недель после развития внутримозговой гематомы [139], в исследовании APACHE-AF, среднее время старта терапии составило 46 дней, средний период наблюдения составил 1 - 9 лет (IQR 1,0 - 3,1; 222 человеко-лет), нефатальный инсульт или сосудистая смерть произошли у 13 (26%) участников, получавших #апиксабан** (годовая частота событий 12,6% [95% ДИ 6,7 - 21,5]) и у 12 (24%) в группе без антикоагулянтной терапии (11,9% [95% ДИ 6,2 - 20,8]; скорректированный ОР 1,05 [95% ДИ 0·48 - 2·31]; p = 0,90) [425]. В открытом рандомизированном пилотном исследовании SoSTART оральные антикоагулянты (B01AA Антагонисты витамина К) назначались в среднем на 115 день (IQR 49 - 265). У 8% из 101 человека в группе начала приема оральных антикоагулянтов (B01AA Антагонисты витамина K) и у 4% из 102 человек в группе отказа от приема оральных антикоагулянтов (B01AA Антагонисты витамина К) наблюдались рецидивы внутричерепного кровоизлияния (скорректированный ОР 2,42 [95% ДИ 0,72 - 8,09]; p = 0,152) [423].
- Рекомендуется закрытие ушка левого предсердия (A16.12.041.007 Эндоваскулярная окклюзия ушка левого предсердия) пациентам с фибрилляцией предсердий и геморрагическим инсультом, которым не подходит антикоагулянтная терапия, для снижения риска тромбоэмболических событий [290, 426].
Уровень убедительности рекомендаций B (уровень достоверности доказательств - 2)
Комментарии: Пациентам с ФП и нВЧК, которым не подходит антикоагулянтная терапия (например, не выключенная аневризма при САК) требует рассмотрения хирургической профилактики сосудистых событий.
Два метаанализа исследования PROTECT-AF (WATCHMAN и исследования PREVAIL WATCHMAN сообщили, что частота ишемического инсульта, а также частота геморрагического инсульта и кровотечения была ниже в группе закрытием ушка левого предсердия (A16.12.041.007 Эндоваскулярная окклюзия ушка левого предсердия), а сердечно-сосудистая смерть была схожей во всех группах лечения [304,426]. У пациентов с анамнезом нВЧК и ФП данные небольшой, нерандомизированной, ретроспективной когорты также показала более низкую сердечно-сосудистую смертность, смертность от всех причин, риск геморрагического инсульта и крупные кровотечения события при закрытии ушка левого предсердия (A16.12.041.007 Эндоваскулярная окклюзия ушка левого предсердия) по сравнению со стандартной медикаментозной терапией [428].
Другие небольшие ретроспективные исследования сообщили о низких частотах событий, аналогичных частотам у пациентов без нВЧК и без ишемического инсульта или нВЧК в течение 30 дней после закрытия ушка левого предсердия (A16.12.041.007 Эндоваскулярная окклюзия ушка левого предсердия) среди пациентов с диагнозом церебральная амилоидная ангиопатия [429].
- Рекомендуется раннее назначение антагонистов витамина K (с 6 по 14 день) пациентам с гипертензивной ВМГ и механическими клапанами в сердце для профилактики ишемических событий эмболического генеза [428, 430].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4)
Комментарии: В одном исследовании [430], проведенном у пациентов с механическими клапанами в сердце, сообщалось, что, хотя число геморрагических осложнений значительно увеличивалось при возобновлении антикоагуляции в терапевтических дозах до 14-го дня после развития гипертензивной ВМГ, посчитанный совокупный риск кровотечения и тромбоэмболии позволял предположить, что антикоагуляция в терапевтических дозах может быть рассмотрена у пациентов с механическими клапанами уже на 6-й день после внутримозговой гематомы. Еще одно исследование [431] показало, что у пациентов с вспомогательными устройствами в левом желудочке возобновление антикоагуляции с помощью #варфарина** в среднем через 14 дней после кровоизлияния в мозг было связано с меньшим количеством смертельных и несмертельных тромботических осложнений, чем возобновление только антитромбоцитарной терапии, при одинаковой частоте рецидивов кровоизлияния в мозг.
Гиполипидемическая терапия
- Рекомендуется нестатиновое гиполипидемическое лечение ингибиторами PCSK9 (C10AX Прочие гиполипидемические средства) пациентов с очень высоким риском развития геморрагического инсульта [432 - 436].
Уровень убедительности рекомендаций B (уровень достоверности доказательств - 2)
Комментарии: У пациентов с нВЧК и установленными показаниями к фармакотерапии ингибиторами ГМГ-КоА-редуктазы риски и польза терапии ингибиторами ГМГ-КоА-редуктазы в отношении исходов и рецидивов нВЧК по сравнению с общей профилактикой сердечно-сосудистых осложнений не ясны. В настоящее время нет консенсуса относительно оптимальной стратегии лечения гиперлипидемии после нВЧК. Связь применения ингибиторов ГМГ-КоА-редуктазы как с острыми исходами, так и со снижением рецидивирующих сосудистых событий у пациентов, перенесших нВЧК, не определена.
Исследование SPARCL выявило повышенный риск ICH при использовании высоких доз аторвастатина** в условиях липопротеинов очень низкой плотности. Дополнительные нерандомизированные, обсервационные исследования не обнаружили связи с использованием ингибиторов ГМГ-КоА-редуктазы у пациентов с ВМК [432, 433].
Другие ретроспективные анализы предполагают потенциал для улучшения результатов после нВЧК с использованием ингибиторов ГМГ-КоА-редуктазы и снижение краткосрочной и долгосрочной смертности при использовании ингибиторов ГМГ-КоА-редуктазы. Однако результаты следует интерпретировать с осторожностью из-за смещения отбора и искажения показаний в этих нерандомизированных исследованиях. Учитывая эту неопределенность, решение об использовании ингибиторов ГМГ-КоА-редуктазы у пациентов с нВЧК зависит от оценки риска ишемических сердечно-сосудистых и цереброваскулярных событий по сравнению с рецидивирующим нВЧК. Клинические испытания препаратов (С10АХ Прочие гиполипидемические средства) до сих пор не предполагали повышенного риска первого нВЧК, но еще не изучали риск рецидива у пациентов с предшествующим ВМК [434 - 436].
- Не рекомендуется регулярный длительный прием нестероидных противовоспалительных и противоревматических препаратов (НПВП) пациентами с геморрагическим инсультом в связи с потенциально повышенным риском кровотечения [412, 432].
Уровень убедительности рекомендаций B (уровень достоверности доказательств - 2)
Комментарии: Использование НПВП связано с повышенным риском кровотечения. Общая частота событий нВЧК низкая в общей популяции, но большой метаанализ обсервационных исследований выявил повышенный риск геморрагического инсульта при использовании диклофенака** и мелоксикама [432]. Последующий большой метаанализ выявил повышенный риск нВЧК при использовании любого НПВП.610 Одно небольшое исследование пациентов с нВЧК с краткосрочными результатами не обнаружило связи между использованием НПВП и результатами и рецидивирующим нВЧК, но последующее наблюдение было ограничено 90 днями [433].
5.2 Диспансерное наблюдение пациентов
Всем пациентам с геморрагическим инсультом после выписки из стационара проводится диспансерное наблюдение. В соответствии с Приказом Министерства здравоохранения РФ от 15 марта 2022 г. N 168н "Об утверждении порядка проведения диспансерного наблюдения за взрослыми", диспансерное наблюдение пациентов, перенесших геморрагический инсульт, в течение 24 месяцев после оказания медицинской помощи в стационарных условиях медицинских организаций, осуществляется врачом-терапевтом, в первый год диспансерного наблюдения не реже 1 раз в 3 месяца, затем не реже 1 раза в 6 месяцев. Контролируемые показатели здоровья включают измерение АД на периферических артериях, измерение ЧСС, исследование уровня холестерина липопротеинов низкой плотности (A09.05.028), регистрация ЭКГ (A05.10.006), при терапии ингибиторами ГМГ-КоА-редуктазы - трансаминазы (A09.05.041 Определение активности аспартатаминотрансферазы в крови, A09.05.04 Определение активности аланинаминотрансферазы в крови 2) и КФК (A09.05.043 Определение активности креатинкиназы в крови) (через 4 недели от начала терапии или при мышечных симптомах). По медицинским показаниям могут быть назначены дополнительные профилактические, диагностические, лечебные и реабилитационные мероприятия. Целесообразно проведение оценки наличия/риска развития спастичности у пациентов, перенесших геморрагический инсульт в рамках диспансерного наблюдения и направления на медицинскую реабилитацию с применением ботулинотерапии с целью увеличения эффективности реабилитационных мероприятий и улучшения функционального восстановления. Также рекомендуется, при наличии медицинских показаний прием (осмотр, консультация) врача-невролога, врача-нейрохирурга, врача-сердечно-сосудистого хирурга, врача-кардиолога при неэффективности медикаментозной терапии (рефрактерные симптомы, недостижение целевых уровней АД, ЧСС, ХС-ЛПНП).
- Рекомендуется проведение первого контрольного ангиографического исследования (КТА или ЦАГ после микрохирургического выключения аневризмы из кровотока; ЦАГ или МРА после эндоваскулярного выключения аневризмы из кровотока) в течение первых 3 - 12 месяцев после операции с последующей консультацией врача-нейрохирурга [208].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
- Рекомендуется проведение повторных контрольных ангиографических исследований (КТА или ЦАГ после микрохирургического выключения аневризмы из кровотока; ЦАГ или МРА после эндоваскулярного выключения аневризмы из кровотока) у пациентов с высокими рисками рецидивирования заболевания с последующей консультацией нейрохирурга [208].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
Комментарий: К группе пациентов с высокими рисками рецидивирования аневризмы головного мозга относят больных с неполным выключением аневризмы из кровотока, наличием пришеечной части аневризмы, с наличием семейного анамнеза, с наличием инфундибулярных расширений устьев интракраниальных артерий, с наличием ряда ассоциированных с аневризмами заболеваний (генетически обусловленные соединительно-тканные заболевания - аутосомно-доминантный поликистоз почек; синдром Элерса-Данло IV типа, синдром Марфана и др.). Периодичность проведения контрольных ангиографических исследований устанавливается индивидуально.
- Рекомендуется длительное диспансерное наблюдение пациентам с артериовенозной мальформацией независимо от проводимых лечебных мероприятий и их эффективности [437, 438].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
Комментарии: целью наблюдения является выявление прогрессирования, рецидива заболевания, коррекции эпилептического синдрома. У пациентов, оперированных по поводу АВМ, в послеоперационном периоде возможно развитие повторного внутричерепного кровоизлияния. Наиболее частыми причинами этих осложнений являются: реканализация мальформаций, резидуальная часть мальформации, сопутствующая аневризма. Продолжительность диспансерного наблюдения: после эрадикации АВМ и отсутствии клинических проявлений - не менее 5 лет; во всех остальных случаях - пожизненно.
Группы наблюдения:
1) пациенты с неоперабельными АВМ;
2) пациенты с резидуальными АВМ после вмешательств;
3) пациенты после эрадикации (удаления, тотальной облитерации) АВМ;
4) пациенты после радиохирургического лечения АВМ.
В большинстве случаев содержание диспансерного наблюдения ограничивается проведением коррекции эпилептиформного синдрома, контроля состояния АВМ.
- Рекомендуется диспансерное наблюдение врачом-неврологом пациентов с гипертензивными внутримозговыми гематомами определяется индивидуально для каждого пациента, не менее 6 месяцев после операции с проведением дальнейших этапов реабилитации [37].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
5.3 Паллиативная помощь
- Рекомендуется паллиативная помощь пациентам с геморрагическим инсультом и градацией оценки по шкале ШРМ 5 - 6 с целью облегчения страданий умирающим пациентам, минимизации нагрузки на членов семьи [439].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
Комментарии: Шкала ШРМ см. приложение Г21.
- Рекомендуется при определении прогноза выживаемости и исхода у пациента после инсульта врачам использовать наилучшие способы оценки и клинический опыт врача [439].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
Комментарии: Наилучшим способом оценки в настоящее время является ШРМ. Разделение этапов оказания помощи при инсульте (инсультное отделение, отделение реабилитации, дом престарелых) может улучшить качество помощи в конкретном месте, но затруднить оценку глобальной перспективы, если существует фрагментарная коммуникация между различными специалистами (врачами-неврологами, анестезиологами-реаниматологами, врачами-нейрохирургами, врачами-физиотерапевтами, персоналом отделений паллиативной помощи, врачами-гериатрами) и учреждениями. Большинство специалистов получают ограниченную подготовку по навыкам общения для оказания помощи, ориентированной на пациента. Однако, пациентоориентированность как стратегия общения с пациентами, перенесшими инсульт, и членами их семей может повысить удовлетворенность, безопасность и результаты лечения [440]. Знание и использование эффективных методов коммуникации является важнейшей ключевой компетенцией для повышения качества принятия решений при инсульте, а также удовлетворенности пациентов и их семей, а также результатов лечения (см. в Приложении А3).
- Рекомендуется принимать решения о проведении жизнеобеспечивающей терапии или процедур на основе общих целей лечения с учетом индивидуальной оценки общей пользы и риска каждого вида лечения, а также предпочтений и ценностей пациента [439].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
Комментарии: Установление целей лечения требует прогнозирования вероятности выживания и качества жизни. В зависимости от стадии заболевания, состояния здоровья пациента и тяжести инсульта, решения, учитывающие предпочтения, могут охватывать весь спектр доступных методов лечения, от различных форм агрессивных реанимационных мероприятий до ограниченных по времени пробных методов лечения, которые обычно не считаются обременительными [420, 422].
6. Организация оказания медицинской помощи
Показания для госпитализации в медицинскую организацию
Все пациенты с ГИ подлежат госпитализации.
При подозрении на ГИ обращение за экстренной медицинской помощью происходит через систему скорой медицинской помощи.
Служба СМП рассматривает вызовы по поводу ГИ как приоритетные и обеспечивает максимально быстрое прибытие медицинского персонала к пациенту.
Служба СМП, осуществляющая медицинскую эвакуацию пациента с ГИ, заранее уведомляет принимающую медицинскую организацию о том, что ожидается прибытие пациента с подозрением на ГИ, с указанием приблизительного времени доезда.
Всем пациентам с предположительным диагнозом ГИ проводится экстренная госпитализация в медицинскую организацию, в структуре которой развернуто неврологическое отделение для лечения пациентов с ОНМК.
Организация консультативной нейрохирургической помощи
После установки диагноза геморрагического инсульта всем пациентам необходимо организовать консультацию врача-нейрохирурга, в том числе с использованием телемедицинских технологий, в течение 60 минут после получения результатов КТ/МРТ-исследования для решения вопроса о необходимости перевода пациента в нейрохирургический стационар.
При отсутствии возможности круглосуточного описания результатов КТ исследований и недоступности системы телерентгенологии для своевременного описания результатов КТ целесообразно применять программное обеспечение для интерпретации рентгеновских изображений на основе технологии искусственного интеллекта в качестве системы помощи принятия врачебных решений при подозрении на ГИ.
Телемедицинские консультации проводятся с участием специалистов (врача-нейрохирурга, врача рентгеноэндоваскулярных методов диагностики и лечения, врача-анестезиолога-реаниматолога и др.).
В ходе телемедицинской консультации возможно обсуждение плана обследования и тактики лечения пациента, а также согласование условий перевода пациента в другой стационар.
Пациентам с ГИ (в том числе с САК) организована круглосуточная консультативная помощь, которая осуществляется выездными консультативными нейрохирургическими бригадами, сформированными на базе отделений по оказанию хирургической помощи пациентам с острой сосудистой патологией головного мозга (как правило, на базе многопрофильного стационара).
Пациенты с геморрагическим инсультом подлежат госпитализации/переводу в медицинскую организацию, где имеются:
А. Нейрохирургическое отделение;
Б. Специалисты, владеющие опытом прямых микрохирургических операций по поводу АГМ, АВМ, гипертензивных ВМГ;
В. Специалисты, владеющие опытом эндоваскулярного выключения АГМ и АВМ;
Г. Специалисты, владеющие опытом минимально инвазивной хирургии гипертензивных ВМГ;
Д. Отделение лучевой диагностики, оснащенное аппаратурой для проведения КТ или МРТ, КТА, МРА.
Е. Ангиографическая операционная для проведения церебральной ангиографии (ЦАГ) и выполнения эндоваскулярных операций;
Ж. Операционная, оснащенная оборудованием в соответствии с действующим Порядком оказания медицинской помощи пациентам с ОНМК;
З. Отделение нейрореанимации/блок интенсивной терапии и реанимации для пациентов с ОНМК;
И. Неврологическое отделение для больных с ОНМК.
Перевод пациента с геморрагическим инсультом из нейрохирургического стационар в неврологический стационар для дальнейшего восстановительного лечения показан при удовлетворительном заживлении послеоперационной раны и отсутствии хирургических осложнений.
Показания к выписке пациента из медицинской организации
Выписка пациента осуществляется в зависимости от состояния по Шкале реабилитационной маршрутизации (ШРМ).
ШРМ 0 - 1 балл - пациент не нуждается в продолжении медицинской реабилитации.
ШРМ 2 - 3 балла - пациент направляется на третий этап медицинской реабилитации в медицинскую организацию первой, второй, третьей и четвертой групп, определяемых в соответствии с Порядком организации медицинской реабилитации взрослых, утвержденным Приказом Министерства здравоохранения Российской Федерации от 31 июля 2020 г. N 788н.
ШРМ 4 - 5 баллов - пациент направляется на второй этап медицинской реабилитации в медицинскую организацию второй, третьей и четвертой групп.
ШРМ 4 - 6 баллов - пациент направляется на второй этап медицинской реабилитации в медицинскую организацию третьей и четвертой групп.
Медицинская реабилитация на втором и третьем этапах осуществляется в отделении медицинской реабилитации пациентов с нарушением функции центральной нервной системы.
Образовательные мероприятия для населения и медицинских специалистов
Специалистам в области организации здравоохранения и общественного здоровья необходимо обеспечить проведение регулярных образовательных мероприятий по оказанию специализированной медицинской помощи при ОНМК для врачей, персонала больниц и службы СМП с целью повышения качества медицинской помощи.
Специалистам в области организации здравоохранения и общественного здоровья необходимо разрабатывать и внедрять общественные образовательные мероприятия, ориентированные на информирование населения о системе оказания медицинской помощи при инсульте и необходимости быстрого обращения за экстренной медицинской помощью при начале заболевания с целью улучшения исхода заболевания.
Региональным организаторам здравоохранения необходимо разработать алгоритмы сортировки и протоколы маршрутизации пациентов с ОНМК, направленные на обеспечение быстрой доставки в медицинскую организацию соответствующего уровня помощи, с целью улучшения исхода заболевания.
7. Дополнительная информация (в том числе факторы, влияющие на исход заболевания или состояния)
Крупные медицинские стационары (национальные и федеральные нейрохирургические центры, областные, краевые и республиканские клинические больницы), оказывающие специализированную помощь пациентам с ГИ (в том числе с САК), на основании собственных научных исследований и практического опыта могут разрабатывать и утверждать на заседании врачебной комиссии (за подписью главврача) или заседании кафедр, аккредитованных для преподавания специальностей "нейрохирургия" и/или "неврология" (за подписью заведующего кафедры) собственные ("внутренние") протоколы лечения пациентов с ГИ.
"Внутренний" протокол лечения пациентов с ГИ в рамках конкретного стационара может вносить дополнения, но не должен вступать в противоречие с основными положениями настоящих клинических рекомендаций.
Критерии оценки качества медицинской помощи
N п/п
Критерии оценки качества
Оценка выполнения
1.
Выполнена компьютерная томография головного мозга или магнитно-резонансная томография головного мозга не позднее 40 минут от момента поступления в стационар
Да/Нет
2.
Выполнен прием (осмотр, консультация) врача-нейрохирурга в срок не позднее 60 минут с момента получения результатов компьютерной томографии больному, у которого по заключению компьютерной томографии или магнитно-резонансной томографии установлены признаки геморрагического инсульта
Да/Нет
3.
Выполнена оценка состоятельности глотания при помощи теста оценки глотания ("трехглотковая проба" с использованием пульсоксиметра) в течение первых 3 часов пребывания пациента в стационаре
Да/Нет
4.
Выполнено хирургическое лечение по поводу удаления внутримозговой гематомы
Да/Нет
5.
Выполнено хиругическое лечение по поводу разорвавшейся аневризмы в остром периоде кровоизлияния
Да/Нет
6.
Выполнена компьютерная томография головного мозга в течение 24 часов после хирургического лечения
Да/Нет
7.
Выполнены лечебная физкультура при заболеваниях центральной нервной системы и головного мозга, и (или) лечебная физкультура с использованием аппаратов и тренажеров при заболеваниях центральной нервной системы и головного мозга, и (или) постуральная коррекция, и (или) эрготерапия, и (или) медико-логопедическое исследование при дисфагии, и (или) медико-логопедическая процедура при афазии, и (или) медико-логопедическая процедура при дизартрии не позднее 48 часов от момента поступления в стационар
Да/Нет
8.
Выполнена компьютерно-томографическая ангиография, или магнитно-резонансная ангиография, или церебральная ангиография для выявления источника кровоизлияния при подозрении на разрыв аневризмы или артериовенозной мальформации по данным компьютерной томографии головного мозга и (или) магнитно-резонансной томографии головного мозга, а также у пациентов моложе 45 лет и при отсутствии гипертонического анамнеза
Да/Нет
Список литературы
1. Крылов В.В., Дашьян В.Г., Винокуров А.Г. и др. Микрохирургия аневризм сосудов головного мозга. Москва: АБВ-пресс, 2022.
2. Morales-Valero S.F. et al. Are parenchymal AVMs congenital lesions?//Neurosurg. Focus. 2014. Vol. 37, N 3. P. E2.
3. Aboian M.S. et al. The putative role of the venous system in the genesis of vascular malformations//Neurosurg. Focus. 2009. Vol. 27, N 5. P. E9.
4. Godkov I.M. et al. Comparative analysis of the results of endoscopic surgery and external ventricular drainage in patients with intraventricular hemorrhage//Russ. J. Neurosurg. 2022. Vol. 24, N 2. P. 25 - 34.
5. Greenberg S.M. et al. 2022 Guideline for the Management of Patients With Spontaneous Intracerebral Hemorrhage: A Guideline From the American Heart Association/American Stroke Association//Stroke. 2022. Vol. 53, N 7.
6. Крылов В.В., Гехт А.Б., Григорьев А.Ю. и др. Нейрохирургия и нейрореаниматология/ed. под редакцией академика РАН профессора В.В. Крылова. Москва: АБВ-пресс, 2018. Vol. 783.
7. Крылов В.В. et al. Хирургия тяжелой черепно-мозговой травмы. Москва: АБВ-пресс, 2022. Vol. 282.
8. Крылов В.В. et al. Хирургия геморрагического инсульта. Москва: Медицина, 2012. Vol. 336.
9. Ворлоу Ч.П. Инсульт: Практическое руководство для ведения больных: Пер. с англ./ed. Скоромец А.А. С.В.А. Санкт-Петербург: Политехника, 1998. Vol. 629.
10. Teasdale G., Jennett B. ASSESSMENT OF COMA AND IMPAIRED CONSCIOUSNESS//Lancet. 1974. Vol. 304, N 7872. P. 81 - 84.
11. Fisher C.M., Kistler J.P., Davis J.M. Relation of Cerebral Vasospasm to Subarachnoid Hemorrhage Visualized by Computerized Tomographic Scanning//Neurosurgery. 1980. Vol. 6, N 1. P. 1 - 9.
12. Frontera J.A. et al. PREDICTION OF SYMPTOMATIC VASOSPASMAFTER SUBARACHNOID HEMORRHAGE//Neurosurgery. 2006. Vol. 59, N 1. P. 21 - 27.
13. Graeb D.A. et al. Computed tomographic diagnosis of intraventricular hemorrhage. Etiology and prognosis.//Radiology. 1982. Vol. 143, N 1. P. 91 - 96.
14. Eliava S.S. et al. The principles for choosing a surgical technique for patients with acute cerebral aneurysm rupture//Vopr. neirokhirurgii Im. N.N. Burdenko. 2016. Vol. 80, N 5. P. 15.
15. Pilipenko Y. V. et al. Reasonability and efficacy of decompressive craniectomy in patients with subarachnoid hemorrhage after microsurgical aneurysm exclusion//Vopr. neirokhirurgii Im. N.N. Burdenko. 2018. Vol. 82, N 1. P. 59.
16. Connolly E.S. et al. Guidelines for the Management of Aneurysmal Subarachnoid Hemorrhage//Stroke. 2012. Vol. 43, N 6. P. 1711 - 1737.
17. Diringer M.N. et al. Critical Care Management of Patients Following Aneurysmal Subarachnoid Hemorrhage: Recommendations from the Neurocritical Care Society's Multidisciplinary Consensus Conference//Neurocrit. Care. 2011. Vol. 15, N 2. P. 211.
18. Hunt W.E., Hess R.M. Surgical risk as related to time of intervention in the repair of intracranial aneurysms//J. Neurosurg. 1968. Vol. 28. P. 14 - 20.
19. Fernandez-L A. et al. Hereditary Hemorrhagic Telangiectasia, a Vascular Dysplasia Affecting the TGF-Signaling Pathway//Clin. Med. Res. 2006. Vol. 4, N 1. P. 66 - 78.
20. Macmurdo C.F. et al. RASA1 somatic mutation and variable expressivity in capillary malformation/arteriovenous malformation (CM/AVM) syndrome//Am. J. Med. Genet. Part A. 2016. Vol. 170, N 6. P. 1450 - 1454.
21. Nishida T. et al. Brain arteriovenous malformations associated with hereditary hemorrhagic telangiectasia: Gene-phenotype correlations//Am. J. Med. Genet. Part A. 2012. Vol. 158A, N 11. P. 2829 - 2834.
22. Saleh M. et al. Brain Arteriovenous Malformations in Patients With Hereditary Hemorrhagic Telangiectasia: Clinical Presentation and Anatomical Distribution//Pediatr. Neurol. 2013. Vol. 49, N 6. P. 445 - 450.
23. Delgado Almandoz J.E., Romero J.M. Advanced CT Imaging in the Evaluation of Hemorrhagic Stroke//Neuroimaging Clin. N. Am. 2011. Vol. 21, N 2. P. 197 - 213.
24. Skidmore C.T., Andrefsky J. Spontaneous intracerebral hemorrhage: epidemiology, pathophysiology, and medical management//Neurosurg. Clin. N. Am. 2002. Vol. 13, N 3. P. 281 - 288.
25. Evidence-Based Guidelines for the Management of Aneurysmal Subarachnoid Hemorrhage English Edition//Neurol. Med. Chir. (Tokyo). 2012. Vol. 52, N 6. P. 355 - 429.
26. Kassell N.F. et al. The International Cooperative Studyon the Timing of Aneurysm Surgery//J. Neurosurg. 1990. Vol. 73, N 1. P. 18 - 36.
27. Hoh B.L. et al. 2023 Guideline for the Management of Patients With Aneurysmal Subarachnoid Hemorrhage: A Guideline From the American Heart Association/American Stroke Association//Stroke. 2023. Vol. 54, N 7.
28. Michelsen J.W. Natural History and Pathophysiology of Arteriovenous Malformations//Neurosurgery. 1979. Vol. 26, N Supplement 1. P. 307 - 313.
29. Al-Shahi R. Prevalence of adults with brain arteriovenous malformations: a community based study in Scotland using capture-recapture analysis//J. Neurol. Neurosurg. Psychiatry. 2002. Vol. 73, N 5. P. 547 - 551.
30. Starke R.M. et al. Treatment guidelines for cerebral arteriovenous malformation microsurgery//Br. J. Neurosurg. 2009. Vol. 23, N 4. P. 376 - 386.
31. Aoun S.G., Bendok B.R., Batjer H.H. Acute Management of Ruptured Arteriovenous Malformations and Dural Arteriovenous Fistulas//Neurosurg. Clin. N. Am. 2012. Vol. 23, N 1. P. 87 - 103.
32. Stapf C. et al. Predictors of hemorrhage in patients with untreated brain arteriovenous malformation//Neurology. 2006. Vol. 66, N 9. P. 1350 - 1355.
33. Stein K.-P. et al. Associated Aneurysms in Supratentorial Arteriovenous Malformations: Impact of Aneurysm Size on Haemorrhage//Cerebrovasc. Dis. 2015. Vol. 39, N 2. P. 122 - 129.
34. Redekop G. et al. Arterial aneurysms associated with cerebral arteriovenous malformations: classification, incidence, and risk of hemorrhage//J. Neurosurg. 1998. Vol. 89, N 4. P. 539 - 546.
35. Kim E.J. et al. THE RELATIONSHIP OF COEXISTING EXTRANIDAL ANEURYSMS TO INTRACRANIAL HEMORRHAGE IN PATIENTS HARBORING BRAIN ARTERIOVENOUS MALFORMATIONS//Neurosurgery. 2004. Vol. 54, N 6. P. 1349 - 1358.
36. Platz J. et al. Frequency, risk of hemorrhage and treatment considerations for cerebral arteriovenous malformations with associated aneurysms//Acta Neurochir. (Wien). 2014. Vol. 156, N 11. P. 2025 - 2034.
37. Hemphill J.C. et al. Guidelines for the Management of Spontaneous Intracerebral Hemorrhage//Stroke. 2015. Vol. 46, N 7. P. 2032 - 2060.
38. Hemphill J.C. et al. The ICH Score//Stroke. 2001. Vol. 32, N 4. P. 891 - 897.
39. Broderick J.P. et al. Volume of intracerebral hemorrhage. A powerful and easy-to-use predictor of 30-day mortality.//Stroke. 1993. Vol. 24, N 7. P. 987 - 993.
40. Клинические рекомендации "Геморрагический инсульт", 2022 год https://ruans.org/Text/Guidelines/hemorrhagic-stroke-2022.pdf [Electronic resource].
41. Pritz M.B. Cerebral Aneurysm Classification Based on Angioarchitecture//J. Stroke Cerebrovasc. Dis. 2011. Vol. 20, N 2. P. 162 - 167.
42. Rice-Canetto T.E. et al. A Review of the Current Literature on Cerebral Aneurysms//Cureus. 2025.
43. Merritt W.C. et al. Definitions of intracranial aneurysm size and morphology: A call for standardization.//Surg. Neurol. Int. 2021. Vol. 12. P. 506.
44. Spetzler R.F., Martin N.A. A proposed grading system for arteriovenous malformations//J. Neurosurg. 1986. Vol. 65, N 4. P. 476 - 483.
45. Spetzler R.F., Ponce F.A. A 3-tier classification of cerebral arteriovenous malformations//J. Neurosurg. 2011. Vol. 114, N 3. P. 842 - 849.
46. Frisoli F.A. et al. Spetzler-Martin Grade III Arteriovenous Malformations: A Comparison of Modified and Supplemented Spetzler-Martin Grading Systems//Neurosurgery. 2021. Vol. 88, N 6. P. 1103 - 1110.
47. Lawton M.T. et al. A Supplementary Grading Scale for Selecting Patients With Brain Arteriovenous Malformations for Surgery//Neurosurgery. 2010. Vol. 66, N 4. P. 702 - 713.
48. Kim H. et al. Validation of the Supplemented Spetzler-Martin Grading System for Brain Arteriovenous Malformations in a Multicenter Cohort of 1009 Surgical Patients//Neurosurgery. 2015. Vol. 76, N 1. P. 25 - 33.
49. Pollock B.E., Flickinger J.C. A proposed radiosurgery-based grading system for arteriovenous malformations//J. Neurosurg. 2002. Vol. 96, N 1. P. 79 - 85.
50. Pollock B.E., Flickinger J.C. MODIFICATION OF THE RADIOSURGERY-BASED ARTERIOVENOUS MALFORMATION GRADING SYSTEM//Neurosurgery. 2008. Vol. 63, N 2. P. 239 - 243.
51. Starke R.M. et al. A practical grading scale for predicting outcome after radiosurgery for arteriovenous malformations: analysis of 1012 treated patients//J. Neurosurg. 2013. Vol. 119, N 4. P. 981 - 987.
52. Recommendations for the Management of Intracranial Haemorrhage - Part I: Spontaneous Intracerebral Haemorrhage//Cerebrovasc. Dis. 2006. Vol. 22, N 4. P. 294 - 316.
53. Qureshi A.I., Mendelow A.D., Hanley D.F. Intracerebral haemorrhage//Lancet. 2009. Vol. 373, N 9675. P. 1632 - 1644.
54. Vespa P.M. et al. Acute seizures after intracerebral hemorrhage//Neurology. 2003. Vol. 60, N 9. P. 1441 - 1446.
55. Mayer S.A. et al. Recombinant Activated Factor VII for Acute Intracerebral Hemorrhage//N. Engl. J. Med. 2005. Vol. 352, N 8. P. 777 - 785.
56. Геморрагический инсульт. Практическое руководство/ed. под ред. Скворцовой В.И. К.В.В. Москва: ГЭОТАР-Медиа, 2005. Vol. 160.
57. Diringer M.N. Management of aneurysmal subarachnoid hemorrhage//Crit. Care Med. 2009. Vol. 37, N 2. P. 432 - 440.
58. Крылов В.В., Дмитриев А.Ю. Клиника и диагностика артериовенозных мальформаций в остром периоде кровоизлияния//Неврологический журнал. 2008. Vol. 13, N 4. P. 26 - 30.
59. Graf C.J., Perret G.E., Torner J.C. Bleeding from cerebral arteriovenous malformations as part of their natural history//J. Neurosurg. 1983. Vol. 58, N 3. P. 331 - 337.
60. Крылов В.В., Лебедев В.В. Неотложная нейрохирургия: Руководство для врачей. Москва: Медицина, 2000. Vol. 568. 506 - 530 p.
61. Smith E.E. et al. A risk score for in-hospital death in patients admitted with ischemic or hemorrhagic stroke.//J. Am. Heart Assoc. 2013. Vol. 2, N 1. P. e005207.
62. Goldstein L.B. Is This Patient Having a Stroke?//JAMA. 2005. Vol. 293, N 19. P. 2391.
63. Starke R.M. et al. Evaluation of a revised Glasgow Coma Score scale in predicting long-term outcome of poor grade aneurysmal subarachnoid hemorrhage patients//J. Clin. Neurosci. 2009. Vol. 16, N 7. P. 894 - 899.
64. Cote R. et al. The Canadian Neurological Scale: Validation and reliability assessment//Neurology. 1989. Vol. 39. P. 638 - 643.
65. Allen C.M. Predicting the outcome of acute stroke: a prognostic score.//J. Neurol. Neurosurg. Psychiatry. 1984. Vol. 47, N 5. P. 475 - 480.
66. Bruce S.S. et al. A Comparative Evaluation of Existing Grading Scales in Intracerebral Hemorrhage//Neurocrit. Care. 2011. Vol. 15, N 3. P. 498 - 505.
67. Hage V. The NIH stroke scale: a window into neurological status//Nurs. Spectr. 2011. Vol. 24, N 15. P. 44 - 49.
68. Sherman V., Greco E., Martino R. The Benefit of Dysphagia Screening in Adult Patients With Stroke: A Meta-Analysis.//J. Am. Heart Assoc. 2021. Vol. 10, N 12. P. e018753.
69. Martino R. et al. Dysphagia After Stroke//Stroke. 2005. Vol. 36, N 12. P. 2756 - 2763.
70. Feng M.-C. et al. The Mortality and the Risk of Aspiration Pneumonia Related with Dysphagia in Stroke Patients//J. Stroke Cerebrovasc. Dis. 2019. Vol. 28, N 5. P. 1381 - 1387.
71.  ,
,  ,
,  Prognostic Role of Mean Platelet Volume and Platelet Count in Ischemic and Hemorrhagic Stroke//J. Stroke Cerebrovasc. Dis. 2010. Vol. 19, N 1. P. 66 - 72.
Prognostic Role of Mean Platelet Volume and Platelet Count in Ischemic and Hemorrhagic Stroke//J. Stroke Cerebrovasc. Dis. 2010. Vol. 19, N 1. P. 66 - 72.
72. Du J. et al. Association of mean platelet volume and platelet count with the development and prognosis of ischemic and hemorrhagic stroke//Int. J. Lab. Hematol. 2016. Vol. 38, N 3. P. 233 - 239.
73. Morbitzer K.A. et al. Enhanced Renal Clearance in Patients With Hemorrhagic Stroke*//Crit. Care Med. 2019. Vol. 47, N 6. P. 800 - 808.
74. Iribarren C. et al. Low Total Serum Cholesterol and Intracerebral Hemorrhagic Stroke: Is the Association Confined to Elderly Men?//Stroke. 1996. Vol. 27, N 11. P. 1993 - 1998.
75. Wang Y. et al. Retrospective Analysis of the Predictive Effect of Coagulogram on the Prognosis of Intracerebral Hemorrhage. 2011. P. 383 - 385.
76. Tsementzis S.A. et al. Reduced platelet function in subarachnoid hemorrhage//J. Neurosurg. 1986. Vol. 64, N 6. P. 907 - 910.
77. Ziai W.C. et al. Platelet count and function in spontaneous intracerebral hemorrhage//J. Stroke Cerebrovasc. Dis. 2003. Vol. 12, N 4. P. 201 - 206.
78. Kidwell C.S. Comparison of MRI and CT for Detection of Acute Intracerebral Hemorrhage//JAMA. 2004. Vol. 292, N 15. P. 1823.
79. Fiebach J.B. et al. Stroke Magnetic Resonance Imaging Is Accurate in Hyperacute Intracerebral Hemorrhage//Stroke. 2004. Vol. 35, N 2. P. 502 - 506.
80. Chalela J.A. et al. Magnetic resonance imaging and computed tomography in emergency assessment of patients with suspected acute stroke: a prospective comparison//Lancet. 2007. Vol. 369, N 9558. P. 293 - 298.
81. Divani A.A. et al. The ABCs of Accurate Volumetric Measurement of Cerebral Hematoma//Stroke. 2011. Vol. 42, N 6. P. 1569 - 1574.
82. Montes J.M. et al. Stereotactic Computed Tomographic-Guided Aspiration and Thrombolysis of Intracerebral Hematoma//Stroke. 2000. Vol. 31, N 4. P. 834 - 840.
83. Cho D.-Y. et al. Endoscopic surgery for spontaneous basal ganglia hemorrhage: comparing endoscopic surgery, stereotactic aspiration, and craniotomy in noncomatose patients//Surg. Neurol. 2006. Vol. 65, N 6. P. 547 - 555.
84. Lee J.J. et al. Subdural hematoma as a major determinant of short-term outcomes in traumatic brain injury//J. Neurosurg. 2018. Vol. 128, N 1. P. 236 - 249.
85. Buruma O.J. et al. Blood-stained cerebrospinal fluid: traumatic puncture or haemorrhage?//J. Neurol. Neurosurg. Psychiatry. 1981. Vol. 44, N 2. P. 144 - 147.
86. Westerlaan H.E. et al. Intracranial Aneurysms in Patients with Subarachnoid Hemorrhage: CT Angiography as a Primary Examination Tool for Diagnosis-Systematic Review and Meta-Analysis//Radiology. 2011. Vol. 258, N 1. P. 134 - 145.
87. Sailer A.M.H. et al. Diagnosing Intracranial Aneurysms With MR Angiography//Stroke. 2014. Vol. 45, N 1. P. 119 - 126.
88. Delgado Almandoz J.E. et al. Independent Validation of the Secondary Intracerebral Hemorrhage Score With Catheter Angiography and Findings of Emergent Hematoma Evacuation//Neurosurgery. 2012. Vol. 70, N 1. P. 131 - 140.
89. Yeung R. et al. Comparison of CTA to DSA in Determining the Etiology of Spontaneous ICH//Can. J. Neurol. Sci./J. Can. des Sci. Neurol. 2009. Vol. 36, N 2. P. 176 - 180.
90. Donauer E. et al. Intraventricular haemorrhage caused by aneurysms and angiomas//Acta Neurochir. (Wien). 1993. Vol. 122, N 1 - 2. P. 23 - 31.
91. Delgado Almandoz J.E. et al. Systematic Characterization of the Computed Tomography Angiography Spot Sign in Primary Intracerebral Hemorrhage Identifies Patients at Highest Risk for Hematoma Expansion//Stroke. 2009. Vol. 40, N 9. P. 2994 - 3000.
92. Zhu X.L., Chan M.S.Y., Poon W.S. Spontaneous Intracranial Hemorrhage: Which Patients Need Diagnostic Cerebral Angiography?//Stroke. 1997. Vol. 28, N 7. P. 1406 - 1409.
93. Delgado Almandoz J.E. et al. Practical Scoring System for the Identification of Patients with Intracerebral Hemorrhage at Highest Risk of Harboring an Underlying Vascular Etiology: The Secondary Intracerebral Hemorrhage Score//Am. J. Neuroradiol. 2010. Vol. 31, N 9. P. 1653 - 1660.
94. Perrini P. et al. Results of surgical and endovascular treatment of intracranial micro-arteriovenous malformations with emphasis on superselective angiography//Acta Neurochir. (Wien). 2004. Vol. 146, N 8.
95. Derdeyn C.P. et al. Management of Brain Arteriovenous Malformations: A Scientific Statement for Healthcare Professionals From the American Heart Association/American Stroke Association//Stroke. 2017. Vol. 48, N 8.
96. da Costa L. et al. The Natural History and Predictive Features of Hemorrhage From Brain Arteriovenous Malformations//Stroke. 2009. Vol. 40, N 1. P. 100 - 105.
97. Alexander M.D. et al. Association between Venous Angioarchitectural Features of Sporadic Brain Arteriovenous Malformations and Intracranial Hemorrhage//Am. J. Neuroradiol. 2015. Vol. 36, N 5. P. 949 - 952.
98. Sahlein D.H. et al. Features Predictive of Brain Arteriovenous Malformation Hemorrhage//Stroke. 2014. Vol. 45, N 7. P. 1964 - 1970.
99. Suarez J.I. et al. Symptomatic vasospasm diagnosis after subarachnoid hemorrhage: Evaluation of transcranial Doppler ultrasound and cerebral angiography as related to compromised vascular distribution//Crit. Care Med. 2002. Vol. 30, N 6. P. 1348 - 1355.
100. Viski S., Olah L. Use of Transcranial Doppler in Intensive Care Unit//J. Crit. Care Med. 2017. Vol. 3, N 3. P. 99 - 104.
101. Шахнович А.Р. Диагностика нарушений мозгового кровообращения. Транскраниальная допплерография/ed. Шахнович А.Р. Ш.В.А. 1996. Vol. 446.
102. Mitchelle A. et al. CTP for the Screening of Vasospasm and Delayed Cerebral Ischemia in Aneurysmal SAH: A Systematic Review and Meta-analysis//Am. J. Neuroradiol. 2024. Vol. 45, N 7. P. 871 - 878.
103. Cremers C.H.P. et al. Different CT perfusion algorithms in the detection of delayed cerebral ischemia after aneurysmal subarachnoid hemorrhage//Neuroradiology. 2015. Vol. 57, N 5. P. 469 - 474.
104. Malinova V. et al. Defining cutoff values for early prediction of delayed cerebral ischemia after subarachnoid hemorrhage by CT perfusion//Neurosurg. Rev. 2020. Vol. 43, N 2. P. 581 - 587.
105. Лукьянчиков В.А. Обходное шунтирование в лечении ишемии головного мозга, обусловленной сосудистым спазмом после разрыва аневризмы//Нейрохирургия. 2015. Vol. 1. P. 90 - 96.
106. Крылов В.В. et al. Сравнительный анализ данных компьютерной томографии и интракраниальной допплерографии у пациентов с церебральным ангиоспазмом//Неврологический журнал. 2016. Vol. 21, N 6. P. 344 - 352.
107. Mir D.I.A. et al. CT Perfusion for Detection of Delayed Cerebral Ischemia in Aneurysmal Subarachnoid Hemorrhage: A Systematic Review and Meta-Analysis//Am. J. Neuroradiol. 2014. Vol. 35, N 5. P. 866 - 871.
108. Busse T.L. et al. Perfusion Computed Tomography as a Screening Tool for Pending Delayed Cerebral Ischemia in Comatose Patients After Aneurysmal Subarachnoid Hemorrhage: A Retrospective Cohort Study//Neurocrit. Care. 2024. Vol. 40, N 3. P. 964 - 975.
109. КТ-ангиография аневризм головного мозга/ed. под ред. Крылова В.В. Москва: ООО "Принт-Студио", 2019. Vol. 332.
110. Qureshi A.I. Effect of Systolic Blood Pressure Reduction on Hematoma Expansion, Perihematomal Edema, and 3-Month Outcome Among Patients With Intracerebral Hemorrhage//Arch. Neurol. 2010. Vol. 67, N 5. P. 570.
111. Anderson C.S. et al. Intensive blood pressure reduction in acute cerebral haemorrhage trial (INTERACT): a randomised pilot trial//Lancet Neurol. 2008. Vol. 7, N 5. P. 391 - 399.
112. Anderson C.S. et al. Rapid Blood-Pressure Lowering in Patients with Acute Intracerebral Hemorrhage//N. Engl. J. Med. 2013. Vol. 368, N 25. P. 2355 - 2365.
113. Ma L. et al. The third Intensive Care Bundle with Blood Pressure Reduction in Acute Cerebral Haemorrhage Trial (INTERACT3): an international, stepped wedge cluster randomised controlled trial//Lancet. 2023. Vol. 402, N 10395. P. 27 - 40.
114. Moullaali T.J. et al. Blood pressure control and clinical outcomes in acute intracerebral haemorrhage: a preplanned pooled analysis of inpidual participant data//Lancet Neurol. 2019. Vol. 18, N 9. P. 857 - 864.
115. Steiner T. et al. European Stroke Organisation (ESO) and European Association of Neurosurgical Societies (EANS) guideline on stroke due to spontaneous intracerebral haemorrhage//Eur. Stroke J. 2025.
116. Frontera J.A. et al. Guideline for Reversal of Antithrombotics in Intracranial Hemorrhage//Neurocrit. Care. 2016. Vol. 24, N 1. P. 6 - 46.
117. Baranich A.I. et al. Correction of the effect of vitamin K antagonists and antiplatelet agents in hemorrhagic stroke//Burdenko's J. Neurosurg. 2024. Vol. 88, N 6. P. 103.
118. Заболотских И.Б. et al. Гиповолемический шок у взрослых. Клинические рекомендации Общероссийской общественной организации "Федерация анестезиологов и реаниматологов"//Ann. Crit. Care. 2024. N 4. P. 7 - 39.
119. Baranich A.I. et al. Correction of the effect of direct oral and parenteral anticoagulants in hemorrhagic stroke//Burdenko's J. Neurosurg. 2025. Vol. 89, N 1. P. 109.
120. Berger K. et al. A Low-Dose 4F-PCC Protocol for DOAC-Associated Intracranial Hemorrhage//J. Intensive Care Med. 2020. Vol. 35, N 11. P. 1203 - 1208.
121. Guo Y. et al. Tranexamic Acid for Acute Spontaneous Intracerebral Hemorrhage: A Meta-Analysis of Randomized Controlled Trials//Front. Neurol. 2021. Vol. 12.
122. Wong G., Mak, Lu Yeow Yuen G. Review and recommendations on management of refractory raised intracranial pressure in aneurysmal subarachnoid hemorrhage//Vasc. Health Risk Manag. 2013. P. 353.
123. Ошоров А.В., Савин И.А., Горячев А.С. Внутричерепная гипертензия. Патофизиология. Мониторинг. Лечение. Москва: ИП Волков А.А., 2021. Vol. 657.
124. Wang X. et al. Mannitol and Outcome in Intracerebral Hemorrhage//Stroke. 2015. Vol. 46, N 10. P. 2762 - 2767.
125. Lee K. The NeuroICU Book, Second Edition. McGraw-Hill Education, 2017. Vol. 1008.
126. Fink M.E. Osmotherapy for Intracranial Hypertension//Continuum (N. Y). 2012. Vol. 18, N 3. P. 640 - 654.
127. Poungvarin N. et al. Effects of Dexamethasone in Primary Supratentorial Intracerebral Hemorrhage//N. Engl. J. Med. 1987. Vol. 316, N 20. P. 1229 - 1233.
128. Nyquist P. et al. Prophylaxis of Venous Thrombosis in Neurocritical Care Patients: An Evidence-Based Guideline: A Statement for Healthcare Professionals from the Neurocritical Care Society//Neurocrit. Care. 2016. Vol. 24, N 1. P. 47 - 60.
129. Dennis M. et al. The Effect of Graduated Compression Stockings on Long-term Outcomes After Stroke//Stroke. 2013. Vol. 44, N 4. P. 1075 - 1079.
130. Lacut K. et al. Prevention of venous thrombosis in patients with acute intracerebral hemorrhage//Neurology. 2005. Vol. 65, N 6. P. 865 - 869.
131. Dennis M. et al. The Clots in Legs Or sTockings after Stroke (CLOTS) 3 trial: a randomised controlled trial to determine whether or not intermittent pneumatic compression reduces the risk of post-stroke deep vein thrombosis and to estimate its cost-effectiveness//Health Technol. Assess. (Rockv). 2015. Vol. 19, N 76. P. 1 - 90.
132. Li H. et al. Low-molecular-weight heparin in the prevention of venous thromboembolism among patients with acute intracerebral hemorrhage: A meta-analysis//PLoS One. 2024. Vol. 19, N 10. P. e0311858.
133. PACIARONI M. et al. Efficacy and safety of anticoagulants in the prevention of venous thromboembolism in patients with acute cerebral hemorrhage: a meta-analysis of controlled studies//J. Thromb. Haemost. 2011. Vol. 9, N 5. P. 893 - 898.
134. Al-Shahi Salman R. et al. Effects of antiplatelet therapy after stroke due to intracerebral haemorrhage (RESTART): a randomised, open-label trial//Lancet. 2019. Vol. 393, N 10191. P. 2613 - 2623.
135. Alharthi S.Y. et al. Antiplatelet Resumption After Intracerebral Hemorrhage: A Systematic Review and Meta-Analysis//Diagnostics. 2025. Vol. 15, N 14. P. 1780.
136. Dorhout Mees S. et al. Calcium antagonists for aneurysmal subarachnoid haemorrhage//Cochrane Database Syst. Rev. 2007.
137. Yung D. et al. Reinitiation of Anticoagulation After Warfarin-Associated Intracranial Hemorrhage and Mortality Risk: The Best Practice for Reinitiating Anticoagulation Therapy After Intracranial Bleeding (BRAIN) Study//Can. J. Cardiol. 2012. Vol. 28, N 1. P. 33 - 39.
138. Phan T.G., Koh M., Wijdicks E.F.M. Safety of Discontinuation of Anticoagulation in Patients With Intracranial Hemorrhage at High Thromboembolic Risk//Arch. Neurol. 2000. Vol. 57, N 12. P. 1710.
139. Majeed A. et al. Optimal Timing of Resumption of Warfarin After Intracranial Hemorrhage//Stroke. 2010. Vol. 41, N 12. P. 2860 - 2866.
140. Grainger B.T., McFadyen J.D., Tran H. Between a rock and a hard place: resumption of oral anticoagulant therapy after intracranial hemorrhage//J. Thromb. Haemost. 2024. Vol. 22, N 3. P. 594 - 603.
141. Lee H.S. et al. Clinical course of spontaneous gangliothalamic hemorrhage in the acute period: who requires surgical removal?//J. Korean Med. Sci. 1991. Vol. 6, N 2. P. 103.
142. Khosravani H. et al. Emergency Noninvasive Angiography for Acute Intracerebral Hemorrhage//Am. J. Neuroradiol. 2013. Vol. 34, N 8. P. 1481 - 1487.
143. Kuo L.-T. et al. Early endoscope-assisted hematoma evacuation in patients with supratentorial intracerebral hemorrhage: case selection, surgical technique, and long-term results//Neurosurg. Focus. 2011. Vol. 30, N 4. P. E9.
144. Wang Z. et al. [Endoscopic surgery for hypertensive cerebral hemorrhage].//Zhong Nan Da Xue Xue Bao. Yi Xue Ban. 2005. Vol. 30, N 4. P. 424 - 426.
145. Zhu H., Shi W., Wang Z. Keyhole endoscopic hematoma evacuation in patients//Turk. Neurosurg. 2011.
146. Auer L.M. et al. Endoscopic surgery versus medical treatment for spontaneous intracerebral hematoma: a randomized study//J. Neurosurg. 1989. Vol. 70, N 4. P. 530 - 535.
147. Крылов В.В., Дашьян В.Г., Годков И.М. Эндоскопическая хирургия геморрагического инсульта. Москва: Бином, 2014. Vol. 96.
148. Dashyan V.G. et al. Open and minimally invasive surgery for hypertensive intracranial hemorrhages. Surgey outcomes of 500 patients//Russ. J. Neurosurg. 2022. Vol. 23, N 4. P. 33 - 43.
149. Godkov I.M., Dashyan V.G. Comparing the results of surgical and conservative treatment of patients with supratentorial hypertensive intracerebral hemorrhage. A new look at previously known randomized studies//Ann. Clin. Exp. Neurol. 2021. Vol. 15, N 1.
150. Dashyan V.G. et al. Endoscopic surgery for hemorrhagic stroke in regional vascular centers//Russ. J. Neurosurg. 2019. Vol. 21, N 1. P. 35 - 44.
151. Dash'ian V.G. et al. [Endoscopic surgery of hemorrhagic stroke].//Zhurnal Nevrol. i psikhiatrii Im. S.S. Korsakova. 2014. Vol. 114, N 3 Pt 2. P. 7 - 13.
152. Morgenstern L.B. et al. Guidelines for the Management of Spontaneous Intracerebral Hemorrhage//Stroke. 2010. Vol. 41, N 9. P. 2108 - 2129.
153. van Loon J. et al. Controversies in the management of spontaneous cerebellar haemorrhage a consecutive series of 49 cases and review of the literature//Acta Neurochir. (Wien). 1993. Vol. 122, N 3 - 4. P. 187 - 193.
154. Li L. et al. Surgical Evacuation of Spontaneous Cerebellar Hemorrhage: Comparison of Safety and Efficacy of Suboccipital Craniotomy, Stereotactic Aspiration, and Thrombolysis and Endoscopic Surgery//World Neurosurg. 2018. Vol. 117. P. e90-e98.
155. Xu X. et al. Minimally invasive surgeries for spontaneous hypertensive intracerebral hemorrhage (MISICH): a multicenter randomized controlled trial//BMC Med. 2024. Vol. 22, N 1. P. 244.
156. Skvortsova V.I. et al. Reduction in stroke death rates through a package of measures to improve medical care for patients with vascular diseases in the Russian Federation//Profil. meditsina. 2018. Vol. 21, N 1. P. 4.
157. Wang W.-Z. et al. Minimally Invasive Craniopuncture Therapy vs. Conservative Treatment for Spontaneous Intracerebral Hemorrhage: Results from a Randomized Clinical Trial in China//Int. J. Stroke. 2009. Vol. 4, N 1. P. 11 - 16.
158. Dye J.A. et al. Frontal bur hole through an eyebrow incision for image-guided endoscopic evacuation of spontaneous intracerebral hemorrhage//J. Neurosurg. 2012. Vol. 117, N 4. P. 767 - 773.
159. Mendelow A.D. The international surgical trial in intracerebral haemorrhage (ISTICH)//Brain Edema XII. Vienna: Springer Vienna, 2003. P. 441 - 443.
160. Пилипенко Ю.В. et al. Локальный фибринолиз нетравматических внутримозговых и внутрижелудочковых кровоизлияний//Журнал вопросы нейрохирургии им. академика Н.Н. Бурденко. 2012. Vol. 76, N 6. P. 3 - 13.
161. Krylov V. V. et al. LOCAL FIBRINOLYSIS IN SURGICAL TREATMENT OF NON-TRAUMATIC INTRACRANIAL HEMORRHAGES//Ann. Russ. Acad. Med. Sci. 2013. Vol. 68, N 7. P. 24 - 31.
162. Hattori N. et al. Impact of stereotactic hematoma evacuation on activities of daily living during the chronic period following spontaneous putaminal hemorrhage: a randomized study//J. Neurosurg. 2004. Vol. 101, N 3. P. 417 - 420.
163. Kaneko M. et al. Long-term evaluation of ultra-early operation for hypertensive intracerebral hemorrhage in 100 cases//J. Neurosurg. 1983. Vol. 58, N 6. P. 838 - 842.
164. Rabinstein A.A., Atkinson J.L., Wijdicks E.F.M. Emergency craniotomy in patients worsening due to expanded cerebral hematoma//Neurology. 2002. Vol. 58, N 9. P. 1367 - 1372.
165. Wakai S., Kumakura N., Nagai M. Lobar intracerebral hemorrhage//J. Neurosurg. 1992. Vol. 76, N 2. P. 231 - 238.
166. Mendelow A.D. et al. Early surgery versus initial conservative treatment in patients with spontaneous supratentorial lobar intracerebral haematomas (STICH II): a randomised trial//Lancet. 2013. Vol. 382, N 9890. P. 397 - 408.
167. Крылов В.В. et al. Пункционная аспирация и локальный фибринолиз в хирургии внутричерепных кровоизлияний. Москва: Авторская академия. Товарищество научных изданий КМК, 2009. Vol. 160.
168. Gaberel T. et al. Intraventricular Fibrinolysis Versus External Ventricular Drainage Alone in Intraventricular Hemorrhage//Stroke. 2011. Vol. 42, N 10. P. 2776 - 2781.
169. Kondziolka D., McLaughlin M.R., Kestle J.R.W. Simple Risk Predictions for Arteriovenous Malformation Hemorrhage//Neurosurgery. 1995. Vol. 37, N 5. P. 851 - 855.
170. Nasser J.A. et al. Stereotactic fibrinolysis of spontaneous intracerebral hematoma using infusion of recombinant tissue plasminogen activator//Arq. Neuropsiquiatr. 2002. Vol. 60, N 2B. P. 362 - 366.
171. Teernstra O.P.M. et al. Stereotactic Treatment of Intracerebral Hematoma by Means of a Plasminogen Activator//Stroke. 2003. Vol. 34, N 4. P. 968 - 974.
172. Сарибекян А.С. Хирургическое лечение геморрагического инсульта методом пункционной аспирации и локального фибринолиза. Москва: Летопись, 2009. Vol. 288.
173. Dashyan V.G. et al. Decompressive craniectomy in the treatment of supratentorial hypertensive intracerebral hematomas//Russ. J. Neurosurg. 2021. Vol. 23, N 2. P. 66 - 76.
174. Коновалов А.Н., Крылов В.В., Филатов Ю.М. и соавт. Рекомендательный протокол ведения больных с субарахноидальным кровоизлиянием вследствие разрыва аневризм головного мозга//Журнал "Вопросы нейрохирургии" имени Н.Н. Бурденко". 2006. N 3. P. 3 - 11.
175. Steiner T. et al. European Stroke Organization Guidelines for the Management of Intracranial Aneurysms and Subarachnoid Haemorrhage//Cerebrovasc. Dis. 2013. Vol. 35, N 2. P. 93 - 112.
176. Cobler-Lichter M.J. et al. Safety and Outcomes of Valproic Acid in Subarachnoid Hemorrhage Patients: A Retrospective Study//Clin. Neuropharmacol. 2025. Vol. 48, N 2. P. 43 - 50.
177. Yerram S. et al. Seizure prophylaxis in the neuroscience intensive care unit//J. Intensive Care. 2018. Vol. 6, N 1. P. 17.
178. Zafar S.F. et al. Antiseizure Medication Treatment and Outcomes in Patients with Subarachnoid Hemorrhage Undergoing Continuous EEG Monitoring//Neurocrit. Care. 2022. Vol. 36, N 3. P. 857 - 867.
179. Lehecka M., Laakso A., Hernesniemi J. Helsinki Microneurosurgery. Basics and Tricks. 2011. Vol. 343.
180. Горячев А.С., Савин И.А. Основы ИВЛ. Москва: Аксиом Графикс Юнион, 2017. Vol. 258.
181. Calviere L. et al. Rebleeding After Aneurysmal Subarachnoid Hemorrhage in Two Centers Using Different Blood Pressure Management Strategies.//Front. Neurol. 2022. Vol. 13. P. 836268.
182. Roquilly A. et al. Balanced versus chloride-rich solutions for fluid resuscitation in brain-injured patients: a randomised double-blind pilot study//Crit. Care. 2013. Vol. 17, N 2. P. R77.
183. Bercker S. et al. Hydroxyethyl starch for volume expansion after subarachnoid haemorrhage and renal function: Results of a retrospective analysis//PLoS One. 2018. Vol. 13, N 2. P. e0192832.
184. Allen G.S. et al. Cerebral Arterial Spasm - A Controlled Trial of Nimodipine in Patients with Subarachnoid Hemorrhage//N. Engl. J. Med. 1983. Vol. 308, N 11. P. 619 - 624.
185. Choudhari K.A. et al. Aneurysms unsuitable for endovascular intervention: Surgical outcome and management challenges over a 5-year period following International Subarachnoid Haemorrhage Trial (ISAT)//Clin. Neurol. Neurosurg. 2007. Vol. 109, N 10. P. 868 - 875.
186. Molyneux A.J. et al. International subarachnoid aneurysm trial (ISAT) of neurosurgical clipping versus endovascular coiling in 2143 patients with ruptured intracranial aneurysms: a randomised comparison of effects on survival, dependency, seizures, rebleeding, subgroups, and aneurysm occlusion//Lancet. 2005. Vol. 366, N 9488. P. 809 - 817.
187. Крылов В.В. et al. Выбор сроков открытого хирургического лечения больных с разрывом церебральных аневризм, осложненных массивным базальным субарахноидальным кровоизлиянием (Fisher 3)//Нейрохирургия. 2015. N 3. P. 11 - 17.
188. Элиава Ш.Ш. et al. Хирургическое лечение аневризм головного мозга в остром периоде кровоизлияния/ed. под ред. Ш.Ш. Элиава. Москва: Издательство ИП Т.А. Алексеева, 2019. Vol. 232.
189. Oshiro E.M. et al. A New Subarachnoid Hemorrhage Grading System Based on the Glasgow Coma Scale: A Comparison with the Hunt and Hess and World Federation of Neurological Surgeons Scales in a Clinical Series//Neurosurgery. 1997. Vol. 41, N 1. P. 140 - 148.
190. Tommasino N. et al. Epidemiologic and Evolutionary Profile of Patients With Subarachnoid Hemorrhage With Glasgow Coma Scale Score of 8 or Less Who Entered the Follow-Up Program of the National Institute of Donation and Transplantation//Transplant. Proc. 2018. Vol. 50, N 2. P. 405 - 407.
191. Bailes J.E. et al. Management morbidity and mortality of poor-grade aneurysm patients//J. Neurosurg. 1990. Vol. 72, N 4. P. 559 - 566.
192. Molyneux A. International Subarachnoid Aneurysm Trial (ISAT) of neurosurgical clipping versus endovascular coiling in 2143 patients with ruptured intracranial aneurysms: a randomised trial//Lancet. 2002. Vol. 360, N 9342. P. 1267 - 1274.
193. Wach J. et al. A Long-Term Comparative Analysis of Endovascular Coiling and Clipping for Ruptured Cerebral Aneurysms: An Inpidual Patient-Level Meta-Analysis Assessing Rerupture Rates//J. Clin. Med. 2024. Vol. 13, N 6. P. 1778.
194. Pierot L. et al. Rebleeding and bleeding in the year following intracranial aneurysm coiling: analysis of a large prospective multicenter cohort of 1140 patients-Analysis of Recanalization after Endovascular Treatment of Intracranial Aneurysm (ARETA) Study//J. Neurointerv. Surg. 2020. Vol. 12, N 12. P. 1219 - 1225.
195. Spetzler R.F. et al. Ten-year analysis of saccular aneurysms in the Barrow Ruptured Aneurysm Trial//J. Neurosurg. 2020. Vol. 132, N 3. P. 771 - 776.
196. Lindgren A. et al. Endovascular coiling versus neurosurgical clipping for people with aneurysmal subarachnoid haemorrhage//Cochrane Database Syst. Rev. 2018. Vol. 2018, N 8.
197. Heiskanen O. et al. Acute surgery for intracerebral haematomas caused by rupture of an intracranial arterial aneurysm//Acta Neurochir. (Wien). 1988. Vol. 90, N 3 - 4. P. 81 - 83.
198.  E. et al. SUBARACHNOID HEMORRHAGE AND INTRACEREBRAL HEMATOMA//Neurosurgery. 2008. Vol. 63, N 6. P. 1088 - 1094.
E. et al. SUBARACHNOID HEMORRHAGE AND INTRACEREBRAL HEMATOMA//Neurosurgery. 2008. Vol. 63, N 6. P. 1088 - 1094.
199. Ryttlefors M. et al. International Subarachnoid Aneurysm Trial of Neurosurgical Clipping Versus Endovascular Coiling//Stroke. 2008. Vol. 39, N 10. P. 2720 - 2726.
200. Mitchell P. et al. Could late rebleeding overturn the superiority of cranial aneurysm coil embolization over clip ligation seen in the International Subarachnoid Aneurysm Trial?//J. Neurosurg. 2008. Vol. 108, N 3. P. 437 - 442.
201. Eliava S.S. et al. Microsurgical treatment of 723 cerebral aneurysms: a single-center prospective study//Burdenko's J. Neurosurg. 2025. Vol. 89, N 3. P. 60.
202. Spetzler R.F. et al. The Barrow Ruptured Aneurysm Trial: 6-year results//J. Neurosurg. 2015. Vol. 123, N 3. P. 609 - 617.
203. Colby G.P., Coon A.L., Tamargo R.J. Surgical Management of Aneurysmal Subarachnoid Hemorrhage//Neurosurg. Clin. N. Am. 2010. Vol. 21, N 2. P. 247 - 261.
204. Biebuyck J.F., Young W.L., Pile-Spellman J. Anesthetic Considerations for Interventional Neuroradiology//Anesthesiology. 1994. Vol. 80, N 2. P. 427 - 456.
205. Manninen P.H., Chan A.S., Papworth D. Conscious sedation for interventional neuroradiology: a comparison of midazolam and propofol infusion//Can. J. Anaesth. 1997. Vol. 44, N 1. P. 26 - 30.
206. Komotar R.J. et al. Efficacy of lamina terminalis fenestration in reducing shunt-dependent hydrocephalus following aneurysmal subarachnoid hemorrhage: a systematic review//J. Neurosurg. 2009. Vol. 111, N 1. P. 147 - 154.
207. Элиава Ш.Ш., Шехтман О.Д., Пилипенко Ю.В. и соавт. Интраоперационная флуоресцентная ангиография с индоцианином в хирургии аневризм головного мозга. Первый опыт применения и обзор литературы//Журнал "Вопросы нейрохирургии" имени Н.Н. Бурденко". 2015. Vol. 1. P. 33 - 41.
208. Etminan N. et al. European Stroke Organisation (ESO) guidelines on management of unruptured intracranial aneurysms//Eur. Stroke J. 2022. Vol. 7, N 3.
209. Azhari S. et al. The Diagnostic Value of CT Angiography in the Diagnosis of Residual Aneurysm After Brain Aneurysm Surgery//Iran. J. Radiol. 2018. Vol. 15, N 1.
210. Selles M. et al. Advances in metal artifact reduction in CT images: A review of traditional and novel metal artifact reduction techniques//Eur. J. Radiol. 2024. Vol. 170. P. 111276.
211. Krylov V. V. et al. Prevention of cerebral vasospasm and delayed cerebral ischemia in patients with massive aneurysmal subarachnoid hemorrhage//Russ. J. Neurosurg. 2019. Vol. 21, N 1. P. 12 - 26.
212. Lu X. et al. Intrathecal Fibrinolysis for Aneurysmal Subarachnoid Hemorrhage: Evidence From Randomized Controlled Trials and Cohort Studies//Front. Neurol. 2019. Vol. 10.
213. Jang K.M. et al. The Effect of Locally Administered Fibrinolytic Drugs Following Aneurysmal Subarachnoid Hemorrhage: A Meta-Analysis with Eight Randomized Controlled Studies.//J. Korean Neurosurg. Soc. 2021. Vol. 64, N 2. P. 207 - 216.
214. Bader E.R. et al. Thrombolysis for aneurysmal subarachnoid haemorrhage//Cochrane Database Syst. Rev. 2025. Vol. 2025, N 1.
215. Wiebers D.O. Unruptured intracranial aneurysms: natural history, clinical outcome, and risks of surgical and endovascular treatment//Lancet. 2003. Vol. 362, N 9378. P. 103 - 110.
216. Шалыгин К.В. et al. Ультраранняя рентгенэндоваскулярная эмболизация церебральных аневризм при субарахноидальном кровоизлиянии//Эндоваскулярная хирургия. 2019. Vol. 6, N 4. P. 312 - 320.
217. Rizvi A. et al. Long-Term Rupture Risk in Patients with Unruptured Intracranial Aneurysms Treated with Endovascular Therapy: A Systematic Review and Meta-Analysis//Am. J. Neuroradiol. 2020. Vol. 41, N 6. P. 1043 - 1048.
218. Salimi Ashkezari S.F. et al. Blebs in intracranial aneurysms: prevalence and general characteristics//J. Neurointerv. Surg. 2021. Vol. 13, N 3. P. 226 - 230.
219. Funakoshi Y. et al. Predictors of Cerebral Aneurysm Rupture after Coil Embolization: Single-Center Experience with Recanalized Aneurysms//Am. J. Neuroradiol. 2020. Vol. 41, N 5. P. 828 - 835.
220. Greve T. et al. Initial Raymond-Roy Occlusion Classification but not Packing Density Defines Risk for Recurrence after Aneurysm Coiling//Clin. Neuroradiol. 2021. Vol. 31, N 2. P. 391 - 399.
221. Raymond J. et al. Long-term angiographic recurrences after selective endovascular treatment of aneurysms with detachable coils.//Stroke. 2003. Vol. 34, N 6. P. 1398 - 1403.
222. Eliava S.S. et al. Unruptured asymptomatic brain aneurysms: modern approaches to the choice of surgical method and treatment outcomes//Vopr. neirokhirurgii Im. N.N. Burdenko. 2021. Vol. 85, N 6. P. 6.
223. Shapiro M. et al. Stent-Supported Aneurysm Coiling: A Literature Survey of Treatment and Follow-Up//Am. J. Neuroradiol. 2012. Vol. 33, N 1. P. 159 - 163.
224. Кандыба Д. et al. Роль ассистирующих методов при внутрисосудистой окклюзии аневризм головного мозга//Патология кровообращения и кардиохирургия. 2012. Vol. 16, N 3. P. 27 - 33.
225. Arthur A.S. et al. The safety and effectiveness of the Woven EndoBridge (WEB) system for the treatment of wide-necked bifurcation aneurysms: final 12-month results of the pivotal WEB Intrasaccular Therapy (WEB-IT) Study//J. Neurointerv. Surg. 2019. Vol. 11, N 9. P. 924 - 930.
226. Berestov V. V. et al. Stent-assisted coiling of acute ruptured cerebral aneurysms//Сибирский научный медицинский журнал. 2021. Vol. 41, N 4. P. 40 - 47.
227. Ramakrishnan P. et al. Intra-Arterial Eptifibatide in the Management of Thromboembolism during Endovascular Treatment of Intracranial Aneurysms: Case Series and a Review of the Literature//Interv. Neurol. 2013. Vol. 2, N 1. P. 19 - 29.
228. Cho Y.-H. et al. Imaging follow-up strategy after endovascular treatment of Intracranial aneurysms: A literature review and guideline recommendations//J. Cerebrovasc. Endovasc. Neurosurg. 2024. Vol. 26, N 1. P. 1 - 10.
229. Chung D.Y., Mayer S.A., Rordorf G.A. External Ventricular Drains After Subarachnoid Hemorrhage: Is Less More?//Neurocrit. Care. 2018. Vol. 28, N 2. P. 157 - 161.
230. Hasan D., Tanghe H.L.J. Distribution of cisternal blood in patients with acute hydrocephalus after subarachnoid hemorrhage//Ann. Neurol. 1992. Vol. 31, N 4. P. 374 - 378.
231. Heros R.C. Acute hydrocephalus after subarachnoid hemorrhage.//Stroke. 1989. Vol. 20, N 6. P. 715 - 717.
232. Di Rienzo A. et al. Endoscope-assisted microsurgical evacuation versus external ventricular drainage for the treatment of cast intraventricular hemorrhage: results of a comparative series//Neurosurg. Rev. 2020. Vol. 43, N 2. P. 695 - 708.
233. Tunkel A.R. et al. 2017 Infectious Diseases Society of America's Clinical Practice Guidelines for Healthcare-Associated Ventriculitis and Meningitis*//Clin. Infect. Dis. 2017. Vol. 64, N 6. P. e34-e65.
234. Konovalov A. et al. External Ventricular Drainage in Patients With Acute Aneurysmal Subarachnoid Hemorrhage After Microsurgical Clipping: Our 2006 - 2018 Experience and a Literature Review//Cureus. 2021.
235. Chung D.Y. et al. Evidence-Based Management of External Ventricular Drains//Curr. Neurol. Neurosci. Rep. 2019. Vol. 19, N 12. P. 94.
236. Fried H.I. et al. The Insertion and Management of External Ventricular Drains: An Evidence-Based Consensus Statement//Neurocrit. Care. 2016. Vol. 24, N 1. P. 61 - 81.
237. ![]() J. et al. Diagnosis of external ventricular drainage related infections with real-time 16S PCR and third-generation 16S sequencing//Infect. Dis. (Auckl). 2024. Vol. 56, N 7. P. 521 - 530.
J. et al. Diagnosis of external ventricular drainage related infections with real-time 16S PCR and third-generation 16S sequencing//Infect. Dis. (Auckl). 2024. Vol. 56, N 7. P. 521 - 530.
238. Gigante P. et al. External ventricular drainage following aneurysmal subarachnoid haemorrhage//Br. J. Neurosurg. 2010. Vol. 24, N 6. P. 625 - 632.
239. Karvouniaris M. et al. Current Perspectives on the Diagnosis and Management of Healthcare-Associated Ventriculitis and Meningitis//Infect. Drug Resist. 2022. Vol. Volume 15. P. 697 - 721.
240. Xie Z. et al. Predictors of Shunt-dependent Hydrocephalus After Aneurysmal Subarachnoid Hemorrhage? A Systematic Review and Meta-Analysis//World Neurosurg. 2017. Vol. 106. P. 844 - 860.e6.
241. Brandecker S. et al. Primary decompressive craniectomy in poor-grade aneurysmal subarachnoid hemorrhage: long-term outcome in a single-center study and systematic review of literature//Neurosurg. Rev. 2021. Vol. 44, N 4. P. 2153 - 2162.
242. Дашьян В.Г. et al. Декомпрессивная краниотомия в хирургии разорвавшихся аневризм головного мозга//Российский нейрохирургический журнал им. проф. А.Л. Поленова. 2015. Vol. 7, N 4. P. 18 - 25.
243. Dorfer C. et al. Decompressive Hemicraniectomy After Aneurysmal Subarachnoid Hemorrhage//World Neurosurg. 2010. Vol. 74, N 4 - 5. P. 465 - 471.
244. Buschmann U. et al. Decompressive hemicraniectomy in patients with subarachnoid hemorrhage and intractable intracranial hypertension//Acta Neurochir. (Wien). 2007. Vol. 149, N 1. P. 59 - 65.
245. Alotaibi N.M. et al. Management of raised intracranial pressure in aneurysmal subarachnoid hemorrhage: time for a consensus?//Neurosurg. Focus. 2017. Vol. 43, N 5. P. E13.
246. Liu C.-C. et al. Efficacy of propofol-based anesthesia against risk of brain swelling during craniotomy: A meta-analysis of randomized controlled studies//J. Clin. Anesth. 2024. Vol. 92. P. 111306.
247. Zhou Z., Ying M., Zhao R. Efficacy and safety of sevoflurane vs propofol in combination with remifentanil for anesthesia maintenance during craniotomy//Medicine (Baltimore). 2021. Vol. 100, N 51. P. e28400.
248. Chui J. et al. Comparison of propofol and volatile agents for maintenance of anesthesia during elective craniotomy procedures: systematic review and meta-analysis//Can. J. Anesth. Can.  . 2014. Vol. 61, N 4. P. 347 - 356.
. 2014. Vol. 61, N 4. P. 347 - 356.
249. Bhardwaj A. et al. Comparison of propofol and desflurane for postanaesthetic morbidity in patients undergoing surgery for aneurysmal SAH: a randomized clinical trial//J. Anesth. 2018. Vol. 32, N 2. P. 250 - 258.
250. Yi J. et al. Maintaining intraoperative normothermia reduces blood loss in patients undergoing major operations: a pilot randomized controlled clinical trial//BMC Anesthesiol. 2018. Vol. 18, N 1. P. 126.
251. Ingram A., Harper M. The health economic benefits of perioperative patient warming for prevention of blood loss and transfusion requirements as a consequence of inadvertent perioperative hypothermia//J. Perioper. Pract. 2018. Vol. 28, N 9. P. 215 - 222.
252. Mestdagh F.P. et al. Pain management after elective craniotomy//Eur. J. Anaesthesiol. 2023. Vol. 40, N 10. P. 747 - 757.
253. Kulikov A. et al. Preoperative Versus Postoperative Scalp Block Combined With Incision Line Infiltration for Pain Control After Supratentorial Craniotomy//Clin. J. Pain. 2021. Vol. 37, N 3. P. 194 - 198.
254. Uribe A.A. et al. Postoperative Nausea and Vomiting After Craniotomy: An Evidence-based Review of General Considerations, Risk Factors, and Management//J. Neurosurg. Anesthesiol. 2021. Vol. 33, N 3. P. 212 - 220.
255. Kundra S. et al. Principles of neuroanesthesia in aneurysmal subarachnoid hemorrhage//J. Anaesthesiol. Clin. Pharmacol. 2014. Vol. 30, N 3. P. 328.
256. Hagerty T. et al. Risk Factors for Catheter-Associated Urinary Tract Infections in Critically Ill Patients With Subarachnoid Hemorrhage//J. Neurosci. Nurs. 2015. Vol. 47, N 1. P. 51 - 54.
257. Menegaz de Almeida A. et al. Hypertonic Saline Solution Versus Mannitol for Brain Relaxation During Craniotomies: A Systematic Review and Updated Meta-Analysis//Neurosurgery. 2024. Vol. 95, N 3. P. 517 - 526.
258. Robba C. et al. Clinical practice and effect of carbon dioxide on outcomes in mechanically ventilated acute brain-injured patients: a secondary analysis of the ENIO study//Intensive Care Med. 2024. Vol. 50, N 2. P. 234 - 246.
259. Ravishankar N. et al. Management Strategies for Intracranial Pressure Crises in Subarachnoid Hemorrhage//J. Intensive Care Med. 2020. Vol. 35, N 3. P. 211 - 218.
260. Pasternak J.J. et al. Hyperglycemia in Patients Undergoing Cerebral Aneurysm Surgery: Its Association With Long-term Gross Neurologic and Neuropsychological Function//Mayo Clin. Proc. 2008. Vol. 83, N 4. P. 406 - 417.
261. Kruyt N.D. et al. Hyperglycemia and Clinical Outcome in Aneurysmal Subarachnoid Hemorrhage//Stroke. 2009. Vol. 40, N 6.
262. Whiting P. et al. Viscoelastic point-of-care testing to assist with the diagnosis, management and monitoring of haemostasis: a systematic review and cost-effectiveness analysis//Health Technol. Assess. (Rockv). 2015. Vol. 19, N 58. P. 1 - 228.
263. Gruenbaum S.E., Bilotta F. Postoperative ICU management of patients after subarachnoid hemorrhage//Curr. Opin. Anaesthesiol. 2014. Vol. 27, N 5. P. 489 - 493.
264. Lee J.M. et al. Necessity of mandatory postoperative intensive care unit management after clipping surgery for unruptured intracranial aneurysms//Clin. Neurol. Neurosurg. 2023. Vol. 228. P. 107703.
265. Akbik F. et al. Jugular Venous Catheterization is Not Associated with Increased Complications in Patients with Aneurysmal Subarachnoid Hemorrhage//Neurocrit. Care. 2025. Vol. 42, N 3. P. 929 - 936.
266. Porto G.B.F. et al. Blood Pressure Guideline Adherence in Patients with Ischemic and Hemorrhagic Stroke in the Neurointensive Care Unit Setting//Neurocrit. Care. 2015. Vol. 23, N 3. P. 313 - 320.
267. Deem S. et al. Hemodynamic Management in the Prevention and Treatment of Delayed Cerebral Ischemia After Aneurysmal Subarachnoid Hemorrhage//Neurocrit. Care. 2023. Vol. 39, N 1. P. 81 - 90.
268. Merrill D. et al. The Impact of Fluid Balance on Acute Kidney Injury in Nontraumatic Subarachnoid Hemorrhage//J. Intensive Care Med. 2024. Vol. 39, N 7. P. 693 - 700.
269. Lee J.W. et al. Hypotension and Adverse Outcomes in Moderate to Severe Traumatic Brain Injury//JAMA Netw. Open. 2024. Vol. 7, N 11. P. e2444465.
270. Kutum C. et al. Intraoperative goal-directed fluid therapy in neurosurgical patients: A systematic review//Surg. Neurol. Int. 2024. Vol. 15. P. 233.
271. Ohkuma H., Tsurutani H., Suzuki S. Incidence and Significance of Early Aneurysmal Rebleeding Before Neurosurgical or Neurological Management//Stroke. 2001. Vol. 32, N 5. P. 1176 - 1180.
272. Naidech A.M. et al. Predictors and Impact of Aneurysm Rebleeding After Subarachnoid Hemorrhage//Arch. Neurol. 2005. Vol. 62, N 3. P. 410.
273. Treggiari M.M. et al. Guidelines for the Neurocritical Care Management of Aneurysmal Subarachnoid Hemorrhage//Neurocrit. Care. 2023. Vol. 39, N 1. P. 1 - 28.
274. Burnol L. et al. Impact of Head-of-Bed Posture on Brain Oxygenation in Patients with Acute Brain Injury: A Prospective Cohort Study//Neurocrit. Care. 2021. Vol. 35, N 3. P. 662 - 668.
275. Preiser J.-C. et al. A guide to enteral nutrition in intensive care units: 10 expert tips for the daily practice//Crit. Care. 2021. Vol. 25, N 1. P. 424.
276. Stechmiller J.K. et al. Guidelines for the prevention of pressure ulcers//Wound Repair Regen. 2008. Vol. 16, N 2. P. 151 - 168.
277. Taleb C. et al. Liberal versus restrictive transfusion strategies in subarachnoid hemorrhage: a secondary analysis of the TRAIN study//Crit. Care. 2025. Vol. 29, N 1. P. 67.
278. English S.W. et al. Liberal or Restrictive Transfusion Strategy in Aneurysmal Subarachnoid Hemorrhage//N. Engl. J. Med. 2025. Vol. 392, N 11. P. 1079 - 1088.
279. Mori T. et al. Improved efficiency of hypervolemic therapy with inhibition of natriuresis by fludrocortisone in patients with aneurysmal subarachnoid hemorrhage//J. Neurosurg. 1999. Vol. 91, N 6. P. 947 - 952.
280. Harrigan M.R. Cerebral Salt Wasting Syndrome//Crit. Care Clin. 2001. Vol. 17, N 1. P. 125 - 138.
281. Ali A. et al. Effectiveness of human albumin for clinical outcome in aneurysmal subarachnoid hemorrhages: a protocol for randomized controlled (HASH) trial//Trials. 2025. Vol. 26, N 1. P. 53.
282. Chou S.H.-Y. Subarachnoid Hemorrhage//Continuum (N. Y). 2021. Vol. 27, N 5. P. 1201 - 1245.
283. Marc S. Greenberg: Handbook of neurosurgery, 6th edn. Thieme Medical Publishers, 2006.
284. Lysakowski C. et al. Transcranial Doppler Versus Angiography in Patients With Vasospasm due to a Ruptured Cerebral Aneurysm//Stroke. 2001. Vol. 32, N 10. P. 2292 - 2298.
285. Frontera J.A. et al. Defining Vasospasm After Subarachnoid Hemorrhage//Stroke. 2009. Vol. 40, N 6. P. 1963 - 1968.
286. Vergouwen M.D.I. et al. Definition of Delayed Cerebral Ischemia After Aneurysmal Subarachnoid Hemorrhage as an Outcome Event in Clinical Trials and Observational Studies//Stroke. 2010. Vol. 41, N 10. P. 2391 - 2395.
287. de Oliveira Manoel A.L. et al. The critical care management of poor-grade subarachnoid haemorrhage//Crit. Care. 2016. Vol. 20, N 1. P. 21.
288. Sloan M.A. et al. Assessment: Transcranial Doppler ultrasonography: [RETIRED]//Neurology. 2004. Vol. 62, N 9. P. 1468 - 1481.
289. Francoeur C.L., Mayer S.A. Management of delayed cerebral ischemia after subarachnoid hemorrhage//Crit. Care. 2016. Vol. 20, N 1. P. 277.
290. Suarez J.I. et al. The Albumin in Subarachnoid Hemorrhage (ALISAH) multicenter pilot clinical trial: safety and neurologic outcomes.//Stroke. 2012. Vol. 43, N 3. P. 683 - 690.
291. Otsubo H. et al. Normovolaemic induced hypertension therapy for cerebral vasospasm after subarachnoid haemorrhage//Acta Neurochir. (Wien). 1990. Vol. 103, N 1 - 2. P. 18 - 26.
292. Kosnik E.J., Hunt W.E. Postoperative hypertension in the management of patients with intracranial arterial aneurysms//J. Neurosurg. 1976. Vol. 45, N 2. P. 148 - 154.
293. Chalouhi N. et al. Endovascular management of cerebral vasospasm following aneurysm rupture: Outcomes and predictors in 116 patients//Clin. Neurol. Neurosurg. 2014. Vol. 118. P. 26 - 31.
294. Bashir A. et al. Intra-arterial nimodipine for cerebral vasospasm after subarachnoid haemorrhage: Influence on clinical course and predictors of clinical outcome//Neuroradiol. J. 2016. Vol. 29, N 1. P. 72 - 81.
295. Mikeladze K.G. et al. Intra-arterial administration of verapamil for prevention and treatment of cerebral angiospasm after SAH due to cerebral aneurysm rupture//Vopr. neirokhirurgii Im. N.N. Burdenko. 2018. Vol. 82, N 4. P. 23.
296. Claassen J., Park S. Spontaneous subarachnoid haemorrhage//Lancet. 2022. Vol. 400, N 10355. P. 846 - 862.
297. Suarez-Rivera O. Acute Hydrocephalus After Subarachnoid Hemorrhage//Surg. Neurol. 1998. Vol. 49, N 5. P. 563 - 565.
298. Zoerle T. et al. Intracranial Pressure After Subarachnoid Hemorrhage*//Crit. Care Med. 2015. Vol. 43, N 1. P. 168 - 176.
299. Magni F. et al. High-Resolution Intracranial Pressure Burden and Outcome in Subarachnoid Hemorrhage//Stroke. 2015. Vol. 46, N 9. P. 2464 - 2469.
300. Okazaki T. et al. Association between dexmedetomidine use and neurological outcomes in aneurysmal subarachnoid hemorrhage patients: A retrospective observational study//J. Crit. Care. 2018. Vol. 44. P. 111 - 116.
301. Quinn T.J. et al. Functional Outcome Measures in Contemporary Stroke Trials//Int. J. Stroke. 2009. Vol. 4, N 3. P. 200 - 205.
302. Элиава Ш.Ш., Филатов Ю.М., Пилипенко Ю.В. и соавт. Микрохирургическое лечение артериовенозных мальформаций головного мозга в НИИ нейрохирургии им. Н.Н. Бурденко (опыт последних лет). 2012. Vol. 76, N 3. P. 34 - 44.
303. Catapano J.S. et al. Intermediate-grade brain arteriovenous malformations and the boundary of operability using the supplemented Spetzler-Martin grading system//J. Neurosurg. 2022. Vol. 136, N 1. P. 125 - 133.
304. Holmes D.R. et al. Left Atrial Appendage Closure as an Alternative to Warfarin for Stroke Prevention in Atrial Fibrillation//J. Am. Coll. Cardiol. 2015. Vol. 65, N 24. P. 2614 - 2623.
305. Martinez J.L., Macdonald R.L. Surgical Strategies for Acutely Ruptured Arteriovenous Malformations. 2016. P. 166 - 181.
306. Крылов В.В., Дашьян В.Г. Хирургическое лечение гипертензивных гематом мозжечка//Cons. Medicum. Неврология. 2009. Vol. 2. P. 9 - 13.
307. Hafez A. et al. Timing of surgery for ruptured supratentorial arteriovenous malformations//Acta Neurochir. (Wien). 2017. Vol. 159, N 11. P. 2103 - 2112.
308. Hernesniemi J. et al. Present State of Microneurosurgery of Cerebral Arteriovenous Malformations. 2010. P. 71 - 76.
309. ![]() J.F. et al. Cerebral microarteriovenous malformations: a series of 28 cases//J. Neurosurg. 2013. Vol. 119, N 3. P. 594 - 602.
J.F. et al. Cerebral microarteriovenous malformations: a series of 28 cases//J. Neurosurg. 2013. Vol. 119, N 3. P. 594 - 602.
310. Stemer A.B. et al. Acute embolization of ruptured brain arteriovenous malformations//J. Neurointerv. Surg. 2013. Vol. 5, N 3. P. 196 - 200.
311. Saatci I. et al. Endovascular treatment of brain arteriovenous malformations with prolonged intranidal Onyx injection technique: long-term results in 350 consecutive patients with completed endovascular treatment course//J. Neurosurg. 2011. Vol. 115, N 1. P. 78 - 88.
312. Potts M.B. et al. Curing arteriovenous malformations using embolization//Neurosurg. Focus. 2014. Vol. 37, N 3. P. E19.
313. Wong J. et al. Microsurgery for ARUBA Trial (A Randomized Trial of Unruptured Brain Arteriovenous Malformation)-Eligible Unruptured Brain Arteriovenous Malformations//Stroke. 2017. Vol. 48, N 1. P. 136 - 144.
314. Valavanis A., Yasargil M.G. The Endovascular Treatment of Brain Arteriovenous Malformations. 1998. P. 131 - 214.
315. Ding D. et al. Radiosurgery for ruptured intracranial arteriovenous malformations//J. Neurosurg. 2014. Vol. 121, N 2. P. 470 - 481.
316. Niini T. et al. Perioperative Treatment of Brain Arteriovenous Malformations Between 2006 and 2014: The Helsinki Protocol//Neurocrit. Care. 2019. Vol. 31, N 2. P. 346 - 356.
317. Starke R.M. et al. Stereotactic radiosurgery for cerebral arteriovenous malformations: evaluation of long-term outcomes in a multicenter cohort//J. Neurosurg. 2017. Vol. 126, N 1. P. 36 - 44.
318. Abla A.A. et al. A treatment paradigm for high-grade brain arteriovenous malformations: volume-staged radiosurgical downgrading followed by microsurgical resection//J. Neurosurg. 2015. Vol. 122, N 2. P. 419 - 432.
319. Cho W.-S. et al. Korean Clinical Practice Guidelines for Aneurysmal Subarachnoid Hemorrhage//J. Korean Neurosurg. Soc. 2018. Vol. 61, N 2. P. 127 - 166.
320. Thompson B.G. et al. Guidelines for the Management of Patients With Unruptured Intracranial Aneurysms//Stroke. 2015. Vol. 46, N 8. P. 2368 - 2400.
321. Karbe A.-G., Vajkoczy P. Postoperative management and follow-up after resection of arteriovenous malformations//J. Neurosurg. Sci. 2018. Vol. 62, N 4.
322.  ,
,  , Lawton M.T. Intraoperative arteriovenous malformation rupture: causes, management techniques, outcomes, and the effect of neurosurgeon experience//Neurosurg. Focus. 2014. Vol. 37, N 3. P. E12.
, Lawton M.T. Intraoperative arteriovenous malformation rupture: causes, management techniques, outcomes, and the effect of neurosurgeon experience//Neurosurg. Focus. 2014. Vol. 37, N 3. P. E12.
323. Choque-Velasquez J. et al. Current advances in epilepsy among patients with arteriovenous malformations//Explor. Neurosci. 2024. Vol. 3, N 3. P. 175 - 197.
324. Englot D.J. et al. Seizure Predictors and Control After Microsurgical Resection of Supratentorial Arteriovenous Malformations in 440 Patients//Neurosurgery. 2012. Vol. 71, N 3. P. 572 - 580.
325. Zheng P. et al. Early rehabilitation after acute intracerebral hemorrhage in China-a need for new research directions and more data: A systematic review//Geriatr. Nurs. (Minneap). 2025. Vol. 64. P. 103339.
326. Juckett L.A. et al. Implementation Science to Advance Health Equity in Stroke Rehabilitation//J. Am. Heart Assoc. 2024. Vol. 13, N 7.
327. Liu N. et al. Randomized Controlled Trial of Early Rehabilitation After Intracerebral Hemorrhage Stroke//Stroke. 2014. Vol. 45, N 12. P. 3502 - 3507.
328. Bako A.T. et al. Postacute Discharge Destination and Major Adverse Cardiovascular Events Among Patients With Intracerebral Hemorrhage//Stroke. 2025. Vol. 56, N 9. P. 2658 - 2668.
329. Приказ Минздрава РФ от 31 июля 2020 г. N 788Н об утверждении порядка организации медицинской реабилитации взрослых. Российская Федерация, 2020.
330. Белкин А.А. et al. Разработка и валидация ПИТС-индекса для оценки тяжести синдрома последствий интенсивной терапии: описательное проспективное несравнительное когортное исследование//Ann. Crit. Care. 2024. N 4. P. 58 - 72.
331. Hiser S.L. et al. Post-intensive care syndrome (PICS): recent updates//J. Intensive Care. 2023. Vol. 11, N 1. P. 23.
332. Belkin A.A. et al. Rehabilitation in the intensive care unit (RehabICU). Clinical practice recommendations of the national Union of Physical and Rehabilitation Medicine Specialists of Russia and of the national Federation of Anesthesiologists and Reanimatologists//Ann. Crit. Care. 2022. N 2. P. 7 - 40.
333. Spies C.D. et al. Instruments to measure outcomes of post-intensive care syndrome in outpatient care settings - Results of an expert consensus and feasibility field test//J. Intensive Care Soc. 2021. Vol. 22, N 2. P. 159 - 174.
334. Beadman M., Carraretto M. Key elements of an evidence-based clinical psychology service within adult critical care//J. Intensive Care Soc. 2023. Vol. 24, N 2. P. 215 - 221.
335. Reimers A., Odin P., Ljung H. Drug-Induced Cognitive Impairment//Drug Saf. 2025. Vol. 48, N 4. P. 339 - 361.
336. Chu Y. et al. Instruments to measure postintensive care syndrome: a scoping review protocol//BMJ Open. 2022. Vol. 12, N 10. P. e061048.
337. Nakanishi N. et al. Instruments to assess post-intensive care syndrome assessment: a scoping review and modified Delphi method study//Crit. Care. 2023. Vol. 27, N 1. P. 430.
338. Xiao Z. et al. Development and validation of early prediction models for new-onset functional impairment in patients after being transferred from the ICU//Sci. Rep. 2024. Vol. 14, N 1. P. 11902.
339. Mazwi N. et al. Effects of mobility dose on discharge disposition in critically ill stroke patients//PM&R. 2023. Vol. 15, N 12. P. 1547 - 1556.
340. Yen H.-C. et al. Early Mobilization of Mild-Moderate Intracerebral Hemorrhage Patients in a Stroke Center: A Randomized Controlled Trial//Neurorehabil. Neural Repair. 2020. Vol. 34, N 1. P. 72 - 81.
341. Yang X. et al. More is less: Effect of ICF-based early progressive mobilization on severe aneurysmal subarachnoid hemorrhage in the NICU//Front. Neurol. 2022. Vol. 13.
342. Foudhaili A. et al. Early mobilization in patients with aneurysmal subarachnoid haemorrhage may im-prove functional status and reduce cerebral vasospasm rate: a systematic review with meta-analysis//J. Rehabil. Med. 2024. Vol. 56. P. jrm41225.
343. Mariana de Aquino Miranda J. et al. Early mobilization in acute stroke phase: a systematic review//Top. Stroke Rehabil. 2023. Vol. 30, N 2. P. 157 - 168.
344.  P. et al. Protocolized strategies to encourage early mobilization of critical care patients: challenges and success//Crit. Care Sci. 2025. Vol. 37.
P. et al. Protocolized strategies to encourage early mobilization of critical care patients: challenges and success//Crit. Care Sci. 2025. Vol. 37.
345. Kinoshita T. et al. Evaluation of severe adverse events during rehabilitation for acute-phase patients//Medicine (Baltimore). 2022. Vol. 101, N 25. P. e29516.
346. Woodbridge H.R. et al. Assessing the safety of physical rehabilitation in critically ill patients: a Delphi study//Crit. Care. 2024. Vol. 28, N 1. P. 144.
347. Schaller S.J. et al. Guideline on positioning and early mobilisation in the critically ill by an expert panel//Intensive Care Med. 2024. Vol. 50, N 8. P. 1211 - 1227.
348. Gregori-Pla C. et al. Blood flow response to orthostatic challenge identifies signatures of the failure of static cerebral autoregulation in patients with cerebrovascular disease//BMC Neurol. 2021. Vol. 21, N 1. P. 154.
349. Rethnam V. et al. Early mobilisation post-stroke: a systematic review and meta-analysis of inpidual participant data//Disabil. Rehabil. 2022. Vol. 44, N 8. P. 1156 - 1163.
350. Клинические рекомендации Союза реабилитологов России. Вертикализация пациентов в процессе реабилитации. URL: https://rehabrus.ru/Docs/Protokol_Vertikalizaciya.pdf [Electronic resource].
351. Zavaliy L.B. et al. Passive verticalization of patients in a multiprofile ICU//Anesteziol. i Reanimatol. 2020. N 6. P. 44.
352. Kumble S. et al. Physiological Effects of Early Incremental Mobilization of a Patient with Acute Intracerebral and Intraventricular Hemorrhage Requiring Dual External Ventricular Drainage//Neurocrit. Care. 2017. Vol. 27, N 1. P. 115 - 119.
353. ![]() A.O. et al. The association of early passive mobilization with intracranial pressure in the adult intensive care unit: A prospective, cohort study//Nurs. Crit. Care. 2025. Vol. 30, N 3.
A.O. et al. The association of early passive mobilization with intracranial pressure in the adult intensive care unit: A prospective, cohort study//Nurs. Crit. Care. 2025. Vol. 30, N 3.
354. Ramazanov G.R. et al. Progressive Early Rehabilitation Program Applied to Patients with Acute Cerebrovascular Accident//Russ. Neurol. J. 2020. Vol. 25, N 3. P. 17 - 25.
355. Imai R. et al. Regional cerebral oxygen saturation during initial mobilization of critically ill patients is associated with clinical outcomes: a prospective observational study//Intensive Care Med. Exp. 2025. Vol. 13, N 1. P. 13.
356. Yang Y. et al. Clinical effect of pulmonary rehabilitation in patients with mechanical ventilation: A meta-analysis//Int. J. Artif. Organs. 2024. Vol. 47, N 2. P. 96 - 106.
357. Rodrigues-Gomes R.M. et al. Effects of rapid chest compression technique on intracranial and cerebral perfusion pressures in acute neurocritical patients: a randomized controlled trial//Crit. Care. 2025. Vol. 29, N 1. P. 159.
358. Rose L. et al. Interventions to enable communication for adult patients requiring an artificial airway with or without mechanical ventilator support//Cochrane Database Syst. Rev. 2021. Vol. 2021, N 10.
359. Klem H.E. et al. Tidlig aktivitet hos respiratorpasienter - en metaanalyse//Tidsskr. Den Nor. legeforening. 2021.
360. Eimer C. et al. The Effect of Physical Therapy on Regional Lung Function in Critically Ill Patients//Front. Physiol. 2021. Vol. 12.
361. Shahid J., Kashif A., Shahid M.K. A Comprehensive Review of Physical Therapy Interventions for Stroke Rehabilitation: Impairment-Based Approaches and Functional Goals.//Brain Sci. 2023. Vol. 13, N 5.
362. Langton-Frost N. et al. Development and Implementation of a New Model of Care for Patients With Stroke, Acute Hospital Rehabilitation Intensive SErvices//Am. J. Phys. Med. Rehabil. 2023. Vol. 102, N 2S. P. S13-S18.
363. Zhou W. et al. Effect of early mobilization combined with early nutrition on acquired weakness in critically ill patients (EMAS): A dual-center, randomized controlled trial//PLoS One. 2022. Vol. 17, N 5. P. e0268599.
364. Formenti P. et al. Combined Effects of Early Mobilization and Nutrition on ICU-Acquired Weakness//Nutrients. 2025. Vol. 17, N 6. P. 1073.
365. Suputtitada A. et al. Best Practice Guidelines for the Management of Patients with Post-Stroke Spasticity: A Modified Scoping Review//Toxins (Basel). 2024. Vol. 16, N 2. P. 98.
366. Verduzco Gutierrez M. et al. AAPM&R consensus guidance on spasticity assessment and management//PM&R. 2024. Vol. 16, N 8. P. 864 - 887.
367. Badjatia N. et al. Neuromuscular Electrical Stimulation and High-Protein Supplementation After Subarachnoid Hemorrhage: A Single-Center Phase 2 Randomized Clinical Trial.//Neurocrit. Care. 2021. Vol. 35, N 1. P. 46 - 55.
368. Zayed Y. et al. Effects of neuromuscular electrical stimulation in critically ill patients: A systematic review and meta-analysis of randomised controlled trials//Aust. Crit. Care. 2020. Vol. 33, N 2. P. 203 - 210.
369. Dziewas R. et al. Decannulation ahead: a comprehensive diagnostic and therapeutic framework for tracheotomized neurological patients//Neurol. Res. Pract. 2025. Vol. 7, N 1. P. 18.
370. Dunn K., Rumbach A., Finch E. Dysphagia in non-traumatic subarachnoid haemorrhage: a scoping review//Neurosurg. Rev. 2020. Vol. 43, N 4. P. 1079 - 1087.
371. Skoretz S.A. et al. A Systematic Review of Tracheostomy Modifications and Swallowing in Adults//Dysphagia. 2020. Vol. 35, N 6. P. 935 - 947.
372. Belkin A.A., Ershov V.I., Ivanova G.E. Impairment of swallowing in urgent conditions-postextubation dysphagia//Anesteziol. i Reanimatol. 2018. N 4. P. 76.
373. McIntyre M. et al. Risk Factors for Postextubation Dysphagia: A Systematic Review and Meta analysis//Laryngoscope. 2022. Vol. 132, N 2. P. 364 - 374.
374. Suntrup-Krueger S. et al. Pharyngeal electrical stimulation for postextubation dysphagia in acute stroke: a randomized controlled pilot trial//Crit. Care. 2023. Vol. 27, N 1. P. 383.
375. McRae J. et al. The role of speech and language therapists in the intensive care unit//J. Intensive Care Soc. 2020. Vol. 21, N 4. P. 344 - 348.
376. Barra M.E. et al. Multidisciplinary Approach to Sedation and Early Mobility of Intubated Critically Ill Neurologic Patients Improves Mobility at Discharge//The Neurohospitalist. 2023. Vol. 13, N 4. P. 351 - 360.
377. Liu Y. et al. Pharmacological Prevention of Postoperative Delirium: A Systematic Review and Meta-Analysis of Randomized Controlled Trials//Evidence-Based Complement. Altern. Med. 2019. Vol. 2019. P. 1 - 10.
378. Burry L. et al. Pharmacological interventions for the treatment of delirium in critically ill adults//Cochrane Database Syst. Rev. 2019. Vol. 2019, N 9.
379. Ottens T.H. et al. The Delphi Delirium Management Algorithms. A practical tool for clinicians, the result of a modified Delphi expert consensus approach.//Delirium. 2024.
380. Potievskaya V.I. et al. Sedation of patients in intensive care units//Anesteziol. i Reanimatol. 2020. N 5. P. 7.
381. Porhomayon J. et al. The Impact of High Versus Low Sedation Dosing Strategy on Cognitive Dysfunction in Survivors of Intensive Care Units: A Systematic Review and Meta-Analysis//J. Cardiovasc. Thorac. Res. 2015. Vol. 7, N 2. P. 43 - 48.
382. Fischer T. et al. Strategies for Pain Assessment in Adult Patients With Delirium: A Scoping Review//J. Pain Symptom Manage. 2019. Vol. 58, N 3. P. 487 - 502.e11.
383. Nordness M.F. et al. Depression predicts long-term cognitive impairment in survivors of critical illness//J. Trauma Acute Care Surg. 2021. Vol. 90, N 1. P. 79 - 86.
384. Tilburgs B. et al. Associations Between Physical, Cognitive, and Mental Health Domains of Post-Intensive Care Syndrome and Quality of Life: A Longitudinal Multicenter Cohort Study//Crit. Care Med. 2025. Vol. 53, N 1. P. e74-e86.
385. Mercier L.J. et al. Development and integration of a music therapy program in the neurologic inpatient setting: a qualitative study//Disabil. Rehabil. 2025. Vol. 47, N 9. P. 2304 - 2313.
386. Byun E. et al. Sleep Disturbance and Self-management in Adults With Subarachnoid Hemorrhage: A Qualitative Study//Clin. Nurs. Res. 2022. Vol. 31, N 4. P. 632 - 638.
387. Tang B.H.Y. et al. Melatonin Use in the ICU: A Systematic Review and Meta-Analysis//Crit. Care Med. 2025. Vol. 53, N 9. P. e1714-e1724.
388. Fang C. et al. Effect of earplugs and eye masks on the sleep quality of intensive care unit patients: A systematic review and meta analysis//J. Adv. Nurs. 2021. Vol. 77, N 11. P. 4321 - 4331.
389. International Stroke Conference (ISC) 2017. Abstract 93. Presented February 22, 201. (2017). ICH Survivors at High Risk for Depression then Dementia. 23 - 24.
390. Algeo N., Aitken L.M. The evolving role of occupational therapists in adult critical care in England//Irish J. Occup. Ther. 2019. Vol. 47, N 2. P. 74 - 94.
391. Prohaska C.C. et al. Patterns of utilization and effects of hospital-specific factors on physical, occupational, and speech therapy for critically ill patients with acute respiratory failure in the USA: results of a 5-year sample//Crit. Care. 2019. Vol. 23, N 1. P. 175.
392. Bellon F. et al. The efficacy of nursing interventions on sleep quality in hospitalized patients: A systematic review of randomized controlled trials//Int. J. Nurs. Stud. 2021. Vol. 115. P. 103855.
393. Belkin A.A. et al. Prolonged Disorder of Consciousness - a New Concept in the Evaluation of Chronical Disorders of Consciousness in ICU Patients. A Multi-Disciplinary Concensus//Ann. Crit. Care. 2021. N 2. P. 7 - 16.
394. Stein J. et al. Which Road to Recovery?: Factors Influencing Postacute Stroke Discharge Destinations: A Delphi Study//Stroke. 2022. Vol. 53, N 3. P. 947 - 955.
395. Winstein C.J. et al. Guidelines for Adult Stroke Rehabilitation and Recovery//Stroke. 2016. Vol. 47, N 6.
396. Chen Y.-T. et al. Assessment of rehabilitation following subarachnoid haemorrhage in China: findings from the Chinese Stroke Center Alliance//BMC Neurol. 2023. Vol. 23, N 1. P. 291.
397. Hayward K.S. et al. Control intervention design for preclinical and clinical trials: Consensus-based core recommendations from the third Stroke Recovery and Rehabilitation Roundtable//Int. J. Stroke. 2024. Vol. 19, N 2. P. 169 - 179.
398. Teasell R. et al. Canadian Stroke Best Practice Recommendations: Rehabilitation, Recovery, and Community Participation following Stroke. Part One: Rehabilitation and Recovery Following Stroke; 6th Edition Update 2019//Int. J. Stroke. 2020. Vol. 15, N 7. P. 763 - 788.
399. Ifejika N.L. et al. Improving Access to Stroke Rehabilitation and Recovery: A Policy Statement From the American Heart Association/American Stroke Association//Stroke. 2025. Vol. 56, N 9.
400. Fedor B.A. et al. Motor Rehabilitation Provides Modest Functional Benefits After Intracerebral Hemorrhage: a Systematic Review and Meta-Analysis of Translational Rehabilitation Studies//Transl. Stroke Res. 2025. Vol. 16, N 2. P. 484 - 511.
401. Dunn K., Rumbach A., Finch E. Language function in the acute phase following non-traumatic subarachnoid haemorrhage: A prospective cohort study//J. Commun. Disord. 2022. Vol. 96. P. 106192.
402. Huang J. et al. Effects of physical therapy-based rehabilitation on recovery of upper limb motor function after stroke in adults: a systematic review and meta-analysis of randomized controlled trials//Ann. Palliat. Med. 2022. Vol. 11, N 2. P. 521 - 531.
403. Chen J., Or C.K., Chen T. Effectiveness of Using Virtual Reality-Supported Exercise Therapy for Upper Extremity Motor Rehabilitation in Patients With Stroke: Systematic Review and Meta-analysis of Randomized Controlled Trials//J. Med. Internet Res. 2022. Vol. 24, N 6. P. e24111.
404. Zhang T. et al. Chinese Stroke Association guidelines for clinical management of cerebrovascular disorders: executive summary and 2019 update of clinical management of stroke rehabilitation//Stroke Vasc. Neurol. 2020. Vol. 5, N 3. P. 250 - 259.
405. Laver K.E. et al. Telerehabilitation services for stroke//Cochrane Database Syst. Rev. 2020. Vol. 2020, N 1.
406. ZHU Jinfeng, ZHANG Yuanxing, WANG Fang et al. The effectiveness and safety of telerehabilitation management in stroke patients an overview of systematic reviews//Chinese J. Nurs. 2022. Vol. 57, N 12. P. 1447 - 1455.
407. Nascimento L.R. et al. Home-based exercises are as effective as equivalent doses of centre-based exercises for improving walking speed and balance after stroke: a systematic review//J. Physiother. 2022. Vol. 68, N 3. P. 174 - 181.
408. Puthucheary Z. et al. The Post-ICU presentation screen (PICUPS) and rehabilitation prescription (RP) for intensive care survivors part II: Clinical engagement and future directions for the national Post-Intensive care Rehabilitation Collaborative//J. Intensive Care Soc. 2022. Vol. 23, N 3. P. 264 - 272.
409. Sazonov I.E. et al. The use of cytoflavin in the acute period of hemorrhagic stroke//Zhurnal Nevrol. i psikhiatrii im. S.S. Korsakova. 2018. Vol. 118, N 2. P. 23.
410. Belkin A.A. et al. Results of a cohort single-center randomized study of the modulating effect of the drug Mexidol in the rehabilitation of patients who suffered acute cerebral insufficiency//S.S. Korsakov J. Neurol. Psychiatry. 2024. Vol. 124, N 4. P. 108.
411. Belkin A.A. et al. Adjuvant pharmacological modulation with Cytoflavin in rehabilitation at stages 2 - 3 in patients with acute cerebral insufficiency and post-intensive care syndrome//S.S. Korsakov J. Neurol. Psychiatry. 2025. Vol. 125, N 3. P. 78.
412. Belkin A.A., Belkin V.A., Vasilchenko I.E. Dynamics of emotional-cognitive and motor disorder domains in the Post Intensive Care Syndrome structure in acute cerebral insufficiency patients//Phys. Rehabil. Med. Med. Rehabil. 2024. Vol. 6, N 4. P. 348 - 359.
413. Marquez-Romero J.M. et al. Fluoxetine for motor recovery after acute intracerebral hemorrhage, the FMRICH trial//Clin. Neurol. Neurosurg. 2020. Vol. 190. P. 105656.
414. Kubiszewski P. et al. Association of Selective Serotonin Reuptake Inhibitor Use After Intracerebral Hemorrhage With Hemorrhage Recurrence and Depression Severity//JAMA Neurol. 2021. Vol. 78, N 1. P. 61.
415. Epprecht L. et al. Sexual Dysfunction After Good-Grade Aneurysmal Subarachnoid Hemorrhage//World Neurosurg. 2018. Vol. 111. P. e449 - e453.
416. Голанов А.В., Костюченко В.В. Нейрохирургия на Гамма-Ноже. 2018. Vol. 708.
417. Thrash G.W. et al. Stereotactic radiosurgery treatment of pediatric arteriovenous malformations: a PRISMA systematic review and meta-analysis//Child's Nerv. Syst. 2025. Vol. 41, N 1. P. 188.
418. Lim J.H., Kim M.J. Considerations for the Use of Stereotactic Radiosurgery to Treat Large Arteriovenous Malformations//Biomedicines. 2024. Vol. 12, N 9. P. 2003.
419. Shaaban A. et al. Repeat Single-Session Stereotactic Radiosurgery for Cerebral Arteriovenous Malformations: A Systematic Review, Meta-Analysis, and International Stereotactic Radiosurgery Society Practice Guidelines//Neurosurgery. 2025. Vol. 96, N 1. P. 29 - 40.
420. Chapman N. et al. Effects of a Perindopril-Based Blood Pressure-Lowering Regimen on the Risk of Recurrent Stroke According to Stroke Subtype and Medical History//Stroke. 2004. Vol. 35, N 1. P. 116 - 121.
421. Biffi A. et al. Association Between Blood Pressure Control and Risk of Recurrent Intracerebral Hemorrhage//JAMA. 2015. Vol. 314, N 9. P. 904.
422. Hilkens N.A. et al. Blood pressure levels and the risk of intracerebral hemorrhage after ischemic stroke//Neurology. 2017. Vol. 88, N 2. P. 177 - 181.
423. Al-Shahi Salman R. et al. Effects of oral anticoagulation for atrial fibrillation after spontaneous intracranial haemorrhage in the UK: a randomised, open-label, assessor-masked, pilot-phase, non-inferiority trial//Lancet Neurol. 2021. Vol. 20, N 10. P. 842 - 853.
424. Pennlert J. et al. Optimal Timing of Anticoagulant Treatment After Intracerebral Hemorrhage in Patients With Atrial Fibrillation//Stroke. 2017. Vol. 48, N 2. P. 314 - 320.
425. Schreuder F.H.B.M. et al. Apixaban versus no anticoagulation after anticoagulation-associated intracerebral haemorrhage in patients with atrial fibrillation in the Netherlands (APACHE-AF): a randomised, open-label, phase 2 trial//Lancet Neurol. 2021. Vol. 20, N 11. P. 907 - 916.
426. Reddy V.Y. et al. 5-Year Outcomes After Left Atrial Appendage Closure//J. Am. Coll. Cardiol. 2017. Vol. 70, N 24. P. 2964 - 2975.
427. Hucker W.J. et al. WATCHMAN implantation in patients with a history of atrial fibrillation and intracranial hemorrhage//J. Interv. Card. Electrophysiol. 2020. Vol. 59, N 2. P. 415 - 421.
428. Nielsen-Kudsk J.E. et al. Left atrial appendage occlusion versus standard medical care in patients with atrial fibrillation and intracerebral haemorrhage: a propensity score-matched follow-up study//EuroIntervention. 2017. Vol. 13, N 3. P. 371 - 378.
429. Schrag M. et al. Left Atrial Appendage Closure for Patients with Cerebral Amyloid Angiopathy and Atrial Fibrillation: the LAA-CAA Cohort//Transl. Stroke Res. 2021. Vol. 12, N 2. P. 259 - 265.
430. Kuramatsu J.B. et al. Management of therapeutic anticoagulation in patients with intracerebral haemorrhage and mechanical heart valves//Eur. Heart J. 2018. Vol. 39, N 19. P. 1709 - 1723.
431. Cho S.-M. et al. Reversal and Resumption of Antithrombotic Therapy in LVAD-Associated Intracranial Hemorrhage//Ann. Thorac. Surg. 2019. Vol. 108, N 1. P. 52 - 58.
432. Islam M.M. et al. Risk of Hemorrhagic Stroke in Patients Exposed to Nonsteroidal Anti-Inflammatory Drugs: A Meta-Analysis of Observational Studies//Neuroepidemiology. 2018. Vol. 51, N 3 - 4. P. 166 - 176.
433. Ungprasert P., Matteson E.L., Thongprayoon C. Nonaspirin Nonsteroidal Anti-Inflammatory Drugs and Risk of Hemorrhagic Stroke//Stroke. 2016. Vol. 47, N 2. P. 356 - 364.
434. Sabatine M.S. et al. Evolocumab and Clinical Outcomes in Patients with Cardiovascular Disease//N. Engl. J. Med. 2017. Vol. 376, N 18. P. 1713 - 1722.
435. Robinson J.G. et al. Efficacy and Safety of Alirocumab in Reducing Lipids and Cardiovascular Events//N. Engl. J. Med. 2015. Vol. 372, N 16. P. 1489 - 1499.
436. Sanz-Cuesta B.E., Saver J.L. Lipid-Lowering Therapy and Hemorrhagic Stroke Risk//Stroke. 2021. Vol. 52, N 10. P. 3142 - 3150.
437. Barr J.C., Ogilvy C.S. Selection of Treatment Modalities or Observation of Arteriovenous Malformations//Neurosurg. Clin. N. Am. 2012. Vol. 23, N 1. P. 63 - 75.
438. Brain arteriovenous malformations. 2021. P. 171 - 178.
439. Holloway R.G. et al. Palliative and End-of-Life Care in Stroke//Stroke. 2014. Vol. 45, N 6. P. 1887 - 1916.
440. Epstein R.M. et al. Why The Nation Needs A Policy Push On Patient-Centered Health Care//Health Aff. 2010. Vol. 29, N 8. P. 1489 - 1495.
441. Fromme E.K. et al. POLST Registry Do-Not-Resuscitate Orders and Other Patient Treatment Preferences//JAMA. 2012. Vol. 307, N 1. P. 34.
442. Rosen D.S., Macdonald R.L. Subarachnoid Hemorrhage Grading Scales: A Systematic Review//Neurocrit. Care. 2005. Vol. 2, N 2. P. 110 - 118.
443. Report of World Federation of Neurological Surgeons Committee on a Universal Subarachnoid Hemorrhage Grading Scale//J. Neurosurg. 1988. Vol. 68, N 6.
444. Roy D., Milot G., Raymond J. Endovascular Treatment of Unruptured Aneurysms//Stroke. 2001. Vol. 32, N 9. P. 1998 - 2004.
445. Suponeva N.A. et al. Validation of the modified Rankin Scale in Russia//Neurol. Neuropsychiatry, Psychosom. 2018. Vol. 10, N 4. P. 36 - 39.
446. Meng X. et al. Radiosurgery-Based AVM Scale Is Proposed for Combined Embolization and Gamma Knife Surgery for Brain Arteriovenous Malformations//Front. Neurol. 2021. Vol. 12.
447. Zabolotskikh I.B. et al. Anesthesia and intensive care for patients with COVID-19. Russian Federation of anesthesiologists and reanimatologists guidelines//Ann. Crit. Care. 2021. N 1-S. P. 9 - 143.
448. Adams H.P. et al. Baseline NIH Stroke Scale score strongly predicts outcome after stroke//Neurology. 1999. Vol. 53, N 1. P. 126 - 126.
449. Ivankova E.O., Darvin V. V., Bessmertnykh M.A. Evaluation of the immediate and long-term results of endovascular treatment of ruptured vertebrobasilar artery aneurysms in an acute period of hemorrhage//Russ. J. Neurosurg. 2019. Vol. 20, N 4. P. 31 - 37.
Приложение А1
СОСТАВ
РАБОЧЕЙ ГРУППЫ ПО РАЗРАБОТКЕ И ПЕРЕСМОТРУ
КЛИНИЧЕСКИХ РЕКОМЕНДАЦИЙ
1. Нейрохирурги и эндоваскулярные хирурги
Крылов Владимир Викторович - академик РАН, д.м.н., профессор, главный внештатный специалист нейрохирург Министерства здравоохранения Российской Федерации, директор Института функциональной нейрохирургии ФГБНУ РЦНН, заведующий кафедрой фундаментальной нейрохирургии Института нейронаук и нейротехнологий ФГАОУ ВО "Российский научно-исследовательский медицинский университет имени Н.И. Пирогова" Минздрава России, главный научный сотрудник отделения неотложной нейрохирургии ГБУЗ "НИИ СП им. Н.В. Склифосовского ДЗМ"
Усачев Дмитрий Юрьевич - академик РАН, д.м.н., профессор, директор ФГАУ "НМИЦ нейрохирургии им. академика Н.Н. Бурденко" МЗ РФ, заведующий кафедрой нейрохирургии ФГБОУ ДПО "Российская медицинская академия непрерывного профессионального образования" МЗ РФ, президент Ассоциации нейрохирургов России
Арустамян Сергей Размикович - д.м.н., ведущий научный сотрудник 4 отделения ФГАУ "НМИЦ нейрохирургии им. академика Н.Н. Бурденко" МЗ РФ, профессор кафедры нейрохирургии с курсами нейронаук ФГАУ "НМИЦ нейрохирургии им. академика Н.Н. Бурденко" МЗ РФ
Бахарев Евгений Юрьевич - к.м.н., старший научный сотрудник отделения неотложной нейрохирургии ГБУЗ "НИИ СП им. Н.В. Склифосовского ДЗМ"
Берестов Вадим Вячеславович - к.м.н., научный сотрудник НИЦ эндоваскулярный нейрохирургии ФГБУ ФЦМН ФМБА РФ, врач-нейрохирург ГБУЗ "МДГКБ ДЗМ"
Годков Иван Михайлович - д.м.н., руководитель службы нейрохирургии и нейротравмы Московского многопрофильного клинического центра "Коммунарка" ДЗМ, доцент кафедры фундаментальной нейрохирургии Института нейронаук и нейротехнологий ФГАОУ ВО "Российский научно-исследовательский медицинский университет имени Н.И. Пирогова" Минздрава России
Дмитриев Александр Юрьевич - к.м.н., доцент кафедры нейрохирургии ФГБОУ ВО "Российский университет медицины" МЗ РФ, врач-нейрохирург отделения неотложной нейрохирургии ГБУЗ "НИИ СП им. Н.В. Склифосовского ДЗМ"
Орлов Кирилл Юрьевич - д.м.н., профессор кафедры неврологии и нейрохирургии с курсом комплексной реабилитации ФНМО МИ ФГАОУ ВО "Российский университет дружбы народов имени Патриса Лумумбы", руководитель научно-исследовательского центра эндоваскулярной нейрохирургии ФГБУ "Федеральный центр мозга и нейротехнологий" ФМБА России, врач-нейрохирург нейрохирургического отделения ГБУЗ города Москвы "Морозовская детская городская клиническая больница Департамента здравоохранения города Москвы", директор Ассоциации эндоваскулярных нейрохирургов имени академика Ф.А. Сербиненко
Пилипенко Юрий Викторович - д.м.н., ведущий научный сотрудник 3 отделения ФГАУ "НМИЦ нейрохирургии им. академика Н.Н. Бурденко" МЗ РФ, доцент кафедры нейрохирургии с курсами нейронаук ФГАУ "НМИЦ нейрохирургии им. академика Н.Н. Бурденко" МЗ РФ
Полунина Наталья Алексеевна - д.м.н., доцент кафедры фундаментальной нейрохирургии Института нейронаук и нейротехнологий ФГАОУ ВО "Российский научно-исследовательский медицинский университет имени Н.И. Пирогова" Минздрава России, старший научный сотрудник отделения неотложной нейрохирургии ГБУЗ "НИИ СП им. Н.В. Склифосовского ДЗМ", нейрохирург Московского многопрофильного клинического центра "Коммунарка" ДЗМ
Природов Александр Владиславович - д.м.н., профессор кафедры фундаментальной нейрохирургии Института нейронаук и нейротехнологий ФГАОУ ВО "Российский научно-исследовательский медицинский университет имени Н.И. Пирогова" Минздрава России, заведующий нейрохирургическим отделением, ведущий научный сотрудник ГБУЗ "НИИ СП им. Н.В. Склифосовского ДЗМ"
Рак Вячеслав Августович - к.м.н., доцент кафедры фундаментальной нейрохирургии Института нейронаук и нейротехнологий ФГАОУ ВО "Российский научно-исследовательский медицинский университет имени Н.И. Пирогова" Минздрава России
Хамурзов Валерий Альбертович - врач-нейрохирург отделения неотложной нейрохирургии ГБУЗ "НИИ СП им. Н.В. Склифосовского ДЗМ"
Хейреддин Али Садек - д.м.н., ведущий научный сотрудник ФГАУ НМИЦ нейрохирургии им. Н.Н. Бурденко МЗ РФ
Элиава Шалва Шалвович - член-корр. РАН, д.м.н., профессор, заведующий 3 отделением ФГАУ "НМИЦ нейрохирургии им. академика Н.Н. Бурденко" МЗ РФ
Яковлев Сергей Борисович - д.м.н., заведующий 4 отделением ФГАУ "НМИЦ нейрохирургии им. академика Н.Н. Бурденко" МЗ РФ, профессор кафедры детской нейрохирургии ФГБОУ ДПО "Российская медицинская академия непрерывного профессионального образования" МЗ РФ
2. Неврологи
Шамалов Николай Анатольевич - д.м.н., профессор, главный внештатный специалист невролог Министерства здравоохранения Российской Федерации, главный внештатный специалист невролог Департамента здравоохранения г. Москвы, директор института цереброваскулярной патологии и инсульта ФГБУ "Федеральный центр мозга и нейротехнологий" ФМБА России, ответственный секретарь Национальной ассоциации по борьбе с инсультом.
Алашеев Андрей Марисович - д.м.н., главный внештатный специалист невролог Минздрава России по Уральскому федеральному округу, заведующий неврологическим отделением для больных с НМК ГАУЗ СО "Свердловская областная клиническая больница N 1", член WSO и fellow-член ESO.
Белоусова Ольга Беннуановна - д.м.н., главный научный сотрудник 3 отделения ФГАУ "НМИЦ нейрохирургии им. академика Н.Н. Бурденко МЗ РФ, профессор кафедры нейрохирургии с курсами нейронаук ФГАУ "НМИЦ нейрохирургии им. академика Н.Н. Бурденко" МЗ РФ
Вознюк Игорь Алексеевич - д.м.н., профессор, главный внештатный специалист-невролог Комитета по Здравоохранению Санкт-Петербурга, главный внештатный специалист-невролог Минздрава России по Северо-Западному федеральному округу, профессор кафедры неврологии, заместитель главного врача по неврологии ФГБОУ ВО ПСПбГМУ им. академ. И.П. Павлова.
Гехт Алла Борисовна - д.м.н., профессор, член-корреспондент РАН, директор ГБУЗ "Научно-практический психоневрологический центр имени З.П. Соловьева" Департамента здравоохранения города Москвы, профессор кафедры неврологии, нейрохирургии и медицинской генетики ФГАОУ ВО "Российский научно-исследовательский медицинский университет имени Н.И. Пирогова" Минздрава России, член президиума Национальной ассоциации по борьбе с инсультом, ученый секретарь Всероссийского общества неврологов
Гусев Евгений Иванович - д.м.н., академик РАН, профессор кафедры неврологии, нейрохирургии и медицинской ФГАОУ ВО "Российский научно-исследовательский медицинский университет имени Н.И. Пирогова" Минздрава России, президент Национальной ассоциации по борьбе с инсультом, председатель Всероссийского общества неврологов.
Завалий Леся Богдановна - к.м.н., старший научный сотрудник научного отделения неотложной неврологии и восстановительного лечения, врач-невролог ГБУЗ "НИИ скорой помощи имени Н.В. Склифосовского ДЗМ".
Кольцов Иван Алексеевич - к.м.н., старший научный сотрудник Научно-исследовательской лаборатории сосудистых заболеваний головного мозга ФГАОУ ВО РНИМУ им. Н.И. Пирогова Минздрава России, старший научный сотрудник отдела нейроиммунологии ФГБУ ФЦМН ФМБА России.
Марская Наталия Андреевна - научный сотрудник отдела сосудистых заболеваний нервной системы ФГБУ "Федеральный центр мозга и нейротехнологий" ФМБА России.
Мартынов Михаил Юрьевич - д.м.н., профессор, член-корреспондент РАН, первый заместитель генерального директора ФГБУ "Федеральный центр мозга и нейротехнологий" ФМБА России, заведующий кафедрой неврологии, нейрохирургии и медицинской генетики ФГАОУ ВО "Российский научно-исследовательский медицинский университет имени Н.И. Пирогова" Минздрава России, ученый секретарь Всероссийского общества неврологов, член правления Национальной ассоциации по борьбе с инсультом.
Фидлер Михаил Сергеевич - эксперт-аналитик отдела аналитической работы управления по реализации функций НМИЦ по неврологии, ассистент кафедры неврологии, нейрохирургии и медицинской генетики лечебного факультета ФГАОУ ВО РНИМУ им. Н.И. Пирогова Минздрава России.
Харитонова Татьяна Витальевна - к.м.н., старший научный сотрудник ГБУ "Санкт-Петербургский НИИ Скорой помощи им. И.И. Джанелидзе".
Хасанова Дина Рустемовна - д.м.н., профессор, профессор кафедры неврологии ФГБОУ ВО "Казанский государственный медицинский университет" Министерства здравоохранения Российской Федерации, главный внештатный невролог Министерства здравоохранения Российской Федерации по ПФО, член правления Национальной ассоциации по борьбе с инсультом, член Правления Всероссийского общества неврологов.
Щукин Иван Александрович - к.м.н., доцент кафедры неврологии, нейрохирургии и медицинской генетики лечебного факультета ФГАОУ ВО РНИМУ им. Н.И. Пирогова Минздрава России, старший научный сотрудник отдела нейроиммунологии ФГБУ ФЦМН ФМБА России
Янишевский Станислав Николаевич - д.м.н., профессор, заведующий НИЛ неврологии и нейрореабилитации, профессор кафедры неврологии и с клиникой НМИЦ им. В.А. Алмазова, президент Ассоциации "Общество неврологов Санкт-Петербурга и Ленинградской области"
3. Рентгенологи
Григорьева Елена Владимировна - д.м.н., заведующая кафедрой рентгенологии ФГБОУ ВО "Российский Университет медицины" Минздрава РФ НОИ клинической медицины им. Н.А. Семашко, заведующая отделением лучевой диагностики Университетской клиники НОИ клинической медицины им. Н.А. Семашко
Пронин Игорь Николаевич - академик РАН, д.м.н., профессор, руководитель отделения рентгеновских и радиоизотопных методов диагностики, заместитель директора ФГАУ "НМИЦ" нейрохирургии им. Ак. Н.Н. Бурденко Минздрава России
4. Радиотерапевты
Голанов А.В. - член-корр. РАН, д.м.н., профессор, заведующий отделением радиотерапии ФГАУ "НМИЦ нейрохирургии им. академика Н.Н. Бурденко" МЗ РФ
Лестровая Арина Игоревна - к.м.н., младший научный сотрудник отделения радиотерапии ФГАУ "НМИЦ нейрохирургии им. академика Н.Н. Бурденко" МЗ РФ
5. Анестезиологи и реаниматологи
Баранич Анастасия Ивановна - к.м.н., врач анестезиолог-реаниматолог, клинический фармаколог отделения анестезиологии-реанимации ФГАУ "НМИЦ нейрохирургии им. академика Н.Н. Бурденко" МЗ РФ
Карпунин Андрей Юрьевич - к.м.н., первый заместитель министра здравоохранения Республики Алтай, заместитель директора ГБУЗ "НИИ СП им. Н.В. Склифосовского ДЗМ" по организационной методической работе
Куликов Александр Сергеевич - д.м.н., заведующий отделением анестезиологии-реанимации ФГАУ "НМИЦ нейрохирургии им. академика Н.Н. Бурденко" МЗ РФ
Курдюмова Наталия Вячеславовна - д.м.н., врач анестезиолог-реаниматолог отделения анестезиологии-реанимации ФГАУ "НМИЦ нейрохирургии им. академика Н.Н. Бурденко" МЗ РФ
Лубнин Андрей Юрьевич - д.м.н., профессор, ведущий научный сотрудник отделения анестезиологии-реанимации ФГАУ "НМИЦ нейрохирургии им. академика Н.Н. Бурденко" МЗ РФ
Петриков Сергей Сергеевич - академик РАН, профессор РАН, д.м.н., директор ГБУЗ "НИИ СП им. Н.В. Склифосовского ДЗМ", заведующий кафедрой анестезиологии, реаниматологии и неотложной медицины ФГБОУ ВО "Российский университет медицины" МЗ РФ, президент МОО "Объединение нейроанестезиологов и нейрореаниматологов"
Савин Иван Анатольевич - д.м.н., заведующий отделением реанимации и интенсивной терапии отделения анестезиологии-реанимации ФГАУ "НМИЦ нейрохирургии им. академика Н.Н. Бурденко" МЗ РФ
6. Реабилитологи
Иванова Галина Евгеньевна - д.м.н., профессор, руководитель научно-исследовательского центра медицинской реабилитации ФГБУ "ФЦМН" ФМБА России, заведующая отделом медико-социальной реабилитации инсульта НИИ цереброваскулярной патологии и инсульта, заведующая кафедрой медицинской реабилитации ИНОПР ФГАОУ ВО "Российский научно-исследовательский медицинский университет имени Н.И. Пирогова" Минздрава России, Председатель диссертационного совета при ФГАОУ ВО "Российский научно-исследовательский медицинский университет имени Н.И. Пирогова" Минздрава России, главный внештатный специалист по медицинской реабилитации Минздрава России, Председатель президиума Общероссийской общественной организации содействия развитию медицинской реабилитологии "Союз реабилитологов России", генеральный секретарь Российской ассоциации по спортивной медицине и реабилитации больных и инвалидов.
Белкин Андрей Августович - д.м.н., профессор кафедр анестезиологии-реаниматологии, физической реабилитационной медицины и нервных болезней ФГБОУ ВО "Уральский государственный медицинский университет", директор Клинического института мозга, главный внештатный специалист МЗ РФ по реабилитации в Уральском федеральном округе.
Конфликт интересов: отсутствует.
Приложение А2
МЕТОДОЛОГИЯ РАЗРАБОТКИ КЛИНИЧЕСКИХ РЕКОМЕНДАЦИЙ
Целевая аудитория данных клинических рекомендаций:
1. врачи-неврологи
2. врачи-нейрохирурги
3. врачи-анестезиологи-реаниматологи
4. врачи по медицинской реабилитации
5. врачи-рентгенологи
Таблица 1. Шкала оценки уровней достоверности доказательств (УДД) для методов диагностики (диагностических вмешательств)
УДД
Расшифровка
1
Систематические обзоры исследований с контролем референсным методом или систематический обзор рандомизированных клинических исследований с применением мета-анализа
2
Отдельные исследования с контролем референсным методом или отдельные рандомизированные клинические исследования и систематические обзоры исследований любого дизайна, за исключением рандомизированных клинических исследований, с применением мета-анализа
3
Исследования без последовательного контроля референсным методом или исследования с референсным методом, не являющимся независимым от исследуемого метода или нерандомизированные сравнительные исследования, в том числе когортные исследования
4
Несравнительные исследования, описание клинического случая
5
Имеется лишь обоснование механизма действия или мнение экспертов
Таблица 2. Шкала оценки уровней достоверности доказательств (УДД) для методов профилактики, лечения и реабилитации (профилактических, лечебных, реабилитационных вмешательств)
УДД
Расшифровка
1
Систематический обзор РКИ с применением мета-анализа
2
Отдельные РКИ и систематические обзоры исследований любого дизайна, за исключением РКИ, с применением мета-анализа
3
Нерандомизированные сравнительные исследования, в т.ч. когортные исследования
4
Несравнительные исследования, описание клинического случая или серии случаев, исследования "случай-контроль"
5
Имеется лишь обоснование механизма действия вмешательства (доклинические исследования) или мнение экспертов
Таблица 3. Шкала оценки уровней убедительности рекомендаций (УУР) для методов профилактики, диагностики, лечения и реабилитации (профилактических, диагностических, лечебных, реабилитационных вмешательств)
УУР
Расшифровка
A
Сильная рекомендация (все рассматриваемые критерии эффективности (исходы) являются важными, все исследования имеют высокое или удовлетворительное методологическое качество, их выводы по интересующим исходам являются согласованными)
B
Условная рекомендация (не все рассматриваемые критерии эффективности (исходы) являются важными, не все исследования имеют высокое или удовлетворительное методологическое качество и/или их выводы по интересующим исходам не являются согласованными)
C
Слабая рекомендация (отсутствие доказательств надлежащего качества (все рассматриваемые критерии эффективности (исходы) являются неважными, все исследования имеют низкое методологическое качество и их выводы по интересующим исходам не являются согласованными)
Порядок обновления клинических рекомендаций.
Механизм обновления клинических рекомендаций предусматривает их систематическую актуализацию - не реже чем один раз в три года, а также при появлении новых данных с позиции доказательной медицины по вопросам диагностики, лечения, профилактики и реабилитации конкретных заболеваний, наличии обоснованных дополнений/замечаний к ранее утвержденным КР, но не чаще 1 раза в 6 месяцев.
Приложение А3
СПРАВОЧНЫЕ МАТЕРИАЛЫ,
ВКЛЮЧАЯ СООТВЕТСТВИЕ ПОКАЗАНИЙ К ПРИМЕНЕНИЮ
И ПРОТИВОПОКАЗАНИЙ, СПОСОБОВ ПРИМЕНЕНИЯ И ДОЗ ЛЕКАРСТВЕННЫХ
ПРЕПАРАТОВ, ИНСТРУКЦИИ ПО ПРИМЕНЕНИЮ
ЛЕКАРСТВЕННОГО ПРЕПАРАТА
1. Федеральный закон от 21.11.2011 N 323-ФЗ (ред. от 02.07.2021) "Об основах охраны здоровья граждан в Российской Федерации" (Собрание законодательства Российской Федерации, 2011, N 48, ст. 6724) (с изм. и доп., вступ. в силу с 01.10.2021) (https://roszdravnadzor.gov.ru/documents/100)
2. Приказ Минздрава России от 10.05.2017 N 203н "Об утверждении критериев качества оценки медицинской помощи"; (Зарегистрировано в Минюсте России 17.05.2017 N 46740); (http://publication.pravo.gov.ru/Document/View/0001201705170016?rangeSize=1) действовал до 31.08.2025;
3. Приказ Министерства здравоохранения Российской Федерации от 14 апреля 2025 г. N 203н "Об утверждении критериев оценки качества медицинской помощи"; (Зарегистрировано в Минюсте России 28 мая 2025 г. N 82382); (http://publication.pravo.gov.ru/document/0001202505290045); вступил в силу с 01.09.2025;
4. Приказ Министерства здравоохранения РФ от 28.02.2019 N 103н "Об утверждении порядка и сроков разработки клинических рекомендаций, их пересмотра, типовой формы клинических рекомендаций и требований к их структуре, составу и научной обоснованности включаемой в клинические рекомендации информации".
5. Международная классификация болезней, травм и состояний, влияющих на здоровье (МКБ-10) (https://mkb-10.com/);
6. Государственный реестр лекарственных средств (http://www.grls.rosminzdrav.ru/grls.aspx);
7. Приказ Минздрава России N 804н от 13 октября 2017 г. "Об утверждении номенклатуры медицинских услуг", зарегистрирован в Минюсте 7 ноября 2017, регистрационный N 48808 (ред. 24.03.2020)
Таблица 1. Методы коммуникации с пациентом после инсульта, применяемые при оказании паллиативной помощи [439]
Метод
Комментарий/Пример
Стратегии построения доверия
Поощряйте пациентов и их семьи к общению; признайте ошибки; будьте скромны; проявляйте уважение; не навязывайте решения; внимательно слушайте, прежде чем ответить.
"Предупредительный выстрел"
Когда начинаете обсуждение плохих новостей: "Боюсь, мне нужно поделиться с вами неприятными новостями".
Используйте тишину эффективно
После сообщения плохих новостей не поддавайтесь искушению заполнить паузу новыми медицинскими фактами.
Информация о темпе и периодическая обратная связь
"Мы на верном пути?"
"Что важного для вас мы не упомянули?"
Используйте слово "умирание" эффективно.
"Судя по тому, что с вами происходит, и насколько сильно вы заболели, я считаю, что вы (ваш близкий человек) умираете".
Осторожно используйте слово "извините".
Часто ошибочно интерпретируется как отчужденность, жалость или признание ответственности.
Высказывания типа "Я хотел бы"
Одновременное выражение эмпатии и ограничений лечения: "Я хотел бы, чтобы у нас были лучшие методы лечения вашего заболевания".
Помогите разработать стратегии преодоления трудностей.
"Что вам дает силы или поддержку?"
"Что помогало в прошлом?"
Инструменты коммуникации для разрешения конфликтов
Активное слушание, самораскрытие, объяснение своей точки зрения, переосмысление и мозговой штурм
Стратегии переосмысления надежды
Легкий юмор, обзор жизни, концентрация на значимых действиях
Подытожьте и сформулируйте свое понимание.
"Позвольте мне убедиться, что я вас правильно понял".
Реакция на эмоции:
Назовите выраженную эмоцию.
"Я вижу, что это очень расстраивает".
"Кажется, вы потрясены этой новостью".
Поймите и проявите сочувствие, если оно искреннее.
"Представляю, как это тяжело".
"Я бы, наверное, чувствовал то же самое".
"Не могу представить, насколько это тяжело для вас".
Уважайте поведение семьи.
"Любой на вашем месте расстроился бы".
"Многие сейчас рассердились бы".
Поддержите семью, выразив готовность помочь.
"Мы справимся с этим вместе".
"Вы хотите, чтобы я кому-нибудь позвонил?"
Узнайте больше о том, что скрывается за эмоцией
"Расскажите, что вас больше всего расстраивает"
"Расскажите, что вас больше всего беспокоит"
Приложение Б
АЛГОРИТМЫ ДЕЙСТВИЙ ВРАЧА
Приложение Б1
АЛГОРИТМ
ВЕДЕНИЯ ПАЦИЕНТА С ГЕМОРРАГИЧЕСКИМ ИНСУЛЬТОМ ПО ТИПУ
ФОРМИРОВАНИЯ ГИПЕРТЕНЗИВНОЙ ВНУТРИМОЗГОВОЙ ГЕМАТОМЫ
(ДИАГНОСТИКА И ВЫБОР МЕТОДА ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ)
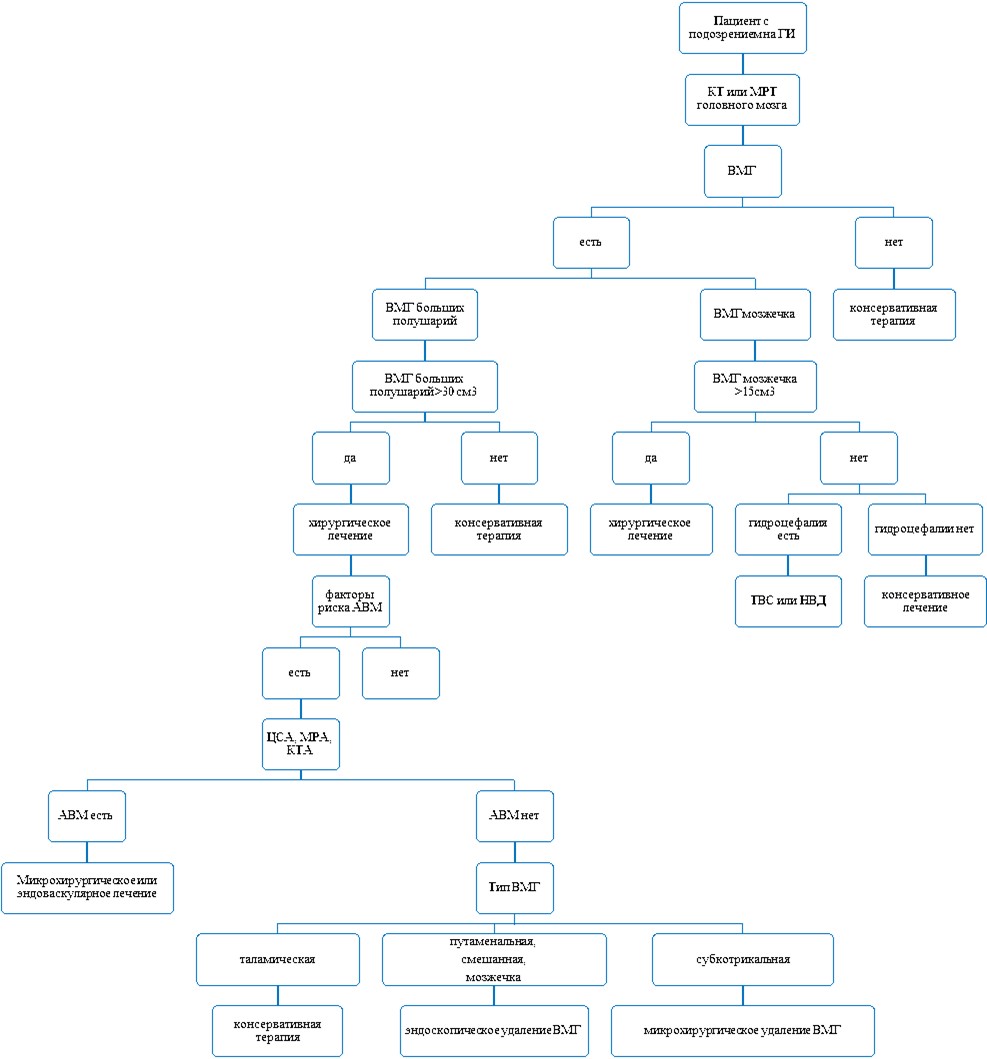
Приложение Б2
АЛГОРИТМ
ИНАКТИВАЦИИ АНТИТРОМБОТИЧЕСКИХ СРЕДСТВ (B01) НА ФОНЕ
ГИПЕРТЕНЗИВНОЙ ВНУТРИМОЗГОВОЙ ГЕМАТОМЫ [5, 37, 116, 117]
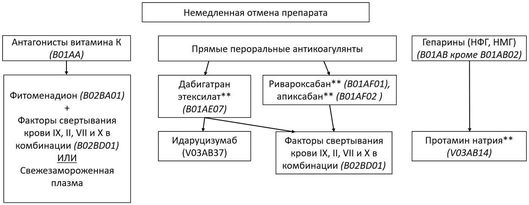
Приложение Б3
СТОП-СИГНАЛЫ
НАЧАЛА И ПРОДОЛЖЕНИЯ РЕАБИЛИТАЦИОННЫХ ПРОЦЕДУР [330, 331]
Абсолютные противопоказания к началу мобилизации:
- Острый инфаркт миокарда в момент начала мобилизации
- Субарахноидальное кровоизлияние при неклипированной аневризме
- Шок
- Тромбоэмболия легочной артерии, прогрессирующий тромбоз вен нижних конечностей по данным ультразвукового исследования или наличие флотирующего тромба (в отсутствии кава-фильтра, временного, постоянного***)
- Нестабилизированный перелом позвоночника, таза, нижних конечностей
- Отказ пациента
- Необходимость нейромышечной блокады
- Активное кровотечение
- Наружная кардиостимуляция
Относительные противопоказания к началу мобилизации:
- Отсутствие в составе МДРК подготовленного врача-анестезиолога--реаниматолога, врача по медицинской реабилитации, а также возможности адекватного аппаратного мониторинга на этапах реабилитации
Динамические СТОП-сигналы
N
Раздел мониторинга
Диапазон допустимых значений ![]()
Метод регистрации
Противопоказания к началу или STOP сигналы в ходе проведения* ![]()
Обязательные модальности
1
Волемический статус
отрицательный PLR-test
клинический тест
положительный PLR-тест
2
Систолическое давление (САД)
> 90; < 180 мм рт. ст.
> 90; < 200
неинвазивный (инвазивный при показаниях по основному заболеванию) аппаратный мониторинг
Снижение САД более, чем на 20 мм рт. ст. или 20% от исходного
САД < 100 или > 180 в течение более 3 минут манипуляции
3
Диастолическое давление (ДАД)
> 50; < 110 мм рт. ст.
Снижение ДАД на 10 мм рт. ст. или 20% от исходного уровня в течение более 3 минут
ДАД < 50 или > 110
4
Среднее артериальное давление (СрАД)
> 60 мм рт. ст. < 110 мм рт. ст.
СрАД < 60 или > 110
Снижение среднего АД на 15 мм рт. ст.
5
Центральная гемодинамика
отсутствие признаков острого коронарного синдрома
Мониторирование электрокардиографических данных (ЭКГ мониторинг)
Депрессия сегмента ST (> 2 мм) с нормальной ЭКГ покоя
Подъем ST сегмента (> 1 мм) в отведениях без патологических зубцов Q (кроме V1 или AVR)
Отрицательные или нарастающие Т
6
Сердечный ритм
Синусовый ритм или постоянная форма фибрилляции предсердий
Остро возникшая аритмия]
Появление блокады ножки пучка Гиса, особенно если она неотличима от желудочковой тахикардии ("тахикардия с широкими комплексами")
Нарастание желудочковой экстрасистолии, особенно если она превышает 30% от синусовых комплексов
7
Частота сердечных сокращений (ЧСС)
> 50; < 130 в мин
неинвазивный аппаратный или клинический мониторинг
< 60 или > 130 в течение 3 минут или нарастание частоты на 20%
8
Фармакологическая поддержка гемодинамики
Дофамин < 10 мкг/кг/мин
Норадреналин < 0,1 мкг/кг/мин
Повышение в течение 3 минут после начала маневра расхода препаратов для адекватного гемодинамического обеспечения
9
Сатурация (SpO2)
> 90%
пульсоксиметрия
Снижение < 90% в течение 3 минут десатурация на 4% 5% и более от начального уровня
10
Уровень сознания или седации
шкала седации RASS = [-5; 2]
Состояние пациента, не требующее назначения дополнительно седации и (или) нейролепсии ("спокойный пациент").
клинический мониторинг или BIS (ЭЭГ) - мониторинг (Электроэнцефалография с видеомониторингом)
RASS < -3 или > 2
Снижение уровня сознания на 1 и более 2 баллов
Повышение потребности в седации (в том числе и для синхронизации с аппаратом ИВЛ)
Судорожная активность
Психомоторное возбуждение
11
Болевой статус
0 по шкале болевого поведения BPS или 0 по шкале ВАШ
клинический мониторинг
появление или усиление боли
12
Частота дыхания (ЧДД)
> 10; < 40
> 5; < 40
неинвазивный аппаратный или клинический мониторинг
Бради- или тахипноэ
одышка и свистящее дыхание
13
Аксиллярная температура
> 36,0; < 38,5 oC
термометрия
< 36.0 или > 38.5
14
Индекс одышки Борг
<11 - 13>
клинический мониторинг
Индекс одышки Борга > 13
15
Статус вегетативной нервной системы
отсутствие клинических признаков дисфункции
клинический контроль
Пароксизм острой дисавтономии:
появление потоотделения;
тахикардии;
гипертермии;
повышение мышечного тонуса, побледнение, слабость
Дополнительные модальности для пациентов на ИВЛ
1
Синхронность с ИВЛ
Синхронность
клиническое наблюдение
Десинхронизация
2
Содержание кислорода во вдыхаемом воздухе (FiO2)
< 60%
газоанализатор аппарата ИВЛ
повышение потребности в кислороде
Респираторный индекс PaO2/FiO2
< 300 - острое повреждение легких; < 200 - острый респираторный дистресс синдром
Норма 500
(PaO2: FiO2 = 100 мм рт. ст./0,21 = 476)
газоанализатор
Любое снижение респираторного индекса
4
Показатель парциального напряжения углекислого газа в артериальной крови (PaCO2)
< 60 мм рт. ст.
газоанализатор
нарастание гиперкапнии
З
Положительное давление конца выдоха РЕЕР
< 10 см H2 O
монитор аппарата ИВЛ
Повышение уровня РЕЕР
Приложение В
ИНФОРМАЦИЯ ДЛЯ ПАЦИЕНТА
Информация для пациента, родственников пациента, ухаживающих лиц
Инсульт - острое заболевание головного мозга, вызванное разрывом или закупоркой сосуда, кровоснабжающего его. Признаками инсульта считаются внезапное возникновение слабости мышц лица или конечностей, особенно на одной половине тела, нарушение чувствительности чаще также на одной половине, затруднение произношения или понимания речи. В тяжелых случаях бывает потеря сознания.
Распознать заболевание возможно на месте, немедленно. Для этого используется тест "УЗП". Для этого попросите пострадавшего:
"У" - улыбнуться. Улыбка может быть кривая, уголок губ с одной стороны может быть направлен вниз, а не вверх, лицо может быть перекошено.
"З" - заговорить. Речь может быть невнятная, или отсутствует понимание задания.
"П" - поднять обе руки. Руки поднимаются не одинаково или одна не поднимается совсем.
Очень важно отметить, что все перечисленные симптомы возникают ВНЕЗАПНО (ОСТРО)! Если пострадавший затрудняется выполнить какое-то из этих заданий, необходимо немедленно вызвать скорую помощь, описать симптомы и указать время начала заболевания прибывшим на место медикам. До приезда "скорой" пациента необходимо уложить удобно, голова и плечи должны лежать на возвышение, чтобы не было сгибания, расстегнуть стесняющую одежду, дать достаточный приток свежего воздуха. Ничего не давать в рот, лечение пациента с инсультом осуществляется только в больнице в специализированном отделении.
После проведенного курса лечения в стационаре при выписке пациенту рекомендуют продолжить лечение, которое включает прием препаратов, для предотвращения повторного инсульта. Пациент должен неукоснительно выполнять все рекомендации врача, который будет наблюдать его в течение необходимого времени. При появлении каких-либо новых симптомов следует незамедлительно обратиться за медицинской помощью.
Пациент, перенесший геморрагический инсульт, нуждается в наблюдении врача-невролога по месту жительства, контроле артериального давления (необходимо заполнять дневник артериального давления), повышении физической активности, контроле веса тела, правильном питании, отказе от курения.
Дневник контроля артериального давления и частоты сердечных сокращений у пациента с геморрагическим инсультом
Дата
Утро
Вечер
Артериальное давление
Частота сердечных сокращений
Артериальное давление
Частота сердечных сокращений
Приложение Г1 - ГN
ШКАЛЫ ОЦЕНКИ, ВОПРОСНИКИ И ДРУГИЕ ОЦЕНОЧНЫЕ ИНСТРУМЕНТЫ
СОСТОЯНИЯ ПАЦИЕНТА, ПРИВЕДЕННЫЕ В КЛИНИЧЕСКИХ РЕКОМЕНДАЦИЯХ
Приложение Г1
КЛАССИФИКАЦИЯ HUNT-HESS
Название на русском языке: Классификация Hunt-Hess
Оригинальное название: Classification of patients with intracranial aneurysms according to surgical risk
Источник: [18]
Тип: шкала оценки
Назначение: оценка хирургического риска в зависимости от времени вмешательства при пластике внутричерепных аневризм
Содержание (шаблон) и ключ (интерпретация):
Стадия
Описание
I
Бессимптомное течение или легкая головная боль,
небольшая ригидность затылочных мышц, парез ЧМН
II
Парез ЧМН (III пары) или головная боль от умеренной до сильной, ригидность затылочных мышц, парез ЧМН
III
Сонливость, спутанность сознания или легкая очаговая симптоматика
IV
Ступор, гемипарез от умеренного до сильного, начальные признаки децеребрации и вегетативных нарушений
V
Глубокая кома, децеребральная ригидность, агональное состояние
--------------------------------
<*> Серьезные системные заболевания и/или ангиоспазм, переводят пациента в нижележащую стадию.
Приложение Г2
СТЕПЕНЬ ВЫРАЖЕННОСТИ КРОВОИЗЛИЯНИЯ ПО ДАННЫМ КТ
НА ОСНОВАНИИ ОРИГИНАЛЬНОЙ И МОДИФИЦИРОВАННОЙ ШКАЛЫ FISHER
Название на русском языке: шкала Fisher (оригинальная и модифицированная)
Оригинальное название: Fisher scale, modified Fisher scale
Источник: [11,12]
Тип: шкала оценки
Назначение: оценка степени выраженности кровоизлияния по данным КТ
Содержание (шаблон) и ключ (интерпретация):
Градация
Оригинальная шкала Fisher
Модифицированная шкала Fisher
0
-
Нет САК и ВЖК
1
Нет САК и ВЖК
САК, тонкий слой, нет ВЖК
2
САК, тонкий слой < 1 мм
САК, тонкий слой < 1 мм, есть ВЖК
3
САК, толстый слой > 1 мм
САК, толстый слой > 1 мм, нет ВЖК
4
ВМГ или ВЖК
САК, толстый слой > 1 мм, есть ВЖК
Приложение Г3
СТЕПЕНЬ ВЫРАЖЕННОСТИ ВНУТРИЖЕЛУДОЧКОВЫХ
КРОВОИЗЛИЯНИЙ ПО GRAЕB D.A
Название на русском языке: Степень выраженности внутрижелудочковых кровоизлияний по Graеb D.A.
Оригинальное название: нет
Источник): [13]
Тип: шкала оценки
Назначение: оценка степени выраженности внутрижелудочковых кровоизлияний
Содержание (шаблон) и ключ (интерпретация):
Локализация
Количество баллов
Боковые желудочки (каждый желудочек считается отдельно)
0 - нет крови
1 - следы крови или незначительное кровоизлияние
2 - менее половины желудочка заполнено кровью
3 - более половины желудочка заполнено кровью
4 - желудочек заполнен и растянут кровью
Третий и четвертый желудочки
0 - нет крови
1 - наличие крови, желудочек не увеличен
2 - желудочек заполнен и растянут кровью
Количество баллов
0 - 12
Приложение Г4
ШКАЛА КОМЫ ГЛАЗГО
Название на русском языке: шкала комы Глазго
Оригинальное название: Glasgow Coma Scale
Источник: [442]
Тип: шкала оценки
Назначение: оценка хирургического риска в зависимости от времени вмешательства при пластике внутричерепных аневризм
Содержание (шаблон):
Баллы
Открывание глаз
Речевая реакция
Двигательная реакция
1
Нет
Никаких звуков
Не двигается
2
Открывает на болевое раздражение
Издает звуки, но не слова
Патологическое разгибание в ответ на боль (децеребрационная ригидность)
3
Открывает в ответ на голос
Произносит отдельные слова
Патологическое сгибание в ответ на боль (декортикационная ригидность)
4
Открывает самопроизвольно, наблюдает
Произносит фразы, но речь спутанная
Бессмысленные движения в ответ на боль
5
-
Ориентирован, быстрый и правильный ответ на заданный вопрос
Локализует боль, пытается ее избежать
6
-
-
Выполнение движений по голосовой команде
Ключ (интерпретация):
Баллы
Степени нарушения сознания
15
Ясное сознание
13 - 14
Умеренное оглушение
10 - 12
Глубокое оглушение
8 - 9
Сопор
6 - 7
Кома умеренная
4 - 5
Кома глубокая
3
Кома запредельная
Приложение Г5
ОЦЕНКА ТЯЖЕСТИ СОСТОЯНИЯ ПАЦИЕНТОВ С САК ПО ШКАЛЕ WFNS
Название на русском языке: Оценка субарахноидального кровоизлияния (САК) Всемирной федерации неврологических хирургов (WFNS)
Оригинальное название: World Federation of Neurological Surgeons (WFNS) Subarachnoid Hemorrhage (SAH) Grading
Источник: [443]
Тип: шкала оценки
Назначение: Оценка тяжести состояния пациентов с субарахноидальным кровоизлиянием
Содержание (шаблон) и ключ (интерпретация):
0 степень САК по шкале WFNS: неразорвавшаяся аневризма.
I степень САК по шкале WFNS: оценка по шкале комы Глазго 15 баллов, грубый неврологический дефицит (афазия, гемипарез/гемиплегия) отсутствует.
II степень САК по шкале WFNS: оценка по шкале комы Глазго 13 - 14 баллов, грубый неврологический дефицит отсутствует.
III степень САК по шкале WFNS: оценка по шкале комы Глазго 13 - 14 баллов, грубый неврологический дефицит присутствует.
IV степень САК по шкале WFNS: оценка по шкале комы Глазго 7 - 12 баллов, грубый неврологический дефицит присутствует/отсутствует.
V степень САК по шкале WFNS: оценка по шкале комы Глазго 3 - 6 баллов, грубый неврологический дефицит присутствует/отсутствует.
Приложение Г6
ШКАЛА
HIJDRA ДЛЯ ОЦЕНКИ ИНТЕНСИВНОСТИ АНЕВРИЗМАТИЧЕСКОГО САК
Название на русском языке: Шкала Hijdra
Оригинальное название: Hunt-Hess classification
Источник: [18]
Тип: шкала оценки
Назначение: оценка интенсивности аневризматического субарахноидального кровоизлияния
Содержание (шаблон) и ключ (интерпретация):
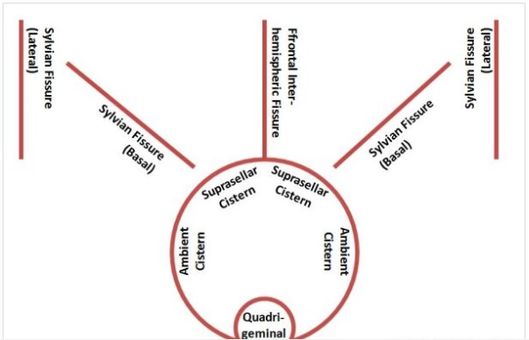
Оценка каждой из 10 базальных цистерн и щелей отдельно по шкале в соответствии с количеством крови:
нет крови = 0,
малое количество = 1,
умеренное количество = 2,
полностью заполнена кровью = 3.
<*> сгустки крови, которые превосходят истинные размеры цистерны или щели, оценивают как 3 балла
Расчет количества крови в субарахноидальном пространстве [сумма баллов]; вариабельность = 0 - 30.
Средний бал используют при неадекватной визуализируемой цистерне или щели.
Оценка крови в четырех желудочках мозга:
нет крови = 0,
седиментация в нижней части желудочка = 1,
частично заполнены = 2,
полностью заполнены = 3.
Расчет количества крови в желудочках мозга [сумма баллов]; вариабельность = 0 - 12
Приложение Г7
КЛАССИФИКАЦИЯ СТЕПЕНЕЙ ВЫКЛЮЧЕНИЯ АНЕВРИЗМ RAYMOND
Название на русском языке: Классификация Raymond
Оригинальное название: нет
Источник: [444]
Тип: другое (классификация)
Назначение: оценка степеней выключения аневризм
Содержание (шаблон):
ангиографическая схема, используемая для оценки степени окклюзии (закупорки) внутричерепных аневризм после эндоваскулярного лечения.
Ключ (интерпретация):
Raymond I - полная окклюзия аневризмы
Raymond II - заполнение пришеечной части аневризмы
Raymond III - остаточное заполнение аневризмы
Приложение Г8
ШКАЛА ПРОГНОЗОВ ИСХОДА ВНУТРИМОЗГОВОГО КРОВОИЗЛИЯНИЯ
Название на русском языке: Шкала прогнозов исхода внутримозгового кровоизлияния
Оригинальное название: The ICH score
Источник: [38]
Тип: шкала оценки
Назначение: оценка прогнозов исхода внутримозгового кровоизлияния
Содержание (шаблон):
Показатель
Баллы
Шкала комы Глазго, баллы
3 - 4
2
5 - 12
1
13 - 15
0
Объем ВМГ, см3
30 или более
1
Менее 30
0
Внутрижелудочковое кровоизлияние
есть
1
нет
0
Субтенториальная локализация ВМГ
да
1
нет
0
Возраст пациента, годы
80 и более
1
Менее 80
0
Общее количество баллов
0 - 6
Ключ (интерпретация): летальность зависит от количества баллов и составляет: при 0 баллов - 0, при 1 балле - 13%, при 2 баллах - 26%, при 3 баллах - 72%, при 4 баллах - 97%, при 5 - 6 баллах - 100%.
Приложение Г9
МОДИФИЦИРОВАННАЯ ШКАЛА РЭНКИНА
Название на русском языке: Модифицированная шкала Рэнкина
Оригинальное название: The Modified Rankin Scale (mRS)
Источник: [445]
Тип: шкала оценки
Назначение: степени ограничения жизнедеятельности пациентов после перенесенного инсульта (для оценки общей инвалидизации и примерной степени зависимости больного от помощи других лиц)
Содержание (шаблон) и ключ (интерпретация):
Балл
Описание состояния
0
Нет симптомов
1
Отсутствие значимых нарушений жизнедеятельности, несмотря на имеющиеся симптомы заболевания; пациент способен выполнять свои обычные повседневные обязанности
2
Легкое нарушение функций жизнедеятельности; пациент неспособен выполнять ряд своих прежних обязанностей, но может еще справляться со своими делами без посторонней помощи
3
Нарушение жизнедеятельности, умеренное по своей выраженности. Нуждается в некоторой помощи со стороны, но передвигается пешком (прогуливается) без посторонней помощи
4
Выраженное нарушение проявлений жизнедеятельности. Невозможность передвигаться самостоятельно (без помощи другого человека). Пациент не способен справляться со своими естественными потребностями без посторонней помощи
5
Грубое нарушение процессов жизнедеятельности. Пациент прикован к постели. Имеется недержание кала и мочи. Нуждается в постоянном внимании, помощи и уходе
6
Пациент умер
Ключ (интерпретация): 0 баллов соответствует отсутствию у пациента ограничений жизнедеятельности, в том числе незначительных; 1 балл соответствует отсутствию у пациента существенных нарушений, несмотря на наличие некоторых симптомов. Пациент может выполнять все свои обычные действия и обязанности; 2 балла соответствуют легкой степени инвалидности. Пациент не способен выполнять прежние действия, но может справляться с повседневными обязанностями без посторонней помощи; 3 балла соответствуют умеренной степени инвалидности. Пациент нуждается в некоторой посторонней помощи, но может самостоятельно ходить (в том числе с использованием приспособлений для ходьбы или ходунков); 4 балла соответствуют выраженной степени инвалидности. Пациент не способен ходить и обслуживать себя без посторонней помощи; 5 баллов соответствуют тяжелой степени инвалидности. Пациент прикован к постели, страдает недержанием мочи и кала. Требуется постоянный уход.
Пояснения: специалист, выполняющий оценку, не должен пытаться разделить инвалидизацию ввиду инсульта и инвалидизацию по другим причинам.
Приложение Г10
ШКАЛА SPETZLER-MARTIN (1986)
Название на русском языке: Шкала Spetzler-Martin
Оригинальное название: Spetzler-Martin Scale
Источник: [44]
Тип: другое (классификация)
Назначение: система классификации артериовенозных мальформаций
Содержание (шаблон) и ключ (интерпретация):
АВМ 1 - 2 балла имеют низкий риск хирургического лечения, 3 балла - промежуточный, 4 - 5 баллов - высокий.
Анатомическая форма АВМ
Количество баллов
Максимальный размер АВМ
менее 3 см
1
3 - 6 см
2
более 6 см
3
Наличие глубинного дренирования <*>
нет
0
да
1
Локализация АВМ в функционально значимой зоне <**>
нет
0
да
1
--------------------------------
Комментарий: <*> Дренаж АВМ считают глубинным, если отток крови хотя бы по одной из вен происходит в вену Галена, внутренние вены мозга, базальные вены Розенталя и прецентральные мозжечковые вены.
<**> Функционально значимые зоны: сенсомоторная, речевая, зрительная кора, гипоталамус, таламус, внутренняя капсула, ствол мозга, ножки и глубокие ядра мозжечка.
Приложение Г11
ШКАЛА SPETZLER-PONCE (2011)
Название на русском языке: Шкала Spetzler-Ponce
Оригинальное название: Spetzler-Ponce scale
Источник: [45]
Тип: шкала оценки
Назначение: разделение пациентов с артериовенозными мальформациями головного мозга на классы риска хирургического лечения
Содержание (шаблон):
Класс
Степень риска по шкале S - M
Рекомендованная тактика
A
I, II
удаление
B
III
мультимодальное лечение
C
IV, V
консервативное ведение <*>
--------------------------------
Комментарий:
<*> исключение составляют больные с повторными кровоизлияниями, прогрессирующим неврологическим дефицитом, АВМ с синдромом обкрадывания и гемодинамическими аневризмами
Приложение Г12
ШКАЛА SICH В УПРОЩЕННОМ ВИДЕ (2010)
Название на русском языке: Шкала SICH
Оригинальное название: Secondary Intracerebral Hemorrhage Score
Источник: [93]
Тип: шкала оценки
Назначение: выявление пациентов с внутримозговым кровоизлиянием с самым высоким риском наличия основной сосудистой этиологии
Содержание (шаблон):
Параметр
Количество баллов
Вероятность аномалии сосудов по данным нативной КТ <*>
высокая
2
средняя
1
низкая
0
Возраст пациента (годы)
18 - 45
2
46 - 70
1
71 и более
0
Пол
жен
1
муж
0
Артериальная гипертензия и нарушения коагуляции <**>
нет
1
есть
0
Ключ (интерпретация):
Рекомендации для клиник, выполняющих КТ-ангиографию не всем больным с нетравматическими внутримозговыми кровоизлияниями:
SICH 0 - КТА и ЦАГ не показаны;
SICH 1 - 2 - выполняют КТА и лишь при наличии сосудистой патологии или подозрении на нее проводят ЦАГ;
SICH 3 - 6 - выполняют ЦАГ без КТА.
Рекомендация для клиник, в которых всем больным с ВМГ выполняют КТ-ангиографию:
SICH 0 - 2 - ЦАГ проводят при наличии сосудистой патологии или подозрении на нее при КТА;
SICH 3 - 6 - всем больным проводят ЦАГ вне зависимости от наличия патологии при КТА.
--------------------------------
<*> К высокой вероятности наличия сосудистой аномалии по данным нативной КТ относят:
1) расширенные сосуды или кальцинаты вдоль краев ВМГ;
2) гиперденсивные очаги в венозных синусах или в корковых венах на пути предполагаемого венозного дренирования ВМГ;
К низкому риску наличия сосудистой аномалии по данным КТ без контрастирования относят:
1) отсутствие критериев высокого риска наличия сосудистой аномалии (см. выше);
2) расположение ВМГ в подкорковых ядрах, таламусе или стволе мозга.
О среднем риске наличия сосудистой аномалии по данным КТ без контрастирования говорят при отсутствии критериев высокой и низкой вероятности наличия сосудистой аномалии (при лобарных и мозжечковых ВМГ).
<**> Критерии нарушения коагуляции по шкале SICH:
1) ежедневный прием ацетилсалициловой кислоты** или клопидогрела**;
2) тромбоцитопения менее 50 000 в 1 мкл;
3) МНО более 3,0;
4) активированное частичное тромбопластиновое время более 80 секунд.
Приложение Г13
ШКАЛА LAWTON-YOUNG (2010)
Название на русском языке: Шкала Lawton-Young
Оригинальное название: Grading Scale for Selecting Patients with Brain Arteriovenous Malformations for Surgery
Источник: [47]
Тип: шкала оценки
Назначение: отбор пациентов с артериовенозными мальформациями головного мозга для хирургического вмешательства
Содержание (шаблон):
Факторы риска хирургии АВМ
Количество баллов
Возраст пациента
менее 20 лет
1
20 - 40 лет
2
более 40 лет
3
Кровоизлияние в анамнезе
нет
1
да
0
Размытость АВМ
нет
0
да
1
Ключ (интерпретация): при комбинации с классификацией Spetzler-Martin АВМ 2 - 6 баллов имеют низкий риск хирургического лечения, 7 - 10 баллов - высокий.
Комбинация шкал Spetzler-Martin и Lawton-Young
Шкала S-M
Баллы
Дополнительные признаки
По размеру:
Возраст:
менее 3 см
1
менее 20 лет
3 - 6 см
2
20 - 40
более 6 см
3
более 40 лет
По локализации:
Кровоизлияние в анамнезе
вне функционально-значимой зоны <*>
0
Нет
в пределах функционально-значимой зоны
1
Да
По дренированию крови:
Размытость АВМ:
Нет глубоких дренажных вен <**>
0
Да
Есть
1
Нет
--------------------------------
Комментарий: <*> Дренаж АВМ считают глубинным, если отток крови хотя бы по одной из вен происходит в вену Галена, внутренние вены мозга, базальные вены Розенталя и прецентральные мозжечковые вены.
<**> Функционально значимые зоны: сенсомоторная, речевая, зрительная кора, гипоталамус, таламус, внутренняя капсула, ствол мозга, ножки и глубокие ядра мозжечка.
Приложение Г14
КЛАССИФИКАЦИЯ VIRGINIA RADIOSURGERY AVM SCALE (VRAS, 2013)
Название на русском языке: Классификация VRAS
Оригинальное название: Virginia radiosurgery AVM scale
Источник: [51]
Тип: шкала оценки
Назначение: прогнозирование исхода после радиохирургического лечения артериовенозных мальформаций
Содержание (шаблон):
Анатомическая форма АВМ
Количество баллов
Объем АВМ в мл
менее 2
0
2 - 4
1
более 4
2
Локализация АВМ в функционально значимой зоне
нет
0
да
1
Кровоизлияние в анамнезе
нет
0
да
1
Ключ (интерпретация): При радиохирургии АВМ, оцененных в 0 баллов, отличный исход (полная облитерация АВМ без нарастания неврологических нарушений) прогнозируют в 83%, 1 балл - в 79%, 2 балла - в 70%, 3 балла - в 48%, 4 балла - в 39%.
Приложение Г15
ШКАЛА RBAS (RADIOSURGERY-BASED AVM SCORE),
МОДИФИЦИРОВАННЫЙ ВАРИАНТ (2008)
Название на русском языке: Шкала RBAS, модифицированный вариант (2008)
Оригинальное название: Radiosurgery-based AVM score
Источник: [446]
Тип: индекс
Назначение: прогнозирование исходов радиохирургического лечения пациентов с АВМ
Содержание (шаблон):
Оценка АВМ = (0,1) x (объем АВМ в мл) + (0,02) x (возраст пациента в годах) + (0,5) x (расположение мальформации*).
Комментарии:
<*> Локализация АВМ:
0 баллов - лобная и височная доли
1 балл - теменная, затылочная доли, внутрижелудочковое расположение, мозолистое тело и мозжечок
2 балла - базальные ядра, таламус, ствол мозга.
Ключ (интерпретация): при градации АВМ в 1 балл и менее отличный исход (полная облитерация АВМ без нарастания неврологических нарушений) прогнозируют в 95%, 1,25 балла - в 80%, 1,5 балла - в 70%, 1,75 балла - в 60%, 2 балла - в 50%, более 2 баллов - менее, чем в 40%.
Приложение Г16
ШКАЛА ДЛЯ ОЦЕНКИ ТЯЖЕСТИ ПИТ-СИНДРОМА
Название на русском языке: Шкала для оценки тяжести ПИТ-синдрома
Оригинальное название: -
Источник: [447]
Тип: шкала оценки
Назначение: оценка тяжести ПИТ-синдрома
Содержание (шаблон):
N
Признак
Баллы
1.
Пролежни
0,5
2.
Инфекции дыхательных путей/трахеостома
0,5
3.
Уроинфекция/мочевой катетер, эпицистостома
0,5
4.
Боль/пароксизмальная симпатическая гиперактивность
1,0
5.
Диссомния, приобретенная в ОРИТ
0,5
6.
Нутритивная недостаточность
0,5
7.
Дефицит массы тела
0,5
8.
Снижение гравитационного градиента/ортостатическая недостаточность
1,0
9.
Слабость, приобретенная в ОРИТ
0,5
10.
Полимионейропатия критических состояний
1,0
11.
Респираторная нейропатия/продленная ИВЛ
0,5
12.
Дисфагия, приобретенная в ОРИТ/назогастральный зонд, гастростома
1,0
13.
Нарушение памяти, ориентированности
0,5
14.
Делирий/возбуждение
1,0
15.
Сниженный фон настроения
0,5
ИТОГО
10,0
Примечание: градация по степени тяжести ПИТС определяется как:
1 - 3 балла - легкая степень
4 - 6 баллов - средняя степень
6 - 10 баллов - тяжелая степень
Приложение Г17
ШКАЛА ИНСУЛЬТА НАЦИОНАЛЬНОГО ИНСТИТУТА ЗДОРОВЬЯ
(NATIONAL INSTITUTES OF HEALTH STROKE SCALE) ДЛЯ ОЦЕНКИ
ТЯЖЕСТИ НЕВРОЛОГИЧЕСКОГО ДЕФИЦИТА У ПАЦИЕНТОВ С ИНСУЛЬТОМ
Название на русском языке: Шкала инсульта Национального института здоровья
Оригинальное название: National Institutes of Health Stroke Scale (NIHSS)
Источник: [448]
Тип: шкала оценки
Назначение: для оценки тяжести неврологического дефицита у пациентов с инсультом
Содержание:
1а. Уровень сознания. Исследователь должен выставить соответствующий балл, даже если оценка затруднена вследствие наличия интубационной трубки, языкового барьера, оротрахеальной травмы, повязки. Три балла выставляется только в том случае, если в ответ на болевой стимул у пациента не возникает двигательных реакций (исключение - защитные знаки). Задайте пациенту два или три общих вопроса касательно обстоятельств его поступления в стационар. Основываясь на полученных ответах, оцените результаты. Помните, что не следует помогать пациенту.
0 = ясное сознание, пациент реагирует на осмотр незамедлительно.
1 = оглушение, при легкой стимуляции пациент реагирует на осмотр.
2 = сопор, требуются повторные стимуляции пациента для ответной реакции, или при отсутствии эффекта необходимо проводить более интенсивную стимуляцию с целью получения нестереотипного двигательного ответа.
3 = кома, ответная реакция только в виде рефлекторных двигательных актов либо самопроизвольные двигательные акты, либо полное отсутствие реакции со стороны пациента, атония, арефлексия.
1b. Уровень сознания. Вопросы. Спросить у пациента: "Какой сейчас месяц? Сколько Вам лет?" Близкие, но неверные ответы не засчитываются. Пациенты с афазией и/или снижением уровня бодрствования, которые не могут правильно ответить на два поставленных вопроса, получат 2 балла. Пациенты, которые не могут говорить вследствие эндотрахеальной интубации, оротрахеальной травмы, тяжелой дизартрии, ввиду языкового барьера, либо по другим причинам (кроме афазии) получат 1 балл. Засчитывается только первая попытка, не допускается вербальная и невербальная помощь со стороны врача.
0 = правильный ответ на два вопроса.
1 = правильный ответ на один вопрос.
2 = ни на один вопрос не дан правильный ответ.
1с. Уровень сознания. Выполнение команд. Необходимо попросить пациента закрыть и открыть глаза, сжать кисть непаретичной руки в кулак, а затем разжать. Если для оценки данного пункта не может быть использована рука пациента, то можно заменить данную команду другой. Если пациент не может понять команды, то задание может быть продемонстрировано ему. Пациенты с травмой, ампутацией или другим физическим дефектом должны быть оценены при помощи одной шаговой команды. Засчитывается только первая попытка. Вопросы задаются также только один раз.
0 = обе команды выполнены правильно.
1 = одна команда выполнена верно.
2 = ни одна команда не выполнена правильно.
1. Движения глазных яблок. Учитываются только горизонтальные движения глазных яблок. Оцениваются самостоятельные или рефлекторные (окулоцефалический рефлекс) движения глазных яблок. Проведение калорического теста не допускается. Если у пациента имеется содружественное отведение глазных яблок, которое пациент может самостоятельно преодолеть, либо при помощи вызывания окулоцефалического рефлекса, выставляется 1 балл. В случае наличия у пациента изолированного пареза мышц глазного яблока, иннервируемых III, IV или VI парами черепных нервов, выставляется 1 балл. Движения глазных яблок должны исследоваться у всех пациентов, в том числе и у пациентов с афазией. Пациенты с травмой глазного яблока, повязкой, предшествующей слепотой или другими расстройствами остроты или полей зрения должны быть обследованы при помощи вызывания окулоцефалического рефлекса. С целью выявления частичного пареза взора рекомендуется установить зрительный контакт со стороны пациента и походить из стороны в сторону относительно пациента.
0 = норма.
1 = частичный парез взора, преодолеваемый пациентом либо при помощи вызывания окулоцефалического рефлекса.
2 = тоническое отведения глазных яблок, не преодолеваемое вызыванием окулоцефалического рефлекса.
2. Поля зрения. Поля зрения (верхние и нижние квадранты) исследуются отдельно. При необходимости может использоваться счет пальцев или внезапное появление в поле зрения пациента зрительного стимула (палец исследователя). Во время проведения тестирования пациент должен смотреть в лицо исследователю, однако, если он следит за движением пальцев, это может оцениваться как нормальная положительная реакция. При наличии односторонней слепоты или энуклеации, поля зрения оцениваются в здоровом глазу. При наличии четко очерченного выпадения поля зрения в виде верхнее- или нижнеквадрантной гемианопсии выставляется 1 балл. В случае слепоты пациента по каким-либо другим причинам выставляется 3 балла. Также должна быть выполнена синхронная двусторонняя стимуляция. Если в результате выявляются различия (уменьшение поля зрения в сторону больного глаза), выставляется 1 балл, и результаты теста используются для ответа на вопрос N 11. Два балла соответствуют случаям полной гемианопсии, а наличие какого-либо частичного нарушения поля зрения, включая квадрантную гемианопсию, соответствует 1 баллу.
0 = норма.
1 = частичная гемианопсия.
2 = полная гемианопсия.
3 = билатеральная гемианопсия (слепота, включая корковую).
3. Парез лицевой мускулатуры. Используя вербальные и невербальные приемы, попросите пациента показать зубы, поднять брови, закрыть глаза, зажмурить глаза. Допускается демонстрация данных команд врачом. Оцените симметричность болевой гримасы в ответ на болевой стимул у пациентов, которые не могут вас понять. В случае наличия повязки на лице, оротрахеальной интубации или других барьеров они должны быть удалены (насколько это возможно) на время оценки.
0 = норма.
1 = минимальный парез, асимметрия лица в виде сглаженности носогубной складки, асимметрия при улыбке.
2 = частичный паралич (частичный или полный паралич нижней мимической мускулатуры).
3 = полный паралич нижней и верхней мимической мускулатуры с одной или двух сторон (полное отсутствие движений в верхней и нижней мимической мускулатуре).
5a. Движения в верхних конечностях (левая рука). Конечности пациента необходимо установить в следующем положении: вытянуть руки (ладонями вниз) под углом 90° (если пациент сидит) или 45° (если пациент лежит на спине). Каждая конечность оценивается поочередно, начиная с непаретичной руки. Допускается демонстрация выполнения приема врачом у пациентов с афазией. Не допускается нанесение болевых стимулов. В случае ампутации конечности или поражения плечевого сустава, исследователь должен выставить в соответствующей графе UN (untestable). Четко считайте вслух до десяти и демонстрируйте счет на пальцах так, чтобы пациент это видел. Начинайте считать, как только отпустите конечность пациента.
0 = конечность удерживается под углом 90° или 45° в течение 10 секунд без малейшего опускания.
1 = конечность опускается в течение 10 секунд, но не касается постели или другой опоры.
2 = конечности не могут сохранять поднятое положение (опускаются на постель или другую опору в течение 10 секунд), но производят некоторое сопротивление силе тяжести.
3 = конечности падают без сопротивления силе тяжести, имеются минимальные движения.
4 = нет активных движений в конечности.
ЦЫ = ампутация конечности или повреждение плечевого сустава.
5b. Движения в верхних конечностях (правая рука).
6a. Движения в нижних конечностях (левая нога). Конечности устанавливаются в соответствующее положение: под углом 30° в положении лежа на спине. Допускается демонстрация выполнения приема врачом у пациентов с афазией. Нанесение болевых стимулов не допускается. Каждая конечность оценивается поочередно, начиная с непаретичной ноги. Только в случае ампутации конечности или повреждения тазобедренного сустава, исследователь должен выставить в соответствующей графе UN (untestable). Четко считайте вслух до пяти и демонстрируйте счет на пальцах так, чтобы пациент это видел. Начинайте считать, как только отпустите конечность пациента.
0 = конечность удерживается в течение 5 секунд под углом 30° без малейшего опускания.
1 = конечность опускается в течение 5 секунд, но не касается постели или другой опоры.
2 = конечности не могут сохранять поднятое положение (опускаются на постель или другую опору в течение 5 секунд), но производят некоторое сопротивление силе тяжести.
3 = конечности падают без сопротивления силе тяжести, но присутствуют минимальные движения.
4 = нет активных движений в конечности.
ЦЫ = ампутация конечности или повреждение тазобедренного сустава.
6b. Движения в нижних конечностях (правая нога).
4. Атаксия конечностей. Оцениваются односторонние мозжечковые симптомы. Тест проводится с открытыми глазами. В случае наличия какого-либо дефекта зрения проведите тестирование в ненарушенном поле зрения. Атаксия будет отсутствовать у пациента, который не понимает, что от него требуется или парализован. В случае повреждения суставов или ампутации конечности выставляется UN (untastable). Попросите пациента выполнить пальце-носовую, пальце-пальцевую и пяточно-коленную пробы обеими конечностями. В случае слепоты необходимо исключить пальце-пальцевую пробу. Пациент с афазией часто будет способен выполнить тест нормально, если перед этим исследователь подвигает конечностью.
0 = симптомы атаксии отсутствуют.
1 = симптомы атаксии присутствуют в одной конечности.
2 = симптомы атаксии присутствуют в двух конечностях.
5. Чувствительные нарушения. Учитывается только снижение чувствительности, обусловленное настоящим заболеванием. Исследователь должен подвергнуть тестированию как можно больше участков тела пациента (лицо; руки, кроме кистей; ноги, кроме стоп; туловище). У пациентов в сопоре и/или с афазией выставляется 1 балл, у пациентов с инсультом в стволе мозга и билатеральным нарушением чувствительности - 2 балла. Если пациент не реагирует на внешние раздражители и имеется тетраплегия, то выставляются 2 балла, так же, как и при нарушении уровня сознания до комы.
0 = нет чувствительных нарушений.
1 = умеренное снижение чувствительности; с пораженной стороны пациент ощущает несильный укол булавкой или тупую боль от укола.
2 = сильная или полная потеря чувствительности; пациент не ощущает прикосновения в области лица, рук и ног.
6. Афазия. Пациента просят описать прилагаемую картинку, перечислить изображенные на листе бумаги предметы и прочесть предложения из прилагаемого списка. В случае слепоты пациента, он должен назвать предметы, взяв их в руку, повторить что-либо за исследователем или сказать что-либо самостоятельно. Интубированного пациента следует просить отвечать письменно. Три балла следует выставлять только в том случае, если пациент не реагирует ни на одну команду и не отвечает на вопросы. Легкая форма афазии оценивается в 1 балл. Для правильного выбора между 1 и 2 баллами используйте предлагаемые материалы; предполагается, что пациент, пропустивший более 2/3 предлагаемых для этого предметов или выполнивший небольшое количество простых команд, получит 2 балла. В случае коматозного состояния выставляется 3 балла.
0 = нет афазии.
1 = легкая или умеренная афазия.
2 = тяжелая афазия.
3 = тотальная афазия.
7. Дизартрия. Если состояние пациента оценивается как нормальное, он должен быть способен адекватно разговаривать, отвечая на просьбу исследователя прочесть что-либо или повторить слова из прилагаемого списка. В случае наблюдения у пациента признаков тяжелой афазии, четкость артикуляции оценивается в процессе спонтанной речи. Только если пациент интубирован или существует какое-либо другое физическое препятствие речи, состояние пациента оценивается 9 баллами, и исследователь должен предоставить четкое письменное объяснение причины невозможности оценить состояние пациента. Не сообщайте пациенту причину проведения его/ее тестирования.
Для тестирования всех пациентов пользуйтесь предлагаемым списком слов и не сообщайте им, что вы проводите тест проверки ясности речи. Как правило, при неотчетливом произношении одного или нескольких слов такое состояние оценивается как нормальное. Ноль баллов выставляется пациентам, которые читают все слова внятно. Пациенты, страдающие афазией или те, кто не читает, оцениваются на основании качества их спонтанной речи или повторения произносимых исследователем вслух слов. Два балла ставят в тех случаях, когда пациента совершенно невозможно понять или пациентам, которые молчат.
0 = норма.
1 = дизартрия от слабой до умеренной; пациент нечетко произносит как минимум несколько слов; в худшем случае, произносимые им слова можно понять с трудом.
2 = сильная дизартрия; речь пациента настолько невнятна, что не воспринимается вовсе при отсутствии или непропорционально имеющейся афазии; или пациент молчит (не способен изъясняться членораздельно).
UN = пациент интубирован или присутствует какая-либо другая физическая преграда, препятствующая способности говорить.
8. Угнетение восприятия или невнимание (ранее использовали термин "игнорирование"). Для выявления игнорирования (невнимания) достаточно информации, полученной в ходе выполнения предыдущих тестов. Если в силу тяжелого нарушения зрения у пациента одновременная двусторонняя визуальная стимуляция проведена быть не может, но реакция на кожные стимулы нормальная, то его состояние оценивается как нормальное. Если у пациента афазия, но по всем признакам он внимательно следит за голосом с двух сторон, то его состояние оценивается как нормальное. Наличие зрительного пространственного игнорирования, или анозогнозия, расценивается как патология. Поскольку патология оценивается в баллах только в случае ее наличия, данный пункт тестируется всегда.
Можно предположить, что при оценке этого пункта возможна значительная вариация мнений исследователей, так как все неврологи используют несколько различающиеся методы для тестирования игнорирования. Поэтому в целях повышения достоверности исследования проводите только двустороннюю одновременную стимуляцию на визуальные и тактильные стимулы. При одностороннем игнорировании стимулов обеих модальностей оценивайте невнимание как 2, а при одностороннем игнорировании стимула одной модальности - как 1. Если пациент в сознании, но демонстрирует какой-либо другой ярко-выраженный тип игнорирования, оценивайте уровень невнимания как 1.
0 = отсутствие отклонений.
1 = угнетение реакции (игнорирование, невнимание) при одновременной двусторонней стимуляции на стимулы одной из перечисленных модальностей (зрительные, тактильные, слуховые, пространственные).
2 = выраженное одностороннее игнорирование или игнорирование стимулов более чем одной модальности; пациент не узнает (не различает) собственную руку или другие ориентиры только с одной стороны.
Ключ (интерпретация): максимальное количество баллов - 42. Отсутствие неврологического дефицита соответствует 0 баллов.
Пояснения: пункты шкалы оцениваются по порядку. Недопустимо инструктировать пациента, даже если это противоречит обычной клинической практике. Фиксируется первая реакция пациента. Оценивается только настоящая реакция пациента, а не его (по-вашему) возможные действия. Необходимо отмечать все имеющиеся у больного симптомы, включая те из них, которые могли возникнуть вследствие ранее перенесенных инсультов.
Для изучения речевой продукции пациента просят описать события на картинке, назвать предметы, прочесть предложения и слова, представленные оценивающим врачом.
Приложение Г18
КАНАДСКАЯ НЕВРОЛОГИЧЕСКАЯ ШКАЛА
Название на русском языке: Канадская неврологическая шкала
Оригинальное название: Сanadian neurological scale (СNS)
Источник: [64]
Тип: шкала оценки
Назначение: для оценки тяжести неврологического дефицита у пациентов с инсультом
Содержание:
Когнитивные функции
Оценка
Уровень сознания
Ясное
3,0
Оглушение
1,5
Ориентация
Ориентирован
1,0
Дезориентирован/неадекватен
0,0
Речь
Нормальная
1,0
Дефицит экспрессии
0,5
Дефицит восприятия
0,0
ИТОГ: _________
Раздел А1
Двигательные функции
Слабость
Оценка
Нет дефицита понимания
Лицевая мускулатура
Нет
0,5
Есть
0,0
Рука: проксимальные отделы
Нет
1,5
Легкая
1,0
Значительная
0,5
Тотальная
0
Рука: дистальные отделы
Нет
1,5
Легкая
1,0
Значительная
0,5
Тотальная
0
Нога: проксимальные отделы
Нет
1,5
Легкая
1,0
Значительная
0,5
Тотальная
0
Нога: дистальные отделы
Нет
1,5
Легкая
1,0
Значительная
0,5
Тотальная
0
Итог:_________
Раздел А2
Двигательные функции
Слабость
Оценка
Дефицит понимания
Лицевая мускулатура
Симметричная
0,5
Асимметричная
0,0
Руки
Равная
1,5
Неравная
0,0
Ноги
Равная
1,5
Неравная
0,0
Итог: _________
Приложение Г19
КЛАССИФИКАЦИЯ RAYMOND ROY
Название на русском языке: Классификация Raymond Roy
Оригинальное название: Raymond-Roy Occlusion Classification
Источник: [221, 449]
Тип: шкала оценки
Назначение: для оценки степени окклюзии аневризмы
Содержание:
3 степени окклюзии аневризмы:
I степень - полная облитерация, II степень - остаточная шейка,
III степень - аневризма заполняется контрастом между витками спирали или контраст свободно заполняет часть купола аневризмы вдоль стенки.
Пояснения:
I степень считается хорошим результатом,
II - удовлетворительным,
III - неудовлетворительным.
Приложение Г20
СКРИНИНГОВОЕ ТЕСТИРОВАНИЕ ГЛОТАНИЯ
Название на русском языке: Скрининговое тестирование глотания
Оригинальное название: -
Источник: -
Тип: -
Назначение: для оценки функции глотания
Содержание:
"__" ___________ 20__ г. Время ФИО пациента ____________ ИБ N _____________
ОЦЕНКА ФУНКЦИИ ГЛОТАНИЯ
Симптомы настораживающие в отношении дисфагии
1
Затруднение зевания
2
Нарушение гигиены рта
3
Слюнотечение и неспособность глотать слюну
4
Неаккуратное пищевое поведение, выпадение пищи во время еды изо рта
5
Смазанная речь
6
Кашель или постоянная прочистка горла до, во время или после еды
7
Изменение качества голоса во время или после глотания ("булькающий" голос, хрипота, временная потеря голоса
8
Срыгивание
9
Затрудненное дыхание, удушье
10
Повышение температуры тела
11
Снижение веса
12
Потеря интереса к еде, плохой аппетит или отказ от пищи
13
Увеличение продолжительности сна после еды
14
Ощущение, что еда или жидкость застревает в горле во время еды
15
Тревожность по поводу приема пищи у больного
ПОДГОТОВКА К ОЦЕНКЕ ГЛОТАНИЯ
1. Пациент активно бодрствует и активно реагирует на обращение к нему
Пациент находится в положении сидя (при необходимости посадить)
Пациент может самостоятельно контролировать положение головы
2. Пациент может покашлять
Пациент может контролировать слюну (проглатывать во время, нет слюнотечения изо рта)
Пациент может свободно дышать
3. Голос не влажный и не хриплый
ОЦЕНКА ГЛОТАНИЯ
1 чанная ложка воды
SO2
До
Через 30 сек
![]()
Нет попыток проглотить
![]()
Вода выливается изо рта
![]()
Кашель или прочистка горла
![]()
Влажный или хриплый голос
![]()
Одышка, затруднение дыхания, удушье
![]()
Срыгивание
2 чанная ложка воды
SO2
До
Через 30 сек
![]()
Нет попыток проглотить
![]()
Вода выливается изо рта
![]()
Кашель или прочистка горла
![]()
Влажный или хриплый голос
![]()
Одышка, затруднение дыхания, удушье
![]()
Срыгивание
3 чанная ложка воды
S02
SO2
До
Через 30 сек
![]()
Нет попыток проглотить
![]()
Вода выливается изо рта
![]()
Кашель или прочистка горла
![]()
Влажный или хриплый голос
![]()
Одышка, затруднение дыхания, удушье
![]()
Срыгивание
1/2 стакана воды
SO2
До
Через 30 сек
![]()
Нет попыток проглотить
![]()
Вода выливается изо рта
![]()
Кашель или прочистка горла
![]()
Влажный или хриплый голос
![]()
Одышка, затруднение дыхания, удушье
![]()
Срыгивание
Приложение Г21
ШКАЛА РЕАБИЛИТАЦИОННОЙ МАРШРУТИЗАЦИИ
Название на русском языке: Шкала реабилитационной маршрутизации (ШРМ)
Оригинальное название: - Шкала реабилитационной маршрутизации 2025 [329]
Источник: Союз реабилитологов России
Тип: шкала оценки
Назначение: для оценки нарушений жизнедеятельности и определения реабилитационного потенциала
Градации оценки
Описание статуса
При заболеваниях или состояниях центральной нервной системы
При заболеваниях или состояниях опорно-двигательного аппарата и периферической нервной системы
При соматических заболеваниях
0
Отсутствие нарушений жизнедеятельности
Ключевой признак: Преморбидный уровень активности и социальной жизни (работа, обучение)
Нет жалоб и признаков нарушения жизнедеятельности
1
Отсутствие значимых нарушений жизнедеятельности, несмотря на имеющиеся симптомы заболевания;
Ключевой признак: преморбидный уровень (работа, обучение), активности и социальной жизни, несмотря на имеющиеся симптомы заболевания
1) способен вернуться к прежнему образу жизни (работа, обучение, другое);
2) тратит столько же времени на выполнение дел, как и до болезни.
2
Легкое нарушение функций жизнедеятельности
Ключевой признак: проживание в домашних условиях в одиночку более 1 недели без посторонней помощи и наблюдения
Комбинация уточняющих признаков 1:
1) способен передвигаться самостоятельно за пределами дома, ходить в магазин, совершать небольшие путешествия и переезды;
2) способен самостоятельно выполнять все простые виды повседневной активности (одевание, раздевание, туалет, прием пищи);
3) нуждается в посторонней помощи при выполнении одного из сложных видов бытовой активности: приготовлении пищи, уборки дома, ведении финансовых дел и пр.
ИЛИ
Уточняющий признак:
4) не способен выполнять один из сложных видов социальной активности (вождение автомобиля, чтение, письмо, работа, хобби и другие) на преморбидном уровне.
Комбинация уточняющих признаков 1:
1) может выполнять преморбидно доступные виды (вождение автомобиля, чтение, письмо, работа и другие) деятельности без посторонней помощи, но с меньшей уверенностью и степенью активности, которая была до болезни;
2) может самостоятельно себя обслуживать (сам одевается и раздевается, ходит в магазин, готовит еду, может совершать небольшие путешествия и переезды, самостоятельно передвигается);
3) испытывает незначительные затруднения со стороны одной из систем жизнедеятельности (активность руки, походка).
Комбинация уточняющих признаков 1
1) обычная физическая нагрузка не вызывает выраженного утомления, слабости, одышки или сердцебиения;
2) стенокардия развивается при значительном, ускоренном или особо длительном напряжении (усилии).
ИЛИ
Комбинация уточняющих признаков 2
3) тесты с физической нагрузкой: велоэргометрия или эргоспирометрия ![]() 125 Вт/7 МЕТ;
125 Вт/7 МЕТ;
4) при отсутствии данных эргометрических проб - тест с шестиминутной ходьбой (ТШХ) > 425 м
3
Нарушение жизнедеятельности, умеренное по своей выраженности.
Ключевой признак: проживание в домашних условиях самостоятельно до 1 недели с периодическими еженедельными визитами второго лица
Комбинация уточняющих признаков 1:
1) Способен самостоятельно передвигаться без посторонней помощи под визуальным присмотром с ассистентным оборудованием (1 - 2 трости, ходунки) с подъемом по лестнице и выходом на улицу;
2) способен самостоятельно выполнять все простые виды бытовой активности (одевание, раздевание, туалет, прием пищи, гигиенические процедуры);
3) нуждается в посторонней помощи при выполнении более одного из сложных видов бытовой активности: приготовлении пищи, уборки дома, походе в магазин за покупками, ведении финансовых дел и пр.
ИЛИ
Уточняющий признак:
4) не способен выполнять более одного из видов социальной активности (вождение автомобиля, чтение, письмо, работа, хобби и другие) на преморбидном уровне.
Комбинация уточняющих признаков 1:
1) может передвигаться самостоятельно с помощью трости;
2) незначительное ограничение самообслуживания при одевании, раздевании, посещении туалета, приеме пищи), при необходимости может позвать на помощь
3) нуждается в посторонней помощи при выполнении сложных видов бытовой активности: приготовлении пищи, уборки дома, походе в магазин за покупками и других;
4) нуждается в помощи для выполнения операций с денежными средствами.
ИЛИ
Комбинация уточняющих признаков 2
5) умеренно выраженный болевой синдром во время ходьбы (4 - 5 балла по визуальной аналоговой шкале (ВАШ),
6) незначительно выраженный болевой синдром в покое (1 - 3 балла по визуальной аналоговой шкале боли (ВАШ);
Комбинация уточняющих признаков 1:
1) может передвигаться самостоятельно, без посторонней помощи;
2) способен самостоятельно выполнять все простые виды бытовой активности (одевание, раздевание, туалет, прием пищи, гигиенические процедуры);
3) нуждается в посторонней помощи при выполнении сложных видов бытовой активности: приготовление пищи, уборка дома, поход в магазин за покупками;
4) патологические симптомы в покое отсутствуют, обычная физическая нагрузка вызывает слабость, утомляемость, сердцебиение, одышку
5) стенокардия развивается при ходьбе на расстояние > 500 м по ровной местности, при подъеме на > 1 пролет обычных ступенек в среднем темпе в нормальных условиях.
ИЛИ
Комбинация уточняющих признаков 2
6) тесты с физической нагрузкой: велоэргометрия/эргоспирометрия = 75 - 100 Вт/4 - 6,9 МЕТ;
7) при отсутствии данных эргометрических проб ТШХ = 301 - 425 м
4
Выраженное нарушение проявлений жизнедеятельности.
Ключевой признак: проживание в домашних условиях самостоятельно с возможностью оставить без наблюдения и помощи второго лица от 6 до 12 часов
Комбинация уточняющих признаков 1:
1) вертикализирован до уровня пребывания в кресле не менее 6 часов в сутки с возможностью самостоятельной смены положения в кресле;
2) способен передвигаться с односторонней поддержкой и/или с ассистентным оборудованием без подъема по лестнице/без выхода на улицу.
ИЛИ
Комбинация уточняющих признаков 2:
3) нуждается в периодической посторонней помощи при выполнении одного и более из простых видом бытовой активности: одевание, раздевание, туалет, прием пищи, гигиенические процедуры и пр.;
4) способен к коммуникации не ниже уровня выражения потребности
5) способен привлечь помощь с использованием технических средств (телефон, компьютер).
Комбинация уточняющих признаков 1
1) умеренное ограничение возможности передвижения, не может передвигаться самостоятельно без дополнительного средства опоры - костылей;
2) нуждается в периодической помощи при выполнении одного и более одного из простых видом бытовой активности: одевание, раздевание, туалет, прием пищи, гигиенические процедуры и пр.;
ИЛИ
Комбинация уточняющих признаков 2
3) выраженный болевой синдром во время движений (6 - 8 баллов по ВАШ),
4) умеренно выраженный болевой синдром в покое (4 - 5 баллов по ВАШ).
Комбинация уточняющих признаков 1
1) умеренное ограничение возможностей передвижения;
2) нуждается в периодической посторонней помощи при выполнении одного и более одного из простых видом бытовой активности: одевание, раздевание, туалет, прием пищи, гигиенические процедуры и пр.;
3) стенокардия возникает при ходьбе от 100 до 500 м по ровной местности, при подъеме на 1 пролет обычных ступенек в среднем темпе в нормальных условиях.
ИЛИ
Комбинация уточняющих признаков 2
4) тесты с физической нагрузкой: велоэргометрия/эргоспирометрия = 25 - 50 Вт/2 - 3,9 МЕТ;
5) при отсутствии данных эргометрических проб ТШХ = 150 - 300 м
5
Грубое нарушение процессов жизнедеятельности
Ключевой признак: пребывание в условиях круглосуточной зависимости с возможностью оставить без наблюдения и помощи не более, чем на 6 часов
Комбинация уточняющих признаков 1:
1) вертикализирован до уровня пребывания в кресле менее 6 часов в сутки из-за потребности в ассистенции в смене положения в кресле;
2) нуждается в двусторонней поддержке при ходьбе в пределах комнаты.
ИЛИ
Комбинация уточняющих признаков 2:
3) нуждается в периодическом внимании второго лица и периодической помощи при выполнении всех простых видов бытовой активности: одевание, раздевание, туалет, гигиенические процедуры, прием пищи и др.;
4) способен привлечь внимание с помощью ассистентных средств (вызывная кнопка) и выразить потребность с использованием альтернативных средств коммуникации (пиктограмма).
ИЛИ
Уточняющий признак 3:
5) нуждается в круглосуточном медицинском уходе из-за трахеопищеводного разобщения (зонд, гастростома, трахеостома), и/или тазовых дисфункций.
Комбинация уточняющих признаков 1
1) не может передвигаться самостоятельно без дополнительного средства опоры - ходунки или самостоятельное передвижение в коляске; не может ходить по лестнице, перемещение ограничено пределами квартиры/стационарного отделения;
2) нуждается в периодическом внимании второго лица и периодической помощи при выполнении всех простых видов бытовой активности: одевание, раздевание, туалет, гигиенические процедуры, прием пищи и др.
ИЛИ
Уточняющий признак 2:
3) выраженный болевой синдром в покое (8 - 10 баллов по ВАШ), усиливающийся при движении.
1) не может передвигаться самостоятельно без посторонней помощи;
2) нуждается в периодическом внимании второго лица и периодической помощи при выполнении всех простых видов бытовой активности: одевание, раздевание, туалет, гигиенические процедуры, прием пищи и др.;
3) пациент комфортно чувствует себя только в состоянии покоя, минимальные физические нагрузки приводят к появлению слабости, сердцебиения, одышки, болям в сердце;
4) ТШХ < 150 м
6
Нарушение процессов жизнедеятельности тяжелой степени
Ключевой признак: потребность в коррекции нарушений гомеостаза и ПИТ-синдрома как барьера для реализации реабилитационного потенциала, требующая пребывание (до 3 суток) в условиях отделения интенсивной терапии и реанимации реабилитационного центра
Уточняющие признаки (не менее 2 признаков):
1) нуждается в лечении ПИТ-синдрома среднетяжелой степени (> 3 баллов);
2) нуждается в контроле и коррекции гомеостаза (нутритивный, водно-электролитный баланс) в том числе, из-за нарушения глотания с риском аспирации;
3) нуждается в визуальном контроле (в том числе персоналом ОРИТ) и ассистенции медицинского персонала 24 часа в сутки из-за неспособности привлечь внимание и выразить потребность
4) нуждается в пассивной (роботизированной) мобилизации: позиционировании, вертикализации, пассивных движениях из-за глубокого двигательного дефицита (менее 36 баллов по MRC) и/или сниженного гравитационного градиента (< 60°) в условиях аппаратного мониторинга;
5) нуждается в восстановлении трахеопищеводного сообщения (зонд, гастростома, трахеостома).
или
Ключевой признак: потребность в постоянном пребывании в условиях ОМР или/и отделения интенсивной терапии и реанимации реабилитационного центра
Уточняющие признаки (достаточно 1 признака):
6) статус продленного или хронических нарушений сознания
7) нуждается в круглосуточном мониторинге и/или поддержке витальных функций (дыхание, кровообращение), в том числе, в переводе с искусственной вентиляции легких на полное спонтанное дыхание.
