"Клинические рекомендации "Суправентрикулярные (наджелудочковые) тахикардии"
МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ
КЛИНИЧЕСКИЕ РЕКОМЕНДАЦИИ
СУПРАВЕНТРИКУЛЯРНЫЕ (НАДЖЕЛУДОЧКОВЫЕ) ТАХИКАРДИИ
Кодирование по Международной статистической классификации болезней и проблем, связанных со здоровьем: I45.6, I47.1, I47.9, I48
Год утверждения (частота пересмотра): 2025
Пересмотр не позднее: 2027
ID:973_1
Возрастная категория: Дети
Специальность:
Разработчик клинической рекомендации
Ассоциация сердечно-сосудистых хирургов России, Всероссийская общественная организация "Ассоциация детских кардиологов России", Всероссийское научное общество специалистов по клинической электрофизиологии, аритмологии и кардиостимуляции
Одобрено Научно-практическим Советом Минздрава России
Список сокращений
ААП - антиаритмические препараты
ААТ - антиаритмическая терапия
АВ - атриовентрикулярный
АВРТ - атриовентрикулярная реципрокная тахикардия
АВУРТ - атриовентрикулярная узловая реципрокная тахикардия
ВПУ - Вольфа-Паркинсона-Уайта синдром (феномен)
ВПС - врожденный порок сердца
ДПП - дополнительный проводящий путь
ДАВС - дополнительное атриовентрикулярное соединение
ЛЖ - левый желудочек
ПБЛНПГ - полная блокада левой ножки пучка Гиса
ПБПНПГ - полная блокада правой ножки пучка Гиса
Риентри (reentry) - повторный вход волны возбуждения
РЧА - радиочастотная абляция аритмогенных зон
СВТ - суправентрикулярная тахикардия
СР - синусовый ритм
СТ - синусовая тахикардия
СУ - синусовый узел
ТП - трепетание предсердий
УДД - уровень достоверности доказательств
УУР - уровень убедительности рекомендаций
ФВ - фракция выброса
ФП - фибрилляция предсердий
ХМ - холтеровское (суточное) мониторирование сердечного ритма
ХСН - хроническая сердечная недостаточность
ЧСС - частота сердечных сокращений
ЧЖС - частота желудочковых сокращений
ЧПС - частота предсердных сокращений
ЧПЭФИ - чреспищеводное электрофизиологическое исследование сердца
ЭКГ - электрокардиограмма
ЭФИ - электрофизиологическое исследование
ЭХОКГ - эхокардиография
** - препарат включен в перечень жизненно необходимых и важнейших лекарственных препаратов
# - при использовании препарата возможны отклонения от официальной инструкции по его применению
*** - медицинское изделие, имплантируемое в организм человека, при оказании медицинской помощи в рамках программы государственных гарантий бесплатного оказания гражданам медицинской помощи
Термины и определения
Пароксизмальная тахикардия - приступообразное увеличение частоты сердечных сокращений, с внезапным началом и окончанием приступа.
Непароксизмальная (хроническая) тахикардия - постоянная тахикардия или непрерывно-рецидивирующая тахикардия, занимающая большую часть времени суток.
Реципрокная тахикардия - тахикардия по механизму повторного входа возбуждения (макро-риентри).
Фокусная (очаговая) тахикардия - тахикардия, обусловленная выработкой частых патологических импульсов из небольшого ограниченного участка миокарда - "точечного источника", функционирующего по механизму аномального автоматизма/триггерной активности/микро-риентри.
Устойчивый приступ тахикардии - приступ тахикардии длительностью более 30 секунд.
Тахииндуцированная кардиомиопатия - расширение полостей сердца и снижение сократительной функции сердца в результате ремоделирования миокарда, вызванного тахикардией.
1. Краткая информация по заболеванию или состоянию (группы заболеваний или состояний)
1.1 Определение заболевания или состояния (группы заболеваний или состояний)
Суправентрикулярная (наджелудочковая) тахикардия (СВТ) - три и более последовательных сокращения сердца с частотой, превышающей верхнюю границу возрастной нормы у детей при условии наджелудочковой локализации источника аритмии: в синусовом узле (СУ), миокарде предсердий, мышечных муфтах легочных и полых вен, атриовентрикулярном (АВ) соединении, а также при участии в механизме аритмии дополнительных проводящих путей (ДПП).
Обычно во время СВТ регистрируется частый регулярный ритм с узкими комплексами QRS. Для предсердных тахикардий с вариабельным АВ-проведением характерен нерегулярный ритм. К СВТ с широкими комплексами QRS относятся: антидромная АВ-реципрокная тахикардия, другие СВТ с антероградным проведением по ДПП, СВТ с аберрантным проведением (с ПБПНПГ или ПБЛНПГ).
1.2 Этиология и патогенез заболевания или состояния (группы заболеваний или состояний)
В формировании СВТ могут участвовать несколько патофизиологических механизмов: повышенный автоматизм, аномальный автоматизм, триггерная активность и риентри (от англ. reentry).
Повышенный (ускоренный) автоматизм - нарушение формирования импульса в клетках СУ или латентных водителях ритма в результате увеличения скорости диастолической деполяризации. Повышенный автоматизм СУ приводит к хронической синусовой тахикардии, а латентных водителей ритма - к возникновению ускоренных выскальзывающих комплексов и ускоренных ритмов. Повышенный автоматизм возникает в клетках водителей ритма с исходно присущей им функцией спонтанной диастолической деполяризации. Этим данная категория отличается от аномального автоматизма.
Аномальный автоматизм - нарушение формирования импульса в результате возникновения спонтанной диастолической деполяризации в клетках миокарда предсердий, желудочков и проводящей системы сердца, которым в норме это не свойственно. В результате возникают эктопические центры частого патологического ритма. У детей патологические очаги автоматизма могут появляться из-за нарушения формирования специализированной ткани проводящей системы сердца в процессе кардиогенеза. Механизм аномального автоматизма является основной причиной фокусной предсердной тахикардии.
Триггерная активность - это возникновение дополнительных вторичных деполяризаций, которые связаны с предшествующим потенциалом действия. Если дополнительные экстравозбуждения возникают до завершения реполяризации клетки, то в этом случае они называются ранними постдеполяризациями. Они могут появляться во время II фазы (тип 1) или III фазы (тип 2) потенциала действия. Поздние или задержанные постдеполяризации возникают после завершения реполяризации клетки, т.е. в IV фазе потенциала действия. Триггерная активность может играть определенную роль в возникновении фокусных тахикардий (предсердной и узловой).
Риентри - механизм аритмии, заключающийся в повторном возбуждении участка миокарда одним и тем же импульсом, совершающим круговое движение. Для реализации этого механизма необходимы два пути проведения, причем по одному из них прохождение импульса нарушено вследствие местной однонаправленной блокады. В зависимости от размеров петли этот механизм подразделяется на макро-риентри и микро-риентри. При макро-риентри циркуляция осуществляется по анатомически определенному пути, например, с участием дополнительного АВ-соединения (ДАВС) при синдроме Вольфа-Паркинсона-Уайта (ВПУ). При микро-риентри циркуляция импульса происходит по функциональным путям. Тахикардии, в основе которых заложен механизм риентри, принято называть реципрокными.
СВТ в 95% случаев обнаруживаются у детей со структурно нормальным сердцем. Для манифестации СВТ необходима аритмогенная зона, в которой возникает и поддерживается патофизиологический механизм. Факторами риска и триггерами для СВТ у детей являются: отягощенный перинатальный анамнез, незрелость структур сердца у детей раннего возраста, нарушение нейровегетативной регуляции сердечного ритма, психологические особенности личности в виде психоэмоциональной лабильности и высокого уровня невротизации, экстракардиальная патология (заболевания центральной нервной системы, эндокринная патология, болезни обмена веществ, острые и хронические инфекционные заболевания), лихорадка, метаболические и электролитные нарушения, отравления. В более редких случаях возникновение СВТ связано с органической патологией сердца (врожденные и приобретенные пороки сердца, кардиомиопатии, воспалительные заболевания сердца). В процессе постнатального формирования структур сердца у детей раннего возраста часто происходит спонтанное исчезновение аритмии, например, из-за прекращения функционирования ДАВС [1 - 6].
1.3 Эпидемиология заболевания или состояния (группы заболеваний или состояний)
Частота встречаемости СВТ у детей - 0,1 - 0,4%. Частота встречаемости различных электрофизиологических вариантов СВТ зависит от возраста ребенка. В структуре СВТ во всех возрастных группах преобладают АВ-реципрокные тахикардии с участием ДАВС. Этот вид тахикардии составляет до 80% всех СВТ в возрасте до 1 года и 60 - 70% в более старшем возрасте.
Пароксизмальная АВ-узловая реципрокная тахикардия составляет 13 - 24% случаев всех СВТ у детей, причем ее встречаемость имеет четкую возрастную зависимость - от единичных случаев у детей раннего возраста до 30% всех СВТ у подростков. Предсердная тахикардия встречается реже: у 15 - 25% детей в возрасте до 1,5 лет и у 4 - 6% - в более старшем возрасте, при этом чаще у пациентов с врожденными пороками сердца. Фибрилляция предсердий редко возникает в детском возрасте.
До 30 - 50% СВТ, выявленных в неонатальном периоде, спонтанно исчезают к возрасту 18 мес. Особенно благоприятный прогноз у детей с синдромом Вольфа-Паркинсона-Уайта - если пароксизмальная АВ-реципрокная тахикардия с участием ДАВС возникает в первые месяцы жизни, то в большинстве случаев происходит спонтанная резолюция заболевания к первому году жизни, однако у трети пациентов аритмия вновь появляется в более позднем детстве. При возникновении СВТ в возрасте старше 5 лет спонтанное выздоровление наблюдается редко [7 - 8].
1.4 Особенности кодирования заболевания или состояния (группы заболеваний или состояний) по Международной статистической классификации болезней и проблем, связанных со здоровьем
I45.6 - Синдром преждевременного возбуждения.
I47.1 - Наджелудочковая тахикардия.
I47.9 - Пароксизмальная тахикардия неуточненная.
I48 - Фибрилляция и трепетание предсердий.
1.5 Классификация заболевания или состояния (группы заболеваний или состояний)
1. Синусовые тахикардии:
1.1. Физиологическая синусовая тахикардия
1.2. Нефизиологическая (хроническая) синусовая тахикардия
1.3. Синусовая узловая реципрокная тахикардия
2. Предсердные тахикардии:
2.1. Фокусная (очаговая) предсердная тахикардия
2.2. Полифокусная (хаотическая) предсердная тахикардия
2.3. Внутрипредсердная реципрокная тахикардия (инцизионная предсердная тахикардия)
2.4. Трепетание предсердий
2.5. Фибрилляция предсердий
3. Атриовентрикулярные узловые тахикардии:
3.1. Атриовентрикулярная узловая реципрокная тахикардия
3.1.1. Типичная
3.1.2. Атипичная
3.2. Фокусная (очаговая) тахикардия из АВ-соединения
3.2.1. Врожденная
3.2.2. Постоперационная
3.2.3. "Взрослый" вариант
4. Атриовентрикулярные тахикардии:
4.1. Атриовентрикулярная реципрокная тахикардия с участием ДПП (ДАВС и др.)
4.1.1. Ортодромная
4.1.2. Антидромная
1.6 Клиническая картина заболевания или состояния (группы заболеваний или состояний)
Пароксизмальная СВТ характеризуется внезапным началом и окончанием приступа, продолжительностью от нескольких секунд до нескольких часов (реже суток). У новорожденных и детей младшего возраста приступы СВТ сопровождаются беспокойством или вялостью, отказом от еды, тахипноэ, в тяжелых случаях - острой сердечной недостаточностью и кардиогенным шоком. Дети школьного возраста жалуются на сердцебиение, "дрожание" грудной клетки, чувство страха, ощущение нехватки воздуха, слабость, головокружение, потливость, боли в области сердца. Ребенка и его родителей следует расспросить о действиях, которые помогают купировать приступ тахикардии. Это могут быть стандартные вагусные маневры или другие успешные приемы, например, питье холодной воды, задержка дыхания, эффективное применение которых свидетельствует в пользу СВТ.
У 15% больных в момент приступа тахикардии развиваются предобморочные или обморочные состояния. Тяжелые клинические проявления характерны для детей с высокой ЧСС во время приступа тахикардии: 250 - 300 уд/мин у детей первого года жизни, 200 - 250 уд/мин у пациентов более старшего возраста. Провоцирующими факторами для возникновения приступа тахикардии у детей раннего возраста являются возбуждение, лихорадка, интоксикация, а у детей старшего возраста - психоэмоциональный стресс и физическая нагрузка. Приступ СВТ может возникать в покое без каких-либо провоцирующих факторов.
При непароксизмальной (хронической) СВТ часто дети не предъявляют жалоб и аритмия выявляется случайно при профилактических осмотрах и обследованиях по поводу интеркуррентных заболеваний. ЧСС во время хронической тахикардии обычно меньше, чем при пароксизмальной тахикардии, но у детей раннего возраста также может быть высокой и составлять 220 - 250 уд./мин. При длительном существовании хроническая СВТ осложняется развитием тахииндуцированной кардиомиопатии, что в конечном счете приводит к появлению сердечной недостаточности. После восстановления синусового ритма достаточно быстро, обычно в течение не более нескольких недель, размеры полостей сердца и сократительная функция миокарда возвращаются к возрастной норме [14 - 17].
2. Диагностика заболевания или состояния (группы заболеваний или состояний) медицинские показания и противопоказания к применению методов диагностики
Критерии установления диагноза:
Диагноз СВТ устанавливается на основании жалоб пациента, данных анамнеза, физикального обследования, результатов лабораторных и инструментальных исследований. Основой диагностики и дифференциальной диагностики СВТ является ее ЭКГ-регистрация, способ которой определяется частотой возникновения и продолжительностью приступов сердцебиения, наличием расстройств гемодинамики и другими особенностями СВТ [9 - 11].
2.1 Жалобы и анамнез
см. раздел "Клиническая картина"
Необходима оценка анамнеза заболевания: возраст появления аритмии, связь с перенесенными заболеваниями, вакцинацией, наличие заболеваний сердечно-сосудистой системы, ВПС, способы кардиохирургической коррекции ВПС, наличие синкопальных состояний. Немаловажной является оценка семейного анамнеза с выявлением случаев аритмии, приступов потери сознания и внезапной смерти членов семьи ребенка, находящегося на обследовании.
2.2 Физикальное обследование
У пациентов с имеющейся или предполагаемой СВТ необходимо оценить антропометрические показатели (измерение роста, измерение массы тела), наличие и распространенность цианоза, отеков. Детям проводят термометрию общую, исследование пульса, измеряют артериальное давление на периферических артериях, измеряют частоту дыхания, оценивают состояние шейных вен (набухание, пульсация), размеры печени, изменения щитовидной железы. Больным выполняют пальпацию, перкуссию и аускультацию (перкуссия при патологии сердца и перикарда, аускультация при патологии сердца и перикарда).
2.3 Лабораторные диагностические исследования
Если СВТ является осложнением какого-либо заболевания сердечно-сосудистой системы (миокардит, врожденный порок сердца, кардиомиопатия и др.), то лабораторные исследования должны соответствовать диагностическому поиску при определении основного заболевания.
- Рекомендуется проведение общего (клинического) анализа крови в рамках первичного обследования и в процессе динамического наблюдения у всех пациентов с СВТ для исключения сопутствующих заболеваний и осложнений лечения [9 - 11].
(УДД 5 УУР C)
- Рекомендуется проведение анализа крови биохимического общетерапевтического у всех пациентов с СВТ в рамках первичного обследования и в процессе динамического наблюдения для исключения сопутствующих заболеваний и осложнений лечения [9 - 11].
(УДД 5 УУР C)
Комментарии:
В исследование необходимо включать определение уровня электролитов в крови (исследование уровня калия, натрия, общего кальция, общего магния), так как гипокалиемия, гипонатриемия, гипокальциемия, гипомагниемия сами по себе оказывают аритмогенное действие, уменьшают эффективность ААТ и создают условие для проаритмий. Целевые значения калия составляют 4,5 - 5 ммоль/л.
При подозрении на заболевания сердца необходимо определение маркеров повреждения миокарда (исследование уровня тропонинов I, Т в крови) [18].
- Рекомендуется исследование уровня тиреотропного гормона (ТТГ) в крови, уровня свободного тироксина (СТ4) в крови, определение содержания антител к тиреопероксидазе в крови у всех пациентов с СВТ в рамках первичного обследования и в процессе динамического наблюдения для исключения сопутствующих заболеваний и осложнений лечения [9 - 11].
(УДД 5 УУР C)
2.4 Инструментальные диагностические исследования
- В тех случаях, когда анамнез, жалобы или физикальные данные позволяют предположить СВТ, ее наличие рекомендуется подтвердить с помощью регистрации ЭКГ или какой-либо другой методики с регистрацией электрокардиосигнала (Холтеровское мониторирование сердечного ритма, регистрация электрической активности проводящей системы сердца (A05.10.001)) [9 - 11, 18 - 23].
(УДД 4 УУР C)
Комментарии:
ЭКГ в 12 отведениях с регистрацией СВТ позволяет провести дифференциальную диагностику аритмии, основанную на оценке регулярности, количества и соотношения зубцов P и QRS-комплексов (Приложении Б2). ЭКГ вне приступа позволяет выявить признаки предвозбуждения желудочков, сопутствующие нарушения ритма и проводимости сердца, изменения, характерные для заболеваний сердца.
Холтеровское мониторирование сердечного ритма (ХМ) редко позволяет зарегистрировать пароксизмальную тахикардию (за исключением детей с частыми пароксизмами), но помогает оценить представленность хронической тахикардии в структуре суточного ритма сердца, а также выявить сопутствующие нарушения ритма и проводимости сердца.
Регистрация электрической активности проводящей системы сердца (путем чреспищеводного электрофизиологического исследования сердца (ЧПЭФИ)) позволяет в плановом порядке индуцировать и зарегистрировать пароксизмальную тахикардию с верификацией ее электрофизиологического варианта. ЧПЭФИ позволяет оценить электрофизиологические свойства СУ, АВ-узла и ДАВС. ЭРП ДАВС 250 мс и менее является дополнительным критерием для определения показаний к проведению РЧА ДАВС.
- У больных, получающих ААТ, рекомендуется регулярная регистрация ЭКГ в 12 отведениях и/или ХМ для оценки ее эффективности и безопасности [9 - 11].
(УДД 5 УУР C)
Комментарии: При назначении ААТ допустима умеренная медикаментозная брадикардия и умеренные изменения интервалов на ЭКГ в рамках электрофизиологических воздействий применяемых препаратов. При назначении #пропафенона** длительность PQ-интервала и ширина комплекса QRS не должны увеличиваться более чем на 25%; при назначении #амиодарона** длительность корригированного интервала QT не должна превышать 500 мс. Превышение данных параметров может привести к проаритмиям [18].
- Пациентам с СВТ для оценки размеров, объемов камер и сократительной функции сердца рекомендуется проведение трансторакальной эхокардиографии [9 - 11, 22].
(УДД 4 УУР C)
Комментарии: Цель проведения ЭХОКГ - диагностика структурной патологии сердца, органической патологии миокарда, признаков дисфункции миокарда, оценка гемодинамической значимости аритмии. Под тахииндуцированной кардиомиопатией подразумевают вторичную обратимую дисфункцию миокарда, вызванную тахиаритмией, проявляющуюся дилатацией полостей сердца, снижением сократительной способности миокарда желудочков, возникновением относительной митральной регургитации и развитием застойной сердечной недостаточности. Своевременное выявление этих осложнений позволяет правильно определить тактику ведения больного с аритмией. Восстановление ритма у детей без органического поражения сердца приводит к нормализации морфофункциональных параметров, а ЭХОКГ служит основным методом контроля динамики этих изменений [22 - 23].
2.5 Иные диагностические исследования
Другие методы визуализации сердца, такие как магнитно-резонансная томография сердца с контрастированием, компьютерная томография сердца с контрастированием, проводятся при подозрении на заболевания сердца по соответствующим им показаниям.
Проведение теста с однократной физической нагрузкой меняющейся интенсивности (стресс-тесты: велоэргометрия, тредмил-тест) позволяет установить связь НРС с физической нагрузкой. Но достаточно редко во время теста, если он проводится по стандартному протоколу, удается спровоцировать пароксизм СВТ, даже если спонтанные приступы тахикардии связаны с физической нагрузкой.
- В случаях предобморочных состояний и обмороков неясного генеза, при которых возникает подозрение на СВТ, рекомендуется проведение тилт-теста, при котором можно спровоцировать синкопальное состояние с оценкой физиологических параметров пациента (ЭКГ, ЭЭГ, АД) или имплантация петлевого регистратора для долговременной регистрации электрической активности проводящей системы сердца (кардиомонитор имплантируемый***), в памяти которого сохраняется и, впоследствии, анализируется ЭКГ во время приступа, если другие методы исследования оказались неэффективными [9 - 11].
(УДД 5 УУР C)
- Рекомендуется проведение внутрисердечного электрофизиологического исследования сердца (ЭФИ) детям, направленным на интервенционное лечение аритмии, а также в ряде случаев для уточнения природы аритмии и степени ее опасности для пациента, а также для выявления незарегистрированных нарушений ритма сердца, например, при невозможности установить генез повторяющихся приступов потери сознания при помощи других методов исследования [9 - 11].
(УДД 5 УУР C)
3. Лечение, включая медикаментозную и немедикаментозную терапии, диетотерапию, обезболивание, медицинские показания и противопоказания к применению методов лечения
Лечение СВТ включает в себя меры по восстановлению синусового ритма при пароксизме тахикардии, длительную медикаментозную терапию для профилактики рецидивов тахикардии и хирургическое (интервенционное) лечение [10, 11, 18].
3.1. Неотложная терапия
Проведение неотложной терапии находится в сфере профессиональной компетенции врача-анестезиолога-реаниматолога и должно осуществляться в отделении интенсивной терапии или в отделении реанимации детского медицинского учреждения под контролем монитора ЭКГ, АД, дыхания, сатурации кислорода и других жизненных функций. В случаях сохранения СВТ на фоне проведения стандартного протокола купирования приступа СВТ, при необходимости, проводится консультация с детским кардиологом по тактике дальнейшего лечения пациента.
Основными факторами, определяющими тактику медикаментозного лечения больных с СВТ, являются: состояние гемодинамики (стабильное или нестабильное), форма тахикардии (пароксизмальная или непароксизмальная), электрофизиологический вариант аритмии, возраст ребенка, сократительная функция сердца. Неправильная клиническая интерпретация клинико-электрокардиографических изменений, например, ошибочная диагностика пароксизмального характера тахикардии у детей с хронической СВТ, ведет к назначению неадекватной терапии, при этом попытки купирования хронической тахикардии быстрым введением больших доз ААП сопряжены с появлением осложнений вплоть до развития гемодинамического коллапса и остановки сердца. СВТ с блокадой ножек пучка Гиса и антидромную АВ-реципрокную тахикардию необходимо дифференцировать с желудочковой тахикардией. Купирование пароксизмальной тахикардии следует проводить под контролем ЭКГ и АД.
- Для неотложной терапии пароксизма СВТ с нестабильной гемодинамикой (клинические признаки сердечной недостаточности, низкое артериальное давление, синкопальное состояние) рекомендуется проведение наружной электрической кардиоверсии (синхронизированной кардиоверсии) [10, 11, 18, 24].
(УДД 5 УУР C)
Комментарии: Схема наложения электродов дефибриллятора для детей: один электрод помещают справа от грудины под ключицей, а второй - в проекции левой срединно-подмышечной линии. Если такое расположение электродов невозможно из-за маленького размера грудной клетки, то в экстренных случаях можно использовать следующие позиции: первый электрод - над проекцией сердца, а второй - на боковой стенке грудной клетки на уровне первого электрода. Энергия разряда для детей с СВТ составляет 0,5 - 1 - 2 Дж/кг.
Электрическая кардиоверсия эффективна при наличии риентри механизма тахикардии (фибрилляция и трепетание предсердий, АВ-реципрокная тахикардия с участием ДАВС, АВ-узловая реципрокная тахикардия, предсердная реципрокная тахикардия), но не купирует тахикардии по механизму аномального автоматизма (фокусная предсердная и узловая тахикардии). Электрическая кардиоверсия является методом выбора при неонатальном трепетании предсердий, после купирования которого в большинстве случаев не требуется ААТ.
При купировании пароксизма фибрилляции предсердий, длительность которого составляет более 48 ч, повышается риск тромбоэмболических осложнений, поэтому перед выполнением электрической кардиоверсии желательно проведение чреспищеводной ЭХОКГ, и в случае подозрения на наличие тромбов назначается варфарин** в течение 4 недель в дозе 0,1 мг/кг/сутки 1 раз в день (целевое значение международного нормализованного отношения 2,0 - 3,0). При ургентности ситуации перед проведением электрической кардиоверсии проводится внутривенное введение гепарина натрия** в дозе 100 ЕД/кг [25].
- У гемодинамически стабильных пациентов для купирования СВТ рекомендуется проведение вагусных приемов [10, 11, 18].
(УДД 5 УУР C)
Комментарии: у детей раннего возраста используют рефлекс погружения (прикладывание к лицу пузыря со льдом или резиновой перчатки со льдом и охлажденной водой на 5-10 сек), установку назогастрального зонда, переворот вниз головой; у детей школьного возраста - пробу Вальсальвы (глубокий вдох, натуживание, напряжение мышц брюшного пресса); нажатие на корень языка. Эффективность маневров при условии их правильного выполнения составляет 19 - 54%. Многие из этих приемов имеют минимальный риск развития осложнений и могут быть выполнены самим пациентом, родителями ребенка или медицинским персоналом. Необходимо обучить пациентов и их родителей технике выполнения данных приемов. Вагусные приемы носят как лечебный, так и диагностический характер, т.к. купируют реципрокные тахикардии с включением в круг риентри АВ-узла [26].
- При неэффективности вагусных приемов рекомендуется использование чреспищеводной электрокардиостимуляции для купирования устойчивой СВТ [10, 11, 18].
(УДД 5 УУР C)
Комментарии: Чреспищеводная электрокардиостимуляция наиболее эффективна при купировании пароксизмов АВ-реципрокной тахикардии и трепетания предсердий.
- При неэффективности вагусных приемов рекомендуется внутривенное введение #трифосаденина для купирования устойчивой СВТ [9 - 11, 27 - 29].
(УДД 5 УУР C)
Комментарии: Применяют следующую дозировку #трифосаденина (1% раствор, в ампуле 1 мл - 10 мг АТФ): последовательно осуществляется внутривенное введение препарата в нарастающих дозах 0,1 - 0,2 - 0.3 мг/кг, но не более 12 мг под контролем электрокардиограммы (каждая последующая доза вводится при неэффективности предыдущей через 1 - 2 минуты); у детей первого года жизни первая доза составляет 0,15 мг/кг [28, 29]. Эффективность составляет 90 - 100%, однако из-за очень короткого периода полувыведения (5 - 10 сек) возможно возобновление тахикардии в 1/3 случаев [9, 12].
#Трифосаденин вводится внутривенно болюсной инъекцией (через крупную вену) в течение 1-2 секунд с немедленным последующим введением 0,9% раствора натрия хлорида**. Эта методика известна как "методика двойного шприца". Для нее требуется внутривенный катетер и двухходовой кран с двумя шприцами для обеспечения эффективного введения аденозина и 0,9% раствора натрия хлорида**. Допустимо использование одношприцевой методики: 1 мл #трифосаденина разводится в шприце 0,9% раствором натрия хлорида** до объема 10 мл (содержание #трифосаденина в приготовленном растворе 1 мг/мл), а затем внутривенно водится рассчитанное для пациента количество препарата [29].
При введении #трифосаденина возникает пауза ритма из-за кратковременной АВ-блокады и угнетения СУ, однако длительной брадикардии не наблюдается, тем не менее к применению препарата у пациентов с дисфункцией синусового узла следует подходить с осторожностью. Сразу после введения препарата возможны: чувство жара, покраснение лица, одышка, но данная симптоматика также носит кратковременный характер [30].
- При неэффективности вагусных приемов и при отсутствии признаков предвозбуждения желудочков на ЭКГ (во время и вне приступа) детям в возрасте старше 1 года рекомендуется внутривенное введение #верапамила** для купирования устойчивой СВТ [9 - 11].
(УДД 5 УУР C)
Комментарии: #Верапамил** - блокатор кальциевых каналов (С08: Блокаторы кальциевых каналов). Угнетает автоматизм синусового узла и деполяризацию в АВ-узле. Вводится внутривенно в дозе 0,1 мг/кг в течение 2 мин [9, 10]. При внутривенном введении препарат быстро метаболизируется и обладает депрессивным влиянием на контрактильную функцию сердца. Внутривенное введение #верапамила** приводит к купированию пароксизма СВТ в 64 - 98% случаев, однако ассоциировано с развитием артериальной гипотензии. Поэтому препарат не следует применять у пациентов с нестабильной гемодинамикой, СН с низкой фракцией выброса ЛЖ. #Верапамил** не применяется у детей первого года жизни, т.к. может вызвать у них неконтролируемую гипотензию. #Верапамил** противопоказан пациентам с синдромом Вольфа-Паркинсона-Уайта, а также при тахикардии с широкими комплексами QRS, если этиология тахикардии не известна [18, 31 - 33].
- При неэффективности вагусных приемов, #трифосаденина и/или #верапамила** рекомендуется внутривенное введение #амиодарона** [9 - 11].
(УДД 5 УУР C)
Комментарии: #Амиодарон** - антиаритмический препарат III класса (С01BD: Антиаритмические препараты, класс III). Удлиняет продолжительность потенциала действия и рефрактерность в клетках миокарда, включая ДАВС, вследствие блокады калиевых каналов, торможения быстрого входящего натриевого тока, локального антиадренергического (как альфа-, так и бета-блокирующего) действия, блокады кальциевых каналов, что приводит к урежению ритма сердца, замедлению проведения в АВ-узле, дилатации периферических и коронарных сосудов. Препарат вводится внутривенно в нагрузочной дозе 5 - 10 мг/кг в течение 40 - 60 мин, затем в поддерживающей дозе 5 - 15 мкг/кг/мин (на основе 5% р-ра декстрозы**) [9] быстрое введение препарата и превышение рекомендуемых доз может привести к гемодинамическому коллапсу, особенно у детей раннего возраста с дисфункцией миокарда. Пик концентрации препарата в сыворотке крови достигается в течение 30 мин. При необходимости введение препарата в поддерживающей дозе можно проводить в течение нескольких суток (не более 5 дней). Если в дальнейшем в качестве ААТ планируется пероральный прием #амиодарона**, то пероральное насыщение #амиодароном** в рекомендуемых дозах (см. раздел 3.2) можно начинать на фоне внутривенного введения препарата, если необходимо продолжать инфузию (например, при частых рецидивах тахикардии). Если планируется другая постоянная ААТ (например, #пропафенон**), то ее желательно назначать после окончания внутривенной инфузии #амиодарона**. Во время введения #амиодарона** необходимо мониторирование ЭКГ и АД [34 - 38].
3.2. Медикаментозная терапия
Длительная ААТ назначается при частых, клинически и гемодинамически значимых приступах СВТ или при хронической СВТ с риском развития тахииндуцированной кардиомиопатии и при невозможности проведения интервенционного лечения (масса тела ребенка менее 15 кг, близость субстрата аритмии к структурам нормальной проводящей системы сердца или коронарным артериям, отказ пациента от РЧА и др. причины).
Длительная ААТ чаще применяется у новорожденных и детей раннего возраста. Целью ААТ у данной группы пациентов является предупреждение повторных приступов тахикардии, которые в раннем возрасте сложно отследить, но которые в случае затяжного характера часто приводят к развитию сердечной недостаточности. Поэтому ААТ назначается сразу после первого зарегистрированного приступа СВТ на срок 4 - 12 мес. в зависимости от клинической картины и динамики ЭКГ [18].
Оценка эффективности лечения базируется на изменении клинического течения заболевания и объективной регистрации выраженности аритмии современными методами неинвазивной электрокардиографической диагностики (отсутствие приступов тахикардии, уменьшение представленности хронической тахикардии). Необходим постоянный контроль безопасности ААТ, для чего проводится оценка электрофизиологических эффектов ААП по данным ЭКГ (изменение длительности интервалов PQ, QTc, ширины комплекса QRS) и отслеживаются возможные аритмогенные и экстракардиальные осложнения. Особое внимание следует обратить на мониторинг функционального состояния щитовидной железы при постоянном применении #амиодарона**. При подборе терапии ААП назначаются последовательно, начиная с препаратов с меньшим периодом полувыведения. Эффективная доза ААП, за исключением #амиодарона**, подбирается путем титрования (постепенного увеличения). При неэффективности монотерапии, применяется комбинированная ААТ. При стойкой медикаментозной ремиссии аритмии проводится плановая отмена терапии. Перед снятием с диспансерного учета проводится контрольное кардиологическое обследование [18, 33, 39 - 45].
Сведения о дозах ААП, их возможных побочных действиях представлены в Приложении А3.1.
- #Пропранолол** рекомендуется для лечения симптомных пациентов с СВТ [9 - 11, 18, 43].
(УДД 5 УУР C)
Комментарии: #Пропранолол** - неселективный бета-адреноблокатор, оказывает мембраностабилизирующее действие, уменьшает частоту сердечных сокращений, снижает автоматизм СУ, замедляет АВ-проведение. Принимается внутрь в дозе 1 - 3 мг/кг/сутки в 3-4 приема [9].
- #Атенолол** рекомендуется для лечения симптомных пациентов с СВТ [9 - 11, 46, 47].
(УДД 4 УУР C)
Комментарии: #Атенолол** - селективный бета-адреноблокатор, не обладает мембраностабилизирующей активностью. Уменьшает частоту сердечных сокращений, снижает автоматизм СУ, замедляет АВ-проведение. Принимается внутрь в дозе 0,3 - 1,3 мг/кг/сутки в один прием [18]. #Атенолол** оказывает менее выраженное влияние на гладкую мускулатуру бронхов и периферических артерий, чем пропранолол. Однако кардиоселективность #атенолола** снижается при увеличении дозы препарата [18, 47].
- #Пропафенон** рекомендуется для лечения симптомных пациентов с СВТ [9 - 11, 18, 48 - 50].
(УДД 4 УУР C)
Комментарии: #Пропафенон** (С01BC: Антиаритмические препараты, класс Ic) блокирует быстрые Na-каналы, что сопровождается замедлением проведения импульса по предсердиям, желудочкам, АВ-соединению и ДАВС. Обладает М-холиноблокирующим и слабым бета-адреноблокирующим эффектом. Препарат принимается внутрь в дозе 5 - 15 мг/кг/сутки в 3 приема или по 200 - 600 мг/м2 в сутки в 3 приема [9, 50]. Начальная доза составляет 5 - 7 мг/кг/сутки с дальнейшим титрованием дозы до эффективной [50].
У пациентов с предсердными макро-риентри тахикардиями не рекомендуется применение #пропафенона** в качестве монотерапии. #Пропафенон** удлиняет рефрактерность в клетках предсердий, тем самым удлиняя цикл предсердной тахикардии (уменьшается частота предсердных сокращений), что может привести к устранению функциональной АВ-блокады и значительному увеличению частоты желудочковых сокращений (например, имеется трепетание предсердий с ЧПС 300 в мин и АВ-блокадой 2:1, т.е. ЧЖС 150 уд/мин; на фоне #пропафенона** ЧПС сокращается до 240 в мин, становится возможным АВ-проведение 1:1 и ЧЖС увеличивается до 240 уд/мин). Для исключения такой ситуации можно использовать #пропафенон** в комбинации с препаратами, угнетающими АВ-проведение (#пропафенон**+бета-адреноблокаторы). Также противопоказан #пропафенон** пациентам с заболеваниями миокарда в случае наличия у них выраженной дисфункции желудочков, низкой фракции выброса, выраженной гипертрофии миокарда и тяжелого фиброза [10 - 11, 18, 49 - 50].
- #Соталол** рекомендуется для лечения симптомных пациентов с СВТ [9 - 11, 18, 51-53].
(УДД 4 УУР C)
Комментарии: #Соталол** - бета-адреноблокатор по АТХ классификации, антиаритмический препарат III класса по классификации E.Vaughan-Williams. Неселективно блокирует 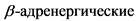 рецепторы и калиевые каналы (в высоких дозах), пролонгируя продолжительность потенциала действия и эффективный рефрактерный период в предсердиях, желудочках, АВ-узле, системе Гиса-Пуркинье и в дополнительных проводящих путях. Препарат принимается внутрь в дозе 2 - 8 мг/кг/сутки в 2 приема [9, 18]. Начальная доза препарата составляет 2 мг/кг/сутки с последующим осторожным титрованием до эффективной под контролем ЭКГ и АД. Обычно максимальная доза не превышает 4 - 6 мг/кг/сутки [53].
рецепторы и калиевые каналы (в высоких дозах), пролонгируя продолжительность потенциала действия и эффективный рефрактерный период в предсердиях, желудочках, АВ-узле, системе Гиса-Пуркинье и в дополнительных проводящих путях. Препарат принимается внутрь в дозе 2 - 8 мг/кг/сутки в 2 приема [9, 18]. Начальная доза препарата составляет 2 мг/кг/сутки с последующим осторожным титрованием до эффективной под контролем ЭКГ и АД. Обычно максимальная доза не превышает 4 - 6 мг/кг/сутки [53].
- #Амиодарон** рекомендуется для лечения симптомных пациентов с СВТ [9 - 11, 18, 37, 54, 55].
(УДД 5 УУР C)
Комментарии: #Амиодарон** - (С01BD: Антиаритмические препараты, класс III) обычно назначается при неэффективности бета-адреноблокаторов и #пропафенона**. Является препаратом выбора у детей со сниженной фракцией выброса левого желудочка. Доза насыщения составляет 10 мг/кг в сутки в два приема внутрь в течение 10 дней (длительность насыщения определяется клинической картиной и степенью удлинения QTc). Поддерживающая доза - 5 мг/кг/сутки внутрь в один прием. Препарат не применяется при исходно увеличенном или пограничном интервале QTc. На фоне приема препарата интервал QTc не должен увеличиваться более 500 мс [9, 18].
- #Верапамил** рекомендуется для лечения симптомных пациентов старше 1-го года с СВТ без признаков предвозбуждения желудочков на ЭКГ (во время тахикардии и на ЭКГ покоя) при неэффективности других ААП [9 - 11, 18].
(УДД 5 УУР C)
Комментарии: #Верапамил** - блокатор кальциевых каналов. Препарат действует на медленные входящие кальциевые токи, угнетая автоматизм синусового узла и деполяризацию в АВ-узле. Оказывает отрицательный инотропный эффект, снижает АД. Редко применяется у детей, обычно при неэффективности или противопоказаниях к другим ААП. Не используется у детей первого года жизни и у пациентов с синдромом Вольфа-Паркинсона-Уайта. #Верапамил** может быть полезен для контроля частоты сокращений желудочков при предсердных тахикардиях, в том числе при фибрилляции предсердий. Препарат может быть эффективен у детей с пароксизмальной АВ-узловой реципрокной тахикардией. Рекомендуемые дозы - 4 - 8 мг/кг в сутки внутрь в 3 приема [18].
- #Дигоксин** рекомендуется для лечения симптомных пациентов с СВТ без признаков предвозбуждения желудочков на ЭКГ (во время тахикардии и на ЭКГ покоя) [9 - 11, 18, 43].
(УДД 4 УУР C)
Комментарии: #Дигоксин** обычно применяется у детей с предсердными тахикардиями в структуре комбинированной ААТ. #Дигоксин** повышает парасимпатическую активность и стимулирует мускариновые рецепторы 2-го типа. В результате замедляется частота сердечных сокращений и АВ-проводимость. Цель назначения #дигоксина** - контроль частоты сокращения желудочков.
#Дигоксин** не назначается пациентам с синдромом Вольфа-Паркинсона-Уайта вследствие укорочения ЭРП ДАВС и риска развития жизнеугрожающей аритмии в случае возникновения фибрилляции предсердий.
#Дигоксин** назначается внутрь в поддерживающей доз (таблица 1) разделенной на 2 приема [56].
Таблица. Поддерживающие дозы дигоксина** у детей
Возрастная группа
Поддерживающая доза
Новорожденные недоношенные
5,0 - 8,0 мкг/кг/сутки
Новорожденные недоношенные
6,0 - 10,0 мкг/кг/сутки
1 месяц - 2 года
10,0 - 12,0 мкг/кг/сутки
2 года - 5 лет
7,5 - 10,0 мкг/кг/сутки
5 - 10 лет
5,0 - 10,0 мкг/кг/сутки
Старше 10 лет
2,5 - 5,0 мкг/кг/сутки
3.3. Хирургическое (интервенционное) лечение
Безопасность и высокая эффективность радиочастотной абляции аритмогенных зон (РЧА) сделали ее методом выбора для лечения большинства пациентов с СВТ. Эффективность операции РЧА оценивается интраоперационно на основании электрофизиологических критериев, а также в раннем и отдаленном послеоперационных периодах на основании исчезновения тахикардии и признаков предвозбуждения желудочков по данным ЭКГ и ХМ. У детей раннего возраста риск развития осложнений выше, чем в старшей возрастной группе, а также имеются технологические особенности проведения операций. Поэтому в определении показаний к РЧА придерживаются "разумного" консерватизма у детей раннего возраста, что связано в том числе и с высокой вероятностью спонтанного исчезновения СВТ к 18-месячному возрасту. Однако, у 30% из них аритмия в последующем рецидивирует, что требует наблюдения и принятия решения о дальнейшей тактике лечения. У детей с массой тела < 15 кг предпочтение отдается медикаментозной терапии, а РЧА выполняется по жизненным показаниям в наиболее подготовленных клиниках. Эффективность РЧА у детей составляет от 77% при предсердных тахикардиях до 97 - 100% при АВ-узловой реципрокной тахикардии и синдроме Вольфа-Паркинсона-Уайта. В ряде случаев для ограничения зоны повреждения и снижения риска поражения проводящей системы сердца используется методика криоабляции аритмогенных зон, в основу которой положено воздействие низкими температурами [18, 57 - 65].
- Рекомендуется проведение РЧА при наличии следующих состояний [9, 18, 59 - 61]:
1.
1.1. Синдром Вольфа-Паркинсона-Уайта с эпизодом внезапной остановки кровообращения в анамнезе в любом возрасте.
1.2. Синдром Вольфа-Паркинсона-Уайта с синкопе в анамнезе и предикторами развития внезапной остановки кровообращения: множественные ДАВС, значение антероградного эффективного рефрактерного периода ДАВС ![]() 250 мс, либо величина интервала RR в пароксизме фибрилляции предсердий с АВ-проведением по ДАВС
250 мс, либо величина интервала RR в пароксизме фибрилляции предсердий с АВ-проведением по ДАВС ![]() 250 мс в любом возрасте.
250 мс в любом возрасте.
1.3. Рецидивирующая симптомная предсердная тахикардия у пациентов с ВПС (не ранее, чем через 3 - 6 мес. после кардиохирургической коррекции), когда медикаментозная терапия неэффективна и/или связана с побочными эффектами в любом возрасте.
1.4. Постоянная или рецидивирующая СВТ в отсутствии эффекта от ААТ, включая комбинации препаратов, либо прием ААП сопровождается развитием побочных эффектов в любом возрасте.
1.5. Постоянная или рецидивирующая СВТ при наличии дисфункции миокарда желудочков у пациентов с массой тела ![]() 15 кг.
15 кг.
1.6. Постоянная или рецидивирующая СВТ с гемодинамическими нарушениями (гипотензия, обмороки) у пациентов с массой тела ![]() 15 кг.
15 кг.
1.7. Рецидивирующая СВТ, при купировании которой использовалась синхронизированная кардиоверсия (для пациентов с массой тела ![]() 15 кг).
15 кг).
1.8. Постоянная или рецидивирующая СВТ при наличии желания у пациента и его родителей (законных представителей) отказаться от длительного приема ААП (для пациентов с массой тела ![]() 15 кг).
15 кг).
2.
2.1. Феномен Вольфа-Паркинсона-Уайта при наличии предикторов внезапной остановки кровообращения (множественные ДАВС; значение антеградного эффективного рефрактерного периода ДАВС ![]() 250 мс, либо величина интервала RR в индуцированном пароксизме фибрилляции предсердий с АВ-проведением по ДАВС
250 мс, либо величина интервала RR в индуцированном пароксизме фибрилляции предсердий с АВ-проведением по ДАВС ![]() 250 мс) у пациентов с массой тела
250 мс) у пациентов с массой тела ![]() 15 кг.
15 кг.
2.2. Дисфункция миокарда на фоне внутрижелудочковой диссинхронии, связанной с наличием ДАВС (для пациентов с массой тела ![]() 15 кг).
15 кг).
2.3. Феномен Вольфа-Паркинсона-Уайта при наличии синкопе и в отсутствии предикторов внезапной остановки кровообращения у пациентов с массой тела ![]() 15 кг
15 кг
2.4. Феномен Вольфа-Паркинсона-Уайта у пациентов с массой тела ![]() 15 кг, когда наличие преэкзитации является противопоказанием к занятию спортом и сопровождается профессиональными ограничениями.
15 кг, когда наличие преэкзитации является противопоказанием к занятию спортом и сопровождается профессиональными ограничениями.
2.5. Наличие единичных эктопических фокусов, запускающих пароксизм фибрилляции предсердий, расположенных в предсердиях или в устье одной из легочных вен.
(УДД 5 УУР C)
Комментарии: Несмотря на осторожное отношение к РЧА у детей с массой тела ![]() 15 кг существует категория детей раннего возраста с медикаментозно-рефрактерными и жизнеопасными СВТ, которым показан данный метод лечения. Процедура РЧА у детей с массой тела
15 кг существует категория детей раннего возраста с медикаментозно-рефрактерными и жизнеопасными СВТ, которым показан данный метод лечения. Процедура РЧА у детей с массой тела ![]() 15 кг выполняется специалистами, имеющими опыт лечения пациентов данного возраста. Более безопасно выполнять РЧА в аритмологических центрах, где есть возможность кардиохирургической поддержки для лечения возможных осложнений [59].
15 кг выполняется специалистами, имеющими опыт лечения пациентов данного возраста. Более безопасно выполнять РЧА в аритмологических центрах, где есть возможность кардиохирургической поддержки для лечения возможных осложнений [59].
- Рекомендуется прием #ацетилсалициловой кислоты** после выполнения РЧА [66]
(УДД 4 УУР C)
Комментарии: Назначение низких доз #ацетилсалициловой кислоты** (2 - 5 мг/кг в сутки) в течение 6 - 8 недель после РЧА обосновано, когда воздействия были выполнены в системном желудочке/предсердии, а так же при наличии внутрисердечных шунтов [66].
4. Медицинская реабилитация и санаторно-курортное лечение, медицинские показания и противопоказания к применению методов медицинской реабилитации, в том числе основанных на использовании природных лечебных факторов
Необходимость в реабилитации больных с СВТ определяется наличием и тяжестью основного заболевания сердечно-сосудистой системы и наличием коморбидной патологии. В связи с этим оказываются необходимые услуги по медицинской реабилитации пациента с заболеваниями сердечно-сосудистой системы и другой патологией. В большинстве случаев реабилитация детям с СВТ не требуется, имеются лишь некоторые ограничения в выполнении физических нагрузок.
- Ограничение физических нагрузок в течение 3-х месяцев рекомендуется всем пациентам, перенесшим успешную РЧА по поводу СВТ. При отсутствии осложнений проведения специальных реабилитационных мероприятий не требуется [9].
(УУР C УДД 5)
Комментарии: В случаях возникновения любых осложнений после РЧА, в том числе отсроченных, показана скорейшая госпитализация в специализированный кардиологический/кардиохирургический стационар для проведения необходимых лечебно-диагностических мероприятий [18].
5. Профилактика и диспансерное наблюдение, медицинские показания и противопоказания к применению методов профилактики
- Рекомендуется диспансерное наблюдение пациентов с СВТ (пароксизмальными и непароксизмальными) врачом-детским кардиологом или врачом-педиатром по месту жительства не реже 1 раза в 6 мес. для оценки эффективности лечения. В стандартный план обследования входят ЭКГ в 12 стандартных отведениях, ЭХОКГ, холтеровское мониторирование сердечного ритма [9].
(УУР C УДД 5)
Комментарии: У пациентов, получающих длительную ААТ, ЭКГ в 12 стандартных отведениях регистрируется не реже, чем 1 раз в 3 мес. ЭХОКГ, Холтеровское мониторирование сердечного ритма проводятся не реже 1 раза в 6 мес., у детей раннего возраста - не реже 1 раза в 2 - 3 мес. Развитие новых, не зарегистрированных ранее, нарушений ритма сердца, удлинение интервала QTc, появление внутрижелудочковых и атриовентрикулярных блокад на фоне приема ААП является основанием для коррекции терапии. При длительном назначении #амиодарона** не реже 1 раза в 6 мес. проводятся исследования уровня тиреотропного гормона (ТТГ) в крови, исследование уровня свободного тироксина (CТ4 сыворотки крови), определение содержания антител к тиреопероксидазе в крови, проводится биохимический общетерапевтический анализ крови.
У детей первого года жизни ААТ назначается после регистрации СВТ и обычно продолжается 4 - 6 мес., после чего при условии ее эффективности отменяется с последующим контрольным обследованием. Бета-адреноблокаторы, #пропафенон**, #соталол** отменяются постепенно путем уменьшения разовых доз препарата в течение 3 - 7 дней. Амиодарон отменяется единовременно. При рецидиве СВТ, ААТ возобновляется.
В случаях успешной РЧА аритмогенных зон и при отсутствии осложнений, связанных с данной процедурой, больные без заболеваний сердца не нуждаются в длительном диспансерном наблюдении. После осложненной РЧА аритмогенных зон больные с СВТ требуют тщательного диспансерного наблюдения у врача-детского кардиолога/врача-сердечно-сосудистого хирурга, регулярность которого определяется характером осложнения.
При возникновении показаний для применения высокотехнологических методов диагностики и лечения на любом этапе диспансерного наблюдения пациенты с СВТ направляются на консультацию к врачу-детскому кардиологу специализированного аритмологического центра [9].
- Рекомендуется после проведения РЧА аритмогенных зон через 3 месяца в ходе диспансерного наблюдения провести контрольное обследование (ЭКГ в 12 отведениях, ЭХОКГ, ХМ) с целью оценки эффективности лечения [9].
(УУР C УДД 5)
Комментарии:
При наличии жалоб на незарегистрированные на ЭКГ приступы сердцебиений проводится ЧПЭФИ. При отсутствии данных за аритмию пациент снимается с диспансерного учета.
После проведения РЧА предсердной тахикардии обследования (ЭКГ в 12 отведениях, ЭХОКГ, ХМ) проводятся через 3, 6 и 12 месяцев. При отсутствии данных за рецидив аритмии пациент снимается с диспансерного учета. Наличие СВТ у пациента без воспалительных заболеваний сердца не является противопоказанием к вакцинации.
6. Организация оказания медицинской помощи
Показания для экстренной госпитализации в медицинскую организацию:
1. Клинически значимый пароксизм СВТ при отсутствии эффекта неотложной помощи на догоспитальном этапе.
2. Впервые зарегистрированная СВТ у ранее не обследованного ребенка.
3. Побочные и аритмогенные эффекты ААП.
Показания для плановой госпитализации в медицинскую организацию:
1. Оказание специализированной кардиологической помощи, требующей постоянного врачебного наблюдения и выполнения лечебных процедур.
2. Оказание высокотехнологичной медицинской помощи.
3. Невозможность проведения диагностических и лечебных мероприятий в амбулаторно-поликлинических условиях.
4. Территориальная отдаленность больного от стационара (с учетом потенциально возможного ухудшения течения заболевания).
5. Неэффективность амбулаторного лечения пациентов с СВТ.
Плановая госпитализация осуществляется при наличии у больного результатов диагностических исследований, которые могут быть проведены в амбулаторных условиях (согласно перечню обязательного объема обследования больных, направляемых на плановую госпитализацию), и при возможности проведения необходимых методов обследования в лечебно-профилактическом учреждении. Максимальное время ожидания определяется очередью на плановую госпитализацию.
Показания к выписке пациента из медицинской организации:
1. При выздоровлении пациента.
2. При стойком улучшении, когда по состоянию здоровья больной может без ущерба для здоровья продолжать лечение амбулаторно под наблюдением участкового врача.
3. При отсутствии показаний к дальнейшему лечению в стационаре.
4. При необходимости перевода больного в другое лечебное учреждение.
5. По требованию больного или его законного представителя.
6. В случаях несоблюдения пациентом предписаний или правил внутреннего распорядка лечебно-профилактического учреждения, если это не угрожает жизни больного и здоровью окружающих.
7. Дополнительная информация (в том числе факторы, влияющие на исход заболевания или состояния)
СВТ в большинстве случаев не относятся к угрожающим жизни аритмиям. Опасность представляют: СВТ с гемодинамическими нарушениями, СВТ с развитием тахииндуцированной кардиомиопатии, ФП и ТП у детей с синдромом Вольфа-Паркинсона-Уайта с большой частотой желудочкового ритма, СВТ у детей с заболеваниями сердца. Гемодинамические нарушения, вплоть до кардиогенного шока, характерны для новорожденных и грудных детей с затянувшимися приступами тахикардии, приводящими к снижению сократительной способности сердца. Тахииндуцированная кардиомиопатия также характерна для хронической СВТ. При возникновении пароксизмальной СВТ у детей в первые месяцы жизни прогноз благоприятный при ее медикаментозном контроле - в большинстве случаев имеется спонтанная резолюция заболевания к первому году жизни, что позволяет отменить ААТ. Если приступы СВТ появляются в школьном возрасте, в большинстве случаев они самостоятельно не исчезнут, но в данной возрастной группе меньше ограничений для проведения радикального лечения - РЧА, что также позволяет говорить о положительном исходе заболевания [18].
Критерии оценки качества медицинской помощи
N
Критерии качества
Оценка выполнения (да/нет)
1
Наличие СВТ подтверждено с помощью ЭКГ в 12 отведениях или Холтеровского мониторирования сердечного ритма
да/нет
2
Выполнена ЭХОКГ
да/нет
3
Выполнен общий (клинический) анализ крови
да/нет
4
Выполнен биохимический общетерапевтический анализ крови
да/нет
5
Проведено исследование уровня тиреотропного гормона (ТТГ) в крови, исследование уровня свободного тироксина (CТ4) сыворотки крови, определение содержания антител к тиреопероксидазе в крови
да/нет
6
Выполнена наружная электрическая кардиоверсия (дефибрилляция) пациенту с гемодинамически нестабильным приступом СВТ
да/нет
7
Выполнены вагусные приемы у гемодинамически стабильных пациентов
да/нет
8
При неэффективности вагусных приемов выполнено внутривенное введение #трифосаденина для купирования устойчивой СВТ
да/нет
9
Пациент с синдромом Вольфа-Паркинсона-Уайта с эпизодом внезапной остановки кровообращения в анамнезе направлен на радиочастотную абляцию аритмогенных зон
да/нет
11
Пациент с синдромом Вольфа-Паркинсона-Уайта с синкопе в анамнезе и предикторами развития внезапной остановки кровообращения направлен на радиочастотную абляцию аритмогенных зон
да/нет
12
Пациент с постоянной или рецидивирующей СВТ в отсутствии эффекта от антиаритмической терапии, включая комбинации препаратов, либо если прием препаратов сопровождался развитием побочных эффектов, направлен на радиочастотную абляцию аритмогенных зон
да/нет
Список литературы
1. J.K. Ko, B.J. Deal, J.F. Strasburger, D.W. Benson. Supraventricular tachycardia mechanisms and their age distribution in pediatric patients. Am. J. Cardiol. 1992; 69: 1028 - 1032.
2. Moak J.P. Supraventricular tachycardia in the neonate and infant. Prog. Pediatr. Cardoiol. 2000; 11: 25 - 38.
3. М.А. Школьникова, Л.А. Кравцова, В.В. Березницкая. Тахикардии у детей первого года жизни. Педиатрия. 2012; 91 (3):. 90 - 99.
4. Practical management of pediatric cardiac arrhythmias. Edited by Vicki L. Zeigler and Pan: С Gillette. New York, Futura Publishing Company, Inc.; 2001. 422 p.
5. Miyoshi T, Maeno Y, Hamasaki T et al. Japan Fetal Arrhythmia Group. Antenatal Therapy for Fetal Supraventricular Tachyarrhythmias: Multicenter Trial. J Am Coll Cardiol. 2019; 74 (7): 874 - 885.
6. Wu M-H, Chen H-C, Kao F-Y, Huang S-K. et al. Postnatal cumulative incidence of supraventricular tachycardia in a general pediatric population: a national birth cohort database study. Heart Rhythm. 2016; 13: 2070 - 2075.
7. Кручина Т.К., Новик Г.А., Егоров Д.Ф. Клинические варианты и частота возникновения суправентрикулярных тахикардий у детей. Лечащий врач. 2011; 10: 64 - 68.
8. L.M. Rodriges, C. Chillou, J. Schlapfer et al. Age at onset and gender of patients with different types of supraventricular tachycardias. Am. J. Cardiol. 1992; 70: 1213 - 1215.
9. Ковалев И.А., Хамнагадаев И.А., Свинцова Л.И. и др. Суправентрикулярные (наджелудочковые) тахикардии у детей. Педиатрическая фармакология. 2019; 16(3): 133 - 143.
10. Brugada J., Katritsis D.G., Arbelo E. et al. 2019 ESC Guidelines for the management of patients with supraventricular tachycardia. Eur Heart J. 2020; 41(5): 655 - 720.
11. Клинические рекомендации "Наджелудочковые тахикардии" (для взрослых), разработанные Российским кардиологическим обществом при участии Всероссийского научного общества специалистов по клинической электрофизиологии, аритмологии и кардиостимуляции, Ассоциации сердечно-сосудистых хирургов России (Одобрено на заседании Научно-практического совета Министерства здравоохранения Российской Федерации (заседание от 16.10.2020 г. протокол N 38/2-3-4))
12. Кручина Т.К., Егоров Д.Ф. Суправентрикулярные тахикардии у детей: клиника, диагностика, методы лечения. СПб.: Человек, 2011. 356 с.
13. Кушаковский МС. Аритмии сердца: Руководство для врачей. 3-е изд., испр. и доп. - СПб.: Фолиант, 2004: с 672.
14. S.P. Seslar, M.M. Garrison, C. Larison, J.C. Salerno A Multi-institutional Analysis of Inpatient Treatment for Supraventricular Tachycardia in Newborn and Infants. Pediatr. Cardiol. 2013; 34: 408 - 414.
15. Quattrocelli A., Lang J., Davis A., Pflaumer A. Age makes a difference: Symptoms in pediatric supraventricular tachycardia. J Arrhythm. 2018 Aug 13; 34(5): 565 - 571.
16. Michelson KA, Neuman MI, Porter JJ et all. Care of Children with Supraventricular Tachycardia in the Emergency Department. Pediatr Cardiol. 2021 Mar; 42(3): 569 - 577.
17. Baksiene ND, Sileikiene R, Sileikis V et al. Atrial tachyarrhythmias in infants. The Turkish Journal of Pediatrics. 2008; 50: 143 - 148.
18. Brugada J, Blom N, Sarquella-Brugada G. et al. Pharmacological and non-pharmacological therapy for arrhythmias in the pediatric population: EHRA and AEPC-Arrhythmia Working Group joint consensus statement. Europace. 2013; 15: 1337 - 1382.
19. Brembilla-Perrot B, Sellal JM, Olivier A. et al. Influence of advancing age on clinical presentation, treatment efficacy and safety, and long-term outcome of inducible paroxysmal supraventricular tachycardia without pre-excitation syndromes: A cohort study of 1960 patients included over 25 years. PLoS One. 2018 Jan 5; 13(1): e0187895.
20. Akin A, ![]() ,
,  T et al. Sensitivity of transesophageal electrophysiologic study in children with supraventricular tachycardia on electrocardiography. Pacing Clin Electrophysiol. 2014 Aug; 37(8): 1002 - 1008.
T et al. Sensitivity of transesophageal electrophysiologic study in children with supraventricular tachycardia on electrocardiography. Pacing Clin Electrophysiol. 2014 Aug; 37(8): 1002 - 1008.
21. Zipes DP, Calkins H, Daubert JP et al. 2015 ACC/AHA/HRS Advanced Training Statement on Clinical Cardiac Electrophysiology (A Revision of the ACC/AHA 2006 Update of the Clinical Competence Statement on Invasive Electrophysiology Studies, Catheter Ablation, and Cardioversion). Am Coll Cardiol. 2015 Dec 22; 66(24): 2767 - 2802.
22. L'Italien K, Conlon S., Kertesz N. et al. Usefulness of Echocardiography in Children with New-Onset Supraventricular Tachycardia. J Am Soc Echocardiogr. 2018 Oct; 31(10): 1146 - 1150.
23. Рекомендации по проведению реанимационных мероприятий Европейского совета по реанимации (пересмотр 2015 г.). Под ред. Чл.-корр. РАН Мороза В.В. 3е издание, переработанное и дополненное. М.: НИИОР, НСР. 2016: 192 с.
24. Giglia T.M., Massicotte M. P., Tweddell JS. et al. Prevention and Treatment of Thrombosis in Pediatric and Congenital Heart Disease: A Scientific Statement From the American Heart Association. Circulation, 2013; 128: 2622 - 2703.
25. Campbell M, Silvia Ruiz Buitrago SR. BET 2: Ice water immersion, other vagal manoeuvres or adenosine for SVT in children. Emerg Med J. 2017 Jan; 34(1): 58 - 60.
26. Кручина Т.К., Новик Г.А., Егоров Д.Ф. Вагусные приемы для купирования приступов тахикардии у детей: оценка клинико-электрофизиологических факторов эффективности пробы Вальсальвы. Педиатрическая фармакология. 2015; 12(6): 639 - 644.
27. Kim JH, Jung JY, Lee SU et al. Delayed adenosine therapy is associated with the refractory supraventricular tachycardia in children. Am J Emerg Med. 2020 Nov; 38(11): 2291 - 2296.
28. Nathalie Oeffl, Lukas Schober, Patrick Faudon, Sabrina Schweintzger et al. Antiarrhythmic Drug Dosing in Children-Reviewof the Literature. Children. 2023; 10 (5), 847. doi.org/10.3390/children10050847.
29. Emaan Abbasi, Sakethram Saravu Vijayashankar, Ran D. Goldman. Management of acute supraventricular tachycardia in children. Canadian Family Physician. 2023; 69: 839-41. doi: 10.46747/cfp.6912839.
30. Fragakis N, Antoniadis AP, Korantzopoulos P et al. Sinus nodal response to adenosine relates to the severity of sinus node dysfunction. Europace 2012; 14: 859 - 864.
31. Lapage MJ, Bradley DJ, Dick M 2nd. Verapamil in infants: an exaggerated fear? Pediatr Cardiol. 2013 Oct; 34(7): 1532 - 1534.
32. Paul T, Bertram H,  , Hausdorf G. Supraventricular tachycardia in infants, children and adolescents: diagnosis, and pharmacological and interventional therapy. Paediatr Drugs. 2000. May-Jun; 2(3): 171 - 181.
, Hausdorf G. Supraventricular tachycardia in infants, children and adolescents: diagnosis, and pharmacological and interventional therapy. Paediatr Drugs. 2000. May-Jun; 2(3): 171 - 181.
33. Колбасова Е.В., Лукушкина Е.Ф., Егоров Д.Ф. и др. Тактика неотложной терапии при нарушениях ритма и проводимости сердца у детей. Клиническая и неотложная педиатрия. Новости, Мнения. Обучение. 2016: 1: 46 - 50.
34. Maghrabi K, Uzun O, Kirsh JA et al. Cardiovascular Collapse with Intravenous Amiodarone in Children: A Multi-Center Retrospective Cohort Study. Pediatr Cardiol. 2019 Jun; 40(5): 925 - 933.
35. Ramusovic S, ![]() , Meibohm B. et al. Pharmacokinetics of intravenous amiodarone in children. Arch Dis Child. 2013 Dec; 98(12): 989 - 93.
, Meibohm B. et al. Pharmacokinetics of intravenous amiodarone in children. Arch Dis Child. 2013 Dec; 98(12): 989 - 93.
36. Lane RD, Nguyen KT, Niemann JT, et al. Amiodarone for the emergency care of children. Pediatr Emerg Care. 2010 May; 26(5): 382 - 389.
37. Saul JP, Scott WA, Brown S. et al. Intravenous Amiodarone Pediatric Investigators. Intravenous amiodarone for incessant tachyarrhythmias in children: a randomized, double-blind, antiarrhythmic drug trial. Circulation. 2005 Nov 29; 112(22): 3470 - 3477.
38. Кручина Т.К., Васичкина Е.С., Новик Г.А., Егоров Д.Ф. Синдром Вольфа-Паркинсона-Уайта у детей: клиника, диагностика, лечение. Педиатрическая фармакология. 2011; 8 (5): 49 - 53.
39. Creo A, Anderson H, Cannon B. et al. Patterns of amiodarone-induced thyroid dysfunction in infants and children. Heart Rhythm. 2019 Sep; 16(9): 1436 - 1442.
40. Свинцова Л.И., Джаффарова О.Ю., Плотникова И.В. Прогнозирование эффективности антиаритмической терапии у детей. Российский врач-кардиологический журнал. 2019; 24(7): 75 - 82.
41. Furtak A,  , Kalicka-Kasperczyk A. et al. Amiodarone-induced thyroid dysfunction in the developmental period: prenatally, in childhood, and adolescence - case reports and a review of the literature. Endokrynol Pol. 2019; 70(5): 392 - 400.
, Kalicka-Kasperczyk A. et al. Amiodarone-induced thyroid dysfunction in the developmental period: prenatally, in childhood, and adolescence - case reports and a review of the literature. Endokrynol Pol. 2019; 70(5): 392 - 400.
42. Montenez S, Moniotte S, Robert A et al. Amiodarone-induced thyroid dysfunction in children: insights from the THYRAMIO study. Ther Adv Endocrinol Metab. 2021 Apr 24; 12: 20420188211001165.
43. Bolin EH, Lang SM, Tang X, Collins RT. Propranolol Versus Digoxin in the Neonate for Supraventricular Tachycardia (from the Pediatric Health Information System). Am J Cardiol. 2017 May 15; 119(10): 1605 - 1610.
44. Guerrier K, Shamszad P, Czosek RJ, et al. Variation in Antiarrhythmic Management of Infants Hospitalized with Supraventricular Tachycardia: A Multi-Institutional Analysis. Pediatr Cardiol. 2016 Jun; 37(5): 946 - 52.
45. Sanatani S, Potts JE, Reed JH et al. The study of antiarrhythmic medications in infancy (SAMIS): a multicenter, randomized controlled trial comparing the efficacy and safety of digoxin versus propranolol for prophylaxis of supraventricular tachycardia in infants. Circ Arrhythm Electrophysiol. 2012 Oct; 5(5): 984 - 91.
46. Ko JK, Ban JE, Kim YH, Park IS. Long-term efficacy of atenolol for atrioventricular reciprocating tachycardia in children less than 5 years old. Pediatr Cardiol. 2004 Mar-Apr; 25(2): 97 - 101.
47. Mehta AV, Subrahmanyam AB, Anand R. Long-term efficacy and safety of atenolol for supraventricular tachycardia in children. Pediatr Cardiol. 1996 Jul - Aug; 17(4): 231 - 6.
48. Janousek J, Paul T. Safety of oral propafenone in the treatment of arrhythmias in infants and children (European retrospective multicenter study). Working Group on Pediatric Arrhythmias and Electrophysiology of the Association of European Pediatric Cardiologists. Am J Cardiol. 1998 May 1; 81(9): 1121 - 4.
49. Tunca Sahin G, Ozturk E, Kasar T, et al. Sustained tachyarrhythmia in children younger than 1 year of age: Six year single-center experience. Pediatr Int. 2018 Feb; 60(2): 115 - 121.
50. Кручина Т.К., Ковальчук Т.С., Васичкина Е.С., Татарский Б.А. Опыт применения пропафенона у новорожденных и детей раннего возраста с нарушениями ритма сердца. Российский врач-кардиологический журнал. 2020; 25(7): 3462.
51. Knudson JD, Cannon BC, Kim JJ, Moffett BS. High-dose sotalol is safe and effective in neonates and infants with refractory supraventricular tachyarrhythmias. Pediatr Cardiol. 2011 Oct; 32(7): 896 - 903.
52. Saul JP, Ross B, Schaffer MS et al. Pediatric Sotalol Investigators. Pharmacokinetics and pharmacodynamics of sotalol in a pediatric population with supraventricular and ventricular tachyarrhythmia. Clin Pharmacol Ther. 2001 Mar; 9(3): 145 - 57.
53. ![]() , Elshoff JP, Meibohm B et al. Development of a safe and effective pediatric dosing regimen for sotalol based on population pharmacokinetics and pharmacodynamics in children with supraventricular tachycardia. J Am Coll Cardiol. 2005 Oct 4; 46(7): 1322 - 30.
, Elshoff JP, Meibohm B et al. Development of a safe and effective pediatric dosing regimen for sotalol based on population pharmacokinetics and pharmacodynamics in children with supraventricular tachycardia. J Am Coll Cardiol. 2005 Oct 4; 46(7): 1322 - 30.
54. Amrousy DE, Elshehaby W, Feky WE, Elshmaa NS. Safety and Efficacy of Prophylactic Amiodarone in Preventing Early Junctional Ectopic Tachycardia (JET) in Children After Cardiac Surgery and Determination of Its Risk Factor. Pediatr Cardiol. 2016 Apr; 37(4): 734 - 739.
55. Hill AC, Silka MJ, Bar-Cohen Y. A comparison of oral flecainide and amiodarone for the treatment of recurrent supraventricular tachycardia in children. Pacing Clin Electrophysiol. 2019 Jun; 42(6): 670 - 677.
56. Ricardo Munoz, Eduardo M. da Cruz, Carol G. Vetterly, David S. Cooper, Donald Berry. Handbook of Pediatric Cardiovascular Drugs. Second Edition Springer-Verlag London 2014. - 825 p.
57. Akdeniz C., Ergul Ya, Kiplapinar N, Tuzcu V. Catheter ablation of drug resistant supraventricular tachycardia in neonates and infants. C.Cardiology J. 2013; 20(3): 241 - 246.
58. Blaufox, A.D. Cateter Ablation of Tachyarrhythmias in Small Children. Indian Pacing and Electrophysiology Journal. 2005; 5: 51 - 62.
59. Philip SJ, Kanter RJ, Abrams D. et al. PACES/HRS expert consensus statement on the use of catheter ablation in children and patients with congenital heart disease: Developed in partnership with the Pediatric and Congenital Electrophysiology Society (PACES) and the Heart Rhythm Society (HRS). Endorsed by the governing bodies of PACES, HRS, the American Academy of Pediatrics (AAP), the American Heart Association (AHA), and the Association for European Pediatric and Congenital Cardiology (AEPC). Heart Rhythm. 2016 Jun; 13(6): 251 - 289.
60. Svintsova L.I., Popov S.V., Kovalev I.A. Radiofrequency ablation in small children younger than 1 year of age: single-center experience. Pediatric Cardiology. 2013; 34(6): 1321 - 1329.
61. Клинические рекомендации по проведению электрофизиологических исследований, катетерной абляции и применению имплантируемых антиаритмических устройств. Всероссийское научное общество специалистов по клинической электрофизиологии, аритмологии и кардиостимуляции (ВНОА). Новая редакция - 2017.
62. Свинцова Л.И., Джаффарова О.Ю., Плотникова И.В. Осложнения радиочастотной аблации аритмий у детей дошкольного возраста. Педиатрия. 2018; 97(3): 61 - 68.
63. Марцинкевич Г.И., Соколов А.А., Ковалев И.А. и др. Электромеханическое сопряжение миокарда в норме и у детей с синдромом Вольфа-Паркинсона-Уайта. Вестник аритмологии. 2004; 35: 38 - 44.
64. Хамнагадаев И.А., Школьникова М.А., Коков Л.С. и др. Диастолическая функция правого желудочка у больных с манифестным синдромом и электрокардиографическим феноменом Вольфа-Паркинсона-Уайта. Вестник аритмологии. 2012; 68: 21 - 27.
65. Кручина Т.К., Лукушкина Е.Ф., Колбасова Е.В. Жизнеопасные состояния у детей с суправентрикулярными тахикардиями: оценка факторов риска и профилактика. Вопросы диагностики в педиатрии. 2011; 3. (6): 40 - 44.
66. Eman Abdelghani. Clifford L. Cua. Jean Giver. Vilmarie Rodriguez. Thrombosis Prevention and Anticoagulation Management in the Pediatric Patient with Congenital Heart Disease. Cardiology and Therapy. 2021; Volume10: 325 - 348
67. Recommendations for competitive sports participation in athletes with cardiovascular disease. A consensus document from the Study Group of Sports Cardiology of the Working Group of Cardiac Reabilitation and Exercise Physiology and the Working Group of Myocardial and Pericardial Disease of the European Society of Cardiology. Pelliccia A, Fagard R,  , et al. European Heart Journal. 2005; 26: 1422 - 1445.
, et al. European Heart Journal. 2005; 26: 1422 - 1445.
68. Recommendations for participation in competitive sport in adolescent and adult athletes with Congenital Heart Disease (CHD): position statement of the Sports Cardiology & Exercise Section of the European Association of Preventive Cardiology (EAPC), the European Society of Cardiology (ESC) Working Group on Adult Congenital Heart Disease and the Sports Cardiology, Physical Activity and Prevention Working Group of the Association for European Paediatric and Congenital Cardiology (AEPC). Werner Budts, Guido E Pieles, Jolien W Roos-Hesselink et al. Eur Heart J. 2020 Nov 14; 41(43): 4191 - 4199.
69. Maron BJ, Zipes DP, Kovacs RJ. Eligibility and Disqualification Recommendations for Competitive Athletes With Cardiovascular Abnormalities: Preamble, Principles, and General Considerations. J Am Coll Cardiol. 2015 Dec 1; 66 (21): 2343 - 2349.
Приложение А1
СОСТАВ
РАБОЧЕЙ ГРУППЫ ПО РАЗРАБОТКЕ И ПЕРЕСМОТРУ
КЛИНИЧЕСКИХ РЕКОМЕНДАЦИЙ
1. Кручина Т.К., д.м.н., член Ассоциации детских кардиологов России (руководитель рабочей группы)
2. Колбасова Е.В., к.м.н., член Ассоциации детских кардиологов России (отв. секретарь рабочей группы)
3. Березницкая В.В., к.м.н., член Ассоциации детских кардиологов России
4. Иваницкий Э.А., д.м.н., член "Всероссийское научное общество специалистов по клинической электрофизиологии, аритмологии и кардиостимуляции"
5. Кандинский М.Л., к.м.н., член член "Всероссийское научное общество специалистов по клинической электрофизиологии, аритмологии и кардиостимуляции"
6. Ковалев И.А., д.м.н., профессор, Президент Ассоциации детских кардиологов России
7. Кравцова Л.А., к.м.н., член Ассоциации детских кардиологов России
8. Свинцова Л.И., д.м.н., член Ассоциации детских кардиологов России
9. Татарский Б.А., д.м.н, член "Всероссийское научное общество специалистов по клинической электрофизиологии, аритмологии и кардиостимуляции"
10. Термосесов С.А., член Ассоциации сердечно-сосудистых хирургов России, член "Всероссийского научное общество специалистов по клинической электрофизиологии, аритмологии и кардиостимуляции"
11. Хамнагадаев И.А., к.м.н., член Ассоциации сердечно-сосудистых хирургов России, член "Всероссийского научное общество специалистов по клинической электрофизиологии, аритмологии и кардиостимуляции"
12. Школьникова М.А., д.м.н., профессор, Почетный президент Ассоциации детских кардиологов России
Авторы подтверждают отсутствие финансовой поддержки/конфликта интересов, который необходимо обнародовать.
Приложение А2
МЕТОДОЛОГИЯ РАЗРАБОТКИ КЛИНИЧЕСКИХ РЕКОМЕНДАЦИЙ
Целевая аудитория данных клинических рекомендаций:
1. Врачи-педиатры
2. Врачи-детские кардиологи
3. Врачи-сердечно-сосудистые хирурги
4. Врачи общей практики (семейные врачи)
Таблица 1. Шкала оценки уровней достоверности доказательств (УДД) для методов диагностики (диагностических вмешательств)
УДД
Расшифровка
1
Систематические обзоры исследований с контролем референсным методом или систематический обзор рандомизированных клинических исследований с применением мета-анализа
2
Отдельные исследования с контролем референсным методом или отдельные рандомизированные клинические исследования и систематические обзоры исследований любого дизайна, за исключением рандомизированных клинических исследований, с применением мета-анализа
3
Исследования без последовательного контроля референсным методом или исследования с референсным методом, не являющимся независимым от исследуемого метода или нерандомизированные сравнительные исследования, в том числе когортные исследования
4
Несравнительные исследования, описание клинического случая
5
Имеется лишь обоснование механизма действия или мнение экспертов
Таблица 2. Шкала оценки уровней достоверности доказательств (УДД) для методов профилактики, лечения и реабилитации (профилактических, лечебных, реабилитационных вмешательств)
УДД
Расшифровка
1
Систематический обзор РКИ с применением мета-анализа
2
Отдельные РКИ и систематические обзоры исследований любого дизайна, за исключением РКИ, с применением мета-анализа
3
Нерандомизированные сравнительные исследования, в т.ч. когортные исследования
4
Несравнительные исследования, описание клинического случая или серии случаев, исследования "случай-контроль"
5
Имеется лишь обоснование механизма действия вмешательства (доклинические исследования) или мнение экспертов
Таблица 3. Шкала оценки уровней убедительности рекомендаций (УУР) для методов профилактики, диагностики, лечения и реабилитации (профилактических, диагностических, лечебных, реабилитационных вмешательств)
УУР
Расшифровка
A
Сильная рекомендация (все рассматриваемые критерии эффективности (исходы) являются важными, все исследования имеют высокое или удовлетворительное методологическое качество, их выводы по интересующим исходам являются согласованными)
B
Условная рекомендация (не все рассматриваемые критерии эффективности (исходы) являются важными, не все исследования имеют высокое или удовлетворительное методологическое качество и/или их выводы по интересующим исходам не являются согласованными)
C
Слабая рекомендация (отсутствие доказательств надлежащего качества (все рассматриваемые критерии эффективности (исходы) являются неважными, все исследования имеют низкое методологическое качество и их выводы по интересующим исходам не являются согласованными)
Порядок обновления клинических рекомендаций.
Механизм обновления клинических рекомендаций предусматривает их систематическую актуализацию - не реже чем один раз в три года, а также при появлении новых данных с позиции доказательной медицины по вопросам диагностики, лечения, профилактики и реабилитации конкретных заболеваний, наличии обоснованных дополнений/замечаний к ранее утвержденным КР, но не чаще 1 раза в 6 месяцев.
Приложение А3
СПРАВОЧНЫЕ МАТЕРИАЛЫ,
ВКЛЮЧАЯ СООТВЕТСТВИЕ ПОКАЗАНИЙ К ПРИМЕНЕНИЮ
И ПРОТИВОПОКАЗАНИЙ, СПОСОБОВ ПРИМЕНЕНИЯ И ДОЗ ЛЕКАРСТВЕННЫХ
ПРЕПАРАТОВ, ИНСТРУКЦИИ ПО ПРИМЕНЕНИЮ
ЛЕКАРСТВЕННОГО ПРЕПАРАТА
1. Приказ Министерства здравоохранения Российской Федерации от 28.02.2019 N 103н "Об утверждении порядка и сроков разработки клинических рекомендаций, их пересмотра, типовой формы клинических рекомендаций и требований к их структуре, составу и научной обоснованности, включаемой в клинические рекомендации информации".
2. Приказ Министерства здравоохранения Российской Федерации от 25 октября 2012 г. N 440н "Об утверждении Порядка оказания медицинской помощи по профилю "детская кардиология".
3. Приказ Министерства здравоохранения Российской Федерации от 10 мая 2017 г. N 203н "Об утверждении критериев оценки качества медицинской помощи".
4. Методические рекомендации по оценке достоверности доказательств и убедительности рекомендаций. ФГБУ ЦЭККМП Минздрава России, 2018.
5. Распоряжение Правительства РФ от 31 декабря 2018 г. N 3053-р "Об утверждении перечня медицинских изделий, имплантируемых в организм человека при оказании медицинской помощи в рамках программы государственных гарантий бесплатного оказания гражданам медицинской помощи, а также перечня медицинских изделий, отпускаемых по рецептам на медицинские изделия при предоставлении набора социальных услуг".
6. Распоряжение Правительства РФ от 12 октября 2019 г. N 2406-р "Об утверждении перечня жизненно необходимых и важнейших лекарственных препаратов, а также перечней лекарственных препаратов для медицинского применения и минимального ассортимента лекарственных препаратов, необходимых для оказания медицинской помощи".
Приложение А3.3
АНТИАРИТМИЧЕСКИЕ ПРЕПАРАТЫ,
ЗАРЕГИСТРИРОВАННЫЕ В РОССИЙСКОЙ ФЕДЕРАЦИИ
ААП
Суточная доза, рассчитанная на массу тела
Параметры ЭКГ, требующие внимания при подборе дозы препарата
Возможные побочные эффекты
#Пропранолол** (код АТХ C07BA05)
1 - 3 мг/кг/сутки в 3 - 4 приема [9]
Брадикардия, дисфункция СУ, удлинение PQ-интервала
Синусовая брадикардия, АВ-блокада, гипотензия, усугубление СН, бронхообструктивный синдром
#Атенолол** (код АТХ C07AB03)
0,3 - 1,3 мг/кг/сутки в 1 прием [9 - 11, 44, 45].
Брадикардия, дисфункция СУ, удлинение PQ-интервала
Синусовая брадикардия, АВ-блокада, гипотензия, усугубление СН
#Верапамил** (код АТХ C08DA01)
4 - 8 мг/кг/сутки в 3 приема [9 - 11, 18].
Брадикардия, дисфункция СУ, удлинение PQ-интервала
Синусовая брадикардия, АВ-блокада, снижение сократимости миокарда, гипотензия, отеки
#Пропафенон** (код АТХ C01BC03)
5 - 15 мг/кг/сутки в 3 приема [9 - 11, 18, 46, 48].
Расширение комплекса QRS более 25%, брадикардия, удлинение PQ более 25%
Синусовая брадикардия, АВ-блокада, БНПГ, мономорфная желудочковая тахикардия, фибрилляция желудочков, усугубление СН, повышение порогов электрокардиостимуляции и дефибрилляции сердца
#Соталол** (код АТХ C07AA07)
2 - 8 мг/кг/сутки в 2 приема [9 - 11, 18, 49 - 51].
удлинение интервала QTс более 500 мс, брадикардия, удлинение PQ-интервала
гипотензия, усугубление СН, веретенообразная желудочковая тахикардия
#Амиодарон** (код АТХ C01BD01)
насыщение: 10 мг/кг/сутки в 2 приема в течение 10 дней; поддерживающая: 5 мг/кг/сутки в один прием [9 - 11, 18, 35].
удлинение интервала QTс более 500 мс, удлинение PQ-интервала
Синусовая брадикардия, АВ-блокада, веретенообразная желудочковая тахикардия, нарушение функции щитовидной железы, фотосенсибилизация, интерстициальная пневмония или альвеолит, увеит, отложение липофусцина в эпителии роговицы
Приложение А3.2
РЕКОМЕНДАЦИИ
ПО УЧАСТИЮ В СОРЕВНОВАНИЯХ ДЛЯ СПОРТСМЕНОВ С НАРУШЕНИЯМИ
РИТМА СЕРДЦА И АРИТМОГЕННЫМИ ЗАБОЛЕВАНИЯМИ [67 - 69]
Заболевание или патологические состояние
Критерии принятия решения
Рекомендации по занятию спортом (разрешается при наличии соответствующих критериев)
Пароксизмальная СВТ (АВ-узловая реципрокная тахикардия, АВ-реципрокная тахикардия с участием ДАВС)
а) через 3 месяца после успешной РЧА при отсутствии заболеваний сердца
б) если РЧА не выполнялась, отсутствуют синдром Вольфа-Паркинсона-Уайта, заболевания сердца, эпизоды СВТ спорадические, без гемодинамических нарушений и связи с физической нагрузкой
а) все виды спорта
б) все виды спорта, за исключением видов с высоким риском развития синкопальных состояний <*>
Феномен Вольфа-Паркинсона-Уайта
После успешной РЧА и при отсутствии заболеваний сердца
все виды спорта
Фибрилляция предсердий (пароксизмальная или постоянная форма)
а) после пароксизма ФП: если нет заболеваний сердца, нет синдрома Вольфа-Паркинсона-Уайта и стабильный синусовый ритм в течение более 3 месяцев
б) постоянная форма ФП
а) все виды спорта
б) не рекомендуется
Трепетание предсердий
После успешной РЧА, при отсутствии симптомов более 3 месяцев, при исключении заболеваний сердца
все виды спорта
--------------------------------
Примечание. <*> - виды спорта с высоким риском развития синкопальных состояний (автогонки, ныряние, конный спорт, мотоспорт, бобслей, санный спорт, альпинизм, водные лыжи, виндсерфинг, горнолыжный спорт, сноуборд, велоспорт, триатлон).
Приложение Б
АЛГОРИТМЫ ДЕЙСТВИЙ ВРАЧА
Приложение Б1
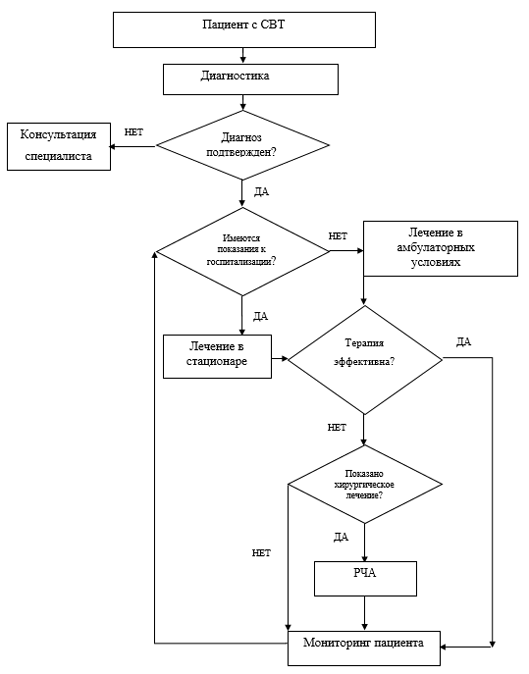
Приложение Б2
ДИФФЕРЕНЦИАЛЬНАЯ ЭКГ-ДИАГНОСТИКА ВАРИАНТОВ СВТ
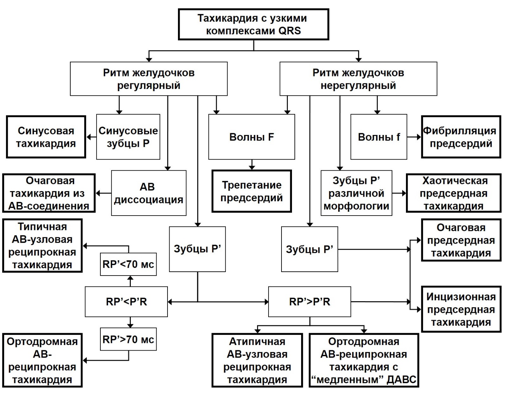
Приложение В
ИНФОРМАЦИЯ ДЛЯ ПАЦИЕНТА
Суправентрикулярная (наджелудочковая) тахикардия (СВТ) - это форма аритмии, вызванная врожденными или приобретенными причинами и проявляющаяся возникновением частого ритма, источник которого находится не в синусовом узле, как это должно быть в норме. Во время приступа СВТ, который может продлиться несколько часов, сердце бьется быстро, пульс часто "не сосчитать". Частота сердечных сокращений достигает 180 - 250 ударов в минуту, а иногда и больше. В здоровом сердце каждое сокращение инициируется электрическим импульсом из синусового узла (водителя ритма сердца), расположенного в правом предсердии. Затем импульс проходит во второй узел (атриовентрикулярный), который проводит импульс в желудочки. При СВТ синусовый узел не контролирует сердечные сокращения: из-за наличия патологических проводящих путей, по которым электрический импульс постоянно циркулирует, или из-за образования несинусового очага электрической активности, который "перебивает" нормальный источник ритма, не дает ему задавать нормальный ритм.
СВТ чаще впервые появляется у детей первого года жизни или у подростков, хотя это заболевание возможно в любом возрасте. В некоторых случаях причина СВТ - врожденное нарушение проводящей системы сердца. Существуют две основные формы СВТ: пароксизмальная и непароксизмальная. При пароксизмальной форме приступ тахикардии начинается и заканчивается внезапно. Приступы, как правило, начинаются без видимых причин, но их может спровоцировать физическая нагрузка, возбуждение, температура, кофеин и алкоголь. Ребенок ощущает приступ в виде внезапно начавшегося сильного сердцебиения, "дрожания" грудной клетки, через некоторое время, если частота сердечных сокращений высокая (180 в мин. и выше), возникает слабость, головокружение, "холодный пот". Однако, при невысокой частоте сердечных сокращений (140 - 150 в мин.), ребенок может нормально переносить приступ, ощущая только лишь ускорение работы сердца.
Осложнением СВТ является сердечная недостаточность (утомляемость, одышка, снижение аппетита вплоть до отказа от приема пищи (у детей первого года жизни)). В некоторых случаях длительный приступ СВТ может понизить давление до угрожающего уровня.
Если врач предполагает СВТ, то пациента направят на ЭКГ-исследования (обычную ЭКГ и Холтеровское мониторирование ЭКГ). Возможны дополнительные исследования для выявления тахикардии, например, чреспищеводное электрофизиологическое исследование сердца. Необходимо зарегистрировать приступ тахикардии, только после этого врач сможет разработать план лечения. Поэтому при возникновении приступа необходимо сразу обратиться за медицинской помощью и снять ЭКГ (медицинский кабинет в школе, любое медицинское учреждение рядом с вами, вызов скорой медицинской помощи). Пациенту с подозрением на СВТ проводят также ЭХОКГ-исследование для диагностики строения сердца, его функции, его размеров, наличия или отсутствия пороков сердца, признаков заболеваний сердца, а также влияния аритмии на его работу.
При продолжительных и тяжелых приступах СВТ требуется срочное стационарное лечение. В больнице пациенту купируют приступ и восстановят нормальный ритм путем введения лекарств или другими методами. Для купирования приступа, как правило, детям требуется госпитализация в отделение реанимации и интенсивной терапии, чтобы контролировать его состояние, постоянно мониторировать ЭКГ, артериальное давление, насыщение крови кислородом и купировать приступ, опираясь на эти параметры. В некоторых случаях проводят электроимпульсную терапию, чтобы восстановить нормальный сердечный ритм.
Пациенты с короткими и редкими приступами СВТ могут сами, без лекарств, прервать приступ и восстановить нормальный ритм. Это называется "стимуляция блуждающего нерва". Детям старшего возраста с этой целью можно сделать глубокий вдох и натужиться, увеличив тем самым давление в грудной клетке и сделав ритм более редким. Однако, только врач, в соответствии с возрастом и заболеванием ребенка, может профессионально рассказать об этих методах стимуляции. Тяжелые приступы СВТ можно лечить продолжительным курсом антиаритмических лекарственных средств. Также для лечения СВТ применяют радиочастотную абляцию, которую выполняют во время электрофизиологических исследований. При этом разрушают патологические проводящие пути и очаги патологической электрической активности. В большинстве случаев СВТ не влияет на продолжительность жизни.
Приложение Г1 - ГN
ШКАЛЫ ОЦЕНКИ, ВОПРОСНИКИ И ДРУГИЕ ОЦЕНОЧНЫЕ ИНСТРУМЕНТЫ
СОСТОЯНИЯ ПАЦИЕНТА, ПРИВЕДЕННЫЕ В КЛИНИЧЕСКИХ РЕКОМЕНДАЦИЯХ
В рамках данных клинических рекомендаций не предусмотрены.
