"Клинические рекомендации "Трансплантация почки, наличие трансплантированной почки, отмирание и отторжение трансплантата почки"
МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ
КЛИНИЧЕСКИЕ РЕКОМЕНДАЦИИ
ТРАНСПЛАНТАЦИЯ ПОЧКИ, НАЛИЧИЕ ТРАНСПЛАНТИРОВАННОЙ ПОЧКИ,
ОТМИРАНИЕ И ОТТОРЖЕНИЕ ТРАНСПЛАНТАТА ПОЧКИ
Кодирование по Международной статистической классификации болезней и проблем, связанных со здоровьем: Z94.0, T86.1
Год утверждения (частота пересмотра): 2025 Пересмотр не позднее: 2027
ID: 934_1
Возрастная категория: Взрослые, Дети
Специальность:
Разработчик клинической рекомендации Российское трансплантологическое общество
Одобрено Научно-практическим Советом Минздрава России
Список сокращений
HLA - (англ., human leukocyte antigen, лейкоцитарные антигены человека) главный комплекс гистосовместимости человека
IgG - иммуноглобулин класса G
IgM - иммуноглобулин класса M
mTOR - мишень рапамицина млекопитающих
АЛТ - аланинаминотрансфераза
анти-HLA - антитела к антигенам системы HLA
АПФ - ангиотензинпревращающий фермент
АСТ - аспартатаминотрансфераза
ВИЧ - вирус иммунодефицита человека
ГГТ - глутамилтранспептидаза
ДНК - дезоксирибонуклеиновая кислота
ЗПА - заболевание периферических артерий
ЗПТ - заместительная почечная терапия
ИЛ-2 - интерлейкин 2
ИБС - ишемическая болезнь сердца
ИМТ - индекс массы тела
ИМФДГ - инозинмонофосфатдегидрогеназа
ИФ - интерстициальный фиброз
КА - канальцевая атрофия
КТ - компьютерная томография
НМУ - номенклатура медицинских услуг
ОФТ - отсроченная функция трансплантата
ПЦР - полимеразная цепная реакция
РКИ - рандомизированное клиническое исследование
СКФ - скорость клубочковой фильтрации
ТИА - транзиторная ишемическая атака
ТП - трансплантация почки (НМУ: пересадка почки).
УЗИ - ультразвуковое исследование
ХБП - хроническая болезнь почек
ЦВД - центральное венозное давление
ЭКГ - электрокардиография (НМУ: регистрация электрокардиограммы)
ЭхоКГ - эхокардиография
Термины и определения
Аллотрансплантат - донорский орган, полученный от человека, не являющимся однояйцевым близнецом для, который был перемещен в организм реципиента посредством хирургической операции.
Гемодиализ - метод, основанный на принципе диффузионного и фильтрационного переноса через полупроницаемую мембрану низкомолекулярных субстанций и жидкости между циркулирующей экстракорпорально кровью и диализирующим раствором.
Живой (прижизненный) родственный донор - лицо в возрасте 18 лет и старше, дееспособный человек, выразивший согласие предоставить и (или) предоставивший при жизни свой донорский орган в целях родственной трансплантации.
Заместительная почечная терапия - комплекс специализированных методов замещения выделительной функции почек. К ним относят диализ (гемо- и перитонеальный) и трансплантацию почки. Последний метод позволяет восстановить весь спектр утраченных функций почек.
Острое повреждение почек - патологическое состояние, развивающееся в результате непосредственного острого воздействия ренальных и/или экстраренальных повреждающих факторов, продолжающееся до 7-ми суток и характеризующееся быстрым (часы-дни) развитием признаков повреждения или дисфункции почек различной степени выраженности. Поскольку острое повреждение почечной паренхимы может быть обусловлено не только ренальными (почечными), но также преренальными и постренальными факторами, англоязычному термину "acute kidney injury" соответствует перевод "острое повреждение почек". Термин "острое почечное повреждение", который возник по аналогии с термином "острая почечная недостаточность", не рекомендуется к использованию.
Отторжение трансплантированной почки - патологический процесс, при котором иммунная система реципиента распознает почечный трансплантат как чужеродный объект и активируется система антителоопосредованного (гуморального) и/или клеточного воспалительного ответа, что может привести к выраженной дисфункции трансплантата.
Перитонеальный диализ - метод заместительной почечной терапии, основанный на принципе диффузионного обмена, фильтрационного и конвекционного переноса через "перитонеальную мембрану" (брюшину) низко- и среднемолекулярных и белковых субстанций, а также жидкости из крови в диализирующий раствор, находящийся в полости брюшины.
Посмертный (трупный) донор органов - человек, признанный умершим в установленном порядке (биологическая смерть или смерть головного мозга) и ставший источником органов (объектов трансплантации).
Потенциальный реципиент почки - пациент с 5 стадией хронической болезни почек, не имеющий противопоказаний к трансплантации почки и включенный в лист ожидания.
Реципиент трансплантированной почки - это пациент, перенесший операцию трансплантации почки, в отношении которого проводится комплекс лечебных мероприятий, направленных на предотвращение дисфункции почечного трансплантата, обусловленное такими патологическими процессами, как отторжение, возвратная патология, инфекционное поражение, нефротоксический эффект лекарственных препаратов и другие.
Терминальная почечная недостаточность (ТПН) - это патологическое состояние, характеризующееся величиной СКФ менее 15 мл/мин/1,73 м2, что соответствует 5-й стадии ХБП.
Трансплантация почки - медицинская технология, направленная на замещение необратимо утраченной функции почек и включающая к себя как неотъемлемый этап хирургическое вмешательство, заключающийся перемещение почки, полученной от другого человека (донора) в организм реципиента с восстановлением в нем кровоснабжения и оттока мочи (НМУ: пересадка почки).
Трансплантация почки - это хирургическая операция: метод заместительной почечной терапии, заключающийся в пересадке человеку почки, полученной от другого человека.
Хроническая болезнь почек - повреждение почек либо снижение их функции в течение 3 месяцев и более вследствие действия различных этиологических факторов, анатомической основой которого является процесс замещения нормальных анатомических структур фиброзом, приводящим к его дисфункции. Заболевание классифицируется на 5 стадий, которые различаются по тактике ведения пациента и риску развития терминальной почечной недостаточности и сердечно-сосудистых осложнений.
1. Краткая информация по заболеванию или состоянию (группы заболеваний или состояний)
В данных рекомендациях представлено описание технологий оказания медицинской помощи, предполагающей проведение обследований с целью выбора тактики ведения больных с хронической болезнью почек в терминальной стадии, определения показаний для трансплантации почки, порядка для включения больных в лист ожидания, а также стабилизации клинического состояния и оценки возможности восстановления/реабилитации больного после проведения операции трансплантации почки. Глобальная цель трансплантации почки заключается в максимально длительном удовлетворительном функционировании почечного аллотрансплантата и максимальной продолжительности жизни пациента, страдающего от терминальной почечной недостаточности, в состоянии, свободном от диализных методов терапии.
Причины утраты функции почечного трансплантата достаточно разнообразны. В раннем посттрансплантационном периоде, они связаны в первую очередь с хирургическими осложнениями виде тяжелых ишемических и реперфузионных повреждений, тромбозами и стенозами сосудов трансплантата, раневыми инфекциями, урологическими осложнениями трансплантированной почки. Другой важной причиной потерь является иммунологическая реакция на чужеродные антигены, проявляющаяся в виде сверхострой (антителоопосредованной), ускоренной, острой клеточной и хронической антитело-опосредованной реакции отторжения. В отдаленном периоде значимую долю в причинах потерь почечных с трансплантатов начинают составлять нефротоксичность ингибиторов кальциневрина, возвратная почечная патология и смерть пациентов с функционирующим трансплантатом.
Настоящие рекомендации, предназначены для врачей-хирургов (трансплантологов), врачей-нефрологов и врачей широкого профиля.
1.1 Определение заболевания или состояния (группы заболеваний или состояний)
Трансплантация почки - медицинская технология, направленная на замещение необратимо утраченной функции почек и включающая к себе как неотъемлемый этап хирургическое вмешательство, заключающееся в перемещение почки, полученной от другого человека (донора), в организм реципиента с восстановлением в нем кровоснабжения и оттока мочи.
Реципиент почки - это пациент, перенесший операцию трансплантации почки, в отношении которого проводится комплекс лечебных мероприятий, направленных на предотвращение дисфункции почечного трансплантата, обусловленной такими патологическими процессами, как отторжение, возвратная патология, инфекционное поражение, нефротоксический эффект лекарственных препаратов и другие.
Отторжение трансплантированной почки - патологический процесс, при котором иммунная система реципиента распознает почечный трансплантат как чужеродный объект, активируется система антителоопосредованного (гуморального) и/или клеточного воспалительного ответа, что может привести к выраженной дисфункции трансплантата.
Категория возрастная: взрослые, дети;
Пол: любой;
Стадия: C5, терминальная (по классификации и стратификации стадий ХБП по уровню СКФ);
Осложнения: отмирание и отторжение трансплантата почки;
Вид медицинской помощи: ВМП, ОМС;
Условия оказания медицинской помощи: амбулаторно, стационарно;
Форма оказания медицинской помощи: плановая, неотложная, экстренная.
1.2 Этиология и патогенез заболевания или состояния (группы заболеваний или состояний)
Показанием к трансплантации почки является 5 стадия хронической болезни почек (ХБП), требующая проведения заместительной почечной терапии. Само понятие ХБП является наднозологическим [1, 2], но ХБП не является формальным объединением хронических повреждений почек различной природы. Этиология и патогенез ХБП подробно изложены в клинических рекомендациях по ХБП [3].
Несмотря на то, что еще можно встретить попытки дать систематизированную оценку этиологическим причинам ХБП (чаще всего причинами терминальной ХБП являются гломерулонефрит/гломерулосклероз (46,1%), сахарный диабет (12%), поликистоз почек (10%), пиелонефрит (9,4%), а также сосудистые заболевания почек (1,2%), нефропатии неизвестной этиологии (3%) и другие причины болезни почек (13,3%), [4]), на сегодняшний день понятно, что данное состояние является полиэтиологичным, а основное значение должно придаваться оценке факторов риска развития и прогрессирования хронического патологического процесса в почечной ткани. Только при учете таких факторов, оценке их значимости и модифицируемости можно эффективно осуществлять меры первичной и вторичной профилактики хронических заболеваний почек (см. табл. 1) [5 - 16].
Таблица 1. Основные факторы риска развития ХБП
Немодифицируемые
Модифицируемые
Пожилой возраст
Исходно низкое число нефронов (низкая масса тела при рождении)
Расовые и этнические особенности
Наследственные факторы (в том числе семейный анамнез по ХБП)
Перенесенное острое повреждение почек
Сахарный диабет
Артериальная гипертензия
Дислипопротеидемия
Табакокурение
Ожирение/метаболический синдром
Неалкогольная жировая болезнь печени
Гиперурикемия
Аутоиммунные болезни
Хроническое воспаление/системные инфекции
Инфекции и конкременты мочевых путей
Обструкция нижних мочевых путей
Лекарственная токсичность
Высокое потребление белка
Беременность
Этиологией наличия трансплантированной почки, является проведенное хирургическое вмешательство по ее перемещению из организма донора в организм реципиента, целью которой является обеспечение одного из вариантов заместительной почечной терапии. Больной, перенесший операцию по трансплантации почки называется реципиентом почки.
В свою очередь, отторжение почечного трансплантата - это патофизиологический процесс реакции врожденного и приобретенного иммунитета в организме реципиента в ответ на появление донорских аллогенов. В реакции отторжения принимают участие клетки иммунной системы, а также иммунологически активные молекулы: иммуноглобулины (антитела) и цитокины. Итогом взаимодействия становится распознавание антигенной чужеродности трансплантата и его деструкция. Отторжение является одним из значимых факторов, определяющих прогноз после трансплантации почки. Являясь проявлением защитной реакции организма реципиента против чужеродных клеток, реакция отторжения включает механизмы врожденного, клеточного и антителоопосредованного гуморального иммунного ответа. Процесс отторжения реализуется через T-клеточную (реакция гиперчувствительности IV типа) или антителоопосредованную цитотоксичность (реакция гиперчувствительность II типа).
В зависимости от патогенеза отторжение почечного трансплантата можно разделить по следующим категориям [17, 18]:
Сверхострое отторжение: развивается немедленно - в течение часа после восстановления кровообращения, и причиной его являются предсуществующие антитела к антигенам групп крови (AB0), главному комплексу гистосовместимости (HLA). Патогенез сверхострого отторжения включает образование комплексов "антиген-антитело" на эндотелии сосудов трансплантата, что ведет к повреждению эндотелиальных клеток, нарушению проницаемости сосудов, изменению реологических показателей, появлению диссеминированного тромбоза микрососудистого русла трансплантата. В настоящее время встречается редко из-за доступности высокочувствительных тестов на перекрестную совместимость, проводимых перед трансплантацией.
Острое отторжение: может произойти в любое время после трансплантации, обычно в течение нескольких дней или недель после трансплантации.
1) Антитело-опосредованное отторжение вследствие повреждения эндотелия трансплантата циркулирующими донор-специфическими аллоантителами. Активированные T-лимфоциты могут стимулировать B-лимфоциты, способствуя их активации, пролиферации и дифференциации в плазмоциты, продуцирующие антитела. Гуморальное (или антитело-опосредованное) отторжение в первую очередь обусловлено действием антител реципиента против антигенов эндотелия сосудов донорского органа. Диагностируется по морфологическим признакам антитело-опосредованного повреждения почки, таких как микрососудистое воспаление клубочков (гломерулит) или перитубулярных капилляров (перитубулярный капиллярит) в совокупности с отложением C4d компонента комплемента.
2) Острое T-клеточное отторжение является реакцией гиперчувствительности замедленного типа (IV тип реакции), обусловлено влиянием активированных T-лимфоцитов, характеризуется лимфоцитарной инфильтрацией канальцев, интерстиция и иногда интимы артерий. Признаки отторжения проявляются не ранее 24 - 48 часов после трансплантации, чаще всего - в первые 3 - 6 месяцев после трансплантации почки.
Хроническое отторжение: обычно развивается в сроки более 3 месяцев после трансплантации. Механизм его не полностью ясен, по-видимому, хроническое отторжение является следствием активации как специфического клеточного, так и гуморального иммунитета в ответ на презентацию АПК донорских аллоантигенов.
Смешанное: сочетание признаков острого отторжения, которое накладываются на хроническое отторжение.
Так как при трансплантации почки в подавляющем большинстве случаев орган получен от донора, имеющего отличный от реципиента генотип, процесс отторжения начинается с момента реперфузии органа и продолжается на протяжении всего срока его нахождения в организме реципиента. В связи с этим пациенты, перенесшие операцию по трансплантации почки, получают постоянную поддерживающую иммуносупрессивную терапию, направленную на замедление процессов иммунологического повреждения донорского органа.
1.3 Эпидемиология заболевания или состояния (группы заболеваний или состояний)
Согласно статистике Всемирной организации здравоохранения, в 2010 году заместительную почечную терапию получали порядка 2,6 млн. человек [19], а к 2030 году это число, по оценкам экспертов, увеличится до 5,4 млн. В 2020 году трансплантация почки выполнялась в 93 странах мира, а общее количество операций составило 81005 операций (10,4 операций на 1 млн. населения) [20].
По данными отчета Общероссийского Регистра заместительной почечной терапии Российского диализного общества [21] обеспеченность заместительной почечной терапией в 2020 году в России составила 414,2 больных/млн., общее количество пациентов, получавших терапию диализом на 31.12.2020 г., составило 50563 человек (83,5% от числа получавших ЗПТ в целом), а 9984 (68,3 человек/млн.) человек жили с функционирующим почечным трансплантатом. Согласно XV сообщению регистра Российского трансплантологического общества в 2023 году в России было выполнено 1817 (12,4 операций на 1 млн. населения) трансплантации почки. По сравнению с 2022 г. число трансплантаций почки увеличилось на 16,3% (+255). Число трансплантаций почки от посмертного донора в 2022 г. составило 1620. Число трансплантаций почки от живого родственного донора составило 197. В 2022 г. 8 центров трансплантации почки выполнили более 50 операций за год - это ФГБУ "Национальный медицинский исследовательский центр трансплантологии и искусственных органов им. акад. В.И. Шумакова" МЗ РФ (359), ГБУЗ г. Москвы "Научно-исследовательский институт скорой помощи им. Н.В. Склифосовского Департамента здравоохранения города Москвы", Москва (238), ГБУЗ г. Москвы "Городская клиническая больница им. С.П. Боткина ДЗМ", Москва (118), Республиканская клиническая больница, Казань (116), "Научно-исследовательский институт урологии и интервенционной радиологии им. Н.А. Лопаткина" - филиал ФГБУ "Национальный медицинский исследовательский центр радиологии" МЗ РФ, Москва (76), ГБУЗ "Кузбасская областная клиническая больница им. С.В. Беляева", Кемерово (64), ГБУЗ МО "Московский областной научно-исследовательский клинический институт им. М.Ф. Владимирского", Московская область (63), ФГБОУ ВО "Самарский государственный медицинский университет" МЗ РФ, Самара (51). От 30 до 49 операций за год сделали 11 центров, еще 12 центров выполнили от 15 до 29. Остальные 19 (38%) выполнили менее 15 трансплантаций почки за год. В 2023 году в 30 центрах (60%) выполнялись родственные трансплантации почки, всего было проведено 197 трансплантаций. Только 4 центра трансплантации почки сделали 7 и более операций за год - это "НМИЦ ТИО им. акад. В.И. Шумакова" (96) и его филиал (9), "НМИЦ здоровья детей" (11), "РНЦХ им. акад. Б.В. Петровского" (8), "СГМУ им. В.И. Разумовского" (7). При этом 53,3% всех родственных трансплантаций почки в РФ выполняет "НМИЦ ТИО им. акад. В.И. Шумакова" и его филиал (105). Средняя частота использования прижизненного донорства почки в 2023 г. составила 10,8% от общего числа трансплантаций почки (в 2022 г. - 14,6%). Трансплантации почки детям (несовершеннолетним до 17 лет включительно) в 2023 г. выполнялись в 6 центрах, всего было проведено 133 пересадки (в 2022 г. - 118), в том числе в "НМИЦ ТИО им. акад. В.И. Шумакова" (61), в "Российской детской клинической больнице" (41), в "НМИЦ здоровья детей" (20) [22].
1.4 Особенности кодирования заболевания или состояния (группы заболеваний или состояний) по Международной статистической классификации болезней и проблем, связанных со здоровьем
Так как трансплантация почки является одним из видов заместительной почечной терапии, применяемой при терминальных заболеваниях почек, при кодировании заболевания также необходимо учитывать классификацию хронической болезни почек, указанную в клинических рекомендациях по ХБП [323].
Для кодирования этиологического фактора (болезни, приведшей к развитию ХБП) должны быть использованы соответствующие коды МКБ-10 в дополнение к основному коду. Для кодирования осложнений ХБП и ассоциированных состояний должны быть использованы соответствующие коды МКБ-10 в дополнение к коду ХБП согласно клиническим рекомендациям по ХБП [323].
Для обозначения наличия трансплантированной почки и при отсутствии каких-либо признаков ее дисфункции: клинических, лабораторных, инструментальных или морфологических - рекомендуется применять код - Z94.0 - наличие трансплантированной почки.
В случае выявления признаков нарушения функции или выявления структурных изменений в почечном трансплантате (см. раздел 1.5.1) необходимо применять код - T86.1 - отмирание и отторжение трансплантата почки.
1.5 Классификация заболевания или состояния (группы заболеваний или состояний)
В связи с большим количеством различных аспектов в трансплантации почки существует несколько используемых классификаций. В отношении непосредственно процедуры трансплантации почки может быть применена следующая классификация (таблица 2):
Таблица 2. Классификации трансплантации почки
Классификация в зависимости от возраста реципиента
Трансплантация почки взрослым
Трансплантация почки детям
Классификация в зависимости от источника донорского органа
Трансплантация почки от посмертного донора
Трансплантация почки от живого родственного донора
Классификация в зависимости от числа предыдущих трансплантаций
Трансплантация почки первичная
Трансплантация почки повторная
Классификация в зависимости от числа трансплантируемых одномоментно органов
Трансплантация почки изолированная
Трансплантация почки сочетанная (с другими органами)
Классификация в зависимости от совместимости по системе AB0
Трансплантация почки совместимая по системе AB0
Трансплантация почки не совместимая по системе AB0
Классификация в зависимости от предшествующей заместительной почечной терапии
Трансплантация почки до начала ЗПТ
Трансплантация почки после начала ЗПТ
1.5.1 Классификация отторжения почечного трансплантата.
Banff-классификация, являющаяся попыткой стандартизовать патологические находки в биоптате трансплантированной почки, была создана на конференции, прошедшей в городе Banff, Канада, 2 - 4 августа 1991 года и была впервые опубликована в 1993 г. В настоящее время используется ее модификация от 2022 года [24].
Критерии поражения Banff оценивают наличие и степень гистопатологических изменений в различных отделах биоптата почечного трансплантата, ориентируясь, в первую очередь, но не исключительно, на диагностические признаки, наблюдаемые при отторжении. Эти показатели поражения сами по себе не всегда достаточны - для определения диагноза могут потребоваться дополнительные диагностические параметры. Классификация отторжения почечного трансплантата Banff (2022 г) представлена в приложении А3.
1.6 Клиническая картина заболевания или состояния (группы заболеваний или состояний)
1.6.1 Клиническая картина.
Трансплантация почки - медицинская технология, направленная на замещение необратимо утраченной функции почек и включающая в себя как неотъемлемый этап хирургическое вмешательство, заключающийся в перемещении почки, полученной от другого человека (донора) в организм реципиента с восстановлением в нем кровоснабжения и оттока мочи. В связи с эти она не может быть описана с точки зрения клинической картины заболевания. Клиническая картина терминальных заболеваний почек описана в соответствующем разделе клинических рекомендаций "Хроническая болезнь почек" [3].
Наличие трансплантированной почки выявляется в ходе сбора анамнеза, когда устанавливается факт выполненной пациенту операции по аллотрансплантации почки, по результатам объективного осмотра, при котором виден послеоперационный рубец, как правило в левой или правой подвздошной области, в большинстве случаев в тех же областях пальпируется почечный трансплантат, и при применении инструментальных методов исследования (ультразвуковое исследование, компьютерная томография и магнитно-резонансная томография, радиоизотопная сцинтиграфия) при которых можно визуализировать почечный трансплантат. При этом ценность визуализирующих методов исследования выше в связи с тем, что у пациента может быть выполнена третья или четвертая трансплантация почки, при которой послеоперационный рубец и почечный трансплантат может находится в нетипичном месте. Необходимо отметить, что состояние, описываемое как Z94.0 - наличие трансплантированной почки, предполагает хорошо функционирующий почечный трансплантат без хирургических осложнений, дефектов функции и признаков отторжения. В случае присутствия вышеописанных нарушений для описания состояния используется код МКБ T86.1. При этом причины дисфункций почечного трансплантата достаточно общины и разнообразны: гемо- и уродинамические, инфекционные, возвратная патология, нефротоксичность обусловленная приемом ингибиторов кальциневрина, а также реакция иммунной системы на чужеродные аллогены. Тем не менее, предметом данных клинических рекомендаций, как этиологической причины дисфункции почечного трансплантата, рассматривается преимущественно отмирание и отторжение трансплантата почки T86.1.
Клинически дисфункция почечного трансплантата может проявляться разнообразными симптомами и синдромами. Она может протекать как в виде острого повреждения почек, так и в виде прогрессирования хронической болезни почки, проявляющегося в виде снижения скорости клубочковой фильтрации. В то же время, дисфункция почечного трансплантата непосредственно сразу после проведенной операции трансплантации может быть вариантом естественного течения посттрансплантационного периода, при котором будет происходить поэтапное восстановление почечной функции. Данное состояние можно рассматривать в аналогии с восстановлением почечной функции при остром повреждении почек. При этом сложность ведения пациента с отсроченной функцией почечного трансплантата заключается в том, что на фоне дисфункции почечного трансплантата, обусловленной его ишемическими повреждениями и повреждениями канальцевого эпителия, может развиваться реакция отторжения.
Острое клеточно-опосредованное отторжение.
Острое клеточное отторжение чаще всего развивается не ранее четвертых суток и может возникать течение всего периода существования почечного трансплантата и обусловлено, в основном, активированными T-лимфоцитами. В течение первого года после трансплантации почки острое клеточное отторжение развивается у 5 - 20% реципиентов. У большинства пациентов острое отторжение трансплантата на ранних стадиях имеет типичные клинические признаки: уменьшение количества мочи, повышение артериального давления, уплотнение и увеличение почечного трансплантата, определяемые пальпаторно, изменение характера почечного кровотока, выявляемое при ультразвуковом исследовании, повышение уровня креатинина и мочевины сыворотки крови. В то же время у ряда пациентов отторжение трансплантата может не иметь явных клинических проявлений и проявляться неспецифическими симптомами - общим недомоганием, утомляемостью, слабостью, тошнотой, рвотой, повышением температуры. Это обуславливает необходимость проведения регулярных плановых осмотров врачом-нефрологом и проведения лабораторных и инструментальных исследований, направленных на оценку состояния почечного трансплантата, определения показаний для проведения биопсии с целью раннего выявления признаков отторжения и своевременного начала лечения.
Антитело-опосредованное отторжение и микрососудистое воспаление/повреждение (гуморальное отторжение).
Гуморальное (антителоопосредованное) отторжение почечного трансплантата является одной из основных причин утраты функции почечного трансплантата. Антитело-опосредованное отторжение может проявляться быстрым нарушением функции трансплантата в раннем посттрансплантационном периоде, но также может иметь скрытое или субклиническое начало, проявляясь в более отдаленные сроки после трансплантации, в то же время признаки гуморального отторжения могут быть обнаружены при гистологическом исследовании материала при отсутствии каких-либо клинических симптомов. Антитела к HLA также могут присутствовать до трансплантации (предсуществующие донор-специфические антитела) или формироваться после трансплантации (de novo) при недостаточной иммуносупрессии. В некоторых случаях имеют место морфологические признаки отторжения при отсутствии выявления антител к HLA. По сроку дебюта клинических проявлений антитело-опосредованное отторжение можно разделить на ранее (менее 30 дней после трансплантации) и позднее (более 30 дней после трансплантации) у пациентов с предсуществующими донор-специфическими антителами и антителами, возникшими de novo, что может влиять на выбор тактики лечения реципиента почки с отторжением [25].
Раннее антитело-опосредованное отторжение как правило наблюдается у сенсибилизированных пациентов высокого риска (с предсуществующими донор-специфичными антителами). Эта форма активного отторжения обычно сопровождается резким нарастанием донор-специфических антител, дисфункцией аллотрансплантата (повышение креатинина, олигурия с протеинурией или без нее). При отсутствии лечения возможно развитие кортикального некроза и потеря трансплантата в течение нескольких дней. Как правило, отмечается отложение C4d и признаки активного антитело-опосредованного отторжения при морфологическом исследовании трансплантата [26]. Возможно обнаружение кровоизлияний в интерстиции, фибриновых тромбов и некроза капилляров клубочка. При своевременном начале лечения возможно восстановление функции аллотрансплантата [26, 27].
В остальных случаях признаки активного антитело-опосредованного отторжения сохраняются, и развивается хроническое активное антитело-опосредованное отторжение, дисфункция аллотрансплантата вплоть до утраты функции.
У пациентов признаки антитело-опосредованного отторжения наблюдаются в большинстве случаев в сроки более 30 дней. В клинической картине отмечается постепенное, но неуклонное снижение СКФ и/или протеинурия, но в итоге этот процесс приводит к утрате функции трансплантата в течение нескольких лет [28, 29]. При морфологическом исследовании трансплантата у таких пациентов преобладают признаки микрососудистого воспаления (в клубочках, перитубулярных капиллярах) и отложение C4d [30, 31]. Форма антитело-опосредованного отторжения, связанная с продукцией ДСА de novo (более 3 мес. после трансплантации), проявляется также дисфункцией трансплантата в сочетании с предшествующим или сопутствующим клеточным отторжением. В одном из исследований было показано, что форма отторжения, ассоциированная с de novo ДСА протекает более агрессивно и сопровождается худшей выживаемостью почечного трансплантата, однако нельзя исключить, что такие исходы в исследовании были связаны с более поздней диагностикой отторжения [32].
2. Диагностика заболевания или состояния (группы заболеваний или состояний) медицинские показания и противопоказания к применению методов диагностики
2.1 Жалобы и анамнез
- Рекомендуется тщательный сбор жалоб и анамнеза у пациента с целью оценки состояния пациента [1 - 2].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5).
- Рекомендуется не рассматривать возраст пациента как показание/противопоказание к трансплантации почки [33].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5).
- Рекомендуется провести нейрокогнитивную оценку у детей - кандидатов на трансплантацию почки, у которых диагностирована терминальная стадия ХБП в возрасте до 5 лет [33].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5).
Комментарий: Трансплантация почки, может быть, не показана пациентам с психическими расстройствами, если невозможно обеспечить адекватный режим иммуносупрессивной терапии. Трансплантация может проводиться, если пациент способен к адекватному восприятию необходимых процедур и терапии.
- Всем кандидатам на ТП рекомендуется воздерживаться от употребления табака как минимум за 1 месяц до внесения в лист ожидания или трансплантации от живого родственного донора [36 - 39].
Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1).
- Рекомендуется при наличии у пациента в анамнезе злокачественных новообразований добиться контроля онкологического процесса перед выполнением трансплантации и началом иммуносупрессивной терапии для повышения выживаемости пациентов. Наличие активного онкологического процесса является не противопоказанием к выполнению трансплантации органов, поскольку течение основного заболевания (в данном случае злокачественного новообразования) может ухудшаться на фоне иммуносупрессивной терапии, тем самым угрожая жизни пациента и ставя под сомнение успешность трансплантации [33].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5).
Комментарий: Сроки рекомендуемого безрецидивного течения ЗНО перед выполнением трансплантации почки у больных ХБП представлены в приложении А3.
- Не рекомендуется исключать кандидатов на трансплантацию из-за ожирения (по определению ИМТ). Рекомендуется прилагать меры по снижению веса кандидатам с ожирением до ТП. Возможность проведения операции по трансплантации почки у пациентов с ИМТ более 35 должно оставаться на усмотрение конкретного трансплантационного центра [40 - 45, 324].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4) - взрослые.
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5) - дети.
Комментарий: Ожирение является основным фактором риска развития сахарного диабета, артериальной гипертензии и сердечно-сосудистых заболеваний. Тем не менее трансплантация почки позволяет увеличить продолжительность и качество жизни диализных пациентов с избыточной массой тела.
Ожирение широко распространено в развитых странах и все чаще встречается в развивающихся странах. В США почти 70% взрослого населения имеют избыточный вес или страдают ожирением, а 6,7% имеют ожирение III стадии (ИМТ >= 40). Ожирение в рамках метаболического синдрома является сильным фактором риска развития ХБП 5. Однако четкой связи между ожирением и терминальной ХБП при отсутствии метаболического синдрома выявлено не было.
Ожирение ассоциировалось с увеличением частоты хирургических осложнений, таких как раневая инфекция (P < 0,001), несостоятельность операционного шва (P = 0,023) и лимфоцеле (P = 0,010). ИМТ >= 25 является независимым фактором риска отсроченной функции трансплантата и первично нефункционирующего трансплантата. Кроме того, продолжительность пребывания в больнице была значительно дольше в группах с пациентами с ожирением по сравнению с пациентами с нормальной и избыточной массой тела. Средняя выживаемость оказывается достоверно ниже у пациентов с ожирением. Пациентам с ожирением II или III степени (ИМТ >= 35 кг/м2) целесообразен прием (осмотр, консультация) врача-диетолога или бариатрическая хирургия. Строгого ограничения по ИМТ при постановке в лист ожидания нет.
В некоторых работах показано, что роботизированная трансплантация обладает лучшими результатами у пациентов, страдающих ожирением [46]. К трансплантации почки пациентам с ИМТ >= 40 кг/м2 следует подходить с осторожностью. В таких случаях важно предупредить пациентов об экстремально высоком риске развития осложнений после трансплантации.
В Великобритании в период с 2015 по 2021 год, только 0,2% трансплантаций были проведены реципиентам с ИМТ >= 40 кг/м2. Большинство трансплантационных центров не выполняют операции по трансплантации почки пациентам с крайней степенью ожирения. Успешная трансплантация возможна у пациентов с ИМТ >= 40 кг/м2, но несет в себе дополнительный риск. Ожирение не должно быть единственным фактором, учитываемым при принятии решения о возможности проведения операции по трансплантации почки. Для оптимизации результатов следует рассмотреть возможность ограничения трансплантации небольшим числом центров с большим объемом выполняемых операций.
- Не рекомендуется отмена антитромботических средств пациентам, ожидающим трансплантацию почки от посмертного донора. Рекомендуется пациентам прекратить прием антитромботических средств за 5 дней до ТП от живого родственного донора и на время всего периоперационного периода [33, 35, 47 - 51].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5).
Комментарии: Пациентам с коагулопатией в анамнезе требуется дополнительное обследование и отдельное внимание, поскольку гиперкоагуляция может привести к тромбозу сосудов трансплантата и гибели трансплантата, а гипокоагуляция - к кровотечению и гибели реципиента. Наличие в анамнезе тромбозов сосудистых доступов или продолжительных кровотечений позволяет предположить коагулопатию [48 - 51].
2.2 Физикальное обследование
- Рекомендуется физикальный осмотр, оценка психоэмоционального статуса потенциального реципиента почки [33, 35, 52 - 56].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5).
Комментарии: психосоциальная оценка потенциальных кандидатов на трансплантацию почки обычно проводится в междисциплинарном контексте. Это дает возможность оценить психологическое, поведенческое здоровье пациента, а также семейное и социальное окружение, которые могут облегчить или затруднить адаптацию к сложностям и проблемам хронического заболевания, трансплантации, модификации образа жизни [52 - 56].
- Рекомендуется прием (осмотр, консультация) врачом-хирургом первичный потенциальных реципиентов почки с целью исключения значимой хирургической патологии. Рекомендуется обследовать кандидатов к ТП на заболевания, препятствующие заживлению ран, включая ожирение, недоедание, употребление табака, перенесенные операции на брюшной полости, чтобы выявить риски заживления ран и образования грыж [35, 40 - 45, 57 - 60].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4).
Комментарии: Все процедуры по пересадке почки сопряжены с риском развития раневых осложнений, включая инфекцию и образование грыжи, что частично обусловлено воздействием иммунодепрессантов на заживление ран. Сопутствующие заболевания, повышающие этот риск, включают диабет, поликистозную болезнь почек, предшествующие хирургические процедуры (включая трансплантацию или герниопластику в анамнезе) и табакокурение. Частота возникновения послеоперационной грыжи составляет примерно 7% в возрасте 10 лет и увеличивается в 2 раза у пациентов, которые ведут активный образ жизни или являются курильщиками. На заживление ран также влияет развитие поверхностных и глубоких тканевых инфекций. Факторы риска развития посттрансплантационных раневых инфекций включают ожирение, диабет, заболевания периферических сосудов, ревматологические заболевания (включая волчанку) и предшествующее употребление наркотиков [57 - 59].
У пациентов с избыточной массой тела отмечается более высокая частота хирургических и нехирургических осложнений, а также повышается риск отсроченной функции трансплантата [20].
- Рекомендуется прием (осмотр, консультация) врачом-стоматологом первичный потенциального реципиента почки, согласно заключению которого, при наличии показаний, проводится санация ротовой полости [61 - 63].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4).
Комментарии: Осмотр врачом-стоматологом имеет важное значение с целью выявления инфекций ротовой полости, санации очагов инфекции перед трансплантацией и началом иммуносупрессивной терапии. Диабетики имеют повышенный риск заболеваний пародонта [61 - 63].
- Рекомендуется прием (осмотр, консультация) врачом-урологом первичный потенциального реципиента почки (мужчин и женщин) с целью исключения патологии мочевыводящих путей, рака почек, мочевого пузыря, простаты [33, 35, 64 - 66].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5).
- Рекомендуется прием (осмотр, консультация) врачом-онкологом первичный (маммологом для женщин старше 40 лет для исключения новообразования молочных желез) [33, 35, 67, 68].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5).
- Рекомендуется пациентам с признаками или симптомами активного сердечного заболевания (например, стенокардией, аритмией, сердечной недостаточностью, пороком клапанов сердца - после проведенных инструментальных и функциональных методов обследования) пройти обследование у врача-кардиолога (прием (осмотр, консультация) врача-кардиолога первичный) и лечиться в соответствии с действующими клиническими рекомендациями до дальнейшего рассмотрения вопроса о пересадке почки [33, 35, 66, 69, 70].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5).
- Рекомендуется прием (осмотр, консультация) врачом-неврологом первичный потенциального реципиента почки с целью исключения патологии нервной системы, а также пациентам, имеющим в анамнезе инсульт или ТИА [33, 35, 69 - 72].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5).
Комментарии: предлагается воздержаться от постановки в лист ожидания пациентов, ранее 6 месяцев после перенесенного инсульта, ранее 3 месяцев после ТИА. Пациентам должен быть проведен скрининг каротидных артерий [69 - 72].
- Рекомендуется прием (осмотр, консультация) врачом-эндокринологом первичный потенциального реципиента почки с целью исключения патологии органов эндокринной системы [33, 35, 73 - 76].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4).
Комментарии: Диабетическая нефропатия является наиболее распространенной причиной ХБП. В связи с более высокой распространенностью сопутствующих заболеваний среди больных сахарным диабетом вероятность ТП у них несколько ниже, чем у людей с ХБП от таких причин, как гломерулонефрит и поликистозная болезнь почек, поэтому данным пациентам необходима более тщательная предоперационная подготовка. Более низкие показатели выживаемости пациентов и почек у больных сахарным диабетом отмечались в течение многих лет, что объясняется более высокой частотой сосудистых, хирургических и инфекционных осложнений [73 - 75]. Впервые выявленный посттрансплантационный сахарный диабет является распространенным осложнением, встречающимся у 10 - 40% реципиентов [76].
- Рекомендуется рассматривать пациента, страдающего сахарным диабетом I типа и хронической болезнью почек 5 стадии, как кандидата на сочетанную трансплантацию поджелудочной железы и почки [53, 78 - 80].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5).
- При невозможности проведения сочетанной трансплантации поджелудочной железы и почки рекомендуется рассматривать пациента, страдающего сахарным диабетом I типа и хронической болезнью почек 5 стадии как кандидата на трансплантацию островковых клеток для улучшения контроля гликемии, повышения чувствительности к гипогликемии, снижения темпов прогрессирования дисфункции почечного трансплантата и выживаемости пациента [312, 313, 314, 315, 345 - 346].
Уровень убедительности рекомендаций A (уровень достоверности доказательств - 2) - взрослые.
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4) - дети.
Трансплантация островковых клеток больным сахарным диабетом I типа может проводиться как одновременно с трансплантацией почки, так и после трансплантации почки, и не сопровождается повышением рисков, связанных с иммуносупрессией, поскольку пациенты с трансплантированной почкой пожизненно получают эту терапию. Кроме того, заместительная терапия островковыми клетками ведет к снижению темпов прогрессирования почечной недостаточности и повышению выживаемости трансплантата и пациента [314, 315, 316].
Показатели, характеризующие использование донорской поджелудочной железы, выше при трансплантации островковых клеток (40% использования донорской поджелудочной железы) [317], чем при трансплантации поджелудочной железы (17,6% использования донорской поджелудочной железы) [318]. Многоцентровое проспективное исследование III фазы продемонстрировало снижение количества эпизодов тяжелых гипогликемий, улучшение контроля гликемии в целом. Приблизительно у половины пациентов в течение 1 года прекращена инсулинотерапия [19 320]. Подтверждение этих результатов получено в другом многоцентровом исследовании, использующее те же конечные точки: HbA1c < 7% и исчезновение эпизодов тяжелых гипогликемий у 82% реципиентов, у 53% - прекращение инсулинотерапии в среднем в течение 26 месяцев, и 35% все еще оставались независимыми от инсулина в конце наблюдения [321, 344 - 346].
- Рекомендуется прием (осмотр, консультация) врачом-терапевтом первичный потенциального реципиента почки с целью обобщения результатов инструментальных и лабораторных исследований, заключений других специалистов [33, 35, 66].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5).
Комментарий: На фоне приема иммунодепрессантов после выполнения трансплантации почки может отмечаться обострение течения некоторых заболевании и патологических состоянии, что в свою очередь может приводить к возникновению жизнеугрожающих осложнений. Характерными примерами служат дивертикулез (с ранее отмечавшимися эпизодами дивертикулита или без них), желчнокаменная болезнь, гиперпаратиреоз. Предтрансплантационная тактика в подобных случаях должна определяться коллегиально (с участием специалистов различного профиля), а также с учетом особенностей конкретного клинического случая. Заболевания почек, характеризующиеся высокой частотой рецидивирования, приводящие к ранней потере трансплантата, являются противопоказанием к трансплантации почки. К соответствующей группе нозологии можно отнести болезнь Вальденстрема, первичный оксалоз и другие.
2.3 Лабораторные диагностические исследования
- Рекомендуется определение основных групп по системе AB0, определение антигена D системы Резус (резус-фактор) реципиенту перед трансплантацией почки [81 - 84].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4).
Комментарии: При трансплантации почки от посмертного донора потенциальные донор и реципиент почки должны быть совместимыми по группе крови AB0 [33, 35, 81 - 83].
- Рекомендовано HLA-типирование (определение антигенов (генов) главного комплекса гистосовместимости I и II классов) реципиенту и донору, проба на совместимость иммунных антител реципиента к антигенам главного комплекса гистосовместимости донора, определение содержания антител к антигенам главного комплекса гистосовместимости в сыворотке крови потенциальному реципиенту почки [33, 35, 85 - 89].
Уровень убедительности рекомендаций A (уровень достоверности доказательств - 2).
Комментарии: При трансплантации почки от посмертного донора необходимо отдавать предпочтение реципиентам с наибольшим уровнем совпадения по антигенам (генам) главного комплекса гистосовместимости. На момент трансплантации реципиент должен иметь отрицательный результат перекрестного комплементзависимого лимфоцитотоксического теста [33, 35, 85 - 89].
- Рекомендуется выполнение общего (клинического) анализа крови, оценка гематокрита (Hct), исследование уровня эритроцитов, тромбоцитов, лейкоцитов, соотношения лейкоцитов в крови, уровня общего гемоглобина и скорости оседания эритроцитов потенциальному реципиенту почки с целью диагностики и дифференциальной диагностики анемии [33, 35, 66, 90, 91].
Уровень убедительности рекомендаций B (уровень достоверности доказательств - 2).
- Рекомендуется исследование уровня натрия в крови, исследование уровня калия в крови, исследование уровня хлоридов в крови, исследование кислотно-основного состояния и газов крови потенциальному реципиенту почки [33, 35, 66].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5).
- Рекомендуется исследование уровня железа сыворотки крови, общего белка, альбумина, мочевины, креатинина, общего билирубина, билирубина связанного (конъюгированного), билирубина свободного (неконъюгированного), глюкозы, холестерина, общего кальция, неорганического фосфора в крови, определение активности аспартатаминотрансферазы, аланинаминотрансферазы, гамма-глютамилтрансферазы, щелочной фосфатазы в крови, потенциальному реципиенту почки с целью диагностики метаболических нарушений [33, 35, 66, 74 - 76].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5).
- Рекомендуется определение ДНК вируса гепатита B (Hepatitis B virus) в крови методом ПЦР, качественное исследование, определение РНК вируса гепатита C (Hepatitis C virus) в крови методом ПЦР, качественное исследование, молекулярно-биологическое исследование крови на вирус иммунодефицита человека ВИЧ-1 (Human immunodeficiency virus HIV-1); молекулярно-биологическое исследование крови на цитомегаловирус (Cytomegalovirus), молекулярно-биологическое исследование крови на вирус Эпштейна-Барр (Epstein - Barr virus), определение антигена (HbsAg) вируса гепатита B (Hepatitis B virus) в крови, определение антител к вирусу гепатита C (Hepatitis C virus) в крови, определение антител классов M, G (IgM, IgG) к вирусу иммунодефицита человека ВИЧ-1 (Human immunodeficiency virus HIV 1) в крови, определение антител классов M, G (IgM, IgG) к вирусу иммунодефицита человека ВИЧ-2 (Human immunodeficiency virus HIV 2) в крови, определение антител к бледной трепонеме (Treponema pallidum) в нетрепонемных тестах (RPR, РМП) (качественное и полуколичественное исследование) в сыворотке крови у потенциальных реципиентов почки [35, 92 - 97].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5).
Комментарии: У потенциального донора должны быть исключены, вирус иммунодефицита человека (ВИЧ-1 и ВИЧ-2), вирус гепатита B (HBV), вирус гепатита C (HCV). Цитомегаловирусная (ЦМВ) инфекция и вирус Эпштейна-Барр являются не являются препятствиями для донорства органов и наиболее часто встречающимися клинически значимыми вирусными инфекциями после трансплантации почки. Тем не менее, они увеличивают риск хронической дисфункции трансплантата, а также посттрансплантационных лимфопролиферативных заболеваний и оппортунистической инфекции, в связи с чем требуют лабораторного контроля методом молекулярно-биологического исследования крови в посттрансплантационном периоде [35, 92 - 99].
- Рекомендуется исследование коагулограммы (ориентировочное исследование гемостаза) потенциальному реципиенту почки с целью исключения тромбофилии/гемофилии, которые могут привести к тромбозу сосудов трансплантата или кровотечению в интраоперационном или раннем послеоперационном периодах [33, 35, 49 - 51, 100, 101].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5).
- Рекомендуется исследование общего (клинического) анализа мочи (визуальное исследование мочи, определение концентрации водородных ионов (pH) мочи, определение белка в моче, исследование уровня глюкозы в моче, микроскопическое исследование осадка мочи) у потенциального реципиента почки при сохраненном диурезе [33, 35, 66, 102, 103].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5).
- Рекомендуется проводить диагностику протеинурии у потенциального реципиента почки при сохраненном диурезе [33, 35, 102, 103].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5).
2.4 Инструментальные диагностические исследования
- Рекомендуется проводить ультразвуковое исследование органов брюшной полости (комплексное) потенциальному реципиенту почки с целью исключения патологии органов брюшной полости [33, 35, 66].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5).
- Рекомендуется проводить дуплексное сканирование сосудов (артерий и вен) нижних конечностей, дуплексное сканирование сосудов малого таза потенциальному реципиенту почки с целью исключения окклюзий периферических артерий [35, 49, 50, 104, 105].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5).
Комментарий: Потенциальным реципиентам почки без очевидных клинических проявлений окклюзионных заболеваний периферических артерий (ЗПА), но имеющим риск этих заболеваний, целесообразно пройти неинвазивное исследование сосудов. Потенциальные реципиенты почки с клинически выраженным ЗПА должны пройти визуализацию и лечение своего ЗПА после консультации с врачом - сердечно-сосудистым хирургом (флебологом) до трансплантации почки. Потенциальным реципиентам почки с клинически выраженным ЗПА необходимо пройти компьютерную томографию органов брюшной полости и забрюшинного пространства и компьютерную томографию органов таза для визуализации брюшной полости/таза с целью оценки артериальной кальцификации и уточнения клинической картины для планирования предстоящей операции [104, 105]. Наше экспертное мнение заключается в том, что дуплексное сканирование сосудов малого таза и нижних конечностей (артерий и вен) до трансплантации почки также следует проводить детям для оценки возможных вариантов развития сосудов.
- Рекомендуется прицельная рентгенография органов грудной клетки потенциальному реципиенту почки с целью исключения патологии легких. При наличии какой-либо патологии органов грудной клетки или при наличии иных показаний рекомендована компьютерная томография органов грудной полости [33 - 35, 38, 39, 66].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5).
- Рекомендуется выполнение ЭКГ потенциальному реципиенту почки с целью определения имеющихся очагов ишемии или кардиомиопатии [33 - 35, 66, 106 - 109].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5).
- Рекомендуется выполнение ЭхоКГ, а также холтеровского мониторирования сердечного ритма потенциальному реципиенту почки с целью определения функционального резерва сердца. При неоднозначных результатах исследований или при наличии иных показаний выполняется коронарография [52, 107 - 109].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5).
Комментарий: Потенциальным реципиентам почки, которые были на диализе не менее двух лет или имели факторы риска легочной гипертензии (например, портальная гипертензия, заболевание соединительной ткани, врожденные пороки сердца, хроническая обструктивная болезнь легких), необходимо пройти эхокардиографию. Имеются доказательства того, что аномальные результаты эхокардиографии и положительные результаты неинвазивных стресс-тестов являются значимыми прогностическими факторами ИБС, сердечных событий и смерти пациентов. Пока нет убедительных доказательств того, что коронарография требуется у бессимптомных пациентов с отрицательным неинвазивным стресс-тестом.
- Рекомендуется выполнение компьютерной томографии органов брюшной полости с внутривенным болюсным контрастированием потенциальному реципиенту почки с целью определения сосудистой анатомии, диагностики новообразовании, проходимости нижней полой вены [33, 35, 66].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5).
- Рекомендуется провести эзофагогастродуоденоскопию потенциальному реципиенту почки с целью исключения эрозивно-язвенного поражения верхних отделов желудочно-кишечного тракта [33, 35, 66, 110, 111].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5).
- Рекомендуется выполнить цистоскопию потенциальному взрослому реципиенту почки для скрининга карциномы мочевого пузыря (у кандидатов с повышенным риском) [112 - 115].
Уровень убедительности рекомендаций B (уровень достоверности доказательств - 3).
2.5 Иные диагностические исследования
- Рекомендуется при выявлении дисфункции почечного трансплантата в раннем или отдаленном периодах проведение пункционной биопсии почки у реципиента почки для оценки наличия/отсутствия острого или антителоопосредованного отторжения трансплантированной почки, ишемического и реперфузионного повреждений, определения нефротоксичности ингибиторов кальциневрина [24, 33, 66, 115 - 125].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4).
- Рекомендуется у реципиентов трансплантата почки мониторировать функцию трансплантата по уровню креатинина, расчетной скорости клубочковой фильтрации и определять целевые уровни ингибиторов кальциневрина в крови для своевременной диагностики отторжения и улучшения выживаемости трансплантата [325 - 330].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4).
Комментарий: Для контроля функции трансплантата следует проводить исследование уровня креатинина в крови и рСКФ каждый день в течение 7 дней после операции, 2 - 3 раза в неделю в течение 4 недель, 1 раз в неделю в течение 2-го и 3-го месяцев, каждые 2 недели в течение 4 - 6 месяца, 1 раз в месяц в течение 7 - 12 месяцев, далее 1 раз в 3 месяца (Приложение А3).
Концентрации ингибиторов кальциневрина в крови следует определять через день до достижения целевого уровня после операции, 2 раза в неделю в течение первого месяца, 1 раз в неделю в течение второго месяца, 1 раз в 2 недели в течение третьего месяца, 1 раз в месяц в течение года (4 - 12 мес.), далее 1 раз в 3 - 4 месяца.
- Рекомендуется у реципиентов трансплантата почки мониторировать показатели гликемии (исследование уровня глюкозы в крови, исследование уровня гликированного гемоглобина в крови) и липидов (исследование уровня холестерина в крови, исследование уровня холестерина липопротеинов низкой плотности, исследование уровня холестерина липопротеинов высокой плотности в крови, исследование уровня триглицеридов в крови) для профилактики сердечно-сосудистых осложнений и улучшения выживаемости [126 - 130].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4).
Комментарий: Сообщается, что впервые выявленный сахарный диабет после трансплантации наблюдается у 4 - 25% реципиентов почечного трансплантата. Факторами риска развития посттрансплантационного сахарного диабета является более старший возраст, семейный анамнез СД 2 типа, ожирение, прием кортикостероидов системного действия, ингибиторов кальциневрина (такролимус** с большей степенью риска, чем циклоспорин**) [126, 127].
У реципиентов почечных трансплантатов, у которых развился NODAT, риск фатальных и нефатальных сердечно-сосудистых заболеваний в 2 - 3 раза выше по сравнению с пациентами, не страдающими диабетом. Также было показано, что развитие NODAT связано с неблагоприятным влиянием на выживаемость пациентов и повышенным риском отторжения и потери трансплантата, а также с увеличением частоты инфекционных осложнений, а ранняя диагностика и начало лечения снижает этот риск [128, 129, 130].
Скрининг гликемии у пациентов с отсутствием диабета до ТП проводится 1 раз в неделю в течение 1 месяца, 1 раз в 3 месяца в течение года, далее ежегодно, а уровня липидов 1 раз в 2 - 3 месяца после трансплантации.
3. Лечение, включая медикаментозную и немедикаментозную терапии, диетотерапию, обезболивание, медицинские показания и противопоказания к применению методов лечения
3.1 Консервативное лечение
- Рекомендуется представить пациенту с ХБП в стадии 4 - 5 (СКФ < 30 мл/мин/1,73 м2) полную информацию о возможности проведения трансплантации почки как одного из методов заместительной почечной терапии [33, 34, 35, 115].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5).
Комментарии: При отсутствии противопоказаний пациентам должна быть представлена полная информация о методике трансплантации почки, ее преимуществах перед другими методами ЗПТ, возможных осложнениях при пересадке почки [33, 115].
Целесообразность трансплантации почки сомнительна у пациентов с:
- Множественной миеломой;
- Амилоидозом со значительным внепочечным поражением;
- Декомпенсированным циррозом (необходимо рассмотреть возможность одновременной пересадки печени);
- Онкологическими поражениями органов;
- Обструктивными заболеваниями легких в необратимой стадии, декомпенсированной дыхательной недостаточностью;
- Тяжелой сердечно-сосудистой недостаточностью, не поддающейся лечению (необходимо заключение врача-кардиолога);
- Прогрессирующим дегенеративным заболеванием ЦНС.
При наличии потенциального родственного донора почки возможна трансплантация почки до начала диализной терапии или включение в лист ожидания почки от посмертного донора (при наличии симптомов или при расчетной СКФ < 10 мл/мин/1,73 м2 (< 15 мл/мин/1,73 м2 в педиатрии, при терминальной ХПН в исходе диабетической нефропатии) [33 - 35, 115, 131, 132].
- Рекомендуется проведение гемодиализа или консервативных мер потенциальным реципиентам почки перед трансплантацией для коррекции дисбаланса жидкости и электролитов [66, 133, 134].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5).
Комментарии: Рутинное использование гемодиализа непосредственно перед трансплантацией почки не показано [134]. Гиперкалиемия является наиболее распространенным показанием для гемодиализа до операции. Риски гемодиализа по сравнению с медикаментозной терапией должны учитываться наряду с рисками интраоперационной перегрузки жидкостью, электролитных и кислотно-щелочных нарушений, особенно в тех случаях, когда почка от посмертного донора трансплантируется со значительным риском развития ОФТ. Предоперационный гемодиализ может инициировать провоспалительное состояние, отложить хирургическое вмешательство, увеличить время холодной ишемии и повысить риск развития ОФТ.
- Рекомендуется оценить риски, связанные с приемом антитромботических средства перед операцией по трансплантации почки совместно с врачом-кардиологом/врачом-гематологом/врачом-нефрологом [33, 35, 66, 100, 101, 135 - 140].
Уровень убедительности рекомендаций A (уровень достоверности доказательств - 2).
Комментарии: Многие пациенты, находящиеся в активном листе ожидания, имеют сосудистые заболевания и/или протромботические состояния, которые должны быть оценены до трансплантации. Двойная антитромботическая терапия обычно назначается пациентам со стентами коронарных артерий в течение шести - двенадцати месяцев; планы периоперационного лечения этих пациентов следует обсудить с врачом-кардиологом, чтобы полностью исключить риск отмены антитромботических средств. Возможности отмены антикоагулянтной и послеоперационной антикоагулянтной терапии следует обсудить до внесения пациентов в лист ожидания.
Некоторые пациенты листа ожидания продолжают принимать антитромботические средства. Показания для антитромботических средств должны быть четко документированы для каждого человека. Потенциальный повышенный риск периоперационного кровотечения необходимо соотнести с риском от артериального или венозного тромбоза. В исследовании на небольшом количестве пациентов было показано, что продолжение антитромбоцитарной терапии клопидогрелем** (антиагреганты, кроме гепарина), ацетилсалициловой кислотой** не дает значительно большего риска пери/послеоперационных осложнений. Влияние антитромботических средств может быть уменьшено интраоперационным введением концентрата тромбоцитов.
- Рекомендуется назначать антитромботические средства (группа гепарина) реципиентам почечного трансплантата с профилактической целью только по показаниям [137, 138].
Уровень убедительности рекомендаций A (уровень достоверности доказательств - 2).
Комментарии: Периоперационное введение антитромботических средств (группа гепарина) снижает послеоперационный риск венозного тромбоза (в том числе в подвздошно-бедренных и почечных венах), однако в связи с сопутствующей повышенной кровопотерей введение требует знания индивидуальных факторов риска пациента. Ни одно из существующих основных руководств по профилактике тромбозов непосредственно не касается тромбопрофилактики в периоперационном периоде почечного трансплантата. Небольшое рандомизированное клиническое исследование РКИ не показало различий в ранней послеоперационной потере трансплантата или тромбоэмболических осложнениях с профилактической антикоагулянтной терапией или без нее [99]. Те, кто получали профилактическую антикоагулянтную терапию, имели значительно более низкий гемоглобин, в то время как те, кто получали с профилактической целью гепарин натрия**, имели длительный лимфодренаж. На основании этого исследования рутинная фармакологическая профилактика может не применяться у реципиентов низкого риска, получивших орган от живого родственного донора. Механические меры по снижению илеофеморального тромбоза глубоких вен могут быть использованы при отсутствии противопоказаний из-за заболевания периферических сосудов, особенно там, где есть опасения по поводу риска кровотечения с фармакологической профилактикой.
Данные систематического обзора всех доступных тематических исследований антикоагулянтной и/или антитромбоцитарной профилактики тромбоза при трансплантации почки, результаты которых были объединены в пропорциональном метаанализе, свидетельствуют о том, что антикоагулянты и дезагреганты (B01A антитромботические средства), как отдельно, так и в сочетании, уменьшают частоту острого тромбоза аллотрансплантата после трансплантации почки. Тем не менее более высокая частота геморрагических осложнений была отмечена в группе пациентов, получивших антикоагулянты [138].
В другом метаанализе рандомизированных контролируемых исследований установлено, что исследований в области профилактики тромбоза трансплантата мало. Из-за отсутствия доказательств высокого качества остается неясным, способна ли какая-либо терапия снизить частоту раннего тромбоза трансплантата при любом типе трансплантации солидных органов. В свою очередь нефракционированный гепарин (гепарин натрия**) может увеличить риск кровотечения у реципиентов трансплантата почки, однако данный вывод основан на низком уровне доказательности [139].
- Рекомендуется антибиотикопрофилактика у реципиентов почечного трансплантата в периоперационном и послеоперационном периодах для профилактики инфекционных и бактериальных осложнений согласно общехирургическим принципам [140, 141].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4).
Комментарии: имеется ограниченное количество хорошо спланированных рандомизированных исследований в отношении целесообразности периоперационной антибактериальной профилактики при трансплантации почки. Традиционно периоперационная антибиотикопрофилактика используется в хирургии при трансплантации почки. Ретроспективное сравнение периоперационной внутривенной профилактики цефазолином** по сравнению с отсутствием антибактериальной терапии не выявило различий в инфекционных осложнениях (хирургическая зона, мочевыводящие пути, бактериемия или инфекция, связанная с центральным венозным катетером) в первый месяц после трансплантации почки [141]. Метаанализ рандомизированных контролируемых исследований выявил только 8 подходящих для анализа исследований, по результатам которого авторы делают вывод, что из-за методологических ограничений, значительной гетерогенности проведенных исследований, современные доказательства профилактического периоперационного использования антибактериальных препаратов системного действия при трансплантации базируются на исследованиях очень низкого качества [142].
- Рекомендуется в периоперационном периоде уточнение сухого веса пациента и объема ультрафильтрации во время сеанса гемодиализа для возможности восполнения объема жидкости в интраоперационном периоде [33, 35, 66, 143, 144].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5).
Комментарии: Для оптимальной функции почечного трансплантата необходимо тщательное соблюдение пери- и послеоперационного баланса жидкости. При использовании нормального (0,9%) раствора натрия хлорида** в периоперационном периоде необходим мониторинг метаболического ацидоза [102]. Проспективное двойное слепое РКИ сравнило применение нормального (0,9%) раствора натрия хлорида** с натрия хлорида раствором сложным [Калия хлорид + Кальция хлорид + Натрия хлорид]** в качестве интраоперационной внутривенной жидкостной терапии. Уровень креатинина в сыворотке крови на третий день после операции не отличался в двух группах. Однако натрия хлорида раствор сложный [Калия хлорид + Кальция хлорид + Натрия хлорид]** вызывал меньше гиперкалиемии и метаболического ацидоза, чем нормальный (0,9%) раствор натрия хлорида**. Сбалансированные растворы могут быть оптимальным и более безопасным вариантом интраоперационной внутривенной жидкостной терапии [143].
Небольшое проспективное неслепое РКИ сравнивало два режима введения нормального (0,9%) раствора натрия хлорида**: постоянную инфузию (10 - 12 мл/кг-1/ч-1 от начала операции до реперфузии) и инфузию на основе центрального венозного давления (целевое ЦВД, соответствующее этапу операции) [144]. Ориентированная на ЦВД инфузия обеспечивала более стабильный гемодинамический профиль, лучший диурез и раннюю функцию трансплантата. Управляемая гидратация может уменьшить ОФТ, а измерение ЦВД может помочь оптимизировать раннюю функцию трансплантата.
- Не рекомендуется регулярно использовать адренергические и дофаминергические средства в малых дозах в раннем послеоперационном периоде у реципиента почки [145 - 150].
Уровень убедительности рекомендаций B (уровень достоверности доказательств - 2) - взрослые.
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4) - дети.
- Рекомендуется применение сеансов терапевтического афереза потенциальному реципиенту почки с целью подготовки к трансплантации почки от прижизненного донора несовместимого по группе крови. Рекомендуемый объем замещения - 1 - 1,5 объема циркулирующей плазмы. Рекомендуемая замещающая жидкость - альбумин человека**, свежезамороженная плазма (IV группа крови). Рекомендуемая частота проведения процедур - каждый день или через день [33, 115, 151, 152].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5).
Комментарии: В связи с дефицитом донорских органов прижизненным донором может быть родственник совместимый или несовместимый по группе крови с реципиентом. Большинство протоколов используют терапевтический плазмообмен, двойную каскадную фильтрацию или специфическую иммуноадсорбцию в комбинации с иммуносупрессивной терапией. Кроме того, применяются внутривенное введение больших доз #иммуноглобулина человека нормального** и иммуноглобулина антитимоцитарного** [331 - 332].
Наиболее распространенной в европейских странах является так называемый "Стокгольмский протокол", который включает в себя однократное введение #Ритуксимаба** дозе 375 мг/м2 за 14 - 30 дней до трансплантации, сеансы селективной иммуноадсорбции (4 обязательных сеанса до операции и 3 после независимо от уровня антител) и однократное внутривенное введение #иммуноглобулина человека нормального** в дозе 0,5 мг/кг массы тела. У детей #Ритуксимаб** применялся в дозе 375 мг/м2 с 10 лет [152]. Схема дополняется назначением трехкомпонентной иммуносупрессивной терапии в предоперационном периоде [152]. Количество процедур терапевтического афереза, входящих в курс подготовки к трансплантации почки от донора, несовместимого по группе крови, зависит от титра антигрупповых антител. При достижении целевого уровня выполняется трансплантация почки. После трансплантации при росте антигрупповых антител проводятся дополнительные сеансы терапевтического афереза [151].
- Рекомендуется применение сеансов терапевтического афереза пациентам с высоким уровнем антител к HLA с целью десенсибилизации. Рекомендуемый объем замещения - 1 - 1,5 объема циркулирующей плазмы. Рекомендуемая замещающая жидкость - альбумин человека**, свежезамороженная плазма. Рекомендуемая частота проведения процедур - каждый день или через день [33, 115, 151].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5).
Комментарии: Антитела к HLA образуются в результате контакта реципиента с чужеродными антигенами главного комплекса гистосовместимости, например при гемотрансфузиях, предшествующих трансплантациях, у женщин - при беременности. Наличие антител является барьером к трансплантации в связи с высоким риском антителоопосредованного отторжения в раннем посттрансплантационном периоде.
В основе протоколов десенсибилизации лежит применение терапевтического плазмообмена, двойной каскадной фильтрации или иммуноадсорбции. В настоящее время для десенсибилизации пациентов используются комбинация из 3 - 5 сеансов плазмообмена с последующей инфузией внутривенного #иммуноглобулина человека нормального** (500 мг/кг) и на 8 день одна доза #Ритуксимаба** 375 мг/м2 (для детей с 10 лет) [152, 331 - 332].
Количество процедур терапевтического афереза, входящих в курс десенсибилизации, точно не определен. Целевыми показателями при проведении являются отрицательная перекрестная лимфоцитотоксическая проба, а также снижение уровня средней интенсивности флуоресценции (MFI) при определении антител на платформе Люминекс [151].
3.2 Хирургическое лечение
- Рекомендуется выполнить превентивную или одновременную с ТП нефрэктомию (радикальную нефрэктомию или лапароскопическую нефрэктомию) кандидатам с аутосомно-доминантной поликистозной болезнью почек, у которых поликистозные почки являются источником инфекции, хронической боли, кровотечений или размеры почек препятствуют проведению трансплантации [153 - 157].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5).
Комментарий: При наличии поликистозной болезни почек, а также при наличии определенных условии (недостаточное пространство для трансплантации, наличие осложнении, хронических инфекционных процессов, подозрении на злокачественные новообразования) имеются показания для предтрансплантационной или одномоментной с ТП нефрэктомии.
- Рекомендуется оценить почечный трансплантат от посмертного донора до начала трансплантации почки с целью оценки пригодности почечного трансплантата [33, 35, 66, 115, 147].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5).
Комментарии: Обработка трансплантата на отдельном столе (back-table preparation) является важным шагом в процессе трансплантации. Для оценки качества органа и исключения экзофитных опухолей почка должна быть обработана во время нахождения в стерильной ледяной крошке шуге, по возможности с удалением околопочечного жира. На отдельном столе может быть выполнена биопсия почки. Подозрительные поражения паренхимы также требуют биопсии.
Необходимо выявить количество, качество и целостность почечных сосудов и мочеточника (мочеточников). В воротах почки должны быть перевязаны лимфатические сосуды. Необходимо оценить качество интимы донорской почечной артерии. Ветви почечной артерии, не идущие в почку или мочеточник(и), должны быть перевязаны.
При трансплантации почки от посмертного донора необходимо определить качество аортальной площадки. Если виден тяжелый атероматоз площадки, устья или дистальной части почечной артерии, то аортальная площадка и/или дистальная часть почечной артерии могут быть отсечены, чтобы обеспечить лучшее качество донорской почечной артерии для имплантации.
Следует оценить длину почечной вены. Впадающие ветви почечных вен должны быть надежно перевязаны. Для правой донорской почки от посмертного донора при необходимости может быть выполнено удлинение почечной вены на отдельном столе при помощи донорской нижней полой вены. Методы удлинения короткой правой почечной вены от живого донора при помощи гонадной вены или подкожной вены реципиента требуют предоперационного планирования.
Следует установить длину, качество и количество мочеточника (мочеточников). Необходимо сохранять парауретеральную клетчатку.
- Рекомендуется использовать подвздошную ямку справа или слева забрюшинным доступом либо брюшную полость при повторных трансплантациях почки или трансплантациях почки маловесным детям [33, 66, 115, 158].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5).
- Рекомендуется лигирование паравазальных лимфатических протоков реципиента почки для профилактики образования послеоперационного лимфоцеле [66, 115, 147].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5).
- Рекомендуется оценить вену трансплантата почки с возможной ее реконструкцией на этапе обработки трансплантата [147, 158 - 161].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4).
Комментарии: Технические подходы при короткой почечной вене могут быть рассмотрены как у донора, так и у реципиента. Для подъема подвздошной вены и предотвращения натяжения анастомоза почечной вены может понадобиться лигирование внутренних подвздошных вен. Транспозиция подвздошных артерии и вены также может улучшить положение венозного анастомоза [159]. Правая почечная вена может удлиняться. В почках от посмертных доноров это обычно делается при помощи донорской нижней полой вены [160]. У живых доноров удлинение почечной вены может быть обеспечено с помощью донорской гонадной вены, извлеченной при донорской нефрэктомии, или с помощью большой подкожной вены реципиента [161], хотя оба требуют специального согласия и в целом предпочтительны другие вышеупомянутые методы.
- Рекомендуется использование подвздошных сосудов реципиента для формирования анастомозов с сосудами трансплантата (общая, наружная, внутренняя подвздошные артерии справа/слева для артериального анастомоза "конец в бок" с почечной артерией трансплантата или анастомоза "конец в конец" при формировании с внутренней подвздошной артерией); в качестве венозного анастомоза почечного трансплантата возможно использование наружной, общей, нижней полой вен [66, 115, 162].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5).
Комментарии: Небольшое РКИ (n = 38), сравнивающее анастомоз с внутренней подвздошной артерией "конец в конец" с анастомозом с наружной подвздошной артерией "конец в бок", показало, что оба метода имеют аналогичные результаты в раннем послеоперационном периоде и в течение трех лет наблюдения. Места сосудистых анастомозов следует выбирать тщательно в зависимости от длины почечной артерии и вены, чтобы избежать перегибов сосудов при помещении почки в ее конечное положение, обычно в подвздошную ямку. В месте артериального анастомоза следует избегать атероматозных бляшек в подвздошной артерии, чтобы уменьшить риск расслоения подвздошной артерии. Интима артерий донора и реципиента должна быть проверена до начала артериального анастомоза, чтобы убедиться, что нет ее разрыва или отслоения, при наличии - необходимо устранить до или во время артериального анастомоза.
- Рекомендуется при наличии добавочных артерий донорской почки сохранить все питающие артерии трансплантата у реципиента почки, используя различные методики артериальной реконструкции - раздельные анастомозы почечных артерий или анастомозы между артериями трансплантата, для обеспечения кровоснабжения во всех полюсах почечного трансплантата [115, 147, 163 - 166].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4).
Комментарии: Множественные почечные артерии, снабжающие почку от посмертного донора, могут быть сохранены на площадке Карреля (соответствующей длины) и имплантированы как один анастомоз. При трансплантации почки от живого донора множественные почечные артерии требуют различных методик для достижения оптимальной реперфузии. Две артерии могут быть имплантированы отдельно или с формированием единого анастомоза; очень маленькая вторая артерия (особенно если она снабжает верхний полюс) может быть перевязана; две артерии могут быть соединены вместе (лоскут в виде "штанов"); или меньшая артерия может быть анастомозирована в бок основной артерии (анастомоз "конец в бок"). Нижняя полюсная артерия может быть реваскуляризована с помощью анастомоза в нижнюю эпигастральную артерию.
- Рекомендуется выполнять методику экстравезикального мочеточникового анастомоза типа Лич-Грегуара (Lich-Gregoir) для минимизации возникновения урологических осложнений у реципиентов почечного трансплантата [66, 115, 167 - 170].
Уровень убедительности рекомендаций A (уровень достоверности доказательств - 2).
Комментарии: Результаты метаанализа двух РКИ и 24 наблюдательных исследований склоняются к экстравезикальной методике Лич-Грегуара (Lich-Gregoir) для снижения общих осложнений (в частности, мочевого затека, стриктуры и послеоперационной гематурии). По данным одного РКИ при экстравезикальном подходе наблюдалось меньшее количество инфекций мочевыводящих путей по сравнению с интравезикальным методом. Донорский мочеточник должен быть оставлен как можно короче с сохранением периуретерального жира для обеспечения адекватного кровоснабжения мочеточника.
- Рекомендуется выполнять пиело-уретеральный или уретеро-уретеральный анастомозы с использованием нативного мочеточника как альтернативу при недостаточной длине мочеточника или при его повреждении при эксплантации [66, 115, 170 - 175].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5).
Комментарии: Пиело- или уретероуретероанастомоз к ипсилатеральному нативному мочеточнику описаны как первичный метод у реципиентов с нерефлюксирующими нативными мочеточниками. В случаях повреждения донорского мочеточника при извлечении может быть выполнена нативная пиелоуретеростомия или пиелонеоцистотомия. Для наложения мочевого анастомоза следует использовать монофиламентные рассасывающиеся швы, чтобы предотвратить образование камней вокруг шовного материала.
- Рекомендуется использование мочеточниковых стентов (стент мочеточниковый полимерный***) при трансплантации почки реципиентам как метод профилактики урологических осложнений в раннем послеоперационном периоде [115, 170, 176, 177].
Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1).
Комментарии: Мочеточниковый анастомоз трансплантата может быть выполнен с мочеточниковым стентом или без него. Кохрановский обзор показал, что стенты используются для уменьшения основных урологических осложнений, особенно мочевых затеков. Оптимальные сроки для удаления стента еще не определены, однако, если стент установлен более 30 дней, отмечается высокий уровень инфекций мочевыделительной системы.
- При удвоенных мочеточниках рекомендуется использование тех же хирургических принципов, как и для отдельных мочеточников, и анастомозирование их отдельно или совместно [178, 179].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4).
Особенности хирургического лечения у детей
- Рекомендуется выбирать место для размещения почечного трансплантата у детей индивидуально в зависимости от соотношения размеров трансплантата и реципиента [180].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5).
Комментарий: При невозможности размещения трансплантата в забрюшинном пространстве трансплантат помещается в брюшную полость.
1. Рекомендуется односторонняя или двусторонняя нефрэктомия у детей в связи с врожденной аномалией строения почек, тяжелой протеинурией [181].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4).
Комментарий: Урологические аномалии более чем в трети случаев являются причиной терминальной почечной недостаточности у детей. Урологические осложнения, генетические аномалии развития часто сочетаются с патологией других органов [181].
3.2.1 Хирургические осложнения
- Рекомендуется дренирование (дренирование забрюшинного пространства) под ультразвуковым контролем или хирургическое вмешательство (ревизия послеоперационной раны под наркозом) реципиенту почки в случае гематом больших размеров в послеоперационном периоде при возникновении клинических проявлений дисфункции трансплантата в связи с компрессией трансплантата или сосудов [182, 183].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4).
- Рекомендуется ультразвуковое исследование почек и дуплексное сканирование артерий почек (почечного трансплантата) первые часы после трансплантации при подозрении на тромбоз артерии трансплантата. В случае выявления неудовлетворительной перфузии по данным ультразвукового исследования показана ревизия [66, 115, 182, 184, 185].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4).
- Рекомендуется выполнить тромбэктомию при интраоперационном выявлении артериального тромбоза, если трансплантат жизнеспособен [66, 115, 182].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4).
- Рекомендуется выполнить трансплантатэктомию (удаление импланта, трансплантата) при интраоперационном выявлении артериального тромбоза при признании нежизнеспособности трансплантата [66, 115, 182, 184, 185].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4).
Комментарии: Тромбоз артерии трансплантата является редким осложнением с частотой возникновения 0.5 - 3.5%. И, как правило, является следствием технической ошибки при наложении анастомоза. Однако, возможны другие причины, связанные как с артерией донора, так и с артерией реципиента (атеросклероз), надрыв интимы во время эксплантации, эпизод острого отторжения, компрессия извне гематомой, тромбофилия, тяжелая гипотония, токсичность компонентов иммуносупрессивной терапии (циклоспорин** (капсулы, раствор для приема внутрь, с учетом возрастных ограничений по инструкции)). Клиническими проявлениями являются анурия, рост уровня креатинина и мочевины в сыворотке крови, что часто приводит к потере трансплантата.
- Рекомендуется дуплексное сканирование вен почечного трасплантата в первые часы после трансплантации при подозрении на тромбоз вены трансплантата. В случае выявления неудовлетворительной перфузии по данным ультразвукового исследования показана ревизия [66, 115, 186 - 189, 334, 335].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4).
- Рекомендуется выполнять тромбэктомию при венозном тромбозе, подтвержденном интраоперационно, если трансплантат жизнеспособен. Рекомендуется выполнять трансплантатэктомию (удаление импланта, трансплантата), если трансплантат нежизнеспособен [66, 115, 182].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4).
- Не рекомендуется медикаментозная профилактика тромбоза вены трансплантата [115, 182, 186 - 190].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5).
Комментарии: Одной из причин потери трансплантата в течение первого месяца после операции является тромбоз вены трансплантата (частота возникновения 0,5 - 4%). Причинами являются интраоперационные хирургические осложнения, а также скрытая тромбофилия у реципиента. Дуплексное сканирование вен почечного трасплантата выявит отсутствие кровотока по вене и атипичный кровоток по артерии (чаще всего обратный диастолический ток, похожий на плато). Также, в связи с венозным тромбозом можно увидеть увеличение трансплантата в размерах. Несмотря на то, что в большинстве случаев венозный тромбоз приводит к потере трансплантата, показана ревизия. В случае, если венозный тромбоз не привел к потере трансплантата, то во время ревизии может быть выполнена тромбэктомия с предварительным пережатием подвздошной вены.
- Рекомендуется проводить диагностику с помощью ультразвукового исследования в режиме цветного допплеровского картирования или компьютерной томографии почек и верхних мочевыводящих путей с внутривенным болюсным контрастированием (почечного трансплантата) для диагностики стеноза артерии трансплантата в случае стойкой артериальной гипертензии, резистентной к медикаментозной терапии и/или повышение уровня креатинина в сыворотке крови без нарушения оттока мочи или инфекции мочевыводящих путей [191 - 193].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4).
- Рекомендуется выполнять транслюминальную баллонную ангиопластику почечной артерии и стентирование почечной артерий при стенозе почечной артерии трансплантата [115, 188 - 194].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5).
Комментарии: Частота стеноза артерии трансплантата составляет от 1% до 25%. Факторами риска являются маленький диаметр и атеросклероз артерии трансплантата, травма артерии во время эксплантации или обработки почечного трансплантата, отсутствие артериальной площадки, хирургическая техника (узловые швы или непрерывный шов) и повреждение подвздошной артерии во время трансплантации. Чаще стеноз возникает в области анастомоза. Диагностика проводится с помощью ультразвукового исследования в режиме цветного допплеровского картирования (дуплексное сканирование артерий почек), по данным которого в артерии трансплантата пиковая систолическая скорость выше 200 см/с. В сомнительных случаях может быть выполнена магнитно-резонансная ангиограмма (магнитно-резонансная ангиография с контрастированием (одна область)) или КТ с ангиографией (компьютерно-томографическая ангиография одной анатомической области или компьютерно-томографическая ангиография брюшной аорты и подвздошных сосудов). Важно определить, является ли стеноз гемодинамически значимым. Обычно наличие стеноза больше 50% считается высоким риском повреждения трансплантата. В случае слабовыраженного стеноза (< 50%) и при отсутствии симптомов повреждения трансплантата проводится консервативное лечение, однако в связи с возможным риском дисфункции трансплантата проводится строгое наблюдение клинической и ультразвуковой картины. В случае клинически значимого стеноза и/или > 50% по данным ультразвукового исследования в режиме цветного допплеровского картирования, с целью подтверждения выполняется (ангиография сосудов почек). Если диагноз подтвержден, начинают с рентгенэндоваскулярного вмешательства, в то время как пациентам после недавно выполненной трансплантации, с множественными, протяженными и критическими сужениями или после неудачной попытки ангиопластики, хирургическое вмешательство может быть более эффективно.
- Рекомендуется чрескожное дренирование забрюшинного пространства при наличии клинически значимых лимфоцеле, при неэффективности процедуры рекомендуется выполнение лапароскопической фенестрации лимфоцеле [195 - 198].
Уровень убедительности рекомендаций B (уровень достоверности доказательств - 2).
Комментарии: Выполнение лапароскопической фенестрации лимфоцеле, в случае клинических значимых лимфоцеле, имеет наименьшую частоту рецидива (8%) и осложнений (14%) по сравнению с открытым оперативным вмешательством и аспирационной терапией.
- Рекомендуется применять консервативные методы лечения в виде катетеризации мочевого пузыря, чрескожной пункционной нефростомии под контролем ультразвукового исследования, антеградная/ретроградная установка стента в мочевыводящие пути трансплантата почки при возникновении урологических осложнений, таких как мочевой затек в раннем послеоперационном периоде. В случае неэффективности консервативной тактики выполняется хирургическая реконструкция [115, 173 - 175, 199 - 206].
Уровень убедительности рекомендаций B (уровень достоверности доказательств - 2).
Комментарии: Мочевой затек возникает в 0 - 9,3% случаев [154]. Мочевой затек в области анастомоза может быть как со стороны мочеточника, так и со стороны мочевого пузыря. Самыми частыми причинами являются некроз мочеточника и/или несостоятельность анастомоза. Мочевой затек может быть заподозрен при возникновении болевого синдрома в области послеоперационной раны, обильного промокания послеоперационной раны, снижения диуреза или увеличения отделяемого по страховочному дренажу (при наличии). С целью снижения риска некроза мочеточника важно сохранять васкуляризацию его дистальной части. Кроме того, показана рутинная установка стента в мочевыводящие пути при трансплантации почки. Тактика в отношении мочевого затека зависит от локализации (почечная лоханка трансплантата, проксимальный или дистальный отдел мочеточника, мочевой пузырь), времени возникновения и объема затека. Возможно применение консервативной тактики (в том числе установка катетера Фолея, чрескожная пункционная нефростомия под контролем ультразвукового исследования, установка стента в мочевыводящие пути почечного трансплантата) для ранних и небольших по объему затеков. В случае неэффективности консервативной тактики необходима хирургическая коррекция: формирование неоуретероцистоанастомоза.
- Рекомендована чрескожная пункционная нефростомия под контролем ультразвукового исследования для диагностики уровня, протяженности стриктуры мочеточника и выбора тактики лечения [207 - 211, 336].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4).
- Рекомендуется эндоскопическая коррекция стриктур мочеточника трансплантата почки протяженностью менее 3 см. Рекомендуется выполнение открытой или лапароскопической хирургической реконструкции при протяженности стриктуры более 3 см и/или при рецидиве стриктуры в отдаленном послеоперационном периоде [115, 174, 200, 206 - 213].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4).
Комментарии: Стеноз мочеточника - частое осложнение у реципиентов почки, частота возникновения которого 0,6 - 10,5%. Причиной раннего (в течение трех месяцев с момента операции) стеноза является хирургическая погрешность или скомпрометированное кровоснабжение мочеточника. Причинами стеноза в отдаленном послеоперационном периоде (более шести месяцев с момента операции) являются инфекция, фиброз, прогрессирующая сосудистая недостаточность и/или отторжение. Клинически значимая стриктура мочеточника проявляется стойким гидронефрозом по данным УЗИ с ухудшением функции трансплантата. В первую очередь для лечения стриктуры выполняется чрескожная пункционная нефростомия под контролем ультразвукового исследования с антеградной пиелоуретерографией. Последующие лечебные мероприятия зависят в основном от времени, степени восстановления функции трансплантата, локализации стриктуры, состояния пациента, сопутствующих заболеваний и предпочтений врача-хирурга. Коррекция стриктур протяженностью менее 3 см проводится эндоскопически либо чрескожной баллонной дилатацией, либо антеградной уретероскопией с рассечением фиброзных тканей лазером. В данном случае вероятность успешного исхода около 50%. В случае рецидива после попытки эндоскопической коррекции стриктуры и/или при протяженности стриктуры более 3 см, должна быть выполнена хирургическая реконструкция в виде реимлантации, пиело-везикальной реимплантации (с подтяжкой к подвздошной мышце и/или формированием лоскута по Боари) или уретеро-уретероанастомоза, в случае сохраненного собственного мочеточника.
3.3 Иное лечение
3.3.1. Индукционная иммуносупрессивная терапия после трансплантации почки
- Базиликсимаб** рекомендуется в качестве индукционной терапии у реципиентов почки с обычными иммунологическими рисками с целью снижения частоты острого отторжения [214 - 219].
Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1).
Комментарии: Базиликсимаб** представляет собой моноклональные антитела с высоким сродством к рецепторам интерлейкина-2 (ИЛ-2). Препарат одобрен для профилактики отторжения в посттрансплантационном периоде [214 - 219]. Базиликсимаб** назначается интраоперационно и на четвертый день после трансплантации. В проведенных рандомизированных клинических испытаниях было доказано, что антитела к рецепторам ИЛ-2 безопасны и снижают частоту острого клеточного отторжения примерно на 40% [214 - 219]. Данные метаанализов подтверждают его эффективность [214 - 216, 219]. Положительный клинический эффект базиликсимаба**, а также улучшение выживаемости трансплантата продемонстрированы проспективными исследованиями [217, 218].
Антитела к рецептору интерлейкина-2 могут дать возможность отмены преднизолона** или метилпреднизолона** [219], несмотря на описанную в литературе высокую частоту отторжений. Применение антител к рецептору ИЛ-2 позволяет существенно снизить дозировку ингибиторов кальциневрина, с сохранением эффективности и почечной функции [214 - 219]. По этой причине данная схема предложена в качестве первоочередной у пациентов со средним или низким иммунологическим риском [218].
- Иммуноглобулин антитимоцитарный** может быть рекомендован в качестве индукционной иммуносупрессивной терапии у пациентов с высоким иммунологическим риском [214, 220, 221, 217 - 219]
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 1).
Комментарии: В качестве профилактики острого отторжения у реципиентов почки высокого иммунологического риска может использоваться "индукционная" терапия с использованием иммуноглобулина антитимоцитарного** [214, 220, 221, 217, 218, 219]. Кроме того, препарат используется для лечения эпизодов тяжелого стероид-резистентного отторжения [220].
Использование иммуноглобулина антитимоцитарного** у пациентов с низким иммунологическим риском не улучшает результаты в отдаленном послеоперационном периоде, так как повышает риск развития тяжелых оппортунистических инфекций и злокачественных новообразований, особенно посттрансплантационных лимфопролиферативных заболеваний [214, 220, 221, 217, 218, 219]. Некоторые центры трансплантации используют данные препараты у реципиентов почки с ишемическим повреждением трансплантата для профилактики отторжения до достижения терапевтической концентрации ингибиторов кальциневрина, однако исследований, подтверждающих эффективность методики, недостаточно [220].
- Рекомендуется назначать индукционную иммуносупрессивную терапию моноклональными (базиликсимабом**) и/или поликлональными (антитимоцитарный иммуноглобулин**) в сочетании с метилпреднизолоном** и поддерживающую иммуносупрессивную терапию ингибиторами кальциневрина (циклоспорин**, микофенолата мофетил** (микофеноловая кислота**), метилпреднизолоном** реципиенту почки с целью профилактики отторжения [33, 66, 115, 214, 215, 216, 220, 221, 222, 223, 224, 336].
Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1).
Комментарии: #Микофенолата мофетил** и #микофеноловая кислота** применяются у детей вне инструкции по медицинскому применению. Дозы иммунодепрессантов, которые применяются в детском возрасте, представлены в таблице 1 (Приложение А3) [336].
3.3.2. Поддерживающая иммуносупрессивная терапия
Иммуносупрессивная терапия особенно важна в раннем послеоперационном периоде, поскольку риск возникновения отторжения в этот период высок. Принципом, лежащим в основе успешной иммуносупрессивной терапии, является соблюдение баланса дозировок препаратов для сохранности трансплантата и без риска для здоровья пациента. Расширение знаний об иммунологическом отторжении привело к разработке современных иммунодепрессантов [217, 218], снижающих активность сенсибилизированных лимфоцитов против трансплантата.
В отдаленном послеоперационном периоде возникает так называемая "адаптация трансплантата", проявляющаяся более низкой частотой возникновения отторжений на фоне поддерживающей иммуносупрессивной терапии. Следовательно, профилактика отторжения ослабляется за счет постепенной отмены метилпреднизолона** и снижения дозировки ингибиторов кальциневрина (циклоспорин**, такролимус** (капсулы), такролимус** (капсулы пролонгированного действия) [217, 218, 225].
Побочные эффекты иммунодепрессантов включают в себя высокий риск развития злокачественных новообразований и инфекционных заболеваний, в особенности оппортунистических инфекций [217, 218, 225]. При этом все иммунодепрессанты имеют дозозависимые специфические побочные эффекты. Цель современных протоколов иммуносупрессивной терапии - снижение специфических побочных эффектов путем использования синергии лекарственных препаратов для сохранения эффективности при снижении побочных эффектов.
Современные режимы базовой иммуносупрессивной терапии обеспечивают превосходную эффективность с хорошей переносимостью [217, 218, 219, 225]. Перечень основных препаратов, которые пациенты получают на текущий момент:
- ингибиторы кальциневрина (преимущественно такролимус** (капсулы), такролимус** (капсулы пролонгированного действия), реже циклоспорин** (с учетом возрастных ограничений по инструкции));
- микофенолата мофетил** или микофеноловая кислота**;
- преднизолон** (таблетки) или метилпреднизолон** (таблетки);
- индукционная терапия (у пациентов с невысокими рисками преимущественно используется базиликсимаб**, а у пациентов с высоким риском - иммуноглобулин антитимоцитарный**).
Дозы препаратов, которые применяются в детском возрасте, представлены в таблице 1 (Приложение 3) [336]. #Микофенолата мофетил** и #микофеноловая кислота** применяются у детей вне инструкции по медицинскому применению.
Многокомпонентная иммуносупрессивная терапия является стандартным методом лечения у большинства реципиентов по всему миру и может быть скорректирована в зависимости от конкретных условий проявления побочных эффектов, эффективности и иммунологического риска [217, 218, 225].
3.3.2.1. Ингибиторы кальциневрина
- Рекомендуется использовать ингибиторы кальциневрина реципиентам почки для профилактики развития отторжения [115, 219, 225 - 227].
Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1).
- Рекомендуется использовать такролимус** (капсулы), такролимус** (капсулы пролонгированного действия) в качестве ингибиторов кальциневрина первой линии реципиентам почки в связи с более высокой эффективностью [115, 219, 225 - 227].
Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1).
- Рекомендуется проводить контроль ингибиторов кальциневрина у реципиентов почки для коррекции оптимальной дозы ингибиторов кальциневрина с целью профилактики отторжения почечного трансплантата, нефротоксичности, нейротоксичности [115, 224, 217, 218, 225, 219, 226, 227, 228 - 234].
Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1).
Комментарии: Как циклоспорин**, так и такролимус** имеют существенные побочные эффекты, которые потенциально опасны как для трансплантата, так и для пациента [219, 225 - 227]. Препараты обладают нефротоксичностью, и длительное их применение является существенной причиной хронической дисфункции трансплантата, что может привести к потере трансплантата почки. Ингибиторы кальциневрина относятся к препаратам с "узким терапевтическим окном" (выход за рамки которого может привести к тяжелой интоксикации либо отсутствию достаточного эффекта) и высокой вероятностью лекарственного взаимодействия, поэтому необходим контроль их уровня в крови.
Метаанализ эффективности такролимуса** и циклоспорина** выявил сходные результаты с учетом выживаемости пациента и трансплантата [217, 218, 219, 224 - 234]. По данным цензурированных исследований, такролимус** обеспечивает лучшую профилактику отторжения и лучшую выживаемость трансплантата. Функция почки у пациентов, принимающих такролимус**, удовлетворительная. В связи с более высокой эффективностью при остром отторжении текущие международные рекомендации предлагают использовать в качестве ингибитора кальциневрина первой линии такролимус** [218].
Ингибиторы кальциневрина имеют несколько фармакологических аналогов. При конверсии с одного аналога на другой необходимо соблюдать меры предосторожности (в том числе контроль лабораторных показателей и определение концентрации ингибиторов кальциневрина в плазме) [229 - 233]. При возникновении специфических побочных эффектов ингибиторов кальциневрина (таких как гирсутизм, алопеция, гиперплазия десен, полиомавирусная нефропатия), конверсия на другой ингибитор кальциневрина может снизить нежелательные проявления [214 - 217, 220 - 224, 235 - 237]. Поскольку существуют значительные различия в эффективности и безопасности у различных ингибиторов кальциневрина, назначение конкретного препарата должно быть основано на индивидуальных рисках и пользе для каждого пациента.
Несмотря на побочные эффекты, ингибиторы кальциневрина являются основой современных протоколов иммуносупрессивной терапии больше 20 лет, поскольку они продемонстрировали значительное улучшение выживаемости почечного трансплантата. Цель разрабатываемых протоколов иммуносупрессивной терапии - снижение дозировки или полная отмена ингибиторов кальциневрина [225, 228, 234, 238]. Однако до тех пор, пока новые протоколы не продемонстрируют более высокую эффективность, ингибиторы кальциневрина останутся в стандартных схемах лечения [217, 218, 239]. При тяжелых проявлениях побочных эффектов ингибиторов кальциневрина, при необходимости возможно снижение дозировки, конверсия или полная отмена ингибиторов кальциневрина [217, 225, 228, 234, 238]. Циклоспорин** назначают с учетом возрастных ограничений по инструкции. Дозы препаратов, которые применяются в детском возрасте, представлены в таблице 1 (Приложение А3) [336].
3.2.2 Микофенолата мофетил** (микофеноловая кислота**)
- Рекомендуется назначать реципиентам почки микофенолата мофетил** (микофеноловая кислота**) совместно с метилпреднизолоном** (преднизолоном**) и ингибиторами кальциневрина в рамках поддерживающей иммуносупрессивной терапии [217, 219, 238 - 245];
Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1).
Комментарии: #Микофенолата мофетил** и #микофеноловая кислота** применяются у детей вне инструкции по медицинскому применению. Дозы иммунодепрессантов, которые применяются в детском возрасте, представлены в таблице 1 (Приложение А3) [336].
Микофенолата мофетил** (микофеноловая кислота**) ингибирует инозинмонофосфатдегидрогеназу (ИМФДГ) [239 - 244]. Это приводит к угнетению de novo пуринового пути метаболизма за счет снижения скорости синтеза гуанозин монофосфата. Функция и пролиферация лимфоцитов больше зависит от синтеза пуриновых нуклеотидов de novo, по сравнению с другими клетками, ингибиторы ИМФДГ могут обеспечить более избирательную иммуносупрессивную терапию, направленную на лимфоциты.
Совместное назначение микофенолата мофетила** (микофеноловой кислоты**), преднизолона** и ингибиторов кальциневрина обеспечивает стойкое снижение частоты отторжений по данным биопсии [217, 219, 240 - 244]. Микофеноловая кислота** не обладает нефротоксичностью, однако она угнетает функцию костного мозга и может быть причиной возникновения ЦМВ инфекции, а также гастроинтестинальных нарушений, в особенности диареи [217, 219, 240 - 244]. При применении микофенолата мофетила** (микофеноловой кислоты**) повышается риск развития полиомавирусной нефропатии, особенно в комбинации с такролимусом** [245].
Микофенолата мофетил** (микофеноловая кислота**) эффективны и практически одинаково безопасны [238 - 242], тем не менее, по данным некоторых проспективных исследований, пациенты, страдающие от гастроинтестинальных осложнений, отмечают улучшение при приеме микофеноловой кислоты**, несмотря на то, что убедительность проспективных рандомизированных исследований сомнительна [240 - 244].
Стандартными дозировками для взрослых в комбинации с циклоспорином** являются 1 г два раза в сутки для микофенолата мофетила** или 720 мг два раза в сутки для микофеноловой кислоты**, хотя были предложены более высокие стартовые дозировки [217, 219, 240 - 244]. Несмотря на частое использование микофенолата мофетила** (микофеноловой кислоты**) с такролимусом**, дозировка в данной комбинации не имеет научного подтверждения [217, 240, 242]. Такролимус** не оказывает влияние на накопление микофеноловой кислоты** в крови, однако при этом накопление (биодоступность) микофеноловой кислоты** в крови на 30% выше по сравнению с циклоспорином**. В связи с высокой частотой развития побочных эффектов некоторые центры практикуют плановое снижение дозы микофенолата мофетила** (микофеноловой кислоты**) у пациентов, принимающих такролимус** [219, 245]. Пациентам, получающим микофенолата мофетил** (микофеноловую кислоту**) в комбинации с такролимусом**, следует регулярно контролировать вирусную нагрузку полиомавируса [217, 245]. Эффективность лабораторного контроля уровня микофенолата мофетила** (микофеноловой кислоты**) в крови сомнительна и на данный момент рутинно не целесообразна [240, 242, 243, 246].
У большинства реципиентов, принимающих микофенолата мофетил** (микофеноловую кислоту**) после пересадки почки, возможна успешная отмена метилпреднизолона** [219] или существенное снижение дозировки ингибиторов кальциневрина, что позволит снизить нефротоксичность и улучшить функцию трансплантата [217, 218, 219, 225, 228, 229]. Несмотря на наличие публикаций, демонстрирующих протоколы без ингибиторов кальциневрина, только с микофенолата мофетилом** (микофеноловой кислотой**) и метилпреднизолоном**, по данным проспективных рандомизированных исследований, отмена ингибиторов кальциневрина в первые три года связана с существенным повышением риска отторжения и ухудшением исхода [217, 225, 238]. В то же время существуют ограниченные данные которые свидетельствуют о возможности отмены ингибиторов кальциневрина во время приема микофенолата мофетила** (микофеноловой кислоты**) и метилпреднизолона** у реципиентов через 5 лет после трансплантации, что в результате приводит к улучшению почечной функции [238, 247].
- Рекомендуется проводить профилактику ЦМВИ или использовать превентивную тактику с регулярным контролем виремии ЦМВ пациентам, принимающим микофенолата мофетил** (микофеноловая кислота**), в связи с высокой частотой возникновения ЦМВ-инфекции [97, 98, 99, 217, 243].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5).
В связи с высокой частотой возникновения ЦМВ инфекции у пациентов, принимающих микофенолата мофетил** (микофеноловую кислоту**) [244], проводится профилактика ЦМВ либо используется превентивная тактика с регулярным контролем виремии ЦМВ [97, 99, 180, 217].
3.3.2.3 Преднизолон** или метилпреднизолон**
- Рекомендуется вводить преднизолон** или метилпреднизолон** в стартовую иммуносупрессивную терапию в периоперационный и ранний послеоперационный периоды [217, 218, 219, 225, 248].
Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1).
Комментарии: У преднизолона** или метилпреднизолона** много побочных эффектов [217, 218, 219, 225, 248], особенно при длительном применении. Преднизолон** или метилпреднизолон** до сих пор считают основным компонентом иммуносупрессивной терапии, даже с учетом последующей успешной отмены по данным многих проспективных рандомизированных исследований [217, 218, 219, 225, 248]. Данные исследования предполагают, что риски при отмене преднизолона** или метилпреднизолона** зависят от использования сопутствующих иммунодепрессантов, иммунологического риска, расовой принадлежности реципиента и срока после трансплантации. Хотя с течением времени риск отторжения снижается, возможная польза от отмены после длительного периода лечения преднизолоном** или метилпреднизолоном** может быть не столь значимой [217, 218, 219, 225, 248].
3.3.2.4 Азатиоприн**
- Азатиоприн** может быть рекомендован к использованию у пациентов с низким иммунологическим риском в качестве иммунодепрессанта, особенно у пациентов с непереносимостью микофенолата мофетил** (микофеноловая кислота**) [217, 218, 219, 240 - 244].
Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1).
Комментарии: Вместо азатиоприна** в большинстве трансплантологических центров по всему миру в качестве стандартной иммуносупрессивной терапии используются микофенолата мофетил** (микофеноловая кислота**). Согласно проспективным рандомизированным исследованиям микофенолата мофетил** (микофеноловая кислота**) значительно снижают частоту отторжений по сравнению с азатиоприном** [217, 218, 219, 240 - 244]. Хотя по данным большого проспективного исследования, азатиоприн** может давать приемлемые результаты у пациентов с низким иммунологическим риском, но чаще азатиоприн** применяется пациентами с непереносимостью микофенолата мофетила** (микофеноловой кислоты**) [217, 218, 240 - 242]. По данным мета-анализа, нет значимых улучшений по основным показателям при добавлении азатиоприна** к двойной терапии циклоспорином** и преднизолоном** или метилпреднизолоном** [249].
3.3.2.5 Эверолимус** (сиролимус)
- Эверолимус** (сиролимус) могут быть рекомендованы к использованию для предотвращения отторжения у реципиентов почки, которые не переносят стандартную иммуносупрессивную терапию [219, 225, 228, 234, 250 - 253].
Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1).
Комментарий: У взрослых сиролимус назначают в однократной ударной дозе 6 мг, затем снижают до 2 - 4 мг в сутки (целевая концентрация 4 - 12 нг/мл) [340, 341]. Эверолимус** (таблетки) у взрослых применяют в дозе 1,5 - 3 мг в сутки с достижением целевой концентрации 3 - 8 нг/мл) [342, 343].
#Эверолимус** и #сиролимус применяются у детей вне инструкции по медицинскому применению. Дозы препаратов, которые применяются в детском возрасте, представлены в таблице 1 (Приложение А3) [336].
- Рекомендуется значительно снижать дозировку ингибиторов кальциневрина реципиентам почки с целью предотвращения нефротоксичности при использовании в комбинации с эверолимусом** (сиролимусом) [217, 219, 234, 250 - 252].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5).
- Не рекомендуется проводить конверсию на эверолимус** (сиролимус) при неудовлетворительной функции трансплантата или выраженной протеинурии у реципиента почки [217, 219, 234, 250 - 252].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5).
- Рекомендуется проводить контроль концентрации эверолимуса** (сиролимуса) для оптимальной коррекции дозы препаратов [217, 219, 234, 250 - 253].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5).
Комментарии: Иммунодепрессанты сиролимус и эверолимус** ингибируют мишень рапамицина млекопитающих (mTOR), подавляя тем самым пролиферацию и дифференцировку лимфоцитов [217, 234, 250 - 252]. Они ингибируют множественные внутриклеточные пути и блокируют цитокины, дающие сигнал к пролиферации T-лимфоцитов. Подобный эффект можно наблюдать с B-лимфоцитами, эндотелиальными клетками, фибробластами и опухолевыми клетками. С целью профилактики отторжения эверолимус** обладает такой же эффективностью, как и микофеноловая кислота** в комбинации с ингибиторами кальциневрина [217, 219, 234, 250 - 252]. Однако, эверолимус** (сиролимус) обладают дозозависимой миелотоксичностью [217, 219, 234, 250 - 253]. Прочие побочные эффекты включают в себя гиперлипидемию, отек, формирование лимфоцеле, замедленное заживление раны, пневмонит, протеинурию и угнетение репродуктивной функции.
На сегодняшний день нет исследований, сравнивающих эффективность сиролимуса и эверолимуса**. Оба препарата имеют практически одинаковые побочные эффекты и отличаются, в основном, фармакокинетическими свойствами [217, 234, 250 - 253]. Эверолимус** обладает периодом полувыведения около 24 часов, принимается 2 раза в день и зарегистрирован для профилактики отторжения у реципиентов почки, печени и сердца. Эверолимус** одобрен к применению с циклоспорином**, в связи с чем, его можно принимать одновременно с циклоспорином**, в то время как сиролимус принимается через 4 часа после приема циклоспорина**. Сиролимус одобрен к применению в комбинации с преднизолоном** или метилпреднизолоном**, с целью отмены циклоспорина** в стандартной трехкомпонентной терапии. В связи с узким терапевтическим окном и высоким риском нежелательного лекарственного взаимодействия следует проводить мониторинг минимальной остаточной концентрации препарата [217, 234, 250 - 253].
При использовании в комбинации с ингибиторами кальциневрина, с целью профилактики пневмонии, вызванной Pneumocystis jirovecii, в течение первого года после трансплантации проводится антибиотикопрофилактика, в том числе низкими дозами ко-тримоксазола [Сульфаметоксазол + Триметоприм]** [217, 250 - 252]. Хотя эверолимус** (сиролимус) не обладают нефротоксичностью, в комбинации с ингибиторами кальциневрина они значительно усиливают нефротоксичность ингибиторов кальциневрина [217]. По данным некоторых исследований, данная комбинация не дает удовлетворительных результатов в отдаленном послеоперационном периоде, особенно в случае сохранения стандартной дозировки ингибиторов кальциневрина [217, 219, 228]. Благодаря синергии, в комбинации с эверолимусом** (сиролимусом) возможно снижение дозировки ингибитора кальциневрина без потери эффективности [234, 250 - 254].
Некоторые исследования предполагают, что эверолимус** (сиролимус) не могут заменить ингибиторы кальциневрина на ранних сроках после трансплантации в связи с низкой эффективностью и неблагоприятными побочными эффектами, особенно такими, как замедленное заживление раны и формирование лимфоцеле [217, 218, 232, 249, 250, 252]. По данным других исследований, на поздних стадиях (более 3 месяцев с момента трансплантации) возможна замена ингибиторов кальциневрина на эверолимус** (сиролимус), с улучшением функции трансплантата [217, 219, 225, 228, 234, 250 - 252, 254]. Тем не менее, несмотря на пользу от отсутствия нефротоксического эффекта, одновременно повышается риск отторжения и возникновения анти-HLA [217, 225, 234, 255]. На текущий момент крайне мало данных о пациентах, получающих в отдаленном послеоперационном периоде эверолимус** (сиролимус).
Протеинурия и ухудшение функции трансплантата во время конверсии является признаками неблагоприятного исхода [217, 225, 234, 250, 251, 252]. Конверсия не целесообразна пациентам с протеинурией более 800 мг/сут, а у пациентов с СКФ менее 30 мл/мин должна быть рассмотрена индивидуально.
Пациентам, у которых высокий риск развития злокачественных новообразований или выявлены злокачественные новообразования после трансплантации, конверсия с ингибиторов кальциневрина на эверолимус** (сиролимус) может быть полезной из-за низкой частоты малигнизации и антипролиферативного эффекта эверолимуса** (сиролимуса) [217, 225, 234, 250 - 252, 254, 256, 257]. По данным нескольких клинических исследований и опубликованных клинических случаев, отмечен положительный клинический эффект конверсии с ингибиторов кальциневрина на эверолимус** (сиролимус) у пациентов с саркомой Капоши [257].
В целом, эверолимус** (сиролимус) рассматриваются в качестве иммунодепрессанта в раннем послеоперационном периоде, в связи с побочными эффектами и высокой частотой отмены [218]. Несмотря на это, эверолимус** (сиролимус) достаточно хорошо изучены, чтобы быть иммунодепрессантами второй линии.
#Эверолимус** и #сиролимус применяются у детей вне инструкции по медицинскому применению. Дозы препаратов, которые применяются в детском возрасте, представлены в таблице 1 (Приложение А3) [336].
Лечение острого клеточного отторжения трансплантата почки
- Рекомендуется для лечения острого клеточного отторжения трансплантата почки Banff класс I применять внутривенное введение метилпреднизолона** в дозах 250 - 500 мг в день в течение 3 дней и/или усиление поддерживающей иммуносупрессии [258 - 262].
Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1).
Комментарий: В одном рандомизированном исследовании внутривенное введение высоких доз преднизолона** было сопоставимо по эффективности с высокими дозами преднизолона** per os, однако токсичность глюкокортикоидов была ниже при внутривенном введении [259]. Введение метилпреднизолона** в дозе 250 - 500 мг внутривенно не было ассоциировано в проспективном исследовании с развитием стероид-резистентного клеточного отторжения по сравнению с более высокими дозами [260, 261, 262].
- Рекомендуется у пациентов с клеточным отторжением трансплантата почки Banff класс II - III, стероид-резистентным клеточным отторжением или возвратом острого клеточного отторжения применять иммуноглобулин антитимоцитарный** для улучшения выживаемости трансплантата [263 - 265].
Уровень убедительности рекомендаций B (уровень достоверности доказательств - 1).
Комментарий: Примерно у 25 - 30% пациентов отторжение не устраняется только кортикостероидной терапией. У этих реципиентов требуется более интенсивная иммуносупрессивная терапия. Когда уровень креатинина в сыворотке не восстанавливается до исходного значения (до отторжения) после пульс-терапии глюкокортикоидами в течение 14 дней с момента начала приема препаратов, эпизод считается стероидорезистентным [264]. До 5-го дня у пациентов со стероид-чувствительным и стероид-резистентным острым отторжением наблюдались схожие изменения уровня креатинина в сыворотке. Однако после 5 дня уровень креатинина у пациентов с ответом значительно снижается, в то время как у не ответивших остается высоким [265].
В метаанализе 11 рандомизированных исследований (76 сообщений, 1680 участников) было показано, что терапия антителами лучше стероидной терапии (RR = 0,50; 95% ДИ: 0,30 - 0,82) в купировании первого эпизода острого отторжения и предотвращения последующих отторжений (RR = 0,70; 95% ДИ: 0,50 - 0,99) и приводит к улучшению выживаемости трансплантата (RR с цензурированием смерти = 0,80; 95% ДИ: 0,57 - 1,12) [263].
Лечение активного антитело-опосредованного отторжения трансплантата почки
- Рекомендуется у пациентов с активным антитело-опосредованным отторжением применять плазмаферез или иммуноадсорбцию для удаления циркулирующих донор-специфических антител и улучшения выживаемости трансплантата [266 - 270].
Уровень убедительности рекомендаций A (уровень достоверности доказательств - 1).
Комментарий: В трех рандомизированных исследованиях с более длительным периодом наблюдения (2 - 5 лет) было продемонстрировано преимущество удаления антител - плазмафереза и иммуноадсорбции [266, 267, 268] по сравнению с отсутствием вмешательства. Долговременный эффект удаления ДСА, который заключался в повышении выживаемости трансплантата, был подтверждена в метаанализе этих исследований (n = 92; HR 0,46; 95% ДИ 0,26 - 0,82; P = 0,009) [269]. В хорошо спланированном рандомизированном исследовании при сравнении группы пациентов, которым выполнялась иммуносорбция, и контрольной группы, с применением только #иммуноглобулина человека нормального** была продемонстрирована потеря трансплантата у 80% пациентов в контрольной группе, исследование было завершено досрочно [270].
- Рекомендуется у пациентов с активным антитело-опосредованным отторжением применять #иммуноглобулин человека нормальный** внутривенно 2 г/кг в сочетании с методами удаления циркулирующих донор-специфических антител для улучшения выживаемости трансплантата [271, 347].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4).
Комментарий: Было также проведено два ретроспективных когортных исследования, изучающих плазмаферез с применением внутривенного #иммуноглобулина человека нормального**, которые включали пациентов с острым и хроническим антитело-опосредованным отторжением трансплантата почки, а у некоторых пациентов отмечены оба элемента. В первом исследовании со средним периодом наблюдения 7 лет было отмечено улучшение выживаемости трансплантата при проведении вмешательства по сравнению с группой сравнения (HR 0,26; 95% ДИ не сообщается; P < 0,001) [271].
Во втором исследовании не было обнаружено достоверной разницы в развитии дисфункции трансплантата между группами, однако большинство (63% пациентов) уже имели признаки хронического поражения на момент постановки диагноза [272].
- Рекомендуется у пациентов с сосудистым антитело-опосредованным отторжением для подавления выработки донор-специфических антител применять #ритуксимаб** 375 мг/м2 в комбинированной терапии с плазмаферезом и введением #иммуноглобулина человека нормального** 2 г/кг [273 - 276].
Уровень убедительности рекомендаций B (уровень достоверности доказательств - 3).
Комментарий: Эффект #ритуксимаба** в сочетании с плазмаферезом и внутривенным введением #иммуноглобулина человека нормального** был продемонстрирован в нескольких ретроспективных исследованиях у пациентов с сосудистым антитело-опосредованным отторжением [273, 274, 275]. Кроме того, в одном нерандомизированном одноцентровом исследовании включение #ритуксимаба** в комбинированную терапию предотвращало выработку ДСА и являлось подходом к десенсибилизации у высокосенсибилизированных пациентов [276].
Лечение хронического антитело-опосредованного отторжения трансплантата почки
- Рекомендуется у пациентов с преобладанием признаков хронического антитело-опосредованного отторжения для улучшения выживаемости трансплантата оптимизировать базовую иммуносупрессивную терапию [272].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5).
Комментарий: В случаях хронического активного антитело-опосредованного отторжения или хронической трансплантационной васкулопатии целями терапии должны быть стабилизация или снижение темпов падения СКФ, протеинурии, при минимизации токсичности препаратов. Использование #иммуноглобулина человека нормального**, плазмафереза с добавлением #ритуксимаба** или без него не показало улучшения выживаемости трансплантата у пациентов с хроническим активным антитело-опосредованным отторжением (в отличие от острого активного антитело-опосредованного отторжения). В этом случае необходима оптимизация иммуносупрессии и поддерживающей терапии, поддержанием целевой концентрации ИКН, контроль артериальной гипертензии и метаболических нарушений.
4. Медицинская реабилитация и санаторно-курортное лечение, медицинские показания и противопоказания к применению методов медицинской реабилитации, в том числе основанных на использовании природных лечебных факторов
Медицинская реабилитация - комплекс мероприятий медицинского и психологического характера, направленных на полное или частичное восстановление нарушенных и (или) компенсацию утраченных функций пораженного органа либо системы организма, поддержание функций организма в процессе завершения остро развившегося патологического процесса или обострения хронического патологического процесса в организме, а также на предупреждение, раннюю диагностику и коррекцию возможных нарушений функций поврежденных органов либо систем организма, предупреждение и снижение степени возможной инвалидности, улучшение качества жизни, сохранение работоспособности пациента и его социальную интеграцию в общество.
Санаторно-курортное лечение включает в себя медицинскую помощь, осуществляемую медицинскими организациями (санаторно-курортными организациями) в профилактических, лечебных и реабилитационных целях на основе использования природных лечебных ресурсов, в том числе в условиях пребывания в лечебно-оздоровительных местностях и на курортах. Санаторно-курортное лечение направлено на:
1) активацию защитно-приспособительных реакций организма в целях профилактики заболеваний, оздоровления;
2) восстановление и (или) компенсацию функций организма, нарушенных вследствие травм, операций и хронических заболеваний, уменьшение количества обострений, удлинение периода ремиссии, замедление развития заболеваний и предупреждение инвалидности в качестве одного из этапов медицинской реабилитации [277].
Находясь на ЗПТ, пациенты часто подвергаются диетическим ограничениям, связанным с прогрессирующей ХБП. После трансплантации нутритивный фактор является одним из способствующих увеличению веса, метаболическому синдрому, диабету и его последствиям. Реципиенты трансплантата должны быть обеспечены доступными для понимания рекомендациями по питанию и, при необходимости, обеспечены рекомендациями по снижению веса. В частности, следует избегать приема грейпфрутового сока из-за возможности его вмешательства в метаболизм иммунодепрессантов, что приводит к повышению уровня ингибиторов кальциневрина.
Важно вести активный образ жизни. После трансплантации почки не следует заниматься теми видами спорта, при которых возможны прямые удары или другие повреждения трансплантированной почки (например, кикбоксинг) [278 - 280].
Злоупотребление алкоголем или немедицинская (неадекватная) форма рекуррентного потребления химических веществ, оказывающих влияние на настроение или поведение человека, может увеличить риск нежелательных событий [281, 282].
4.1 Трансплантация при беременности
4.1.1 Планирование беременности
- Рекомендуется планировать беременность только в условиях хорошего общего состояния, стабильной функции трансплантата и при постоянной иммуносупрессивной терапии, а также при отсутствии признаков отторжения трансплантата, артериальной гипертензии, протеинурии, гидронефроза или хронической инфекции. Оптимальным сроком для беременности является второй год после выполненной ТП [283 - 286].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4).
Комментарий: Хроническая почечная недостаточность зачастую сопровождается нарушениями сексуальной и репродуктивной функций. После трансплантации почки половая жизнь и репродуктивная функция восстанавливаются [283]. Мужчины и женщины с терминальной стадией почечной недостаточности должны быть хорошо информированы по вопросам беременности. Беременность должна протекать при хорошем состоянии общего здоровья и трансплантата, обычно не ранее чем через 1 - 2 года после выполнения трансплантации [284]. При наступлении беременности через несколько лет после трансплантации имеется риск развития хронического отторжения и/или ухудшения функции почек.
При стабильном функциональном состоянии трансплантата и постоянной иммуносупрессивной терапии, а также при отсутствии признаков отторжения трансплантата, артериальной гипертензии, протеинурии, гидронефроза или хронической инфекции не отмечается существенного различия исходов ранней, оптимальной или поздней беременности [285]. При гидронефрозе отмечается более высокий риск прерывания беременности вследствие увеличения вероятности развития инфекции или мочекаменной болезни, которые могут осложнять течение III триместра беременности. Необходимо как можно раньше диагностировать беременность для максимально раннего начала динамического наблюдения и коррекции иммуносупрессивной терапии. Беременность у женщин, перенесших трансплантацию органов, зачастую не является проблемой, однако данные пациентки во всех случаях должны включаться в категорию повышенного риска; беременность должна протекать под динамическим наблюдением врача-акушера-гинеколога, врача-нефролога и врача-уролога.
4.1.2 Тактика ведения беременности
- Рекомендуется контролировать факторы риска при ведении беременных женщин, ранее перенесших трансплантацию почки [283 - 289].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4).
Комментарий: (Общий (клинический) анализ мочи) следует выполнять с периодичностью 1 раз в месяц (ранняя диагностика инфекций мочеполовой системы), устранять бактериурию независимо от наличия клинических проявлений. Во избежание фето- и нефротоксичности необходимо назначать бета-лактамные антибактериальные препараты: пенициллины. Необходима профилактика и подавление любых вирусных инфекций во избежание внутриутробных дефектов (например, умственная отсталость ребенка после перенесенной внутриутробной ЦМВ-инфекции). При подозрении на внутриутробные инфекции необходимо осуществлять определение ДНК цитомегаловируса (Cytomegalovirus) в амниотической жидкости методом ПЦР.
4.1.3 Иммуносупрессивная терапия при беременности
- Не рекомендуется использование микофенолата мофетила** (микофеноловой кислоты**) и эверолимуса** (сиролимуса) для поддерживающей иммуносупресивной терапии при беременности у реципиенток почек [286, 290 - 294].
Уровень убедительности рекомендаций B (уровень достоверности доказательств - 3).
Комментарий: Препарат такролимус** (капсулы), такролимус** (капсулы пролонгированного действия), применяющийся с целью иммунносупрессивной терапии после трансплантации почки, характеризуется достаточно высокой безопасностью. Лишь отдельные исследования свидетельствуют о том, что микофенолата мофетил** и сиролимус обладают тератогенностью, поэтому их использование противопоказано при беременности.
- Рекомендуются естественные роды реципиенткам почки при отсутствии фоновой патологии беременности или гипоксии плода [283, 284, 285, 286].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4).
Комментарий: Показатели частоты спонтанных (14%) или по медицинским показаниям (20%) абортов у женщин, перенесших трансплантацию донорских органов, аналогичны соответствующим общепопуляционным показателям. Несмотря на то, что наличие трансплантированного органа в тазу не препятствует механически естественному механизму родов, в группе беременных женщин, перенесших трансплантацию донорских органов, чаще (50%) отмечаются преждевременные роды и родоразрешения путем кесарева сечения. Указанная закономерность объясняется наличием многочисленных факторов риска (неконтролируемое течение артериальной гипертензии, гипоксия плода, преждевременный разрыв плодных оболочек на фоне кортикостероидной терапии).
- Не рекомендуется грудное вскармливание реципиенткам почки после рождения ребенка в связи с высоким риском попадания иммунодепрессантов в организм новорожденного [283, 284, 285, 286].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 4).
5. Профилактика и диспансерное наблюдение, медицинские показания и противопоказания к применению методов профилактики
- Рекомендуется пожизненное регулярное наблюдение после трансплантации опытным и обученным специалистом по трансплантации. Оценка функции почечного трансплантата производится ежемесячно в первые 3 месяца, далее 1 раз в 3 месяца в течение первого года, потом ежегодно [33, 34, 115, 295, 296].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5).
Комментарии: Регулярное долгосрочное наблюдение опытных врачей-хирургов (трансплантологов), врачей-нефрологов имеет важное значение для раннего выявления осложнений или дисфункции трансплантата и для контроля строгого соблюдения предписанного иммуносупрессивного режима.
Необходимо регулярно контролировать (приблизительно каждые 4 - 8 недель в первые 6 месяцев после ТП) уровень креатинина в сыворотке крови, расчетную скорость клубочковой фильтрации, давление крови, экскрецию белка мочой, иммуносупрессивную терапию и осложнения после трансплантации почки. Изменения этих параметров с течением времени должны инициировать дальнейшие диагностические исследования, включая биопсию почки, поиск инфекционных причин и анти-HLA.
Риск развития злокачественных новообразований и сердечно-сосудистых заболеваний в несколько раз выше у трансплантированных пациентов, чем в общей популяции. Другими важными отдаленными проблемами являются несоблюдение предписанного режима терапии, развитие анти-HLA, рецидивирование исходного заболевания и нефротоксичность, связанная с ингибиторами кальциневрина [115, 217, 218, 225, 297, 298].
Многие пациенты теряют свои трансплантаты из-за хронической дисфункции аллотрансплантата [120, 121, 217, 218, 295]. В случае дисфункции почечного трансплантата показано внеочередное обследование. В биоптате трансплантированной почки обычно выявляют хронический процесс интерстициального фиброза и канальцевой атрофии (ИФ/КА) [299]. Некоторые пациенты имеют хроническое антителоопосредованное отторжение [300]. ИФ и КА развиваются месяцами или годами и проявляются протеинурией и гипертонией с одновременным или отсроченным повышением уровня креатинина в сыворотке в течение месяца [218, 299]. Вполне вероятно, что (ИФ/КА) чаще встречается у пациентов, которые перенесли ранние кризы острого отторжения или инфекции. Хроническая нефротоксичность встречается у пациентов, принимающих ингибиторы кальциневрина и получивших трансплантат от доноров с расширенными критериями с предсуществующим повреждением почки [295, 299, 301].
У пациентов с хронической нефротоксичностью, диагностированной путем биопсии трансплантата почки на ранней стадии, особенно при наличии доказательств токсичности ингибиторов кальциневрина, прогрессирование заболевания может замедляться путем перехода на режим без ингибиторов кальциневрина [228]. Перевод на эверолимус** является вариантом для пациентов без значительной протеинурии (< 800 мг/день), но с умеренной удовлетворительной функцией почек. В качестве альтернативы была описана успешная схема конверсии на основе микофенолата мофетила** (микофеноловой кислоты**), особенно у пациентов по истечении первых трех лет после трансплантации [217, 218, 225]. Кроме того, может быть успешным перевод на режим на основе азатиоприна**, если имеется непереносимость эверолимуса** или микофенолата мофетила** (микофеноловой кислоты**), хотя при этом требуется более тщательное наблюдение ввиду более высокого риска отторжения [303, 304].
Режим иммуносупрессии без ингибиторов кальциневрина сопряжен с крайне высоким риском развития отторжения и потери почечного трансплантат, в связи с этим он может быть применен только в исключительных случаях при доказанной нефротоксичности и отсутствия эффекта от режимов с минимизаций ингибиторов кальциневрина.
У пациентов с протеинурией замедлить прогрессирование почечной недостаточности может воздействие ингибиторов АПФ или антагонистами рецепторов ангиотензина II [218, 295] вместе со строгим контролем артериального давления. Другие вспомогательные меры включают лечение гипертонии, гиперлипидемии, диабета, анемии, ацидоза и заболеваний костей. Однако в итоге пациенту может потребоваться повторная трансплантация или диализная терапия. С появлением ингибиторов натрийзависимого переносчика глюкозы 2 типа их стали применять для лечения пациентов с хронической болезнью почек. Тем не менее количество исследований, и данные об их эффективности и безопасности в отношении пациентов после трансплантации почки на сегодняшний день ограничены [305].
- Рекомендуется использовать комбинацию иммунодепрессантов как поддерживающую терапию, включая ингибиторы кальциневрина и препаратов микофеноловой кислоты** или селективных иммунодепрессантов эверолимуса** (сиролимуса), с приемом или без приема преднизолона** или метилпреднизолона** [217, 218, 225, 306 - 309].
Уровень убедительности рекомендаций B (уровень достоверности доказательств - 3).
Комментарии: Поддерживающая терапия должна обеспечивать максимальную продолжительность жизни реципиента с функционирующим трансплантатом, что определяется адекватностью подавления аллоиммунного ответа, с одной стороны, и минимизацией риска побочных эффектов иммунодепрессантов, с другой стороны. После успешной трансплантации почки поддерживающая иммуносупрессивная терапия в подавляющем большинстве случаев включает три компонента, причем ее базисным препаратом, как правило, является ингибитор кальциневрина (циклоспорин** или такролимус** (капсулы), (капсулы пролонгированного действия), в сочетании с микофенолата мофетилом** (микофеноловой кислотой**), реже азатиоприном**, и преднизолоном** или метилпреднизолоном** в минимальной дозе. В последние годы для поддерживающей иммуносупрессивной терапии применяются также селективные иммунодепрессанты (эверолимус** (сиролимус). Через 3 месяца после пересадки почки концентрацию такролимуса** обычно поддерживают на уровне - 8 - 10 нг/мл, по истечении шести месяце - 5 - 8 нг/мл. В сроки более 12 месяцев после трансплантации у пациентов с низким функциональным резервом трансплантата, малой массой функционирующих нефронов или особой чувствительностью к нефротоксическому действию такролимуса** концентрацию можно снизить до 3 - 5 нг/мл. При этом также важно помнить о риске отторжения и при необходимости увеличить дозу сопутствующих препаратов.
#Микофенолата мофетил**, #микофеноловая кислота**, #эверолимус и #сиролимус применяются у детей вне инструкции по медицинскому применению. Дозы иммунодепрессантов, которые применяются в детском возрасте, представлены в таблице 1 (Приложение А3) [336].
6. Организация оказания медицинской помощи
6.1 Показания для плановой госпитализации
1. Подготовка к AB0-несовместимой трансплантации.
2. Подготовка к трансплантации почки (санация очага инфекции, нефрэктомия).
3. Госпитализация для выполнения родственной ТП.
4. Дисфункция трансплантата почки.
5. Нестабильность концентрации ингибиторов кальциневрина.
6. Выполнение пункционной биопсии трансплантата.
6.2 Показания для экстренной госпитализации
1. Наличие совместимой донорской почки от посмертного донора.
2. Дисфункция трансплантата почки при угрожающих жизни состояниях.
3. Хирургические/урологические осложнения после ТП.
4. Острые состояния или обострения хронических заболеваний в раннем посттрансплантационном периоде.
6.3 Показания к выписке пациента из стационара
1. Удовлетворительная функция трансплантата.
2. Отсутствие показаний для нахождения в стационаре.
7. Дополнительная информация (в том числе факторы, влияющие на исход заболевания или состояния)
Морфологические признаки дисфункции трансплантированной почки
Эпизод острого отторжения является следствием иммунного ответа реципиента с целью разрушения трансплантата. Он имеет клеточное (лимфоциты) и (или) гуморальное (циркулирующие антитела) происхождение. Острое отторжение клинически подозревается у пациентов при повышении уровня креатинина в сыворотке крови после исключения других причин дисфункции трансплантата (как правило, подтверждается биопсией). С первых дней после трансплантации до начала эффективной иммуносупрессивной терапии отсутствие лечения криза отторжения неизбежно приводит к утрате трансплантата.
Острое отторжение характеризуется снижением функции трансплантата в совокупности с детально установленными морфологическими критериями, выявляемыми при биопсии. Субклиническое острое отторжение определяется присутствием гистологических изменений, характерных для острого отторжения на скрининговых или протокольных биопсиях, в случае отсутствия при этом клинических симптомов или признаков [218].
I. Морфологические типы отторжения трансплантированной почки
1. Сверхострое отторжение аллотрансплантированной почки
Этиология связана с наличием в крови реципиента предсуществующих цитотоксических антител. Прогнозирование этого вида отторжения основано на проведении перекрестной пробы лимфоцитов донора с сывороткой предполагаемого реципиента (реакция cross-match). Отторжение развивается с первой же минуты после включения почки в кровоток. Почка становиться дряблой, цианотичной, отсутствует пульсация сосудов. Если трансплантат удаляют, при гистологическом исследовании выявляют распространенный тромбоз сосудов микроциркуляторных путей, некротические изменения каких-либо структур отсутствуют, отмечаются только дистрофические изменения извитых канальцев. В биоптатах, взятых в интервале от 1 до 3-х суток, присоединяется диффузная инфильтрация интерстиция нейтрофильными лейкоцитами. Реже, при низком уровне предсуществующих антител, возможно отсроченное развитие сверхострого отторжения (через 12 - 24 ч после операции), требуется проведение дифференциальной диагностики между ишемическими повреждением и сверхострым отторжением на основании исследования пункционных биоптатов. При обоих видах отмечается некроз паренхимы почки, но при сверхостром отторжении аллотрансплантированной почки присутствует распространенный тромбоз микроциркуляторных путей [116, 118 - 122].
2. Ускоренное отторжение аллотрансплантированной почки
Ускоренное отторжение аллотрансплантированной почки развивается в первые несколько суток после включения почки в кровоток реципиента (от 12 до 72 часов). В патогенезе этого вида отторжения принимают участие не только гуморальные факторы, но и клеточный иммунитет. Гистологически выявляется полнокровие и стазы крови в сосудах микроциркуляторного русла коркового вещества, инфильтрация лимфоцитами и повреждение паренхиматозных органов [116, 118 - 122].
3. Острое отторжение аллотрансплантированной почки
Острое отторжение аллотрансплантированной почки по-прежнему остается одним из основных осложнений, обуславливающих снижение и даже прекращение функции АТП. При исследовании пункционных биоптатов аллотрансплантированной почки оценку наличия или отсутствия острого клеточного отторжения проводят по следующим полуколичественным параметрам: а) оценка степени воспаления клубочков (гломерулит-g): g0 - нет гломерулита; g1 - гломерулит < 25% клубочков; g2 - гломерулит 25% - 75% клубочков; g3 - гломерулит всех или почти всех клубочков. б) оценка стенки воспаления канальцев (тубулит-t): t0 - отсутствие лимфоцитов в стенке канальцев; t1 - 1 - 4 лимфоцита в стенке поперечного среза канальца; t2 - 5 - 10 лимфоцитов в стенке канальца; t3 - более 10 лимфоцитов в стенке поперечного среза канальца. в) оценка степени воспаления стенки артерий (васкулиты-v): v0 - артериит отсутствует; v1 - эндартериит с воспалением < 25% интимы по окружности хотя бы одной артерии; v2 - эндартериит с воспалением > 25% интимы по окружности хотя бы одной артерии; v3 - тяжелый панартериит с некрозом гладкомышечных клеток и/или фибриноидным некрозом. г) оценка степени воспаления интерстиция (i): i0 - отсутствие либо инфильтрация интерстиция лимфоцитами < 10% кортикального слоя; i2 - 26 - 50% кортикального слоя инфильтрировано лимфоцитами; i3 - инфильтрация лимфоцитами > 50% кортикального слоя. В настоящее время для оценки степени клеточного острого отторжения аллотрансплантированной почки используется классификация Banff 97. В зависимости от полуколичественных показателей диагностируют следующие виды отторжения:
- пограничные изменения - не относятся к острому отторжению, но являются его предикторами g0, t1, v0, i1;
- острое отторжение интерстициального типа (типы 1a, 1b)
Тип 1a: g0-1, t2, v0, i2-3;
Тип 2b: g0-2, t3, v0, i2-3;
- острое отторжение сосудистого типа (типы 2a, 2b)
Тип 2a: g0-1, t0-1, v1, i2-3;
Тип 2b: g0-2, t0-2, v2, i2-3;
- тяжелое острое отторжение
Тип 3: g2-3, t2-3, v3, i2-3.
Разделение на типы острого клеточного отторжения имеет большое клиническое значение, так как от типа отторжения зависят лечение криза и коррекция базовой иммуносупрессивной терапии.
Гуморальные факторы при остром отторжении играют значительную роль. Острое антителоопосредованное (гуморальное) отторжение характеризуется острой стероидрезистентной дисфункцией трансплантата, наличием в сыворотке крови реципиента донорспецифических антител и наличием компонента комплимента C4d в перитубулярных капиллярах [116 - 122].
Наиболее точная дифференциальная диагностика патологии АТП может быть осуществлена только прижизненным патологоанатомическим исследованием биопсийного (операционного) материала почки с применением иммуногистохимических методов. Морфологическую верификацию (морфологическую диагностику) патологии в аллотрансплантированной почке осуществляют путем исследования материала чрескожной пункционной биопсии. Клинический диагноз отторжения почки не может быть правомочен без подтверждения результатами гистологического исследования биоптата трансплантированной почки [85]. Для стандартизации подходов к оценке степени отторжения АТП под эгидой Международного общества нефрологов (ISN) была разработана классификация, принятая в августе 1991 года в Канаде и получившая название по тому городу, в котором проходила работа комиссии, - Banff. Впоследствии эта классификация неоднократно пересматривалась и дополнялась [116 - 122].
4. Хроническое отторжение аллотрансплантированной почки.
За последнее время достигнуты большие успехи в области иммуносупрессивной терапии, что привело к сокращению числа случаев острого отторжения и увеличению выживаемости трансплантированных органов. Однако хроническая дисфункция АТП остается главной клинической проблемой. Одной из причин этого является хроническая нефропатия [87, 88].
Хроническое отторжение представляет собой антителоопосредованное отторжение. Продукция антител к антигенам эндотелиальных клеток сосудов трансплантата с последующим образованием на эндотелиоцитах комплексов антиген-антитело при участии комплимента приводит к повреждению эндотелия, повышению сосудистой проницаемости, плазматическому пропитыванию, пролиферации субэндотелиальной соединительной ткани, инфильтрации интимы мононуклеарными клетками. В результате просветы мелких артерий уменьшаются или могут полностью закрыться. Недостаточность кровотока ведет к повреждению паренхимы. Первые морфологические признаки хронического отторжения могут проявляться уже в сроки от 4 - 6 месяцев после операции. В стенке артерий определяется отложение иммуноглобулинов различных классов, но преимущественно IgM, в интиме - фиксация C4d компонента комплимента [89 - 91]. По классификации Banff 97 при хроническом отторжении выявляется атрофия канальцев, склероз интерстициальной ткани, продуктивный эндартериит. В интерстиции как в зонах склероза, так вне этих участков, паравазально, отмечается различная степень очаговой инфильтрации мононуклеарными клетками, среди которых большое количество плазмобластов и плазматических клеток. В артериальных ветвях - пролиферация соединительной ткани в интиме с уменьшением сечения их просветов. Выявляется различная степень склеротического поражения клубочков. Нарушения кровообращения при хроническом отторжении ведет к развитию диффузного нефросклероза [116, 118 - 122].
II. Нефротоксичность ингибиторов кальциневрина
Циклоспорин** и такролимус** уменьшают риск развития отторжения и увеличивают длительность выживания аллотрансплантата и реципиента. Низкий уровень ингибиторов кальциневрина в крови повышает риск острого отторжения, а высокий, как правило, ведет к развитию циклоспориновой нефротоксичности. Различают острое и хроническое действие препаратов.
Гистологическим признаком острой токсичности ингибиторов кальциневрина является появление изометрической вакуолизации в цитоплазме проксимальных отделов извитых канальцев, выявляемой с помощью окраски гематоксилином и эозином.
Хроническая нефротоксичность развивается не ранее чем через четыре месяца после трансплантации почки. Гистологически выявляется полосчатый склероз интерстициальной ткани, атрофия канальцев, нодулярный гиалиноз артериол и мелких артерий [116, 118 - 122].
III. Инфекционные осложнения после аллотрансплантации почки
Этиология инфекционных осложнений после трансплантации почки связана с вирусной, бактериальной, грибковой флорой, а также простейшими. Частота бактериальных инфекций со времени начала применения ингибиторов кальциневрина у больных после трансплантации органов значительно снизилась. Источником бактериальной инфекции аллотрансплантированной почки может быть операционная рана при присоединении госпитальной инфекции, гематомы и лимфоцеле в области ложа трансплантата, нарушение пассажа мочи по мочевыводящим путям при обструкции мочеточника или его фистулах. При гистологическом исследовании в материале пункционной биопсии определяется характер неспецифического или специфического (например, туберкулезного) воспаления, иногда удается определить бактериальную и грибковую флору. Бактериальные инфекции при гистологическом исследовании биоптатов вызывают острый интерстициальный нефрит, проявляющийся отеком интерстиция ткани почки, инфильтрацией лейкоцитами и эозинофилами. Актуальной проблемой остаются вирусные инфекции, среди которых важное значение занимает ЦМВ-инфекция и полиомавирусная инфекция (полиомавирус ВК, Human polyomavirus I из рода Betapolyomavirus). При прижизненном патологоанатомическом исследовании биопсийного материала (гистологическом исследовании) в ядрах эпителиоцитов эндотелия сосудов обнаруживают специфические включения [116, 118 - 122].
IV. Ишемические и реперфузионные повреждения
В течение первых двух месяцев после операции одной из причин дисфункции АТП является их ишемическое и репефузионное повреждение. При исследовании пункционных биоптатов трансплантированных почек, полученных в первые недели после операции, всегда выявляются признаки ишемического повреждения паренхимы. Гистологическим его проявлением является острый канальцевый некроз, степень которого и определяет степень ишемического повреждения АТП.
1. Легкая степень ишемического повреждения - дистрофические изменения в эпителиальных клетках целых групп извитых канальцев, некроз отдельных эпителиальных клеток.
2. Средняя степень ишемического повреждения - характеризуется такими же изменениями, как и при легкой степени, однако увеличивается количество наркотизированных клеток.
3. Тяжелая степень ишемического повреждения - отмечается диффузный некроз эпителиальных клеток извитых канальцев, сопровождающийся тубулорексисом и нарушением микроциркуляции в интертубулярных сосудах [116, 118 - 122].
Критерии оценки качества медицинской помощи
Критерии оценки качества медицинской помощи пациентам при постановке в лист ожидания на трансплантацию почки, при проведении операции по трансплантации почки и при отмирание и отторжение трансплантата почки представлены в Табл. 3 - 5.
Таблица 3. Критерии оценки качества медицинской помощи пациентам при постановке в лист ожидания на трансплантацию почки
N
Критерии качества
Оценка выполнения
1.
Пациенту с ХБП в стадии 4 - 5 (СКФ < 30 мл/мин/1,73 м2) предоставлена информацию о возможности проведения трансплантации почки как одного из методов заместительной почечной терапии
Да/Нет
2.
Потенциальным реципиентам с ожирением рекомендовано снижение веса до ТП
Да/Нет
3.
Выполнен физикальный осмотр
Да/Нет
4.
Выполнен прием (осмотр, консультация) врачом-хирургом первичный
Да/Нет
5.
Выполнен прием (осмотр, консультация) врачом-стоматологом первичный
Да/Нет
6.
Выполнен прием (осмотр, консультация) врачом-урологом первичный
Да/Нет
7.
Выполнен прием (осмотр, консультация) врачом-онкологом первичный (маммологом для женщин старше 40 лет)
Да/Нет
8.
Выполнен прием (осмотр, консультация) врачом-неврологом первичный
Да/Нет
9.
Выполнено обследование у врача-кардиолога (прием (осмотр, консультация) врача-кардиолога первичный)
Да/Нет
10.
Выполнен прием (осмотр, консультация) врачом-эндокринологом первичный
Да/Нет
11.
Выполнен прием (осмотр, консультация) врачом-терапевтом первичный
Да/Нет
12.
Выполнено исследование уровня железа сыворотки крови, исследование уровня общего белка в крови, исследование уровня альбумина в крови, исследование уровня мочевины в крови, исследование уровня креатинина в крови, исследование уровня общего билирубина в крови, исследование уровня билирубина связанного (конъюгированного) в крови, исследование уровня билирубина свободного (неконъюгированного) в крови, исследование уровня глюкозы в крови, исследование уровня холестерина в крови, исследование уровня общего кальция в крови, исследование уровня неорганического фосфора в крови, определение активности аспартатаминотрансферазы в крови, определение активности аланинаминотрансферазы в крови, определение активности гамма-глютамилтрансферазы в крови, определение активности щелочной фосфатазы в крови, анализ крови биохимический общетерапевтический
Да/Нет
13.
Выполнено исследование коагулограммы (ориентировочное исследование гемостаза)
Да/Нет
14.
Выполнено исследование общего (клинического) анализа мочи (визуальное исследование мочи, определение концентрации водородных ионов (pH) мочи, определение белка в моче, исследование уровня глюкозы в моче, микроскопическое исследование осадка мочи) у потенциального реципиента почки при сохраненном диурезе
Да/Нет
15.
Выполнена диагностика протеинурии у потенциального реципиента почки при сохраненном диурезе
Да/Нет
16.
Выполнено ультразвуковое исследование органов брюшной полости (комплексное)
Да/Нет
17.
Выполнена прицельная рентгенография органов грудной клетки
Да/Нет
18.
Выполнена компьютерная томография органов грудной клетки при наличии какой-либо патологии органов грудной клетки или при наличии иных показаний
Да/Нет
19.
Выполнено ЭКГ
Да/Нет
20.
Выполнено ЭхоКГ, а также холтеровское мониторирование сердечного ритма
Да/Нет
21.
Выполнена компьютерная томография органов брюшной полости с внутривенным болюсным контрастированием
Да/Нет
22.
Выполнена эзофагогастродуоденоскопия
Да/Нет
Таблица 4. Критерии оценки качества медицинской помощи пациентам при проведении операции по трансплантации почки
N
Критерии качества
Оценка выполнения
1.
Определена группа крови по системе AB0, определен антиген D системы Резус (резус-фактор)
Да/Нет
2.
Выполнено HLA-типирование (определение антигенов (генов) главного комплекса гистосовместимости I и II классов) реципиенту и донору, проба на совместимость иммунных антител реципиента к антигенам главного комплекса гистосовместимости донора, определено содержание антител к антигенам главного комплекса гистосовместимости в сыворотке крови потенциального реципиента
Да/Нет
3.
Выполнен общий (клинический) анализ крови, оценка гематокрита (Hct), исследование уровня эритроцитов, тромбоцитов, лейкоцитов, соотношения лейкоцитов в крови, уровня гемоглобина и скорости оседания эритроцитов
Да/Нет
4.
Выполнено исследование уровня натрия в крови, исследование уровня калия в крови, исследование уровня хлоридов в крови, исследование кислотно-основного состояния и газов крови
Да/Нет
5.
Выполнено определение ДНК вируса гепатита B (Hepatitis B virus) в крови методом ПЦР, качественное исследование, определение РНК вируса гепатита C (Hepatitis C virus) в крови методом ПЦР, качественное исследование, молекулярно-биологическое исследование крови на вирус иммунодефицита человека ВИЧ-1 (Human immunodeficiency virus HIV-1); молекулярно-биологическое исследование крови на цитомегаловирус (Cytomegalovirus), молекулярно-биологическое исследование крови на вирус Эпштейна-Барр (Epstein - Barr virus), определение антигена (HbsAg) вируса гепатита B (Hepatitis B virus) в крови, определение антител к вирусу гепатита C (Hepatitis C virus) в крови, определение антител классов M, G (IgM, IgG) к вирусу иммунодефицита человека ВИЧ-1 (Human immunodeficiency virus HIV 1) в крови, определение антител классов M, G (IgM, IgG) к вирусу иммунодефицита человека ВИЧ-2 (Human immunodeficiency virus HIV 2) в крови, определение антител к бледной трепонеме (Treponema pallidum) в нетрепонемных тестах (RPR, РМП) (качественное и полуколичественное исследование) в сыворотке крови у потенциальных реципиентов почки
Да/Нет
6.
Проведены гемодиализ или консервативные меры потенциальным реципиентам почки перед трансплантацией для коррекции дисбаланса жидкости и электролитов (при наличии показаний)
Да/Нет
7.
Проведена периоперационная антибиотикопрофилактика
Да/Нет
8.
До начала операции почечный трансплантат от посмертного донора оценен (обработан) на отдельном столе
Да/Нет
9.
Использован стент мочеточниковый полимерный***
Да/Нет
10.
При подозрении на тромбоз артерии трансплантата выполнено ультразвуковое исследование почек и дуплексное сканирование артерий почек (почечного трансплантата)
Да/Нет
11.
При подозрении на тромбоз вены трансплантата выполнено ультразвуковой контроль в режиме цветового допплеровского картирования (дуплексное сканирование вен почечного трасплантата)
Да/Нет
12.
Использована индукционная иммуносупрессивная терапия базиликсимабом** или/и иммуноглобулин антитимоцитарный** в сочетании с метилпреднизолоном** и поддерживающая иммуносупрессивная терапия ингибиторами кальциневрина (циклоспорин**, такролимус** (капсулы), такролимус** (капсулы пролонгированного действия), микофенолата мофетил** (микофеноловая кислота**), метилпреднизолоном** реципиенту почки с целью профилактики отторжения
Да/Нет
13.
В качестве ингибиторов кальциневрина первой линии использован такролимус** (капсулы), такролимус** (капсулы пролонгированного действия)
Да/Нет
14.
Проведен контроль концентрации ингибиторов кальциневрина
Да/Нет
15.
Проведена профилактика ЦМВ пациентам, принимающим микофенолата мофетил** (микофеноловую кислоту**)
Да/Нет
16.
В раннем послеоперационном периоде использованы преднизолон** или метилпреднизолон**
Да/Нет
17.
Эверолимус** (сиролимус) использован у реципиентов почки, которые не переносят стандартную иммуносупрессивную терапию
Да/Нет
Таблица 5. Критерии оценки качества медицинской помощи пациентам и при отмирании и отторжение трансплантата почки
N
Критерии качества
Оценка выполнения
1.
Проведена диагностика стеноза артерии трансплантата в случае стойкой артериальной гипертензии, резистентной к медикаментозной терапии и/или повышение уровня креатинина в сыворотке крови без гидронефроза или мочевой инфекции
Да/Нет
2.
Диагностика стеноза почечной артерии проведена с помощью ультразвукового исследования в режиме цветного допплеровского картирования или компьютерной томографии почек и верхних мочевыводящих путей с внутривенным болюсным контрастированием (почечного трансплантата)
Да/Нет
3.
Выполнена баллонная дилатация со стентированием почечной артерии при стенозе почечной артерии трансплантата
Да/Нет
4.
При наличии лимфоцеле клинически значимых размеров выполнено чрескожное дренирование забрюшинного пространства, а при его неэффективности выполнена лапароскопическая фенестрация лимфоцеле
Да/Нет
5.
При возникновении мочевого затека в раннем послеоперационном периоде выполнены консервативные методы лечения в виде катетеризации мочевого пузыря, чрескожной пункционной нефростомии под ультразвуковым исследованием, антеградного/ретроградного стентирования мочеточника трансплантата почки. В случае неэффективности консервативной тактики выполнена хирургическая реконструкция
Да/Нет
6.
Выполнена чрескожная пункционная нефростомия под контролем ультразвукового исследования для диагностики уровня, протяженности стриктуры мочеточника и выбора тактики лечения
Да/Нет
7.
Выполнена эндоскопическая коррекция стриктур мочеточника трансплантата почки протяженностью менее 3 см. Выполнена открытая или лапароскопическая хирургическая реконструкция при протяженности стриктуры более 3 см и/или при рецидиве стриктуры в отдаленном послеоперационном периоде
Да/Нет
8.
Проведен контроль концентрации ингибиторов кальциневрина
Да/Нет
9.
Выполнена пункционная биопсия почечного трансплантата при наличии клинических, лабораторных и инструментальных признаков его дисфункции и отсутствии противопоказаний
Да/Нет
Список литературы
1. National Kidney Foundation. K/DOQI clinical practice guidelines for chronic kidney disease: evaluation, classification, and stratification. Am J Kidney Dis 2002; 39 (2 Suppl 1): S 1 - 266.
2. Kidney Disease: Improving Global Outcomes (KDIGO) CKD Work Group. KDIGO 2012 Clinical Practice Guideline for the Evaluation and Management of Chronic Kidney Disease. Kidney Int Suppl 2013; 3: 1 - 150.
3. Клинические рекомендации "Хроническая болезнь почек (ХБП)" (одобрены Минздравом России) 2024.
4. Kramer A., Boenink R., Stel V.S. et al. The ERA-EDTA Registry Annual Report 2018: a summary//Clinical Kidney Journal. https://doi.org/10.1093/ckj/sfaa271
5. Tsai WC, Wu HY, Peng YS et al. Risk Factors for Development and Progression of Chronic Kidney Disease: A Systematic Review and Exploratory Meta-Analysis. Medicine (Baltimore) 2016; 95(11): e3013. doi: 10.1097/MD.0000000000003013
6. Shen Y, Cai R, Sun J et al. Diabetes mellitus as a risk factor for incident chronic kidney disease and end-stage renal disease in women compared with men: a systematic review and meta-analysis. Endocrine 2017; 55(1): 66 - 76. doi: 10.1007/s12020-016-1014-6
7. Chang AR, Grams ME, Ballew SH et al. Adiposity and risk of decline in glomerular filtration rate: meta-analysis of inpidual participant data in a global consortium. BMJ 2019; 364: k5301. doi: 10.1136/bmj.k5301
8. Nitsch D, Grams M, Sang Y et al. Associations of estimated glomerular filtration rate and albuminuria with mortality and renal failure by sex: a meta-analysis. BMJ 2013; 346: f324. doi: 10.1136/bmj. f324
9. See EJ, Jayasinghe K, Glassford N et al. Long-term risk of adverse outcomes after acute kidney injury: a systematic review and meta-analysis of cohort studies using consensus definitions of exposure. Kidney Int 2019; 95(1): 160 - 172. doi: 10.1016/j.kint.2018.08.036
10. Rashidbeygi E, Safabakhsh M, Delshad Aghdam S et al. Metabolic syndrome and its components are related to a higher risk for albuminuria and proteinuria: Evidence from a meta-analysis on 10, 603, 067 subjects from 57 studies. Diabetes Metab Syndr 2019; 13(1): 830 - 843. doi: 10.1016/j.dsx.2018.12.006
11. Xia J, Wang L, Ma Z et al. Cigarette smoking and chronic kidney disease in the general population: a systematic review and meta-analysis of prospective cohort studies. Nephrol Dial Transplant 2017; 32(3): 475 - 487. doi: 10.1093/ndt/gfw452
12. Garofalo C, Borrelli S, Pacilio M et al. Hypertension and Prehypertension and Prediction of Development of Decreased Estimated GFR in the General Population: A Meta-analysis of Cohort Studies. Am J Kidney Dis 2016; 67(1): 89 - 97. doi: 10.1053/j.ajkd.2015.08.027
13. Shang W, Li L, Ren Y et al. History of kidney stones and risk of chronic kidney disease: a meta-analysis. PeerJ 2017; 5: e2907. doi: 10.7717/peerj.2907
14. Musso G, Gambino R, Tabibian JH et al. Association of non-alcoholic fatty liver disease with chronic kidney disease: a systematic review and meta-analysis. PLoS Med 2014; 11(7): e1001680. doi: 10.1371/journal.pmed.1001680
15. Mantovani A, Zaza G, Byrne CD et al. Nonalcoholic fatty liver disease increases risk of incident chronic kidney disease: A systematic review and meta-analysis. Metabolism 2018; 79: 64 - 76. doi: 10.1016/j.metabol.2017.11.003
16. Yu X, Yuan Z, Lu H et al. Relationship between birth weight and chronic kidney disease: evidence from systematics review and two-sample Mendelian randomization analysis. Hum Mol Genet 2020; 29(13): 2261 - 2274. doi: 10.1093/hmg/ddaa074
17. Nankivell BJ, Alexander SI. Rejection of the kidney allograft. N Engl J Med. 2010 Oct 07; 363(15): 1451 - 62]:
18. Joosten SA, Sijpkens YW, van Kooten C, Paul LC. Chronic renal allograft rejection: pathophysiologic considerations. Kidney Int. 2005 Jul; 68(1): 1 - 13.]
19. Fresenius medical care annual report 2018. https://www.freseniusmedicalcare.com/fileadmin/data/com/pdf/Media_Center/Publications/Annual_Reports/FME_Annual-Report_2018.pdf
20. http://www.transplant-observatory.org/summary/
21. Заместительная почечная терапия хронической болезни почек 5 стадии в Российской Федерации 2016 - 2020 гг. Краткий отчет по данным Общероссийского Регистра заместительной почечной терапии Российского диализного общества/А. М. Андрусев, Н. Г. Перегудова, М. Б. Шинкарев, Н. А. Томилина//Нефрология и диализ. - 2022. - Т. 24, N 4. - С. 555 - 565. - DOI 10.28996/2618-9801-2022-4-555-565. - EDN RBZZBH.
22. Готье С.В., Хомяков С.М. Донорство и трансплантация органов в Российской Федерации в 2023 году. XVI сообщение регистра Российского трансплантологического общества. Вестник трансплантологии и искусственных органов. 2024; 26(3): 8 - 31. https://doi.org/10.15825/1995-1191-2024-3-8-31
23. National Center for Health Statistics. WHO Collaborating Centre for the WHO Family of International Classifications. https://www.who.int/classifications/icd/ICD-10%20Updates%202007.pdf
24. https://banfffoundation.org/central-repository-for-banff-2019-resources-3
25. Schinstock CA, Mannon RB, Budde K, Chong AS, Haas M, Knechtle S, Lefaucheur C, Montgomery RA, Nickerson P, Tullius SG, Ahn C, Askar M, Crespo M, Chadban SJ, Feng S, Jordan SC, Man K, Mengel M, Morris RE, O'Doherty I, Ozdemir BH, Seron D, Tambur AR, Tanabe K, Taupin JL, O'Connell PJ. Recommended Treatment for Antibody-mediated Rejection After Kidney Transplantation: The 2019 Expert Consensus From the Transplantion Society Working Group. Transplantation. 2020 May; 104(5): 911 - 922. doi: 10.1097/TP.0000000000003095
26. Tan EK, Bentall A, Dean PG, et al. Use of eculizumab for active antibody-mediated rejection that occurs early post-kidney transplantation: a consecutive series of 15 cases. Transplantation. 2019; 103: 2397 - 2404.
27. Orandi BJ, Zachary AA, Dagher NN, et al. Eculizumab and splenectomy as salvage therapy for severe antibody-mediated rejection after HLA-incompatible kidney transplantation. Transplantation. 2014; 98: 857 - 863.
28. Loupy A, Vernerey D, Tinel C, et al. Subclinical rejection phenotypes at 1 year post-transplant and outcome of kidney allografts. J Am Soc Nephrol. 2015; 26: 1721 - 1731.
29. Stegall MD, Diwan T, Raghavaiah S, et al. Terminal complement inhibition decreases antibody-mediated rejection in sensitized renal transplant recipients. Am J Transplant. 2011; 11: 2405 - 2413.
30. Wavamunno MD, O'Connell PJ, Vitalone M, et al. Transplant glomerulopathy: ultrastructural abnormalities occur early in longitudinal analysis of protocol biopsies. Am J Transplant. 2007; 7: 2757 - 2768.
31. Bentall A, Cornell LD, Gloor JM, et al. Five-year outcomes in living donor kidney transplants with a positive crossmatch. Am J Transplant. 2013; 13: 76 - 85.].
32. Aubert O, Loupy A, Hidalgo L, et al. Antibody-mediated rejection due to preexisting versus de novo donor-specific antibodies in kidney allograft recipients. J Am Soc Nephrol. 2017; 28: 1912 - 1923.]
33. KDIGO Clinical Practice Guideline on the Evaluation and Management of Candidates for Kidney Transplantation. Transplantation, 2020. 104, 4S: 1 - 103.
34. Tonelli M, Wiebe N, Knoll G, et al. Systematic review: kidney transplantation compared with dialysis in clinically relevant outcomes. Am J Transplant. 2011; 11: 2093 - 2109
35. Dudley C, Harden P. Renal Association Clinical Practice Guideline on the assessment of the potential kidney transplant recipient. Nephron Clin Pract. 2011; 118 Suppl 1: c209 - 224.
36. Thomsen T, Villebro N, Moller AM. Interventions for preoperative smoking cessation. Cochrane Database Syst Rev. 2014: CD002294.
37. Duerinckx N, Burkhalter H, Engberg SJ, et al. Correlates and Outcomes of Posttransplant Smoking in Solid Organ Transplant Recipients: A Systematic Literature Review and Meta-Analysis. Transplantation. 2016; 100: 2252 - 2263.
38. Nourbala MH, Nemati E, Rostami Z, et al. Impact of cigarette smoking on kidney transplant recipients: a systematic review. Iran J Kidney Dis. 2011; 5: 141 - 148.
39. Corbett C, Armstrong MJ, Neuberger J. Tobacco smoking and solid organ transplantation. Transplantation. 2012; 94: 979 - 987.
40. Schold JD, Srinivas TR, Guerra G, et al. A "weight-listing" paradox for candidates of renal transplantation? Am J Transplant. 2007; 7: 550 - 559.
41. Molnar MZ, Streja E, Kovesdy CP, et al. Associations of body mass index and weight loss with mortality in transplant-waitlisted maintenance hemodialysis patients. Am J Transplant. 2011; 11: 725 - 736.
42. Gill JS, Lan J, Dong J, et al. The survival benefit of kidney transplantation in obese patients. Am J Transplant. 2013; 13: 2083 - 2090.
43. Kostakis ID, Kassimatis T, Bianchi V, Paraskeva P, Flach C, Callaghan C, Phillips BL, Karydis N, Kessaris N, Calder F, Loukopoulos I. UK renal transplant outcomes in low and high BMI recipients: the need for a national policy. J Nephrol. 2020 Apr; 33(2): 371 - 381. doi: 10.1007/s40620-019-00654-7. Epub 2019 Oct 3. PMID: 31583535.
44. Gillespie H, O'Neill S, Curtis RMK, Callaghan C, Courtney AE. When There is No Guidance From the Guidelines: Renal Transplantation in Recipients With Class III Obesity. Transpl Int. 2023 Sep 15; 36: 11428. doi: 10.3389/ti.2023.11428. PMID: 37779511; PMCID: PMC10540226.
45. Scheuermann U, Babel J, Pietsch UC, Weimann A, Lyros O, Semmling K, Hau HM, Seehofer D, Rademacher S, Sucher R. Recipient obesity as a risk factor in kidney transplantation. BMC Nephrol. 2022 Jan 18; 23(1): 37. doi: 10.1186/s12882-022-02668-z. PMID: 35042452; PMCID: PMC8767742.
46. Oberholzer J, Giulianotti P, Danielson KK, et al. Minimally invasive robotickidney transplantation for obese patients previously denied access to transplantation. Am J. Transplant. 2013; 13: 721 - 728
47. Zimmerman D, Sood MM, Rigatto C, et al. Systematic review and meta-analysis of incidence, prevalence and outcomes of atrial fibrillation in patients on dialysis. Nephrol Dial Transplant. 2012; 27: 3816 - 3822.
48. Garg L, Chen C, Haines DE. Atrial fibrillation and chronic kidney disease requiring hemodialysis - Does warfarin therapy improve the risks of this lethal combination? Int J Cardiol. 2016; 222: 47 - 50.
49. Douketis, J.D., et al. Perioperative Management of Antithrombotic Therapy: Antithrombotic Therapy and Prevention of Thrombosis, 9th ed: American College of Chest Physicians Evidence-Based Clinical Practice Guidelines. Chest, 2012. 141. https://pubmed.ncbi.nlm.nih.gov/22315266
50. Pawlicki, J., et al. Risk factors for early hemorrhagic and thrombotic complications after kidney transplantation. Transplant Proc, 2011. 43: 3013. https://pubmed.ncbi.nlm.nih.gov/
51. Rouviere, O., et al. Acute thrombosis of renal transplant artery: graft salvage by means of intraarterial fibrinolysis. Transplantation, 2002. 73: 403.
52. Campbell S, Pilmore H, Gracey D, et al. KHA-CARI guideline: recipient assessment for transplantation. Nephrology (Carlton). 2013; 18: 455 - 462.
53. Kasiske BL, Cangro CB, Hariharan S, et al. The evaluation of renal transplantation candidates: clinical practice guidelines. Am J Transplant. 2001; 1 Suppl 2: 3 - 95
54. European Renal Best Practice Transplantation Guideline Development G. ERBP Guideline on the Management and Evaluation of the Kidney Donor and Recipient. Nephrol Dial Transplant. 2013; 28 Suppl 2: ii1-71.
55. Olbrisch ME, Benedict SM, Ashe K, et al. Psychological assessment and care of organ transplant patients. J Consult Clin Psychol. 2002; 70: 771 - 783.
56. Dew MA, Switzer GE, DiMartini AF, et al. Psychosocial assessments and outcomes in organ transplantation. Prog Transplant. 2000; 10: 239 - 259.
57. Broggi E, Bruyere F, Gaudez F, et al. Risk factors of severe incisional hernia after renal transplantation: a retrospective multicentric casecontrol study on 225 patients. World J Urol. 2017; 35: 1111 - 1117.
58. Ooms LS, Verhelst J, Jeekel J, et al. Incidence, risk factors, and treatment of incisional hernia after kidney transplantation: An analysis of 1,564 consecutive patients. Surgery. 2016; 159: 1407 - 1411
59. Smith CT, Katz MG, Foley D, et al. Incidence and risk factors of incisional hernia formation following abdominal organ transplantation. Surg Endosc. 2015; 29: 398 - 404.
60. NIH National Institute of Diabetes and Digestive and Kidney Diseases. Overweight & Obesity Statistics. (2017). https://www.niddk.nih.gov/health-information/health-statistics/Pages/overweight-obesity-statistics.aspx (Accessed February 28, 2020).
61. Nylund KM, Meurman JH, Heikkinen AM, et al. Oral health in patients with renal disease: a longitudinal study from predialysis to kidney transplantation. Clin Oral Investig. 2018; 22: 339 - 347.
62. Nylund K, Meurman JH, Heikkinen AM, et al. Oral health in predialysis patients with emphasis on periodontal disease. Quintessence Int. 2015; 46: 899 - 907.
63. Veisa G, Tasmoc A, Nistor I, et al. The impact of periodontal disease on physical and psychological domains in long-term hemodialysis patients: a cross-sectional study. Int Urol Nephrol. 2017; 49: 1261 - 1266.
64. Grossman DC, Curry SJ, Owens DK, et al. Screening for Prostate Cancer: US Preventive Services Task Force Recommendation Statement. JAMA. 2018; 319: 1901 - 1913.
65. Wong G, Howard K, Webster AC, et al. Screening for renal cancer in recipients of kidney transplants. Nephrol Dial Transplant. 2011; 26: 1729 - 1739.
66. Данович ГМ. Трансплантация почки. М: ГЭОТАР-Медиа; 2013: 848.
67. Smith RA, Andrews KS, Brooks D, et al. Cancer screening in the United States, 2019: A review of current American Cancer Society guidelines and current issues in cancer screening. CA Cancer J Clin. 2019; 69: 184 - 210.
68. Siu AL. Screening for Breast Cancer: U.S. Preventive Services Task Force Recommendation Statement. Ann Intern Med. 2016; 164: 279 - 296.
69. Sanders RD, Bottle A, Jameson SS, et al. Independent preoperative predictors of outcomes in orthopedic and vascular surgery: the influence of time interval between an acute coronary syndrome or stroke and the operation. Ann Surg. 2012; 255: 901 - 907.
70. Jorgensen ME, Torp-Pedersen C, Gislason GH, et al. Time elapsed after ischemic stroke and risk of adverse cardiovascular events and mortality following elective noncardiac surgery. JAMA. 2014; 312: 269 - 277.
71. LeFevre ML, Force USPST. Screening for asymptomatic carotid artery stenosis: U.S. Preventive Services Task Force recommendation statement. Ann Intern Med. 2014; 161: 356 - 362.
72. Rossitter CW, Vigo RB, Gaber AO, et al. Evaluation of Carotid Ultrasonography Screening Among Kidney Transplant Candidates: A Single-Center, Retrospective Study. Transplant Direct. 2017; 3: e135.
73. Chadban SJ, Staplin ND. Is it time to increase access to transplantation for those with diabetic end-stage kidney disease? Kidney Int. 2014; 86: 464 - 466.
74. Keddis MT, El Ters M, Rodrigo E, et al. Enhanced posttransplant management of patients with diabetes improves patient outcomes. Kidney Int. 2014; 86: 610 - 618.
75. Boucek P, Saudek F, Pokorna E, et al. Kidney transplantation in type 2 diabetic patients: a comparison with matched non-diabetic subjects. Nephrol Dial Transplant. 2002; 17: 1678 - 1683.
76. Yates CJ, Fourlanos S, Hjelmesaeth J, et al. New-onset diabetes after kidney transplantation-changes and challenges. Am J Transplant. 2012; 12: 820 - 828.
77. Argente-Pla M,  A, Martinez-Millana A, et al. Simultaneous Pancreas Kidney Transplantation Improves Cardiovascular Autonomic Neuropathy with Improved Valsalva Ratio as the Most Precocious Test. J Diabetes Res. 2020; 7574628. doi: 10.1155/2020/7574628.
A, Martinez-Millana A, et al. Simultaneous Pancreas Kidney Transplantation Improves Cardiovascular Autonomic Neuropathy with Improved Valsalva Ratio as the Most Precocious Test. J Diabetes Res. 2020; 7574628. doi: 10.1155/2020/7574628.
78. St Michel D, Donnelly T, Jackson T, et al. Assessing Pancreas Transplant Candidate Cardiac Disease: Preoperative Protocol Development at a Rapidly Growing Transplant Program. Methods Protoc. 2019; 2(4): 82. doi: 10.3390/mps2040082.
79. Chadban SJ, Staplin ND. Is it time to increase access to transplantation for those with diabetic end-stage kidney disease? Kidney Int. 2014; 86: 464 - 466.
80. Мартынов СА, Северина АС, Ларина ИИ, и др. Подготовка пациента с сахарным диабетом 1 типа на заместительной почечной терапии диализом к трансплантации почки. Проблемы Эндокринологии. 2020; 66(6): 18 - 30. https://doi.org/10.14341/probl12686.
81. ![]() G, Kumlien G, Berg UB. ABO-incompatible kidney transplantation in children. Pediatr Transplant. 2011; 15(5): 502 - 4.
G, Kumlien G, Berg UB. ABO-incompatible kidney transplantation in children. Pediatr Transplant. 2011; 15(5): 502 - 4.
82. Hourmant M, Figueres L, Gicquel A, et al. New rules of ABO-compatibility in kidney transplantation. Transfus Clin Biol. 2019; 26(3): 180 - 183.
83. Gloor JM, Lager DJ, Moore SB, et al. ABO-incompatible kidney transplantation using both A2 and non-A2 living donors. Transplantation. 2003; 75: 971 - 977.
84. Bohmig, G.A., et al. Strategies to overcome the ABO barrier in kidney transplantation. Nat Rev Nephrol, 2015. 11: 732.
85. De Clippel D, Baeten M, Torfs A, et al. Screening for HLA antibodies in plateletpheresis donors with a history of transfusion or pregnancy. Transfusion. 2014; 54: 3036 - 3042.
86. Shi X, Lv J, Han W, Zhong X, Xie X, Su B, Ding J. What is the impact of human leukocyte antigen mismatching on graft survival and mortality in renal transplantation? A meta-analysis of 23 cohort studies involving 486,608 recipients. BMC Nephrol. 2018 May 18; 19(1): 116. doi: 10.1186/s12882-018-0908-3. PMID: 29776389; PMCID: PMC5960106.
87. Filippone EJ, Farber JL. Humoral immune response and allograft function in kidney transplantation. Am J Kidney Dis. 2015; 66: 337 - 347.
88. Tait BD, ![]() C, Gebel HM, et al. Consensus guidelines on the testing and clinical management issues associated with HLA and non-HLA antibodies in transplantation. Transplantation. 2013; 95: 19 - 47.
C, Gebel HM, et al. Consensus guidelines on the testing and clinical management issues associated with HLA and non-HLA antibodies in transplantation. Transplantation. 2013; 95: 19 - 47.
89. Shi X, Liu R, Xie X, Lv J, Han W, Zhong X, Ding J. Effect of human leukocyte antigen mismatching on the outcomes of pediatric kidney transplantation: a systematic review and meta-analysis. Nephrol Dial Transplant. 2017 Nov 1; 32(11): 1939 - 1948. doi: 10.1093/ndt/gfx259.
90. Shiferaw WS, Akalu TY, Aynalem YA. Risk Factors for Anemia in Patients with Chronic Renal Failure: A Systematic Review and Meta-Analysis. Ethiop J Health Sci. 2020 Sep; 30(5): 829 - 842. doi: 10.4314/ejhs.v30i5.23. PMID: 33911845; PMCID: PMC8047269.
91. Fowler AJ, Ahmad T, Phull MK, Allard S, Gillies MA, Pearse RM. Meta-analysis of the association between preoperative anaemia and mortality after surgery. Br J Surg. 2015 Oct; 102(11): 1314 - 24. doi: 10.1002/bjs.9861. PMID: 26349842.
92. Allen UD, Preiksaitis JK, AST Infectious Diseases Community of Practice. Epstein-Barr virus and posttransplant lymphoproliferative disorder in solid organ transplantation. Am J Transplant. 2013; 13 Suppl 4: 107 - 120.
93. Malinis M, Boucher HW. Screening of donor and candidate prior to solid organ transplantation-Guidelines from the American Society of Transplantation Infectious Diseases Community of Practice. Clin Transplant. 2019. 33(9): e13548. doi: 10.1111/ctr.13548.
94. Levitsky J, Doucette K, AST Infectious Diseases Community of Practice. Viral hepatitis in solid organ transplantation. Am J Transplant. 2013; 13 Suppl 4: 147 - 168.
95. Burdick RA, Bragg-Gresham JL, Woods JD, et al. Patterns of hepatitis B prevalence and seroconversion in hemodialysis units from three continents: the DOPPS. Kidney Int. 2003; 63: 2222 - 2229.
96. Kidney Disease: Improving Global Outcomes (KDIGO) Hepatitis C Work Group. KDIGO 2018 Clinical Practice Guideline on the Prevention, Diagnosis, Evaluation, and Treatment of Hepatitis C in Chronic Kidney Disease. Kidney Int Suppl. 2018; 8: 91 - 165.
97. Kotton CN, Kumar D, Caliendo AM, et al. Updated international consensus guidelines on the management of cytomegalovirus in solid organ transplantation. Transplantation. 2013; 96: 333 - 360.
98. Hardinger KL, Brennan DC. Cytomegalovirus Treatment in Solid Organ Transplantation: An Update on Current Approaches. Ann Pharmacother. 2024 Nov; 58(11): 1122 - 1133. doi: 10.1177/10600280241237534. Epub 2024 Mar 19. PMID: 38501850.
99. Прокопенко Е.И. Цитомегаловирусная инфекция после трансплантации почки: реальные достижения и перспективы изучения патогенеза, профилактики и лечения. Вестник трансплантологии и искусственных органов. 2019; 21(3): 151 - 165. https://doi.org/10.15825/1995-1191-2019-3-151-165
100. Российские клинические рекомендации по диагностике, лечению и профилактике венозных тромбоэмболических осложнений (ВТЭО). Флебология, Т. 9, выпуск 2, N 4, 2015.
101. Douketis JD, Spyropoulos AC, Spencer FA, et al. Perioperative management of antithrombotic therapy: antithrombotic therapy and prevention of thrombosis, 9th ed: American College of Chest Physicians Evidence-Based Clinical Practice Guidelines. Chest 2012; 141 (2 Suppl): e326-50.
102. Chang CY, Chien YJ, Kao MC, Lin HY, Chen YL, Wu MY. Pre-operative proteinuria, postoperative acute kidney injury and mortality: A systematic review and meta-analysis. Eur J Anaesthesiol. 2021 Jul 1; 38(7): 702 - 714. doi: 10.1097/EJA.0000000000001542
103. Levey AS, Becker C, Inker LA. Glomerular filtration rate and albuminuria for detection and staging of acute and chronic kidney disease in adults: a systematic review. JAMA. 2015 Feb 24; 313(8): 837 - 46. doi: 10.1001/jama.2015.0602. PMID: 25710660; PMCID: PMC4410363.
104. Chen J, Mohler ER, 3rd, Garimella PS, et al. Ankle Brachial Index and Subsequent Cardiovascular Disease Risk in Patients With Chronic Kidney Disease. J Am Heart Assoc. 2016; 5: pii: e003339.
105. Wu SW, Lin CK, Hung TW, et al. Subclinical peripheral arterial disease in renal transplantation. Am J Med Sci. 2014; 347: 267 - 270.
106. Gill JS, Ma I, Landsberg D, et al. Cardiovascular events and investigation in patients who are awaiting cadaveric kidney transplantation. J Am Soc Nephrol. 2005; 16: 808 - 816.
107. Fleisher LA, Fleischmann KE, Auerbach AD, et al. 2014 ACC/AHA guideline on perioperative cardiovascular evaluation and management of patients undergoing noncardiac surgery: a report of the American College of Cardiology/American Heart Association Task Force on practice guidelines. J Am Coll Cardiol. 2014; 64: e77 - 137.
108. Lentine KL, Costa SP, Weir MR, et al. Cardiac disease evaluation and management among kidney and liver transplantation candidates: a scientific statement from the American Heart Association and the American College of Cardiology Foundation: endorsed by the American Society of Transplant Surgeons, American Society of Transplantation, and National Kidney Foundation. Circulation. 2012; 126: 617 - 663.
109. Segall L, Nistor I, Covic A. Heart failure in patients with chronic kidney disease: a systematic integrative review. Biomed Res Int. 2014; 2014: 937398. doi: 10.1155/2014/937398. Epub 2014 May 15. PMID: 24959595; PMCID: PMC4052068.
110. Sarkio S, Halme L, Kyllonen L, et al. Severe gastrointestinal complications after 1,515 adult kidney transplantations. Transpl Int. 2004; 17: 505 - 510.
111. Telkes G, Peter A, Tulassay Z, et al. High frequency of ulcers, not associated with Helicobacter pylori, in the stomach in the first year after kidney transplantation. Nephrol Dial Transplant. 2011; 26: 727 - 732.
112. Hajj P, Ferlicot S, Massoud W, et al. Prevalence of renal cell carcinoma in patients with autosomal dominant polycystic kidney disease and chronic renal failure. Urology, 2009, 74, 631 - 634.
113. Boissier R, Hevia V, Bruins H, et al. The risk of tumour recurrence of patients undergoing renal transplantation for end-stage renal disease after previous treatment for a urological cancer: a systematic review. Eur Urol, 2018, 73, 94 - 108.
114. Boissier R, Hevia V, Bruins H, et al. The risk of tumour recurrence of patients undergoing renal transplantation for end-stage renal disease after previous treatment for a urological cancer: a systematic review. Eur Urol, 2018, 73, 94 - 108.
115. https://uroweb.org/guidelines/renal-transplantation
116. Ильинский И.М., Розенталь Р.Л. Патология почечных аллотрансплантатов. - "Зинатне". - Рига. - 1990. - 175 с.
117. Трансплантология. Руководство для врачей/Под редакцией академика В.И. Шумакова. - Москва. - Медицинское информационное агентство. - 2006. - 540 с.
118. Тырин В.В. Пункционная биопсия трансплантированной почки в интерпретации ее дисфункции и выборе тактики лечения/Автореферат диссертации ... доктора медицинских наук. - Москва. - 2006. - 50 с.
119. Suhorukov Vadim. The role of core biopsy in kidney graft pathology diagnostics/Summary of Doctoral Thesis for obtaining a Doctor of Medicine degree Speciality - Transplantation. - Riga. - 2011. - 38 p.
120. Столяревич Е.С. Хроническая дисфункция трансплантированной почки: морфологическая картина, особенности течения, подходы к профилактике и лечению/Автореферат диссертации ... доктора медицинских наук. - Москва. - 2010. - 48 с.
121. Столяревич Е.С. Хроническая трансплантационная нефропатия: клинико-морфологические сопоставления и факторы прогрессирования/Автореферат диссертации ... кандидата медицинских наук. - Москва. - 2002. - 25 с.
122. Малов И.П. Гистологическое и иммуноморфологическое исследование аллотрансплантированных почек в позднем послеоперационном периоде/Автореферат диссертации ... кандидата медицинских наук. - Москва. - 2002. - 27 с.
123. Шумаков В.И., Ильинский И.М., Белецкая Л.В., Малов И.П., Тырин В.В., Зайденов В.А., Томилина Н.А. Гистологическое и иммуноморфологическое исследование хронического отторжения аллотрансплантированных почек//Вестник трансплантологии и искусственных органов. - 2000. - N 3. - С. 30 - 34.
124. Шумаков В.И., Малов И.П., Ильинский И.М., Тырин В.В., Белецкая Л.В., Зайденов В.В., Томилина Н.А., Гордюшина В.С. Виды патологии аллотрансплантированных трупных почек в позднем послеоперационном периоде по данным исследования пункционных биоптатов//Вестник трансплантологии и искусственных органов. - 2000. - N 1. - С. 11 - 14.
125. Ротова И.Д. Гистологическая и иммуногистохимическая диагностика цитомегаловирусной инфекции в пункционных биоптатах аллотрансплантированных почек/Автореферат диссертации ... кандидата медицинских наук. - Москва. - 2007. - 23 с.
126. Pham PT, Pham PM, Pham SV, Pham PA, Pham PC. New onset diabetes after transplantation (NODAT): an overview. Diabetes Metab Syndr Obes. 2011; 4: 175 - 86. doi: 10.2147/DMSO.S19027.
127. Vincenti F, Friman S, Scheuermann E, Rostaing L, Jenssen T, Campistol JM, Uchida K, Pescovitz MD, Marchetti P, Tuncer M, Citterio F, Wiecek A, Chadban S, El-Shahawy M, Budde K, Goto N; DIRECT (Diabetes Incidence after Renal Transplantation: Neoral C Monitoring Versus Tacrolimus) Investigators. Results of an international, randomized trial comparing glucose metabolism disorders and outcome with cyclosporine versus tacrolimus. Am J Transplant. 2007 Jun; 7(6): 1506 - 14. doi: 10.1111/j.1600-6143.2007.01749.x.
128. Kasiske BL, Snyder JJ, Gilbertson D, Matas AJ. Diabetes mellitus after kidney transplantation in the United States. Am J Transplant. 2003 Feb; 3(2): 178 - 85. doi: 10.1034/j.1600-6143.2003.00010.x. PMID: 12603213.
129. Ojo AO. Cardiovascular complications after renal transplantation and their prevention. Transplantation. 2006 Sep 15; 82(5): 603 - 11. doi: 10.1097/01.tp.0000235527.81917.fe. PMID: 16969281.
130. Hjelmesaeth J, Hartmann A, Leivestad T, Holdaas H, Sagedal S, Olstad M, Jenssen T. The impact of early-diagnosed new-onset post-transplantation diabetes mellitus on survival and major cardiac events. Kidney Int. 2006 Feb; 69(3): 588 - 95. doi: 10.1038/sj.ki.5000116. PMID: 16395250.].
131. Spoto B, Pisano A, Zoccali C. Insulin resistance in chronic kidney disease: a systematic review. Am J Physiol Renal Physiol. 2016 Dec 1; 311(6): F1087 - F1108. doi: 10.1152/ajprenal.00340.2016. Epub 2016 Oct 5. PMID: 27707707.
132. Thomas G, Sehgal AR, Kashyap SR, Srinivas TR, Kirwan JP, Navaneethan SD. Metabolic syndrome and kidney disease: a systematic review and meta-analysis. Clin J Am Soc Nephrol. 2011 Oct; 6(10): 2364 - 73. doi: 10.2215/CJN.02180311. Epub 2011 Aug 18. PMID: 21852664; PMCID: PMC3186450.
133. Van Loo, A.A., et al. Pretransplantation hemodialysis strategy influences early renal graft function. J Am Soc Nephrol, 1998. 9: 473. https://www.ncbi.nlm.nih.gov/pubmed/9513911
134. Abramowicz, D., et al. European Renal Best Practice Guideline on kidney donor and recipient evaluation and perioperative care. Nephrol Dial Transplant, 2015. 30: 1790. https://www.ncbi.nlm.nih.gov/pubmed/25007790
135. Task Force for Preoperative Cardiac Risk. Guidelines for pre-operative cardiac risk assessment and perioperative cardiac management in non-cardiac surgery. Eur Heart J, 2009. 30: 2769. https://academic.oup.com/eurheartj/article/30/22/2769/478458
136. Benahmed, A., et al. Ticlopidine and clopidogrel, sometimes combined with aspirin, only minimally increase the surgical risk in renal transplantation: A case-control study. Nephrol Dial Transplant, 2014. 29: 463. https://www.ncbi.nlm.nih.gov/pubmed/24275542
137. Osman, Y., et al. Necessity of Routine Postoperative Heparinization in Non-Risky Live-Donor Renal Transplantation: Results of a Prospective Randomized Trial. Urology, 2007. 69: 647. https://www.ncbi.nlm.nih.gov/pubmed/17445644
138. Guerra R, Kawano PR, Amaro MP, Yamamoto HA, Gomes Filho FF, Amaro JL, El Dib RP, Garcia-Perdomo HA, Reis LO. Acute graft thrombosis in patients who underwent renal transplant and received anticoagulant or antiplatelet agents. A systematic review and meta-analysis. Am J Clin Exp Urol. 2022 Jun 15; 10(3): 129 - 141. PMID: 35874286; PMCID: PMC9301061.
139. Surianarayanan V, Hoather TJ, Tingle SJ, Thompson ER, Hanley J, Wilson CH. Interventions for preventing thrombosis in solid organ transplant recipients. Cochrane Database Syst Rev. 2021 Mar 15; 3(3): CD011557. doi: 10.1002/14651858.CD011557.pub2. PMID: 33720396; PMCID: PMC8094924.
140. Orlando, G., et al. One-shot versus multidose perioperative antibiotic prophylaxis after kidney transplantation: a randomized, controlled clinical trial. Surgery, 2015. 157: 104. https://www.ncbi.nlm.nih.gov/pubmed/25304836
141. Choi, S.U., et al. Clinical significance of prophylactic antibiotics in renal transplantation. Transplant Proc, 2013. 45: 1392. https://www.ncbi.nlm.nih.gov/pubmed/23726580
142. Chan S, Ng S, Chan HP, Pascoe EM, Playford EG, Wong G, Chapman JR, Lim WH, Francis RS, Isbel NM, Campbell SB, Hawley CM, Johnson DW. Perioperative antibiotics for preventing post-surgical site infections in solid organ transplant recipients. Cochrane Database Syst Rev. 2020 Aug 4; 8(8): CD013209. doi: 10.1002/14651858.CD013209.pub2. PMID: 32799356; PMCID: PMC7437398.
143. O'Malley, C.M., et al. A randomized, double-blind comparison of lactated Ringer's solution and 0.9% NaCl during renal transplantation. Anesth Analg, 2005. 100: 1518. https://www.ncbi.nlm.nih.gov/pubmed/15845718
144. Othman, M.M., et al. The impact of timing of maximal crystalloid hydration on early graft function during kidney transplantation. Anesth Analg, 2010. 110: 1440. https://www.ncbi.nlm.nih.gov/pubmed/20418304
145. Dalton, R.S., et al. Physiologic impact of low-dose dopamine on renal function in the early post renal transplant period. Transplantation, 2005. 79: 1561. https://www.ncbi.nlm.nih.gov/pubmed/15940046
146. Ciapetti, M., et al. Low-dose dopamine in kidney transplantation. Transplant Proc, 2009. 41: 4165. https://www.ncbi.nlm.nih.gov/pubmed/20005360
147. Chedid, M.F., et al. Living donor kidney transplantation using laparoscopically procured multiple renal artery kidneys and right kidneys. J Am Coll Surg, 2013. 217: 144.
148. Dalton, R.S., et al. Physiologic impact of low-dose dopamine on renal function in the early post renal transplant period. Transplantation, 2005. 79: 1561. https://pubmed.ncbi.nlm.nih.gov/15940046
149. Ciapetti, M., et al. Low-dose dopamine in kidney transplantation. Transplant Proc, 2009. 41: 4165. https://pubmed.ncbi.nlm.nih.gov/20005360
150. Hanif, F., et al. Outcome of renal transplantation with and without intra-operative diuretics. Int J Surg, 2011. 9: 460
151. Joseph S. et al. Guidelines on the use of therapeutic apheresis in clinical practice - evidence-based approach from the writing committee of the American Society for Apheresis: the 7th special issue. Journal of Clinical Apheresis 2016. 31: 149 - 338.
152. Мойсюк Я.Г., Сушков А.И. Несовместимые по группе крови родственные трансплантации почки: отдаленные результаты. Альманах клинической медицины. 2017; 45(7): 535 - 546. https://doi.org/10.18786/2072-0505-2017-45-7-535-546.
153. Veroux M, Zerbo D, Basile G, et al. Simultaneous Native Nephrectomy and Kidney Transplantation in Patients With Autosomal Dominant Polycystic Kidney Disease. PLoS One. 2016; 11: e0155481.
154. Chebib FT, Prieto M, Jung Y, et al. Native Nephrectomy in Renal Transplant Recipients with Autosomal Dominant Polycystic Kidney Disease. Transplant Direct. 2015; 1: e43.
155. Ahmad SB, Inouye B, Phelan MS, et al. Live Donor Renal Transplant With Simultaneous Bilateral Nephrectomy for Autosomal Dominant Polycystic Kidney Disease Is Feasible and Satisfactory at Long-term Follow-up. Transplantation. 2016; 100: 407 - 415.
156. Биктимиров, Т.Р. Оперативное лечение аутосомно-доминантного поликистоза почек/Т.Р. Биктимиров, А.Г. Мартов, Р.Г. Биктимиров, А.В. Баранов, И.А. Милосердов, А.А. Капутовский, А.М. Хитрых//Урология. - 2021. - N 4. - С. 121 - 125. DOI: 10.18565/urology.2021.4.121-125
157. Hajj P, Ferlicot S, Massoud W, et al. Prevalence of renal cell carcinoma in patients with autosomal dominant polycystic kidney disease and chronic renal failure. Urology, 2009, 74, 631 - 634.
158. Phelan, P.J., et al. Left versus right deceased donor renal allograft outcome. Transpl Int, 2009. 22: 1159. https://www.ncbi.nlm.nih.gov/pubmed/19891044
159. Ciudin, A., et al. Transposition of iliac vessels in implantation of right living donor kidneys. Transplant Proc, 2012. 44: 2945. https://www.ncbi.nlm.nih.gov/pubmed/23195003
160. Feng, J.Y., et al. Renal vein lengthening using gonadal vein reduces surgical difficulty in living-donor kidney transplantation. World J Surg, 2012. 36: 468. https://www.ncbi.nlm.nih.gov/pubmed/21882021
161. Nghiem, D.D. Use of spiral vein graft in living donor renal transplantation. Clin Transplant, 2008. 22: 719. https://www.ncbi.nlm.nih.gov/pubmed/18673376
162. Matheus, W.E., et al. Kidney transplant anastomosis: internal or external iliac artery? Urol J, 2009. 6: 260. https://www.ncbi.nlm.nih.gov/pubmed/20027554.
163. Галеев, Ш.Р. Пересадка почки при вариантных формах почечных сосудов: специальность 14.00.27: диссертация на соискание ученой степени кандидата медицинских наук/Галеев Шамиль Ринатович. - Казань, 2005. - 104 с. - EDN NPZQCN.
164. El-Sherbiny, M., et al. The use of the inferior epigastric artery for accessory lower polar artery revascularization in live donor renal transplantation. Int Urol Nephrol, 2008. 40: 283. https://www.ncbi.nlm.nih.gov/pubmed/17721826
165. Firmin, L.C., et al. The use of explanted internal iliac artery grafts in renal transplants with multiple arteries. Transplantation, 2010. 89: 766. https://www.ncbi.nlm.nih.gov/pubmed/20308866
166. Oertl, A.J., et al. Saphenous vein interposition as a salvage technique for complex vascular situations during renal transplantation. Transplant Proc, 2007. 39: 140. https://www.ncbi.nlm.nih.gov/pubmed/17275492
167. Alberts, V.P., et al. Ureterovesical anastomotic techniques for kidney transplantation: a systematic review and meta-analysis. Transpl Int, 2014. 27: 593. https://www.ncbi.nlm.nih.gov/pubmed/24606191
168. Slagt, I.K., et al. A randomized controlled trial comparing intravesical to extravesical ureteroneocystostomy in living donor kidney transplantation recipients. Kidney Int, 2014. 85: 471. https://www.ncbi.nlm.nih.gov/pubmed/24284515
169. Dadkhah, F., et al. Modified ureteroneocystostomy in kidney transplantation to facilitate endoscopic management of subsequent urological complications. Int Urol Nephrol, 2010. 42: 285. https://www.ncbi.nlm.nih.gov/pubmed/19760513
170. Сайдулаев Д.А., Милосердов И.А., Готье С.В. Профилактика и хирургические методы лечения урологических осложнений у реципиентов почки. Вестник трансплантологии и искусственных органов. 2019; 21(3): 166 - 173. https://doi.org/10.15825/1995-1191-2019-3-166-173
171. Timsit, M.O., et al. Should routine pyeloureterostomy be advocated in adult kidney transplantation? A prospective study of 283 recipients. J Urol, 2010. 184: 2043. https://www.ncbi.nlm.nih.gov/pubmed/20850818
172. Kehinde, E.O., et al. Complications associated with using nonabsorbable sutures for ureteroneocystostomy in renal transplant operations. Transplant Proc, 2000. 32: 1917. https://www.ncbi.nlm.nih.gov/pubmed/11119999
173. Сайдулаев Д.А., Садовников С.В., Биктимиров Р.Г., Гаджиева П.М., Милосердов И.А. Успешные клинические случаи реконструктивно пластических лапароскопических операций на мочеточнике трансплантированной почки. Вестник трансплантологии и искусственных органов. 2021; 23(3): 61 - 65. https://doi.org/10.15825/1995-1191-2021-3-61-65
174. Галеев Р.Х. Полное замещение мочеточника лоскутом мочевого пузыря (операция Боари) после пересадки донорской почки/Р.Х. Галеев, Р.Ш. Гильмутдинов, Д.А. Назаров, С.П. Мартыненко//Урология. - 2003. - N 3. - С. 58 - 60.
175. Лопаткин Н.А. Урологические осложнения при трансплантаци почки/Н.А. Лопаткин, М.Ф. Трапезникова, Д.В. Перлин [и др.]. - М.: Издательский дом ГЭОТАР-МЕД, 2004. - 224 с.
176. Wilson, C.H., et al. Routine intraoperative ureteric stenting for kidney transplant recipients. Cochrane Database Syst Rev, 2013: CD004925. https://www.ncbi.nlm.nih.gov/pubmed/23771708
177. Tavakoli, A., et al. Impact of stents on urological complications and health care expenditure in renal transplant recipients: results of a prospective, randomized clinical trial. J Urol, 2007. 177: 2260. https://www.ncbi.nlm.nih.gov/pubmed/17509336.
178. Heidari, M., et al. Transplantation of kidneys with duplicated ureters. Scand J Urol Nephrol, 2010. 44: 337. https://www.ncbi.nlm.nih.gov/pubmed/20653492
179. Alberts, V.P., et al. Duplicated ureters and renal transplantation: a case-control study and review of the literature. Transplant Proc, 2013. 45: 3239. https://www.ncbi.nlm.nih.gov/pubmed/24182792
180. Roach, J. P., Bock, M. E., & Goebel, J. (2017). Pediatric kidney transplantation. Seminars in Pediatric Surgery, 26(4), 233 - 240. doi: 10.1053/j.sempedsurg.2017.07.006.
181. Ghane Sharbaf F, Bitzan M, Szymanski KM, et al. Native nephrectomy prior to pediatric kidney transplantation: biological and clinical aspects. Pediatr Nephrol. 2012; 27: 1179 - 1188.
182. Dimitroulis, D., et al. Vascular complications in renal transplantation: a single-center experience in 1367 renal transplantations and review of the literature. Transplant Proc, 2009. 41: 1609. https://www.ncbi.nlm.nih.gov/pubmed/19545690
183. Pawlicki, J., et al. Risk factors for early hemorrhagic and thrombotic complications after kidney transplantation. Transplant Proc, 2011. 43: 3013. https://www.ncbi.nlm.nih.gov/pubmed/21996213
184. Rouviere, O., et al. Acute thrombosis of renal transplant artery: graft salvage by means of intra-arterial fibrinolysis. Transplantation, 2002. 73: 403. https://www.ncbi.nlm.nih.gov/pubmed/11884937
185. Domagala, P., et al. Complications of transplantation of kidneys from expanded-criteria donors. Transplant Proc, 2009. 41: 2970. https://www.ncbi.nlm.nih.gov/pubmed/19857652
186. Giustacchini, P., et al. Renal vein thrombosis after renal transplantation: an important cause of graft loss. Transplant Proc, 2002. 34: 2126. https://www.ncbi.nlm.nih.gov/pubmed/12270338
187. Wuthrich, R.P. Factor V Leiden mutation: potential thrombogenic role in renal vein, dialysis graft and transplant vascular thrombosis. Curr Opin Nephrol Hypertens, 2001. 10: 409. https://www.ncbi.nlm.nih.gov/pubmed/11342806
188. Parajuli, S., et al. Hypercoagulability in Kidney Transplant Recipients. Transplantation, 2016. 100: 719. https://www.ncbi.nlm.nih.gov/pubmed/26413991
189. Granata, A., et al. Renal transplant vascular complications: the role of Doppler ultrasound. J Ultrasound, 2015. 18: 101. https://www.ncbi.nlm.nih.gov/pubmed/26191097
190. Hogan, J.L., et al. Late-onset renal vein thrombosis: A case report and review of the literature. Int J Surg Case Rep, 2015. 6C: 73. https://www.ncbi.nlm.nih.gov/pubmed/25528029
191. Hurst, F.P., et al. Incidence, predictors and outcomes of transplant renal artery stenosis after kidney transplantation: analysis of USRDS. Am J Nephrol, 2009. 30: 459. https://www.ncbi.nlm.nih.gov/pubmed/19776559
192. Willicombe, M., et al. Postanastomotic transplant renal artery stenosis: association with de novo class II donor-specific antibodies. Am J Transplant, 2014. 14: 133. https://www.ncbi.nlm.nih.gov/pubmed/24354873
193. Ghazanfar, A., et al. Management of transplant renal artery stenosis and its impact on long-term allograft survival: a single-centre experience. Nephrol Dial Transplant, 2011. 26: 336. https://www.ncbi.nlm.nih.gov/pubmed/20601365
194. Seratnahaei, A., et al. Management of transplant renal artery stenosis. Angiology, 2011. 62: 219. https://www.ncbi.nlm.nih.gov/pubmed/20682611
195. Atray, N.K., et al. Post transplant lymphocele: a single centre experience. Clin Transplant, 2004. 18 Suppl 12: 46. https://www.ncbi.nlm.nih.gov/pubmed/15217407
196. Ulrich, F., et al. Symptomatic lymphoceles after kidney transplantation - multivariate analysis of risk factors and outcome after laparoscopic fenestration. Clin Transplant, 2010. 24: 273. https://www.ncbi.nlm.nih.gov/pubmed/19719727
197. Lucewicz, A., et al. Management of primary symptomatic lymphocele after kidney transplantation: a systematic review. Transplantation, 2011. 92: 663. https://www.ncbi.nlm.nih.gov/pubmed/21849931
198. Capocasale, E., et al. Octreotide in the treatment of lymphorrhea after renal transplantation: a preliminary experience. Transplant Proc, 2006. 38: 1047. https://www.ncbi.nlm.nih.gov/pubmed/16757259
199. Kayler, L., et al. Kidney transplant ureteroneocystostomy techniques and complications: review of the literature. Transplant Proc, 2010. 42: 1413. https://www.ncbi.nlm.nih.gov/pubmed/20620446
200. Secin, F.P., et al. Comparing Taguchi and Lich-Gregoir ureterovesical reimplantation techniques for kidney transplants. J Urol, 2002. 168: 926. https://www.ncbi.nlm.nih.gov/pubmed/12187192
201. Dinckan, A., et al. Early and late urological complications corrected surgically following renal transplantation. Transpl Int, 2007. 20: 702. https://www.ncbi.nlm.nih.gov/pubmed/17511829
202. Kumar, A., et al. Evaluation of the urological complications of living related renal transplantation at a single center during the last 10 years: impact of the Double-J* stent. J Urol, 2000. 164: 657. https://www.ncbi.nlm.nih.gov/pubmed/10953120
203. Mazzucchi, E., et al. Primary reconstruction is a good option in the treatment of urinary fistula after kidney transplantation. Int Braz J Urol, 2006. 32: 398. https://www.ncbi.nlm.nih.gov/pubmed/16953905
204. Davari, H.R., et al. Urological complications in 980 consecutive patients with renal transplantation. Int J Urol, 2006. 13: 1271. https://www.ncbi.nlm.nih.gov/pubmed/17010003
205. Sabnis, R.B., et al. The development and current status of minimally invasive surgery to manage urological complications after renal transplantation. Indian J Urol, 2016. 32: 186. https://www.ncbi.nlm.nih.gov/pubmed/27555675
206. Suttle, T., et al. Comparison of Urologic Complications Between Ureteroneocystostomy and Ureteroureterostomy in Renal Transplant: A Meta-Analysis. Exp Clin Transplant, 2016. 14: 276. https://www.ncbi.nlm.nih.gov/pubmed/26925612
207. Breda, A., et al. Incidence of ureteral strictures after laparoscopic donor nephrectomy. J Urol, 2006. 176: 1065. https://www.ncbi.nlm.nih.gov/pubmed/16890691
208. Kaskarelis, I., et al. Ureteral complications in renal transplant recipients successfully treated with interventional radiology. Transplant Proc, 2008. 40: 3170. https://www.ncbi.nlm.nih.gov/pubmed/19010224
209. He, B. Classification of ureteral stenosis and associated strategy for treatment after kidney transplant/B. He, A. Bremner, Y. Han. - Текст: непосредственный//Experimental and Clinical Transplantation. - 2013. - Vol. 11. - Iss. 2. - P. 122 - 127. doi: 10.6002/ect.2012.0179.
210. Kristo, B., et al. Treatment of renal transplant ureterovesical anastomotic strictures using antegrade balloon dilation with or without holmium: YAG laser endoureterotomy. Urology, 2003. 62: 831. https://www.ncbi.nlm.nih.gov/pubmed/14624903
211. Nie, Z., et al. Comparison of urological complications with primary ureteroureterostomy versus conventional ureteroneocystostomy. Clin Transplant, 2010. 24: 615. https://www.ncbi.nlm.nih.gov/pubmed/19925475
212. Chaykovska, L., et al. Kidney transplantation into urinary conduits with ureteroureterostomy between transplant and native ureter: single-center experience. Urology, 2009. 73: 380. https://www.ncbi.nlm.nih.gov/pubmed/19022489
213. Helfand, B.T., et al. Reconstruction of late-onset transplant ureteral stricture disease. BJU Int, 2011. 107: 982. https://www.ncbi.nlm.nih.gov/pubmed/20825404
214. Liu, Y., et al. Basiliximab or antithymocyte globulin for induction therapy in kidney transplantation: a meta-analysis. Transplant Proc, 2010. 42: 1667. https://www.ncbi.nlm.nih.gov/pubmed/20620496
215. Sun, Z.J., et al. Efficacy and Safety of Basiliximab Versus Daclizumab in Kidney Transplantation: A Meta-Analysis. Transplant Proc, 2015. 47: 2439. https://www.ncbi.nlm.nih.gov/pubmed/26518947
216. 216Webster, A.C., et al. Interleukin 2 receptor antagonists for kidney transplant recipients. Cochrane Database Syst Rev, 2010: CD003897. https://www.ncbi.nlm.nih.gov/pubmed/20091551
217. Bamoulid, J., et al. Immunosuppression and Results in Renal Transplantation. Eur UrolSuppl, 2016. 15: 415. https://www.sciencedirect.com/science/article/pii/S1569905616300823
218. Kidney Disease Improving Global Outcomes Transplant Work Group. KDIGO clinical practice guideline for the care of kidney transplant recipients. Am J Transplant, 2009. 9 Suppl 3: S1. https://www.ncbi.nlm.nih.gov/pubmed/19845597
219. Jones-Hughes, T., et al. Immunosuppressive therapy for kidney transplantation in adults: a systematic review and economic model. Health Technol Assess, 2016. 20: 1. https://www.ncbi.nlm.nih.gov/pubmed/27578428
220. Bamoulid, J., et al. Anti-thymocyte globulins in kidney transplantation: focus on current indications and long-term immunological side effects. Nephrol Dial Transplant, 2016. https://www.ncbi.nlm.nih.gov/pubmed/27798202
221. Malvezzi, P., et al. Induction by anti-thymocyte globulins in kidney transplantation: a review of the literature and current usage. J Nephropathol, 2015. 4: 110. https://www.ncbi.nlm.nih.gov/pubmed/26457257
222. Nashan B. Review of the proliferation inhibitor everolimus. ExpertOpin Investig Drugs, 2002; 11: 1845 - 1857.
223. Knight S.R., Morris P.J. Does the evidence support the use of mycophenolate mofetil therapeutic drug monitoring in clinical practice? A systematic review. Transplantation, 2008; 85: p. 1675 - 1685.
224. Kyllonen L.E., Salmela K.T.. Early cyclosporine C0 and C2 monitoring in de novo kidney transplant patients: A prospective randomized single-center pilot study. Transplantation, 2006; 81: 1010 - 1015.
225. Bamoulid, J., et al. The need for minimization strategies: current problems of immunosuppression. Transpl Int, 2015. 28: 891. https://www.ncbi.nlm.nih.gov/pubmed/25752992
226. Leas, B.F., et al., in Calcineurin Inhibitors for Renal Transplant. 2016: Rockville.
227. Webster, A.C., et al. Tacrolimus versus ciclosporin as primary immunosuppression for kidney transplant recipients: meta-analysis and meta-regression of randomised trial data. BMJ, 2005. 331: 810. https://www.ncbi.nlm.nih.gov/pubmed/16157605.
228. Sawinski, D., et al. Calcineurin Inhibitor Minimization, Conversion, Withdrawal, and Avoidance Strategies in Renal Transplantation: A Systematic Review and Meta-Analysis. Am J Transplant, 2016. 16: 2117. https://www.ncbi.nlm.nih.gov/pubmed/26990455.
229. Caillard, S., et al. Advagraf((R)), a once-daily prolonged release tacrolimus formulation, in kidney transplantation: literature review and guidelines from a panel of experts. Transpl Int, 2016. 29: 860. https://www.ncbi.nlm.nih.gov/pubmed/26373896.
230. McCormack, P.L. Extended-release tacrolimus: a review of its use in de novo kidney transplantation. Drugs, 2014. 74: 2053. https://www.ncbi.nlm.nih.gov/pubmed/25352392.
231. Molnar, A.O., et al. Generic immunosuppression in solid organ transplantation: systematic review and meta-analysis. BMJ, 2015. 350: h3163. https://www.ncbi.nlm.nih.gov/pubmed/26101226.
232. Staatz, C.E., et al. Clinical Pharmacokinetics of Once-Daily Tacrolimus in Solid-Organ Transplant Patients. Clin Pharmacokinet, 2015. 54: 993. https://www.ncbi.nlm.nih.gov/pubmed/26038096.
233. van Gelder, T., et al. European Society for Organ Transplantation Advisory Committee recommendations on generic substitution of immunosuppressive drugs. Transpl Int, 2011. 24: 1135. https://www.ncbi.nlm.nih.gov/pubmed/22032583.
234. Diekmann, F. Immunosuppressive minimization with mTOR inhibitors and belatacept. Transpl Int, 2015. 28: 921. https://www.ncbi.nlm.nih.gov/pubmed/25959589.
235. Burton SA, Amir N, Asbury A, Lange A, Hardinger KL. Treatment of antibody-mediated rejection in renal transplant patients: a clinical practice survey. Clin Transplant 2015; 29; 118 - 123.
236. Ruangkanchanasetr P et al. Intensive plasmapheresis and intravenous immunoglobulin for treatment of antibody-mediated rejection after kidney transplant. Exp Clin Transplant 2014; 12; 328 - 333.
237. Сушков А.И., Шаршаткин А.В. Трудные решения при лечении острого гуморального отторжения пересаженной почки. Вестник трансплантологии и искусственных органов. 2016; 18(2): 125 - 130. https://doi.org/10.15825/1995-1191-2016-2-125-130
238. Kamar, N., et al. Calcineurin inhibitor-sparing regimens based on mycophenolic acid after kidney transplantation. Transpl Int, 2015. 28: 928. https://www.ncbi.nlm.nih.gov/pubmed/25557802.
239. Snanoudj, R., et al. Immunological risks of minimization strategies. Transpl Int, 2015. 28: 901. https://www.ncbi.nlm.nih.gov/pubmed/25809144.
240. Budde, K., et al. Enteric-coated mycophenolate sodium. Expert Opin Drug Saf, 2010. 9: 981. https://www.ncbi.nlm.nih.gov/pubmed/20795786.
241. Cooper, M., et al. Enteric-coated mycophenolate sodium immunosuppression in renal transplant patients: efficacy and dosing. Transplant Rev (Orlando), 2012. 26: 233. https://www.ncbi.nlm.nih.gov/pubmed/22863029.
242. Staatz, C.E., et al. Pharmacology and toxicology of mycophenolate in organ transplant recipients: an update. Arch Toxicol, 2014. 88: 1351. https://www.ncbi.nlm.nih.gov/pubmed/24792322.
243. van Gelder, T., et al. Mycophenolate revisited. Transpl Int, 2015. 28: 508. https://www.ncbi.nlm.nih.gov/pubmed/25758949.
244. Wagner, M., et al. Mycophenolic acid versus azathioprine as primary immunosuppression for kidney transplant recipients. Cochrane Database Syst Rev, 2015: CD007746. https://www.ncbi.nlm.nih.gov/pubmed/26633102.
245. Hirsch, H.H., et al. European perspective on human polyomavirus infection, replication and disease in solid organ transplantation. Clin Microbiol Infect, 2014. 20 Suppl 7: 74. https://www.ncbi.nlm.nih.gov/pubmed/24476010.
246. Le Meur, Y., et al. Therapeutic drug monitoring of mycophenolates in kidney transplantation: report of The Transplantation Society consensus meeting. Transplant Rev (Orlando), 2011. 25: 58. https://www.ncbi.nlm.nih.gov/pubmed/21454067.
247. Mathis, A.S., et al. Calcineurin inhibitor sparing strategies in renal transplantation, part one: Late sparing strategies. World J Transplant, 2014. 4: 57. https://www.ncbi.nlm.nih.gov/pubmed/25032096.
248. Haller, M.C., et al. Steroid avoidance or withdrawal for kidney transplant recipients. Cochrane Database Syst Rev, 2016: CD005632. https://www.ncbi.nlm.nih.gov/pubmed/27546100.
249. Kunz, R., et al. Maintenance therapy with triple versus double immunosuppressive regimen in renal transplantation: a meta-analysis. Transplantation, 1997. 63: 386. https://www.ncbi.nlm.nih.gov/pubmed/9039928.
250. Halleck, F., et al. An evaluation of sirolimus in renal transplantation. Expert Opin Drug Metab Toxicol, 2012. 8: 1337. https://www.ncbi.nlm.nih.gov/pubmed/22928953.
251. Ventura-Aguiar, P., et al. Safety of mTOR inhibitors in adult solid organ transplantation. Expert Opin Drug Saf, 2016. 15: 303. https://www.ncbi.nlm.nih.gov/pubmed/26667069.
252. Witzke, O., et al. Everolimus immunosuppression in kidney transplantation: What is the optimal strategy? Transplant Rev (Orlando), 2016. 30: 3. https://www.ncbi.nlm.nih.gov/pubmed/26603484.
253. Xie, X., et al. mTOR inhibitor versus mycophenolic acid as the primary immunosuppression regime combined with calcineurin inhibitor for kidney transplant recipients: a meta-analysis. BMC Nephrol, 2015. 16: 91. https://www.ncbi.nlm.nih.gov/pubmed/26126806.
254. Shipkova, M., et al. Therapeutic Drug Monitoring of Everolimus: A Consensus Report. Ther Drug Monit, 2016. 38: 143. https://www.ncbi.nlm.nih.gov/pubmed/26982492.
255. Liefeldt, L., et al. Donor-specific HLA antibodies in a cohort comparing everolimus with cyclosporine after kidney transplantation. Am J Transplant, 2012. 12: 1192. https://www.ncbi.nlm.nih.gov/pubmed/22300538.
256. Halleck, F., et al. Transplantation: Sirolimus for secondary SCC prevention in renal transplantation. Nat Rev Nephrol, 2012. 8: 687. https://www.ncbi.nlm.nih.gov/pubmed/23026948.
257. Ponticelli, C., et al. Skin cancer in kidney transplant recipients. J Nephrol, 2014. 27: 385. https://www.ncbi.nlm.nih.gov/pubmed/24809813.
258. Ho J, Okoli GN, Rabbani R, Lam OLT, Reddy VK, Askin N, Rampersad C, Trachtenberg A, Wiebe C, Nickerson P, Abou-Setta AM. Effectiveness of T cell-mediated rejection therapy: A systematic review and meta-analysis. Am J Transplant. 2022 Mar; 22(3): 772 - 785. doi: 10.1111/ajt.16907. Epub 2021 Dec 10. PMID: 34860468; PMCID: PMC9300092.
259. Gray D, Shepherd H, Daar A, Oliver DO, Morris PJ. Oral versus intravenous high-dose steroid treatment of renal allograft rejection. The big shot or not? Lancet. 1978 Jan 21; 1(8056): 117 - 8. doi: 10.1016/s0140-6736(78) 90417-8. PMID: 87551.
260. Stromstad SA, Kauffman HM, Sampson D, Stawicki AT. Randomized steroid therapy of human kidney transplant rejection. Surg Forum. 1978; 29: 376 - 7.
261. Kauffman HM Jr, Stromstad SA, Sampson D, Stawicki AT. Randomized steroid therapy of human kidney transplant rejection. Transplant Proc. 1979 Mar; 11(1): 36 - 8.
262. Lui SF, Sweny P, Scoble JE, Varghese Z, Moorhead JF, Fernando ON. Low-dose vs high-dose intravenous methylprednisolone therapy for acute renal allograft rejection in patients receiving cyclosporin therapy. Nephrol Dial Transplant. 1989; 4(5): 387 - 9. doi: 10.1093/oxfordjournals.ndt.a091895.].
263. Webster AC, Pankhurst T, Rinaldi F, Chapman JR, Craig JC. Monoclonal and polyclonal antibody therapy for treating acute rejection in kidney transplant recipients: a systematic review of randomized trial data. Transplantation. 2006; 81: 953 - 965. doi: 10.1097/01.tp.0000215178.72344.9d.]
264. Eikmans M, Roelen DL, Claas FH. Molecular monitoring for rejection and graft outcome in kidney transplantation. Expert Opin Med Diagn. 2008; 2: 1365 - 1379. doi: 10.1517/17530050802600683.
265. Shinn C, Malhotra D, Chan L, Cosby RL, Shapiro JI. Time course of response to pulse methylprednisolone therapy in renal transplant recipients with acute allograft rejection. Am J Kidney Dis. 1999; 34: 304 - 307. doi: 10.1016/s0272-6386(99)70359-8.
266.  GA, Wahrmann M, Regele H, et al. Immunoadsorption in severe C4d-positive acute kidney allograft rejection: a randomized controlled trial. Am J Transplant. 2007; 7: 117 - 121.
GA, Wahrmann M, Regele H, et al. Immunoadsorption in severe C4d-positive acute kidney allograft rejection: a randomized controlled trial. Am J Transplant. 2007; 7: 117 - 121.
267. Bonomini V, Vangelista A, ![]() GM, et al. Effects of plasmapheresis in renal transplant rejection: a controlled study. Trans Am Soc Artif Intern Organs. 1985; 31: 698 - 703.
GM, et al. Effects of plasmapheresis in renal transplant rejection: a controlled study. Trans Am Soc Artif Intern Organs. 1985; 31: 698 - 703.
268. Blake P, Sutton D, Cardella CJ. Plasma exchange in acute renal transplant rejection. Prog Clin Biol Res. 1990; 337: 249 - 252
269. Wan SS, Ying TD, Wyburn K, Roberts DM, Wyld M, Chadban SJ. The Treatment of Antibody-Mediated Rejection in Kidney Transplantation: An Updated Systematic Review and Meta-Analysis. Transplantation. 2018 Apr; 102(4): 557 - 568. doi: 10.1097/TP.0000000000002049.
270.  GA, Wahrmann M, Regele H, et al. Immunoadsorption in severe c4d-positive acute kidney allograft rejection: a randomized controlled trial. Am J Transplant. 2007; 7: 117 - 121.
GA, Wahrmann M, Regele H, et al. Immunoadsorption in severe c4d-positive acute kidney allograft rejection: a randomized controlled trial. Am J Transplant. 2007; 7: 117 - 121.
271. Lee CY, Lin WC, Wu MS, et al. Repeated cycles of high-dose intravenous immunoglobulin and plasmapheresis for treatment of late antibody-mediated rejection of renal transplants. J Formos Med Assoc. 2016; 115: 845 - 852
272. Schinstock CA, Mannon RB, Budde K, Chong AS, Haas M, Knechtle S, Lefaucheur C, Montgomery RA, Nickerson P, Tullius SG, Ahn C, Askar M, Crespo M, Chadban SJ, Feng S, Jordan SC, Man K, Mengel M, Morris RE, O'Doherty I, Ozdemir BH, Seron D, Tambur AR, Tanabe K, Taupin JL, O'Connell PJ. Recommended Treatment for Antibody-mediated Rejection After Kidney Transplantation: The 2019 Expert Consensus From the Transplantion Society Working Group. Transplantation. 2020; 104(5): 911 - 922. doi: 10.1097/TP.0000000000003095.
273. Roberts DM, Jiang SH, Chadban SJ. The treatment of acute antibody-mediated rejection in kidney transplant recipients - a systematic review. Transplantation. 2012; 94: 775 - 783.
274. Wan SS, Ying TD, Wyburn K, et al. The treatment of antibody-mediated rejection in kidney transplantation: an updated systematic review and meta-analysis. Transplantation. 2018; 102: 557 - 568.
275. Lefaucheur C, Loupy A, Vernerey D, et al. Antibody-mediated vascular rejection of kidney allografts: a population-based study. Lancet. 2013; 381: 313 - 319.]
276. Vo AA, Lukovsky M, Toyoda M, et al. Rituximab and intravenous immune globulin for desensitization during renal transplantation. N Engl J Med. 2008; 359: 242 - 251.
277. Федеральный закон "Об основах охраны здоровья граждан в Российской Федерации" от 21.11.2011 N 323-ФЗ
278. Heiwe S, Jacobson SH. Exercise training in adults with CKD: a systematic review and meta-analysis. Am J Kidney Dis. 2014 Sep; 64(3): 383 - 93. doi: 10.1053/j.ajkd.2014.03.020. Epub 2014 Jun 7. PMID: 24913219.
279. Williams AD, Fassett RG, Coombes JS. Exercise in CKD: why is it important and how should it be delivered? Am J Kidney Dis. 2014 Sep; 64(3): 329 - 31. doi: 10.1053/j.ajkd.2014.06.004. PMID: 25150853.
280. Pei G, Tang Y, Tan L, Tan J, Ge L, Qin W. Aerobic exercise in adults with chronic kidney disease (CKD): a meta-analysis. Int Urol Nephrol. 2019 Oct; 51(10): 1787 - 1795. doi: 10.1007/s11255-019-02234-x. Epub 2019 Jul 22. PMID: 31332699.
281. Parker R, Armstrong MJ, Corbett C, Day EJ, Neuberger JM. Alcohol and substance abuse in solid-organ transplant recipients. Transplantation. 2013 Dec 27; 96(12): 1015 - 24. doi: 10.1097/TP.0b013e31829f7579. PMID: 24025323.
282. Zwaan M, Erim Y,  S, Vitinius F, Buchholz A,
S, Vitinius F, Buchholz A, ![]() M; guideline group "Psychosocial Diagnosis and Treatment of Patients before and after Organ Transplantation"*. Psychosocial Diagnosis and Treatment Before and After Organ Transplantation. Dtsch Arztebl Int. 2023 Jun 16; 120(24): 413 - 416. doi: 10.3238/arztebl.m2023.0087. PMID: 37101343; PMCID: PMC10437037.
M; guideline group "Psychosocial Diagnosis and Treatment of Patients before and after Organ Transplantation"*. Psychosocial Diagnosis and Treatment Before and After Organ Transplantation. Dtsch Arztebl Int. 2023 Jun 16; 120(24): 413 - 416. doi: 10.3238/arztebl.m2023.0087. PMID: 37101343; PMCID: PMC10437037.
283. Pezeshki M, Taherian AA, Gharavy M, Ledger WL. Menstrual characteristics and pregnancy in women after renal transplantation. Int J Gynaecol Obstet 2004; 85(2): 119 - 25. http://www.ncbi.nlm.nih.gov/pubmed/15099772.
284. Bar J, Ben-Rafael Z, Pados A, Orvieto R, Boner G, Hod M. Prediction of pregnancy outcome in subgroups of women with renal disease. Clin Nephrol 2000; 53(6): 437 - 44. http://www.ncbi.nlm.nih.gov/pubmed/10879663.
285. Stratta P, Canavese C, Giacchino F, Mesiano P, Quaglia M, Rossetti M. Pregnancy in kidney transplantation: satisfactory outcomes and harsh realities. J Nephrol 2003; 16(6): 792 - 806. http://www.ncbi.nlm.nih.gov/pubmed/14736006.
286. Mustafa MS, Noorani A, Abdul Rasool A, Tashrifwala FAA, Jayaram S, Raja S, Jawed F, Siddiq MU, Shivappa SG, Hameed I, Dadana S. Pregnancy outcomes in renal transplant recipients: A systematic review and meta-analysis. Womens Health (Lond). 2024 Jan - Dec; 20: 17455057241277520. doi: 10.1177/17455057241277520. PMID: 39287599; PMCID: PMC11418342.
287. Davison JM, Milne JEC. Pregnancy and renal transplantation. Br J Urol 1997; 80 (Suppl 1): 29 - 32. http://www.ncbi.nlm.nih.gov/pubmed/9240221.
288. Sgro MD, Barozzino T, Mirghani HM, Sermer M, Moscato L, Akoury H, Koren G, Chitayat DA. Pregnancy outcome post renal transplantation. Teratology 2002; 65(1): 5 - 9. http://www.ncbi.nlm.nih.gov/pubmed/11835226.
289. Ponticelli C, Zaina B, Moroni G. Planned Pregnancy in Kidney Transplantation. A Calculated Risk. J Pers Med. 2021 Sep 26; 11(10): 956. doi: 10.3390/jpm11100956. PMID: 34683097; PMCID: PMC8537874.
290. Kainz A, Harabacz I, Cowlrick IS, Gadgil SD, Hagiwara D. Review of the course and outcome of 100 pregnancies in 84 women treated with tacrolimus. Transplantation 2000; 70(12): 1718 - 21. http://www.ncbi.nlm.nih.gov/pubmed/11152103.
291. Jain A, Venkataramanan R, Fung JJ, Gartner JC, Lever J, Balan V, Warty V, Starzl TE. Pregnancy after liver transplantation under tacrolimus. Transplantation 1997; 64(4): 559 - 65. http://www.ncbi.nlm.nih.gov/pubmed/9293865.
292. Sifontis NM, Coscia LA, Costantinescu S, Lavelanet AF, Moritz MJ, Armenti VT. Pregnancy outcomes in solid organ transplant recipients with exposure to micophenolate mofetil or sirolimus. Transplantation 2006; 82(12): 1698 - 702. http://www.ncbi.nlm.nih.gov/pubmed/17198262.
293. Bramham K, Nelson-Piercy C, Gao H. et al. Pregnancy in renal transplant recipients: a UK national cohort study. Clin J Am Soc Nephrol 2013; 8: 290 - 298 - PMC - PubMed
294. EBPG Expert Group on Renal Transplantation. European best practice guidelines for renal transplantation. Section IV: Long-term management of the transplant recipient. IV.10. Pregnancy in renal transplant recipients. Nephrol Dial Transplant 2002; 17 (Suppl 4): 50 - 55 - PubMed
295. Nankivell, B.J., et al. Diagnosis and prevention of chronic kidney allograft loss. Lancet, 2011. 378: 1428. https://www.ncbi.nlm.nih.gov/pubmed/22000139.
296. Westall, G.P., et al. Antibody-mediated rejection. Curr Opin Organ Transplant, 2015. 20: 492. https://www.ncbi.nlm.nih.gov/pubmed/26262460.
297. Jardine, A.G., et al. Prevention of cardiovascular disease in adult recipients of kidney transplants. Lancet, 2011. 378: 1419. https://www.ncbi.nlm.nih.gov/pubmed/22000138.
298. Liefeldt, L., et al. Risk factors for cardiovascular disease in renal transplant recipients and strategies to minimize risk. Transpl Int, 2010. 23: 1191. https://www.ncbi.nlm.nih.gov/pubmed/21059108.
299. Boor, P., et al. Renal allograft fibrosis: biology and therapeutic targets. Am J Transplant, 2015. 15: 863. https://www.ncbi.nlm.nih.gov/pubmed/25691290.
300. Westall, G.P., et al. Antibody-mediated rejection. Curr Opin Organ Transplant, 2015. 20: 492. https://www.ncbi.nlm.nih.gov/pubmed/26262460.
301. Chapman, J.R. Chronic calcineurin inhibitor nephrotoxicity-lest we forget. Am J Transplant, 2011. 11: 693.https://www.ncbi.nlm.nih.gov/pubmed/21446974.
302. Higgins, R.M., et al. Antibody-incompatible kidney transplantation in 2015 and beyond. Nephrol Dial Transplant, 2015. 30: 1972.https://www.ncbi.nlm.nih.gov/pubmed/25500804.
303. Naesens, M. Zero-Time Renal Transplant Biopsies: A Comprehensive Review. Transplantation, 2016. 100: 1425. https://www.ncbi.nlm.nih.gov/pubmed/26599490.
304. Kasiske, B.L., et al. The role of procurement biopsies in acceptance decisions for kidneys retrieved for transplant. Clin J Am Soc Nephrol, 2014. 9: 562. https://www.ncbi.nlm.nih.gov/pubmed/24558053.
305. Ujjawal A, Schreiber B, Verma A. Sodium-glucose cotransporter-2 inhibitors (SGLT2i) in kidney transplant recipients: what is the evidence? Ther Adv Endocrinol Metab. 2022 Apr 13; 13: 20420188221090001. doi: 10.1177/20420188221090001. PMID: 35450095; PMCID: PMC9016587.
306. Трансплантология. Фармакотерапия без ошибок//руководство для врачей/под ред. С. В. Готье и Я. Г. Мойсюка. - М.: Е-ното, 2014. - 432 с.
307. Jones-Hughes, T., et al. Immunosuppressive therapy for kidney transplantation in adults: a systematic review and economic model. Health Technol Assess, 2016. 20: 1. https: //pubmed.ncbi.nlm.nih.gov/27578428
308. Leas, B.F., et al., Calcineurin Inhibitors for Renal Transplant. 2016: Rockville (MD): AHRQ. https: //www.ncbi.nlm.nih.gov/books/NBK356377
309. Sawinski, D., et al. Calcineurin Inhibitor Minimization, Conversion, Withdrawal, and Avoidance Strategies in Renal Transplantation: A Systematic Review and Meta-Analysis. Am J Transplant, 2016. 16: 2117.
310. Knechtle SJ, Marson LP, Morris PJ. Kidney transplantation: principles and practice, 8 Edition, 2020, Elsevier
311. "Трансплантология. Фармакотерапия без ошибок" руководство для врачей/под ред. С. В. Готье и Я. Г. Мойсюка. - М.: Е-ното, 2014. - 432 с.
312. Markmann JF, Rickels MR, Eggerman TL, Bridges ND, Lafontant DE, Qidwai J, Foster E, Clarke WR, Kamoun M, Alejandro R, Bellin MD, Chaloner K, Czarniecki CW, Goldstein JS, Hering BJ, Hunsicker LG, Kaufman DB, Korsgren O, Larsen CP, Luo X, Naji A, Oberholzer J, Posselt AM, Ricordi C, Senior PA, Shapiro AMJ, Stock PG, Turgeon NA. Phase 3 trial of human islet-after-kidney transplantation in type 1 diabetes. Am J Transplant. 2021 Apr; 21(4): 1477 - 1492. doi: 10.1111/ajt.16174
313. Catarinella, Davide et al. Long-term outcomes of pancreatic islet transplantation alone in type 1 diabetes: a 20-year single-centre study in Italy. The Lancet Diabetes & Endocrinology, Volume 13, Issue 4, 279 - 293
314. Maanaoui, Mehdi Armanet, Mathieu et al. Islet-after-kidney transplantation versus kidney alone in kidney transplant recipients with type 1 diabetes (KAIAK): a population-based target trial emulation in France. The Lancet Diabetes & Endocrinology, Volume 12, Issue 10, 716 - 724.
315. Lindahl JP, Reinholt FP, Eide IA, Hartmann A, Midtvedt K, Holdaas H, Dorg LT, Reine TM, Kolset SO, Horneland R, ![]() O, Brabrand K, Jenssen T. In patients with type 1 diabetes simultaneous pancreas and kidney transplantation preserves long-term kidney graft ultrastructure and function better than transplantation of kidney alone. Diabetologia. 2014 Nov; 57(11): 2357 - 65. doi: 10.1007/s00125-014-3353-2.
O, Brabrand K, Jenssen T. In patients with type 1 diabetes simultaneous pancreas and kidney transplantation preserves long-term kidney graft ultrastructure and function better than transplantation of kidney alone. Diabetologia. 2014 Nov; 57(11): 2357 - 65. doi: 10.1007/s00125-014-3353-2.
316. Lehmann R, et al. Glycemic Control in Simultaneous Islet-Kidney Versus Pancreas-Kidney Transplantation in Type 1 Diabetes: A Prospective 13-Year Follow-up. Diabetes care. 2015; 38: 752 - 759. doi: 10.2337/dc14-1686
317. Kempf MC, et al. Logistics and transplant coordination activity in the GRAGIL Swiss-French multicenter network of islet transplantation. Transplantation. 2005; 79: 1200 - 5. doi: 10.1097/01.tp.0000161224.67535.41
318. Hillberg AL, et al. Improving alginate-poly-L-ornithine-alginate capsule biocompatibility through genipin crosslinking. J Biomed Mater Res B Appl Biomater. 2013; 101: 258 - 68. doi: 10.1002/jbm.b.32835.
319. Hering B, et al. Phase 3 Trial of Transplantation of Human Islets in Type 1 Diabetes Mellitus Complicated by Severe Hypoglycemia. Diabetes Care. 2016 doi: 10.2337/dc15-1988. in Press. The results of this single arm Phase 3 Trial will be instrumental in obtaining licensure for a human islet product from the FDA which is required to fund future clinical allogeneic islet transplant procedures.
320. Bartlett ST, et al. Report from IPITA-TTS Opinion Leaders Meeting on the Future of beta-Cell Replacement. Transplantation. 2016; 100 (Suppl 2): S1 - S44. doi: 10.1097/TP.0000000000001055.
321. O'Connell PJ, et al. Multicenter Australian trial of islet transplantation: improving accessibility and outcomes. American journal of transplantation: official journal of the American Society of Transplantation and the American Society of Transplant Surgeons. 2013; 13: 1850 - 1858. doi: 10.1111/ajt.12250.
322. https://cr.minzdrav.gov.ru/preview-cr/469_3 Хроническая болезнь почек, взрослые
323. Altemose KE, Nailescu C. Management of pediatric obesity as a pathway towards kidney transplantation. Front Pediatr. 2024 Feb 15; 12: 1367520. doi: 10.3389/fped.2024.1367520.
324. Mahalati K, Belitsky P, Sketris I, West K, Panek R. Neoral monitoring by simplified sparse sampling area under the concentration-time curve: its relationship to acute rejection and cyclosporine nephrotoxicity early after kidney transplantation. Transplantation. 1999; 68(1): 55 - 62. doi: 10.1097/00007890-199907150-00011
325. Gaynor JJ, Ciancio G, Guerra G, Sageshima J, Roth D, Goldstein MJ, Chen L, Kupin W, Mattiazzi A, Tueros L, Flores S, Hanson L, Ruiz P, Vianna R, Burke GW 3rd. Lower tacrolimus trough levels are associated with subsequently higher acute rejection risk during the first 12 months after kidney transplantation. Transpl Int. 2016 Feb; 29(2): 216 - 26. doi: 10.1111/tri.12699. Epub 2015 Nov 3. PMID: 26442829.
326. Wallemacq P, Goffinet JS, O'Morchoe S et al. Multi-site analytical evaluation of the Abbott ARCHITECT tacrolimus assay. Ther Drug Monit 2009; 31: 198-204.
327. Jorgensen K, Povlsen J, Madsen S et al. C2 (2-h) levels are not superior to trough levels as estimates of the area under the curve in tacrolimus-treated renal-transplant patients. Nephrol Dial Transplant 2002; 17: 1487 - 1490.
328. Kasiske BL, Andany MA, Danielson B. A thirty percent chronic decline in inverse serum creatinine is an excellent predictor of late renal allograft failure. Am J Kidney Dis 2002; 39: 762 - 768
329. Kasiske BL, Andany MA, Hernandez D et al. Comparing methods for monitoring serum creatinine to predict late renal allograft failure. Am J Kidney Dis 2001; 38: 1065 - 1073.
330. Loupy A, Bouquegneau A, Stegall MD, Montgomery RA. Clinical outcomes after ABO-incompatible renal transplantation. Lancet (2019) 394(10213): 1988 - 9. doi: 10.1016/S0140-6736(19)32490-0
331. Kanter Berga J, Sancho Calabuig A, Gavela Martinez E, Puig Alcaraz N, Avila Bernabeu A, Crespo Albiach J, Molina Vila P,  Catalan S,
Catalan S,  Mateu L. Desensitization Protocol in Recipients of Deceased Kidney Donor With Donor-Specific Antibody-Low Titers. Transplant Proc. 2016 Nov; 48(9): 2880 - 2883. doi: 10.1016/j.transproceed.2016.07.050.
Mateu L. Desensitization Protocol in Recipients of Deceased Kidney Donor With Donor-Specific Antibody-Low Titers. Transplant Proc. 2016 Nov; 48(9): 2880 - 2883. doi: 10.1016/j.transproceed.2016.07.050.
332. Green H, Nesher E, Aizner S, Israeli M, Klein T, Zakai H, Rahamimov R, Rozen-Zvi B, Mor E. Long-term results of desensitization protocol with and without rituximab in sensitized kidney transplant recipients. Clin Transplant. 2019 Jun; 33(6): e13562. doi: 10.1111/ctr.13562.
333. Mutze, S., ![]() , I.,
, I.,  , B. et al. Colour-coded duplex sonography in the diagnostic assessment of vascular complications after kidney transplantation in children. Pediatric Radiology 27, 898 - 902 (1997). https://doi.org/10.1007/s00247005026
, B. et al. Colour-coded duplex sonography in the diagnostic assessment of vascular complications after kidney transplantation in children. Pediatric Radiology 27, 898 - 902 (1997). https://doi.org/10.1007/s00247005026
334. Nixon JN, Biyyam DR, Stanescu L, Phillips GS, Finn LS, Parisi MT. Imaging of pediatric renal transplants and their complications: a pictorial review. Radiographics. 2013 Sep - Oct; 33(5): 1227 - 51. doi: 10.1148/rg.335125150.
335. Castagnetti M, Angelini L, Ghirardo G, Zucchetta P, Gamba P, Zanon G, Murer L, Rigamonti W. Ureteral complications after renal transplant in children: timing of presentation, and their open and endoscopic management. Pediatr Transplant. 2014 Mar; 18(2): 150 - 4. doi: 10.1111/petr.12207
336. Balani SS, Jensen CJ, Kouri AM, Kizilbash SJ. Induction and maintenance immunosuppression in pediatric kidney transplantation - Advances and controversies. Pediatr Transplant. 2021 Nov; 25(7): e14077. doi: 10.1111/petr.14077. ]
337. Prytula A, van Gelder T. Clinical aspects of tacrolimus use in paediatric renal transplant recipients. Pediatric nephrology (Berlin, Germany). 2019; 34: 31 - 43.
338. Weber LT, Shipkova M, Lamersdorf T, et al. Pharmacokinetics of mycophenolic acid (MPA) and determinants of MPA free fraction in pediatric and adult renal transplant recipients. German Study Group on Mycophenolate Mofetil Therapy in Pediatric Renal Transplant Recipients. J Am Soc Nephrol 1998; 9: 1511
339. Ettenger, Robert 1, 3; Sarwal, Minnie M.2. Mycophenolate Mofetil in Pediatric Renal Transplantation. Transplantation 80(2S): p S201 - S210, October 15, 2005. DOI: 10.1097/01.tp.0000186957.32801.c0
340. Gonwa T, Mendez R, Yang HC, Weinstein S, Jensik S, Steinberg S; Prograf Study Group. Randomized trial of tacrolimus in combination with sirolimus or mycophenolate mofetil in kidney transplantation: results at 6 months. Transplantation. 2003 Apr 27; 75(8): 1213 - 20. doi: 10.1097/01.TP.0000062837.99400.60.
341. Campbell SB, Walker R, Tai SS, Jiang Q, Russ GR. Randomized controlled trial of sirolimus for renal transplant recipients at high risk for nonmelanoma skin cancer. Am J Transplant. 2012 May; 12(5): 1146 - 56. doi: 10.1111/j.1600-6143.2012.04004.x.
342. Nashan B, Curtis J, Ponticelli C, Mourad G, Jaffe J, Haas T; 156 Study Group. Everolimus and reduced-exposure cyclosporine in de novo renal-transplant recipients: a three-year phase II, randomized, multicenter, open-label study. Transplantation. 2004 Nov 15; 78(9): 1332 - 40. doi: 10.1097/01.tp.0000140486.97461.49
343. Pascual J. Concentration-controlled everolimus (Certican): combination with reduced dose calcineurin inhibitors. Transplantation. 2005 May 15; 79(9 Suppl): S76 - 9. doi: 10.1097/01.tp.0000162434.62591.f3. PMID: 15880020.
344. Hoyer PF, Ettenger R, Kovarik JM, et al. Everolimus** in pediatric de nova renal transplant patients. Transplantation. 2003; 75: 2082 - 2085.
345. Lablanche S, Vantyghem MC, Kessler L, Wojtusciszyn A, Borot S, Thivolet C, Girerd S, Bosco D, Bosson JL, Colin C, Tetaz R, Logerot S, Kerr-Conte J, Renard E, Penfornis A, Morelon E, Buron F, Skaare K, Grguric G, Camillo-Brault C, Egelhofer H, Benomar K, Badet L, Berney T, Pattou F, Benhamou PY; TRIMECO trial investigators. Islet transplantation versus insulin therapy in patients with type 1 diabetes with severe hypoglycaemia or poorly controlled glycaemia after kidney transplantation (TRIMECO): a multicentre, randomised controlled trial. Lancet Diabetes Endocrinol. 2018 Jul; 6(7): 527 - 537. doi: 10.1016/S2213-8587(18)30078-0.
346. Vantyghem MC, Chetboun M, Gmyr V, Jannin A, Espiard S, Le Mapihan K, Raverdy V, Delalleau N, Machuron F, Hubert T, Frimat M, Van Belle E, Hazzan M, Pigny P, Noel C, Caiazzo R, Kerr-Conte J, Pattou F; Members of the Spanish Back Pain Research Network Task Force for the Improvement of Inter-Disciplinary Management of Spinal Metastasis. Ten-Year Outcome of Islet Alone or Islet After Kidney Transplantation in Type 1 Diabetes: A Prospective Parallel-Arm Cohort Study. Diabetes Care. 2019 Nov; 42(11): 2042 - 2049. doi: 10.2337/dc19-0401. Erratum in: Diabetes Care. 2020 May; 43(5): 1164. doi: 10.2337/dc20-er05.
347. Lefaucheur C, Nochy D, Andrade J, et al. Comparison of combination plasmapheresis/IVIG/anti-CD20 versus high-dose IVIG in the treatment of antibody-mediated rejection. Am J Transplant 200991099-1107.
Приложение А1
СОСТАВ
РАБОЧЕЙ ГРУППЫ ПО РАЗРАБОТКЕ И ПЕРЕСМОТРУ
КЛИНИЧЕСКИХ РЕКОМЕНДАЦИЙ
Ватазин Андрей Владимирович
заведующий кафедрой трансплантологии, нефрологии и искусственных органов ФУВ ГБУЗ МО МОНИКИ им. М.Ф. Владимирского (Московская область), д.м.н., профессор
Гаджиева Патимат Магомедовна
врач-педиатр педиатрического отделения ФГБУ "Национальный медицинский исследовательский центр трансплантологии и искусственных органов им. ак. В.И. Шумакова" Минздрава России (г. Москва), к.м.н.
Галеев Шамиль Ринатович
заместитель директора - руководитель филиала ФГБУ "Национальный медицинский исследовательский центр трансплантологии и искусственных органов им. ак. В.И. Шумакова" Минздрава России в г. Волжский (г. Волжский), главный внештатный специалист трансплантолог Минздрава России Южного и Северо-Кавказского федеральных округов, д.м.н.
Гичкун Ольга Евгеньевна
ведущий научный сотрудник отдела регуляторных механизмов в трансплантологии ФГБУ "Национальный медицинский исследовательский центр трансплантологии и искусственных органов им. ак. В.И. Шумакова" Минздрава России (г. Москва), к.м.н., доцент
Готье Сергей Владимирович
директор ФГБУ "Национальный медицинский исследовательский центр трансплантологии и искусственных органов им. ак. В.И. Шумакова" Минздрава России (г. Москва), академик РАН, главный специалист трансплантолог Минздрава России, председатель ОООТ "Российское трансплантологическое общество", д.м.н., профессор, академик РАН
Зеленин Константин Николаевич
заведующий нефрологическим центром, заведующим отделением диализа ГБУЗ "Первая городская КБСМП им. Е.Е. Волосевич", главный внештатный специалист нефролог и трансплантолог Минздрава Архангельской области, к.м.н. (г. Архангельск)
Климушева Наталья Федоровна
заместитель главного врача по медицинской части ГАУЗ Свердловской области "Свердловская областная клиническая больница N 1", главный внештатный специалист трансплантолог Минздрава России Уральского федерального округа (г. Екатеринбург), д.м.н.
Коробка Вячеслав Леонидович
главный врач ГБУ РО "Ростовская областная клиническая больница (г. Ростов-на-Дону), главный внештатный специалист трансплантолог Минздрава Ростовской области, д.м.н.
Круглов Дмитрий Николаевич
врач-хирург хирургического отделения N 1 (Трансплантация почки, поджелудочной железы) ФГБУ "Национальный медицинский исследовательский центр трансплантологии и искусственных органов им. ак. В.И. Шумакова" Минздрава России (г. Москва)
Курбангулов Ильдар Раисович
врач-хирург хирургического отделения N 1 (Трансплантация почки, поджелудочной железы) ФГБУ "Национальный медицинский исследовательский центр трансплантологии и искусственных органов им. ак. В.И. Шумакова" Минздрава России (г. Москва), к.м.н.
Малахов Алексей Геннадьевич
врач-хирург хирургического отделения N 1 (Трансплантация почки, поджелудочной железы) ФГБУ "Национальный медицинский исследовательский центр трансплантологии и искусственных органов им. ак. В.И. Шумакова" Минздрава России (г. Москва)
Минина Марина Геннадьевна
заместитель главного врача, руководитель Московским координационным центром органного донорства, ГБУЗ ММНКЦ им. С.П. Боткина ДЗМ, д.м.н., профессор РАН
Можейко Наталья Павловна
заведующая патологоанатомическим отделением ФГБУ "Национальный медицинский исследовательский центр трансплантологии и искусственных органов им. ак. В.И. Шумакова" Минздрава России (г. Москва), д.м.н.
Николаев Герман Викторович
руководитель НИЛ торакальной хирургии ФГБУ "НМИЦ им. В. А. Алмазова" Минздрава России, врач-торакальный хирург высшей категории, главный внештатный специалист-трансплантолог Комитета по здравоохранению Санкт-Петербурга, отличник здравоохранения (г. Санкт-Петербург), к.м.н.
Петрова Наталья Юрьевна
заведующая нефрологическим центром ГУЗ "Областная клиническая больница", главный внештатный специалист нефролог Минздрава России по Приволжскому федеральному округу (г. Саратов), к.м.н.
Пиминова Татьяна Анатольевна
заведующая хирургическим отделением N 3, врач-хирург ГАУЗ "Кузбасская областная клиническая больница имени С.В. Беляева", главный внештатный специалист трансплантолог Минздрава России в Сибирском федеральном округе, Минздрава Кемеровской области - Кузбасса (г. Кемерово), к.м.н.
Платонов Вадим Сергеевич
заведующий урологическим отделением по пересадке почки БУЗ ВО "Воронежская областная клиническая больница N 1", главный внештатный специалист трансплантолог (г. Воронеж), к.м.н.
Сайдулаев Джабраил Азизович
заведующий хирургическим отделением N 1 (Трансплантация почки, поджелудочной железы), врач-хирург ФГБУ "Национальный медицинский исследовательский центр трансплантологии и искусственных органов им. ак. В.И. Шумакова" Минздрава России (г. Москва), к.м.н.
Сапожников Аркадий Давидович
заместитель руководителя филиала по организации медицинской помощи, врач-уролог ФГБУ "Национальный медицинский исследовательский центр трансплантологии и искусственных органов им. ак. В.И. Шумакова" Минздрава России в г. Волжский (г. Волжский), к.м.н.
Столяревич Екатерина Сергеевна
старший научный сотрудник Центра лечения критической сердечной недостаточности ФГБУ "Национальный медицинский исследовательский центр трансплантологии и искусственных органов им. ак. В.И. Шумакова" Минздрава России, профессор кафедры нефрологии ФГБОУ ВО МГМСУ имени А.И. Евдокимова (г. Москва), д.м.н.
Строков Александр Григорьевич
заведующий отделением гемодиализа ФГБУ "Национальный медицинский исследовательский центр трансплантологии и искусственных органов им. ак. В.И. Шумакова" Минздрава России (г. Москва), д.м.н.
Хомяков Сергей Михайлович
заместитель директора - руководитель центра организационно-методического руководства учреждениями, осуществляющими деятельность, связанную с трансплантацией органов и (или) тканей человека, ФГБУ "Национальный медицинский исследовательский центр трансплантологии и искусственных органов им. ак. В.И. Шумакова" Минздрава России (г. Москва), к.м.н.
Чеботарева Наталья Викторовна
Заведующая центром совершенствования оказания медицинской помощи по профилю "нефрология", заведующая отделением нефрологии ФГБУ "Национальный медицинский исследовательский центр трансплантологии и искусственных органов им. ак. В.И. Шумакова" Минздрава России (г. Москва), профессор, д.м.н.
Конфликт интересов.
Рабочая группа заявляет об отсутствии конфликта интересов.
Приложение А2
МЕТОДОЛОГИЯ РАЗРАБОТКИ КЛИНИЧЕСКИХ РЕКОМЕНДАЦИЙ
Федеральный закон от 21.11.2011 N 323-ФЗ (ред. от 29.05.2019) "Об основах охраны здоровья граждан в Российской Федерации". Статья 47. Донорство органов и тканей человека и их трансплантация (пересадка).
Целевая аудитория данных клинических рекомендаций:
1. врачи-хирурги;
2. врачи-анестезиологи-реаниматологи;
3. врачи общей практики (семейные врачи);
4. врачи-нефрологи;
5. врачи-урологи;
6. врачи-терапевты;
7. врачи-патологоанатомы.
Таблица 1. Шкала оценки уровней достоверности доказательств (УДД) для методов диагностики (диагностических вмешательств)
УДД
Расшифровка
1
Систематические обзоры исследований с контролем референсным методом или систематический обзор рандомизированных клинических исследований с применением мета-анализа
2
Отдельные исследования с контролем референсным методом или отдельные рандомизированные клинические исследования и систематические обзоры исследований любого дизайна, за исключением рандомизированных клинических исследований, с применением мета-анализа
3
Исследования без последовательного контроля референсным методом или исследования с референсным методом, не являющимся независимым от исследуемого метода или нерандомизированные сравнительные исследования, в том числе когортные исследования
4
Несравнительные исследования, описание клинического случая
5
Имеется лишь обоснование механизма действия или мнение экспертов
Таблица 2. Шкала оценки уровней достоверности доказательств (УДД) для методов профилактики, лечения, медицинской реабилитации, в том числе основанных на использовании природных лечебных факторов (профилактических, лечебных, реабилитационных вмешательств)
УДД
Расшифровка
1
Систематический обзор РКИ с применением мета-анализа
2
Отдельные РКИ и систематические обзоры исследований любого дизайна, за исключением РКИ, с применением мета-анализа
3
Нерандомизированные сравнительные исследования, в т.ч. когортные исследования
4
Несравнительные исследования, описание клинического случая или серии случаев, исследования "случай-контроль"
5
Имеется лишь обоснование механизма действия вмешательства (доклинические исследования) или мнение экспертов
Таблица 3. Шкала оценки уровней убедительности рекомендаций (УУР) для методов профилактики, диагностики, лечения, медицинской реабилитации, в том числе основанных на использовании природных лечебных факторов (профилактических, диагностических, лечебных, реабилитационных вмешательств)
УУР
Расшифровка
A
Сильная рекомендация (все рассматриваемые критерии эффективности (исходы) являются важными, все исследования имеют высокое или удовлетворительное методологическое качество, их выводы по интересующим исходам являются согласованными)
B
Условная рекомендация (не все рассматриваемые критерии эффективности (исходы) являются важными, не все исследования имеют высокое или удовлетворительное методологическое качество и/или их выводы по интересующим исходам не являются согласованными)
C
Слабая рекомендация (отсутствие доказательств надлежащего качества (все рассматриваемые критерии эффективности (исходы) являются неважными, все исследования имеют низкое методологическое качество и их выводы по интересующим исходам не являются согласованными)
Порядок обновления клинических рекомендаций.
Механизм обновления клинических рекомендаций предусматривает их систематическую актуализацию - не реже чем один раз в три года, а также при появлении новых данных с позиции доказательной медицины по вопросам диагностики, лечения, профилактики и реабилитации конкретных заболеваний, наличии обоснованных дополнений/замечаний к ранее утвержденным клиническим рекомендациям, но не чаще 1 раза в 6 месяцев.
Приложение А3
СПРАВОЧНЫЕ МАТЕРИАЛЫ,
ВКЛЮЧАЯ СООТВЕТСТВИЕ ПОКАЗАНИЙ К ПРИМЕНЕНИЮ
И ПРОТИВОПОКАЗАНИЙ, СПОСОБОВ ПРИМЕНЕНИЯ И ДОЗ ЛЕКАРСТВЕННЫХ
ПРЕПАРАТОВ, ИНСТРУКЦИИ ПО ПРИМЕНЕНИЮ
ЛЕКАРСТВЕННОГО ПРЕПАРАТА
Таблица 1. Дозировка иммунодепрессантов в детском возрасте [336]
Препараты
Лекарственная форма
Дозирование
Такролимус**
Капсулы
0,3 мг/кг в сутки, доза разделена на два приема с интервалом 12 часов
0,075 - 0,1 мг/кг/сут в виде продленной инфузии
Раствор для внутривенного и внутримышечного введения
Такролимус пролонгированного действия**
Капсулы
0,2 - 0,3 мг 1 раз в сутки
#Микофенолата мофетил**
Таблетки, капсулы
С циклоспорином 900 мг/м2 два раза в сутки первые 2 - 4 недели, затем 600 мг/м2 два раза в сутки
С такролимусом или без ингибиторов кальциневрина 600 мг/м2 два раза в сутки первые 2 - 4 недели, затем 450 мг/м2 два раза в сутки
#Микофеноловая кислота**
Таблетки кишечнорастворимые
400 мг/м2 2 раза в день (максимальная доза 1440 мг)
Площадь поверхности тела 1,19 - 1,58 м2: 540 мг 2 раза в сутки > 1,58 м2: 720 мг 2 раза в сутки
#Сиролимус**
Таблетки, раствор для приема внутрь
Доза 3 мг/м2, разделенная на 2 раза в сутки с интервалом каждые 12 часов
#Эверолимус**
Таблетки
Доза 1.6 мг/м2, разделенная на 2 раза в сутки с интервалом каждые 12 часов
Таблица 2. Протокол начальной иммуносупрессивной терапии с такролимусом** и индукцией базиликсимабом** [311].
Препарат
Срок введения
Дозы и режимы введения
Базиликсимаб**
С кожным разрезом, затем на 4-е сутки
Внутривенно в течение 30 мин, при массе тела (у детей и подростков) менее 35 кг - 20 мг, разделенная на 2 введения по 10 мг, при массе тела более 35 кг - 40 мг, разделенная на 2 введения по 20 мг
Метилпреднизолон**
Интраоперационно, непосредственно перед реперфузией
Внутривенно, 10 мг/кг
0-й день после операции
Внутривенно, 125 - 250 мг
Метилпреднизолон** (преднизолон**)
1 - 14-й день
Внутрь, 16 (20) мг
1 - 14-й день
Внутрь 12 (15) мг
1 - 14-й день
Внутрь 8 (10) мг
Поддерживающая суточная доза
Внутрь 4 (5) мг, возможна отмена
Такролимус**
1-й день
Внутрь, 0,1 - 0,2 мг/кг в 2 приема (в зависимости от начальной функции)
Поддерживающая доза (начиная со 2-го дня)
Коррекция дозы по целевой концентрации в зависимости от срока после трансплантации (см. таблицу 3)
Микофенолата мофетил** (микофеноловая кислота**)
1 - 14-й день
Внутрь, 1000 (720) мг 2 раза в сутки
С 15-го дня
Внутрь, 500 (360) мг 2 раза в сутки
Дозы такролимуса** и такролимуса пролонгированного действия**, #микофенолата мофетила** (#микофеноловой кислоты**) у детей представлены в таблице 1 (Приложение А3) [336].
Таблица 3. Целевые концентрации иммунодепрессантов в зависимости от схемы иммуносупрессивной терапиии срока после трансплантации почки [311].
Схема терапии
Препарат
C
Концентрация препарата, нг/мл
1 мес
2 - 3 мес
3 - 6 мес
6 - 12 мес
> 12 мес
Циклоспорин** + Микофенолата мофетил** (микофеноловая кислота**) + глюкокортикоиды
Циклоспорин**
C0
200 - 300
180 - 200
170 - 180
150 - 170
120 - 150
C2
1000 - 1400
800 - 1000
800 - 1000
600 - 800
600 - 800
Такролимус** + Микофенолата мофетил** (микофеноловая кислота**) + глюкокортикоиды
Такролимус**
C0
8 - 15
8 - 12
8 - 10
7 - 8
5 - 8
Такролимус** + Микофенолата мофетил** (микофеноловая кислота**)
Такролимус**
C0
10 - 15
10 - 12
9 - 10
8 - 9
7 - 8
Циклоспорин** + эверолимус** + метилпреднизолон**
Циклоспорин**
C0
150 - 200
100 - 150
80 - 100
50 - 70
25 - 50
C2
800 - 1000
600 - 800
450 - 650
350 - 450
300 - 400
Эверолимус**
C0
3 - 8
3 - 8
3 - 8
3 - 8
3 - 8
Такролимус** + эверолимус** + метилпреднизолон**
Такролимус**
C0
8 - 10
6 - 8
4 - 6
4 - 6
3 - 5
Эверолимус**
C0
3 - 8
3 - 8
3 - 8
3 - 8
3 - 8
Краткое изложение пороговых значений для всех шкал повреждения по шкале BANFF
Шкала повреждения Banff
Аббревиатура
0
1
2
3
Интерстициальное воспаление (степень воспаления в нефиброзированных участках коры)
i
Воспаление менее 10% нефиброзированных участков коры
Воспаление от 10 до 25% нефиброзированных участков коры
Воспаление от 26 до 50% нефиброзированных участков коры
Воспаление более 50% нефиброзированных участков коры
Тубулит
(присутствие мононуклеарных клеток в базолатеральной части эпителия почечных канальцев)
t
Отсутствие мононуклеарных клеток в базолатеральной части эпителия почечных канальцев
Два и более очага с 1 - 4 мононуклеарными клетками на поперечный срез канальца (или на 10 эпителиоцитов канальцев)
Два и более очага, по крайней мере один из очагов с 5 - 10 мононуклеарными клетками на поперечный срез канальца (или на 10 эпителиоцитов канальцев)
Два и более очага, по крайней мере один из очагов с более 10 мононуклеарных клеток на поперечный срез канальца или наличие 2 и более областей разрушения тубулярной базальной мембраны, сопровождающиеся воспалением i2/i3 и t2 в других участках
Интимальный артериит
(наличие и степень воспаления в артериальной интиме)
v
Отсутствует
Сужение менее 25% площади просвета артерии
Сужение 25% и более площади просвета артерии
Трансмуральный артериит и/или артериальные фибриноидные изменения и медиальный некроз гладких мышц с лимфоцитарным инфильтратом в сосуде
Гломерулит
(доля клубочков с полной или частичной окклюзией одного или более капилляров за счет лейкоцитарной инфильтрации (полиморфноядерные клетки и мононуклеарные клетки) или увеличения эндотелиальных клеток)
g
Отсутствует
Сегментарный или глобальный гломерулит менее чем в 25% клубочков
Сегментарный или глобальный гломерулит в 25 - 75% клубочков
Сегментарный или глобальный гломерулит более чем в 75% клубочков
Перитубулярный капиллярит
(степень воспаления в перитубулярных капиллярах (ПТК))
ptc
Меньше 3-х лейкоцитов в ПТК
1 или более лейкоцитов в 10% и более кортикальных ПТК с 3 - 4 лейкоцитами в наиболее пораженном ПТК
1 или более лейкоцитов в более 10% кортикальных ПТК с 5 - 10 лейкоцитами в наиболее пораженном ПТК
1 или более лейкоцитов в 10% и более кортикальных ПТК с более 10 лейкоцитов в наиболее пораженном ПТК
C4d
(степень окрашивания C4d на эндотелиальных клетках ПТК и прямых сосудах мозгового вещества)
C4d
Отсутствует
Минимальное (окрашивание менее 10%) на эндотелиальных клетках ПТК и прямых сосудах мозгового вещества
Фокальное (окрашивание от 10 до 50%) на эндотелиальных клетках ПТК и прямых сосудах мозгового вещества
Диффузное (окрашивание более 50%) на эндотелиальных клетках ПТК и прямых сосудах мозгового вещества
Интерстициальный фиброз
(степень кортикального фиброза)
ci
Интерстициальный фиброз до 5% корковой области
Интерстициальный фиброз от 6 до 25% корковой области (легкий)
Интерстициальный фиброз от 26 до 50% корковой области (умеренный)
Интерстициальный фиброз более 50% корковой области (тяжелый)
Тубулярная атрофия
(степень атрофии кортикальных канальцев)
ct
Отсутствует
Тубулярная атрофия, затрагивающая до 25% площади корковых канальцев
Тубулярная атрофия, затрагивающая от 26 до 50% площади корковых канальцев
Тубулярная атрофия, затрагивающая > 50% площади корковых канальцев
Фиброзное утолщение интимы сосудов
(степень утолщения интимы в наиболее пораженной артерии)
cv
Отсутствует
С сужением просвета <= 25%
С сужением просвета от 26 до 50%
С сужением просвета более 50%
Удвоение контуров базальных мембран капиллярных петель клубочков
(наличие и степень выраженности удвоения контуров базальных мембран капилляров клубочков (БМКК) или их расщепления в наиболее пораженном несклерозированном клубочке)
cg
Отсутствует
1a - удвоение контуров БМКК (неполные или циркулярные) по крайней мере в 3 капиллярах клубочков при электронной микроскопии, 1b - двойные контуры БМКК в 1 - 25% капиллярных петель клубочков при световой микроскопии
Удвоение контуров БМКК от 26 до 50% периферических капиллярных петель при световой микроскопии
Удвоение контуров БМКК более 50% периферических капиллярных петель в не ишемизированном и не склерозированном клубочке при световой микроскопии
Расширение мезангиального матрикса
(процент клубочков с расширением мезангиального матрикса в мезангиальном пространстве, превышающим ширину 2 мезангиальных клеток, по крайней мере, в 2 дольках клубочка, по отношению ко всем несклерозированным клубочкам)
mm
Отсутствует
Не более 25% несклерозированных клубочков
От 26 до 50% несклерозированных клубочков
Более 50% несклерозированных клубочков
Гиалиноз артериол
(PAS-положительное артериальное утолщение гиалина)
ah
Отсутствует
От легкого до умеренного утолщения по крайней мере в одной артериоле
От умеренного до выраженного утолщения более чем в одной артериоле
Тяжелый артериальный гиалиноз во многих артериолах
Гиалиновое артериолярное утолщение
(Учитывает циркулярный характер гиалиноза и количество пораженных артериол)
aah
Отсутствует
Нециркулярное замещение дегенерированных гладкомышечных клеток гиалиновыми отложениями только в 1 артериоле
Нециркулярное замещение дегенерированных гладкомышечных клеток гиалиновыми отложениями более, чем в 1 артериоле
Циркулярное замещение дегенерированных гладкомышечных клеток гиалиновыми отложениями, независимо от количества вовлеченных артериол
Общее воспаление
(воспаление в корковом веществе, учитывая все зоны кортикальной паренхимы, в том числе участки интерстициального фиброза и тубулярной атрофии (IFTA <*>), субкапсулярную и периваскулярные зоны, включая очаговые инфильтраты)
ti
Отсутствие или незначительное интерстициальное воспаление (менее 10% от общей кортикальной паренхимы)
Воспаление от 10 до 25% от общей кортикальной паренхимы
Воспаление от 26 до 50% от общей кортикальной паренхимы
Воспаление более 50% от общей кортикальной паренхимы
Воспаление в области IFTA <*>
(описывает степень воспаления в участках фиброзного изменения коркового вещества, соответствующих критериям (ci) и (ct), не учитывая тубулит в сильно атрофированных канальцах, поскольку в таких канальцах тубулит наблюдается даже при минимальном интерстициальном воспалении, а также в биопсиях нативных почек)
i-IFTA
Воспаление в менее 10% площади кортикальной паренхимы с интерстициальным фиброзом и тубулярной атрофией
Воспаление от 10 до 25% площади кортикальной паренхимы с интерстициальным фиброзом и тубулярной атрофией
Воспаление от 26 до 50% площади кортикальной паренхимы с интерстициальным фиброзом и тубулярной атрофией
Воспаление более 50% площади кортикальной паренхимы с интерстициальным фиброзом и тубулярной атрофией
Тубулит в областях интерстициального фиброза
(наличие инфильтратов мононуклеарных клеток в неатрофических, слабо и умеренно атрофических канальцах в зонах интерстициального фиброза)
t-IFTA
Отсутствие мононуклеарных клеток в канальцах в зонах интерстициального фиброза, или только одиночный очаг тубулита
2 и более очагов с 1 - 4 мононуклеарными клетками на поперечный срез канальца (или на 10 эпителиоцитов канальцев) в наиболее пораженном канальце очага, в зонах интерстициального фиброза
2 и более очагов с 5 - 10 мононуклеарными клетками на поперечный срез канальца (или на 10 эпителиоцитов канальцев) в наиболее пораженном канальце очага, в зонах интерстициального фиброза
2 и более очагов с более 10 мононуклеарных клеток на поперечный срез канальца (или на 10 эпителиоцитов канальцев) в наиболее пораженном канальце очага, в зонах интерстициального фиброза
Полиомавирусная нагрузка
(определяется по всему образцу биопсии (кора, мозговое вещество, независимо от фиброзных изменений), соотношением канальцев/протоков, имеющих хотя бы одно положительное ядро, ко всем канальцам/протокам. Ядра канальцевого эпителия считаются положительными при наличии типичных вирусных включений и/или положительным иммуногистохимическом результате
pvl
Нет положительных ядер в канальцах/протоках
Положительные ядра не более чем в 1% канальцев/протоков
Положительные ядра от 1 до 10% канальцев/протоков
Положительные ядра более 10% канальцев/протоков
--------------------------------
<*> IFTA - интерстициальный фиброз и тубулярная атрофия
Диагностические критерии Banff-классификации.
КАТЕГОРИЯ 1: Нормальная биопсия или неспецифические изменения.
Требуется исключение любого состояние из диагностических 2, 3, 4 и 6 категорий BANFF-классификации.
КАТЕГОРИЯ 2: Антитело-опосредованное отторжение и микрососудистое воспаление/повреждение (AMR/MVI)
Активное антитело-опосредованное отторжение (необходимо наличие трех критериев):
1. Констатировано острое повреждение <*>, имеется по крайней мере один из следующих признаков:
--------------------------------
<*> "Тебе пересадили почку..." Руководство для пациентов, ожидающих и перенесших пересадку почки. Под редакцией академика РАН В.И. Шумакова.
- Микрососудистое воспаление (g > 0 и/или ptc > 0), при отсутствии рецидивирующего или de novo гломерулонефрита (при наличии острого клеточно-опосредованного отторжения, пограничных изменений или инфекции, ptc >= 1 недостаточно, требуется g >= 1)
- Интимальный или трансмуральный артериит (v > 0)
- Острая тромботическая микроангиопатия, при отсутствии другой видимой причины
2. Доказано текущее либо недавнее взаимодействие антител с эндотелием сосудов, имеется по крайней мере один из следующих признаков:
- Линейное окрашивание C4d в перитубулярных капиллярах или прямых сосудах мозгового слоя (C4d2 или C4d3 по данным иммунофлюоресценции на замороженных срезах, или C4d > 0 по данным иммуногистохимии на парафиновых срезах)
- Умеренное микрососудистое воспаление ([g + ptc] >= 2) при отсутствии рецидивирующего или de novo гломерулонефрита, при наличии острого клеточно-опосредованного отторжения, пограничных изменений или инфекции недостаточно только ptc >= 2, требуется g >= 1
- Повышенная экспрессия генов, связанных с антитело-опосредованным отторжением, в ткани биоптата.
3. Серологически выявлены донор-специфические антитела (ДСА к HLA или другим антигенам). Окрашивание C4d или экспрессия генов может заменить ДСА. Однако определение ДСА, рекомендуется при наличии критериев 1 и 2.
Хроническое активное антитело-опосредованное отторжение (необходимо наличие трех критериев):
1. Морфологические признаки хронического повреждения ткани, имеется по крайней мере один из следующих признаков:
- Трансплантационная гломерулопатия (cg > 0 и/или тяжелые перитубулярные капилляриты), при отсутствии признаков хронической ТМА, хронического рецидивирующего или de novo гломерулонефрит (изменения очевидны только по электронной микроскопии).
- Тяжелая степень расщепления базальных мембран перитубулярных капилляров (требуется электронная микроскопия).
- Артериальный интимальный фиброз de novo, исключающий другие причины. Наличие лейкоцитов в склерозированной интиме свидетельствует в пользу хронического антитело-опосредованного отторжения, если нет предшествующего анамнеза клеточно-опосредованного отторжения.
2. Идентичен критерию 2 для активного антитело-опосредованного отторжения, указанному выше.
3. Идентичен критерию 3 для активного антитело-опосредованного отторжения, указанному выше.
Хроническое антитело-опосредованное отторжение (необходимо наличие всех трех критериев):
1. cg > 0 и/или тяжелое ptcm (расщепление тубулярных базальных мембран перитубулярных капилляров) и/или артериальный интимальный фиброз de novo, исключающий другие причины. Наличие лейкоцитов в склерозированной интиме свидетельствует в пользу хронического антитело-опосредованного отторжения, если нет предшествующего анамнеза клеточно-опосредованного отторжения.
2. Отсутствие критерия 2, определенного выше, для активного и хронического активного антитело-опосредованного отторжения.
3. Предшествующий документированный диагноз активного или хронического активного антитело-опосредованного отторжения и/или документированные предыдущие (после трансплантации) и/или текущие доказательства ДСА (ДСА, как определено выше в критерии 3 для активного антитело-опосредованного отторжения).
Окрашивание C4d без признаков отторжения (необходимо соблюдение всех 4-х критериев):
1. Линейное окрашивание C4d в перитубулярных капиллярах (C4d2 или C4d3 по данным иммунофлюоресценции на замороженных срезах или C4d > 0 по данным иммуногистохимии на парафиновых срезах)
2. Критерий 1 для активного или хронического активного антитело-опосредованного отторжения не выполнен.
3. Отсутствие молекулярных доказательств антитело-опосредованного отторжения по критерию 2 для активного и хронического активного антитело-опосредованного отторжения.
4. Отсутствие острого или хронического активного клеточно-опосредованного отторжения или пограничные изменения.
Микрососудистое воспаление/повреждение, ДСА-отрицательный и C4d-отрицательный (необходимо соблюдение всех 3-х критериев):
1. По крайней мере умеренное микрососудистое воспаление (g + ptc >= 2), при отсутствии рецидивирующего или de novo гломерулонефрита (при наличии острого клеточно-опосредованного отторжения, пограничных изменений или инфекции, ptc >= 2 недостаточно, g должен быть >= 1)
2. Отсутствие линейного окрашивания C4d в перитубулярных капиллярах (C4d0 или C4d1 по данным иммунофлюоресценции на замороженных срезах или C4d = 0 по данным иммуногистохимии на парафиновых срезах)
3. Отсутствие серологических доказательств циркулирующих донор-специфических антител (ДСА к HLA или другим антигенам, как определено в критерии 3 выше для активного антитело-опосредованного отторжения.
Вероятное антитело-опосредованное отторжение (необходимо соблюдение всех 4-х критериев):
1. Идентично критерию 1 для активного антитело-опосредованного отторжения, указанному выше.
2. Критерий 1 для хронического активного и хронического антитело-опосредованного отторжения не выполнен.
3. Отсутствие критерия 2, определенного для активного и хронического активного антитело-опосредованного отторжения, указанного выше.
4. Идентично критерию 3 для активного антитело-опосредованного отторжения, указанному выше (но C4d должен быть отрицательным).
Окрашивание C4d при остром повреждении канальцев (ATI) (необходимо соблюдение всех 3-х критериев):
1. Присутствует острое повреждение канальцев (ATI)
2. Линейное окрашивание C4d в перитубулярных капиллярах (C4d2 или C4d3 по данным иммунофлюоресценции на замороженных срезах или C4d > 0 по данным иммуногистохимии на парафиновых срезах)
3. Критерий 1 для активного и хронического активного антитело-опосредованного отторжения не выполнен.
КАТЕГОРИЯ 3: Подозрительный (пограничный) для острого клеточно-опосредованного отторжения
Очаги поражения Banff с показателем t > 0 и показатель поражения Banff i = 1 ИЛИ Очаги поражения Banff с показателем t1 и показатель поражения Banff i >= 2.
КАТЕГОРИЯ 4: клеточно-опосредованное отторжение
Острое клеточно-опосредованное отторжение IA показатель поражения Banff i >= 2 и показатель поражения Banff t2
Острое клеточно-опосредованное отторжение IB показатель поражения Banff i >= 2 и показатель поражения Banff t3
Острое клеточно-опосредованное отторжение IIA показатель поражения Banff v1 независимо от показателя поражения Banff i или t
Острое клеточно-опосредованное отторжение IIB показатель поражения Banff v2 независимо от показателя поражения Banff i или t
Острое клеточно-опосредованное отторжение III показатель поражения Banff v3 независимо от показателя поражения Banff i или t
Хроническое активное клеточно-опосредованное отторжение Степень IA показатель поражения Banff ti >= 2 и показатель поражения Banff i-IFTA >= 2, другие известные причины i-IFTA (например, пиелонефрит, BK-вирусный нефрит и т.д.) исключены и показатель поражения Banff t2
Хроническое активное клеточно-опосредованное отторжение Степень IB Оценка поражения по шкале Banff ti >= 2 И оценка поражения по шкале Banff i-IFTA >= 2, другие известные причины i-IFTA исключены И оценка поражения по шкале Banff t3
Хроническое активное клеточно-опосредованное отторжение II степени Фиброз интимы артерий с воспалением мононуклеарных клеток при фиброзе и формирование неоинтимы
КАТЕГОРИЯ 5: IFTA
Степень I (легкая) Оценка поражения по шкале Banff ci1 ИЛИ Оценка поражения по шкале Banff ct1
Степень II (умеренная) Оценка поражения по шкале Banff ci2 ИЛИ Оценка поражения по шкале Banff ct2
Степень III (тяжелая) Оценка поражения по шкале Banff ci3 ИЛИ Оценка поражения по шкале Banff ct3
КАТЕГОРИЯ 6: Другие изменения, не считающиеся вызванными острым или хроническим отторжением
Полиомавирусная нефропатия, посттрансплантационное лимфопролиферативное заболевание, токсичность ингибиторов кальциневрина, острое повреждение канальцев, возврат заболевания в трансплантате, гломерулопатия De Novo (кроме трансплантационной гломерулопатии), пиелонефрит, лекарственно-индуцированный интерстициальный нефрит.
Приложение Б
АЛГОРИТМЫ ДЕЙСТВИЙ ВРАЧА
Б.1. План предварительного обследования потенциального реципиента почки
1. Основные моменты в медицинском и семейном анамнезе потенциального реципиента почки, необходимые для изучения:
- Наличие или отсутствие гематурии, протеинурии, инфекции мочевыводящих путей.
- Наличие периферических отеков.
- Наличие или отсутствие таких заболеваний, как подагра, нефролитиаз, гипертония, сахарный диабет (включая семейный анамнез), ишемическая болезнь сердца, заболевание периферических артерий, другой атеросклероз.
- Наличие или отсутствие факторов риска сердечно-сосудистых заболеваний.
- Наличие или отсутствие тромбоэмболия легочной артерии в анамнезе.
- Наличие или отсутствие серповидноклеточных и другие гемоглобинопатий.
- Наличие или отсутствие расстройств кишечника.
- Перенесенное или имеющееся злокачественное новообразование.
- Наличие или отсутствие системного заболевания, которое может поражать почки.
- Наличие или отсутствие хронической инфекции, например туберкулеза.
- Семейный анамнез почечного заболевания.
- Курение.
- Наличие или отсутствие алкогольной или наркотической зависимости.
- История психического здоровья.
- Акушерский анамнез.
- Периоды проживания за границей, если имеются.
- Наличие или отсутствие осложнений, связанных с предшествующими анестезиями.
- Анамнез травмы спины или шеи. Наличие или отсутствие болей в области спины или шеи.
2. Основные моменты анамнеза в отношении трансмиссивных инфекций:
Перенесенные болезни:
- Желтуха или гепатит.
- Малярия.
- Перенесенные переливание крови.
- Туберкулез/Семейный анамнез туберкулеза.
Повышенный риск заражения ВИЧ, гепатитом B и C:
- Гемофилия.
- Промискуитет.
- Инфекционный гепатит или сифилис в анамнезе.
- Анамнез внутривенного употребления наркотиков.
- Татуировка или пирсинг кожи в течение последних 6 месяцев.
- Половой партнер - с положительной серологией.
- Половой партнер - наркоман.
3. Необходимые консультации специалистов:
- Врача-хирурга (перенесенные операции, настоящая патология);
- Врача-стоматолога (санация полости рта);
- Врача-гинеколога (УЗИ органов малого таза) для женщин, женщинам старше 40 лет также необходима консультация врача-онколога (маммолога);
- Врача-уролога (УЗИ предстательной железы + ПСА крови для мужчин старше 45 лет);
- Врача-проктолога;
- Врача-терапевта (с изложением полного медицинского анамнеза, объективного статуса, принимаемых препаратов);
- Врача-эндокринолога с обследованием на гормоны щитовидной железы (исследование уровня тиреотропного гормона (ТТГ) в крови, исследование уровня общего трийодтиронина (Т3) в крови, исследование уровня свободного тироксина (СТ4) сыворотки крови), УЗИ щитовидной железы, исследование уровня гликированного гемоглобина в крови (при показаниях).
4. Стандартные лабораторные исследования потенциального донора:
- Группа крови, резус фактор;
- Гепатит B и C (HbsAg, HCV);
- ВИЧ (определение антител классов M, G (IgM, IgG) к вирусу иммунодефицита человека ВИЧ-1 (Human immunodeficiency virus HIV 1)/ВИЧ-2 (Human immunodeficiency virus HIV 2) в крови);
- Сифилис (RW, определение AT к бледной трепонеме (Treponema pallidum) в крови);
- Цитомегаловирус (определение ДНК ЦМВ методом ПЦР);
- Вирус Эпштейна-Барра (определение ДНК EBV методом ПЦР);
- Общий (клинический) анализ крови развернутый;
- Анализ крови биохимический общетерапевтический (креатинин, мочевина, щелочная фосфатаза, АЛТ, АСТ, холестерин общий, ГГТ, билирубин общий, общий белок, глюкоза, мочевая кислота, кальций, фосфор, магний, калий, натрий);
- Липидный профиль;
- Клубочковая фильтрация + суточная протеинурия;
- Коагулограмма;
- Общий (клинический) анализ мочи (при наличии диуреза);
- Анализ мочи по Нечипоренко (при наличии диуреза);
- Посев мочи (при наличии диуреза).
5. Заключения инструментальных методов исследования:
- ЭКГ;
- ЭхоКГ;
- Суточное мониторирование артериального давления (СМАД),
- Холтеровское мониторирование сердечного ритма;
- Тредмил-тест (по показаниям);
- Прицельная рентгенография органов грудной клетки;
- Эзофагогастродуоденоскопия;
- Ультразвуковое исследование почек и надпочечников, поджелудочной железы, печени, желчного пузыря и протоков;
- УЗДС сосудов почек, сосудов нижних конечностей, подвздошных артерий и вен, сосудов шеи.
Данные обследования должны быть изложены в виде эпикриза.
Таблица 1. Рекомендуемые временные интервалы безрецидивного течения злокачественных новообразований (ЗНО) у больных ХБП перед трансплантацией почки [311].
ЗНО, ассоциированные с ХБП
Почки (C64)
> 2 лет
Почечная лоханка (C65)
> 2 лет
Мочеточник (C66)
> 2 лет
Мочевой пузырь (C67)
> 2 лет
ЗНО, не ассоциированные с ХБП
Опухоли кожи (немеланомные)
Локальное лечение
Губы (C00)
Локальное лечение
Язык (C01 - 02)
> 2 лет
Ротовая полость (C03 - C06)
> 2 лет
Слюнные железы (C07 - C08)
> 2 лет
Пищевод (C15)
> 2 лет
Желудок (C16)
> 2 лет
Тонкая кишка (C17)
> 2 лет
Толстая кишка (C18)
> 2 лет
Прямая кишка (C19 - C20)
> 2 лет
Анус (C21)
> 2 лет
Печень (C22)
Противопоказано при отсутствии трансплантации печени
Желчный пузырь (C23 - C24)
> 2 лет
Поджелудочная железа (C25)
> 2 лет
Гортань (C32)
> 2 лет
Трахея, бронхи и легкие (C33 - C34)
> 2 лет
Меланома (C43)
> 5 лет - в соответствии с риском метастазирования
Мезотелиома (C43)
> 2 лет
Саркома Капоши (C46)
> 2 лет - для иммуносупрессии применяются ингибиторы mTOR
Образования соединительной ткани и мягких тканей (C47 - C49)
> 2 лет
Молочная железа (C50)
> 5 лет
Вульва (C51)
> 2 лет
Шейка матки (C53)
> 2 лет
Тело матки (C54)
> 2 лет
Яичники (C56)
> 2 лет
Половой член (C60)
> 2 лет
Предстательная железа (C61)
> 2 лет
Яички (C62)
> 2 лет
Глаза (C69)
> 2 лет
Головной мозг (C71)
> 2 лет
Щитовидная железа (C73)
> 2 лет
Лимфогранулематоз (C81)
> 5 лет
Неходжскинская лимфома (C82 - C85)
> 5 лет
Лейкоз (C91 - C95)
> 5 лет
Б.2. Схемы, используемые в клинических рекомендациях
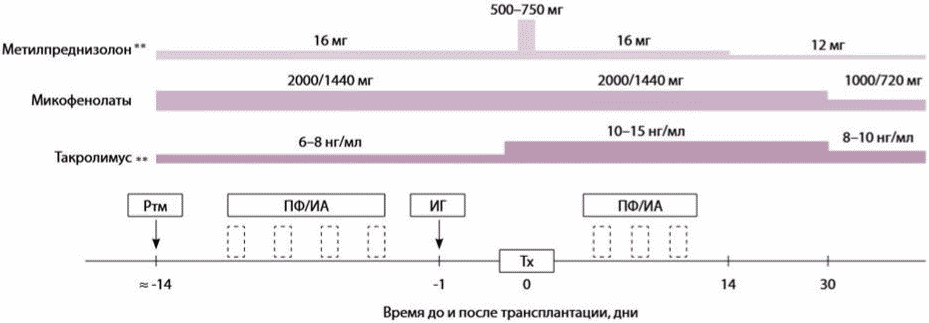
Схема 1. Персонализированный протокол ведения пациентов, которым планируется выполнение трансплантации почки от живого донора, несовместимого по групппе крови [152]
ИС - иммуносупрессивная терапия; ПФ - плазмаферез; ИА - иммуноадсорбция;
ТП - трансплантация почки, Ртм - #ритуксимаб**, ИГ - #иммуноглобулин человека нормальный**, Тx - трансплантация, микофенолаты - макофенолат мофетил** (микофеноловая кислота**).
#Микофенолата мофетил**, #микофеноловая кислота** применяются у детей вне инструкции по медицинскому применению. Дозы иммунодепрессантов, которые применяются в детском возрасте, представлены в таблице 1 (Приложение А3) [336].
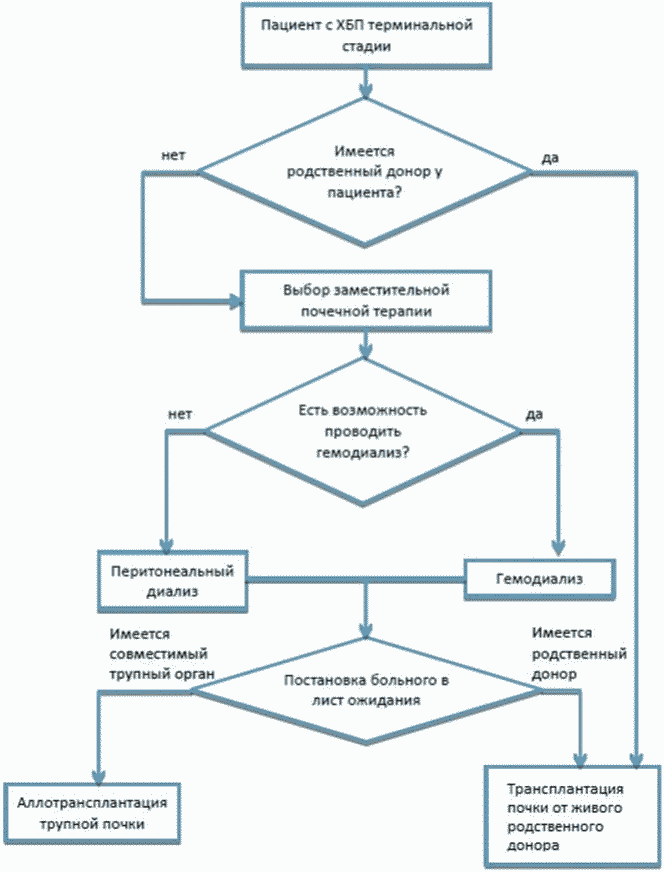
Схема 2. Алгоритм ведения пациента с терминальной стадией почечной недостаточности
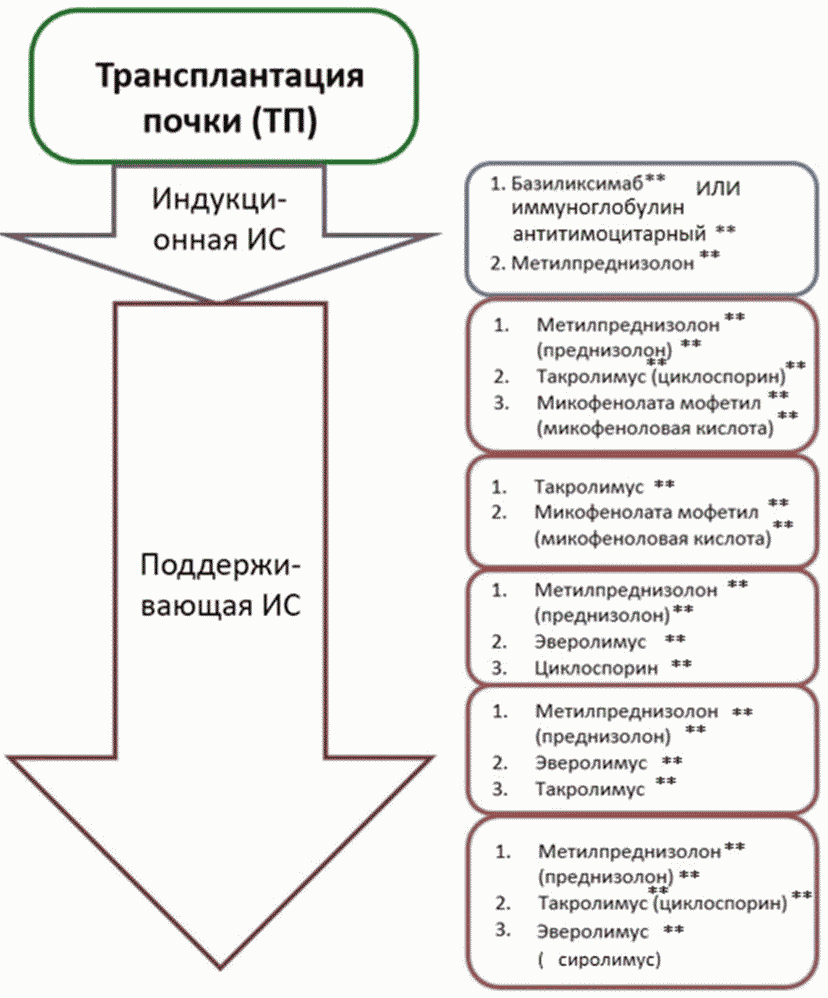
Схема 3. Различные виды иммуносупрессивной терапии. Адаптирована из "Трансплантология. Фармакотерапия без ошибок" руководство для врачей/под ред. С.В. Готье и Я.Г. Мойсюка. - М.: "Е-ното", 2014. - 432 с. [311]
#Микофенолата мофетил**, #микофеноловая кислота**, #эверолимус** и #сиролимус применяются у детей вне инструкции по медицинскому применению. Дозы иммунодепрессантов, которые применяются в детском возрасте, представлены в таблице 1 (Приложение А3) [336].
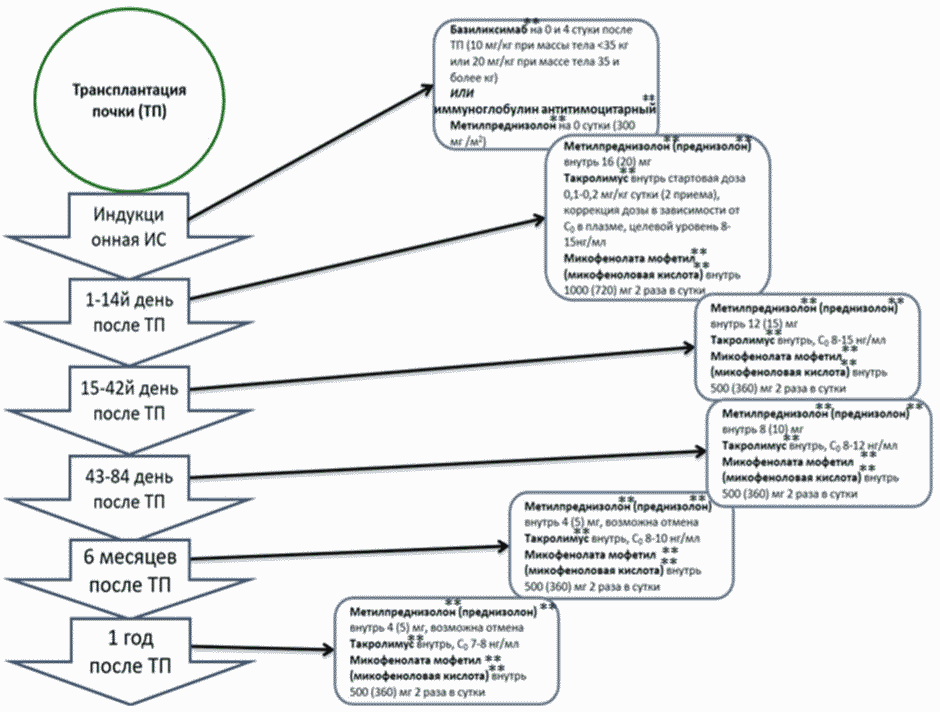
Схема 4. Схема иммуносупрессивной терапии после трансплантации почки. Адаптирована из "Трансплантология. Фармакотерапия без ошибок" руководство для врачей/под ред. С.В. Готье и Я.Г. Мойсюка. - М.: "Е-ното", 2014. - 432 с. [311]
#Микофенолата мофетил** и #микофеноловая кислота** применяются у детей вне инструкции по медицинскому применению. Дозы иммунодепрессантов, которые применяются в детском возрасте, представлены в таблице 1 (Приложение А3) [336].
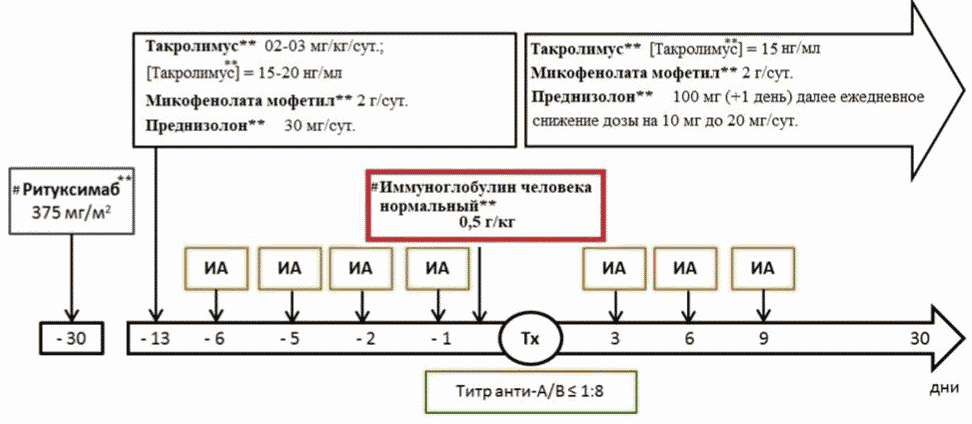
Схема 5. "Стокгольмский" протокол проведения AB0-несовместимой трансплантации почки от живого родственного донора. ИА - специфическая иммуноадсорбция; Тx - трансплантация почки [152].
#Микофенолата мофетил** и #микофеноловая кислота** применяются у детей вне инструкции по медицинскому применению. Дозы иммунодепрессантов, которые применяются в детском возрасте, представлены в таблице 1 (Приложение А3) [336].
Приложение В
ИНФОРМАЦИЯ ДЛЯ ПАЦИЕНТА
В случае, если между Вами и Вашим лечащим врачом будет достигнуто решение о необходимости проведения операции трансплантации почки, необходимо будет пройти процедуру типирования, в результате которой Ваша кровь будет взята для проведения соответствующего анализа на присутствие в ней определенных антигенов, генетически свойственных именно Вашему организму.
Антигенами называют определенные виды белков. Ими могут быть, например, антигены, присущие именно Вашей группе крови, резус-фактор, и т.д. Процедура типирования необходима для того, чтобы можно было подобрать донорский орган, который был бы генетически максимально близким Вашему организму по образцам присутствующих в нем антигенов. Важнейшую роль при этом играют так называемые лейктоцитарные антигены тканевой совместимости (HLA). В результате появляется возможность создать наиболее благоприятные условия приживаемости трансплантата. Совпадение большого числа антигенов может наблюдаться лишь у очень близких родственников, поэтому донорская почка будет подбираться лишь по определенному их числу, и успех приживаемости в послеоперационный период и возможные осложнения во многом будут зависеть от точности подбора донорской почки по результатам типирования.
Учеными установлено, что в реакции иммунного ответа участвуют следующие клетки: T-лимфоциты, макрофаги (фагоциты) и B-лимфоциты. Задача иммуносупрессивной терапии заключается в регуляции деятельности этих клеток.
Иммунные реакции Вашего организма, на присутствие в донорском органе антигенов, не свойственных Вашему организму, будут компенсированы проводимой иммуносупрессивной терапией.
В период предоперационной подготовки следует остерегаться контакта с чужеродными белками иммунной системы организма будущего пациента. Контакт с чужеродными белками приводит к повышению содержания в крови так называемых предсуществующих антител и накоплению их в организме, что препятствует выполнению операции трансплантации, так как это может привести к отторжению трансплантата на ранних сроках.
По результатам HLA-типирования Вы будете включены в лист ожидания донорского органа. Само ожидание занимает довольно длительное время, так как донорская почка должна быть здоровой, подходить Вам по результатам типирования и иметь размеры, массу и возраст, максимально соответствующие Вашему организму. Отметим, что разница в возрасте донора и реципиента не должна превышать 15 лет.
Ожидание почки может продлиться до двух лет, так как это связано с острейшим дефицитом донорских органов. В течение этого времени будет продолжена терапия гемо- или перитонеальным диализом. Всегда имейте в виду, что операция может быть назначена в любое время. Если же к моменту нахождения подходящей почки Вы будете нездоровы или по другим причинам не будете готовы к трансплантации почки, операция может быть отложена на длительное время.
Постарайтесь хорошо подготовиться к этому моменту. Посетите зубного врача. Кариес, пародонтоз и другие заболевания полости рта являются источником инфекции, которая может очень некстати проявить себя в послеоперационный период.
Не забудьте оставить в Центре трансплантации и в Диализном центре все телефоны, по которым лечащему врачу Вас можно будет найти в любое время суток в случае подбора подходящего донорского органа. В Центре трансплантации оставьте также телефон Диализного центра, за которым Вы закреплены. При необходимости отъезда предупредите лечащего врача и оставьте ему контактные телефоны. Всегда держите наготове все необходимое, включая предметы гигиены, домашнего обихода, а также одежду, которая могла бы Вам понадобиться во время пребывания в Центре трансплантации.
Имейте в виду, что в любой момент Вас могут вызвать на операцию, и с этого момента фактор времени будет играть решающую роль.
Однако необходимо отметить, что, к сожалению, не всем нуждающимся можно помочь, так как операции трансплантации почки существует ряд противопоказаний.
Среди абсолютных противопоказаний - злокачественные новообразования, нарушения обмена веществ (оксалоз), активный СПИД или гепатит, активный туберкулез, терминальная стадия другого заболевания, тяжелая сосудистая патология, наркотическая зависимость, а также, если прогнозируемая продолжительность жизни больного - менее пяти лет.
Среди относительных противопоказаний - первичное заболевание почек с высокой вероятностью рецидива в трансплантате, хроническая инфекция мочевыводящих путей, тяжело поддающаяся лечению, декомпенсированный сахарный диабет и эмоциональная неустойчивость больного.
Операции трансплантации почки
Если врачи сообщат Вам о том, что подходящая донорская почка находится в их распоряжении, необходимо, не теряя времени, собрать нужные вещи, предупредить лечащего врача в Диализном центре и ехать в Центр трансплантации.
С момента сообщения Вам о предстоящей операции воздержитесь от принятия воды и пищи.
Попросите своих родственников или друзей сопроводить Вас в Центр трансплантации на автомобиле или такси.
Если же Вы не готовы к предстоящей операции, немедленно поставьте в известность лечащего врача в Центре трансплантации, так как в этом случае донорская почка будет востребована другим больным, нуждающимся в трансплантации.
По прибытии в Центр трансплантации Вы пройдете предоперационное обследование, которое включает взятие анализа крови на предмет выявления грубых электролитных расстройств (К, Na), контроль показателей гемоглобина и гематокрита, измерение давления, температуры и веса. В случае необходимости корректировки показателей крови Вам будет произведен сеанс гемодиализа. Кроме этого, с Вами побеседует врач-анестезиолог для решения вопроса выбора наиболее щадящей формы наркоза для того, чтобы можно было бы свести к минимуму риск связанных с ним проблем.
Необходимо обязательно иметь выписку из стационара, где должны быть подробно указаны последние анализы и обследования.
Вам также потребуется подтвердить согласие на операцию в письменной форме.
После осуществления необходимых санитарно-гигиенических мероприятий непосредственно перед проведением трансплантации Вы будете взяты на операционный стол. Через локтевую или подключичную вену Вам установят катетер для введения на время операции растворов и медикаментов.
Время проведения операции колеблется в пределах трех-четырех часов. Донорская почка пересаживается в правую или левую подвздошную область в забрюшинное пространство в зависимости от того, правая или левая почка находится в распоряжении врача-хирурга. Ваши собственные почки останутся нетронутыми. Кровеносные сосуды донорской почки соединяются с Вашими кровеносными сосудами, а ее мочеточник - с мочевым пузырем. Кроме того, может быть установлен дренажный катетер для удаления жидкости, скапливающейся вокруг пересаженной почки в первые дни после операции.
Первое время Вы будете находиться под постоянным мониторингом в отделении интенсивной терапии, а потом, в зависимости от общего состояния, переведены в палату отделения.
Возможно, в первое время возникнет необходимость в проведении одного или нескольких сеансов гемодиализа. Это связано с тем, что функционирование донорской почки может быть отсрочено, что обусловлено пребыванием донорского трансплантата до проведения операции в консервирующем растворе.
Вставать с постели разрешается на следующий день, при условии, что вы носите послеоперационный бандаж. В случае гладкого послеоперационного периода, раннего восстановления функции трансплантата и нормализации показателей крови Вас выпишут домой уже через 2 - 3 недели после трансплантации почки.
В течение всего времени пребывания в стационаре за функциональным состоянием пересаженной почки и за Вашим состоянием здоровья будет вестись постоянное наблюдение, включающее постоянное измерение температуры, веса, проведение анализов крови и мочи.
Контроль состояния пересаженной почки после операции осуществляется ультразвуковыми радиоизотопными методами, а также допплерографическим исследованием артериального и венозного кровообращения в пересаженном органе.
Также для контроля деятельности трансплантата иногда требуется процедура биопсии. Биопсией почки врачи называют взятие на анализ образца почечной ткани для подтверждения правильности выбранной схемы лечения, либо для диагностирования различных нарушений функции почки, что позволяет сделать выбор в пользу наиболее эффективного метода лечения. С этой целью врач под местной анестезией специальным приспособлением в области пересаженной почки производит укол, а затем исследует полученный образец почечной ткани под микроскопом.
Назначенные в первое время после операции большие дозы медикаментов призваны подавлять иммунитет для того, чтобы донорская почка не отторгалась Вашим организмом. Угнетение же иммунитета, в свою очередь, вызывает большую восприимчивость к различным инфекциям.
Помните, что особенно в первое время опасен контакт с возможными инфекциями, поэтому предупредите лечащего врача об имевших место и возможных контактах с инфекционными больными.
Особое внимание необходимо уделять наблюдению за показателями давления крови и уровня содержания в крови препарата, выполняющего функцию базового иммунодепрессанта. Врач также назначит и скорректирует схему и дозу приема других препаратов.
В дальнейшем необходимо постоянно наблюдаться у лечащего врача. Это позволит эффективно контролировать состояние здоровья и предупредить возможные осложнения.
Приложение Г1 - ГN
ШКАЛЫ ОЦЕНКИ, ВОПРОСНИКИ И ДРУГИЕ ОЦЕНОЧНЫЕ ИНСТРУМЕНТЫ
СОСТОЯНИЯ ПАЦИЕНТА, ПРИВЕДЕННЫЕ В КЛИНИЧЕСКИХ РЕКОМЕНДАЦИЯХ
Нет.
