"Клинические рекомендации "Миокардиты у детей"
МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ
КЛИНИЧЕСКИЕ РЕКОМЕНДАЦИИ
МИОКАРДИТЫ У ДЕТЕЙ
Кодирование по Международной статистической классификации болезней и проблем, связанных со здоровьем: I01.2, I09.0, I40, I41, I51.4
Год утверждения (частота пересмотра): 2025
Пересмотр не позднее: 2027
ID: 408_2
Возрастная категория: Дети
Специальность:
Разработчик клинической рекомендации
Всероссийская общественная организация "Ассоциация детских кардиологов России"
Одобрено Научно-практическим Советом Минздрава России
Список сокращений
BNP - Мозговой натрийуретический пептид (Brain natriuretic peptide)
GLS LV - Глобальная продольная деформация левого желудочка (Left ventricular global longitudinal strain)
LCC - Lake Louise Criteria
LGE - Позднее накопление гадолиний-содержащего контрастного вещества (Late gadolinium enchantment)
NT-proBNP - N-концевой фрагмент промозгового натрийуретического пептида (N-terminal prohormone of brain natriuretic peptide)
NYHA - Нью-Йоркская ассоциация сердца (New York Heart Association)
SIDS - Синдром внезапной смерти младенцев (sudden infant death syndrome)
TAPSE - Систолическая экскурсия кольца трикуспидального клапана (Tricuspid annular plane systolic excursion)
VAD - Устройство поддержки насосной функции желудочков сердца (Ventricular assist device)
АА - Антагонисты ангиотензина II
АВ - Атриовентрикулярный
АД - Артериальное давление
АСЛО - Антистрептолизин-О
ВИЧ - Вирус иммунодефицита человека
ВПС - Врожденный порок сердца
ВСС - Внезапная сердечная смерть
ГК - Глюкокортикоиды
ГЛЖ - Гипертрофия левого желудочка
ГСКВ - Гадолиний содержащее контрастное вещество (АТХ V08CA Парамагнитные контрастные средства)
ДКМП - Дилатационная кардиомиопатия
ДНК - Дезоксирибонуклеиновая кислота
иАПФ - Ингибитор ангиотензинпревращающего фермента (АПФ)
ИВЛ - Искусственная вентиляция легких
КДР - Конечно-диастолический размер
КДО - Конечно-диастолический объем
КМП - Кардиомиопатия
КСО - Конечно-систолический объем
КСР - Конечно-систолический размер
КТИ - Кардиоторакальный индекс
ЛЖ - Левый желудочек сердца
МНО - Международное нормализованное отношение
МРТ - Магнитно-резонансная томография
НПВП - Нестероидные противовоспалительные препараты (АТХ M01A Нестероидные противовоспалительные и противоревматические препараты)
ОЦК - Объем циркулирующей крови
ПМКС - Парамагнитные контрастные средства
ПЦР - Полимеразная цепная реакция
РНК - Рибонуклеиновая кислота
САД - Систолическое артериальное давление
СН - Сердечная недостаточность
СОЭ - Скорость оседания эритроцитов
СРБ - C-реактивный белок
ФВ - Фракция выброса
ФК - Функциональный класс
ФН - Физическая нагрузка
ХСН - Хроническая сердечная недостаточность
ЦВД - Центральное венозное давление
ЭКГ - Электрокардиография (регистрация электрокардиограммы)
ЭКМО - Экстракорпоральная мембранная оксигенация
ЭХОКГ - Эхокардиография
** - препарат включен в перечень жизненно необходимых и важнейших лекарственных препаратов
*** - медицинское изделие, имплантируемое при оказании медицинской помощи в рамках программы государственных гарантий бесплатного оказания гражданам медицинской помощи
# - при использовании препарата возможны отклонения от официальной инструкции по его применению
Термины и определения
Миокардит - это воспалительное поражение миокарда инфекционной, токсической, аллергической, аутоиммунной или неизвестной этиологии с широким спектром клинических проявлений от бессимптомного течения до явлений сердечной недостаточности (СН), жизнеугрожающих нарушений сердечного ритма и проводимости, кардиогенного шока и внезапной сердечной смерти (ВСС) [1, 2].
Миокардит - это воспалительное заболевание миокарда, диагностируемое по совокупности гистологических, иммунологических и иммуногистохимических критериев [3].
Воспалительная кардиомиопатия - миокардит, подтвержденный в соответствии с гистологическими и иммуногистохимическими критериями, с обязательной миокардиальной дисфункцией (по систолическому, диастолическому или смешанному типу) [3].
Дилатационная кардиомиопатия (ДКМП) - это клинический диагноз, характеризующийся развитием дилатации и нарушением сократительной функции левого и/или правого желудочков, которые не могут быть объяснены ишемической болезнью сердца или перегрузкой объемом [3 - 6].
1. Краткая информация по заболеванию или состоянию (группы заболеваний или состояний)
1.1 Определение заболевания или состояния (группы заболеваний или состояний)
Миокардит - это групповое понятие, объединяющее воспалительное поражение миокарда инфекционной, токсической, аллергической, аутоиммунной или неизвестной этиологии с широким спектром клинических проявлений от бессимптомного течения до явлений сердечной недостаточности, жизнеугрожающих нарушений сердечного ритма и проводимости, кардиогенного шока и внезапной сердечной смерти [1, 2].
Миокардит может быть самостоятельным патологическим процессом или сопутствовать инфекционным или системным заболеваниям, таким как дифтерия, корь, инфекционный эндокардит, системные васкулиты, системные заболевания соединительной ткани, и др. [1 - 6].
1.2 Этиология и патогенез заболевания или состояния (группы заболеваний или состояний)
Этиология миокардита
В большинстве случаев в клинической практике не удается установить этиологию миокардита, тем не менее, его причиной может стать любое инфекционное заболевание вирусной, бактериальной, грибковой, риккетсиозной, протозойной, паразитарной, смешанной этиологии, миокардит может быть одним из проявлений аутоиммунных, аллергических, соматических заболеваний, или результатом физического или токсического воздействия, включая лекарственные препараты [6, 7, 8].
Важно отметить, что этиопатогенез, дебют и течение миокардита значительно отличаются в зависимости от инфекционного агента [5].
Наиболее частой причиной миокардита у детей является вирусная инфекция. В настоящее время этиология вирусных миокардитов значительно варьирует в зависимости от возраста, географического региона, популяции, а также имеет тенденцию меняться с течением времени [7, 8, 9].
Следует четко различать вирусы, которые напрямую (кардиотропные и васкулотропные вирусы) или опосредованно (лимфотропные вирусы) проникают в сердце, и также вирусы, которые не обязательно поражают клетки сердца, а индуцируют их повреждение и снижение сократительной способности за счет цитокинового шторма или клеточного иммунного ответа с помощью молекулярной мимикрии [5].
Наиболее распространенными вирусами, связанными с развитием миокардита, являются:
- первично кардиотропные вирусы, которые могут быть элиминированы из сердца, в том числе аденовирусы и энтеровирусы (такие как Коксаки A и B, ECHO);
- васкулотропные вирусы, которые могут персистировать в организме на протяжении всей жизни (Парвовирус B19);
- лимфотропные вирусы, которые персистируют в организме на протяжении всей жизни, принадлежащие к семейству Herpesviridae (такие как вирус герпеса человека 6 (HHV6), вирус Эпштейна-Барра и Цитомегаловирус);
- вирусы, которые могут вызвать миокардит опосредованно, за счет активации иммунной системы, в том числе ВИЧ), вирус гепатита C, вирус гриппа A и B; вирусы из семейства Coronaviridae, в том числе MERS-CoV, SARS-CoV и SARS-CoV-2, которые имеют тропизм к ангиотензинпревращающему ферменту 2 и потенциально могут опосредованно вызвать прямое повреждение сердца. Увеличилась частота выявления двух и более вирусов [5, 10, 11].
У новорожденных и детей раннего возраста наиболее распространенной причиной миокардитов по-прежнему являются энтеровирусы Коксаки (типов B и реже A) и ECHO, а также ряд других кардиотропных вирусов.
Гораздо реже причиной врожденного миокардита могут быть один или несколько инфекционных агентов TORCH-комплекса: T-токсоплазмоз (Toxoplasmosis); O - другие инфекции (others), включая гепатиты, сифилис, хламидиоз, гонококковую инфекцию, листериоз, ВИЧ-инфекцию, ветряную оспу, энтеровирусную инфекцию; R - краснуха (Rubella); C - цитомегаловирусная инфекция (Cytomegalovirus); H - герпес (Herpes simplex virus) [12, 13].
Бактериальные агенты также могут быть причиной миокардита, но встречаются гораздо реже, и всегда в структуре основного заболевания. Из бактериальных миокардитов наиболее опасными являются дифтерийные (инфекционно-токсические), миокардиты при скарлатине, брюшном тифе и сальмонеллезах, туберкулезе, клещевом боррелиозе (болезнь Лайма), иерсиниозах (кишечном и псевдотуберкулезе), при генерализованных стрептококковых и стафилококковых инфекциях. Описаны спирохетозные миокардиты при врожденном и приобретенном висцеральном сифилисе и лептоспирозе, при паразитарных (токсоплазмоз, болезнь Шагаса, трихинеллез) и грибковых (аспергиллез, актиномикоз, кандидоз) заболеваниях, при микоплазменной и хламидийной инфекциях. Возможно, вариантом инфекционного миокардита неизвестной этиологии является болезнь Кавасаки с миокардитом, коронариитом, реже - острой сердечной недостаточностью, как правило у мальчиков до 5 лет [4, 14 - 17]. Также как вариант инфекционного миокардита в настоящее время рассматривается миокардит при SARS-CoV-2 инфекции, постинфекционного - при мультисистемном воспалительном синдроме (после SARS-CoV-2), который имеет общие детерминанты иммунопатогенеза с болезнью Кавасаки [18].
Миокардит может быть вызван различными токсическими веществами и лекарствами. Реакция гиперчувствительности к некоторым препаратам (гидрохлоротиазид**, фуросемид**, пенициллины широкого спектра действия, азитромицин**, сульфаниламиды, тетрациклин, метилдопа**, аминофиллин**, фенитоин**, производные бензодиазепина и др.), а также к вакцинам и сывороткам реализуется в эозинофильный миокардит. Частота таких миокардитов невысокая. Дебют болезни приходится на первые часы/дни после начала терапии, но может быть и отсроченным (подобные случаи описаны для препарата Клозапин) [4].
Максимальное число кардиотоксических осложнений, включая воспалительную кардиомиопатию, описано при использовании противоопухолевых антибиотиков из группы антрациклинов (АТХ L01DB) (доксорубицина**, даунорубицина**, идарубицина**). Согласно современным представлениям, механизм кардиотоксичности связан с блокадой топоизомеразы 2b и разрывом обеих цепей дезоксирибонуклеиновой кислоты (ДНК), что приводит к гибели кардиомиоцитов с развитием асептического воспаления [19, 20, 21].
К числу неинфекционных форм миокардита также относятся:
- миокардиты при системных заболеваниях соединительной ткани с иммунными нарушениями и системных васкулитах (системная красная волчанка, дерматополимиозит, системная склеродермия, ювенильный артрит, гранулематоз Вегенера и др.);
- эозинофильный миокардит в структуре гиперэозинофильного синдрома, глистной инвазии, паразитарных инфекций и др.
К числу редких аутоиммунных и идиопатических миокардитов относятся:
- некротизирующий эозинофильный миокардит, причиной развития которого может быть синдром гиперчувствительности и системный васкулит Чарга-Стросса. При этом нельзя исключить роль вирусной (в частности, герпетической) инфекции, как причины фульминантного течения заболевания с быстрым нарастанием симптомов СН и высокой смертностью;
- идиопатический гигантоклеточный миокардит, характеризующийся крайне тяжелым прогнозом. Чаще всего заболевают подростки. 20% пациентов с верифицированным гигантоклеточным миокардитом имеют еще какое-либо аутоиммунное заболевание и аллергические реакции, в т.ч. на лекарственные препараты;
- саркоидоз сердца - один из видов гранулематозного миокардита, который может развиваться в рамках идиопатического системного заболевания, а может носить изолированный характер [3].
Патогенез миокардита
Современные представления о патогенезе и естественном течении миокардитов базируются, главным образом, на результатах экспериментальных исследований на мышах, зараженных вирусом Коксаки B [22]. В организм человека вирус Коксаки B проникает через желудочно-кишечный тракт или дыхательную систему.
Патогенетический процесс можно концептуально разделить на три фазы: фаза 1 (1 - 7 дней) проникновение вируса в кардиомиоцит и активация врожденного иммунного ответа, фаза 2 (подострая фаза) - активация адаптивного (приобретенного) иммунного ответа (1 - 4 недели) и хроническая фаза (от нескольких месяцев до нескольких лет), при которой отсроченный или неэффективный клиренс вируса на фоне хронического воспаления и ремоделирования сердца может привести к развитию ДКМП [5].
В первую фазу болезни (1 - 7 дней) повреждение миокарда в основном развивается за счет прямого вирусного поражения кардиомиоцитов. Пусковым механизмом развития воспалительного процесса является прикрепление вируса к эндотелиальному рецептору (CAR-рецептор - химерный антигенный рецептор) [23]. Проникнув в кардиомиоциты, вирусы реплицируются, вызывая миоцитолиз и активацию синтеза микроРНК, что в свою очередь приводит к апоптозу и некрозу. Участвующие в этом процессе лимфоциты (CD4+ и CD8+), продукты лимфоцитов, стимулирующие апоптоз (перфорины, сериновые эстеразы), различные цитокины оказывают двоякий эффект: клиренс патогенов и повреждение миокарда. Измененные кардиомиоциты запускают иммунные реакции, приводящие к развитию воспаления в миокарде и формированию воспалительной клеточной инфильтрации. Первая фаза заболевания может завершиться полной элиминацией возбудителя с клиническим выздоровлением в течение 2 - 4 недель, что наблюдается у большинства детей, или развитием острой СН (кардиогенного шока), фатальных аритмий с возможностью летального исхода. Поскольку экспрессия рецепторов CAR максимально выражена в перинатальном периоде, более частое развитие и тяжелое течение заболевания отмечается у детей раннего возраста.
Вторая фаза представляет собой формирование острой или персистирующей миокардиальной дисфункции вследствие вторичного вирус-опосредованного аутоиммунного повреждения миокарда перекрестно-реагирующими антителами. Иммунологическая недостаточность, в том числе генетически детерминированная особенность противоинфекционного иммунного ответа, становится причиной развития аутоиммунных процессов с выработкой антител к структурам кардиомиоцитов и приобретает ведущую роль в дальнейшем миокардиальном повреждении и прогрессировании дисфункции миокарда на следующих этапах болезни.
У части пациентов вирусный геном не покидает клетку, поддерживая иммунное воспаление. Клинически в таком случае имеет место воспалительная кардиомиопатия (подострый/хронический миокардит). Итогом миокардиального ремоделирования становится развитие 3 фазы - стойкой миокардиальной дисфункции, ведущей к формированию ДКМП. Развивающаяся при этом СН сопровождается гиперпродукцией нейрогормонов и дальнейшим системным и миокардиальным синтезом провоспалительных цитокинов ( , ИЛ 1, ИЛ 6, ИЛ 8), поддерживающих ремоделирование и прогрессирующую дисфункцию миокарда.
, ИЛ 1, ИЛ 6, ИЛ 8), поддерживающих ремоделирование и прогрессирующую дисфункцию миокарда.
На фоне анатомо-физиологических особенностей миокарда новорожденных и детей раннего возраста эти процессы являются причиной быстрого дезадаптивного ремоделирования миокарда с развитием сферичности, кардиомегалии с нарушением функции левого желудочка (ЛЖ), быстрой декомпенсации кровообращения, нарушений ритма.
Выделение этих трех фаз на практике не всегда возможно, так как хронологически они могут пересекаться, а первая и вторая фазы могут повториться при уже сформировавшейся дилатации камер и дисфункции миокарда [5, 24, 25].
Имеются данные о роли генетических факторов в предрасположенности к возникновению и вероятности развития тяжелых форм миокардита, особенно у пациентов с отягощенным анамнезом по внезапной сердечной смерти [26].
Генетический анализ пациентов с персистирующей дисфункцией ЛЖ или аритмиями после эпизода острого миокардита показал, что значительная часть из них является носителем патогенного варианта мутации в генах, кодирующих синтез саркомерных или десмосомных белков [27].
1.3 Эпидемиология заболевания или состояния (группы заболеваний или состояний)
Истинную частоту миокардита в педиатрической популяции оценить чрезвычайно сложно из-за большой вариабельности симптомов (от минимальных ЭКГ изменений до кардиогенного шока и внезапной смерти), наличия латентных (бессимптомных) форм, большой частоты спонтанного выздоровления (до 40 - 57%) и отсутствия единых диагностических протоколов для педиатрической популяции пациентов. Крайне редкое применение на практике "золотого стандарта диагностики" - биопсии миокарда также затрудняет верификацию диагноза [28 - 30].
Ежегодная заболеваемость у детей колеблется от 0,26 до 2 случаев на 100 000 детей [31, 32, 33].
Сообщается, что 0,05% всех детских госпитализаций связаны с миокардитом [34].
Заболеваемость миокардитом имеет два возрастных пика: первые несколько лет жизни и подростковый возраст, причем у маленьких детей прогноз хуже [31, 35, 36].
Несмотря на редкую встречаемость, миокардит является одной из частых причин заболеваемости и смертности у детей. Высокий процент пациентов развивает тяжелую сердечную недостаточность, которая требует кардиотонической поддержки, ИВЛ, механической поддержки кровообращения [33, 35, 36, 37].
Общая смертность в остром периоде течения миокардита достигает 7 - 15% [33, 36, 37].
Анализ результатов посмертных исследований позволил выявить значимую клиническую проблему - прижизненную гиподиагностику миокардитов из-за неспецифических признаков дебюта и часто бессимптомного течения заболевания [32].
Признаки миокардита по данным аутопсии при синдроме внезапной детской смерти - SIDS - sudden infant death syndrome) были выявлены в 16 - 20% и стали причиной внезапной смерти у 17% подростков младше 16 лет [33, 38, 39].
30-летний анализ ВСС у детей и молодых людей показал, что среди умерших от сердечных причин детей 3 - 13 лет у 11% был диагностирован и подтвержден при аутопсии миокардит [40].
Морфологически подтвержденный миокардит может иметь место при другой кардиальной патологии, в частности, при кардиомиопатиях. Так, результаты исследования Australian Childhood Cardiomyopathy Study (1986 - 1997 гг.) свидетельствовали, что у 40,2% детей с разными вариантами кардиомиопатии по данным биопсии был также диагностирован миокардит [41].
Летальность при миокардитах зависит от тяжести основного заболевания, преморбидного фона, возраста, пола пациентов. Она резко различается по данным разных авторов и варьирует от 0,03% до 26% [30, 42, 43].
Заболеваемость и смертность от миокардита, по-видимому, выше в популяции лиц, подвергнутых интенсивным физическим нагрузкам, возможно вследствие ослабления противовирусного иммунитета. Установлено, что миокардит явился одной из наиболее частых (среди органических повреждений миокарда) причин внезапной смерти молодых атлетов до 18 лет [44, 45].
1.4 Особенности кодирования заболевания или состояния (группы заболеваний или состояний) по Международной статистической классификации болезней и проблем, связанных со здоровьем
I40 - Острый миокардит
I40.0 - Инфекционный миокардит
I40.1 - Изолированный миокардит
I40.8 - Другие виды миокардита
I40.9 - Острый миокардит неуточненный
I41 - Миокардит при болезнях, классифицированных в других рубриках
I41.0 - Миокардит при бактериальных болезнях, классифицированных в других рубриках
I41.1 - Миокардит при вирусных болезнях, классифицированных в других рубриках
I41.2 - Миокардит при инфекционных и паразитарных болезнях, классифицированных в других рубриках
I41.8 - Миокардит при других болезнях, классифицированных в других рубриках
I51.4 - Миокардит неуточненный
I01.2 - Острый ревматический миокардит
I09.0 - Ревматический миокардит
В МКБ-10 присутствует рубрика "острые" миокардиты и отсутствует рубрика "хронические" миокардиты. Поэтому, если воспалительное заболевание миокарда имеет не тяжелое (затяжное или хроническое), а относительно благоприятное течение, оно может быть отнесено в рубрику "миокардиты" с кодами - I41.1; I41.0; I41; I41.2; I41.8; I51.4.
При неблагоприятном хроническом течении с прогрессирующими кардиомегалией и сердечной недостаточностью заболевание может быть отнесено в рубрику "кардиомиопатии" с кодами I42 - воспалительная кардиомиопатия. Данным термином в большинстве современных исследований называют хронический миокардит.
В этой связи рекомендуется применять любую доступную для лечебного учреждения классификацию параллельно с МКБ-10. Однако при оформлении диагноза или медицинского свидетельства о смерти и кодировании миокардита требуется применять термины и коды МКБ-10 (в диагнозе - с последующей расшифровкой, согласно применяемой классификации).
1.5 Классификация заболевания или состояния (группы заболеваний или состояний)
Общепринятой классификации миокардитов не существует. Предлагаемые классификации в той или иной степени отражают этиологические факторы, патогенетические механизмы развития и варианты течения.
В отечественной детской кардиологии используют рабочую классификацию, согласно которой определяют период возникновения болезни, этиологический фактор, форму, степень тяжести и исходы (таблица 1).
Таблица 1. Классификация миокардитов у детей (по Н.А. Белоконь, 1984 г. в модификации рабочей группы АДКР (Ассоциации детских кардиологов России) 2021 г.)
Период возникновения заболевания
Врожденный
Приобретенный
Этиологический фактор
Вирусный, бактериальный, грибковый, спирохетозный, риккетсиозный, аллергический, токсический, аутоимунный, идиопатический и др.
Течение
Фульминантный (молниеносный)
Острый - до 6 недель от начала заболевания
Подострый - от 6 недель до 6 месяцев
Хронический (активный/персистирующий) - более 6 месяцев от начала заболевания
Тяжесть миокардита
Легкий
Среднетяжелый
Тяжелый
Исходы
Выздоровление, кардиосклероз, дилатационная кардиомиопатия, летальный исход
Осложнения
Кардиогенный шок, нарушение ритма и проводимости, тромбоэмболический синдром, гипертрофия миокарда, легочная гипертензия, поражение клапанов.
В клинической практике используется клинико-морфологическая классификация (E.B. Lieberman с соавт. 1991 г.), согласно которой различают следующие формы миокардита: фульминантный (молниеносный), острый, хронический активный, хронический персистирующий [46]. Однако, использование ее в педиатрической практике ограничено в связи с тем, что одним из основных критериев является гистологическая оценка по данным биопсии миокарда, которая у детей применяется крайне редко. В последующие варианты этой классификации, дополненные другими экспертами, были внесены 2 дополнительных клинических варианта: гигантоклеточный и эозинофильный миокардиты (таблица 2). На сегодняшний день данная классификация используется чаще, чем другие [6, 46].
Таблица 2. Клинико-морфологическая классификация миокардита [6, 15, 46].
Клиническая характеристика
Клиническая форма миокардита
Молниеносные (фульминантные)
Острые
Подострые
Хронические активные
Хронические персистирующие
Гигантоклеточный
Начало заболевания
Молниеносное начало с развитием симптомов сердечной недостаточности в течение нескольких дней от начала заболевания
Менее отчетливое по сравнению с молниеносной формой миокардита
Менее отчетливое по сравнению с молниеносной формой миокардита
Нечетко очерченное
Нечетко очерченное
Дебют острый.
Быстрая прогрессирующая рефрактерная СН, устойчивые желудочковые нарушения ритма и проводимости
Данные биопсии миокарда
Множественные очаги активного воспаления
Активный и пограничный миокардит
У большинства пациентов слабовыраженное воспаление. Активный и пограничный миокардит у 80% и 20% пациентов соответственно
Активный или пограничный миокардит.
Длительное сохранение воспалительной инфильтрации в миокарде в сочетании с некрозом кардиомиацитов
В воспалительном инфильтрате гигантские многоядерные клетки - результат трансформации макрофагов, содержащие фагоцитированные фрагменты разрушенных кардиомиацитов.
Определяются зоны воспалительных инфильтратов с признаками активного воспаления и очаги некроза кардиомиацитов
Выраженность дисфункции
Выраженное снижение ФВ ЛЖ при нормальном или дилатированном ЛЖ
Снижение ФВ ЛЖ при нормальном или дилатированном ЛЖ
Снижение ФВ ЛЖ и дилатация ЛЖ
Умеренное снижение функции ЛЖ
Отсутствие дисфункции желудочков
Выраженное снижение сократительной способности миокарда
Исход
В течение 2 недель или наступает смерть, или полное выздоровление с восстановлением структуры и функции миокарда
Полное восстановление или возможно формирование ДКМП
Высокая частота трансформации в ДКМП
Формирование ДКМП, в некоторых случаях - рестриктивного фенотипа.
В целом прогноз благоприятный
Прогноз заболевания крайне тяжелый. Наиболее эффективный метод лечения - трансплантация сердца.
Молниеносный (фульминантный) миокардит - тяжелая форма воспалительного поражения миокарда, развивающаяся стремительно в виде СН, кардиогенного шока или жизнеугрожающих нарушений ритма и проводимости сердца. Наиболее часто встречается у новорожденных и детей раннего возраста. Удается установить четкую временную связь кардиальных симптомов и жалоб с перенесенной острой вирусной или бактериальной инфекцией, имевшей место за несколько дней - 2 недели до манифеста миокардита.
Дебют болезни всегда внезапный. Часто лихорадка выше 38 °C. Заболевание чаще начинается не с сердечно-сосудистых, а таких симптомов, как рвота, боль в животе, кашель и обморок, в связи с чем в первые несколько суток велика вероятность ошибочного диагноза. Стремительно развиваются гемодинамические расстройства или злокачественные аритмии [47].
При эхокардиографии определяется значительное снижение сократительной способности, отсутствие выраженной дилатации камер сердца, отек миокарда. В биоптатах миокарда выявляются множественные очаги воспалительной инфильтрации, возможно наличие очагов некроза. В течение 2 недель эта форма миокардита может завершиться либо полным выздоровлением и восстановлением функции ЛЖ, либо быстрым прогрессированием СН, стойкой гипотонией и летальным исходом. Летальность при развитии фульминантного миокардита может достигать до 50% [31]. При таком варианте течения заболевания необходимо использование кардиотонических средств (АТХ C01C), искусственной вентиляции легких, максимально раннее применение устройств вспомогательного кровообращения для обеспечения гемодинамической поддержки.
Острый (нефульминантный) миокардит - может иметь клинически более постепенное начало с поражением сердечно-сосудистой системы различной степени тяжести и не всегда полным выздоровлением, с развитием сердечной дисфункции, сердечной недостаточности и, реже, к смерти. Гистологически наблюдаются признаки активного или пограничного миокардита, которые со временем полностью исчезают.
Подострый миокардит - дебют болезни, как правило, стертый. Пациент и его родители затрудняются с хронологией начала заболевания и связью с предшествующим острым инфекционным (респираторным или кишечным) заболеванием, но всегда четко сообщают о манифесте болезни с проявлений СН или болей в грудной клетке ("маска" острого коронарного синдрома). При эхокардиографии определяется значительное расширение полостей сердца и снижение сократительной способности миокарда. Анализ гистологической картины биопсии миокарда позволяет выявить умеренно выраженные воспалительные инфильтраты. Для этой формы миокардита характерен переход в ДКМП.
Хронический активный миокардит - дебют болезни нередко остается не замеченным пациентом, даже тщательный расспрос не позволяет определиться с продолжительностью заболевания. Доминируют жалобы, типичные для хронической СН. При ультразвуковом исследовании сердца определяется умеренное снижение сократительной способности миокарда. Анализ гистологической картины биопсии миокарда позволяет выявить сочетание воспалительных инфильтратов различной степени выраженности с полями выраженного фиброза. В клинической картине доминирует хроническая СН II - III ФК. Типичны рецидивы миокардита и переход в дилатационную кардиомиопатию.
Хронический персистирующий миокардит - дебют болезни чаще остается незамеченным, продолжительность заболевания неизвестна. В клинической картине очень медленно и постепенно нарастают клинические проявления ремоделирования миокарда с дилатационным фенотипом. При ультразвуковом исследовании сердца отсутствует значимая дилатация полостей сердца и определяется умеренное снижение сократительной способности миокарда. Анализ гистологической картины биопсии миокарда позволяет выявить сочетание воспалительных инфильтратов различной степени выраженности с некротическими изменениями и полями фиброза. Исход заболевания благоприятный.
Гигантоклеточный миокардит - дебют заболевания острый. Болеют чаще подростки. Типично быстрое развитие и прогрессирование выраженной, рефрактерной к терапии СН. Вторая особенность клинической картины - устойчивые нарушения ритма и проводимости сердца. В анамнезе часто определяются аутоиммунные заболевания. Анализ гистологической картины биоптатов миокарда позволяет выявить в воспалительном инфильтрате гигантские многоядерные клетки - результат трансформации макрофагов, содержащие фагоцитированные фрагменты разрушенных кардиомиоцитов. Определяются также зоны воспалительных инфильтратов с признаками активного воспаления и очаги некроза. Прогноз заболевания крайне тяжелый. Наиболее эффективный метод лечения - трансплантация сердца.
Эозинофильный миокардит - дебют болезни острый. Доминируют проявления недостаточности кровообращения. При сборе анамнеза необходимо уделить особое внимание анализу аллергологического анамнеза, лекарственной терапии, указаниям на вакцинацию, глистную инвазию, в ряде ситуаций удается предположить связь с приемом нового препарата или продукта питания. Чаще всего острые эозинофильные аллергические миокардиты развиваются на фоне приема сульфаниламидов, противоэпилептических препаратов и психотропных средств.
Специалистами клиники Мейо была предложена простая и удобная классификация миокардитов, основанная на оценке исходного состояния пациентов. Классификация клиники Mayo (Mayo clinic classification) [48] позволяет определиться с прогнозом и выбором тактики лечения. На основе 3 ведущих симптомов: боли в грудной клетке, аритмии, проявления СН различают пациентов высокого, умеренного и низкого риска (таблица 3).
Таблица 3. Клинические варианты дебюта миокардита (классификация клиники Mayo)
Миокардит
Низкий риск
Промежуточный риск ("серая зона")
Высокий риск
Боль в грудной клетке
Умеренно выраженные сохраняющиеся структурные и функциональные изменения миокарда
Стойкая декомпенсация кровообращения
Суправентрикулярные нарушения ритма
Выраженная стойкая дисфункция ЛЖ
АВ-блокады
Нестойкие желудочковые аритмии
Жизнеугрожающие аритмии
Сохранная сократительная функция сердца
Позднее накопление гадолиния в миокарде в отсутствие ремоделирования камер сердца
Стойкие АВ-блокады на фоне выраженной дисфункции ЛЖ
Быстрый ответ на проводимую терапию (1 - 4 недели)
Рецидивирующие синкопальные состояния
Отсутствие жизнеугрожающих нарушений ритма и проводимости
Отсутствие синкопальных состояний
Прогноз благоприятный
Прогноз неопределенный
Прогноз неблагоприятный
Пациенты низкого риска имеют благоприятный прогноз. Болезнь начинается с типичных болей в грудной клетке и суправентрикулярных аритмий. Сократительная функция ЛЖ сохранена. Характерен быстрый ответ на проводимую терапию и нормализация показателей электрокардиографии (ЭКГ) и эхокардиографии (ЭХОКГ) в течение 1 - 4 недель.
У пациентов промежуточного риска прогноз неопределенный. При анализе ЭКГ и ЭХОКГ определяются умеренно выраженные структурные и функциональные изменения ЭХОКГ. Жизнеугрожающие нарушения ритма и проводимости не регистрируются, характерны нестойкие желудочковые аритмии. Синкопальных состояний нет. Типична регистрация позднего накопления парамагнитного контрастного средства (ПМКС), в частности гадолиний-содержащего контрастного вещества (ГСКВ), в миокарде по данным МРТ в отсутствие ремоделирования камер сердца и выраженного снижения сократительной способности ЛЖ.
Пациенты высокого риска: прогноз тяжелый, но во многом зависит от раннего ответа на проводимую терапию, динамики клинических симптомов (симптомы СН, жизнеугрожающие аритмии, атриовентрикулярные блокады, синкопальные состояния) и параметров ЭХОКГ (ФВ ЛЖ).
1.6 Клиническая картина заболевания или состояния (группы заболеваний или состояний)
Анамнез заболевания
Для врожденных миокардитов характерен отягощенный острыми или хроническими инфекционными заболеваниями матери пренатальный анамнез, возможны такие состояния, как задержка внутриутробного развития, нарушение звучности сердечных тонов либо аритмии плода, которые могут стать причиной преждевременного родоразрешения. При ультразвуковом исследовании антенатально у плода также может выявляться дилатация сердечных камер и/или гипертрофия стенок.
Для приобретенных миокардитов, в том числе постнатальных, имеют значение анамнестические указания на связь кардиальных симптомов с предшествующими (1 - 2 недели) эпизодами вирусных, бактериальных инфекций, неясной лихорадки, аллергическими реакциями, вакцинацией.
Следует учитывать контакт с больной матерью или родственниками, эпидемические вирусные инфекции в организованных коллективах, внутрибольничные вспышки.
В то же время необходимо помнить о том, что связь с предшествующей инфекцией и с иными возможными этиологическими факторами миокардитов может отсутствовать.
Клиническая картина
У детей клинические проявления варьируют от бессимптомного или субклинического течения без выраженных кардиальных симптомов и нормальной систолической функцией до тяжелой острой СН, кардиогенного шока и внезапной смерти (синдром внезапной смерти детей грудного и более старшего возраста). Клиническая картина во многом зависит от этиологии и возраста ребенка [30, 38].
Симптомы заболевания разнообразны и часто неспецифичны, могут имитировать другие заболевания, особенно в дебюте, в связи с чем необходимо проявлять клиническую настороженность в отношении миокардита у пациентов детского возраста.
В дебюте миокардита распространенными проявлениями у детей являются симптомы поражения желудочно-кишечного тракта, такие как боль в животе, тошнота, плохой аппетит и рвота [35, 38 49].
Другими частыми симптомами являются снижение толерантности к физической нагрузке (ФН), симптомы поражения верхних дыхательных путей, боли за грудиной, одышка, аритмия и синкопе [38, 50 - 55].
Картину дебюта миокардита дополняют лихорадка, слабость, быстрая утомляемость, выраженность которых не меняется, несмотря на уменьшение объема нагрузок, артралгии.
Начало болезни с быстрого прогрессирования СН всегда обусловлено тяжелым диффузным миокардитом и указывает на высокий риск летального исхода.
В ряде случаев, на начальных стадиях, клиническая манифестация полностью отсутствует, диагноз устанавливается ретроспективно. Ухудшение состояния, вызванное дебютом миокардита, у пациентов, исходно имеющих сердечно-сосудистые заболевания и проявления ХСН, может ошибочно трактоваться как декомпенсация основного заболевания.
При физикальном осмотре могут присутствовать признаки снижения сердечного выброса, такие как тахикардия, слабый пульс, холодные конечности, а также бледность или мраморность кожных покровов. При аускультации тоны сердца часто приглушены, особенно при перикардите, выслушивается тахикардия, не коррелирующая с уровнем гипертермии, ритм галопа, характерен систолический шум мышечного характера, несколько позже присоединяется систолический шум относительной недостаточности атриовентрикулярных клапанов. В легких могут выслушиваться застойные влажные хрипы. Гепатомегалия и умеренное увеличение селезенки наиболее характерны для детей младшего возраста, отеки - для детей более старшего возраста, либо для тяжелой СН. Могут быть нарушения ритма и проводимости.
Особенности клинической картины миокардита у детей разного возраста
Для новорожденных характерны акроцианоз или общий цианоз, одышка, быстрая утомляемость при кормлении, снижение аппетита вплоть до полного отказа от еды, слабость, стонущее дыхание. Также в патологический процесс может вовлекаться центральная нервная система, признаками поражения которой будут являться судороги, сонливость и др. Могут присутствовать гипотермия или гипертермия, олигурия, повышенные уровни ферментов печени, а также повышенный уровень мочевины и креатинина в крови, вызванные прямым вирусным поражением, низким сердечным выбросом или и тем, и другим. Ранняя диагностика в этой группе имеет решающее значение, потому что неонатальный миокардит ассоциируется с более низкой вероятностью восстановления функции сердца и высокой смертностью. Неонатальный миокардит может быть одним из проявлений системной воспалительной реакции или неонатального сепсиса [56, 57].
Для детей первого года жизни симптомы включают отсутствие прибавок в весе, тахипноэ, тахикардию, выраженное потоотделение во время кормления. Также может развиться поражение ЦНС. В тяжелых случаях низкий сердечный выброс приводит к развитию ацидоза и смерти.
У подростков появляются длительные разлитые боли в левой половине грудной клетки, тупого, ноющего, колющего характера, не связанные с физической нагрузкой. Чаще всего боли в сердце обусловлены сопутствующим перикардитом, реже - ишемией миокарда, обусловленной прямым поражением кардиомиоцитов инфекционным или токсическим агентом, а также коронариитом. Кроме того, дети предъявляют жалобы на ощущения "перебоев" в работе сердца, учащенного сердцебиения, снижение толерантности к физическим нагрузкам, одышку, кашель, эпизоды артериальной гипотензии, синкопе. Возможно появление миалгий как клинических проявлений, сопровождающих синдром лихорадки, либо миозитов, вызванных миотропными вирусами Коксаки A, либо вследствие накопления лактата в мышечной ткани на фоне сердечной недостаточности.
При тяжелом течении и развитии сердечной недостаточности у детей всех возрастов появляются жалобы на снижение аппетита, тошноту, боли в животе, рвоту, наличие отеков [4, 58].
Течение и исход острого миокардита во многом определяется этиологией заболевания, выраженностью недостаточности кровообращения и скоростью прогрессирования симптомов.
Дебют болезни с бивентрикулярной СН со значительным снижением ФВ ЛЖ и повышением уровня кардиоспецифических ферментов всегда прогностически неблагоприятен и свидетельствует о высоком риске летального исхода.
Большинство пациентов с миокардитом имеют дилатацию и снижение сократительной способности в острой фазе, которая у части больных не восстанавливается полностью, приводя к развитию хронической сердечной недостаточности, ДКМП и, в некоторых случаях, к летальному исходу. У 50 - 60% пациентов с ДКМП выявляется хронический миокардит [2, 59].
Таким образом, миокардит является одной из ведущих причин развития ДКМП (27% случаев) и трансплантации сердца (80% случаев) у детей без врожденных заболеваний сердца [33, 50].
Характер течения
Тяжелое течение сопровождается быстрым развитием признаков острой левожелудочковой СН с одышкой, цианозом слизистых оболочек, тахикардией, сердцебиением, застойными влажными хрипами в легких, а затем правожелудочковой сердечной недостаточности с увеличением печени, в меньшей степени - селезенки (особенно у детей до 1 года), отеками конечностей, полисерозитом, а также асцитом в терминальной стадии. Другими проявлениями могут быть боли в животе, диспепсические явления, синкопальные состояния, судороги как симптомы застойной СН, синдрома малого сердечного выброса и циркуляторной гипоксии. Сочетание миокардита с перикардитом сопровождается резкой глухостью сердечных тонов вплоть до афонии, развитием преимущественно правожелудочковой СН с гепатомегалией и отечным синдромом.
При среднетяжелых формах критериями миокардита являются умеренная кардиомегалия, электро- и эхокардиографические изменения и умеренно повышенные маркеры некроза кардиомиоцитов (см. ниже).
При легком течении единственными проявлениями текущего миокардита могут быть нарушения ритма и проводимости, электрокардиографические изменения реполяризации.
Варианты клинического течения описываются на основании доминирующих клинических симптомов и включают в себя респираторный, кардиальный, гипоперфузионный и абдоминальный [60].
Для респираторного варианта, наблюдающегося более чем у половины больных с впервые возникшей миокардиальной дисфункцией, характерны диспноэ, стонущее дыхание, одышка, чаще экспираторная. Могут выслушиваться сухие или влажные хрипы в легких, часто имитирующие трахеит, пневмонию или бронхиальную астму.
Кардиальный вариант сопровождается болями в области сердца в качестве ведущего симптома в сочетании с электрокардиографическими изменениями (см. ниже).
Тяжелый гипоперфузионный вариант у 25% больных манифестирует с клинических симптомов синдрома малого сердечного выброса с пре- или синкопальным состоянием, обусловленным гипоперфузией на фоне выраженной миокардиальной дисфункции или с развитием жизнеугрожающей аритмии, могут наблюдаться коматозное состояние и судороги.
Абдоминальный вариант с болями в животе, тошнотой, реже со рвотой и жидким стулом развивается у 10 - 13% больных с миокардитами, чаще у детей младше 10 лет. Возникновение данных симптомов обусловлено гипоперфузией желудочно-кишечного тракта в результате миокардиальной дисфункции. Артериальная гипотония запускает механизм симпатической активации с последующим развитием локальной вазоконстрикции и ишемии различных участков желудочно-кишечного тракта. В случае развития миокардита на фоне доказанной кишечной инфекции, механизм повреждения миокарда обусловлен прямым кардиотоксическим воздействием возбудителя и последующей иммунопатологической реакцией.
2. Диагностика заболевания или состояния (группы заболеваний или состояний) медицинские показания и противопоказания к применению методов диагностики
Учитывая неспецифичность симптомов в дебюте заболевания, необходимо проявлять клиническую настороженность в отношении миокардита у пациентов с развитием клиники сердечной недостаточности, впервые выявленными нарушениями ритма и проводимости сердца, в особенности после воздействия неблагоприятных факторов. [53, 61, 62].
В соответствии с Canadian Cardiovascular Society Consensus Conference guidelines on heart failure (Рекомендации Консенсуса Конференции Канадского Общества по сердечным заболеваниям, 2013 г.), наличие миокардита рекомендуется предполагать в ситуациях:
- у всех детей, независимо от возраста, у которых впервые появились симптомы сердечной недостаточности;
- при проведении дифференциальной диагностики у детей с наличием клиники вирусных инфекций, сопровождающейся респираторными или абдоминальными симптомами, в совокупности с развитием тахикардии, гипотонии или нарушений сердечного ритма, даже при отсутствии кардиомегалии на рентгенограмме грудной клетки [63].
Необходимо выделить среди них тех, кто имеет факторы риска неблагоприятного течения миокардита в анамнезе (в том числе семейном), "угрожающие" симптомы при физикальном осмотре и по результатам ЭКГ и/или рентгенографии.
Всесторонняя клиническая оценка имеет важное значение, поскольку она позволяет заподозрить миокардит клинически на этапе, когда должны быть приняты важные решения о расширении комплекса диагностических обследований и старте терапии, либо в тех случаях, когда проведение МРТ сердца или биопсии миокарда невозможно. Хотя на сегодняшний день не существует четких критериев, которые позволяют только на основании клинических признаков подтвердить диагноз миокардит [62].
При дифференциальной диагностике с дилатационной кардиомиопатией (ДКМП) решающее значение имеет постепенное развитие симптомов застойной сердечной недостаточности, отсутствие или минимальные лабораторные признаки воспалительного процесса в миокарде. Дилатационная кардиомиопатия - прогрессирующее заболевание сердечной мышцы, которое характеризуется увеличением камер сердца и систолической дисфункцией миокарда. Несмотря на существующие критерии диагностики миокардита и кардиомиопатий, дифференциальная диагностика этих состояний, особенно у детей первого года жизни, очень сложна, так как между ними существует не только клиническое и патогенетическое, но и морфологическое сходство, общность электрокардиографических и эхокардиографических характеристик. Диагностическую ценность в данном случае может иметь биопсия миокарда.
Дифференциальный диагноз миокардита у детей раннего возраста необходимо проводить с ВПС, которые приводят к дилатации и снижению сократительной способности левого желудочка, в первую очередь с аномальным отхождением левой коронарной артерии от легочной артерии, коарктацией аорты. При аномальном отхождении левой коронарной артерии от легочной артерии пациенты после рождения асимптомны. Это связано с тем, что высокое давление в легочной артерии обеспечивает достаточный антеградный поток крови в левой коронарной артерии. В течение нескольких недель давление в легочной артерии снижается и при этом поток из правой коронарной артерии через коллатерали ретроградно заполняет левую коронарную артерию - данное явление приводит к ишемии миокарда левого желудочка. Клинические проявления при данной патологии начинаются в первые месяцы жизни.
Кардиомиопатии в структуре наследственных болезней обмена (лизосомальные болезни накопления, митохондриальная патология, в том числе карнитиновая недостаточность, врожденные миопатии и прогрессирующие мышечные дистрофии и т.д.) могут иметь схожую клиническую картину с воспалительным процессом в миокарде.
Аритмогенная дисфункция миокарда с признаками недостаточности миокарда и дилатацией камер сердца развивается у больных с хроническими тахикардиями (эктопической предсердной тахикардией, желудочковой тахикардией, хронической формой трепетания предсердий). Степень поражения варьирует от умеренной дилатации ЛЖ до значительного расширения камер сердца со снижением сократимости миокарда, выраженными признаками хронической сердечной недостаточности. Отсутствие явной связи с перенесенной инфекцией, нормальные значения или умеренное повышение уровня биохимических маркеров повреждения миокарда, постепенное, но довольно быстрое (2 - 4 недели) повышение фракции выброса и нормализация полостей сердца после устранения аритмии, подтверждают предположение об аритмогенном генезе кардиомегалии и дисфункции миокарда [33, 43, 57, 62].
2.1 Жалобы и анамнез
- Рекомендуется провести оценку жалоб пациента и сбор анамнеза, который должен включать в себя следующие положения
- сроки возникновения симптомов и их изменение в динамике
- предшествующие эпизоды вирусных, бактериальных инфекций, гипертермии или аллергических реакций, контакта с токсическими веществами (в том числе лекарственными препаратами)
- особенности течения беременности и родов (особенно важно при подозрении на врожденный миокардит)
- наличие у родственников первой линии родства любой кардиомиопатии, ранее перенесенного миокардита, системных заболеваний соединительной ткани, системных аллергических заболеваний, случаев внезапной смерти в семье
- наличие у ребенка ранее предполагаемого, но неподтвержденного впоследствии диагноза "миокардит"
- наличие сопутствующий заболеваний, данных о диспансерном учете у врача-детского-кардиолога или иных специалистов
- данные о профилактических прививках и туберкулиновых пробах
- эпидемиологический анамнез
- данные о медикаментозной терапии, которую получает пациент на момент осмотра
- оценку динамики физического и психомоторного развития [1, 4, 15, 28, 38, 63 - 65].
УУР C, УДД 5
Комментарии: характерно острое развитие симптомов СН на 5 - 7 день вирусной инфекции (чаще инфекции верхних дыхательных путей с фебрильной лихорадкой, диарейным синдромом), а у детей более старшего возраста - на 1 - 2 неделе реконвалесценции. При врожденных миокардитах клиника сердечной недостаточности проявляется в первые 72 часа после рождения.
При врожденном миокардите и раннем дебюте сердечной недостаточности можно выявить отставание в физическом развитии. Для детей раннего возраста характерны низкие показатели массы тела, плохая прибавка массы в течение первых месяцев жизни.
В настоящее время не существует проспективных клинических исследований, доказавших важность и обязательность определенного перечня вопросов при первичном осмотре.
Характерными жалобами для детей раннего возраста являются: одышка, трудности при кормлении (срыгивания, отказ от еды), диспепсические явления (рвоты, диарея), стонущее, кряхтящее дыхание, повышенное потоотделение, бледность кожных покровов, слабость и адинамия; реже - цианоз, сердцебиение, обморок [63].
У более старших детей частыми характерными симптомами миокардита являются тахикардия и боль в грудной клетке. Болевой синдром может быть связан с наличием воспалительного процесса в субэпикардиальных слоях миокарда, синдромом малого сердечного выброса, присоединением перикардита или развития спазма коронарных артерий, приводящего в ряде случаев к инфаркту миокарда. Кроме того, пациенты предъявляют жалобы на слабость, усталость, снижение толерантности к физической нагрузке, одышку, кашель при перемене положения тела, а также необъяснимый обморок, ощущения "перебоев" в сердце, наличие острых гастроинтестинальных проявлений (тошнота, рвота, диарея), снижение аппетита [4, 38, 64, 65].
Иногда единственными жалобами при миокардите могут быть ощущения "перебоев" в работе сердце или учащенного сердцебиения и/или обморок как проявления нарушений ритма сердца [15, 62].
2.2 Физикальное обследование
- Рекомендуется проведение физикального обследования пациента для оценки тяжести текущего миокардита и степени сердечной недостаточности [1, 4, 15, 58, 66 - 68].
УУР C, УДД 5
Комментарии: при осмотре ребенка необходимо обращать внимание на:
- состояние сознания;
- положение ортопноэ (полусидячее);
- бледность, мраморность кожных покровов, наличие "серого колорита", цианоза
- напряжение и раздувание крыльев носа;
- втяжение податливых мест грудной клетки;
- тахипноэ (реже диспноэ), наличие стонущего, хрипящего или кряхтящего дыхания (больше выражено у детей раннего возраста), у младенцев тахипноэ и потоотделение во время кормления;
- тахикардию (реже брадикардию);
- влажные разнокалиберные хрипы в легких (сначала в нижнебоковых отделах легких и/или преимущественно слева из-за сдавливания левого легкого увеличенным сердцем, затем над всей поверхностью легких);
- субфебрильную или фебрильную лихорадку, как проявление инфекционного процесса, в рамках которого развивается миокардит;
- сердечный горб (при остром миокардите может не выявляться);
- увеличение размеров и болезненность при пальпации печени;
- симптом Плеша (набухание шейных вен при надавливании на область печени);
- умеренное увеличение селезенки (характерно у детей раннего возраста);
- диспептические явления (понос, запор, тошнота, рвота), связанные с застоем крови в мезентериальных сосудах и застойным гастритом;
- периферические отеки на стопах, затем на лодыжках, голенях, у лежачих больных - в области крестца, обычно увеличивающиеся к вечеру (чаще у детей старшего возраста), у детей первых лет жизни - отеки в области лица и мошонки, которые из-за высокой гидрофильности тканей не всегда могут быть видны);
- гидроторакс, асцит, обычно появляющиеся позднее, чем периферические отеки.
При исследовании пульса на периферических артериях помимо изменения частотных и ритмических характеристик, возможно выявление слабого, а при тяжелом состоянии, нитевидного пульса.
При перкуссии может отмечаться расширение границ относительной и абсолютной сердечной тупости. Верхушечный толчок не изменен или умеренно ослаблен, смещен влево в зависимости от степени увеличения размеров сердца.
При аускультации сердца:
- типична постоянная тахикардия, выраженность которой не коррелирует со степенью повышения температуры тела, реже - брадикардия.
- возможно наличие аритмичных тонов сердца за счет развития нарушений ритма и проводимости сердца, которая может быть единственным проявлением заболевания [4, 58, 66, 67].
- приглушенность сердечных тонов, иногда ослабление I тона (из-за снижения наполнения левого желудочка и уменьшения ударного объема);
- возможно появление дополнительных тонов - протодиастолического III и пресистолического IV (как симптома повышения давления в предсердиях или вальвулита митрального клапана), акцента II тона (характерен для легочной гипертензии, чаще при подостром и хроническом процессе). Выявление ритма "галопа" на верхушке является признаком тяжелой недостаточности кровообращения.
- систолический шум относительной недостаточности атриовентрикулярных клапанов, преимущественно митрального, с максимумом звучания на верхушке сердца, с иррадиацией в аксиллярную область [68, 69, 70].
При измерении артериального давления (АД) на периферических артериях может иметь место артериальная гипотензия, наличие которой является признаком тяжелой недостаточности кровообращения и одним из факторов, определяющих показания к госпитализации ребенка в отделение интенсивной терапии.
2.3 Лабораторные диагностические исследования
Обязательным является интерпретация результатов лабораторных исследований в совокупности с клинической картиной и данными инструментальных методов обследования, так как отсутствуют лабораторные маркеры, специфичные именно для миокардита.
Рутинные лабораторные исследования общий (клинический) анализ крови, анализ крови биохимический общетерапевтический, общий (клинический) анализ мочи, исследование кислотно-основного состояния и газов крови) в диагностике миокардитов недостаточно информативны, тем не менее целесообразно их выполнение пациентам для оценки исходного клинического статуса, проведения дифференциального диагноза, анализа их изменений при динамическом наблюдении и исключения иных причин ухудшения состояния у пациента, а также определения предикторов неблагоприятного исхода [63, 71].
Неспецифические маркеры воспаления (скорость оседания эритроцитов, C-реактивный белок) часто повышаются при миокардите, однако, их нормальных уровень не исключает наличие данного заболевания.
- Рекомендуется проведение общего (клинического) анализа крови развернутого, исследование скорости оседания эритроцитов (СОЭ), исследование уровня C-реактивного белка в сыворотке крови у всех пациентов с подозрением на миокардит в рамках первичного обследования и при динамическом наблюдении [3, 28].
УУР C, УДД 5
Комментарии: повышение уровня лейкоцитов, ускорение СОЭ и повышение уровня СРБ не является специфичным, но отражает системную воспалительную реакцию, позволяя врачу только заподозрить миокардит, но не подтвердить диагноз. Сохранение этих показателей на высоких значениях в течение длительного времени позволяет предположить хронизацию общего воспалительного процесса. Нормальный уровень СОЭ и СРБ не исключает диагноз миокардит [4, 6].
Для диагностики эозинофильного миокардита рекомендуется определение числа эозинофилов [72].
Определение маркеров некроза при сердечно-сосудистых заболеваниях широко используется в реальной клинической практике и может помочь в выявлении продолжающегося повреждения миокарда, дать представление о прогнозе. Однако имеющиеся биомаркеры не обладают специфичностью, и ни один из них не позволяет отличить миокардит от других причин острой дисфункции миокарда, травмы или ишемии. При подозрении на острый миокардит целесообразнее определять концентрацию в сыворотке тропонина T и I, так как эти маркеры более чувствительны к повреждению кардиомиоцитов.
- Рекомендуется проведение исследование уровня тропонинов I, T в крови у всех пациентов с миокардитом в рамках первичного обследования и в процессе динамического наблюдения [3, 4, 62, 73]. При технической невозможности исследования уровня тропонинов I, T в крови в условиях медицинского учреждения должна быть обсуждена маршрутизация анализа в другое медицинское учреждение для выполнения данного исследования.
УУР C, УДД 4
Комментарии: при отсутствии клинических и/или ЭКГ-признаков ишемии, возрастание уровней тропонина I или тропонина T в крови указывает на повреждение (некроз) некоронарогенного генеза, что имеет важное значение для педиатрической и неонатальной практики и является более чувствительным признаком для диагностики миокардита, чем исследование уровня/активности изоферментов креатинкиназы в крови (КФК) и исследование уровня МВ-фракции креатинкиназы в крови (КФК-МВ) [3].
Повышение концентрации тропонина I или тропонина T наблюдается при миокардитах, сепсисе и системном воспалительном синдроме, при различных шоковых состояниях, при лекарственной интоксикации противоопухолевыми препаратами с цитостатическим механизмом действия, при травматическом повреждении сердца, включая кардиохирургические вмешательства, после дефибрилляции, при отторжении сердечного трансплантата, при кардиомиопатии, при хронических сердечной и почечной недостаточности, при гипертензии с выраженной гипертрофией левого желудочка, при острой легочной эмболии с дисфункцией правого желудочка. Таким образом, определение уровня тропонинов I, T при этих состояниях характеризует наличие провоспалительного цитокининдуцированного повреждения и энергетический дефицит.
Нормальный уровень тропонина T и I не исключает миокардит. Высокие уровни тропонина T имеют негативное прогностическое значение [62].
- Рекомендуется проведение исследования уровня МВ-фракции креатинкиназы в крови (КФК-МВ), определение активности аспартатаминотрансферазы (АСТ) в крови у всех пациентов с миокардитом в рамках первичного обследования в качестве дополнительных при диагностике миокардита [3, 15, 28, 49, 62, 68].
УУР C, УДД 5
Комментарии: в ряде публикаций отмечено повышение уровня АСТ при нормальном значении аланин-трансаминазы (АЛТ) у пациентов с миокардитом [4, 62, 74].
- Рекомендуется всем пациентам с подозрением на миокардит исследование уровня натрийуретических пептидов (мозгового натрийуретического пептида (BNP) и/или исследование уровня N-терминального фрагмента натрийуретического пропептида мозгового (NT-proBNP) в крови [3, 4, 15, 62, 63].
УУР C, УДД 4
Комментарии: Повышение уровня натрийуретических пептидов (мозгового натрийуретического пептида (BNP) и/или N-терминального фрагмента натрийуретического пропептида мозгового (NT-proBNP) является наиболее информативным маркером сердечной недостаточности. Повышение этих параметров отражает развитие сердечной недостаточности при миокардите, но, вместе с тем, не является специфичным и их нормальные значения не исключают наличие миокардита. Важным является определение этих показателей в динамике, для оценки эффективности терапии.
В педиатрической популяции роль аутокардиальных антител к кардиомиоцитам ![]() адренергическим рецепторам G3, сердечному миозину) в генезе и прогнозе миокардита и ДКМП изучена недостаточно. В небольшом исследовании повышенный уровень антител к сердечному миозину был выявлен как в момент дебюта заболевания или выздоровлении, так и при хронизации процесса. Повышенный титр аутоантител класса IgG, свидетельствует об аутоиммунном характере процесса, однако отсутствие повышенного титра не исключает миокардита, так как наличие воспалительного процесса в миокарде может развиваться без формирования аутоантител. Динамика титра аутоантител позволяет оценить эффективность проводимой иммуносупрессивной или иммуномодулирующей терапии [62].
адренергическим рецепторам G3, сердечному миозину) в генезе и прогнозе миокардита и ДКМП изучена недостаточно. В небольшом исследовании повышенный уровень антител к сердечному миозину был выявлен как в момент дебюта заболевания или выздоровлении, так и при хронизации процесса. Повышенный титр аутоантител класса IgG, свидетельствует об аутоиммунном характере процесса, однако отсутствие повышенного титра не исключает миокардита, так как наличие воспалительного процесса в миокарде может развиваться без формирования аутоантител. Динамика титра аутоантител позволяет оценить эффективность проводимой иммуносупрессивной или иммуномодулирующей терапии [62].
- Не рекомендуется в качестве рутинных проведение вирусологических исследований (с использованием серологических методов, методов молекулярной гибридизации) с целью верификации вирусных миокардитов или дифференциальной диагностики миокардитов [3, 4, 28].
УУР C, УДД 5
- Рекомендуется вирусологические исследования крови методами ПЦР (Определение ДНК цитомегаловируса (Cytomegalovirus) в крови методом ПЦР, качественное определение; Определение ДНК вируса Эпштейна-Барр (Epstein - Barr virus) методом ПЦР в крови, качественное исследование; определение ДНК вируса герпеса 6 типа (HHV6) методом ПЦР в крови, качественное исследование; определение ДНК вируса простого герпеса 1 и 2 типов (Herpes simplex virus types 1, 2) методом ПЦР в крови, качественное исследование; определение ДНК парвовируса B19 (Parvovirus B19) методом ПЦР в периферической крови, количественное исследование; определение ДНК вируса ветряной оспы и опоясывающего лишая (Varicella-Zoster virus) в крови методом ПЦР, качественное исследование; определение ДНК аденовирусов (Adenovirus); определение ДНК вируса иммунодефицита человека методом ПЦР, качественное исследование; определение РНК вируса гепатита C (Hepatitis C virus) в крови методом ПЦР, количественное исследование; определение ДНК вируса гепатита B (Hepatitis B virus) в крови методом ПЦР, количественное исследование в плазме крови (качественное и количественное исследование) при подозрении на наличие у пациента генерализованной вирусной инфекции с вовлечением миокарда в патологический процесс [3, 4, 57, 62, 63, 74].
УУР C, УДД 5
- Рекомендуется проведение молекулярно-биологического исследования слюны на цитомегаловирус (Cytomegalovirus); молекулярно-биологического исследования слюны на вирус герпеса человека 6 типа (HHV6); молекулярно-биологическое исследование слюны на парвовирус B19 (Parvovirus B19). Определение ДНК парвовируса B19 (Parvovirus B19) методом ПЦР в слюне, качественное исследование; определение ДНК парвовируса B19 (Parvovirus B19) методом ПЦР в слюне, количественное исследование; определение ДНК цитомегаловируса (Cytomegalovirus) методом ПЦР в слюне, качественное исследование; определение ДНК цитомегаловируса (Cytomegalovirus) методом ПЦР в слюне, количественное исследование; определение ДНК вирус герпеса человека 6 типа (HHV 6) в слюне, количественное исследование при подозрении на наличие у пациента генерализованной вирусной инфекции с вовлечением миокарда в патологический процесс [3, 4, 57, 62, 63, 74].
УУР C, УДД 5
- Рекомендуется проведение молекулярно-биологического исследования мазков со слизистой оболочки носоглотки на вирус гриппа (Influenza virus), определение РНК вируса гриппа A (Influenza virus A) в мазках со слизистой носоглотки методом ПЦР, определение РНК вируса гриппа B (Influenza virus B) в мазках со слизистой носоглотки методом ПЦР, определение РНК вируса гриппа C (Influenza virus C) в мазках со слизистой носоглотки методом ПЦР; определение РНК респираторно-синцитиального вируса (Human Respiratory Syncytial virus) в мазках со слизистой оболочки носоглотки методом ПЦР; определение ДНК аденовируса (Human Adenovirus) в мазках со слизистой оболочки носоглотки методом ПЦР; определение ДНК цитомегаловируса (Cytomegalovirus) в мазках со слизистой оболочки ротоглотки методом ПЦР, количественное исследование; определение ДНК цитомегаловируса (Cytomegalovirus) в мазках со слизистой оболочки ротоглотки методом ПЦР, качественное исследование; определение ДНК парвовируса B19 (Parvovirus B19) в мазках со слизистой оболочки ротоглотки методом ПЦР, качественное исследование; определение ДНК парвовируса B19 (Parvovirus B19) в мазках со слизистой оболочки ротоглотки методом ПЦР, количественное исследование; определение ДНК вируса Эпштейна-Барр (Epstein - Barr virus) в мазках со слизистой оболочки ротоглотки методом ПЦР, качественное исследование; определение ДНК вируса Эпштейна-Барр (Epstein - Barr virus) в мазках со слизистой оболочки ротоглотки методом ПЦР, количественное исследование; определение ДНК вируса герпеса 6 типа (HHV6) в мазках со слизистой оболочки ротоглотки методом ПЦР, качественное исследование; определение ДНК вируса герпеса 6 типа (HHV6) в мазках со слизистой оболочки ротоглотки методом ПЦР, количественное исследование при подозрении на наличие у пациента генерализованной вирусной инфекции с вовлечением миокарда в патологический процесс [3, 4, 28, 57, 62, 63, 74].
УУР C, УДД 5
- Рекомендуется проведение молекулярно-биологического исследования мочи на цитомегаловирус (Cytomegalovirus): определение ДНК цитомегаловируса (Cytomegalovirus) в моче методом ПЦР, качественное исследование; определение ДНК цитомегаловируса (Cytomegalovirus) в моче методом ПЦР, количественное исследование при подозрении на наличие у пациента генерализованной вирусной инфекции с вовлечением миокарда в патологический процесс [3, 4, 57, 62, 63, 74].
УУР C, УДД 5
Комментарии: наиболее информативным является выявление вируса в биоптате миокарда методом ПЦР, однако, использование данного метода в реальной клинической практике значимо ограничено в связи с инвазивностью исследования [63].
Исследование биологических жидкостей (кровь, слюна, моча и т.д.) методом ПЦР может иметь диагностическое значение при подозрении на наличие у пациента генерализованной вирусной инфекции с вовлечением миокарда в патологический процесс, однако, положительный результат не является подтверждением наличия выявленного вируса в кардиомиоцитах.
Серологические маркеры вирусной инфекции, верифицированные в периферической крови пациента, не являются основанием для диагностического суждения о наличии вирусного миокардита.
Диагностическая значимость серологических методов лимитирована из-за высокой распространенности в популяции вирусов, вызывающих миокардит.
В общей популяции, в том числе и у здоровых людей, циркуляция IgG-антител к кардиотропным вирусам встречается часто и не сопровождается манифестом клиники вирусного миокардита [3, 4, 62, 74].
Проведение серологического тестирования может быть полезным в отдельных случаях, например, при подозрении на гепатит C, ВИЧ у пациентов высокого риска, болезнь Лайма, риккетсиоз в эндемичных районах [3, 28].
- Рекомендуется проведение анализа крови биохимического общетерапевтического с определением уровня натрия, калия, общего магния, общего кальция, хлоридов, глюкозы, мочевины и креатинина, активности аспартатаминотрансферазы и аланинаминотрансферазы всем пациентам с подозрением на миокардит в рамках первичного обследования и в процессе динамического наблюдения [63, 71, 75, 76].
УУР C, УДД 5
- Рекомендуется исследование кислотно-основного состояния и газов крови всем пациентам с подозрением на миокардит в рамках первичного обследования и в процессе динамического наблюдения [63, 75].
УУР C, УДД 5
- Рекомендуется проведение общего (клинического) анализа мочи всем пациентам с подозрением на миокардит в рамках первичного обследования и в процессе динамического наблюдения [63, 75, 76].
УУР C, УДД 5
2.4 Инструментальные диагностические исследования
- Рекомендуется проведение прицельной рентгенографии органов грудной клетки всем пациентам с подозрением на миокардит [15, 62, 63].
УУР C, УДД 4
Комментарии: определяется увеличение размеров сердца. Характерно изменение конфигурации сердца (патологическое ремоделирование) со сглаженностью контуров и развитием сферичности ("шарообразности"), может определяться картина венозного застоя в легких, инфильтрации легочной ткани, умеренный плевральный выпот, признаки развития легочной гипертензии [3, 15, 62, 77 - 79].
Таблица 4. Норма кардиоторакального индекса у детей
Возраст
Средний КТИ
Станд. отклонение
Диапазон
0 - 3 недели
0,55
0,05
0,65 - 0,45
4 - 7 недель
0,58
0,06
0,70 - 0,46
1 год
0,53
0,04
0,61 - 0,45
1 - 2 года
0,49
0,60 - 0,39
2 - 6 лет
0,45
0,52 - 0,40
> 7 лет
< 0,50
0,50 - 0,40
- Рекомендуется регистрация электрокардиограммы в 12 отведениях и мониторирование электрокардиографических данных всем пациентам с подозрением на миокардит [2, 62, 63, 77].
УУР C, УДД 4
Комментарии: изменения на ЭКГ отмечаются практически у всех детей с миокардитом и имеют значительную вариабельность. Специфических ЭКГ-маркеров для диагностики миокардита нет [4, 38, 80].
Наиболее частыми из них являются синусовая тахикардия, изоэлектричный или отрицательный зубец T, изменения сегмента ST (как элевация, так и депрессия), удлинение интервала PR, снижение вольтажа QRS, появление патологических зубцов Q, расширение QRS, удлинение интервала QT [4, 38, 53, 77, 80].
Псевдоинфарктные изменения и выраженные признаки субэндокардиальной ишемии могут быть признаками коронариита.
У 50 - 60% детей регистрируются нарушения ритма в виде экстрасистолии, реже - различные виды тахикардии, синусовая брадикардия и нарушения АВ проведения, вплоть до развития полной АВ блокады, блокады ножек пучка Гиса (чаще левой ножки пучка Гиса).
Жизнеугрожающие нарушения ритма сердца (желудочковая тахикардия, трепетание предсердий, внезапно развившаяся полная АВ блокада, СССУ) регистрируются в 9,5% случаев.
Появление желудочковых аритмий, при выраженной дисфункции миокарда, атриовентрикулярных и внутрижелудочковых блокад прогностически неблагоприятно. Иногда аритмия может быть единственным проявлением миокардита. Миокардит следует всегда исключать у пациента с впервые возникшей полной АВ блокадой [2, 4, 62, 77, 79].
- Рекомендуется проведение эхокардиографии (ЭхоКГ) всем пациентам с подозрением на миокардит [61 - 63, 68].
УУР C, УДД 5
Комментарии: Эхокардиография - обязательный метод диагностики, который следует выполнять всем пациентам с подозрением на миокардит [61]. Эхокардиография позволяет оценить исходное состояние и последующую динамику систолической (глобальной и локальной) и диастолической функции желудочков, размеры камер сердца, толщину стенок, наличие регургитации на митральном и трикуспидальном клапанах, давление в легочной артерии, наличие перикардиального или плеврального выпота, внутриполостных тромбов [77].
На первом этапе диагностического поиска необходимо исключить ВПС, в том числе аномалию коронарных артерий, клапанные пороки сердца, гипертрофическую и рестриктивную кардиомиопатии [3, 5, 62, 77, 79].
Дисфункция левого желудочка может возникать без сопутствующей дилатации его полости.
У пациентов с молниеносной формой миокардита чаще имеет место утолщение стенок вследствие интерстициального отека миокарда, выраженная систолическая дисфункция и нормальные размеры левого желудочка по сравнению с пациентами с острым миокардитом.
Для острого миокардита характерна дилатация камер сердца при нормальной либо увеличенной (вследствие острого воспалительного отека) толщине стенок.
Такие параметры как размеры камер сердца, а также диаметр магистральных сосудов, толщина миокарда зависят от антропометрических данных пациента, а именно площади поверхности тела, и оцениваются в соответствии с z-score (норма +/- 2 z-score).
У всех пациентов необходимо проводить оценку правого желудочка: определение размеров и сократительной способности. Функциональные данные, полученные при применении тканевой допплерографии, TAPSE должны оцениваться в соответствии с возрастом пациента (норма +/- 2 z-score) [81, 82, 83].
У ряда пациентов с воспалительным процессом в миокарде значительное снижение функции правого желудочка было мощным предиктором летального исхода или необходимости трансплантации сердца [6]. Применение тканевой доплерографии, а также определение глобальной деформации ЛЖ (Global Longitudinal Strain - GLS LV) могут помочь обнаружить более тонкие изменения систолической и диастолической функции миокарда, которые коррелируют с данными, полученными при МРТ диагностике, в связи с чем рекомендовано использование данных методик при наличии технической возможности медицинской организации [83, 84, 85].
- Рекомендуется проведение магнитно-резонансной томографии сердца с контрастированием с использованием парамагнитных контрастных средств (АТХ V08CA) детям с подозрением на миокардит при стабильном состоянии с целью диагностики заболевания, при наличии в медицинской организации необходимого оборудования. При технической невозможности выполнения МРТ сердца с контрастированием с использованием ПМКС в условиях медицинского учреждения должна быть обсуждена маршрутизация пациента в другое медицинское учреждение для выполнения данного исследования [3, 4, 62, 63, 77, 86].
УУР C, УДД 4
Комментарии: магнитно-резонансная томография сердца с использованием ПМКС является малоинвазивным информативным методом визуализации очагов воспаления в миокарде, повреждения и некроза кардиомиоцитов и оценки морфометрических параметров сердца, имеющим высокую чувствительность для диагностики миокардита у детей (82%) [3, 4, 62, 77, 86].
В отличии от биопсии миокарда МРТ позволяет оценить весь миокард, а не только локальные участки, из которых проводился забор биоматериала [77].
В 2009 г. международным согласительным консенсусом (The International Consensus Group on CMR Diagnosis of Myocarditis) были утверждены и опубликованы критерии группы экспертов (Lake Louise Criteria - LLC), в которых были обозначены 3 главных МРТ-признака миокардиального воспаления:
- отек ткани миокарда, о котором свидетельствует удлинение времени T2 релаксации миокарда и/или повышение интенсивности сигнала на T2-взвешенных изображениях (глобальное увеличение интенсивности сигнала должно быть количественно определено отношением интенсивности сигнала миокарда к скелетным мышцам >= 2,0). При миокардите он может быть локальным или диффузным;
- гиперемия и отек миокарда, характеристикой которой является интенсивность сигнала раннего контрастного усиления после введения ПМКС, а именно, гадолиний-содержащего контрастного вещества (АТХ V08CA Парамагнитные контрастные средства) на T1-взвешенных изображениях (общий коэффициент увеличения интенсивности сигнала миокарда по сравнению со скелетными мышцами >= 4,0 или абсолютное увеличение сигнала от миокарда >= 45%), соответствует миокардиту в острый период воспаления;
- некроз/фиброз миокарда, на основании T1-взвешенных изображений с поздним накоплением ГСКВ (late gadolinium enchantment - LGE). Изображения должны быть получены как минимум через 5 минут после инъекции ГСКВ, минимум один фокус повреждения. Локализация изменений позволяет провести дифференциальный диагноз между ишемическим и неишемическим повреждением миокарда;
- наличие дисфункции ЛЖ или перикардиального выпота является дополнительным подтверждающим доказательством миокардита [87].
Если 2 из 3 этих критериев положительны, то миокардит может быть диагностирован с чувствительностью 74% и специфичностью 86%, если выполняется только визуализация с поздним накоплением ГСКВ (LGE), диагностическая точность составляет 68% [88].
Однако, результаты метаанализа, проведенные Wei S et al [89] и Kotanidis CP et al [90], показывают, что оценка критериев LLC или отдельных компонентов, по-видимому, имеет умеренную эффективность при диагностике миокардита в клинической практике, но может быть дополнительно улучшена с помощью добавления новых методов параметрического картирования.
К дополнительным критериям относятся T2 картирование отека миокарда, оценка нативных T1 изображений и оценка экстрацеллюлярного объема для выявления миокардиального воспаления [91]. T1-, T2-картирование и оценка экстрацеллюлярного объема предоставляет количественную информацию об изменениях магнитных свойств ткани, которые отражают изменения в составе ткани миокарда, что позволяет получить уникальную информацию и повысить диагностическую ценность МРТ у пациентов с подозрением на миокардит, обеспечивая дополнительную чувствительность и специфичность метода.
В исследованиях у взрослых при использовании расширенных критериев их чувствительность достигает 87,5%, а специфичность - 96,2%, у детей, соответственно, 83 - 91% и 74 - 96% [92, 93, 94].
Диагностическая точность МРТ сердца может варьировать в зависимости от клинической картины и степени некроза клеток у пациентов с острым миокардитом, подтвержденным данными биопсии миокарда [95].
- Рекомендуется выполнить магнитно-резонансную томографию сердца с контрастированием с использованием ПМКС в первые 2 - 3 недели от начала заболевания [28, 43, 91, 94].
УУР C, УДД 5
Комментарии: при очень раннем исследовании (в первые дни заболевания) и в фазе восстановления чувствительность метода будет ниже. В случае отсутствия эпизодов обострения миокардита отек уменьшается через 2 - 4 недели от начала болезни [28, 43, 91, 94].
- Рекомендуется оценить данные, полученные в ходе МРТ сердца с контрастированием с использованием ПМКС, выполненной пациенту с подозрением на миокардит, по критериям LLC, а при наличии технической возможности - и по дополнительным критериям (T1-, T2-картирование и оценка экстрацеллюлярного объема) [87 - 94].
УУР C, УДД 5
- Рекомендуется повторное проведение МРТ сердца с контрастированием с использованием ПМКС через 1 - 2 недели после первоначального исследования, если нет ни одного из критериев LLC, но симптомы появились недавно или существуют убедительные клинические доказательства воспаления миокарда [87].
УУР C, УДД 5
- Рекомендуется проводить магнитно-резонансную томографию сердца с контрастированием детям с миокардитом через 6 - 12 месяцев при стабильном состоянии пациента с целью выявления осложнений и предикторов неблагоприятного прогноза [28, 96, 97, 99].
УУР C, УДД 5
Комментарии: при катамнестическом наблюдении после перенесенного острого миокардита исследование выполняется через 6 - 12 месяцев [28]. Исчезновение отека наблюдается до 84% случаев, тогда как LGE обычно сохраняется (в 89% случаев), что может означать развитие заместительного фиброза [97].
Наличие в межжелудочковой перегородке интрамурального позднего контрастного усиления в сочетании с низкой ФВ ЛЖ являются предикторами неблагоприятного исхода [98].
У пациентов с миокардитом, даже после улучшения клинической картины и нормализации уровня ферментов, может сохраняться, а иногда и увеличиваться объем LGE, что рассматривается как фактор риска неблагоприятных сердечно-сосудистых событий [99].
У пациентов с аритмией и другими артефактами движения качество изображения может не обеспечивать надежную визуализацию или количественную оценку отека [87].
При необходимости у детей МРТ сердца может проводиться с анестезиологическим пособием/использованием медикаментозной седации. Перед использованием МРТ необходимо учитывать риск седации и эндотрахеальной интубации, которые могут вызвать ухудшение клинического состояния [57, 100 - 102].
2.5 Иные диагностические исследования
Биопсия миокарда в настоящий момент является "золотым стандартом" в диагностике миокардита. При правильно выполненном исследовании возможно определить этиологический фактор и тип воспаления (например, гигантоклеточный, эозинофильный миокардит, саркоидоз), что позволяет определить тактику лечения и прогноз [3, 62]. Информативность биопсии миокарда у детей при подозрении на миокардит может достигать 75% [50].
Согласно опубликованным в 1987 году морфологическим критериям The Dallas criteria (морфологические Далласские критерии), определяют 3 типа основных патоморфологических изменений в ткани миокарда: инфильтрация, миоцитолиз и отек (таблица 5).
Таблица 5. Морфологические критерии миокардита (The Dallas criteria, 1987)
Определенный миокардит
Воспалительная инфильтрация миокарда с некрозом и/или дегенерацией прилегающих кардиомиоцитов, не характерная для ишемических изменений при ИБС
Вероятный миокардит
Воспалительные инфильтраты достаточно редки, либо кардиомиоциты инфильтрированы лейкоцитами. Нет участков миоцитонекроза. Миокардит не может быть диагностирован в отсутствие воспаления
Нет миокардита
Нормальный миокард или патологические изменения ткани невоспалительной природы
Однако, изолированное использование этих критериев имеет низкую диагностическую ценность [103, 104].
Помимо стандартного морфологического исследования препарата тканей миокарда, обязательным является проведение патолого-анатомического исследования биопсийного (операционного) материала тканей миокарда с применением электронно-микроскопических методов с применением иммуногистохимических методов исследования биоптата с использованием панели моноклональных и поликлональных антител (включая анти-CD3+ T-лимфоциты, анти-CD68+ макрофаги и анти-HLA-DR) для идентификации и характеристики воспалительного инфильтрата и для обнаружения активации HLA-DR в качестве маркера отсутствия инфекционного генеза и подтверждения аутоиммунного миокардита, что, соответственно, позволит принять решение о назначении иммуносупрессивной терапии.
В инфильтрате идентифицируются T-лимфоциты и T-лимфоциты-хелперы (>= 7 CD3+ на 1 мм2 или 2 в поле зрения, CD4+), T-супрессоры (CD8+), активированные T-лимфоциты (CD45RO), моноциты и макрофаги (CD68+) [3].
Наличие более 14 клеток лимфоцитов и моноцитов/макрофагов на 1 мм2 (x400) является подтверждением активного воспалительного процесса в миокарде.
Признаками острого миокардита является наличие >= 14 лимфоцитов и моноцитов/макрофагов на 1 мм2 в сочетании с некрозом и дистрофией кардиомиоцитов; для хронического миокардита характерно наличие > 14 клеток/мм2 в сочетании с фиброзом, но при отсутствии некроза и дистрофии кардиомиоцитов; наличие в биоптате < 14 клеток/мм2 исключает миокардит (x400) [3].
Для определения этиологии миокардита необходимо проведение молекулярного анализа - ПЦР-амплификации вирусного генома, количественное определение вирусной нагрузки.
В реальной клинической практике использование этого метода имеет значимые ограничения, связанные с инвазивностью исследования, возможными ошибками при заборе биоматериала, различиями в интерпретации результатов разными патоморфологами, невозможностью определить внеклеточное воспаление и др. [105].
Точность диагностики зависит от количества и размера биоптатов, места забора биоматериала и правильности обработки и хранения образцов, стадии заболевания.
Потенциальные осложнения при проведении биопсии миокарда включают перфорацию с развитием тампонады сердца, желудочковые или наджелудочковые аритмии, блокады сердца, повреждение трикуспидального клапана, пневмоторакс, перфорацию стенки сосудов, тромбоэмболию легочной артерии, парез нервов, гематомы, тромбоз глубоких вен, и образование вено-артериальной фистулы внутри сердца, кровотечение из места доступа, вазовагальные обмороки [3, 106].
- Рекомендуется выполнение биопсии миокарда в случае, если, несмотря на проводимое лечение, отсутствует клиническое улучшение или имеет место подозрение на нестандартный инфекционный этиологический фактор [3, 62].
УУР C, УДД 4
- Рекомендуется выполнение биопсии миокарда только в том случае, если подтверждение клинического диагноза миокардита окажет значимое влияние на план лечения пациента [3, 57, 63].
УУР C, УДД 5
- Рекомендуется проведение патолого-анатомического исследования биопсийного (операционного) материала тканей миокарда с применением электронно-микроскопических и иммуногистохимических методов [3, 104, 107].
УУР A, УДД 1
- Рекомендуется молекулярно-биологическое исследование биоптата миокарда на цитомегаловирус, вирус Эпштейна-Барр цитомегаловируса (Cytomegalovirus), вируса Эпштейна-Барр (Epstein - Barr virus), вируса герпеса 6 типа (HHV6): определение ДНК цитомегаловируса (Cytomegalovirus), вируса Эпштейна-Барр (Epstein - Barr virus), вируса герпеса 6 типа (HHV6) в биоптате миокарда методом ПЦР (качественное и количественное исследование) в медицинской организации, обладающей достаточным опытом в подготовке биоматериала и использовании данного метода [3, 60, 107].
УУР C, УДД 5
Комментарии: у детей наиболее часто выявляются геномы парвовируса B19, вирус герпеса 6 типа [60], реже аденовирусов и энтеровирусов [107].
В настоящее время количество биоматериала, необходимое для достижения клинически приемлемой чувствительности к кардиотропным вирусам, неизвестно, диагностическим является только положительный результат ПЦР, тогда как отрицательный результат ПЦР не исключает наличие вируса [69].
- Рекомендуется выполнение биопсии миокарда в медицинской организации, обладающей опытом проведения данной диагностической процедуры [3, 28, 63, 106].
УУР C, УДД 5
Комментарии: риски биопсии миокарда зависят от клинического состояния пациента, опыта врачебной бригады, локализации места доступа, используемых щипцов для биопсии миокарда, наличия БЛНПГ. Если пациент с наличием показаний к биопсии миокарда поступает в медицинский центр, где нет опыта проведения данной процедуры, то следует рассмотреть вопрос о переводе пациента в медицинскую организацию с таким опытом. Риски развития осложнений при выполнении биопсии миокарда в таком случае снижаются до 0 - 0,8% [3, 106].
- Не рекомендуется проведение биопсии миокарда у детей с массой тела менее 10 кг или у пациентов с нестабильной гемодинамикой в связи с высоким риском осложнений и летального исхода [1, 63].
УУР C, УДД 5
- Не рекомендуется использование методов ядерной медицины у детей [3, 15].
УУР C, УДД 5
Комментарий: Методы ядерной медицины не нашли широкого применения в педиатрии, по причине риска чрезмерного радиационного облучения детей [15].
3. Лечение, включая медикаментозную и немедикаментозную терапии, диетотерапию, обезболивание, медицинские показания и противопоказания к применению методов лечения
Существующие рекомендации по лечению миокардитов у детей основаны на мнении экспертов. Лечение сердечной недостаточности при миокардитах должно осуществляться в соответствии с текущими рекомендациями [5, 75, 76, 108 - 110].
- Рекомендуется госпитализация ребенка в острой фазе миокардита в стационар вне зависимости от тяжести течения заболевания на момент установления диагноза в связи с потенциальным риском быстрого прогрессирования СН, развития кардиогенного шока, которые требуют скорейшего лечения, что имеет решающее значение в данной ситуации [15, 62, 63, 68, 70].
УУР C, УДД 5
Лечебные мероприятия направлены на минимизацию гемодинамических затрат организма. На сегодня не существует рекомендованных схем терапии для предотвращения повреждения миокарда, но основной целью профилактики осложнений является поддержание тканевой перфузии.
В зависимости от клинической ситуации лечение миокардитов направлено на:
- неотложную коррекцию жизнеугрожающих состояний (рефрактерная недостаточность кровообращения, нарушения ритма и проводимости сердца);
- коррекцию проявлений сердечной недостаточности, обусловленной дисфункцией миокарда и нейрогуморальной активацией, согласно действующим клиническим рекомендациям по терапии острой и хронической СН;
- специфическое этиопатогенетическое воздействие на вирусную инфекцию и иммунное воспаление;
- коррекцию сопутствующей патологии, которая может усугублять течение основного заболевания.
3.1 Консервативное лечение
3.1.1. Лечение миокардита у пациентов с нестабильной гемодинамикой
Развитие нестабильной гемодинамики, кардиогенного шока наиболее часто сопровождает фульминантный миокардит.
- Рекомендуется пациентов с фульминантным миокардитом, ЭКГ с изменениями сегмента ST (особенно подъемом ST) или с тяжелой сердечной недостаточностью госпитализировать в отделение интенсивной терапии, оснащенное аппаратами для сердечно-легочной реанимации и проведения ИВЛ [15, 62].
УУР C, УДД 4
Комментарии: перечисленные группы пациентов имеют худший исход [79].
- Рекомендуется использование оксигенотерапии у пациентов с миокардитом, осложненным развитием гипоксемии на фоне тяжелой сердечной недостаточности по показаниям [75, 108].
УУР C, УДД 5
Комментарии: оксигенотерапия показана всем пациентам с SpO2 < 90% или PaO2 < 60 мм рт. ст. с целью коррекции гипоксемии. При проведении оксигенотерапии необходим контроль кислотно-основного состояния и SpO2.
Рутинное использование оксигенотерапии всем пациентам не проводится, так как при отсутствии гипоксемии она приводит к развитию вазоконстрикции и снижению сердечного выброса [108].
Искусственную вентиляцию легких следует рассмотреть у пациентов с острой декомпенсированной СН и респираторными нарушениями при отеке легких и/или низком уровне сердечного выброса.
Неинвазивная искусственная вентиляция легких может рассматриваться для лечения детей с острой сердечной недостаточностью, как с отеком легких, так и без него, в качестве дополнения к другим методам [76].
Преимуществом контроля вентиляции и оксигенации, обеспеченного неинвазивным методом в режиме постоянного положительного давления в дыхательных путях, является то, что исключается гипотония, связанная с использованием медикаментов, применяемых для седации и синхронизации с аппаратом ИВЛ [15] и снижается пред- и постнагрузка на левый желудочек по сравнению с использованием стандартной оксигенации через лицевую маску или назальные канюли.
Однако, при сохраняющейся дыхательной недостаточности с гипоксемией (PaO2 < 60 мм рт. ст.), гиперкапнией (PaCO2 > 50 мм рт. ст.) и ацидозом (pH < 7,35) рекомендуется интубация и перевод на ИВЛ [108].
- Рекомендуется катетеризация подключичной и других центральных вен всем пациентам с кардиогенным шоком, что позволяет проводить измерение центрального венозного давления (ЦВД), сатурации центральной венозной крови кислородом и иметь доступ для введения кардиотонических и других препаратов [111 - 113].
УУР C, УДД 5
- Рекомендуется у пациентов с кардиогенным шоком немедленная оценка признаков гипоперфузии и суточное прикроватное мониторирование жизненных функций и параметров (систолического артериального давления (САД), среднего АД, пульсового давления, ритма, частоты дыхания с учетом возраста и сатурации) [70, 106, 114].
УУР C, УДД 5
- Рекомендуется для определения подходов к лечению острой сердечной недостаточности и медикаментозной тактики первоначально оценить состояния перфузии и ОЦК (волемический статус) пациента [63, 109, 110].
УУР C, УДД 5
Комментарии: Алгоритм выбора тактики лечения пациентов с острым миокардитом на основании исходного гемодинамического профиля представлен в приложении Б [109].
Краеугольным камнем лечения в острых случаях является достижение эуволемического состояния с адекватным сердечным выбросом. Соответственно основными группами препаратов являются кардиотонические препараты и диуретики [109, 110].
Пациенты могут иметь симптомы, связанные с перегрузкой жидкостью и/или недостаточной перфузией. Важно иметь ввиду, что неадекватная (массивная) инфузионная терапия в условиях кардиогенного шока или острой сердечной недостаточности может ухудшить гемодинамику и состояние пациента [63].
- Рекомендуется назначение диуретиков у пациентов с миокардитом, осложненным развитием сердечной недостаточности, при наличии задержки жидкости и с целью уменьшения преднагрузки [63, 76].
УУР C, УДД 5
Комментарии: Предпочтительна внутривенная инфузия #фуросемида** со скоростью 0,1 - 0,4 мг/кг/час с титрованием дозы по эффекту. При внутривенном болюсном введении доза 0,5 - 2 мг/кг каждые 6 - 12 часов [63, 75].
- Рекомендуется временное назначение кардиотонических средств кроме сердечных гликозидов (АТХ C01C) внутривенно у детей с кардиогенным шоком и у пациентов с признаками низкого сердечного выброса и гипоперфузии внутренних органов [76].
УУР C, УДД 5
Комментарии: поврежденный миокард имеет ограниченный резерв сократительной способности, в связи с чем при использовании высоких доз кардиотонической поддержки может произойти гемодинамический коллапс.
Применение кардиотонических средств кроме сердечных гликозидов (АТХ C01C) приводит к улучшению сердечного выброса и артериального давления, конечным результатом является увеличение потребления и потребности миокарда в кислороде [75].
Учитывая высокую частоту осложнений (тахисистолия, аритмии и т.д.), их следует использовать в качестве краткосрочной стратегии стабилизации и уменьшения выраженности симптомов. Одновременно с началом кардиотонической поддержки должен быть разработан план эскалации терапии до механической поддержки кровообращения и/или трансплантации сердца, если отсутствуют признаки значимого клинического улучшения [115, 116].
В настоящее время нет данных о преимуществе использования какого-либо из препаратов из группы кардиотонических средств кроме сердечных гликозидов (АТХ C01C) [62].
Кардиотоническая терапия может рассматриваться для облегчения симптомов у пациентов в паллиативном статусе [76, 110].
- Рекомендуется применение препаратов, действующих непосредственно на гладкую мускулатуру артериол (АТХ C02D), у детей с острой сердечной недостаточностью при отсутствии гипотензии, и использование в сочетании с диуретиками для облегчения симптомов у пациентов с отеком легких [63, 76].
УУР C, УДД 5
3.1.2. Лечение пациента с миокардитом и стабильной гемодинамикой
- Рекомендуется постельный режим (не менее 2 недель, а далее в зависимости от тяжести заболевания) с лечебной физкультурой (Лечебная физкультура при заболеваниях сердца и перикарда) и дыхательной гимнастикой без усилия до разрешения острой фазы [62, 68].
УУР C, УДД 5
Комментарии: интенсивная физическая нагрузка способствует усилению репликации вирусов, воспаления и некроза кардиомиоцитов, ремоделирования сердца, повышает риск внезапной смерти [6]. Постельный режим способствует снижению потребления кислорода [62].
- Рекомендуется полноценное рациональное питание [68, 70, 75, 117, 118].
УУР C, УДД 5
Комментарии: у младенцев нутритивная поддержка должна обеспечивать калорийность около 150 ккал/кг/день, рекомендованы небольшие и частые приемы пищи, так как они лучше переносятся.
Детям раннего возраста при тяжелой сердечной недостаточности целесообразен временный переход на кормление через назогастральный зонд (Кормление тяжелобольного пациента через рот и/или назогастральный зонд).
Для детей и подростков рекомендованный калораж составляет 25 - 30 ккал/кг/сут.
Может потребоваться больше или меньше калорий в зависимости от роста ребенка в ответ на их потребление.
Количество углеводов не должно превышать 6 г/кг/сутки, а липидов - 2,5 г/кг/сутки [117, 118].
Рекомендуется обеспечить потребление белка 1,5 - 2,5 г/кг для младенцев и 0,8 - 1,5 г/кг для детей старшего возраста [117].
Для коррекции недостаточности питания обязательно назначение специального лечебного питания в соответствии с рекомендациями врача-диетолога.
Больным в критическом состоянии необходимо обеспечить организм незаменимыми аминокислотами [75].
Ограничение потребления соли должно быть определено степенью сердечной недостаточности.
Уменьшение потребления соли рекомендуется всем пациентам с острой сердечной недостаточностью, а также с отеками и задержкой жидкости [75, 76].
- Рекомендуется соблюдать водный режим [62, 63, 68, 75].
УУР C, УДД 5
Комментарии: ограничение потребления жидкости относительно физиологической потребности (таблица 6) должно быть определено тяжестью дисфункции миокарда и клиникой сердечной недостаточности [63].
Таблица 6. Физиологическая потребность в жидкости детей в зависимости от возраста [119]
Возраст
Масса тела
Ежедневная потребность в жидкости
мл
мл/кг
3 дня
3.0
250 - 300
80 - 100
10 дней
3.2
400 - 500
130 - 150
6 мес.
8.0
950 - 1000
130 - 150
1 год
10.5
1150 - 1300
120 - 140
2 года
14.0
1400 - 1500
115 - 125
5 лет
20.0
1800 - 2000
90 - 100
10 лет
30.5
2000 - 2500
70 - 85
14 лет
46.0
2200 - 2700
50 - 60
18 лет
54.0
2200 - 2700
40 - 50
Ограничение жидкости показано пациентам с отеками, рефрактерными к терапии диуретиками, или с гипонатриемией [75].
Ограничение жидкости целесообразно для пациентов с острой сердечной недостаточностью, независимо от уровня натрия в сыворотке [76].
- Рекомендуется лечение СН согласно действующим клиническим рекомендациям по терапии острой и хронической СН [1, 3, 6, 28, 63, 76].
УУР C, УДД 5
Комментарии: на сегодняшний день для лечения сердечной недостаточности у детей используются ингибиторы ангиотензинпревращающего фермента (АФП) (иАПФ; АТХ C09A), антагонисты рецепторов ангиотензина II (АА; АТХ C09C), бета-адреноблокаторы (АТХ C07), диуретики (АТХ C03), [1, 76]. Диуретики используются для лечения задержки жидкости, связанной с дисфункцией желудочков и, соответственно, снижения преднагрузки, иАПФ/АА уменьшают постнагрузку за счет воздействия на ренин-ангиотензинальдостероновую систему, бета-адреноблокаторы противодействуют патологическим эффектам хронической симпатической активации в миокарде и могут оказывать влияние на процессы ремоделирования ЛЖ.
В педиатрической практике из группы бета-адреноблокаторов наиболее эффективным является #Карведилол** (АТХ C07AG02), который помимо всего прочего обладает сосудорасширяющими свойствами из-за его дополнительного альфа-адреноблокирующего действия и обладает кардиопротективным эффектом за счет опосредованного подавления активности провоспалительных цитокинов при остром миокардите [1]. #Карведилол** является препарат первой линии из группы бета-блокаторов при СН с нормальным систолическим артериальным давлением.
#Карведилол** назначается перорально у пациентов с массой тела менее 62,5 кг в стартовой дозе 0,1 мг/кг/сут. с постепенной титрацией дозы до 0,8 - 1,0 мг/кг/сут. в два приема (из-за особенностей фармакокинетики #Карведилола** у пациентов младше 4 лет суточная доза делится на три приема). При массе тела более 62,5 кг стартовая доза составляет по 3,25 мг 2 раза в сутки с постепенным повышением дозы до 25 мг 2 раза в сутки; при массе тела более 75 кг - по 25 мг 3 раза в сутки [63].
иАПФ/АА и бета-адреноблокаторы могут замедлить прогрессирование сердечной недостаточности и повысить выживаемость, однако, могут иметь место проблемы с их титрацией и переносимостью [110].
Несмотря на отсутствие достаточного количества рандомизированных проспективных исследований, иАПФ являются препаратами первой линии, а бета-адреноблокаторы являются препаратами второй линии для лечения детей.
Следуя рекомендациям для взрослых и не имея данных, относящихся к педиатрической популяции, антагонисты альдостерона также применяются для лечения сердечной недостаточности у детей, в то время как диуретики из других групп следует использовать только для достижения эуволемического статуса [110]. Спиронолактон** (АТХ C03DA01) применяется в дозах от 0,5 до 4 мг/кг/сут. в 2 приема в комбинации с "петлевыми" диуретиками (АТХ C03C), для коррекции гипокалемии, усиления мочегонного эффекта. [63, 68, 75].
Тиазидные диуретики значительно усиливают эффект "петлевых" диуретиков и могут быть добавлены пациентам с ограниченным ответом на "петлевые" диуретики для преодоления рефрактерности. Их часто вводят за 30 минут до дозы петлевого диуретика, чтобы обеспечить синергический эффект. Терапия диуретиками должна проводиться под контролем уровня электролитов, АД, функции почек. [63, 75, 76, 109].
Дигоксин** (АТХ C01AA05) не применяется при лечении острого миокардита [1, 4]. Данное утверждение основано на исследовании Matsumori A et al (1999), которое показало повышенный синтез провоспалительных цитокинов и повышенное повреждение миокарда при его использовании в высоких дозах [120].
- Рекомендуется этиотропная терапия инфекции, подтвержденной бактериологическими, серологическими и/или молекулярно-биологическими исследованиями, с привлечением инфекционистов при принятии решения о назначении специфической терапии [3].
УУР C, УДД 5
Комментарии: основанием для использования противовирусной терапии является тот факт, что большинство случаев миокардита вызваны вирусными инфекциями [6].
Исходя из стадий патогенеза вирусного миокардита, противовирусная терапия обладает наибольшей эффективностью на самой ранней стадии миокардита [4].
Персистенция вируса в кардиомиоцитах рассматривается как самостоятельный негативный прогностический фактор, повышающий риск летального исхода.
На сегодняшний день терапевтическая эффективность специфической противовирусной терапии при остром вирусном миокардите еще не была установлена в рандомизированных клинических исследованиях [5].
У пациентов с герпес-вирусной инфекцией, при рефрактерных к лечению случаях может рассматриваться назначение препаратов из группы нуклеозидов и нуклеотидов, кроме ингибиторов обратной транскриптазы (АТХ J05AB), хотя их клиническая эффективность при миокардите не доказана [6].
При документированной вирусной этиологии генерализованного инфекционного процесса, на фоне которого подозревается поражение миокарда (при отсутствии данных биопсии миокарда), могут использоваться:
при Herpes simplex 1, 2 типа - Ацикловир** (АТХ J05AB01) новорожденным в физиологическом растворе в дозе 60 мг/кг/сутки доношенным, разделенной на 3 равных введения через каждые 8 часов, недоношенным с постконцептуальным возрастом менее 30 недель - 40 мг/кг в сутки, разделенные на 2 введения с интервалом 12 часов. Длительность лечения 14 суток при локализованной ВПГ-инфекции, 21 и более суток - при остальных клинических формах. При ухудшении состояния или нарастании симптоматики поражения ЦНС показано повторное введение препарата в том же режиме еще минимум в течение 7 - 10 суток под контролем ПЦР. В более старшем возрасте: 3 мес. - 12 лет - 25 - 40 мг/кг/сут.; 12 - 18 лет - 15 - 30 мг/кг/сут. в 3 введения. Курс - 2 - 3 недели. Препарат вводят под контролем клиренса креатинина, содержания мочевины и трансаминаз крови, клинического анализа крови. Для профилактики повреждения почек необходимо обеспечить адекватную гидратацию, оптимально вводить препарат внутривенно медленно в течение часа (предупреждение образования кристаллических преципитатов в почечных канальцах) [121 - 124].
При цитомегаловирусной этиологии - #Ганцикловир** (АТХ J05AB06) 5 - 6 мг/кг внутривенно медленно в течение 1 часа каждые 12 часов 2 раза в сутки, продолжительность индукционного курса составляет 14 - 21 день, затем по возможности переходят на прием #Валганцикловира** (АТХ J05AB14) внутрь 16 мг/кг (разовая доза) 2 раза в сутки, либо, в дальнейшем назначают поддерживающий курс #Ганцикловира** (АТХ J05AB06) - 6 мг/кг 5 раз в неделю или 5 мг/кг ежедневно. Продолжительность лечения определяют индивидуально. Возможен старт терапии с назначения #Валганцикловира** (АТХ J05AB14). Препарат назначается энтерально в дозе 16 мг/кг (разовая доза) 2 раза в сутки курсом от 6 недель до 6 месяцев в зависимости от тяжести заболевания и развития побочных эффектов (контроль гемограммы: еженедельно первые 6 недель лечения, далее на 8 неделе и ежемесячно в течение курса терапии; контроль уровня трансаминаз ежемесячно [121, 124 - 127].
В дополнение к терапии может быть использовано одновременное и последовательное назначение Иммуноглобулина человека антицитомегаловирусного (АТХ: J06BB09) в разовой дозе 1 - 2 мл/кг каждые 48 часов, продолжительность курса в зависимости от клинической ситуации [121].
Этиотропная терапия для лечения Эпштейн-Барр-вирусной инфекции не разработана, возможно использование интерферонов (АТХ L03AB), при тяжелых формах - препаратов из группы нуклеозидов и нуклеотидов, кроме ингибиторов обратной транскриптазы (АТХ J05AB), Иммуноглобулина человека нормального для в/в введения** (АТХ J06BA02) в дозе 0,2 - 0,4 г/кг/сутки 4 - 5 введений [129, 130, 131].
Этиотропная терапия для лечения Парвовирусной B19 инфекции не разработана. При тяжелом течении миокардита может использоваться терапия Иммуноглобулином человека нормальным для в/в введения** в высоких дозах по следующим схемам: 2 г/кг на курс на 1 - 2 введения или 0,4 г/кг на 5 последовательных введений; также можно повторять введение иммуноглобулина в дозе 0,4 - 0,6 г/кг раз в 21 - 28 дней в течение нескольких месяцев [131, 132, 133].
Пациенты с миокардитом, ассоциированным с ВИЧ-инфекцией, вирусом гепатита C или вирусом гриппа должны получать лечение согласно действующим клиническим рекомендациям по данным нозологическим формам [62].
Пациенты с коронавирусной инфекцией (MERS-CoV, SARS-CoV, SARS-CoV-2) должны получать терапию в соответствии с действующими клиническими рекомендациями, возможные методы лечения в настоящее время изучаются [5].
В настоящее время проводятся исследования препарата #Интерферон бета-1b** (АТХ L03AB08) для лечения вирусного миокардита, однако, данный препарат на сегодняшний день используется только у взрослых пациентов в случае доказанного наличия энтеровирусов в миокарде пациента [5, 134, 135].
При необходимости назначения антибактериальной терапии применяют препараты, охватывающие наиболее широкий спектр микроорганизмов, в стандартных дозировках (чаще комбинации пенициллинов, включая комбинации с ингибиторами бета-лактамаз (АТХ J01CR), в сочетании с аминогликозидами (АТХ J01G), цефалоспоринами второго (АТХ J01DC), третьего (АТХ J01DD), и четвертого поколения (АТХ J01DE), в течение 2 - 4 недель [68].
- Не рекомендуется назначение нестероидных противовоспалительных и противоревматических препаратов (НПВП) для лечения миокардита, за исключением сочетания с перикардитом [1, 4, 6, 136, 137].
УУР C, УДД 5
Комментарии: имеют место доказательства, что при использовании НПВП отмечается увеличение репликации вируса, выраженности воспаления и смертности [136, 137].
- Рекомендуется использование #Иммуноглобулина человека нормального для в/в введения** в острой фазе миокардита [131, 132, 138 - 144].
УУР C, УДД 4
Комментарии: в литературе описаны данные о положительных эффектах применения #Иммуноглобулина человека нормального для в/в введения** (повышение сократительной способности миокарда, уменьшение размеров ЛЖ, улучшение выживаемости), в связи с чем использование данной терапии в острой фазе миокардита может быть целесообразным, однако, в настоящее время отсутствуют проспективные рандомизированные контролируемые исследования, подтверждающие эффективность использования #Иммуноглобулина человека нормального для в/в введения** при миокардите у детей, а также его влияние на исход и прогноз заболевания в педиатрической популяции [132, 138 - 144].
#Иммуноглобулин человека нормальный для в/в введения** рекомендовано использовать в высоких дозах - 1 - 2 г/кг на курс [131, 142, 143]. На сегодняшний день исследованы и могут быть рекомендованы несколько схем введения: 2 г/кг на курс на 1 - 2 введения; 0,4 г/кг на 5 последовательных введений; также можно повторять введение иммуноглобулина в дозе 0,4 - 0,6 г/кг раз в 21 - 28 дней в течение нескольких месяцев [131].
- Рекомендуется применение глюкокортикоидов (ГК) для лечения отдельных групп миокардитов (аутоиммунный, гигантоклеточный, эозинофильный, гранулематозный), а также у пациентов с тяжелым рефрактерным течением заболевания [4, 6].
УУР C, УДД 5
- Не рекомендуется использование ГК в рутинной практике при лечении острого миокардита [63, 149 - 152].
УУР C, УДД 5
Комментарии: в более ранних исследованиях сообщалось, что высокие дозы ГК обладают терапевтическим эффектом при миокардите у детей и могут способствовать восстановлению систолической функции левого желудочка при остром миокардите [145 - 148]. Однако недавние обзоры и метаанализы показали, что терапия высокими дозами ГК не оказывала значительного влияния на клинические исходы и не снижала уровень смертности [149 - 152].
ГК, в том числе в структуре, комбинированной иммуносупрессивной терапии, используются при лечении вирус-негативного: аутоиммунного, эозинофильного, гигантоклеточного, гранулематозного миокардита [4].
А также их назначение может обсуждаться в рефрактерных к терапии случаях с высоким воспалительным компонентом при отсутствии признаков вирусной репликации по данным ПЦР биоптата [6].
Иммуноабсорбция - метод, основанный на удалении антикардиальных антител, титр которых повышен у пациентов с аутоиммунными заболеваниями и острым аутоиммунным миокардитом. В настоящее время нет ни одного большого проспективного клинического исследования по оценке влияния этого метода на жесткие конечные точки, в связи с чем в настоящее время не рекомендовано использование иммуноабсорбции для лечения острого миокардита в качестве обязательного базового метода лечения. Однако, в небольших по численности контролируемых исследованиях иммуноабсорбция приводила к улучшению гемодинамических показателей и выраженности воспалительной реакции у пациентов с ДКМП [153, 154]. У детей в настоящее время данные методики не используются.
- Рекомендуется при нарушениях ритма сердца назначение антиаритмической терапии в соответствии с национальными рекомендациями по лечению аритмий [3, 76].
УУР C, УДД 5
Комментарии: перед назначением антиаритмической терапии необходимо в первую очередь провести коррекцию экстракардиальных причин (электролитный дисбаланс, метаболические нарушения и т.д.). Учитывая наличие побочных эффектов, препараты должны использоваться по строгим показаниям при клинически значимых аритмиях [76].
Основными патогенетическими механизмами развития аритмии у больных острым миокардитом являются электрическим нестабильность миокарда вследствие прямого цитопатического эффекта, ишемия из-за вовлечения коронарных сосудов, дисфункция межклеточного взаимодействия, нарушение метаболизма кальция и вовлечение проводящей системы в воспалительный процесс. Риск внезапной сердечной смерти у пациентов с острым миокардитом не всегда связан с тяжестью воспаления в миокарде и может сохраняться после разрешения острой фазы миокардита [5, 155, 156].
- Не рекомендуется назначение антиаритмических препаратов IA и IC классов, бета-адреноблокаторов, селективных блокаторов кальциевых каналов с прямым действием на сердце, обладающих отрицательным инотропным эффектом, у пациентов с умеренной и выраженной дисфункцией миокарда [157, 158, 159].
УУР C, УДД 5
- Рекомендуется у пациентов с умеренной и выраженной дисфункцией миокарда применение антиаритмических препаратов III класса [63, 157, 158, 159].
УУР C, УДД 5
- Рекомендуется коррекция электролитных нарушений пациентам с сердечной недостаточностью и аритмиями на фоне миокардита [63, 75, 76, 158].
УУР C, УДД 5
- Рекомендуется коррекция анемии пациентам с сердечной недостаточностью вследствие миокардита [62, 76, 160, 161].
УУР C, УДД 5
Комментарий: целесообразно рассмотреть возможность использования парентеральных препаратов трехвалентного железа (АТХ B03AC) для лечения железодефицитной анемии, а если анемия сохраняется после восполнения запасов железа - использования других антианемических средств, стимулирующих эритропоэз, для лечения анемии у детей с сердечной недостаточностью [76]. Для оптимизации транспорта кислорода может потребоваться переливание эритроцитарной массы [15].
Нет никаких доказательств, подтверждающих использование парентеральных препаратов трехвалентного железа или других антианемических препаратов, стимулирующих эритропоэз, для профилактики анемии, ассоциированной с наличием СН у детей [76].
- Рекомендуется при наличии показаний и отсутствии противопоказаний терапия антитромботическими средствами [15, 76].
УУР C, УДД 5
Комментарий: Рутинное использование антитромботических средств у пациентов с систолической сердечной недостаточностью и без тромбоэмболических событий в анамнезе не рекомендуется [76].
3.2 Хирургическое лечение
- Рекомендуется рассмотреть вопрос о проведении временной механической поддержки кровообращения у пациентов с крайне тяжелыми и фульминантными формами миокардита [1, 15, 57].
УУР C, УДД 5
Комментарии: Системы для экстракорпоральной мембранной оксигенации (ЭКМО), аппараты для экстракорпоральной поддержки работы сердца и комплекс универсальный для механической поддержки насосной функции левого и правого желудочков сердца в детской практике в большинстве случаев используются как "мост" к восстановлению сократительной функции миокарда или "мост" к трансплантации сердца.
Вено - артериальная ЭКМО применяется при остро развившихся состояниях, при которых прогнозируется восстановление сократительной функции миокарда в течение 1 - 2 недель. Признаки улучшения выброса левого желудочка обычно появляются менее, чем через неделю после начала ЭКМО.
Если для восстановления функции миокарда требуется больше времени, временная или долговременная установка аппаратов для экстракорпоральной поддержки работы сердца или комплекса универсального для механической поддержки насосной функции левого и правого желудочков сердца (ventricular assist device - VAD) может быть использована в качестве "моста" либо к выздоровлению, либо к трансплантации сердца [15, 57, 75].
- Рекомендуется рассмотреть вопрос о проведении временной трансвенозной электрокардиостимуляции при развитии выраженной брадикардии или полной атриовентрикулярной блокады в связи с возможным прогрессированием желудочковой дисфункции до разрешения острого процесса в миокарде [3, 162 - 164].
УУР C, УДД 4
- Рекомендуется рассмотреть вопрос о необходимости трансплантации сердца только после разрешения острой фазы дебюта миокардита [3, 165 - 167].
УУР C, УДД 5
Комментарии: вопрос о трансплантации сердца в остром периоде миокардита у пациента может быть рассмотрен только в той ситуации, когда, несмотря на оптимальную фармакологическую терапию и механическую поддержку, не удается стабилизировать гемодинамические параметры [3]. Важно помнить, что у большинства пациентов, вышедших из острой фазы миокардита, произойдет спонтанное восстановление сократительной функции сердца.
Дети после пересадки сердца по поводу миокардита часто имеют тяжелый ранний и поздний послеоперационный период и с большей вероятностью имеют факторы риска неблагоприятных исходов после трансплантации сердца [165 - 167].
Наиболее частой причиной смерти после трансплантации сердца у детей является острое отторжение трансплантата [165].
4. Медицинская реабилитация и санаторно-курортное лечение, медицинские показания и противопоказания к применению методов медицинской реабилитации, в том числе основанных на использовании природных лечебных факторов
Реабилитационные мероприятия при миокардитах определяются фазой заболевания, базируются на принципах реабилитации детей с сердечной недостаточностью и предусматривают этапность и преемственность. Реабилитация детей с миокардитом, как и пациентов других категорий включает медицинский, психологический, социально-экономический аспекты.
Реабилитация детей с миокардитом предусматривает оценку реабилитационного потенциала ребенка, разработку индивидуального плана реабилитационных мероприятий, определение системы мер, структур, методик, а также прогнозирование ожидаемых положительных результатов на основании реабилитационного диагноза [75, 168].
При проведении реабилитационных мероприятий у детей с миокардитом рекомендуется опираться на законодательные акты РФ (Приказ Министерства здравоохранения РФ от 23.10.2019 N 878н "Об утверждении Порядка организации медицинской реабилитации детей"), использовать Международную классификацию функционирования (МКФ), общую для взрослых и детей и рекомендации специалистов многопрофильной реабилитационной команды (МРК) [169]. Методы физической реабилитации у детей с миокардитами не разработаны.
- Рекомендуются ограничения физической активности в острую фазу миокардита [3, 69].
УУР C, УДД 5
Комментарии: острый миокардит является абсолютным противопоказанием для проведения физических тренировок. Противопоказанием к физической активности являются жизнеугрожающие нарушения ритма и проводимости сердца, тяжелая степень сердечной недостаточности, гипотония, острые системные заболевание и/или лихорадка. В период стабилизации состояния пациента рекомендуется расширение физической активности от низкой до умеренной интенсивности [170].
- Рекомендуется проведение нагрузочного тестирования тест с 6-минутной ходьбой, кардиопульмональное нагрузочное тестирование, проба с дозированной физической нагрузкой на велоэргометре или тредмиле с целью оптимизации программы физической реабилитации у пациентов, после разрешения острой фазы, для исходной оценки физической работоспособности и при динамическом наблюдении [76, 168, 171, 172].
УУР C, УДД 5
Комментарии: По результатам теста с 6-минутной ходьбой расстояние менее 150 метров за 6 минут исключает любые нагрузки кроме упражнений для дыхательной мускулатуры, расстояние более 300 метров за 6 минут позволяет рекомендовать ходьбу. В сроки более 6 месяцев после реконвалесценции могут проводиться кардиопульмонологическое нагрузочное тестирование, субмаксимальные пробы с дозированной физической нагрузкой на велоэргометре или тредмиле по принятым в педиатрической практике протоколам, чаще PWC 170. [76, 171].
В программе реабилитации полезны упражнения, которые выполняются в аэробном режиме, когда потребность работающих мышц в кислороде полностью удовлетворяется. Следует чередовать мышечные усилия: начинать занятие с более легких упражнений, затем выполнять более трудные, после которых выполнять дыхательные или упражнения для расслабления мышц. Дозирование физической нагрузки проводится по самочувствию пациента, наступлению утомления с контролем частоты пульса и дыхания [173].
- Рекомендуются аэробные нагрузки (дозированная ходьба на свежем воздухе, ходьба на лыжах, легкий бег, езда на велосипеде), комплекс общеукрепляющих гимнастических упражнений под контролем самочувствия, частоты сердечных сокращений, частоты дыхательных движений, АД, сатурации кислородом периферической крови [173 - 176].
УУР C, УДД 5
Комментарии: исходно умеренные нагрузки и тренировки на уровне 40 - 50% от значений, полученных в ходе оценки толерантности к физическим нагрузкам, полученной при тестировании, с постепенным расширением объема физической активности [176].
В настоящее время активно применяется широкий арсенал физиотерапевтических методов и методик. Любая методика физиотерапии в программе реабилитации миокардита назначается только врачом-физиотерапевтом индивидуально. Аппаратные методы физиотерапии и методы электролечения противопоказаны пациентам с нарушениями сердечного ритма и имплантируемыми электрокардиостимуляторами***/кардиовертерами-дефибрилляторами***.
- Рекомендуется проведение психологической реабилитации, которая начинается уже в период пребывания ребенка в стационаре (в реанимации и в отделении) или амбулаторно после выписки из стационара и включает различные методы детской психотерапии и психокоррекции, которые проводятся медицинским психологом [76, 168, 176].
УУР C, УДД 5
Комментарии: в рамках психологической реабилитации используется индивидуальная и групповая психокоррекция, тренинги, очные и дистанционные школы, телефонные консультации медицинских психологов, врачей-физиотерапевтов (реабилитологов), специально обученным сестринским персоналом, по показаниям применяются компьютерные программы когнитивной стимуляции, патронажная работа [177].
После стабилизации состояния и отсутствии воспалительной активности возможно санаторно-курортное лечение в санаториях кардиологического профиля, с учетом региона проживания ребенка и сезона - целесообразно избегать резкой смены климата.
5. Профилактика и диспансерное наблюдение, медицинские показания и противопоказания к применению методов профилактики
Профилактика и диспансерное наблюдение
Первичной профилактикой миокардита является адекватная профилактика внутриутробных инфекций, плановое обследование беременных, предупреждение энтеровирусных инфекций, внутрибольничных инфекций и инфекций в организованных коллективах, иммунопрофилактика контролируемых инфекций, расширение Национального календаря прививок, неспецифическая и специфическая сезонная профилактика гриппа и ОРВИ, закаливание, иммунореабилитация "часто болеющих" детей и детей групп риска тяжелого течения вирусных инфекций, регулярные профилактические осмотры, санация очаговой инфекции, профилактика тонзиллогенных заболеваний миокарда.
- Рекомендуется проведение вакцинации детям согласно Национальному календарю профилактических прививок с целью первичной профилактики миокардита [76, 178].
УРР C, УДД 5
Вторичная профилактика миокардита заключается в адекватном диспансерном наблюдении и реабилитации реконвалесцентов миокардита, активном выявлении, лечении и реабилитации детей с латентными и субклиническими формами.
- Рекомендуется: диспансерное наблюдение врачом-педиатром и детским кардиологом за детьми, перенесшими острый миокардит, в течение 3-х лет с момента установления диагноза или выписки из стационара, больными хроническим миокардитом - постоянно [3, 62, 68, 70, 179].
УРР C, УДД 5
Комментарии: первые 4 месяца после выписки дети осматриваются 1 раз в месяц, последующий год 1 раз в квартал, далее 1 раз в 6 месяцев, при необходимости чаще.
На каждом приеме контролируют самочувствие, общее состояние больного, симптомы сердечной недостаточности, размеры сердца, критерии ремоделирования миокарда по данным ЭХОКГ, наличие систолической и диастолической дисфункции, ЭКГ в покое, общий (клинический) анализ крови, анализ крови биохимический общетерапевтический, общий (клинический) анализ мочи. ЭКГ и ЭХОКГ проводится при каждом визите, по показаниям - чаще. После острого миокардита в течение первых 6 месяцев дети наблюдаются в 4-й группе здоровья, затем переводятся в 3-ю группу здоровья. Перевод во 2-ю группу решается в зависимости от данных обследования. При хроническом течении миокардита вопрос решается индивидуально в зависимости от клинико-функциональных и лабораторных показателей (3-я или 4-я группа здоровья).
Прививки противопоказаны в течение 6 месяцев - 1 года после перенесенного острого или подострого миокардита, при хроническом - вопрос рассматривается индивидуально: рекомендуется проведение вакцинации в щадящем режиме при условии стабилизации состояния и положительной динамике не ранее, чем через 1 год после дебюта заболевания [68, 70, 179].
- Рекомендуется клиническое обследование и полный спектр функциональных исследований сердечно-сосудистой системы: ЭКГ в покое, холтеровского мониторирования сердечного ритма, субмаксимальные тесты с нагрузкой, исследование уровня натрийуретических пептидов (мозгового натрийуретического пептида (BNP) и/или исследование уровня N-терминального фрагмента натрийуретического пропептида мозгового (NT-proBNP) в крови, ЭХОКГ с изучение морфометрических показателей, насосной и сократительной функции миокарда и состояние перикарда, перед снятием пациента с диспансерного наблюдения. Все вышеуказанные лабораторные показатели должны быть в пределах нормы [155, 179, 180].
УРР C, УДД 5
Социальная реабилитация детей с миокардитом включает индивидуальные режимы обучения (по показаниям), у старших детей - рекомендации по профориентации, по показаниям - установление инвалидности и формирование мероприятий социальной реабилитации в индивидуальной программе реабилитации инвалида (Приказ Минтруда России от 27.08.2019 N 585н (в редакции 19.01.2021) "О классификации и критериях, используемых при осуществлении медико-социальной экспертизы граждан федеральными государственными учреждениями медико-социальной экспертизы").
Качество жизни пациентов зависит от своевременности постановки диагноза и назначения медикаментозной терапии. Критериями эффективности диспансеризации и реабилитации считаются отсутствие жалоб, клинических симптомов и инструментальных признаков сердечной декомпенсации, исчезновение нарушений ритма сердца и проводимости, хорошая переносимость физических нагрузок.
6. Организация оказания медицинской помощи
В острой фазе миокардита ребенок должен быть госпитализирован в стационар вне зависимости от тяжести течения заболевания на момент установления диагноза, в связи с потенциальным риском быстрого прогрессирования СН, развития жизнеугрожающих аритмий, кардиогенного шока, которые требуют скорейшего лечения, что имеет решающее значение в данной ситуации.
Экстренная госпитализация показана при выявлении изменений ЭКГ и/или признаков СН.
Дети с фульминантным миокардитом, с изменениями сегмента ST (особенно подъемом ST) на ЭКГ или с тяжелой сердечной недостаточностью должны быть госпитализированы в отделение интенсивной терапии, оснащенное аппаратами для сердечно-легочной реанимации и проведения ИВЛ, так как вышеописанные группы пациентов имеют худший исход [62, 79].
Показания для госпитализации в медицинскую организацию:
1) подозрение на миокардит у гемодинамически нестабильного пациента.
2) подозрение на миокардит у гемодинамически стабильного пациента, имеющего клинические проявления сердечной недостаточности на уровне II - IV ФК и/или документированную систолическую дисфункцию ЛЖ по ЭХОКГ [16].
3) установленный диагноз "острый миокардит" вне зависимости от тяжести течения заболевания на момент установления диагноза.
Показания для госпитализации в отделение реанимации включают
1) жизнеугрожающую аритмию,
2) тромбоэмболический синдром,
3) признаки гипоперфузии периферических органов,
4) кардиогенный шок и отек легких.
Комментарии: Пациенты с молниеносным (фульминантным) острым миокардитом и нестабильными гемодинамическими показателями должны наблюдаться в реанимационных отделениях, оснащенных необходимым оборудованием, предпочтительно в многопрофильных стационарах [4, 181, 182].
Показания к выписке пациента из стационара
При стойком улучшении клинической картины, исчезновении лихорадки, стабилизации показателей гемодинамики, подтвержденных клинически, инструментально и лабораторно, рекомендуется выписка из стационара с дальнейшим наблюдением и лечением на амбулаторном этапе.
7. Дополнительная информация (в том числе факторы, влияющие на исход заболевания или состояния)
7.1. Осложнения:
- Кардиофиброз
- Стойкие нарушения ритма сердца и проводимости
- ХСН
7.2. Исходы и прогноз
Прогноз пациента зависит от ряда факторов: этиологической причины развития миокардита, течения заболевания, выраженности недостаточности кровообращения, наличия или отсутствия персистенции вируса в ткани миокарда, адекватности и своевременности оказания медицинской помощи [3, 15, 62, 77].
При остром миокардите без ХСН прогноз, как правило, благоприятный.
Острое начало миокардита у детей в раннем возрасте с клиникой ХСН, как правило, так же имеет благоприятный прогноз при условии раннего выявления и адекватной терапии [15]. Длительность заболевания напрямую зависит от степени повреждения миокарда: при минимальных изменениях возможно полное восстановление, при значительном повреждении миокарда и персистенции вируса в миокарде формируется синдром дилатационной кардиомиопатии - кардиомегалия, дилатация полостей сердца, снижение сократительной способности миокарда, что делает прогноз неблагоприятным, так как возрастет риск потребности в трансплантации сердца.
Фульминантное течение миокардита с ХСН может иметь неблагоприятный исход. Прогрессирующая сердечная недостаточность при хроническом миокардите может привести к летальному исходу.
Прогноз крайне неблагоприятен при гигантоклеточном миокардите. Продолжительность жизни при гигантоклеточном миокардите составляет примерно 5,5 мес. с момента появления первых симптомов.
Прогноз всегда тяжелый при эозинофильном миокардите и саркоидозе сердца.
Значимые факторы неблагоприятного прогноза - стойкие угрожающие нарушения ритма, расширение комплекса QRS более 120 мс и синкопальные состояния, наличие которых увеличивает риск внезапной смерти. Своевременное выявление этих факторов риска и их коррекция, в том числе имплантацией ИКД*** или имплантируемое СРТ-устройство (устройств для ресинхронизирующей терапии), позволяют радикально улучшить прогноз.
В период диспансерного наблюдения за пациентом к факторам неблагоприятного прогноза следует отнести прогрессирование симптомов недостаточности кровообращения, стойкое снижение систолического артериального давления, прогрессирующую легочную гипертензию. Эти состояния требуют коррекции базового лечения. Подбор новых доз целесообразно выполнять только в стационаре.
У пациентов со стабильной недостаточностью кровообращения прогноз зависит от приверженности к назначенной полноценной базовой терапии ХСН.
Критерии оценки качества медицинской помощи
N
Критерии качества
Уровень убедительности рекомендаций
Уровень достоверности доказательства
Выполнение рекомендаций
1
Пациент с установленным диагнозом острый миокардит госпитализирован в стационар вне зависимости от тяжести течения
C
5
Да/Нет
2
Пациент с фульминантным миокардитом/тяжелыми проявлениями сердечной недостаточности госпитализирован в отделение интенсивной терапии, оснащенное аппаратами для сердечно-легочной реанимации и проведения ИВЛ
C
4
Да/Нет
3
Проведена оценка анамнеза для выявления связи с перенесенной инфекцией или других возможных этиологических факторов
C
5
Да/Нет
4
Проведена оценка семейного анамнеза для выявления наследственной отягощенности по сердечно-сосудистым и аутоиммунным заболеваниям, наличию случаев внезапной смерти среди родственников
C
5
Да/Нет
5
Проведена оценка жалоб детей раннего возраста с подозрением на миокардит: одышка, трудности при кормлении (срыгивания, отказ от еды), диспепсические явления (рвоты, диарея), стонущее, кряхтящее дыхание, повышенное потоотделение, бледность кожных покровов, слабость и адинамия; иногда цианоз, сердцебиение, обморок
C
5
Да/Нет
6
Проведена оценка жалоб детей старшего возраста с подозрением на миокардит: тахикардия, боль в грудной клетке, слабость, усталость, снижение толерантности к физической нагрузке, одышка, кашель при перемене положения тела, может быть обморок, ощущения "перебоев" в сердце, наличие острых гастроинтестинальных проявлений (тошнота, рвота, диарея), снижение аппетита
C
5
Да/Нет
7
Проведена оценка физикального и клинического обследования детей: оценка состояния, осмотр кожных покровов, измерение частоты сердечных сокращений, АД на периферических сосудах, исследование сердечно-сосудистой системы, бронхолегочной системы, исследование органов брюшной полости, оценка наличия периферических отеков
C
5
Да/Нет
8
Выполнен общий (клинический) анализ крови развернутый, исследование скорости оседания эритроцитов
C
5
Да/Нет
9
Выполнено исследование уровня C-реактивного белка в сыворотке крови
C
5
Да/Нет
10
Выполнено исследование уровня чувствительного тропонина I, T в сыворотке крови. При технической невозможности выполнения данного исследования в условиях медицинского учреждения обсуждена возможность маршрутизации анализа в другое медицинское учреждение
C
4
Да/Нет
11
Выполнено исследование уровня/активности изоферментов креатинкиназы в крови (КФК) и исследование уровня MB-фракции креатинкиназы в крови (КФК-МВ), определение активности аспартатаминотрансферазы в крови в рамках первичного обследования в качестве дополнительных при диагностике миокардита
C
5
Да/Нет
12
Выполнено исследование уровня натрийуретических пептидов (мозгового натрийуретического пептида (BNP) и/или исследование уровня N-терминального фрагмента натрийуретического пропептида мозгового (NT-proBNP) в крови
C
4
Да/Нет
13
Выполнен анализ крови биохимический общетерапевтический с определением уровня натрия, калия, общего кальция, хлоридов, общего магния, мочевины, креатинина, аспартатаминотрансферазы, аланинаминотрасферазы в крови
C
5
Да/Нет
14
Выполнена оценка кислотно-основного состояния и газов крови
C
5
Да/Нет
15
Выполнен общий (клинический) анализ мочи
C
5
Да/Нет
16
Выполнена прицельная рентгенография органов грудной клетки
C
4
Да/Нет
17
Выполнена регистрация электрокардиограммы в 12 отведениях и мониторирование электрокардиографических данных
C
5
Да/Нет
18
Выполнена эхокардиография
C
5
Да/Нет
19
Выполнено холтеровское мониторирование сердечного ритма
C
5
Да/Нет
20
Проведена магнитно-резонансной томографии сердца с контрастированием с использованием парамагнитных контрастных средств (АТХ V08CA) при наличии в медицинской организации необходимого оборудования. При технической невозможности выполнения данного исследования в условиях медицинского учреждения обсуждена возможность госпитализации пациента в другое медицинское учреждение для выполнения данного исследования
C
5
Да/Нет
21
Выполнена биопсия миокарда с проведением патолого-анатомического исследования биопсийного (операционного) материала тканей миокарда с применением электронно-микроскопических, иммуногистохимических методов и молекулярно-биологическое исследование биоптата миокарда на цитомегаловирус, вирус Эпштейна-Барр цитомегаловируса (Cytomegalovirus), вируса Эпштейна-Барр (Epstein - Barr virus), вируса герпеса 6 типа (HHV6): определение ДНК цитомегаловируса (Cytomegalovirus), вируса Эпштейна-Барр (Epstein - Barr virus), вируса герпеса 6 типа (HHV6) в биоптате миокарда методом ПЦР (качественное и количественное исследование). При технической невозможности выполнения данного исследования в условиях медицинского учреждения обсуждена возможность госпитализации пациента в другое медицинское учреждение для выполнения данного исследования
C
4
Да/Нет
22
У детей с диагнозом миокардит и проявлениями сердечной недостаточности назначена оптимальная медикаментозная терапия для коррекции сердечной недостаточности
C
5
Да/Нет
23
У детей с диагнозом миокардит и сопутствующими нарушениями ритма сердца, нуждающимися в коррекции, проведен подбор эффективного антиаритмического препарата
C
5
Да/Нет
24
У детей с диагнозом миокардит при развитии выраженной брадикардии или полной атриовентрикулярной блокады проведена оценка необходимости в проведении временной трансвенозной электрокардиостимуляции
C
5
25
У детей с диагнозом миокардит проведена терапия иммуноглобулином человека нормальным для в/в введения, терапия глюкокортикоидами и/или антитромботическими средствами
C
5
Да/Нет
26
Пациент выписан с рекомендациями диспансерного наблюдения
C
5
Да/Нет
Список литературы
1. Dasgupta S, Iannucci G, Mao C, Clabby M, Oster ME. Myocarditis in the pediatric popu-lation: A review//Congenit Heart Dis. - 2019 Sep. - Vol. 14 (5). - P. 868 - 877. doi: 10.1111/chd.12835.
2. Sagar S, Liu PP, Cooper LT Jr. Myocarditis//Lancet. - 2012 Feb. - Vol. 379(9817). - P. 738 - 747. doi: 10.1016/S0140-6736(11)60648-X
3. Caforio AL, Pankuweit S, Arbustini E, Basso C, et al. European Society of Cardiology Working Group on Myocardial and Pericardial Diseases. Current state of knowledge on aetiology, diagnosis, management, and therapy of myocarditis: a position statement of the European Society of Cardiology Working Group on Myocardial and Pericardial Diseases//European Heart Journal. - 2013 Sep. - Vol. 34(33). - P. 2636 - 2648. doi: 10.1093/eurheartj/eht210
4. Canter CE, Simpson KP. Diagnosis and Treatment of Myocarditis in Children in the Cur-rent Era//Circulation. - 2014 Jan. Vol. 129(1). - P. 115 - 128.
5.  C, Ammirati E, Bozkurt B, Caforio ALP, et al. Myocarditis and inflammatory cardiomyopathy: current evidence and future directions//Nat Rev Cardiol. - 2021 Mar. - Vol. 18 (3). - P. 169 - 193.
C, Ammirati E, Bozkurt B, Caforio ALP, et al. Myocarditis and inflammatory cardiomyopathy: current evidence and future directions//Nat Rev Cardiol. - 2021 Mar. - Vol. 18 (3). - P. 169 - 193.
6. Rroku A, Kottwitz J, Heidecker B. Update on myocarditis - what we know so far and where we may be heading//European Heart Journal. Acute Cardiovascular Care. - 2021 April. - Vol. 10 - Issue 4. - P. 455 - 467. doi.org/10.1177/2048872620910109
7. Elamm C, Fairweather D, Cooper LT. Pathogenesis and diagnosis of myocarditis//Heart. - 2012. Vol. 98. - P. 835 - 840. doi: 10.1136/heartjnl-2012-301686
8. Trachtenberg BH, Hare JM. Inflammatory cardiomyopathic syndromes//Circ Res. - 2017 - Vol. 121. - P. 803 - 818. doi.org/10.1161/CIRCRESAHA.117.310221
9. Pollack A, Kontorovich AR, Fuster V, Dec GW. Viral myocarditisdiagnosis, treatment options, and current controversies//Nat Rev Cardiol. - 2015. - Vol. 12. - P. 670 - 680. doi: 10.1038/nrcardio.2015.108
10. Karatolios K, Pankuweit S, Maisch B. Diagnosis and treatment of myocarditis: the role of endomyocardial biopsy//Curr Treat Options Cardiovasc Med. - 2007 Dec. - Vol. 9(6). - P. 473 - 81.
11. Van Linthout S,  C. Viral myocarditis: a prime example for endomyocardial bi-opsy-guided diagnosis and therapy//Curr Opin Cardiol. - 2018 May. - Vol. 33(3). - P. 325 - 333. doi: 10.1097/HCO.0000000000000515
C. Viral myocarditis: a prime example for endomyocardial bi-opsy-guided diagnosis and therapy//Curr Opin Cardiol. - 2018 May. - Vol. 33(3). - P. 325 - 333. doi: 10.1097/HCO.0000000000000515
12. Zhang M, Wang H, Tang J, He Y, Xiong T, Li W, Qu Y, Mu D. Clinical characteristics of severe neonatal enterovirus infection: a systematic review//BMC Pediatr. - 2021 Mar 15. - Vol. 21 (1). - P. 127. doi: 10.1186/s12887-021-02599-y
13. Maki S, Aizawa Y, Ito Y, Suda M, Saitoh A. Acute heart failure due to dilated cardio-myopathy exacerbated by systemic parechovirus A1 infection in an infant//Int J Infect Dis. - 2021 Mar. - Vol. 104. - P. 273 - 275. doi: 10.1016/j.ijid.2021.01.021
14. Verdonschot J, Hazebroek M, Merken J, et al. Relevance of cardiac parvovirus B19 in myocarditis and dilated cardiomyopathy: review of the literature//Eur J Heart Fail 2016. - Vol. 18 (12). - P. 1430 - 1441. doi: 10.1002/ejhf.665
15. Bejiqi R, Retkoceri R, Maloku A, Mustafa A, et al. The Diagnostic and Clinical Approach to Pediatric Myocarditis: A Review of the Current Literature//Open Access Maced J Med Sci. - 2019 Jan 4. - Vol. 7(1). - P. 162 - 173. doi: 10.3889/oamjms.2019.010
16. Molina KM, Garcia X, Denfield SW, Fan Y, Morrow WR, Towbin JA, Frazier EA, Nelson DP. Parvovirus B19 myocarditis causes significant morbidity and mortality in chil-dren//Pediatr Cardiol. - 2013. - Vol. 34. - P. 390 - 397. doi: 10.1007/s00246-012-0468-4
17. McMurray JC, May JW, Cunningham MW, Jones OY. Multisystem Inflammatory Syndrome in Children (MIS-C), a Post-viral Myocarditis and Systemic Vasculitis-A Critical Review of Its Pathogenesis and Treatment//Front Pediatr. - 2020 Dec 16. - Vol. 8. - P. 626182. doi: 10.3389/fped.2020.626182
18. Dhar D, Dey T, Samim MM, Padmanabha H, Chatterjee A, Naznin P, Chandra SR, Mallesh K, Shah R, Siddiqui S, Pratik K, Ameya P, Abhishek G. Systemic inflammatory syndrome in COVID-19-SISCoV study: systematic review and metaanalysis//Pediatr Res. - 2021 May. - Vol. 18. - P. 1 - 16.
19. Bellissima BL, Vara A, Helsby N, Garavan F, Tingle MD. Incidence and investigation of potential risk-factors for clozapine-associated myocarditis and cardiomyopathy in a New Zealand cohort//Psychiatry Res. - 2021 May. - Vol. 299. - P. 113873. DOI: 10.1016/j.psychres.2021.113873
20. Curigliano G, Cardinale D, Suter T, Plataniotis G, et al. ESMO Guidelines Working Group. Cardiovascular toxicity induced by chemotherapy, targeted agents and radiother-apy: ESMO Clinical Practice Guidelines//Ann Oncol. - 2012 Oct. - 23 Suppl 7. - vii155 - 66. doi: 10.1093/annonc/mds293
21. Curigliano G, Lenihan D, Fradley M, et al. ESMO Guidelines Committee. Management of cardiac disease in cancer patients throughout oncological treatment: ESMO consensus recommendations//Ann Oncol. - 2020 Feb. Vol. 31(2). - P. 171 - 190.
22. Gauntt C. Coxsackievirus experimental heart diseases//Front. Biosci. - 2003. - Vol. 8 (5). - e23 - 35. Doi: 10.2741/928
23. Engler R.J.M. et al. A Prospective Study of the Incidence of Myocarditis/Pericarditis and New Onset Cardiac Symptoms following Smallpox and Influenza Vaccination//PLOS ONE/ed. Horwitz M.S. - 2015. - Vol. 10 (3). - e0118283. doi.org/10.1371/journal.pone.0118283
24. Mason J.W. Myocarditis and dilated cardiomyopathy: an inflammatory link//Cardiovasc. Res. - 2003. - Vol. 60 (1). - P. 5 - 10. doi: 10.1016/s0008-6363(03)00437-1
25. Calabrese F., Thiene G. Myocarditis and inflammatory cardiomyopathy: microbiological and molecular biological aspects//Cardiovasc. Res. - 2003. - Vol. 60 (1). - P. 11 - 25. doi: 10.1016/s0008-6363(03)00475-9
26. Baggio C, Gagno G, Porcari A .et al. Myocarditis: Which Role for Genetics?//Curr Car-diol Rep. - 2021. - Vol. 23 (6). - P. 58 - 63. doi: 10.1007/s11886-021-01492-5
27. Artico J, Merlo M, Delcaro G, .et al. Lymphocytic myocarditis: a genetically predisposed disease?//J Am Coll Cardiol. - 2020. - Vol. 75. - P. 3098 - 3100. doi: 10.1016/j.jacc.2020.04.048
28. Ammirati E, Frigerio M, Adler ED, et al. Management of Acute Myocarditis and Chronic Inflammatory Cardiomyopathy: An Expert Consensus Document//Circ Heart Fail. - 2020 Nov. - Vol. 13(11). - e007405. doi.org/10.1161/CIRCHEARTFAILURE.120.007405
29. Caforio ALP, Malipiero G, Marcolongo R, Iliceto S. Myocarditis: A Clinical Overview//Curr Cardiol Rep. - 2017. - Vol. 19. - P. 63. doi: 10.1007/s11886-017-0870-x
30. Chang Y-J, Hsiao H-J, Hsia S-H, et al. Analysis of clinical parameters and echocardiography as predictors of fatal pediatric myocarditis//PLoS ONE. - 2019. - Vol. 14(3). - e0214087. doi.org/10.1371/journal.pone.0214087
31. Matsuura H, Ichida F, Saji T, et al. Clinical features of acute and fulminant myocarditis in children//Circ J. - 2016. - Vol. 80 (11). - P. 2362 - 2368. doi: 10.1253/circj.CJ-16-0234
32. Arola A, Pikkarainen E.et al. Occurrence and Features of Childhood Myocarditis: A Nationwide Study in Finland//J Am Heart Assoc. - 2017 Nov. - Vol. 6(11). - e005306. doi: 10.1161/JAHA.116.005306
33. Lipshultz SE, Sleeper LA, Towbin JA, et al. The incidence of pediatric cardiomyopathy in two regions of the United States//N Engl J Med. - 2003 Apr. - Vol. 348. - P. 1647 - 1655. DOI: 10.1056/NEJMoa021715
34. Myocarditis Foundation. Myocarditis in children: incidence, clinical characteristics and outcomes//-Published July 29. 2020. Accessed November 15, 2020. https://www.myocarditisfoundation.org/myocarditis-in-children-incidence-clinical-characteristics-and-outcomes/
35. Butts RJ, Boyle GJ, Deshpande SR, et al. Characteristics of clinically diagnosed pediatric myocarditis in a contemporary multicenter cohort//Pediatr Cardiol. - 2017. - Vol. 38(6). - P. 1175 - 1182. doi: 10.1007/s00246-017-1638-1
36. Ghelani SJ, Spaeder MC, Pastor W, Spurney CF, Klugman D (2012) Demographics, trends, and outcomes in pediatric acute myocarditis in the United States, 2006 to 2011//Circ Cardiovasc Qual Outcomes. - 2012 Sep. - Vol. 5(5). - P. 622 - 627. doi: 10.1161/CIRCOUTCOMES.112.965749
37. Klugman D, Berger JT, Sable CA, He J, et al. Pediatric patients hospitalized with myo-carditis: a multiinstitutional analysis//Pediatr Cardiol. - 2010. - Vol. 31. - P. 222 - 228. doi: 10.1007/s00246-009-9589-9
38. Durani Y, Giordano K, Goudie BW. Myocarditis and pericarditis in children//Pediatr Clin North Am. - 2010. - Vol. 57. - P. 1281 - 1303.
39. Neagu O,  AF, Callon D,
AF, Callon D,  L, Cohen MC. Myocarditis Presenting as Sudden Death in Infants and Children: A Single Centre Analysis by ESGFOR Study Group//Pediatr Dev Pathol. - 2021 Apr. - Vol. 19. - P. 10935266211007262. doi: 10.1016/j.pcl.2010.09.012
L, Cohen MC. Myocarditis Presenting as Sudden Death in Infants and Children: A Single Centre Analysis by ESGFOR Study Group//Pediatr Dev Pathol. - 2021 Apr. - Vol. 19. - P. 10935266211007262. doi: 10.1016/j.pcl.2010.09.012
40. Meyer L, Stubbs B, Fahrenbruch C, Maeda C, et al. Incidence, causes, and survival trends from cardiovascular-related sudden cardiac arrest in children and young adults 0 to 35 years of age: a 30-year review//Circulation. - 2012 Sep 11. - Vol. 126(11). - P. 1363 - 72.
41. Nugent AW, Daubeney PE, Chondros P, et al. National Australian Childhood Cardiomyopathy Study. The epidemiology of childhood cardiomyopathy in Australia//N Engl J Med. - 2003 Apr 24. - Vol. 348(17). - P. 1639 - 46. Accessed January 14, 2020. doi: 10.1161/CIRCULATIONAHA.111.076810
42. Vetter VL, Covington TM, Dugan PN, Haley DM, MPH, Dykstra H, Overpeck M et al. Cardiovascular deaths in children: General overview from the National Center for the Review and Prevention of Child Deaths//Am Heart J. - 2015. - Vol. 169(3). - P. 426 - 437.
43. Lv J, Han B, Wang C, Wang J, Jiang D, Zhao L, Yi Y, Zhang J. The Clinical Features of Children With Acute Fulminant Myocarditis and the Diagnostic and Follow-Up Value of Cardiovascular Magnetic Resonance//Front Pediatr. - 2019 Oct. - Vol. 7. - P. 388. doi: 10.3389/fped.2019.00388
44. Winkel BG, Risgaard B, Sadjadieh G, et al. Sudden cardiac death in children (1 - 18 years): symptoms and causes of death in a nationwide setting//Eur Heart J 2014. - Vol. 35. - P. 868 - 875. doi: 10.1093/eurheartj/eht509
45. Bohm P, Scharhag J, Meyer T. Data from a nationwide registry on sportsrelated sudden cardiac deaths in Germany//Eur J Prev Cardiol. - 2016 Apr. - Vol. 23(6). - P. 649 - 56. doi: 10.1177/2047487315594087
46. Lieberman EB, Hutchins GM, Herskowitz A, Rose NR, Baughman KL. Clinicopathologic description of myocarditis//J Am Coll Cardiol. - 1991 Dec. - Vol. 18(7). - P. 1617 - 26. doi: 10.1016/0735-1097(91)90493-s
47. Ginsberg F, Parrillo JE. Fulminant myocarditis//Crit Care Clin. - 2013. - Vol. 29. - P. 465 - 483. doi: 10.1016/j.ccc.2013.03.004
48. Sinagra G, Anzini M, Pereira NL, Bussani R, Finocchiaro G, Bartunek J, Merlo M. Myocarditis in Clinical Practice//Mayo Clin Proc. - 2016 Sep. - Vol. 91(9). - P. 1256 - 66. doi: 10.1016/j.mayocp.2016.05.013
49. Abe T, Tsuda E, Miyazaki A, et al. Clinical characteristics and longterm outcome of acute myocarditis in children//Heart Vessels. - 2013. - Vol. 28(5). - P. 632 - 8. doi: 10.1007/s00380-012-0296-8
50. Degener F, Opgen-Rhein B,  M, et al. Four-Year Experience of the German Multicenter Registry for Pediatric Patients with Suspected Myocarditis: MYKKE//In: 50th Annual Meeting of the German Society for Pediatric Cardiology (DGPK). - 2018. - Vol 66. Georg Thieme Verlag KG. doi: 10.1055/s-0038-1628324
M, et al. Four-Year Experience of the German Multicenter Registry for Pediatric Patients with Suspected Myocarditis: MYKKE//In: 50th Annual Meeting of the German Society for Pediatric Cardiology (DGPK). - 2018. - Vol 66. Georg Thieme Verlag KG. doi: 10.1055/s-0038-1628324
51. Niu L, An X-J, Tian J, et al. 124 cases of clinical analysis of children with viral myocarditis//Eur Rev Med Pharmacol Sci. - 2015. - Vol. 19(15). - P. 2856 - 9.
52. Price S, Bodys A, Celinska A, et al. Interlibrary Loan The value of chosen diagnostic tools in evaluating myocarditis in children and adolescents//Pediatr Pol J Paediatr. - 2018. - Vol. 93(5). - P. 389 - 95.
53. Rodriguez-Gonzalez M, Sanchez-Codez MI, Lubian-Gutierrez M, et al. Clinical presentation and early predictors for poor outcomes in pediatric myocarditis: A retrospective study//World J Clin Cases. - 2019. - Vol. 7(5). - P. 548 - 61. doi: 10.12998/wjcc.v7.i5.548
54. Suthar D, Dodd DA, Godown J. Identifying Noninvasive Tools to Distinguish Acute Myocarditis from Dilated Cardiomyopathy in Children//Pediatr Cardiol. - 2018. - Vol. 39(6). - P. 1134 - 8. doi: 10.1007/s00246-018-1867-y
55. Wu HP, Lin MJ, Yang WC, et al. Predictors of Extracorporeal Membrane Oxygenation Support for Children with Acute Myocarditis//Biomed Res Int. - 2017 May. - Vol. 2017. - P. 8. doi.org/10.1155/2017/2510695
56. Freund MW, Kleinveld G, Krediet TG, et al. Prognosis for neonates with enterovirus myocarditis//Arch Dis Child Fetal Neonatal Ed. - 2010 May. - Vol. 95(3). - F206 - 12. doi: 10.1136/adc.2009.165183.
57. Putschoegl A, Auerbach S. Diagnosis, Evaluation, and Treatment of Myocarditis in Chil-dren//Pediatr Clin N Am. - 2020 Oct. - Vol. 67(5). - P. 855 - 874. doi: 10.1016/j.pcl.2020.06.013
58. Tunuguntla H, Jeewa A, Denfield SW. Acute Myocarditis and Pericarditis in Children//Pediatr Rev. - 2019. - Vol. 40(1). - P. 14 - 25. doi: 10.1542/pir.2018-0044
59. Levine MC, Klugman D, Teach SJ. Update on myocarditis in children//Curr Opin Pediatr. - 2010. - Vol. 22. - P. 278 - 283. doi: 10.1097/MOP.0b013e32833924d2
60. Freedman SB, Haladyn JK, Floh A, Kirsh JA, Taylor G, Thull-Freedman J. Pediatric my-ocarditis: emergency department clinical findings and diagnostic evaluation//Pediatrics. - 2007. - Vol. 120(6). - P. 1278 - 1285. doi: 10.1542/peds.2007-1073
61. Schubert S, Opgen-Rhein B, Boehne M, Weigelt A, et al. MYKKE consortium. Severe heart failure and the need for mechanical circulatory support and heart transplantation in pediatric patients with myocarditis: Results from the prospective multicenter registry "MYKKE"//Pediatr Transplant. - 2019 Nov. - Vol. 23(7). - e13548. doi.org/10.1111/petr.13548
62. Howard A., Hasan A., Brownlee J., Mehmood N., Ali M., et al. Pediatric Myocarditis Protocol: An Algorithm for Early Identification and Management with Retrospective Analysis for Validation//Pediatric Cardiology. - 2020 Feb. - Vol. 41. - P. 316 - 326. doi: 10.1007/s00246-019-02258-1
63. Kantor, P. F., Lougheed, J., Dancea, A., et al. Presentation, diagnosis, and medical management of heart failure in children: Canadian cardiovascular society guidelines//Canadian Journal of Cardiology. - 2013. - Vol. 29(12). - P. 1535 - 1552. doi: 10.1016/j.cjca.2013.08.008
64. Bergmann KR, Kharbanda A, Haveman L Myocarditis and Pericarditis In The Pediatric Patient: Validated Management Strategies//Pediatr Emerg Med Pract. - 2015 Jul. - Vol. 12(7). - P. 1 - 22; quiz 23.
65. Kern J, Modi R, Atalay MK, Kochilas LK. Clinical myocarditis masquerading as acute coronary syndrome//J Pediatr. - 2009 Apr. - Vol. 154(4). - P. 612 - 5. doi: 10.1016/j.jpeds.2008.10.018
66. Cooper LT Jr. Ventricular Arrhythmias and Sudden Cardiac Death in Lymphocytic Myocarditis//J Am Coll Cardiol. - 2020 Mar 10. - Vol. 75(9). - P. 1058 - 1060. doi: 10.1016/j.jacc.2020.01.032
67. Ling N, Li CL, Wang ZZ, Zhang HN, Xu H, An XJ. Heart rate variability in children with myocarditis presenting with ventricular arrhythmias//Eur Rev Med Pharmacol Sci. - 2018 Feb. - Vol. 22(4). - P. 1102 - 1105. doi: 10.26355/eurrev_201802_14397
68. Школьникова М.А., Алексеева Е.И. Клинические рекомендации по детской кардиологии и ревматологии//М. - 2011. - с. 512.
69. Brady WJ, Ferguson JD, Ullman EA, Perron AD. Myocarditis: emergency department recognition and management//Emerg Med Clin North Am. - 2004 Nov. - Vol. 22(4). - P. 865 - 85. doi: 10.1016/j.emc.2004.05.010
70. Балыкова Л.А., Краснопольская А.В., Власова Е.А. Миокардиты у детей: клиническая картина, диагностика и лечение//Педиатрическая фармакология. - 2020. - N 17(2). - С. 137 - 147.
71. Patel M.S., Berg A.M., Vincent R.N., Mahle W.T. Serum parameters and echocardiographic predictors of death or need for transplant in newborns, children, and young adults with heart failure//Am J Cardiol. - 2010. - Vol. 105. - P. 1798 - 1801. doi: 10.1016/j.amjcard.2010.01.357
72. Brambatti M, Matassini MV, Adler ED, Klingel K, Camici PG, Ammirati E. Eosinophilic myocarditis: characteristics, treatment, and outcomes//J Am Coll Cardiol. - 2017. - Vol. 70. - P. 2363 - 2375.
73. Lippi G, Salvagno GL, Guidi GC. Cardiac troponins in pediatric myocarditis//Pediatrics. - 2008. - Vol. 121(4). - P. 864. doi: 10.1542/peds.2008-0031
74. ![]() U., Pauschinger M., et.al. High prevalence of viral genomes and multiple viral infections in the myocardium of adults with "idiopathic" left ventricular dysfunction//Circulation. - 2005 Feb 22. - Vol. 111(7). - P. 887 - 93. doi.org/10.1161/01.CIR.0000155616.07901.35
U., Pauschinger M., et.al. High prevalence of viral genomes and multiple viral infections in the myocardium of adults with "idiopathic" left ventricular dysfunction//Circulation. - 2005 Feb 22. - Vol. 111(7). - P. 887 - 93. doi.org/10.1161/01.CIR.0000155616.07901.35
75. Masarone D, Valente F, Rubino M, Vastarella R, et.al. Pediatric Heart Failure: A Practi-cal Guide to Diagnosis and Management//Pediatr Neonatol. - 2017 Aug. - Vol. 58(4). - P. 303 - 312. doi: 10.1016/j.pedneo.2017.01.001
76. Kirk R, Dipchand AI, Rosenthal DN, et al. The International Society for Heart and Lung Transplantation Guidelines for the management of pediatric heart failure: Executive summary//J Heart Lung Transplant. - 2014. - Vol. 33. - P. 888 - 909. doi: 10.1016/j.healun.2014.06.002
77. JCS Joint Working Group. Guidelines for diagnosis and treatment of myocarditis (JCS 2009): digest version//Circ. J. Off. J. Jpn. Circ. Soc. - 2011. - Vol. 75 (3). - P. 734 - 743. doi: 10.1253/circj.cj-88-0008
78. McNamara D M. Heart Failure as a Consequence of Viral and Nonviral Myocarditis Heart Failure: A Companion to Braunwald's Heart Disease//Elsevier. - 2020. - Vol. 28. - P. 376 - 384.e3
79. Vigneswaran TV, Brown JR, Breuer J, Burch M. Parvovirus B19 myocarditis in children: an observational study//Arch Dis Child. - 2016 Feb. - Vol. 101(2). - P. 177 - 80. doi: 10.1136/archdischild-2014-308080
80. Tuthar D, Dodd DA, Godown J. Identifying Non-invasive Tools to Distinguish Acute Myocarditis from Dilated Cardiomyopathy in Children//PediatrCardiol. - 2018. - Vol. 39(6). - P. 1134 - 8.
81. Foerster SR, Canter CE, Cinar A, et al Ventricular remodeling and survival are more favorable for myocarditis than for idiopathic dilated cardiomyopathy in childhood//Circ Heart Fail. - 2010. - Vol. 3. - P. 689 - 697. doi: 10.1161/CIRCHEARTFAILURE.109.902833
82. Felker GM, Boehmer JP, Hruban RH et al Echocardiographic fndings in fulminant and acute myocarditis//J Am Coll Cardiol. - 2000. - Vol. 36(1). - P. 227 - 32. doi: 10.1016/s0735-1097(00)00690-2.
83. Gursu HA, Cetin AE, Kibar AE, et al The assessment of treatment outcomes in patients with acute viral myocarditis by speckle tracking and tissue Doppler methods//Echocardiography. - 2019. - Vol. 36. - P. 1666 - 1674. doi: 10.1111/echo.14449.
84. Wisotzkey BL, Soriano, BD, Albers, EL, et al Diagnostic role of strain imaging in atypical myocarditis by echocardiography and cardiac MRI//Pediatr Radiol. - 2018. - Vol. 48. - P. 835 - 842. doi: 10.1007/s00247-017-4061-0
85. Khoo NS, Smallhorn, JF, Atallah, J, et al Altered left ventricular tissue velocities, deformation and twist in children and young adults with acute myocarditis and normal ejection fraction//J Am Soc Echocardiogr. - 2012. - Vol. 25. - P. 294 - 303. doi: 10.1016/j.echo.2011.10.010
86. Banka P, Robinson JD, Uppu SC, Harris MA, et al. Cardiovascular magnetic resonance techniques and findings in children with myocarditis: a multicenter retrospective study//Journal of cardiovascular magnetic resonance: official journal of the Society for Cardiovascular Magnetic Resonance. - 2015. - Vol. 17. - P. 96. doi: 10.1186/s12968-015-0201-6.
87. Friedrich MG, Sechtem U, Schulz-Menger J, et al.; International Consensus Group on Cardiovascular Magnetic Resonance in Myocarditis. Cardiovascular magnetic resonance in myocarditis: a JACC white paper//J Am Coll Cardiol. - 2009. - Vol. 53. - P. 1475 - 1487. doi: 10.1016/j.jacc.2009.02.007
88. Pan JA, Lee YJ, Salerno M. Diagnostic performance of extracellular volume, native T1, and T2 mapping versus lake louise criteria by cardiac magnetic resonance for detection of acute myocarditis: a meta-analysis//Circ Cardiovasc Imaging. - 2018. - Vol. 11. - e007598. doi: 10.1161/CIRCIMAGING.118.007598
89. Wei S, Fu J, Chen L, Yu S. Performance of Cardiac Magnetic Resonance Imaging for Diagnosis of Myocarditis Compared with Endomyocardial Biopsy: A Meta-Analysis//Med Sci Monit. - 2017. - Vol. 23. - P. 3687 - 3696. doi: 10.12659/msm.902155
90. Kotanidis CP, Bazmpani MA, Haidich AB, Karvounis C, Antoniades C, Karamitsos TD. Diagnostic accuracy of cardiovascular magnetic resonance in acute myocarditis: A Sys-tematic Review and Meta-Analysis//J Am Coll Cardiol Img. - 2018. - Vol. 11(11). - P. 1583 - 90. doi: 10.1016/j.jcmg.2017.12.008
91. Ferreira VM, Schulz-Menger J, Holmvang G, Kramer CM, Carbone I, Sechtem U, Kin-dermann I, Gutberlet M, Cooper LT, Liu P, et al. Cardiovascular magnetic resonance in nonischemic myocardial inflammation: expert recommendations//J Am Coll Cardiol. - 2018. - Vol. 72. - P. 3158 - 3176.
92. Messroghli DR, Moon JC, Ferreira VM, Grosse-Wortmann L, He T, Kellman P, et al. Clinical recommendations for cardiovascular magnetic resonance mapping of T1, T2, T2* and extracellular volume: a consensus statement by the Society for Cardiovascular Mag-netic Resonance (SCMR) endorsed by the European Association for Cardiovascular Im-aging (EACVI)//J Cardiovasc Magn Reson. - 2017. - Vol. 19(1). - P. 75.
93. Cornicelli M.D., Rigsby, C.K., Rychlik, K. et al. Diagnostic performance of cardiovascular magnetic resonance native T1 and T2 mapping in pediatric patients with acute myo-carditis//J Cardiovasc Magn Reson. - 2019. - Vol. 21 (1). - P. 40. doi: 10.1186/s12968-019-0550-7
94. Luetkens JA, Faron A, Isaak A, Dabir D, Kuetting D, et al. Comparison of original and 2018 lake louise criteria for diagnosis of acute myocarditis: results of a validation cohort//Radiology: Cardiothoracic Imaging. - 2019. - Vol. 1. - e190010. doi.org/10.1148/ryct.2019190010
95. Francone M, et al. CMR sensitivity varies with clinical presentation and extent of cell ne-crosis in biopsyproven acute myocarditis//JACC Cardiovasc. Imaging. - 2014. - Vol. 7. - P. 254 - 263. doi: 10.1016/j.jcmg.2013.10.011
96. ![]()
![]() A,
A,  H,
H,  M, et al. Children With Acute Myocarditis Often Have Persistent Subclinical Changes as Revealed by Cardiac Magnetic Resonance//J Magn Reson Imaging. - 2020 Aug. - Vol. 52(2). - P. 488 - 496.
M, et al. Children With Acute Myocarditis Often Have Persistent Subclinical Changes as Revealed by Cardiac Magnetic Resonance//J Magn Reson Imaging. - 2020 Aug. - Vol. 52(2). - P. 488 - 496.
97. Aquaro GD, Ghebru Habtemicael Y, Camastra G, Monti L, Dellegrottaglie S, Moro C, Lanzillo C, Scatteia A, Di Roma M, Pontone G, et al.; "Cardiac Magnetic Resonance" Working Group of the Italian Society of Cardiology. Prognostic value of repeating cardi-ac magnetic resonance in patients with acute myocarditis//J Am Coll Cardiol. - 2019. - Vol. 74. - P. 2439 - 2448.
98. ![]() C, Eichhorn C,
C, Eichhorn C, ![]() L, Murthy VL, Agarwal V, Kaneko K, Cuddy S, Aghayev A, Steigner M, Blankstein R, et al. Prognostic value of cardiac magnetic resonance tissue characterization in risk stratifying patients with suspected myocarditis//J Am Coll Cardiol. - 2017. - Vol. 70. - P. 1964 - 1976. DOI: 10.1016/j.jacc.2017.08.050
L, Murthy VL, Agarwal V, Kaneko K, Cuddy S, Aghayev A, Steigner M, Blankstein R, et al. Prognostic value of cardiac magnetic resonance tissue characterization in risk stratifying patients with suspected myocarditis//J Am Coll Cardiol. - 2017. - Vol. 70. - P. 1964 - 1976. DOI: 10.1016/j.jacc.2017.08.050
99. Berg J, et al. Cardiac magnetic resonance imaging in myocarditis reveals persistent disease activity despite normalization of cardiac enzymes and inflammatory parameters at 3-month follow-up//Circ. Heart. - 2017. - Vol. 10. - e004262. doi: 10.1161/CIRCHEARTFAILURE.117.004262
100. Rangamani S, Varghese J, Li L, Harvey L, et al. Safety of cardiac magnetic resonance and contrast angiography for neonates and small infants: a 10-year single-institution experience//Pediatr Radiol. - 2012 Nov. - Vol. 42(11). - P. 1339 - 46. DOI: 10.1007/s00247-012-2452-9
101. Jain R, Petrillo-Albarano T, Parks WJ, et al. Efficacy and safety of deep sedation by nonanesthesiologists for cardiac MRI in children//Pediatr Radiol. - 2013 Mar. - Vol. 43(5). - P. 605 - 11. doi: 10.1007/s00247-012-2566-0
102. Schmitz A, Weiss M, Kellenberger C, O'Gorman Tuura R, et al. Sedation for mag-netic resonance imaging using propofol with or without ketamine at induction in pediat-rics-A prospective randomized double-blinded study//Paediatr Anaesth. - 2018 Mar. - Vol. 28(3). - P. 264 - 274. doi: 10.1111/pan.13315
103. Bussani R, Silvestri F, Perkan A, et al. Endomyocardial Biopsy. 2019 May 18. In: Sinagra G, Merlo M, Pinamonti B, editors. Dilated Cardiomyopathy: From Genetics to Clinical Management [Internet]//Cham (CH): Springer. - 2019. - Chapter 9.
104. Katzmann JL, Schlattmann P, Rigopoulos AG, et al Metaanalysis on the im-munohistological detection of inflammatory cardiomyopathy in endomyocardial biopsies//Heart Fail Rev. - 2020 Mar. - Vol. 25(2). - P. 277 - 294. doi: 10.1007/s10741-019-09835-9
105. Baughman KL. Diagnosis of myocarditis: death of Dallas criteria//Circulation. - 2006 Jan 31. - Vol. 113(4). - P. 593 - 5. doi.org/10.1161/CIRCULATIONAHA.105.589663
106. Cooper LT, Baughman KL, Feldman AM, et al American Heart Association; American College of Cardiology; European Society of Cardiology; Heart Failure Society of America; Heart Failure Association of the European Society of Cardiology. The role of endomyocardial biopsy in the management of cardiovascular disease: a scientific state-ment from the American Heart Association, the American College of Cardiology, and the European Society of Cardiology. Endorsed by the Heart Failure Society of America and the Heart Failure Association of the European Society of Cardiology//J Am Coll Cardi-ol. - 2007 Nov 6. - Vol. 50(19). - P. 1914 - 31. doi: 10.1016/j.jacc.2007.09.008
107. Bowles N.E., Ni J., Kearney D.L., et al. Detection of viruses in myocardial tissues by polymerase chain reaction: evidence of adenovirus as a common cause of myocarditis in children and adults//J Am Coll Cardiol. - 2003. - Vol. 42. - P. 466 - 472. doi: 10.1016/s0735-1097(03)00648-x.
108. Ponikowski P, Voors A, Anker S, et al. ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure: The Task Force for the diagnosis and treat-ment of acute and chronic heart failure of the European Society of Cardiology (ESC) Developed with the special contribution of the Heart Failure Association (HFA) of the ESC//Eur Heart J. - 2016 Jul 14. - Vol. 37(27). - P. 2129 - 2200. doi.org/10.1093/eurheartj/ehw128
109. Ahmed H, VanderPluym C. Medical management of pediatric heart failure//Car-diovasc Diagn Ther. - 2021. - Vol. 11(1). - P. 323 - 335. doi: 10.21037/cdt-20-358
110. Das BB. Current State of Pediatric Heart Failure//Children (Basel). - 2018. - Vol. 5(7). - P. 88. doi: 10.3390/children5070088
111. Laghlam D, Benghanem S, Ortuno S, et al. Management of cardiogenic shock: a narrative review.//Ann Intensive Care. - 2024. - Vol. 14(1). - P. 45. doi: 10.1186/s13613-024-01260-y
112. Wooldridge G, Hitayezu J, Venkatasubbu P. Paediatric cardiogenic shock.//Up-date in Anaesthesia. - 2021 doi: 10.1029/WFSA-D-19-00022
113. Koentartiwi D, Candini N, Suwarnianty R. Management of cardiogenic shock in pediatric patients.//Islamic Health Journal. - 2020. - Vol. 9 (2) - P. 60 - 82. doi: 10.33474/jki.v9i2.8891
114. Rossano JW, Kim JJ, Decker JA, et al. Prevalence, morbidity, and mortality of heart failurerelated hospitalizations in children in the United States: a population-based study//J Card Fail. - 2012. - Vol. 18. - P. 459 - 70. doi: 10.1016/j.cardfail.2012.03.001
115. Chioncel O, Parissis J, Mebazaa A, Thiele H et al. Epidemiology, pathophysiology and contemporary management of cardiogenic shock - a position statement from the Heart Failure Association of the European Society of Cardiology//Eur J Heart Fail. - 2020 Aug. - Vol. 22(8). P. 1315 - 1341. doi: 10.1002/ejhf.1922
116. Law YM, Lal AK, Chen S,  D et al. American Heart Association Pediatric Heart Failure and Transplantation Committee of the Council on Lifelong Congenital Heart Disease and Heart Health in the Young and Stroke Council. Diagnosis and Man-agement of Myocarditis in Children: A Scientific Statement From the American Heart Association//Circulation. - 2021 Aug 10. - Vol. 144(6). - e123 - 135. doi: 10.1161/CIR.0000000000001001
D et al. American Heart Association Pediatric Heart Failure and Transplantation Committee of the Council on Lifelong Congenital Heart Disease and Heart Health in the Young and Stroke Council. Diagnosis and Man-agement of Myocarditis in Children: A Scientific Statement From the American Heart Association//Circulation. - 2021 Aug 10. - Vol. 144(6). - e123 - 135. doi: 10.1161/CIR.0000000000001001
117. Caviedes BP, et al. Dilated cardiomyopathy and severe heart failure. An update for pediatricians//Arch Argent Pediatr. - 2018 Jun 1. - Vol. 116(3). - e421 - 428. doi: 10.5546/aap.2018.eng.e421.
118. Miller TL, Neri D, Extein J, Somarriba G, Strickman-Stein N. Nutrition in Pediat-ric Cardiomyopathy//Prog Pediatr Cardiol. - 2007. - Vol. 24(1). P. 59 - 71. doi: 10.1016/j.ppedcard.2007.08.007
119. Лазарев В.В. Особенности детского организма/В.В. Лазарев//Интенсивная терапия: Национальное руководство/под ред. Б.Р. Гельфанда, А.И. Салтанова. - Москва: ГЭОТАРМедиа, 2009. - С. 490 - 505
120. Matsumori A, Igata H, Ono K, Iwasaki A, Miyamoto T, Nishio R, Sasayama S. High doses of digitalis increase the myocardial production of proinflammatory cytokines and worsen myocardial injury in viral myocarditis: a possible mechanism of digitalis toxicity//Jpn Circ J. - 1999. - Vol. 63. - P. 934 - 940.2 doi: 10.1253/jcj.63.934
121. Савенкова М.С., Вашура Л.В., Абдулаев А.К., Анджель А.Е., Балакирева Г.М., Румянцева И.Г., Кузнецова Е.С. Значение герпесвирусных инфекций у детей//Педиатрия. Журнал им. Г.Н. Сперанского. - 2016. - N 2. - С. 134 - 141
122. Pinninti SG, Kimberlin DW. Preventing herpes simplex virus in the newborn//Clin Perinatol. - 2014 Dec. - Vol. 41(4). - P. 945 - 55. doi: 10.1016/j.clp.2014.08.012.
123. 120 Harris JB, Holmes AP. Neonatal Herpes Simplex Viral Infections and Acy-clovir: An Update//J Pediatr Pharmacol Ther. - 2017. - Vol. 22(2). - P. 88 - 93. doi: 10.5863/1551-6776-22.2.88.
124. Васичкина Е.С., Балыкова Л.А., Басаргина Е.Н., Брегель Л.В., Дегтярева Е.А., Ковалев И.А., Котлукова Н.П., Леонтьева И.В., Яковлева Л.В., Грознова О.С. Миокардиты у детей. Современные подходы к лечению и реабилитации.//Вопросы практической педиатрии. - 2024; - N 19(6). - С. 110 - 122. doi: 10.20953/1817-7646-2024-6-110-122
125. Lim Y, Lyall H. Congenital cytomegalovirus - who, when, what-with and why to treat?//J Infect. - 2017 Jun. - 74 Suppl 1. - S89 - S94. doi: 10.1016/S0163-4453(17)30197-4
126. 122 Luck SE, Wieringa JW,  D, Henneke P, et al. ACTM; ES-PID Congenital CMV Group Meeting, Leipzig 2015. Congenital Cytomegalovirus: A Eu-ropean Expert Consensus Statement on Diagnosis and Management//Pediatr Infect Dis J. - 2017 Dec. - Vol. 36(12). - P. 1205 - 1213. doi: 10.1097/INF.0000000000001763.
D, Henneke P, et al. ACTM; ES-PID Congenital CMV Group Meeting, Leipzig 2015. Congenital Cytomegalovirus: A Eu-ropean Expert Consensus Statement on Diagnosis and Management//Pediatr Infect Dis J. - 2017 Dec. - Vol. 36(12). - P. 1205 - 1213. doi: 10.1097/INF.0000000000001763.
127. Rawlinson WD, Boppana SB, Fowler KB, Kimberlin DWet al.Congenital cytomegalovirus infection in pregnancy and the neonate: consensus recommendations for prevention, diagnosis, and therapy//Lancet Infect Dis. - 2017 Jun. - Vol. 17(6). - e177 - 188. doi: 10.1016/S1473-3099(17)30143-3
128. Maisch B, Pankuweit S. Current treatment options in (peri)myocarditis and inflammatory cardiomyopathy//Herz. - 2012. - Vol. 37. - P. 644 - 656. doi: 10.1007/s00059-012-3679-9.
129. Понежева Ж.Б., Гришаева А.А., Попова Т.И. Клинические формы вирусной инфекции Эпштейна - Барр//РМЖ. - 2019. - N 10. - С. 36 - 41.
130. Шестакова И.В. Лечить или не лечить Эпштейна-Барр вирусную инфекцию: подробный обзор различных тактик//Инфекционные болезни: Новости. Мнения. Обучение. - 2013. - N 3 (4). - С. 12 - 23
131. Никитина И.Л., Вершинина Т.Л. Миокардит у детей: проблемы и решения.//Медицинский Совет. - 2017. - N 1ю - С. 238 - 245. doi: 10.21518/2079-701X-2017-1-238-245
132. Dennert R, Velthuis S, Schalla S, et al. Intravenous immunoglobulin therapy for patients with idiopathic cardiomyopathy and endomyocardial biopsy-proven high PVB19 viral load//Antivir Ther. - 2010. - Vol. 15 (2). - P. 193 - 201. doi: 10.3851/IMP1516
133. Чернова Т.М., Тимченко В.Н., Павлова Е.Б., Баракина Е.В., Субботина М.Д. Парвовирусная В19 инфекция: Лекция//Детские инфекции. - 2022. - N 3. - С. 39 - 46
134. Kuhl U., Lassner D., von Schlippenbach J., et al. Interferon- beta improves sur-vival in enterovirus- associated cardiomyopathy//J. Am.Coll. Cardiol. - 2012. - Vol. 60. - P. 1295 - 1296. doi: 10.1016/j.jacc.2012.06.026
135. Schultheiss HP. et al. Betaferon in chronic viral cardiomyopathy (BICC) trial: ef-fects of interferon- ![]() treatment in patients with chronic viral cardiomyopathy//Clin. Res. Cardiol. - 2016. - Vol. 105. - P. 763 - 773. doi: 10.1007/s00392-016-0986-9
treatment in patients with chronic viral cardiomyopathy//Clin. Res. Cardiol. - 2016. - Vol. 105. - P. 763 - 773. doi: 10.1007/s00392-016-0986-9
136. Costanzo-Nordin MR, Reap EA, O'Connell JB, Robinson JA, Scanlon PJ. A non-steroid antiinflammatory drug exacerbates Coxsackie B3 murine myocarditis//J Am Coll Cardiol. - 1985. - Vol. 6. - P. 1078 - 1082. doi: 10.1016/s0735-1097(85)80312-0
137. Khatib R, Reyes MP, Smith F, Khatib G, Rezkalla S. Enhancement of coxsackievirus B4 virulence by indomethacin//J Lab Clin Med. - 1990. - Vol. 116. - P. 662 - 670.
138. Lin MS., Tseng YH., Chen MY. et al. Inhospital and postdischarge outcomes of pediatric acute myocarditis underwent after highdose steroid or intravenous immuno-globulin therapy//BMC Cardiovasc Disorders 19. - 2019.
139. Prasad AN, Chaudhary S. Intravenous immunoglobulin in children with acute my-ocarditis and/or early dilated cardiomyopathy//Indian Pediatr. - 2014. - Vol. 51(7). - P. 583 - 4. doi: 10.1007/s13312-014-0456-2
140. Kim HS, Sohn S, Park JY, Seo JW. Fulminant myocarditis successfully treated with high dose immunoglobulin//Int J Cardiol. - 2004. - Vol. 96(3). - P. 485 - 6. doi: 10.1016/j.ijcard.2003.05.037
141. Tsai YG, Ou TY, Wang CC, Tsai MC et.al. Intravenous gammaglobulin therapy in myocarditis complicated with complete heart block: report of one case//Acta Paediatr Taiwan. - 2001. - Vol. 42(5). - P. 311 - 3.
142. Xin Huang, Yufei Sun, Guanhua Su, Yu Li, Xinxin Shuai, Intravenous Immunoglobulin Therapy for Acute Myocarditis in Children and Adults//International Heart Journal. - 2019. - Vol. 60 (2). - P. 359 - 365. doi: 10.1536/ihj.18-299
143. Drucker NA, Colan SD, Lewis AB, Beiser AS, Wessel DL, Takahashi M, Baker AL, Perez-Atayde AR, Newburger JW. Gamma-globulin treatment of acute myocarditis in the pediatric population//Circulation. - 1994. - Vol. 89. - P. 252 - 257.
144. Maisch B, Hufnagel G,  S, Funck R, Richter A, Rupp H, Herzum M, Pankuweit S. Treatment of inflammatory dilated cardiomyopathy and (peri)myocarditis with immunosuppression and i.v. immunoglobulins//Herz. - 2004 Sep. - Vol. 29(6). - P. 624 - 36.
S, Funck R, Richter A, Rupp H, Herzum M, Pankuweit S. Treatment of inflammatory dilated cardiomyopathy and (peri)myocarditis with immunosuppression and i.v. immunoglobulins//Herz. - 2004 Sep. - Vol. 29(6). - P. 624 - 36.
145. Chan KY, Iwahara M, Benson LN, Wilson GJ, Freedom RM. Immunosuppressive therapy in the management of acute myocarditis in children: a clinical trial//J Am Coll Cardiol. - 1991. - Vol. 17(2). - P. 458 - 60. doi: 10.1016/s0735-1097(10)80115-9
146. Kleinert S, Weintraub RG, Wilkinson JL, Chow CW. Myocarditis in children with dilated cardiomyopathy: incidence and outcome after dual therapy immunosuppression//J Heart Lung Transplant. - 1997. - Vol. 16(12). - P. 1248 - 54.
147. Mason JW, O'Connell JB, Herskowitz A, Rose NR, McManus BM, Billingham ME. Moon TE. A clinical trial of immunosuppressive therapy for myocarditis. The myocarditis treatment trial investigators//N Engl J Med. - 1995. - Vol. 333(5). - P. 269 - 75. doi: 10.1056/NEJM199508033330501
148. Camargo PR, Snitcowsky R, da Luz PL, Mazzieri R, Higuchi ML, Rati M, Stolf N, Ebaid M, Pileggi F. Favorable effects of immunosuppressive therapy in children with dilated cardiomyopathy and active myocarditis//Pediatr Cardiol. - 1995. - Vol. 16(2). - P. 61 - 8. doi: 10.1007/BF00796819
149. Aziz KU, Patel N, Sadullah T, Tasneem H, Thawerani H, Talpur S. Acute viral myocarditis: role of immunosuppression: a prospective randomised study//Cardiol Young. - 2010 Oct. - Vol. 20(5). - P. 509 - 15.
150. Hia CP, Yip WC, Tai BC, Quek SC. Immunosuppressive therapy in acute myocarditis: an 18 year systematic review//Arch Dis Child. - 2004. - Vol. 89(6). - P. 580 - 4. doi: 10.1136/adc.2003.034686
151. Lu C, Qin F, Yan Y, Liu T, Li J, Chen H. Immunosuppressive treatment for myocarditis: a metaanalysis of randomized controlled trials//J Cardiovasc Med (Hager-stown). - 2016. - Vol. 17(8). - P. 631.
152. Chen HS, Wang W, Wu SN, Liu JP. Corticosteroids for viral myocarditis//Cochrane Database Syst Rev. - 2013. - Vol. 2013 (10). doi: 10.1002/14651858.CD004471.pub3
153. Herda L.R. et al. Effects of immunoadsorption and subsequent immunoglobulin G substitution on cardiopulmonary exercise capacity in patients with dilated cardiomyopa-thy//Am. Heart J. - 2010. - Vol. 159(5). - P. 809 - 816. doi: 10.1016/j.ahj.2010.01.012
154. Bulut D. et al. Effect of protein A immunoadsorption on T cell activation in patients with inflammatory dilated cardiomyopathy//Clin. Res. Cardiol. Off. J. Ger. Card. Soc. - 2010. - Vol. 99(10). - P. 633 - 638. doi: 10.1007/s00392-010-0162-6
155. Maron BJ. et al. Eligibility and disqualification recommendations for competitive athletes with cardiovascular abnormalities: Task Force 3: Hypertrophic cardiomyopathy, arrhythmogenic right ventricular cardiomyopathy and other cardiomyopathies, and myocarditis: a scientific statement from the American Heart Association and American Col-lege of Cardiology//Circulation. - 2015. - Vol. 132 (22). - e.273 - 80. doi: 10.1161/CIR.0000000000000239
156. Bozkurt B. et al. Current diagnostic and treatment strategies for specific dilated cardiomyopathies: a scientific statement from the American Heart Association//Circula-tion. - 2016. - Vol. 134. - e579 - 646. doi.org/10.1161/CIR.0000000000000455
157. Леонтьева И.В. Современная стратегия лечения миокардитов у детей//Российский вестник перинатологии и педиатрии. - 2022. - N 67(1). - С.: 28 - 38. doi: 10.21508/1027-4065-2022-67-1-28-38
158. Zeppenfeld K, Tfelt-Hansen J, de Riva M, et al. ESC Scientific Document Group, 2022 ESC Guidelines for the management of patients with ventricular arrhythmi-as and the prevention of sudden cardiac death: Developed by the task force for the man-agement of patients with ventricular arrhythmias and the prevention of sudden cardiac death of the European Society of Cardiology (ESC) Endorsed by the Association for Eu-ropean Paediatric and Congenital Cardiology (AEPC)//European Heart Journal. - 2022. - Vol. 43(40). - P. 3997 - 4126. doi: 10.1093/eurheartj/ehac262
159. Brugada J, Blom N, Sarquella-Brugada G et al. Pharmacological and nonpharmacological therapy for arrhythmias in the pediatric population: EHRA and AEPC-Arrhythmia Working Group joint consensus statement.//EP Europace. - 2013. - Vol. 15(9). - P. 1337 - 1382. doi: 10.1093/europace/eut082
160. Rizzo C, Carbonara R, Ruggieri R, Passantino A, Scrutinio D. Iron Deficiency: A New Target for Patients With Heart Failure//Front Cardiovasc Med. - 2021. Vol. 8; 709872. - e1 - 10. doi: 10.3389/fcvm.2021.709872
161. Peretto G, Sala S, Camaschella C. Iron deficiency in chronic myocarditis: Assess-ment and prognostic significance.//Eur J Intern Med. - 2021. Vol 89. - P. 129 - 131. doi: 10.1016/j.ejim.2021.03.037.
162. Ogunbayo GO, Elayi SC, Ha LD, Olorunfemi O, Elbadawi A, Saheed D, Sorrell VL. Outcomes of heart block in myocarditis: a review of 31,760 patients//Heart Lung Circ. - 2019. - Vol. 28. - P. 272 - 276. doi: 10.1016/j.hlc.2017.12.005
163. Li TT, Cheng J. Clinical analysis of temporary pacemaker implantation in 13 children.//Transl Pediatr. - 2022. - Vol 11(2). - P. 174 - 182. doi: 10.21037/tp-21-586
164. Batra AS, Epstein D, Silka MJ. The clinical course of acquired complete heart block in children with acute myocarditis.//Pediatr Cardiol. - 2003. - Vol. 24(5). - P. 495 - 497. doi: 10.1007/s00246-002-0402-2
165. Gagliardi MG, Fierabracci A, Pilati M, et al. The impact of specific viruses on clinical outcome in children presenting with acute heart failure//Int J Mol Sci. - 2016. - Vol. 17(4). - P. 1 - 10. doi: 10.3390/ijms17040486
166. Kirk R, Naftel D, Hoffman TM, et al. Outcome of pediatric patients with dilated cardiomyopathy listed for transplant: a multi-institutional study//J Heart Lung Transpl. - 2009 Dec. - Vol. 28 (12). - P. 1322 - 8. doi: 10.1016/j.healun.2009.05.027
167. Pietra BA, Kantor PF, Bartlett HL, et al. Early predictors of survival to and after heart transplantation in children with dilated cardiomyopathy//Circulation. - 2012 Aug 28. - Vol. 126 (9). - P. 1079 - 86. doi: 10.1161/CIRCULATIONAHA.110.011999
168. Tikkanen AU, Berry E, LeCount E et al. Rehabilitation in Pediatric Heart Failure and Heart Transplant.//Front Pediatr. - 2021. - Vol. 9; 674156. doi: 10.3389/fped.2021.674156.
169. World Health Organization. International Classification of Functioning, Disability and Health: ICF. Geneva: WHO, 2001. - P. 3 - 29.
170. Piepoli MF, Conraads V, Corra' U. et al. Exercise training in heart failure: from theory to practice. A consensus document of the Heart Failure Association and the European Association for Cardiovascular Prevention and Rehabilitation//Eur. J. Heart. Fail. - 2011. - N. 13. - P. 347 - 357.
171. Paridon SM, Alpert BS, Alpert BS. Clinical stress testing in the pediatric age group: a statement from the American Heart Association council on cardiovascular dis-ease in the young, committee on atherosclerosis, hypertension, and obesity in youth. Circulation. - 2006. - Vol. 113(15). P. 1905 - 1920.
172. Giannitsi S, Bougiakli M, Bechlioulis A, et al. 6-minute walking test: a useful tool in the management of heart failure patients.//Ther Adv Cardiovasc Dis. - 2019. - Vol. 13:1753944719870084. doi: 10.1177/1753944719870084.
173. McBride MG, Burstein DS, Edelson JB, Paridon SM. Cardiopulmonary Rehabilitation in Pediatric Patients With Congenital and Acquired Heart Disease. J Cardiopulm Rehabil Prev. - 2020. - Vol. 40(6). - P. 370 - 377. doi: 10.1097/HCR.0000000000000560.
174. Davies E.J. et al. Exercise training for systolic heart failure: Cochrane systematic review and meta-analysis//Eur. J. Heart Fail. - 2010. - Vol. 12(7). - P. 706 - 715. doi: 10.1093/eurjhf/hfq056
175. Ribeiro J.P., Chiappa G.R., Callegaro C.C. The contribution of inspiratory muscles function to exercise limitation in heart failure: pathophysiological mechanisms//Rev. Bras. Fisioter. Sao Carlos Sao Paulo Braz. - 2012. - Vol. 16(4). - P. 261 - 267. doi.org/10.1590/S1413-35552012005000034
176. Pandey A. et al. Exercise training in patients with heart failure and preserved ejection fraction: metaanalysis of randomized control trials//Circ. Heart Fail. - 2015 Jan. - Vol. 8 (1). - P. 33 - 40. doi: 10.1161/CIRCHEARTFAILURE.114.001615
177. Батышева Т.Т., Медико-психологическая помощь детям с нарушением психического развития в системе комплексной реабилитации//Методические рекомендации, г. Москва. - 2018. - С. 5 - 568.
178. Таточенко В.К., Н.А. Озерецковский. Иммунопрофилактика-2020: справочник, 13-е издание, расширенное//Москва: Боргес. - 2020. - С. 16 - 23.
179. Басаргина Е.Н., Миокардит у детей: трудности диагностики и лечения//журнал "Педиатрия". - г. Москва - 2015. - N. 94(2). - С. 158 - 160.
180. Басаргина Е.Н. Сердечная недостаточность. В кн.: М.А. Школьникова, Е.И. Алексеева, ред. Клинические рекомендации по детской кардиологии и ревматологии//М.: "ООО М-Арт". - 2011. - С. 242 - 276.
181. Mirabel M. et al. Outcomes, longterm quality of life, and psychologic assessment of fulminant myocarditis patients rescued by mechanical circulatory support//Crit. Care Med. - 2011. - Vol. 39 (5). - P. 1029 - 1035. doi: 10.1097/CCM.0b013e31820ead45
182. Hsu K.-H. et al. Extracorporeal membranous oxygenation support for acute fulminant myocarditis: analysis of a single center's experience//Eur. J. Cardio-Thorac. Surg. Off. J. Eur. Assoc. Cardio-Thorac. Surg. - 2011. - Vol. 40 (3). - P. 682 - 688. doi: 10.1016/j.ejcts.2010.12.050
Приложение А1
СОСТАВ
РАБОЧЕЙ ГРУППЫ ПО РАЗРАБОТКЕ И ПЕРЕСМОТРУ
КЛИНИЧЕСКИХ РЕКОМЕНДАЦИЙ
1. Васичкина Е.С. - председатель рабочей группы, д.м.н. (Санкт-Петербург), член Ассоциации детских кардиологов России (АДКР), Российского кардиологического общества (РКО), Европейского общества кардиологов (ESC), Европейского общества аритмологов (EHRA).
2. Грознова О.С. д.м.н. (Москва) - секретарь рабочей группы, член Ассоциации детских кардиологов России (АДКР).
3. Балыкова Л.А. д.м.н., профессор (Саранск), член Ассоциации детских кардиологов России (АДКР), Российского кардиологического общества (РКО), Российского общества Холтеровского мониторирования и неинвазивной электрокардиологии (РОХМиНЭ), Союза педиатров России, Европейской ассоциации педиатров (EPA/UNEPSA), Европейского общества кардиологов (ESC).
4. Басаргина Е.Н. д.м.н., профессор (Москва), член Ассоциации детских кардиологов России (АДКР).
5. Брегель Л. В д.м.н., профессор (Иркутск), член Ассоциации детских кардиологов России (АДКР).
6. Дегтярева Е.А. д.м.н., профессор (Москва), член Ассоциации детских кардиологов России (АДКР).
7. Котлукова Н.П. д.м.н, профессор (Москва), член Ассоциации детских кардиологов России (АДКР).
8. Леонтьева И.В. д.м.н., профессор (Москва), член Ассоциации детских кардиологов России (АДКР), Российского кардиологического общества (РКО), Российского общества Холтеровского мониторирования и неинвазивной электрокардиологии (РОХМиНЭ).
9. Яковлева Л.В. д.м.н., профессор (Уфа), член Ассоциации детских кардиологов России (АДКР).
Конфликт интересов:
Авторы подтверждают отсутствие финансовой поддержки/конфликта интересов, который необходимо обнародовать.
Приложение А2
МЕТОДОЛОГИЯ РАЗРАБОТКИ КЛИНИЧЕСКИХ РЕКОМЕНДАЦИЙ
Целевая аудитория данных клинических рекомендаций:
1. Врачи - педиатры
2. Врачи общей практики (семейные врачи)
3. Врачи - детские кардиологи
4. Студенты медицинских ВУЗов, ординаторы, аспиранты
Таблица 1. Шкала оценки уровней достоверности доказательств (УДД) для методов диагностики (диагностических вмешательств)
УДД
Расшифровка
1
Систематические обзоры исследований с контролем референсным методом или систематический обзор рандомизированных клинических исследований с применением метаанализа
2
Отдельные исследования с контролем референсным методом или отдельные рандомизированные клинические исследования и систематические обзоры исследований любого дизайна, за исключением рандомизированных клинических исследований, с применением метаанализа
3
Исследования без последовательного контроля референсным методом или исследования с референсным методом, не являющимся независимым от исследуемого метода или нерандомизированные сравнительные исследования, в том числе когортные исследования
4
Несравнительные исследования, описание клинического случая
5
Имеется лишь обоснование механизма действия или мнение экспертов
Таблица 2. Шкала оценки уровней достоверности доказательств (УДД) для методов профилактики, лечения и реабилитации (профилактических, лечебных, реабилитационных вмешательств)
УДД
Расшифровка
1
Систематический обзор РКИ с применением метаанализа
2
Отдельные РКИ и систематические обзоры исследований любого дизайна, за исключением РКИ, с применением метаанализа
3
Нерандомизированные сравнительные исследования, в т.ч. когортные исследования
4
Несравнительные исследования, описание клинического случая или серии случаев, исследования "случай-контроль"
5
Имеется лишь обоснование механизма действия вмешательства (доклинические исследования) или мнение экспертов
Таблица 3. Шкала оценки уровней убедительности рекомендаций (УУР) для методов профилактики, диагностики, лечения и реабилитации (профилактических, диагностических, лечебных, реабилитационных вмешательств)
УУР
Расшифровка
A
Сильная рекомендация (все рассматриваемые критерии эффективности (исходы) являются важными, все исследования имеют высокое или удовлетворительное методологическое качество, их выводы по интересующим исходам являются согласованными)
B
Условная рекомендация (не все рассматриваемые критерии эффективности (исходы) являются важными, не все исследования имеют высокое или удовлетворительное методологическое качество и/или их выводы по интересующим исходам не являются согласованными)
C
Слабая рекомендация (отсутствие доказательств надлежащего качества (все рассматриваемые критерии эффективности (исходы) являются неважными, все исследования имеют низкое методологическое качество и их выводы по интересующим исходам не являются согласованными)
Порядок обновления клинических рекомендаций.
Механизм обновления клинических рекомендаций предусматривает их систематическую актуализацию - не реже чем один раз в три года, а также при появлении новых данных с позиции доказательной медицины по вопросам диагностики, лечения, профилактики и реабилитации конкретных заболеваний, наличии обоснованных дополнений/замечаний к ранее утвержденным КР, но не чаще 1 раза в 6 месяцев.
Приложение А3
СПРАВОЧНЫЕ МАТЕРИАЛЫ,
ВКЛЮЧАЯ СООТВЕТСТВИЕ ПОКАЗАНИЙ К ПРИМЕНЕНИЮ
И ПРОТИВОПОКАЗАНИЙ, СПОСОБОВ ПРИМЕНЕНИЯ И ДОЗ ЛЕКАРСТВЕННЫХ
ПРЕПАРАТОВ, ИНСТРУКЦИИ ПО ПРИМЕНЕНИЮ
ЛЕКАРСТВЕННОГО ПРЕПАРАТА
1. Приказ Министерства здравоохранения Российской Федерации от 28.02.2019 N 103н "Об утверждении порядка и сроков разработки клинических рекомендаций, их пересмотра, типовой формы клинических рекомендаций и требований к их структуре, составу и научной обоснованности, включаемой в клинические рекомендации информации" (Зарегистрирован 08.05.2019 N 54588).
2. Министерство здравоохранения и социального развития Российской Федерации приказ 28 февраля 2006 г. N 129 "Об утверждении стандарта медицинской помощи больным миокардитом неуточненным".
3. Приказ Министерства здравоохранения РФ от 10 мая 2017 г. N 203н "Об утверждении критериев оценки качества медицинской помощи".
4. Федеральные клинические рекомендации "Миокардиты", 2020. https://cr.minzdrav.gov.ru/recomend/153_1
5. Приказ Минздравсоцразвития России от 16.04.2012 N 366н (ред. от 21.02.2020) "Об утверждении Порядка оказания педиатрической помощи". (Зарегистрировано в Минюсте России 29.05.2012 N 24361).
6. Приказ Минздрава России от 25.10.2012 N 440н (ред. от 21.02.2020) "Об утверждении Порядка оказания медицинской помощи по профилю "детская кардиология" (Зарегистрировано в Минюсте России 04.12.2012 N 26000).
7. Государственный реестр лекарственных средств https://grls.rosminzdrav.ru/Default.aspx
8. Приказ Министерства здравоохранения Российской Федерации от 06.12.2021 N 1122н "Об утверждении национального календаря профилактических прививок, календаря профилактических прививок по эпидемическим показаниям и порядка проведения профилактических прививок" (Зарегистрирован 20.12.2021 N 66435).
9. Баранов А.А. "Федеральные клинические рекомендации по оказанию медицинской помощи детям с миокардитами" 2015 г. https://www.pediatr-russia.ru/information/klin-rek/deystvuyushchie-klinicheskie-rekomendatsii/
10. Приказ Министерства здравоохранения РФ от 23.10.2019 N 878н "Об утверждении Порядка организации медицинской реабилитации детей".
11. Приказ Минтруда России от 27.08.2019 N 585н (в редакции 19.01.2021) "О классификации и критериях, используемых при осуществлении медико-социальной экспертизы граждан федеральными государственными учреждениями медико-социальной экспертизы".
12. Приказ Минздрава России от 02.03.2021 N 160н "Об утверждении стандартов медицинской помощи взрослым при миокардитах" (вместе со "Стандартом медицинской помощи взрослым при миокардитах (диагностика и лечение)", "Стандартом медицинской помощи взрослым при миокардитах (диспансерное наблюдение)") (Зарегистрировано в Минюсте России 12.04.2021 N 63068).
13. Приказ Минздрава России от 15 ноября 2012 г. N 918н "Об утверждении порядка оказания медицинской помощи больным с сердечно-сосудистыми заболеваниями" (в ред. Приказов Минздрава РФ от 14.04.2014 N 171н, от 22.02.2019 N 89н, от 21.02.2020 N 114н).
Приложение Б
АЛГОРИТМЫ ДЕЙСТВИЙ ВРАЧА
Приложение Б1
АЛГОРИТМ ВЫБОРА ТАКТИКИ ЛЕЧЕНИЯ ПАЦИЕНТОВ С ОСТРЫМ
МИОКАРДИТОМ НА ОСНОВАНИИ ИСХОДНОГО ГЕМОДИНАМИЧЕСКОГО ПРОФИЛЯ
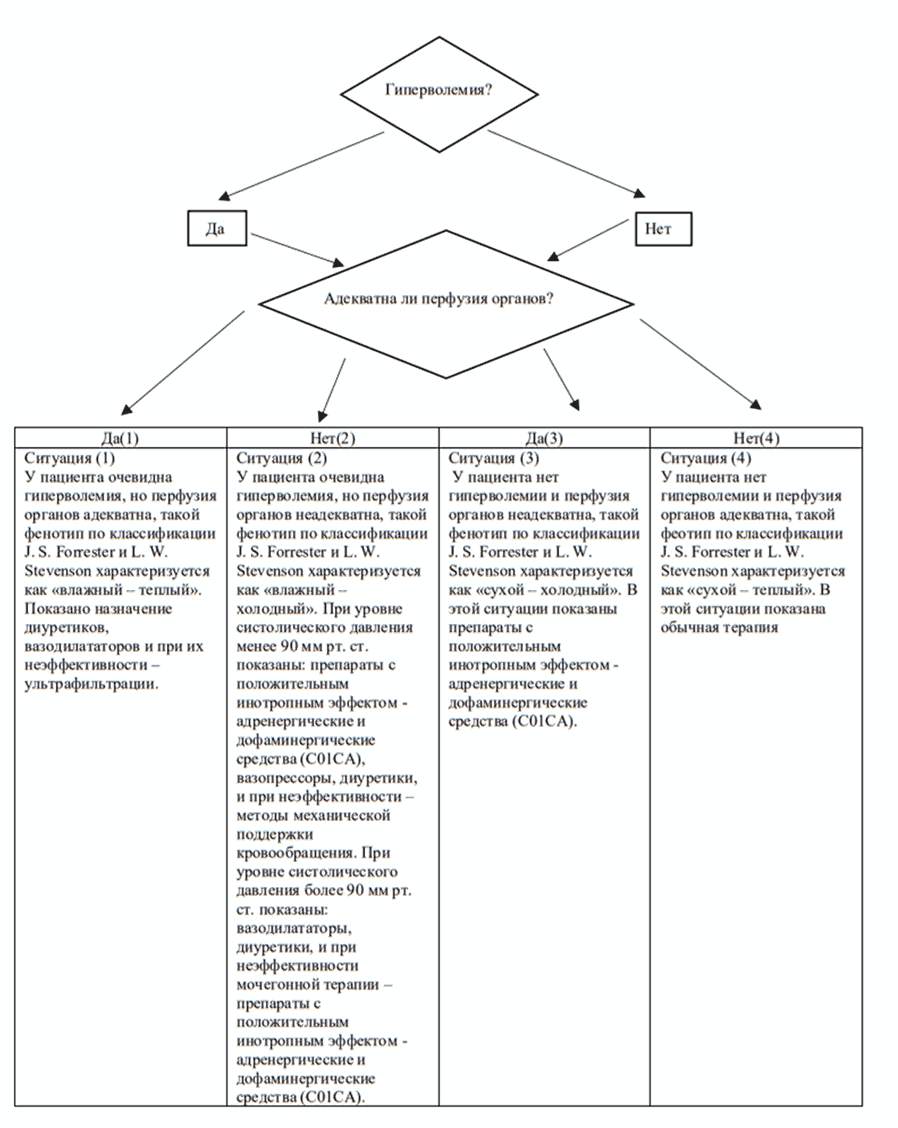
Приложение Б2
АЛГОРИТМ РАННЕЙ ДИАГНОСТИКИ И ВЕДЕНИЯ МИОКАРДИТА У ДЕТЕЙ
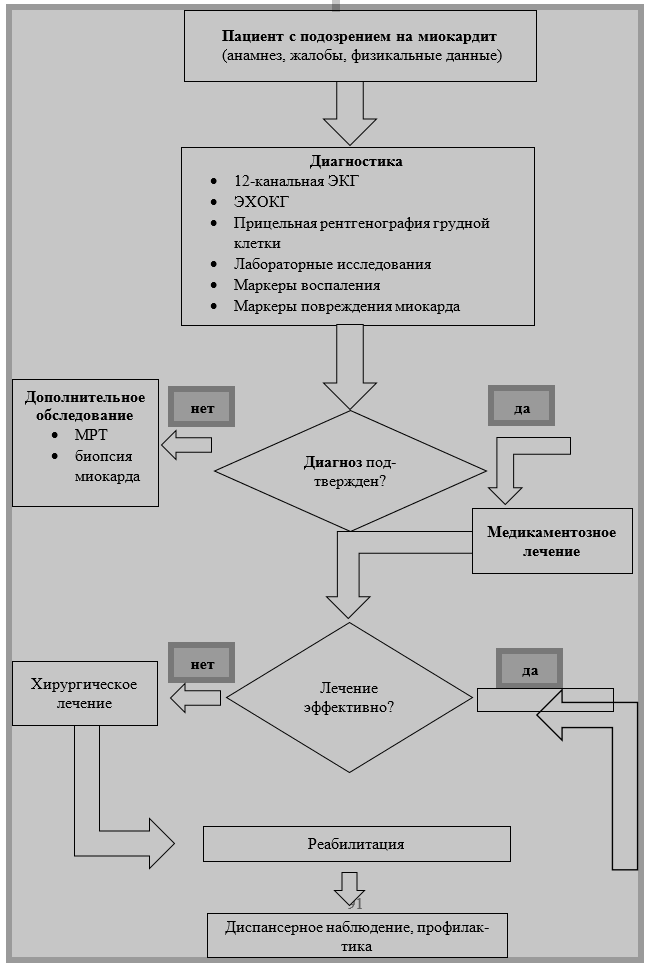
Приложение В
ИНФОРМАЦИЯ ДЛЯ ПАЦИЕНТА
Миокардит - это воспалительное поражение миокарда инфекционной, токсической (в т.ч. лекарственной), аллергической, аутоиммунной или неизвестной этиологии с широким спектром клинических проявлений от бессимптомного течения до развития клиники тяжелой сердечной недостаточности, жизнеугрожающих нарушений ритма и проводимости, кардиогенного шока и внезапной сердечной смерти. Миокардит может быть самостоятельным патологическим процессом или сопутствовать инфекционным, или системным заболеваниям, таким как дифтерия, корь, системные васкулиты, болезни соединительной ткани, инфекционный эндокардит и др.
Диагноз миокардит может быть установлен в любом возрасте, но в подавляющем большинстве встречается в первые несколько лет жизни и подростковом возрасте.
Клинические проявления миокардита также разнообразны и зависят от возраста ребенка.
Следует знать следующее: в случае подозрения на миокардит ребенок должен однозначно госпитализироваться в стационар.
У грудных детей и детей до 3 лет чаще всего заболевание начинается остро, как правило после перенесенной вирусной инфекции, когда после эпизода высокой температуры появляется слабость, одышка, ребенок становится более вялым, капризным, дети грудного возраста начинают хуже сосать из груди, иногда отказываются от кормлений, отмечается повышенная потливость. В этом случае следует немедленно обратиться к врачу или вызвать скорую медицинскую помощь.
В случае выявления патологии сердца ребенок будет госпитализирован в стационар. Врачом будет определена тяжесть состояния, при необходимости ребенок может быть переведен в отделение реанимации для стабилизации состояния.
Ребенку будет проведено необходимое обследование, включающее ЭКГ, ЭХОКГ, рентгенографию грудной клетки, проведены лабораторные обследования, включающие общий и биохимический анализ крови. В зависимости от тяжести состояния и выявленных изменений ребенку будет назначена индивидуальная терапия.
В случае позднего обращения и тяжелого прогрессирующего течения, несмотря на проводимую необходимую терапию, возможен летальный исход.
При стабилизации состояния при условии выполнения всех рекомендаций, возможен переход процесса в хроническую стадию.
Дети с хроническим миокардитом нуждаются в длительном лечении. Любое лечение начинается с немедикаментозных назначений: это ограничение объема потребляемой жидкости - в зависимости от выраженности симптомов сердечной недостаточности необходимо ограничение до 2/3 от нормы для данного возраста, ограничение физических нагрузок. Медикаментозная терапия, как правило, включает применение препаратов, поддерживающих работу сердечной мышцы, диуретиков и ряда других средств. Как правило, лечение хронического миокардита длительное, в течение нескольких лет. При условии восстановления функции миокарда проводится постепенная отмена терапии под контролем врача-кардиолога.
Прогноз заболевания определяет степень поражения миокарда в острую фазу заболевания.
При выявлении значительного повреждения миокарда чаще всего констатируется трансформация в дилатационную кардиомиопатию. В этом случае комплексное лечение продолжается пожизненно.
При средней степени повреждения миокарда - возможно восстановление субнормальных функций сердца, в этом случае не всегда удается полностью отменить терапию, но удается ослабить до 1 - 2 препаратов.
При минимальном повреждении миокарда удается полностью восстановить функции сердца и провести постепенную (в течение нескольких лет) отмену медикаментозной терапии.
Оценивают степень повреждения миокарда с помощью МРТ сердца для определения прогноза заболевания, как правило, спустя несколько лет после начала заболевания. В начале заболевания эти исследования могут только подтвердить текущий воспалительный процесс.
В старшем возрасте дети могут жаловаться на слабость, сердцебиения. Чаще всего миокардит проявляет себя прогрессирующим ухудшением реполяризации по данным ЭКГ (изменения нарастают ежедневно). В этом случае ребенок так же нуждается в госпитализации и проведении своевременного лечения.
Детям также проводится комплекс лабораторно-инструментального обследования и назначается индивидуальная терапия.
После выписки из стационара наблюдение за ребенком осуществляет участковый врач-педиатр и врач-кардиолог (врач-детский кардиолог) по месту жительства.
Длительность зависит от восстановления функции сердца и снятии ограничений врачом-кардиологом. В случае течения заболевания с хронической сердечной недостаточностью - ребенку оформляется инвалидность.
В острый период миокардита и в течение 1 года после выявления заболевания не рекомендуется проведение профилактических прививок. Однако спустя год, при стабилизации состояния целесообразно рассмотреть вопрос о возобновлении прививок по Национальному календарю.
Причем, отдельно хотим отметить, что проведение внутрикожной пробы с туберкулезным аллергеном необходимо ежегодно, так как внутрикожная проба с туберкулезным аллергеном не является прививкой, а является своего рода "анализом" на туберкулез.
В остром периоде миокардита необходимо избегать интенсивных физических нагрузок. В период реабилитации рекомендуется физическая активность от низкой до умеренной интенсивности, под наблюдением врача-специалиста.
Спортсмены с вероятным или диагностированным миокардитом должны быть отстранены от всех соревновательных видов спорта до полного клинического выздоровления, но не менее 6 месяцев после начала клинических проявлений.
Спортсмены могут вернуться к тренировкам по истечении этого периода времени при условии нормализации показателей до исходного уровня по данным эхокардиографии и/ или МРТ сердца, отсутствия клинически значимых аритмий по данным ЭКГ, холтеровского мониторирования сердечного ритма в 12 отведениях и тестов с физической нагрузкой, а также нормализации сывороточных маркеров воспаления/сердечной недостаточности.
Приложение Г1 - ГN
ШКАЛЫ ОЦЕНКИ, ВОПРОСНИКИ И ДРУГИЕ ОЦЕНОЧНЫЕ ИНСТРУМЕНТЫ
СОСТОЯНИЯ ПАЦИЕНТА, ПРИВЕДЕННЫЕ В КЛИНИЧЕСКИХ РЕКОМЕНДАЦИЯХ
Приложение Г1
СХЕМА
СТРАТЕГИИ ВЕДЕНИЯ ПАЦИЕНТА С ПОДОЗРЕНИЕМ НА МИОКАРДИТ
В УСЛОВИЯХ СТАЦИОНАРА
Симптомы миокардита, идентифицированные при поступлении в медицинское учреждение
Лихорадка/Продромальный период с:
- Сердечно-сосудистыми симптомами: нарушение перфузии и гипотензия, боль в груди, одышка или тахипноэ, шок.
- Гастроинтестинальными симптомами: тошнота, рвота, диарея или боль в животе.
- Неврологическими симптомами: вялость, слабость, нарушение поведения, нарушение сознания, обморок.
- У младенцев могут быть неспецифические изменения: лихорадка, раздражительность, вялое сосание, изменение цвета кожных покровов и слизистых оболочек, одышка/апноэ.
- Клиническая картина может иметь значимое сходство с симптомами сепсиса. В дифференциальный ряд должен быть включен миоперикардит.
Подозрение на миокардит и первичная диагностика
- 12-канальная ЭКГ: находки могут включать инверсию зубца T, подъем или депрессию сегмента ST, удлинение интервала PR, патологические зубцы Q, низкий вольтаж комплекса QRS, неспецифические изменения зубца T и сегмента ST.
- Прицельная рентгенография органов грудной клетки: может быть кардиомегалия (обычно ассоциируется с миокардитом), плевральный выпот, усиление легочного рисунка или может быть норма.
- ЭХОКГ: может быть определена глобальная левожелудочковая или бивентрикулярная дисфункция, ДКМП, снижение ФВ ЛЖ, значительная регургитация на митральном или трикуспидальном клапанах или увеличение предсердий. Может быть норма.
- Определение уровня Тропонина: повышенный уровень повышает вероятность миокардита (значение более 0,01 нг/мл).
- Лабораторные показатели: Клинический анализ крови + СОЭ; биохимический анализ крови (повышение уровня АСТ при нормальном уровне АЛТ коррелирует с миокардитом); СРБ; BNP/NTproBNP, панель респираторных вирусов.
- Рекомендована ранняя консультация врача-кардиолога, подключение к кардиомонитору.
Маршрутизация пациентов после первичного обследования
- Пациенты, у которых выявлены любые признаки фульминантного миокардита, такие как короткий продромальный период (< 48 часов) или ЭХО-находки, позволяющие предположить фульминантный миокардит, снижение ФВ ЛЖ, элевация ST, аритмия по данным кардиомонитора, признаки гемодинамической нестабильности или положительный результат ПЦР на Парвовирус B19, должны быть незамедлительно переведены в отделение/палату интенсивной терапии.
- Пациентам, у которых нет вышеупомянутых критериев и которые считаются стабильными по данным осмотра врача детского-кардиолога, может быть продолжено наблюдение и лечение в соматическом/кардиологическом отделении с тщательным полноценным кардиологическим мониторингом.
Ведение ребенка в отделении интенсивной терапии
Кардиомонитор с постоянным контролем ЭКГ, консультация врача-кардиолога, оценка ЭХОКГ в динамике.
Диагностика:
- Рассмотреть необходимость выполнения МРТ сердца.
- Рассмотреть необходимость выполнения биопсии миокарда с ПЦР биоптата на вирусы, если состояние пациента не улучшается.
- Инфекционный статус (подход к оценке с учетом эпидемиологического анамнеза, эндемичности региона проживания).
- Рассмотреть необходимость выполнения обследования на Парвовирус B19, энтеровирусы, аденовирусы, ВЭБ, ЦМВ (ПЦР).
- Оценить статус иммунизации, особенно вакцинация против кори, краснухи, паротита.
- Оценить риски заболевания туберкулезом, рассмотреть возможность проведения внутрикожной пробы с туберкулезным аллергеном или иммунодиагностики (теста высвобождения гамма-интерферона).
- Рассмотреть необходимость выполнения Респираторной вирусной панели (ПЦР).
- Рассмотреть необходимость выполнения риккетсиозной панели у пациентов лихорадкой, головной болью, сыпью в анамнезе.
- Рассмотреть необходимость выполнения обследования на ВИЧ/болезнь Лайма.
Лечение
- Рассмотреть необходимость использования Иммуноглобулина человека нормального** для в/в введения.
- Рассмотреть необходимость использования ГК при выраженном снижении ФВЛЖ.
- Медикаментозная и кардиотоническая поддержка под контролем бригады отделения интенсивной терапии.
- Мониторинг аритмий.
- Механическая вентиляция.
- По показаниям рассмотреть вопрос о трансплантации сердца.
Название на русском языке: Протокол детского миокардита: алгоритм раннего выявления и лечения, подтвержденный ретроспективным анализом.
Оригинальное название: Howard A., Hasan A., Brownlee J., Mehmood N., Ali M., Mehta S., Fergie J. Pediatric Myocarditis Protocol: An Algorithm for Early Identifcation and Management with Retrospective Analysis for Validation Received: Springer Science + Business Media, LLC, part of Springer Nature 2019 Pediatric Cardiology (2020) 41: 316 - 326 https://doi.org/10.1007/s00246-019-02258-1
https://link.springer.com/article/10.1007%2Fs00246-019-02258-1
Источник (официальный сайт разработчиков, публикация с валидацией):
Received: Springer Science + Business Media, LLC, part of Springer Nature 2019 Pediatric Car-diology (2020) 41: 316 - 326 https://doi.org/10.1007/s00246-019-02258-1
https://link.springer.com/article/10.1007%2Fs00246-019-02258-1
