"Клинические рекомендации "Опухоли слюнных желез у детей"
МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ
КЛИНИЧЕСКИЕ РЕКОМЕНДАЦИИ
ОПУХОЛИ СЛЮННЫХ ЖЕЛЕЗ У ДЕТЕЙ
Кодирование по Международной статистической классификации болезней и проблем, связанных со здоровьем: C07, C08, C06.9, D11, D10.3
Год утверждения (частота пересмотра): 2024
Пересмотр не позднее: 2026
ID: 75_2
Возрастная категория: Дети
Специальность:
Разработчик клинической рекомендации
Российское общество детских онкологов и гематологов
Одобрено Научно-практическим Советом Минздрава России
Список сокращений
ГИ - гистологическое исследование
ЛТ - лучевая терапия
МРТ - магнитно-резонансная томография
ЛУ - лимфатические узлы
КТ - компьютерная томография
РИД - радиоизотопное исследование
СЖ - слюнные железы
ОСЖ - околоушная слюнная железа
МЭК - мукоэпидермоидная карцинома
СОД - суммарная очаговая доза
ТАБ - тонкоигольная аспирационная биопсия
ТПАБ - тонкоигольная пункционная аспирационная биопсия
ПЭТ - позитронно-эмиссионная томография
ПЭТ/КТ - позитронно-эмиссионная томография + компьютерная томография
УЗИ - ультразвуковое исследование
ЦИ - цитологическое исследование
TNM - (аббревиатура от tumor, nodus и metastasis) международная классификация стадий развития раковых опухолей
Термины и определения
Инструментальная диагностика - диагностика с использованием для обследования пациента различных приборов, аппаратов и инструментов.
Лабораторная диагностика - совокупность методов, направленных на анализ исследуемого материала с помощью различного специализированного оборудования.
Медицинское вмешательство - выполняемые медицинским работником и иным работником, имеющим право на осуществление медицинскои деятельности, по отношению к пациенту, затрагивающие физическое или психическое состояние человека и имеющие профилактическую, диагностическую, лечебную, реабилитационную или исследовательскую направленность виды медицинских обследовании и (или) медицинских манипуляции, а также искусственное прерывание беременности.
Медицинский работник - физическое лицо, которое имеет медицинское или иное образование, работает в медицинской организации и в трудовые (должностные) обязанности которого входит осуществление медицинской деятельности, либо физическое лицо, которое является индивидуальным предпринимателем, непосредственно осуществляющим медицинскую деятельность.
Рабочая группа - двое или более людей одинаковых или различных профессии, работающих совместно и согласованно в целях создания клинических рекомендации, и несущих общую ответственность за результаты данной работы.
Синдром - совокупность симптомов с общими этиологией и патогенезом.
Хирургическое вмешательство - инвазивная процедура, может использоваться в целях диагностики и/или как метод лечения заболевании.
Хирургическое лечение - метод лечения заболевании путем разъединения и соединения тканей в ходе хирургической операции.
Анализ выживаемости (от анг. Survival analysis) - это класс статистических моделей, позволяющих оценить вероятность наступления события.
Безрецидивная выживаемость (БРВ) - от момента наступления ремиссии до момента возникновения рецидива.
Бессобытийная выживаемость (БСВ) - от начала лечения до момента прекращения ремиссии независимо от причины, приведшей к ней, а также отказ родителей от лечения.
Общая выживаемость (ОВ) - от начала лечения до его окончания или смерти пациента.
Большие слюнные железы: околоушная слюнная железа, подчелюстная слюнная железа, подъязычная слюнная железа
Малые слюнные железы: слюнные железы полости рта, ротоглотки
1. Краткая информация по заболеванию или состоянию (группы заболеваний или состояний)
1.1 Определение заболевания или состояния (группы заболеваний или состояний)
Рак слюнной железы (карцинома) - злокачественная эпителиальная опухоль слюнной железы.
1.2 Этиология и патогенез заболевания или состояния (группы заболеваний или состояний)
Изучены недостаточно. Возможными предрасполагающими факторами развития злокачественных опухолей эпителиального происхождения являются: влияние ионизирующей радиации, ранее проводимая лучевой терапии, хроническая вирусная инфекция [1,2]. Данные об этиологических факторах доброкачественных образований в настоящее время отсутствуют.
1.3 Эпидемиология заболевания или состояния (группы заболеваний или состояний)
Поражения слюнных желез у детей и подростков редкая патология и актуальная проблема челюстно-лицевой хирургии и онкологии. До 75 - 80% поражений слюнных желез имеют доброкачественную природу [3]. Наиболее частым представителем доброкачественных образований у детей и подростков является плеоморфная аденома. Следует отдельно выделить инфантильную гемангиому и лимфатические мальформации, клиническая картина которых сходна с опухолями, но данные заболевания являются сосудистыми мальформациями и подробно рассматриваются в соответствующих клинических рекомендациях.
Плеоморфная аденома наиболее частая доброкачественная опухоль слюнных желез как у взрослых, так и у детей. Так же носит название "смешанной опухоли" ввиду сочетания двух компонентов: эпителиального и миоэпителиального. Средний возраст пациентов - 16 лет, несколько чаще страдают девочки в соотношении 1,43:1. По локализации околоушная слюнная железа встречается в 56% случаев, подчелюстная слюнная железа - 31%, малые слюнные железы - 3,3% [4]
Злокачественные опухоли слюнных желез - редкая патология у детей и подростков и составляют 1 - 8% образований головы и шеи, занимая 4 место, после образований носоглотки, кожи и щитовидной железы [5, 6]. Околоушная слюнная железа поражается наиболее часто до 72%, подчелюстные - 8%, малые железы до 20% [7]. Средний возраст - 14 лет, с некоторым преобладанием пациентов женского пола, в соотношении 1,4:1 [5,7 - 9]. По частоте встречаемости первое место занимает мукоэпидермоидная (МЭК) - до 53%, далее ацинарноклеточная - 29% и аденокистозная карциномы - 5% [7].
1.4 Особенности кодирования заболевания или состояния (группы заболеваний или состояний) по Международной статистической классификации болезней и проблем, связанных со здоровьем
C07 - Злокачественное новообразование околоушной слюнной железы
C08 - Злокачественное новообразование других и неуточненных больших слюнных желез:
C08.0 - Злокачественное новообразование поднижнечелюстной железы
C08.1 - Злокачественное новообразование подъязычной железы
C08.8 - Поражение больших слюнных желез, выходящее за пределы одной или более вышеуказанных локализаций
C08.9 - Злокачественное новообразование большой слюнной железы неуточненной
C06.9 - Злокачественное новообразование рта неуточненное (Малой слюнной железы неуточненной локализации)
D10.3 Доброкачественное новообразование: других и неуточненных частей рта
D11 Доброкачественное новообразование больших слюнных желез
1.5 Классификация заболевания или состояния (группы заболеваний или состояний)
Табл. 1. Международная гистологическая классификация опухолей слюнных желез (ВОЗ, 5-е издание, 2022 г) [10]
Ненеопластические эпителиальные поражения
Доброкачественные эпителиальные опухоли
Эпителиальные злокачественные опухоли
Мезенхимальные опухоли, специфические для слюнных желез
Нодулярная онкоцитарная гиперплазия
Лимфоэпителиальный сиалоаденит
Плеоморфная аденома
Базальноклеточная аденома
Каналикулярная аденома
Опухоль Вартина Онкоцитома
Миоэпителиома
Цистаденома
Сиаладенома
Протоковые папилломы
Лимфаденома Аденома сальных желез
Аденома вставочных протоков
Аденома исчерченных протоков
Склерозирующая поликистозная аденома
Кератоцистома
Мукоэпидермоидная карцинома
Аденокистозная карцинома
Ацинарноклеточная карцинома
Секреторная карцинома
Микросекреторная аденоркацинома
Полиморфная аденокарцинома
Гиалинизирующий светлоклеточный рак
Внутрипротоковая карцинома
Рак протоков слюнных желез
Миоэпителиальная карцинома
Эпителиально-миоэпителиальная карцинома
Склерозирующая микрокистозная аденокарцинома
Карцинома в плеоморфной аденоме
Карциносаркома
Аденокарцинома сальных желез
Лимфоэпителиальная карцинома
Плоскоклеточный рак
Сиалобластома
Карцинома слюнных желез БДУ
Сиалолипома
Комментарий: В рамках 5 пересмотра ВОЗ исключены образования, имеющие локализацию в области железы и прилежащих тканей, такие как: гемангиома, лимфатические мальформации, лимфомы и саркомы. В настоящее время выделяют 4 группы нозологий: ненеопластические эпителиальные поражения СЖ, доброкачественные и злокачественные эпителиальные опухоли и мезенхимальные опухоли, специфические для слюнных желез. Появились новые гистологические подтипы злокачественных образований: микросекреторная, полиморфная и склерозирующая микрокистозная аденокарциномы [10]. Исходя из множество новых данных о молекулярно-генетических особенностях опухолей, новая международная классификация ВОЗ опухолей слюнных желез учитывает типичные перестройки генов, специфичные для конкретного типа опухоли.
Табл. 2. Злокачественные эпителиальные опухоли
Злокачественные эпителиальные опухоли
Ацинарноклеточная карцинома 8550/3
NR4A3 перестройка/активация 86%
MSANTD3 перестройка/амплификация 4%
Мукоэпидермоидная карцинома 8430/3
CRTC1-MAML2 перестройка 40 - 90%
CRTC3-MAML2 перестройка 6%
CDKN2A делеция 25%
Мутации включены в определение подтипа
Аденокистозная карцинома 8200/3
MYB перестройка/активация/амплификация ~ 80% <*>
MYBL1 перестройка/активация/амплификация ~ 10%
NOTCH мутации 14%
Полиморфная аденокарцинома 8525/3
Классический подтип
Крибриформный подтип
PRKD1 мутации 73%
PRKD1 перестройки 38% <*>
PRKD2 перестройки 14% <*>
PRKD3 перестройки 19% <*>
Эпителиально-миоэпителиальная карцинома 8562/3
HRAS мутации 78%
Гиалинизирующий светлоклеточный рак 8310/3
EWSR1-ATF1 перестройки 93% <*>
EWSR1-CREM перестройки < 5%
Базальноклеточная аденокарцинома 8147/3
CYLD мутации 29%
Перестройка CTNNB1
Сальная аденокарцинома 8410/3
MSH2 потеря 10%
Секреторная карцинома 8502/3
ETV6-NTRK3 перестройка > 90% <*>
ETV6-RET перестройка 2 - 5%
ETV6-MET перестройка < 1%
ETV6-MAML3 перестройка < 1%
VIM-RET перестройка < 1%
Микросекреторная аденокарцинома
MEF2C-SS18 перестройка > 90% <*>
Внутрипротоковая карцинома
Карцинома вставочных протоков
Апокриновый подтип
RET перестройки 47%
PIK3CA мутации
HRAS мутации
Рак протоков слюнных желез 8500/3
HER2 амплификация 31%
FGFR1 амплификация 10%
TP53 мутация 56%
PIK3CA мутация 33%
HRAS мутация 33%
AR увеличение копийности 35%
PTEN потеря 38%
CDKN2A потеря 10%
Аденокарцинома, БДУ 8140/3
Миоэпителиальная карцинома 8982/3
PLAG1 перестройки 38%
EWSR1 перестройки 13%
Муцинозная аденокарцинома
папиллярный, коллоидный перстневидный и смешанный подтипы
AKT1 E17K мутации 100% <*>
TP53 мутации 88%
Склерозирующая микрокистозная аденокарцинома
CDK11B мутация (1 случай)
Карцинома в плеоморфной аденоме 8941/3
PLAG1 перестройки/амплификация 73%
HMGA2 перестройки/амплификация 14%
TP53 мутации 60%
Карциносаркома 8980/3
Плоскоклеточный рак 8070/3
Лимфоэпителиальная карцинома 8082/3
Сиалобластома 8974/1
Рак слюнных желез БДУ
Низкодифференцированная карцинома 8020/3
Онкоцитарная карцинома 8290/3
--------------------------------
<*> Мутация включена в определение подтипа.
Комментарий: Биологическое поведение опухоли внутри одного подтипа не одинаково, они могут быть приставлены различными гистологическими вариантами низкой, промежуточной и высокой степени злокачественности. Стратификация по группам риска разработана для мукоэпидермоидной, ацинарноклеточной и аденокистозной карцином и ряда других [10].
Стадирование злокачественных опухолей слюнных желез.
Для оценки распространенности злокачественного опухолевого процесса в слюнных железах используется классификация TNM (8-е издание, 2017 г.). Классификация учитывает размеры первичнои опухоли, наличие/отсутствие пареза мимической мускулатуры, фиксацию опухоли. Классификация первоначально была разработана для опухолей околоушной СЖ, однако в настоящее время применяется для опухолей всех больших СЖ.
Символ T содержит следующие градации:
TX - недостаточно данных для оценки первичной опухоли.
T0 - первичная опухоль не определяется.
T1 - опухоль 2 см или менее в наибольшем измерении без распространения за пределы паренхимы железы
T2 - опухоль более 2 см., но не более 4 см. в наибольшем измерении без распространения за пределы паренхимы железы
T3 - опухоль более 4 см. в наибольшем измерении и/или распространение за пределы паренхимы железы.
T4a - опухоль распространяется на кожу, нижнюю челюсть, слуховой проход и/или лицевой нерв.
T4b - опухоль распространяется на крыловидные отростки, основание черепа или на внутреннюю сонную артерию.
Символ N указывает на наличие или отсутствие метастазов в регионарных ЛУ.
NX - недостаточно данных для оценки регионарных ЛУ. N0 - поражения регионарных ЛУ нет N 1-метастазы в одном ЛУ на стороне поражения не более 3-х см. в наибольшем измерении
N2 - метастазы в одном ЛУ на стороне поражения более 3-х см. но не более 6 см. в наибольшем измерении; или в нескольких ЛУ на стороне поражения не более 6 см. в наибольшем измерении; двухстороннее или контралатеральное поражение ЛУ не более 6 см в наибольшем измерении
N2a - метастазы в одном ЛУ на стороне поражения более 3-х см, но не более 6 см в наибольшем измерении.
N2b - метастазы в нескольких ЛУ на стороне поражения не более 6 см. в наибольшем измерении.
N2c - двухстороннее или контралатеральное метастазы в ЛУ не более 6 см в наибольшем измерении
N3 - метастазы в ЛУ более 6 см в наибольшем измерении
Символ М характеризует наличие или отсутствие отдаленных метастазов.
M0 - отдаленных метастазов нет.
M1 - наличие отдаленных метастазов.
Табл. 3. Группировка по стадиям согласно классификации TNM
Стадия
T
N
M
I
1
0
0
II
2
0
0
III
3
0
0
1
1
0
2
1
0
3
1
0
IVA
4a
0
0
4a
1
0
1
2
0
2
2
0
3
2
0
4a
2
0
IVB
любое T
3
0
4b
любое N
0
IVC
любое T
любое N
1
1.6 Клиническая картина заболевания или состояния (группы заболеваний или состояний)
Доброкачественные опухоли слюнных желез - группа образований с медленным ростом, часто до установления диагноза проходит около 5-ти лет, средний размер - 2,6 см3. Основные жалобы - пальпируемое образование в околоушно-жевательной области, реже встречается поражение лицевого нерва, боль. Тризм и образование боковой стенки глотки характерно для поражения глубокой доли околоушной слюнной железы [4].
Клиническое течение рака СЖ определяется локализациеи, распространенностью и морфологическим строением.
Эпителиальные злокачественные опухоли - группа медленно растущих образований в околоушно-жевательной области или полости рта с крайне низкой потенцией к метастазированию, которые длительное время остаются не диагностированы, в среднем около 8 - 12 месяцев [13]. Это обусловлено анатомическим строением области, стертостью клинических проявлений и редкостью болевого симптома. Основные жалобы пациентов неспецифичны: наличие пальпируемого безболезненного узлового образования в проекции пораженной железы плотно-эластическои консистенции, не спаянного с кожеи - 99%, болезненность в области опухоли - 22% и парез лицевого нерва - 7% [5]. Явления пареза мимической мускулатуры являются крайне неблагоприятным прогностическим признаком, свидетельствующим о местной распространенности процесса [4].
Новообразования могут быть расположены поверхностно или в глубоких отделах СЖ. Злокачественные опухоли глоточного отростка околоушной слюнной железы, несмотря на медленное течение, довольно рано инфильтрируют слизистую глотки.
Средний возраст пациентов составляет 14 лет, с некоторым преобладанием пациентов женского пола, в соотношении 1,4:1 [2, 4, 14, 15]. МЭК у детей в 87% представлена опухолями с низким и промежуточным потенциалом злокачественности. Значительную роль в прогнозе имеет степень злокачественности опухоли. Общая пятилетняя выживаемость составляет 93%, а безрецидивная - 82%, соответственно. В среднем рецидив отмечается через 1 год и 1 месяц после хирургического лечения [5].
2. Диагностика заболевания или состояния (группы заболеваний или состояний) медицинские показания и противопоказания к применению методов диагностики
Для диагностики злокачественных эпителиальных опухолей слюнных желез в детском возрасте необходимо использовать весь комплекс диагностических мероприятий:
1) сбор анамнеза и анализ жалоб пациента;
2) тщательный клинический осмотр, пальпация образования и прилежащих тканей и регионарных ЛУ;
3) УЗИ слюнных желез, мягких тканей лица, лимфатических коллекторов шеи;
4) КТ с контрастным усилением при подозрении на поражение костей основания черепа или челюсти, рецидиве опухоли;
5) МРТ с контрастным усилением для уточнения топики процесса при больших размерах опухоли (T3 - T4), рецидиве заболевания, поражении глоточного отростка ОСЖ, подозрении на интракраниальное распространение;
6) ТПАБ под контролем УЗИ с последующим цитологического исследования биопсийного материала (первичной опухоли, увеличенных или подозрительных ЛУ);
7) рентгенография или МСКТ органов грудной клетки;
8) сцинтиграфию костей скелета при первичной диагностике;
9) патолого-анатомического исследования операционного материала с применением иммуногистохимических методов [5].
Алгоритм обследования при доброкачественных опухолях:
1) сбор анамнеза и анализ жалоб пациента;
2) тщательный клинический осмотр, пальпация образования и прилежащих тканей и регионарных ЛУ;
3) УЗИ слюнных желез, мягких тканей лица, лимфатических коллекторов шеи;
4) МРТ с контрастным усилением для уточнения топики процесса при больших размерах опухоли, рецидиве заболевания, поражении глоточного отростка ОСЖ;
5) ТПАБ под контролем УЗИ с последующим цитологического исследования биопсийного материала (первичной опухоли);
6) патолого-анатомического исследования операционного материала с применением иммуногистохимических методов [5].
Дифференциальную диагностику опухолеи СЖ необходимо проводить внутри самой группы на доброкачественные и злокачественные, а так же с врожденными пороками головы и шеи, сосудистыми поражениями, лимфатическими мальформациями, воспалительными процессами, актиномикозом, туберкулезом, неспецифическими лимфаденопатиями, аутоиммунными заболеваниями. Нельзя также упускать из вида возможность метастатического поражения околоушных, подчелюстных и верхних югулярных лимфатических узлов, при других злокачественных новообразованиях, в первую очередь при раке носоглотки и ретинобластоме, лимфоме.
2.1 Жалобы и анамнез
- Рекомендуется проводить тщательный сбор анамнеза: опрос родителей и пациента (если позволит возраст); учет жалоб ребенка, места жительства до появления признаков заболевания, случаев онкологических заболевании ребенка и родственников, вредные воздействия на организм матери во время беременности и на ребенка, указании на врожденный характер заболевания. При расспросе родителей и пациента рекомендуется обратить внимание на время появления деформации лица, подчелюстнои области, скорость внешних изменении, наличие жалоб, оценить функцию мимической мускулатуры, наличие тризма [1, 2]. Основные жалобы пациентов: наличие медленно растущего образования в околоушно-жевательной области - 99%, болезненность в области опухоли - 22% и парез лицевого нерва - 7% [7].
Уровень убедительности рекомендаций - B (уровень достоверности доказательств - 2)
2.2 Физикальное обследование
Если врач-педиатр (или другой специалист) подозревает по результатам наружного осмотра и пальпации узловое поражение СЖ, то необходимо направить пациента в специализированную клинику (клинику челюстно-лицевой хирургии или детский онкологическии центр).
- Рекомендуется всем пациентам с подозрением на опухоль СЖ или с верифицированной опухолью СЖ провести наружный осмотр, измерения роста, массы тела, уровня физического развития [1, 2].
Уровень убедительности рекомендации - C (уровень достоверности доказательств - 5)
- Рекомендуется всем пациентам с подозрением на опухоль ДЖ или с верифицированной опухолью СЖ провести пальпацию околоушной или подчелюстнои СЖ, оценить подвижность узла, выявить наличие или отсутствие инфильтрации в области опухоли СЖ, оценить величину, подвижность лимфатических узлов шеи [1, 2].
Уровень убедительности рекомендации - C (уровень достоверности доказательств - 5)
- Рекомендуется всем пациентам с подозрением на опухоль СЖ или с верифицированной опухолью СЖ обратить внимание на наличие и выраженность нарушения функции лицевого нерва (парез, паралич), степени открывания рта (тризм), затруднения глотания [1, 2].
Уровень убедительности рекомендации - C (уровень достоверности доказательств - 5)
2.3 Лабораторные диагностические исследования
- Рекомендуется при госпитализации выполнение общего (клинического) анализа крови развернутого с обязательным дифференцированным подсчетом лейкоцитов (лейкоцитарная формула), для оценки состояния пациента и выработки тактики ведения пациента [54].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 5).
- Всем пациентам при госпитализации рекомендуется выполнение анализа крови биохимического общетерапевтического (мочевина, креатинин, общий белок, общего и связанного билирубина, глюкоза, лактатдегидрогеназа (ЛДГ), амилаза, аланинаминотрансфераза (АЛТ), аспартатаминотрансфераза (АСТ), натрий, калий, кальций) для уточнения распространенности заболевания и оценки состояния пациента, в том числе отдельных органов и систем [53].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 5).
- Всем пациентам рекомендуется выполнение коагулограммы (ориентировочное исследование системы гемостаза) для оценки состояния пациента и диагностики/определения вероятности развития тяжелых геморрагических/тромботических осложнений [53].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 5).
- Всем пациентам рекомендуется выполнение общего (клинического) анализа мочи для диагностики возможной сопутствующей патологии и определения тактики сопроводительной терапии [53].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 5).
- Всем пациентам рекомендуется определение основных групп крови по системе AB0, определение антигена D системы Резус (резус-фактор), определение фенотипа по антигенам C, c, E, e, Cw, K, k с целью проведения заместительной терапии компонентами крови при необходимости [53].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 5).
2.4 Инструментальные диагностические исследования
- Всем пациентам СТРОГО рекомендуется выполнить ультразвуковое исследование слюнных желез, ультразвуковое исследование лимфатических узлов (одна анатомическая зона) шеи с тонкоигольной биопсией образования околоушной слюнной железы (и тонкоигольной биопсией лимфатических узлов при подозрении на их поражение при подозрении на злокачественный процесс) с последующим цитологическим исследованием микропрепаратов тонкоигольной аспирационной биопсии с целью верификации природы новообразования и выявления возможного специфического поражения лимфатических узлов [11 - 17].
Уровень убедительности рекомендаций - B (уровень достоверности доказательств - 3)
- Рекомендуется всем пациентам с подозрением на злокачественное образование слюнных желез выполнить магнитно-резонансную томографию мягких тканей головы и магнитно-резонансную томографию шеи с внутривенным контрастированием и строго рекомендуется при подозрении на поражение основания черепа, периневральном росте (поражение ЧМН), интракраниальном распространении, рецидиве или продолженном росте [18 - 21].
Уровень убедительности рекомендаций - B (уровень достоверности доказательств - 2)
- Рекомендуется выполнить компьютерную томографию лицевого отдела черепа с внутривенным болюсным контрастированием всем пациентам при подозрении на поражение костных структур (верхней/нижней челюсти, основания черепа) [22].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 5)
- Всем пациентам с злокачественными образованиями рекомендуется выполнить компьютерную томографию органов грудной клетки с целью поиска возможного вторичного специфического поражения легких [9 - 15].
Уровень убедительности рекомендаций - B (уровень достоверности доказательств - 3)
- Рекомендуется выполнить остеосцинтиграфию всем пациентам со злокачественными образованиями слюнных желез при подозрении на метастатическое поражение костей скелета [21 - 23].
Уровень убедительности рекомендаций - B (уровень достоверности доказательств - 2)
- Рекомендуется проведение позитронной эмиссионной томографии всего тела с туморотропными РФП пациентам только на поздних стадиях болезни для уточнения регионарного и отдаленного метастазирования [23, 24]. Проведение позитронно-эмиссионной томографии (ПЭТ/КТ) с фтордезоксиглюкозой (ФДГ) на начальных стадиях опухолей слюнных желез не показано [25].
Уровень убедительности рекомендаций - B (уровень достоверности доказательств - 2)
- Рекомендуется выполнить ультразвуковое исследование органов брюшной полости (комплексное) и ультразвуковое исследование забрюшинного пространства всем пациентам со злокачественными опухолями слюнных желез с высоким потенциалом злокачественности, такие как аденокарцинома [4, 17, 20].
Уровень убедительности рекомендаций - B (уровень достоверности доказательств - 3)
2.5 Иные диагностические исследования
- Рекомендуется проводить цитологическое исследование микропрепарата тканей слюнных желез всем пациентам при проведении тонкоигольной биопсии образования слюнных желез с целью верификации природы новообразования. Она признана минимально инвазивным и эффективным способом диагностики [11 - 16].
Уровень убедительности рекомендаций - B (уровень достоверности доказательств - 3)
- Рекомендуется проведение толстоигольной (CNB-core needle biopsy) биопсии пациентам с опухолями малых слюнных желез или недиагностической предшествующей тонкоигольной биопсии образования околоушной слюнной железы с целью верификации природы образования [26 - 28].
Уровень убедительности рекомендаций - A (уровень достоверности доказательств - 2)
Комментарий: возможно не проводить ТАБ с последующим цитологическим исследованием у ранее оперированных больных, при наличии ранее установленного гистологически верифицированного диагноза.
- Рекомендуется в заключении цитологического исследования указать риск злокачественного образования (ROM - risk of malignancy) согласно Миланской системе интерпретации результатов цитологического исследования (Milan System for Reporting Salivary Gland Cytopathology (MSRSGC) [29 - 32]: недиагностический материал, неопухолевый процесс, атипии неуточненной значимости, подозрительный на злокачественные и злокачественное образование. При возможности установить степень злокачественности: низкую (low grade) или высокую степень (high grade) [30].
Уровень убедительности рекомендаций - A (уровень достоверности доказательств - 2)
- Рекомендуется проведение открытой биопсии при недиагностической предшествующей ТАБ и/или толстоигольной биопсии (CNB-core needle biopsy), подозрении на неэпителиальные злокачественные опухоли СЖ (резкий рост образования, вовлечение близлежащих тканей, локализация очага вне тканей железы, метастатическое поражение), необходимость получения материала для проведения молекулярно-генетических методов исследования при неоперабельных опухолях [4, 25].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 4)
Комментарий: При обширных поражениях околоушной слюнной железы с вовлечением поверхностной и глубокой долей, подозрением на вовлечение лицевого нерва после 2-хкратной верификации отсутствия злокачественных клеток по результатам цитологического исследования показана дополнительная гистологическая верификация путем биопсии новообразования открытым способом.
- Рекомендуется всем пациентам проводить патолого-анатомическое исследование биопсийного (операционного) материала тканей слюнной железы с применением иммуногистохимических методов удаленного опухолевого препарата и отразить следующие параметры [4]:
1. Размеры опухоли;
2. Глубина инвазии опухоли
3. Гистологическое строение опухоли;
4. Степень дифференцировки опухоли;
5. Оценка краев резекции
6. Наличие лимфоваскулярной, периневральной инвазии (отрицательный результат также должен быть констатирован)
7. pT;
8. pN (с указанием общего числа исследованных и пораженных лимфоузлов, признаков экстранодального распространения опухоли);
Комментарий: пункты 6 - 8 применимы для злокачественных образований, указывать при доброкачественном опухолевом процессе не требуется.
- Рекомендуется провести цитогенетическое исследование биопсийного (операционного) материала пациентам при метастатической форме, неоперабельном случае, при секреторной карциноме, с целью поиска молекулярных мишеней для последующего назначения молекулярно-направленной терапии, а так же в сложных диагностических случаях для поиска мутации как критерия подтипа опухоли [10].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 5)
3. Лечение, включая медикаментозную и немедикаментозную терапии, диетотерапию, обезболивание, медицинские показания и противопоказания к применению методов лечения
3.1 Хирургическое лечение
- Рекомендуется рассматривать хирургическое вмешательство как основной метод радикального лечения пациентов с эпителиальными злокачественными новообразованиями слюнных желез [16,17]. Энуклеация опухоли приводит к продолженному росту и не может рассматриваться как метод лечения [33]. Вмешательство должно проводится в специализированном онкологическом центре [16, 17, 33].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 4)
- Рекомендовано избрать основным методом лечения доброкачественных опухолей - хирургический, в объеме частичная резекция, паротидэктомии или субтотальной резекции с выделением и сохранением лицевого нерва. Вмешательство должно быть проведено в специализированном центре врачом-онкологом, челюстно-лицевым или пластическим хирургом, показания к использованию нейрофизиологического мониторинга остаются актуальными [3, 4].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 4)
- Рекомендуется применение интраоперационного нейрофизиологического мониторинга лицевого нерва, которое строго показано при опухолях больших размеров (T3 - T4), рецидиве опухоли, проведении реоперации, расширенных резекциях с включением в костей основания черепа, а так же при планировании одномоментной реконструкции лицевого нерва и его ветвей [48, 52].
Уровень убедительности рекомендаций - B (уровень достоверности доказательств - 2)
Применимо при лечении злокачественных образований:
При T1 - T2, N0:
- Рекомендуется удаление образований околоушной слюнной железы с выделением и сохранением ветвей лицевого нерва с интраоперационным использованием нейрофизиологического мониторинга лицевого нерва [39, 40, 52].
Уровень убедительности рекомендации - C (уровень достоверности доказательств - 4)
- Пациентам с обнаруженными пораженными лимфоузлами внутри железы рекомендована лимфаденэктомия шейная (IA, II A, IIB и III коллекторов) [39, 40].
Уровень убедительности рекомендации - C (уровень достоверности доказательств - 4)
- Профилактическая лимфаденэктомия шейная на стороне поражения рекомендуется пациентам, у которых в плановом гистологическом исследовании выявлена опухоль с высоким потенциалом злокачественности [39, 40].
Уровень убедительности рекомендации - C (уровень достоверности доказательств - 4)
- При выявлении при плановом патолого-анатомическом исследовании операционного материала опухолеи с высоким потенциалом злокачественности (Hight-grade), положительных краев резекции или периневральнои инвазии рекомендуется рассмотреть вопрос о проведении послеоперационнои ДЛТ [25].
Уровень убедительности рекомендации - C (уровень достоверности доказательств - 4)
- Не рекомендуется проведение профилактической лимфодиссекции у пациентов с опухолями с низким и промежуточным потенциалом злокачественности (кроме пациентов с обнаруженными пораженными лимфоузлами внутри) [39, 40].
Уровень убедительности рекомендации - C (уровень достоверности доказательств - 4)
При T1 - 2, N + M0:
- Рекомендовано полное удаление образований околоушной слюнной железы с выделением и сохранением ветвей лицевого нерва с интраоперационным использованием нейрофизиологического мониторинга лицевого нерва [39, 40, 52]
Уровень убедительности рекомендации - C (уровень достоверности доказательств - 4)
- При обнаружении пораженных лимфоузлов внутри железы рекомендовано проведение лимфаденэктомии шейной (IA, II A, IIB и III коллекторов) [39, 40].
Уровень убедительности рекомендации - C (уровень достоверности доказательств - 4)
- При выявлении при плановом патолого-анатомическом исследовании операционного материала опухолеи с высоким потенциалом злокачественности (Hight-grade), положительных краев резекции или периневральнои инвазии рекомендовано рассмотреть вопрос о проведении послеоперационнои ДЛТ [25].
Уровень убедительности рекомендации - C (уровень достоверности доказательств - 4)
При T3 - 4a, N0 M0:
- Рекомендовано полное удаление образований околоушной слюнной железы с выделением и сохранением ветвей лицевого нерва с обязательным интраоперационным использованием нейрофизиологического мониторинга лицевого нерва в сочетании с шейной лимфаденэктомией шейной со стороны поражения IA, II A, IIB, III и IV коллекторов [39, 40, 52].
Уровень убедительности рекомендации - C (уровень достоверности доказательств - 4)
- В случае выявления при плановом патолого-анатомическом исследовании операционного материала неблагоприятных гистологических признаков (средне-, низкодифференцированная опухоль, положительные края, периневральная инвазия, сосудистая эмболия) рекомендовано рассмотреть вопрос о проведении конкурентной химиолучевой терапии (ХЛТ) [7].
Уровень убедительности рекомендации - C (уровень достоверности доказательств - 4).
При T3 - 4a N + M0:
- Рекомендовано полное удаление образований околоушной слюнной железы с выделением и сохранением ветвей лицевого нерва с обязательным интраоперационным использованием нейрофизиологического мониторинга лицевого нерва в сочетании с шейной лимфаденэктомией шейной расширенной со стороны поражения [39, 40, 52].
Уровень убедительности рекомендации - C (уровень достоверности доказательств - 4)
- В послеоперационном периоде рекомендовано проведение послеоперационной ЛТ [24, 25].
Уровень убедительности рекомендаций - B (уровень достоверности доказательств - 2)
При стадии T4b:
- При невозможности выполнения радикального оперативного вмешательства на первом этапе рекомендовано проведение цитогенетическое исследование биопсийного (операционного) материала с целью поиска молекулярных мишеней для таргетной терапии или проведение ДЛТ, а так же иных комбинаций, по результатам федерального онкологического консилиума [10].
Уровень убедительности рекомендаций - B (уровень достоверности доказательств - 2)
Локорегионарный рецидив:
- Рекомендовано паротидэктомия радикальная с реконструктивно-пластическим компонентом с обязательным интраоперационным использованием нейрофизиологического мониторинга лицевого нерва [39, 40, 52].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 4)
- При невозможности выполнения радикального оперативного вмешательства рекомендовано выполнение цитогенетического исследования биопсийного (операционного) материала для поиска молекулярных мишеней и последующего назначения таргетной терапии, возможно рассмотреть вопрос о назначении конкурентной ХЛТ по результатам онкологического консилиума в федеральном центре [7].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 5)
При первичном нерадикальном хирургическом лечении
- Рекомендовано получение консультации онкологического консилиума в федеральном центре для решения вопроса о проведении повторного ревизионного хирургического вмешательства (second-look операцию) или назначения ЛТ [39].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 5)
Комментарий: Для опухолей с низким и промежуточным потенциалом злокачественности у детей и подростков край резекции 2 мм и более приводит к хорошему контролю над заболеванием [43, 45]. Для опухолей с высоким потенциалом злокачественности (аденокистозного рака) достаточный край резекции считается 5 мм и более. Показана одномоментная биопсия подозрительных лимфоузлов по результатам предоперационного обследования. При пересечении ветвей лицевого нерва во время паротидэктомии выполнять одномоментную пластику нерва путем его сшивания и/или использования аутотрансплантатов из большого ушного или сурального нервов или иных видов пластики [45].
3.2 Принципы лучевой терапии (данный раздел применим для злокачественных образований эпителиального происхождения).
- Рекомендуется рассматривать ЛТ, как важный инструмент в лечении злокачественных эпителиальных опухолей слюнных желез [37].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 5)
- Подходы к лучевой терапии у детей рекомендуется основывать на тех же принципах, что и при проведении ЛТ у взрослых [52, 53].
Уровень убедительности рекомендаций - С (уровень достоверности доказательств - 5)
- ЛТ рекомендована при следующих состояниях [52, 53]:
- низкодифференцированный характер первичной опухоли;
- прорастание опухолью окружающих тканей (основание черепа, мягкие ткани лица);
- наличие метастазов в области шеи;
- наличие опухолевых клеток по краю резекции
- разрыв опухоли во время операции;
- большой остаток опухоли после операции при невозможности его удаления;
- наличие гистологических признаков агрессивного характера опухоли, к примеру, периневральная инвазия, типичная для аденокистозного рака;
- инвазия опухоли в сосуды или лимфатические узлы;
- местное экстрагландулярное распространение на мягкие ткани;
- неоперабельность
Комментарий: технические требования к оборудованию для ДЛТ.
1) Линейный ускоритель электронов с энергией фотонов 6 - 10 МэВ, оснащенный многолепестковым коллиматором и, крайне желательно, системой/системами визуального контроля укладки: компьютерной томографией в коническом пучке (CBCT), портальной визуализацией. Возможно применение протонотерапии сканирующим пучком с использованием методов контроля укладки пациента перед сеансом облучения.
2) Фиксирующие приспособления для головы и тела (термопластические маски, вакуумные матрасы и др.).
3) Рентгеновский компьютерный томограф для топометрии, имеющий плоскую деку с возможностью крепления и индексацией систем фиксации.
4) Система 3D планирования облучения и, крайне желательно, с возможностью расчета облучения с применением методик модулированной по интенсивности лучевой терапии в статическом и динамическом режимах (IMRT/VMAT).
Предлучевую подготовку следует проводить в объеме:
- Выполнение КТ-топометрии должно проводиться на рентгеновском компьютерном томографе, приспособленном для нужд радиотерапии.
- Разметка проводится с использованием индивидуальных средств фиксации: термопластических масок и, возможно, вакуумного матраса.
- В область сканирования должна входить вся голова, шея и средостение до уровня бифуркации трахеи. Сканирование проводится с толщиной среза: 1 - 3 мм,
- Величина поля изображения (Field Of View, FOV) должна быть адекватной для включения всех частей тела и систем фиксации.
- Необходимо предусмотреть, что при топометрии и лучевой терапии пациентов младше 5 лет может потребоваться общая анестезия.
- Планирование проводится на нативной серии КТ-топометрии.
- Применение методик IMRT [2] или протонотерапии [3] сканирующим пучком предпочтительнее
- Рекомендовано учитывать следующие принципы ЛТ [52, 54]:
В случае назначения ЛТ в самостоятельном варианте
- Зона высокого риска: первичная опухоль, а также пораженные лимфатические узлы
- Фракционирование: 66 Гр (2,0 Гр/фракция) ежедневно [52, 54]
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 4)
- Зоны промежуточного и низкого риска: места, предполагаемого субклинического распространения
- Фракционирование: 44 - 50 Гр (2,0 Гр/фракция) ежедневно [52, 54]
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 4)
В качестве послеоперационной ЛТ
Предпочтительный интервал между резекцией и послеоперационной ЛТ составляет менее 6 недель.
- Зона высокого риска: положительные края резекции
- Фракционирование: от 66 Гр (2,0 Гр/фракция) ежедневно [52, 54]
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 4)
- Зоны промежуточного и низкого риска: места, предполагаемого субклинического распространения
- Фракционирование: от 44 - 50 Гр (2,0 Гр/фракция) ежедневно [52, 54]
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 4)
Объем
Определение и описание
GTV66
Околоушная или подчелюстная слюнная железа: остаточная опухоль или ложе удаленной опухоли.
Шейные л\узлы: все л\узлы более одного 1 см в аксиальной плоскости или с некротическим центром
CTV66
GTV66 + 5 мм = CTV66
PTV66
Обычно CTV66 + 3 - 5 мм = PTV66.
Табл. 4. Зона высокого риска
Табл. 5. Зоны промежуточного и низкого риска
Объем
Определение и описание
CTV50
CTV50 должна охватывать всю GTV или ложе удаленной опухоли.
Границы послеоперационного поля околоушной железы:
Передняя - жевательная мышца
Латеральная - мягкие ткани шеи
Медиально - шиловидный отросток
Задняя - сосцевидная кость
Опухоли околоушных желез: включают лицевой нерв, языкоглоточный нерв и тройничный; может потребоваться распространиться на пещеру Меккеля
Подчелюстные и подъязычные опухоли: требуется распространить на пещеру Меккеля, особенно при аденокистозной карциноме.
CTVл\у
Выборочно облучить остальную часть шеи (уровни Ib - V) до 50 Гр; рассмотреть возможность исключения уровня V и IVb
PTVл\у
Обычно CTVл\у + 5 мм = PTVл\у
Дозы: D95 = 95% объема.
D max = максимальная доза на 0,03 куб. см объема
Табл. 6. Ограничение дозы
Структуры
Ограничение дозы
Кости
Max < 70 Гр
нижняя челюсть
D 0.03 сс < 70 Гр
ВНЧС
D 0.03 сс 66 - 70 Гр
Плечевое сплетение
D 0.03 сс 54 - 58 Гр
Спинной мозг
Max 45 Гр
Max_PRV (Cord + 5 мм) 48 Гр
Околоушная
Mean dose < 26 Гр
Подчелюстные железы
Mean dose < 39 Гр or 40 Гр
Полость рта, за исключением PTV
Mean dose of < 32 Гр
Пищевод
Mean dose < 30 Гр
Улитка
Mean < 35 Гр Max < 55 Гр
Губы
Mean < 20 Гр
Гортань
Mean < 35 Гр
Хиазма
< 55 Гр D0.03 cc (Гр)
Оптические нервы
Max 55 Гр D0.03 cc (Гр)
Хрусталики
< Max 55 Гр D0.03 cc (Гр)
Комментарий: Имеются данные, что протонная терапия может иметь преимущества в отношении острой токсичности и дозовых характеристиках [38].
3.3. Химиотерапевтическое лечение (данный раздел применим для злокачественных образований).
- Химиотерапия при опухолях СЖ может быть рекомендована по результатам федерального консилиума после проведения молекулярно-генетического исследования с поиском молекулярных мишеней для последующего назначения молекулярно-направленной терапии в случаях:
- секреторных карцином
- при наличии неоперабельнои опухоли
- и/или отдаленных метастазов [27, 28], когда опции хирургического лечения и лучевой терапии исчерпаны [6, 39, 40].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 5)
4. Медицинская реабилитация и санаторно-курортное лечение, медицинские показания и противопоказания к применению методов медицинской реабилитации, в том числе основанных на использовании природных лечебных факторов
- Рекомендуется включить в план реабилитационных мероприятии на всем протяжении специального лечения оказание социально-педагогическои помощи пациенту, а также социально-психологическую поддержку семьи [1, 4, 38].
Уровень убедительности рекомендации - C (уровень достоверности доказательств - 5)
- Рекомендуется диспансерное наблюдение пациентов со злокачественными образованиями СЖ врачом-детским онкологом, при доброкачественных образованиях врачом-челюстно-лицевым хирургом или врачом-детским хирургом (до достижения пациентом возраста 18 лет), а также врачом-неврологом, врачом-офтальмологом, реабилитологом (врачом лечебной физкультуры), клиническим психологом при наличии пареза лицевого нерва [1, 4].
Уровень убедительности рекомендации - C (уровень достоверности доказательств - 5)
Комментарии: Важным моментом в реабилитации пациентов после операции по поводу опухолеи СЖ является восстановление функции лицевого нерва. При парезе ветвеи лицевого нерва показано проведение гимнастики и стимулирующеи терапии для лицевых мышц, которую пациент может проводить под контролем логопеда и специалиста по лечебнои физкультуре и невролога. При параличе лицевого нерва могут быть применены методики пластики лицевого нерва.
- Рекомендуется при выборе метода лечения парезов и параличеи мимическои мускулатуры ориентироваться на их длительность [4]:
1. при выполнении паротидэктомии и пересечении ветвеи лицевого нерва выполнять одномоментную пластику нерва путем его сшивания, а также использования аутотрансплантатов из большого ушного или сурального нервов;
2. при лечении параличеи мимическои мускулатуры в сроки до 2-х лет проводить неи ропластику с использованием жевательнои ветви тройничного нерва, нисходящей ветви подъязычного нерва, кросс-пластику или их комбинации;
3. при длительности паралича мимическои мускулатуры более 2-х лет и отсутствии нейромышечной активности по данным электромиографии выполнять: транспозицию височной мышцы, пластику с использованием васкуляризированных мышечных трансплантатов (например, струйной мышцей), статические методы коррекции, ботулинотерапию.
Уровень убедительности рекомендации - C (уровень достоверности доказательств - 5)
5. Профилактика и диспансерное наблюдение, медицинские показания и противопоказания к применению методов профилактики
Необходим контроль над группами "риска", к которым отнесены дети и подростки проживающие в регионах с развитой деревообрабатывающей промышленностью, если в анамнезе ребенку проводилась ЛТ на область головы и шеи, также получавших терапию радиоактивным йодом по поводу рака щитовидным железы, проводилась полихимиотерапия.
5.1 Диспансерное наблюдение
- Всем пациентам рекомендованы периодичные контрольные обследования: в первыи год - каждые три месяца; в течение пяти лет - не реже одного раза в полгода; последующие годы - не реже одного раза в год (пожизненно для пациентов со злокачественными опухолями) [53].
Уровень убедительности рекомендации - C (уровень достоверности доказательств - 5)
Комментарий: Объем диагностических мероприятии при контрольных обследованиях включает:
1. общее клиническое обследование;
2. Ультразвуковое исследование слюнных желез и ультразвуковое исследование лимфатических узлов (одна анатомическая зона) шеи;
3. УЗИ органов брюшной полости и забрюшинного пространства;
4. Компьютерную томографию легких не реже 1 раза в год (для пациентов со злокачественными опухолями);
5. Магнитно-резонансная томография мягких тканей головы с внутривенным контрастированием
6. Трехфазная сцинтиграфия мягких тканей и костей не реже 1 раза в год (для пациентов со злокачественными опухолями)
7. Электромиография мимическои мускулатуры с двух сторон при наличии пареза лицевого нерва через 3, 6 месяцев и 1 год
Дальнейшее ведение: наблюдение онколога или челюстно-лицевого хирурга (при доброкачественных опухолях).
6. Организация оказания медицинской помощи
Показания для госпитализации в медицинскую организацию в экстренном порядке:
1. Явления кровотечения с признаками угрозы жизни для пациента.
2. Обтурация верхних дыхательных путей с показаниями для трахеостомии.
3. Острая потеря сознания, кома.
4. Явления компрессии с развитием синдрома сдавления верхней полой вены.
5. Явления остро-возникшего поражения лицевого нерва на стороне поражения
Показания для госпитализации в медицинскую организацию в плановом порядке:
1. Проведение уточняющей диагностики.
2. Проведение этапов специального лечения (хирургического, лучевого, лекарственного).
3. Симптоматическая терапия.
4. Проведение хирургических методов реабилитации, проведение ботулинотерапии при поражениях лицевого нерва
Комментарий: особенности организации специализированной медицинской помощи описаны в разделе А3.
7. Дополнительная информация (в том числе факторы, влияющие на исход заболевания или состояния)
1. В период лечения вакцинация не проводится (исключение составляет вакцинация против гепатита В)
2. Возможность пребывания в организованном коллективе не ограничена, за исключением случаев тяжелого соматического состояния
3. Физические нагрузки исключаются на период лечения, а также в течение 1 месяца после хирургического лечения или более, при наличии осложнений, ограничивающих физическую активность ребенка.
4. Возможен перевод ребенка на домашнее обучения при сохраняющихся признаках поражения лицевого нерва, проблемах в коммуникации со сверстниками, а также глотания и жевания по желанию пациента/законного представителя.
5. Не рекомендуется инсоляция, электромиостимуляции околоушно-жевательной области у пациентов со злокачественными образованиями СЖ в течение первых 5-ти лет.
Критерии оценки качества медицинской помощи
N п/п
Критерии качества
Оценка выполнения
1.
Выполнена тонкоигольная/толстоигольная аспирационная биопсия опухоли и/или измененных регионарных лимфоузлов с последующим цитологическим исследованием (при установлении диагноза) или референс гистологического материала при продолженном росте/рецидиве заболевания
Да/Нет
2.
Выполнено ультразвуковое исследование слюнных желез и/или компьютерная томография лицевого скелета и/или магнитно-резонансная томография основания черепа инициально (при установлении диагноза)
Да/Нет
3.
Выполнено ультразвуковое исследование шеи (при установлении диагноза злокачественного образования)
Да/Нет
4.
Выполнена компьютерная томография органов грудной клетки (при установлении диагноза злокачественного образования)
Да/Нет
5.
Выполнено морфологическое и/или иммуногистохимическое исследование препарата удаленных тканей (при хирургическом вмешательстве)
Да/Нет
6.
Выполнено хирургическое лечение, предусмотренное стадией заболевания (исключение: случай госпитализации, включающий проведение лучевой терапии - выбирается ответ "не применимо)
Да/Нет/не применимо
7.
Проведен онкологический консилиум при необходимости проведения лучевой или химиотерапии
Да/Нет/не применимо
8.
Указан план диспансерного наблюдения при выписке пациента с указанием сроков и методов контрольного исследования
Да/Нет
Список литературы
1. Mozaffari H.R. et al. Malignant salivary gland tumors and Epstein-Barr virus (EBV) infection: A systematic review and meta-analysis // Asian Pacific Journal of Cancer Prevention. Asian Pacific Organization for Cancer Prevention, 2017. Vol. 18, N 5. P. 1201 - 1206.
2. Whatley W.S., Thompson J.W., Rao B. Salivary gland tumors in survivors of childhood cancer // Otolaryngology - Head and Neck Surgery. Mosby Inc., 2006. Vol. 134, N 3. P. 385 - 388.
3. Ethunandan M. et al. Parotid neoplasms in children: experience of diagnosis and management in a district general hospital // Int J Oral Maxillofac Surg. Churchill Livingstone, 2003. Vol. 32, N 4. P. 373 - 377.
4. Fu H. et al. Pleomorphic adenoma of the salivary glands in children and adolescents // J Pediatr Surg. W.B. Saunders, 2012. Vol. 47, N 4. P. 715 - 719.
5. De Ribeiro K.C.B. et al. Epithelial salivary glands neoplasms in children and adolescents: a forty-four-year experience // Med Pediatr Oncol. Med Pediatr Oncol, 2002. Vol. 39, N 6. P. 594 - 600.
6. Yoshida E.J. et al. Salivary gland malignancies in children // Int J Pediatr Otorhinolaryngol. Elsevier, 2014. Vol. 78, N 2. P. 174 - 178.
7. Zamani M. et al. Survival and characteristics of pediatric salivary gland cancer: A systematic review and meta-analysis // Pediatric Blood and Cancer. John Wiley and Sons Inc., 2019. Vol. 66, N 3.
8. Laikui L. et al. Epithelial salivary gland tumors of children and adolescents in west China population: a clinicopathologic study of 79 cases // Journal of Oral Pathology & Medicine. John Wiley & Sons, Ltd, 2008. Vol. 37, N 4. P. 201 - 205.
9. Liu B. et al. Pediatric parotid tumors: Clinical review of 24 cases in a Chinese population // Int J Pediatr Otorhinolaryngol. 2012. Vol. 76, N 7. P. 1007 - 1011.
10. 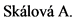 , Hyrcza M.D., Leivo I. Update from the 5th Edition of the World Health Organization Classification of Head and Neck Tumors: Salivary Glands // Head Neck Pathol. Springer, 2022. Vol. 16, N 1. P. 40 - 53.
, Hyrcza M.D., Leivo I. Update from the 5th Edition of the World Health Organization Classification of Head and Neck Tumors: Salivary Glands // Head Neck Pathol. Springer, 2022. Vol. 16, N 1. P. 40 - 53.
11. Ashraf A. et al. Diagnostic reliability of FNAC for salivary gland swellings: A comparative study // Diagn Cytopathol. John Wiley & Sons, Ltd, 2010. Vol. 38, N 7. P. 499 - 504.
12. Carrillo J.F. et al. Diagnostic accuracy of fine needle aspiration biopsy in preoperative diagnosis of patients with parotid gland masses // J Surg Oncol. John Wiley & Sons, Ltd, 2009. Vol. 100, N 2. P. 133 - 138.
13. Eytan D.F. et al. Utility of preoperative fine needle aspiration in parotid lesions // Laryngoscope. John Wiley & Sons, Ltd, 2018. Vol. 128, N 2. P. 398 - 402.
14. Fakhry N. et al. Fine needle aspiration cytology and frozen section in the diagnosis of malignant parotid tumours // Int J Oral Maxillofac Surg. Churchill Livingstone, 2014. Vol. 43, N 7. P. 802 - 805.
15. Gudmundsson J.K., Ajan A., Abtahi J. The accuracy of fine-needle aspiration cytology for diagnosis of parotid gland masses: a clinicopathological study of 114 patients // J Appl Oral Sci. J Appl Oral Sci, 2016. Vol. 24, N 6. P. 561 - 567.
16. Altin F. et al. Is fine needle aspiration biopsy reliable in the diagnosis of parotid tumors? Comparison of preoperative and postoperative results and the factors affecting accuracy // Braz J Otorhinolaryngol. Elsevier, 2019. Vol. 85, N 3. P. 275 - 281.
17. Rzepakowska A. et al. The differential diagnosis of parotid gland tumors with high-resolution ultrasound in otolaryngological practice // European Archives of Oto-Rhino-Laryngology. Springer Verlag, 2017. Vol. 274, N 8. P. 3231 - 3240.
18. Inohara H. et al. The role of fine-needle aspiration cytology and magnetic resonance imaging in the management of parotid mass lesions // Acta Otolaryngol. 2008. Vol. 128, N 10. P. 1152 - 1158.
19. Liu Y. et al. Accuracy of diagnosis of salivary gland tumors with the use of ultrasonography, computed tomography, and magnetic resonance imaging: a meta-analysis // Oral Surg Oral Med Oral Pathol Oral Radiol. Mosby, 2015. Vol. 119, N 2. P. 238 - 245. e2.
20. Alibek S. et al. The Value of Dynamic MRI Studies in Parotid Tumors // Acad Radiol. Elsevier, 2007. Vol. 14, N 6. P. 701 - 710.
21. Zheng Y. et al. Differentiation between benign and malignant palatal tumors using conventional MRI: a retrospective analysis of 130 cases // Oral Surg Oral Med Oral Pathol Oral Radiol. Mosby Inc., 2018. Vol. 125, N 4. P. 343 - 350.
22. Geiger J.L. et al. Management of Salivary Gland Malignancy: ASCO Guideline // J Clin Oncol. 2021. Vol. 39. 1909 - 1941 p.
23. Roh J.-L. et al. Clinical Utility of 18 F-FDG PET for Patients with Salivary Gland Malignancies // J Nucl Med. 2007. Vol. 48. 240 - 246 p.
24. Cermik T.F. et al. FDG PET in detecting primary and recurrent malignant salivary gland tumors // Clin Nucl Med. 2007. Vol. 32, N 4. P. 286 - 291.
25. Kim M.J. et al. Utility of 18F-FDG PET/CT for detecting neck metastasis in patients with salivary gland carcinomas: Preoperative planning for necessity and extent of neck dissection // Ann Surg Oncol. Springer, 2013. Vol. 20, N 3. P. 899 - 905.
26. Schmidt R.L., Hall B.J., Layfield L.J. A systematic review and meta-analysis of the diagnostic accuracy of ultrasound-guided core needle biopsy for salivary gland lesions // American Journal of Clinical Pathology. 2011. Vol. 136, N 4. P. 516 - 526.
27. Kim H.J., Kim J.S. Ultrasound-guided core needle biopsy in salivary glands: A meta-analysis // Laryngoscope. John Wiley & Sons, Ltd, 2018. Vol. 128, N 1. P. 118 - 125.
28. Romano E.B. et al. Fine-needle aspiration with selective use of core needle biopsy of major salivary gland tumors // Laryngoscope. John Wiley & Sons, Ltd, 2017. Vol. 127, N 11. P. 2522 - 2527.
29. Rossi E.D. et al. The Milan System for Reporting Salivary Gland Cytopathology: Analysis and suggestions of initial survey // Cancer Cytopathol. John Wiley & Sons, Ltd, 2017. Vol. 125, N 10. P. 757 - 766.
30. Farahani S.J., Baloch Z. Retrospective assessment of the effectiveness of the Milan system for reporting salivary gland cytology: A systematic review and meta-analysis of published literature // Diagn Cytopathol. John Wiley & Sons, Ltd, 2019. Vol. 47, N 2. P. 67 - 87.
31. Park W. et al. Risk of high-grade malignancy in parotid gland tumors as classified by the Milan System for Reporting Salivary Gland Cytopathology // J Oral Pathol Med. J Oral Pathol Med, 2019. Vol. 48, N 3. P. 222 - 231.
32. Johnson D.N. et al. Cytologic grading of primary malignant salivary gland tumors: A blinded review by an international panel // Cancer Cytopathol. John Wiley and Sons Inc., 2020. Vol. 128, N 6. P. 392 - 402.
33. Qureshi S.S. et al. Clinical characteristics and treatment outcomes of primary and recurrent malignancy involving the salivary glands in children // Head Neck. John Wiley & Sons, Ltd, 2016. Vol. 38, N 6. P. 852 - 856.
34. Zenga J. et al. Close Margins and Adjuvant Radiotherapy in Acinic Cell Carcinoma of the Parotid Gland // JAMA Otolaryngol Head Neck Surg. American Medical Association, 2018. Vol. 144, N 11. P. 1011.
35. Zenga J. et al. Mucoepidermoid Carcinoma of the Parotid: Very Close Margins and Adjuvant Radiotherapy // ORL. S. Karger AG, 2019. Vol. 81, N 1. P. 55 - 62.
36. Stodulski D. et al. Close surgical margin after conservative parotidectomy in early stage low-/intermediate-grade parotid carcinoma: Outcome of watch and wait policy // Oral Oncol. Pergamon, 2017. Vol. 68. P. 1 - 4.
37. Ullah A. et al. Mucoepidermoid Carcinoma of the Salivary Gland: Demographics and Comparative Analysis in U.S. Children and Adults with Future Perspective of Management // Cancers (Basel). MDPI, 2023. Vol. 15, N 1.
38. Grant S.R. et al. Proton versus conventional radiotherapy for pediatric salivary gland tumors: Acute toxicity and dosimetric characteristics // Radiotherapy and Oncology. Elsevier Ireland Ltd, 2015. Vol. 116, N 2. P. 309 - 315.
39. Surun A. et al. Salivary gland carcinoma in children and adolescents: The EXPeRT/PARTNER diagnosis and treatment recommendations // Pediatr Blood Cancer. John Wiley and Sons Inc, 2021. Vol. 68, N S4.
40. Wang X. et al. Management of salivary gland carcinomas-a review. 2017. Vol. 8, N 3. 3946 - 3956 p.
41. Ryan J.T. et al. Primacy of surgery in the management of mucoepidermoid carcinoma in children // Head Neck. John Wiley & Sons, Ltd, 2011. Vol. 33, N 12. P. 1769 - 1773.
42. Spiro R.H. Salivary neoplasms: Overview of a 35-year experience with 2,807 patients // Head Neck Surg. John Wiley & Sons, Ltd, 1986. Vol. 8, N 3. P. 177 - 184.
43. Fushimi C. et al. A prospective phase II study of combined androgen blockade in patients with androgen receptor-positive metastatic or locally advanced unresectable salivary gland carcinoma // Annals of Oncology. Oxford University Press, 2018. Vol. 29, N 4. P. 979 - 984.
44. Morse E. et al. Positive surgical margins in parotid malignancies: Institutional variation and survival association // Laryngoscope. John Wiley & Sons, Ltd, 2019. Vol. 129, N 1. P. 129 - 137.
45. North L. et al. Intermediate-grade carcinoma of the parotid and the impact of adjuvant radiation // Am J Otolaryngol. W.B. Saunders, 2019. Vol. 40, N 6. P. 102282.
46. Glas A.S. et al. Surgical treatment of recurrent pleomorphic adenoma of the parotid gland: A clinical analysis of 52 patients // Head Neck. John Wiley & Sons, Ltd, 2001. Vol. 23, N 4. P. 311 - 316.
47. Aro K., Leivo I., M kitie A. Management of salivary gland malignancies in the pediatric population // Current Opinion in Otolaryngology and Head and Neck Surgery. Lippincott Williams and Wilkins, 2014. Vol. 22, N 2. P. 116 - 120.
48. Xiao C.C. et al. Predictors of Nodal Metastasis in Parotid Malignancies // Otolaryngology-Head and Neck Surgery. John Wiley & Sons, Ltd, 2016. Vol. 154, N 1. P. 121 - 130.
49. Wang Y.L. et al. Predictive index for lymph node management of major salivary gland cancer // Laryngoscope. John Wiley & Sons, Ltd, 2012. Vol. 122, N 7. P. 1497 - 1506.
50. Ali S. et al. Treatment of the neck in carcinoma of the parotid gland // Ann Surg Oncol. Springer New York LLC, 2014. Vol. 21, N 9. P. 3042 - 3048.
51. Lim C.M. et al. Is level V neck dissection necessary in primary parotid cancer? // Laryngoscope. John Wiley & Sons, Ltd, 2015. Vol. 125, N 1. P. 118 - 121.
52. Dominik T. Schneider et al. Salivary gland carcinomas in children and adolescents: A retrospective analysis of the European Cooperative Study Group for Pediatric Rare Tumours (EXPeRT) // EJC Paediatric Oncology Volume 2, December 2023, 100129.
53. Злокачественные опухоли слюнных желез // Клинические рекомендации Минздрава РФ // Год утверждения (частота пересмотра): 2024.
54. E.C. Fortune IV 1, D.J. Indelicato 1, R.Mailhot Vega 1, S. Bradfield 2, J.A. Bradley 1 Outcomes Following Proton Radiotherapy for Pediatric Salivary Gland Tumors.
Приложение А1
СОСТАВ
РАБОЧЕЙ ГРУППЫ ПО РАЗРАБОТКЕ И ПЕРЕСМОТРУ
КЛИНИЧЕСКИХ РЕКОМЕНДАЦИЙ
Грачев Николаи Сергеевич, профессор, доктор медицинских наук, генеральный директор НМИЦ ДГОИ им. Дмитрия Рогачева Минздрава России, заведующий кафедрой детскои хирургии с курсом онкологии и реконструктивно-пластическои хирургии "НМИЦ ДГОИ им. Дмитрия Рогачева" Минздрава России, член федерации специалистов по заболеваниям органов головы и шеи, член Российского общества детских онкологов (РОДО).
Ворожцов Игорь Николаевич, к.м.н., заведующий отделением детской онкологии, хирургии головы и шеи и нейрохирургии ФГБУ "НМИЦ ДГОИ им. Дмитрия Рогачева" Минздрава России, член федерации специалистов по заболеваниям органов головы и шеи.
Калинина Маргарита Павловна, врач-челюстно-лицевои хирург отделения детской онкологии, хирургии головы и шеи и нейрохирургии ФГБУ "НМИЦ ДГОИ им. Дмитрия Рогачева" Минздрава России, заведующая отделением дневного стационара Федерального научно-клинического центра детей и подростков ФМБА России.
Оганесян Раиса Суреновна, врач-детский хирург отделения детской онкологии, хирургии головы и шеи и нейрохирургии ФГБУ "НМИЦ ДГОИ им. Дмитрия Рогачева" Минздрава России.
Жуков Николай Владимирович, доктор медицинских наук, руководитель отдела междисциплинарной онкологии ФГБУ "НМИЦ ДГОИ им. Дмитрия Рогачева" Минздрава России.
Нечеснюк Алексей Владимирович, к.м.н., заведующий отделением лучевой терапии ФГБУ "НМИЦ ДГОИ им. Дмитрия Рогачева" Минздрава России.
Рабаева Лилия Леонидовна, кандидат медицинских наук, врач-детский онколог отделения гематологии/онкологии старшего возраста и нейронкологии ФГБУ "НМИЦ ДГОИ им. Дмитрия Рогачева" Минздрава России.
Горностаев Владимир Васильевич, врач-радиотерапевт отделения лучевой терапии ФГБУ "НМИЦ ДГОИ им. Дмитрия Рогачева" Минздрава России.
Поляков Владимир Георгиевич, академик РАН, д.м.н., профессор, заведующий отделением опухолей головы и шеи НИИ ДОиГ ФГБУ "РОНЦ им. Н.Н. Блохина" Минздрава России, заведующий кафедрои детскои онкологии ФГБОУ ДПО РМАПО Минздрава России, член общества специалистов по опухолям головы и шеи, член федерации специалистов по заболеваниям органов головы и шеи, член России ского общества детских онкологов (РОДО), главный внештатный детский специалист онколог Минздрава России.
Иванова Наталья Владимировна, к.м.н., врач хирургического отделения N 1 НИИ ДОГ ФГБУ "РОНЦ им. Н.Н. Блохина" Минздрава России, член общества специалистов по опухолям головы и шеи, член федерации специалистов по заболеваниям органов головы и шеи, член Российского общества детских онкологов (РОДО).
Приложение А2
МЕТОДОЛОГИЯ РАЗРАБОТКИ КЛИНИЧЕСКИХ РЕКОМЕНДАЦИЙ
Целевая аудитория данных клинических рекомендаций:
1. Врачи-детские онкологи/гематологи
2. Врач-гематологи
3. Врачи-детские онкологи
4. Врачи-онкологи
5. Врачи-педиатры
6. Врачи-радиологи
7. Врачи клинико-лабораторной диагностики
Таблица 7. Шкала оценки уровней достоверности доказательств (УДД) для методов диагностики (диагностических вмешательств)
УДД
Расшифровка
1
Систематические обзоры исследований с контролем референсным методом или систематический обзор рандомизированных клинических исследований с применением мета-анализа
2
Отдельные исследования с контролем референсным методом или отдельные рандомизированные клинические исследования и систематические обзоры исследований любого дизайна, за исключением рандомизированных клинических исследований, с применением мета-анализа
3
Исследования без последовательного контроля референсным методом или исследования с референсным методом, не являющимся независимым от исследуемого метода или нерандомизированные сравнительные исследования, в том числе когортные исследования
4
Несравнительные исследования, описание клинического случая
5
Имеется лишь обоснование механизма действия или мнение экспертов
Таблица 8. Шкала оценки уровней достоверности доказательств (УДД) для методов профилактики, медицинской реабилитации, в том числе основанных на использовании природных лечебных факторов (профилактических, лечебных, реабилитационных вмешательств)
УДД
Расшифровка
1
Систематический обзор РКИ с применением мета-анализа
2
Отдельные РКИ и систематические обзоры исследований любого дизайна, за исключением РКИ, с применением мета-анализа
3
Нерандомизированные сравнительные исследования, в т.ч. когортные исследования
4
Несравнительные исследования, описание клинического случая или серии случаев, исследования "случай-контроль"
5
Имеется лишь обоснование механизма действия вмешательства (доклинические исследования) или мнение экспертов
Таблица 9. Шкала оценки уровней убедительности рекомендаций (УУР) для методов профилактики, диагностики, лечения медицинской реабилитации, в том числе основанных на использовании природных лечебных факторов (профилактических, лечебных, реабилитационных вмешательств)
УУР
Расшифровка
A
Сильная рекомендация (все рассматриваемые критерии эффективности (исходы) являются важными, все исследования имеют высокое или удовлетворительное методологическое качество, их выводы по интересующим исходам являются согласованными)
B
Условная рекомендация (не все рассматриваемые критерии эффективности (исходы) являются важными, не все исследования имеют высокое или удовлетворительное методологическое качество и/или их выводы по интересующим исходам не являются согласованными)
C
Слабая рекомендация (отсутствие доказательств надлежащего качества (все рассматриваемые критерии эффективности (исходы) являются неважными, все исследования имеют низкое методологическое качество и их выводы по интересующим исходам не являются согласованными)
Порядок обновления клинических рекомендаций.
Механизм обновления клинических рекомендаций предусматривает их систематическую актуализацию - не реже чем один раз в три года, а также при появлении новых данных с позиции доказательной медицины по вопросам диагностики, лечения, профилактики и реабилитации конкретных заболеваний, наличии обоснованных дополнений/замечаний к ранее утвержденным КР, но не чаще 1 раза в 6 месяцев.
Приложение А3
СПРАВОЧНЫЕ МАТЕРИАЛЫ,
ВКЛЮЧАЯ СООТВЕТСТВИЕ ПОКАЗАНИЙ К ПРИМЕНЕНИЮ
И ПРОТИВОПОКАЗАНИЙ, СПОСОБОВ ПРИМЕНЕНИЯ И ДОЗ ЛЕКАРСТВЕННЫХ
ПРЕПАРАТОВ, ИНСТРУКЦИИ ПО ПРИМЕНЕНИЮ
ЛЕКАРСТВЕННОГО ПРЕПАРАТА
1. Основные принципы хирургического лечения
Основным методом лечения злокачественных эпителиальных опухолей СЖ как у детей, так и у взрослых является хирургический [31]. Еще в 1986 году Spiro RH сформулирован основные тезисы успешного лечения: радикальное удаление образований с отсутствием опухоли в краях резекции и отдаленных метастазов [32]. По данным M. Zamani и соавторов 95% пациентам проводится хирургическое лечение, послеоперационная лучевая терапия требуется в 24% случаев [7]. По данным Ullah A.2023 года в группе более двух тысяч больных с МЭК, изолированное оперативное лечение педиатрических пациентов имело место в 63,6%, а среди взрослых у 53,3%. Комбинированное лечение проведено 26,1% и 29,6% соответственно [37]. Несмотря на простоту и логичность утверждения Spiro R.H., актуального более 35 лет, в настоящее время остается множество вопросов: резектабельность, радикальность и достаточность краев резекции, сохранение лицевого нерва.
Уровень развития микрохирургии головы и шеи относит опухоли T4b или наличие отдаленных метастазов к нерезектабельным [33]. Энуклеация опухоли приводит к продолженному росту или рецидиву и не может рассматриваться как метод лечения [34]. ASCO опубликовала рекомендации, где проведение поверхностной частичной резекции образований ОСЖ до 4 см (T1/T2 по ВОЗ) возможно, если опухоль низкой степени злокачественности, но с низкой степенью достоверности [22]. Рандомизированных исследований, которые бы учитывали объем резекции при эпителиальных опухолях низкой степени злокачественности нет, но имеется ряд ретроспективных. Клинически течение этих образований сходно с плеоморфными аденомами. Авторы считают, что необходимо обеспечить полное иссечение образования, при этом иссекать дополнительную ткань ОСЖ не требуется ввиду низкой скорости метастазирования.
Выбор оптимального объема резекции основывается не только на размерах первичной опухоли, но и на гистологическом типе и стратификации риска.
Morse E в своей работе показал, как меняется риск развития рецидива/продолженного ростка в зависимости от края резекции для плоскоклеточного рака головы и шеи. При расстоянии более 1 мм нет статистически значимого различия между краем резекции и развитием рецидива [50] (Табл. 2)
Табл. 10. Риск развития рецидива в зависимости от края резекции по Morse E. [50]
Край резекции
Вероятность рецидива/продолженного роста, %
Опухоль в крае
44
Край менее 1 мм
28
1 мм
17
2 мм
13
3 мм
13
4 мм
14,4
5 мм
11
Минимальный, но при этом достаточный край резекции не определен. Сложности, в этом вопросе связаны с отсутствием рандомизированных исследований, особенностями анатомии околоушно-жевательной области, основания черепа, а также различными гистологическими вариантами опухолей.
На ранних стадиях заболевания контроль над заболеванием может обеспечить и узкий край резекции (менее 5 мм) при отсутствии периневральной или лимфоваскулярной инвазии [43,45]. Зависимость краев резекции от гистологического типа опухоли рассматривается в работах Zenga et al. Край резекции в 2 мм в 90% показал отсутствие локорегионарных рецидивов в течение 6 лет у пациентов с МЭК низкой или средней степенью злокачественности при опухолях T1 и T2. В группе ацинарно-клеточных карцином лишь у 1 из 18 пациентов развился рецидив при подобном методе удаления в сроки 64 месяцев [44]. Похожие результаты среди опухолей с низким и промежуточным потенциалом злокачественности показывает Stodulski и соавторы. Безрецидивная выживаемость 32 пациентов составила 90,6% при крае более 1 но менее 5 мм [45]. При любых видах рака с высоким потенциалом злокачественности или поздних стадиях T3 - T4 рекомендованный объем вмешательства поверхностная, с возможным увеличением до субтотальной или тотальной, паротидэктомии. При распространенных формах T3 - T4 оценивается не только размер первичного очага, но и поражение лимфатических узлов [40]. При выборе объема резекции у пациентов с распространенными опухолями (T4) имеются данные среди группы с поражением кожи.
Проведение шейной лимфодиссекции до сих пор вызывает споры, по данным Aro K. и соавторов лишь 17% пациентов имеют регионарные метастазы [47]. Ее выполнение рекомендовано при опухолях T3 и T4 среди образований с высокой степенью злокачественности. В национальной базе National Cancer Database 26% пациентов имели поражение лимфатических узлов [50]. Методом многофакторного анализа Wang Y.L. с коллегами установили, что поражением лимфатических узлов было предиктором вовлечения крупных нервов, высокой степени злокачественности, лимфоваскулярной и экстракапсулярной инвазии [39].
До настоящего времени нет данных о влиянии профилактической лимфодиссекции шеи для контроля над заболеванием в случае проведения послеоперационной лучевой терапии.
Необходимость и уровень лимфодиссекции шеи для лечения различных видов рака ОСЖ в большей степени зависит от гистологического типа и стратификации риска. По данным ASCO с низкой степенью доказательности хирурги должны включать уровни диссекции 2 - 4 в зависимости от локализации первичного очага. Возможно выполнение диссекции до уровней 1 - 5 для опухолей с высоким потенциалом злокачественности [22].
Ali S. и соавторы обнаружили, что коллекторы 2 - 3 (верхние и средние яремные л/у) наиболее часто подвергаются поражением при цитологически N0, уровень 4 (нижне-яремные л/у) - 11%, уровень 1 (подбородочные л/у) - 5%, уровень 5 (заднего треугольника шеи) - 7%. В случае инициального поражения лимфатических узлов (N+) их распространение по группам представляется следующим: 1 уровень - 52%, 2 уровень - 77%, 3 уровень - 73%, 4 уровень - 53% и 5 уровень - 40% соответственно [51]. Lim с соавторами опубликовали данные о высокой частоте поражений лимфоузлов 5 группы у больных с инициальными поражением лимфоузлов до 82% [52].
Объем шейной лимфодиссекции для опухолей T3 и T4 высокой степени злокачественности при отсутствии инициального поражения лимфоузлов - уровни II - V. При проведении терапевтической лимфодиссекции T3 - T4 N+ будут представлены уровнями 1 - 5 для опухолей с высоким потенциалом злокачественности.
2. Особенности организации специализированной медицинской помощи
Медицинская помощь, за исключением медицинской помощи в рамках клинической апробации, в соответствии с федеральным законом от 21.11.2011 N 323-ФЗ (ред. от 25.05.2019) "Об основах охраны здоровья граждан в Российской Федерации" организуется и оказывается:
1) в соответствии с положением об организации оказания медицинской помощи по видам медицинской помощи, которое утверждается уполномоченным федеральным органом исполнительной власти;
2) в соответствии с порядком оказания помощи по профилю "онкология", обязательным для исполнения на территории Российской Федерации всеми медицинскими организациями;
3) на основе настоящих клинических рекомендаций;
4) с учетом стандартов медицинской помощи, утвержденных уполномоченным федеральным органом исполнительной власти.
Первичная специализированная медико-санитарная помощь оказывается врачом-онкологом и иными врачами-специалистами в центре амбулаторной онкологической помощи либо в первичном онкологическом кабинете, первичном онкологическом отделении, поликлиническом отделении онкологического диспансера. При подозрении или выявлении у пациента онкологического заболевания врачи-терапевты, врачи-терапевты участковые, врачи общей практики (семейные врачи), врачи-специалисты, средние медицинские работники в установленном порядке направляют пациента на консультацию в центр амбулаторной онкологической помощи либо в первичный онкологический кабинет, первичное онкологическое отделение медицинской организации для оказания ему первичной специализированной медико-санитарной помощи. Консультация в центре амбулаторной онкологической помощи либо в первичном онкологическом кабинете, первичном онкологическом отделении медицинской организации должна быть проведена не позднее 5 рабочих дней с даты выдачи направления на консультацию. Врач-онколог центра амбулаторной онкологической помощи (в случае отсутствия центра амбулаторной онкологической помощи врач-онколог первичного онкологического кабинета или первичного онкологического отделения) организует взятие биопсийного (операционного) материала, а также организует выполнение иных диагностических исследований, необходимых для установления диагноза, включая распространенность онкологического процесса и стадию заболевания. В случае невозможности взятия в медицинской организации, в составе которой организован центр амбулаторной онкологической помощи (первичный онкологический кабинет, первичное онкологическое отделение), биопсийного (операционного) материала, проведения иных диагностических исследований пациент направляется лечащим врачом в онкологический диспансер или в медицинскую организацию, оказывающую медицинскую помощь пациентам с онкологическими заболеваниями. Срок выполнения патологоанатомических исследований, необходимых для гистологической верификации злокачественного новообразования (ЗНО) слюнных желез, не должен превышать 15 рабочих дней с даты поступления биопсийного (операционного) материала в патологоанатомическое бюро (отделение). При подозрении и (или) выявлении у пациента онкологического заболевания в ходе оказания ему скорой медицинской помощи таких пациентов переводят или направляют в медицинские организации, оказывающие медицинскую помощь больным с онкологическими заболеваниями, для определения тактики ведения и необходимости применения дополнительно других методов специализированного противоопухолевого лечения. Врач-онколог центра амбулаторной онкологической помощи (первичного онкологического кабинета, первичного онкологического отделения) направляет пациента в онкологический диспансер или в медицинские организации, оказывающие медицинскую помощь пациентам с онкологическими заболеваниями, для уточнения диагноза (в случае невозможности установления диагноза, включая распространенность онкологического процесса и стадию заболевания, врачом-онкологом центра амбулаторной онкологической помощи, первичного онкологического кабинета или первичного онкологического отделения) и оказания специализированной, в том числе высокотехнологичной, медицинской помощи.
Срок начала оказания специализированной, за исключением высокотехнологичной, медицинской помощи пациентам с онкологическими заболеваниями в медицинской организации, оказывающей медицинскую помощь пациентам с онкологическими заболеваниями, не должен превышать 14 календарных дней с даты патологоанатомической верификации ЗНО слюнных желез или 14 календарных дней с даты установления предварительного диагноза ЗНО слюнных желез (в случае отсутствия медицинских показаний для проведения патологоанатомических исследований в амбулаторных условиях). Специализированная, в том числе высокотехнологичная, медицинская помощь оказывается врачами-онкологами, врачами-радиотерапевтами в онкологическом диспансере или в медицинских организациях, оказывающих медицинскую помощь пациентам с онкологическими заболеваниями, имеющих лицензию, необходимую материально-техническую базу, сертифицированных специалистов, в стационарных условиях и условиях дневного стационара и включает в себя профилактику, диагностику, лечение онкологических заболеваний, требующих использования специальных методов и сложных уникальных медицинских технологий, а также медицинскую реабилитацию. В медицинской организации, оказывающей медицинскую помощь пациентам с онкологическими заболеваниями, тактика медицинского обследования и лечения устанавливается консилиумом врачей-онкологов и врачей-радиотерапевтов, с привлечением при необходимости других врачей-специалистов. Решение консилиума врачей оформляется протоколом, подписывается участниками консилиума врачей и вносится в медицинскую документацию пациента. Показания для госпитализации в круглосуточный или дневной стационар медицинской организации, оказывающей специализированную, в том числе высокотехнологичную медицинскую помощь по профилю "онкология" определяются консилиумом врачей-онкологов и врачей-радиотерапевтов, с привлечением при необходимости других врачей-специалистов.
Заключение о целесообразности перевода пациента в профильную медицинскую организацию осуществляется после предварительной консультации по предоставленным медицинским документам и/или предварительного осмотра больного врачами специалистами медицинской организации, в которую планируется перевод.
Приложение Б
АЛГОРИТМЫ ДЕЙСТВИЙ ВРАЧА
Приложение В
ИНФОРМАЦИЯ ДЛЯ ПАЦИЕНТА
Частота посещения врача-онколога после завершения специального лечения: каждые 3 месяца - в 1 год после лечения, каждые 6 месяцев в течение 5 лет, 1 раз в год - пожизненно.
Необходимо полностью отказаться от посещения соляриев, не загорать на пляже во время отдыха, физиопроцедуры и прививки должны быть одобрены врачом-онкологом.
После достижения возраста 18 лет пациенты переводятся на диспансерное наблюдение во взрослое отделение.
Приложение Г1 - ГN
ШКАЛЫ ОЦЕНКИ, ВОПРОСНИКИ И ДРУГИЕ ОЦЕНОЧНЫЕ ИНСТРУМЕНТЫ
СОСТОЯНИЯ ПАЦИЕНТА, ПРИВЕДЕННЫЕ В КЛИНИЧЕСКИХ РЕКОМЕНДАЦИЯХ
Не применимо.
