"Клинические рекомендации "Рак желчевыводящей системы"
МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ
КЛИНИЧЕСКИЕ РЕКОМЕНДАЦИИ
РАК ЖЕЛЧЕВЫВОДЯЩЕЙ СИСТЕМЫ
Год утверждения (частота пересмотра): 2024
Пересмотр не позднее: 2026
ID: 495_2
Возрастная категория: Взрослые, Дети
Специальность: Онкология
Разработчик клинической рекомендации
Ассоциация онкологов России, Общероссийская общественная организация "Российское общество клинической онкологии"
Одобрено Научно-практическим Советом Минздрава России
Список сокращений
AJCC - Американский объединенный комитет по раку (American Joint Committee on Cancer)
DCR - Контроль опухолевого процесса (disease control rate)
ECOG - Восточная Кооперативная Онкологическая Группа (The Eastern Cooperative Oncology Group)
EGFR - Рецептор эпидермального фактора роста (epidermal growth factor receptor)
HR - Отношение рисков (hazard ratio)
MSI-H - Высокая микросателлитная нестабильность (microsatellitein stable - high)
OR - Отношение шансов (odds ratio)
PD-L1 - Лиганд программируемой клеточной гибели 1 (programmed cell death 1-ligand 1)
RR - Относительный риск (risk ratio)
АФП - Альфа-фетопротеин
ВБП - Выживаемость без прогрессирования
ГЦР - Гепатоцеллюлярный рак
ДИ - Доверительный интервал
КТ - Компьютерная томография
ЛТ - Лучевая терапия
МРТ - Магнитно-резонансная томография
МРХПГ - Магнитно-резонансная холангиопанкреатография
ОВ - Общая выживаемость
ПЭТ-КТ - Позитронно-эмиссионная компьютерная томография
РЖП - Рак желчного пузыря
РЧА - Радиочастотная абляция
РЭА - Раковый эмбриональный антиген
ТАХЭ - Трансартериальная химиоэмболизация
УЗИ - Ультразвуковое исследование
УЗКТ - Ультразвуковая компьютерная томография
РКТ - Рентгеновская компьютерная томография
ФДТ - Фотодинамическая терапия
ХЛТ - Химиолучевая терапия
Термины и определения
Рак желчевыводящей системы (опухоли билиарного тракта) - опухолевое поражение желчного пузыря и желчных протоков.
Холангиокарцинома - злокачественная опухоль, происходящая из эпителия желчных протоков. Холангиокарциномы делятся по анатомическому расположению на внутри- и внепеченочные.
В зависимости от уровня поражения в клинической практике выделяют внепеченочные холангиокарциномы проксимального и дистального отдела желчных протоков.
Холангиокарцинома проксимального отдела внепеченочных желчных протоков (опухоль Клатскина, перихилярная холангиокарцинома) - опухолевое поражение долевых и общего печеночного протоков, локализующееся проксимальнее места слияния общего печеночного и пузырного протоков до начала сегментарных печеночных протоков второго порядка.
Холангиокарцинома дистального отдела внепеченочных желчных протоков - опухолевое поражение общего желчного протока, локализующееся проксимальнее ампулы большого дуоденального сосочка до места слияния общего печеночного и пузырного протоков.
Рак желчного пузыря (РЖП) - злокачественная опухоль, исходящая из эпителия желчного пузыря; является наиболее распространенным из всех видов рака желчных путей.
1. Краткая информация по заболеванию или состоянию (группы заболеваний или состояний)
1.1 Определение заболевания или состояния (группы заболеваний или состояний)
Рак билиарного тракта - группа опухолей, развивающихся из эпителия желчного пузыря и желчных протоков. Среди пациентов с билиарным раком треть случаев составляют опухоли желчных протоков (холангиокарциномы), две трети - опухоли желчного пузыря.
Рак желчного пузыря (РЖП) - злокачественная опухоль, исходящая из эпителия желчного пузыря; является наиболее распространенным из всех видов рака желчных путей. РЖП характеризуется местной и сосудистой инвазией, обширным регионарным лимфогенным и гематогенным метастазированием.
Рак желчных протоков (холангиокарцинома) - злокачественная опухоль, происходящая из эпителия желчных протоков.
1.2 Этиология и патогенез заболевания или состояния (группы заболеваний или состояний)
Факторами риска развития РЖП являются заболевания, связанные с наличием хронического воспаления, в том числе желчекаменная болезнь. К другим факторам риска относятся: полипы желчного пузыря более 1 см в диаметре, хронические инфекции, склерозирующий холангит, аденоматоз желчного пузыря. Воспалительные заболевания кишечника (неспецифический язвенный колит) также ассоциируются с повышенным риском рака билиарного тракта [1 - 3].
Заболевания, предшествующие развитию ХЦР: склерозирующий аутоиммунный холангит, хронический холангит инфекционной природы, болезнь Caroli, хроническая гельминтная инвазия (Opisthorchisviverrini, Clonorchissinensisи Opisthorchisfelineus). Желчнокаменная болезнь не связана с этиологией холангиокарциномы. Потенциальными факторами риска для развития холангиокарциномявляются воспалительные заболевания кишечника, а также инфицированность гепатитами B или C, цирроз печени, сахарный диабет, ожирение, алкоголь, неалкогольная жировая болезнь печени и курение [4 - 6].
1.3 Эпидемиология заболевания или состояния (группы заболеваний или состояний)
Рак билиарного тракта - холангиоцеллюлярный, рак желчного пузыря и желчных протоков - редкая злокачественная опухоль. В структуре заболеваемости и смертности эти опухоли оцениваются совместно. В Российской Федерации в 2018 году раком печени заболело 8810 пациентов. По грубым подсчетам рак внутрипеченочных желчных протоков составляет около 10% от этого числа, т.е. в 2018 году в России было зарегистрировано около 880 пациентов, заболевших раком внутрипеченочных желчных протоков. Внепеченочные холангиокарциномы и рак желчного пузыря зафиксированы у 3713 первичных пациентов (1424 - мужчины и 2289 - женщины). Точная статистика смертности от билиарного рака в России отсутствует. Тем не менее от рака печени (гепато- и холангиоцеллюлярный раки) умерло 10018 пациентов, а от рака желчного пузыря, внепеченочных желчных протоков и других неуточненных органов пищеварения погибло 3819 пациентов. Заболеваемость увеличивается с возрастом, женщины заболевают ХЦР чаще мужчин [7, 8].
1.4 Особенности кодирования заболевания или состояния (группы заболеваний или состояний) по Международной статистической классификации болезней и проблем, связанных со здоровьем
C22.1 Рак внутрипеченочных желчных протоков
C23 Рак желчного пузыря
C24.0 Рак внепеченочных желчных протоков
Эпителиальные опухоли (билиарные)
а) Доброкачественные
8202/0 Аденома желчных протоков (перибилиарная гамартома и другие)
8202/0 Микрокистозная аденома
9013/0 Билиарнаяаденофиброма
б) Предраковые новообразования
8148/2 Билиарная интраэпителиальная неоплазия, III степень (BiIN-3)
8503/0 Внутрипротоковая папиллярная опухоль с признаками низкой-умеренной интраэпителиальной неоплазии
8503/2 Внутрипротоковая папиллярная опухоль с признаками тяжелой интраэпителиальной неоплазии
8470/0 Муцинозная кистозная опухоль с признаками низкой-умеренной интраэпителиальной неоплазии
8470/2 Муцинозная кистозная опухоль с признаками тяжелой интраэпителиальной неоплазии
Злокачественные новообразования
8160/3 Внутрипеченоная холангиокарцинома
8503/3 Внутрипротоковая папиллярная опухоль в сочетании с инвазивным раком (карциномой)
8470/3 Муцинозная кистозная опухоль в сочетании с инвазивным раком (карциномой)
Внепеченочные желчные протоки и желчный пузырь
Эпителиальные опухоли
Предраковые новообразования
8140/0 Аденома
8211/0 Тубулярная
8260/0 Папиллярная
8263/0 Тубулопапиллярная
8148/2 Билиарная интраэпителиальная неоплазия, III степень (BiIN-3)
8503/0 Внутрипузырная (желчный пузырь) или внутрипротоковая (желчные протоки) папиллярная опухоль с признаками низкой-умеренной интраэпителиальной неоплазии
8503/2 Внутрипузырная (желчный пузырь) или внутрипротоковая (желчные протоки) папиллярная опухоль с признаками тяжелой интраэпителиальной неоплазии
8470/0 Муцинозная кистозная опухоль с признаками низкой-умеренной интраэпителиальной неоплазии
8470/2 Муцинозная кистозная опухоль с признаками тяжелой интраэпителиальной неоплазии
Злокачественные новообразования (рак)
8140/3 Аденокарцинома
8140/3 Аденокарцинома, билиарный тип
8140/3 Аденокарцинома, желудочный фовеолярный тип
8144/3 Аденокарцинома, кишечный (интестинальный) тип
8310/3 Светлоклеточная аденокарцинома
8480/3 Муцинозная аденокарцинома
8490/3 Перстневидно-клеточный рак
8560/3 Железисто-плоскоклеточный рак
8503/3 Внутрипузырная (желчный пузырь) или внутрипротоковая (желчные пути) папиллярная опухоль в сочетании с инвазивным раком (карциномой)
8470/3 Муцинозная кистозная опухоль в сочетании с инвазивным раком (карциномой)
8070/3 Плоскоклеточный рак
8020/3 Недифференцированный рак
1.5 Классификация заболевания или состояния (группы заболеваний или состояний)
Рак билиарного тракта - группа опухолей, развивающихся из эпителия желчного пузыря и желчных протоков. Среди пациентов с билиарным раком треть случаев составляют опухоли желчных протоков (холангиокарциномы), две трети - опухоли желчного пузыря.
Холангиокарциномы разделяют на внутри- и внепеченочные. К последним относят рак общего желчного протока и опухоли желчных протоков ворот печени (опухоль Клацкина). Рак внепеченочных желчных протоков встречается значительно чаще: на опухоль Клацкина приходится 50% от числа холангиокарцином, на опухоли дистальной локализации - 42%, внутрипеченочное поражение встречается в 8% случаев [10]. Среди опухолей желчного пузыря чаще всего (80%) встречаются аденокарциномы, возможны и другие варианты: плоскоклеточныи, анапластическии, мелкоклеточныи рак, лимфомы, саркомы [1]. Более 90% случаев холангиокарцином составляют аденокарциномы, часто (>80%) муцинозные. По характеру роста аденокарциномы желчных путей разделены на три типа:
- склерозирующий (скиррозный) - чаще развивается во внепеченочных желчных протоках, характеризуется сложностью верификации и низкой резектабельностью,
- нодулярный - чаще развивается при внутрипеченочной локализации, характеризуется высокими инвазирующими свойствами и низкой резектабельностью,
- папиллярный - характеризуется ранней манифестацией и высокой резектабельностью.
1.6 Клиническая картина заболевания или состояния (группы заболеваний или состояний)
Ранние симптомы рака внутрипеченочного желчного протока и рака желчного пузыря крайне неспецифичны: дискомфорт, тяжесть в правом подреберье или эпигастрии, снижение аппетита. Иногда проявления можно выявить при изменении биохимических анализов крови (повышение активности трансаминаз или показателей холестаза), а также увеличения уровня опухолевых маркеров в группе повышенного риска (желчекаменная болезнь, полипы желчного пузыря, первичный склерозирующий холангит, паразитарная инвазия), что, впрочем, также не является специфичным.
Более значимые симптомы (боли в верхнем отделе живота, тошнота, рвота, потеря аппетита или даже отвращение к пище, снижение веса, желтуха, зуд, лихорадка, увеличение размеров печени и желчного пузыря, появление асцита) являются признаками поздних стадий заболевания. Симптомы билиарного рака могут маскироваться симптомами фоновых заболеваний (желчекаменной болезни, первичного склерозирующего холангита, язвенного колита).
Рак внепеченочных желчных протоков, напротив, часто манифестирует механической желтухой при обструкции общего печеночного/общего желчного протоков или в связи с двухсторонним блоком правого и левого долевого протоков. До полной обструкции с развернутой картиной механической желтухи могут быть неспецифические жалобы на тяжесть в подреберье, лихорадка, озноб, в последующим - кожный зуд, посветление кала, потемнение мочи. На доклиническом или субклиническом уровне возможны отклонения в биохимическом анализе крови (маркеры цитолиза, холестаза).
Ультразвуковое исследование брюшной полости в качестве скрининга может выявить образование в печени при внутрипеченочной форме холангиокарциноме, наличие инфильтрата в области желчного пузыря или рост ранее выявлено полипа при раке желчного пузыря, а также признаки билиарной гипертензии при раке внепеченочных желчных протоков или осложненных формах рака желчного пузыря/рака внутрипеченочного желчного протока.
Стадирование TNM 8
Стадирование рака желчного пузыря (8-я редакция)
T - первичная опухоль:
Tx - недостаточно данных для оценки первичной опухоли;
T0 - первичная опухоль не определяется;
Tis - рак in situ;
T1 - опухоль прорастает в собственную пластинку или мышечный слой;
T1a - опухоль прорастает в собственную пластинчатую оболочку;
T1b - опухоль прорастает в мышечный слой;
T2 - опухоль проникает в перимускулярную соединительную ткань на брюшной стороне без вовлечения серозы (висцеральной брюшины) или опухоль проникает в перимышечную соединительную ткань на печеночной стороне без врастания в печень;
T2a - опухоль проникает в перимускулярную соединительную ткань на брюшной стороне без вовлечения серозы (висцеральной брюшины);
T2b - опухоль проникает в перимускулярную соединительную ткань на печеночной стороне без врастания в печень;
T3 - опухоль прорастает в серозу (висцеральную брюшину) и/или прямая инвазия в печень и/или другие соседние органы и структуры (желудок, ДПК, ободочная кишка, поджелудочная железа, сальник, внепеченочные желчные протоки);
T4 - инвазия опухоли в воротную вену или печеночную артерию, или инвазия двух и более органов и структур.
N - регионарные лимфатические узлы:
NX - недостаточно данных для оценки поражения лимфоузлов;
N0 - нет признаков метастатического поражения регионарных лимфатических узлов;
N1 - поражение от одного до трех регионарных лимфатических узлов;
N2 - поражение четырех и более лимфатических узлов.
M - отдаленные метастазы:
M0 - нет отдаленных метастазов;
M1 - есть отдаленные метастазы.
Таблица 1. Группировка рака желчного пузыря по стадиям.
Стадия
T
N
M
Стадия 0
Tis
N0
M0
Стадия I
T1
N0
M0
Стадия IIA
T2a
N0
M0
Стадия IIB
T2b
N0
M0
Стадия IIIA
T3
N0
M0
Стадия IIIB
T1-3
N1
M0
Стадия IVA
T4
N0-1
M0
Стадия IVB
Любая T
N2
M0
Любая T
Любая N
M1
Гистологическая градация:
Gx - недостаточно данных для оценки;
G1 - хорошо дифференцированная;
G2 - умеренно дифференцированная;
G3 - низкодифференцированная.
Стадирование рака внутрипеченочных желчных протоков
T - первичная опухоль:
Tx - недостаточно данных для оценки первичной опухоли;
T0 - первичная опухоль не определяется;
Tis - рак insitu (внутрипротоковая опухоль);
T1 - солитарная опухоль без инвазии сосудов <5 см или >5 см;
T1a - солитарная опухоль <5 см без инвазии сосудов;
T1b - солитарная опухоль >5 см без инвазии сосудов;
T2 - солитарная опухоль с внутрипеченочной инвазией сосудов или множественные опухолевые узлы с инвазией или без инвазии сосудов;
T3 - опухоль, прорастающая висцеральную брюшину;
T4 - опухоль, вовлекающая местные структуры путем прямой инвазии.
N - регионарные лимфатические узлы:
Nx - недостаточно данных для оценки состояния регионарных лимфатических узлов;
N0 - нет признаков метастатического поражения регионарных лимфатических узлов;
N1 - имеется поражение регионарных лимфатических узлов метастазами.
M - отдаленные метастазы:
M0 - нет признаков отдаленных метастазов;
M1 - имеются отдаленные метастазы.
Таблица 2. Группировка по стадиям рака внутрипеченочных желчных протоков.
Стадия
T
N
M
Стадия 0
Tis
N0
M0
Стадия IA
T1а
N0
M0
Стадия IB
T1b
N0
M0
Стадия II
T2
N0
M0
Стадия IIIA
T3
N0
M0
Стадия IIIB
T4
N0
M0
Стадия IV
Любая T
Любая N
M1
Гистологическая градация
Gx - недостаточно данных для оценки;
G1 - хорошо дифференцированная;
G2 - умеренно дифференцированная;
G3 - низкодифференцированная.
Стадирование рака внепеченочных желчных протоков (в области ворот печени)
T - первичная опухоль:
Tx - недостаточно данных для оценки первичной опухоли;
T0 - первичная опухоль не определяется;
Tis - рак insitu (высокая степень дисплазии);
T1 - опухоль, ограниченная желчным протоком с расширением до мышечного слоя или волокнистой (фиброзной) ткани;
T2-опухоль проникает за стенку желчного протока в окружающую жировую ткань, или опухоль проникает в соседнюю печеночную паренхиму;
T2a - опухоль прорастает за пределы стенки протока с инвазией в окружающую жировую ткань;
T2b - опухоль прорастает в прилежащую паренхиму печени;
T3 - опухоль прорастает в ветви воротной вены или печеночной артерии с одной стороны;
T4 - опухоль прорастает в главный ствол воротной вены или ее ветви с обеих сторон, или инвазия общей печеночной артерии, или распространение опухоли на протоки 2-го порядка с обеих сторон; поражение протоков 2-го порядка с одной стороны с инвазией контралатеральной ветви воротной вены и печеночной артерии. Печеночная артерия и портальные вены, лимфатические узлы N1, N2.
N - регионарные лимфатические узлы:
NX - недостаточно данных для оценки поражения лимфоузлов;
N0 - нет признаков метастатического поражения регионарных лимфатических узлов;
N1 - от одного до трех положительных лимфатических узлов, поражение лимфоузлов вдоль пузырного протока, общего желчного протока, печеночной артерии, задние панкреатодуоденальной и/или воротной вены;
N2 - четыре или более положительных лимфатических узлов из участков, описанных для N1.
M - отдаленные метастазы:
M0 - нет отдаленных метастазов;
M1 - есть отдаленные метастазы.
Таблица 3. Группировка по стадиям рака внепеченочных желчных протоков (в области ворот печени).
Стадия
T
N
M
Стадия 0
Tis
N0
M0
Стадия I
T1
N0
M0
Стадия II
T2a-b
N0
M0
Стадия IIIA
T3
N0
M0
Стадия IIIB
T4
N0
M0
Стадия IIIС
Любая T
N1
M0
Стадия IVA
Любая T
N2
M0
Стадия IVB
Любая T
Любая N
M1
Гистологическая градация:
Gx - недостаточно данных для оценки;
G1 - хорошо дифференцированная;
G2 - умеренно дифференцированная;
G3 - низкодифференцированная.
Модифицированная система стадирования Вismuth-Corlette классифицирует опухоли проксимальных желчных протоков на 4 типа, основанные на степени участия желчных протоков (таб. 4).
Таблица 4. Классификация Bismuth-Corlette (для рака проксимальных желчных протоков).
Тип I
Поражение общего печеночного протока
Тип II
Поражение слияния печеночных протоков
Тип IIIA
Поражение правого печеночного протока
Тип IIIB
Поражение левого печеночного протока
Тип IV
Поражение обоих печеночных протоков
Стадирование рака внепеченочных желчных протоков (дистальные - ниже впадения пузырного протока)
T - первичная опухоль:
TХ - недостаточно данных для оценки первичной опухоли;
T0 - первичная опухоль не определяется;
Tis - рак insitu (высокая степень дисплазии);
T1 - опухоль проникает в стенку протока на глубину менее 5 мм;
T2 - опухоль проникает в стенку протока на глубину 5-12 мм;
T3 - опухоль проникает в стенку протока на глубину более 12 мм;
T4 - инвазия опухоли в чревный ствол, верхнюю брыжеечную артерию или общую печеночную.
N - регионарные лимфатические узлы:
NX - недостаточно данных для оценки поражения лимфоузлов;
N0 - нет признаков метастатического поражения регионарных лимфатических узлов;
N1 - от одного до трех положительных лимфатических узлов;
N2-четыре или более положительных лимфатических узла.
М - отдаленные метастазы:
М0 - нет отдаленных метастазов;
М1 - есть отдаленные метастазы.
Таблица 5. Группировка по стадиям рака внепеченочных желчных протоков (дистальных).
Стадия
T
N
M
Стадия 0
Tis
N0
M0
Стадия I
T1
N0
M0
Стадия IIА
T1
T2
N1
N0
M0
M0
Стадия IIВ
T2
T3
T3
N1
N0
N1
M0
M0
M0
Стадия IIIA
T1
T2
T3
N2
N2
N2
M0
M0
M0
Стадия IIIB
T4
T4
T4
N0
N1
N2
M0
M0
M0
Стадия IV
Любая T
Любая N
M1
Гистологическая градация:
Gx - недостаточно данных для оценки;
G1 - хорошо дифференцированная;
G2 - умеренно дифференцированная;
G3 - низкодифференцированная.
1.1 Определение заболевания или состояния (группы заболеваний или состояний)
Рак билиарного тракта - включает группу опухолей, развивающихся из эпителия желчного пузыря и желчных протоков. Менее трети случаев билиарного рака составляют опухоли желчного пузыря, остальные - внутрипеченочные и внепеченочные холангиокарциномы. Исключены из опухолей желчевыводящей системы опухоли Фатерова сосочка.
1.2 Этиология и патогенез заболевания или состояния (группы заболеваний или состояний)
Потенциальными факторами риска для развития внутрипеченочных холангиокарцином являются воспалительные заболевания кишечника, а также хронический вирусный гепатит В или С, цирроз печени, сахарный диабет, ожирение, алкоголь, неалкогольная жировая болезнь печени и курение [4 - 6].
Заболевания, предшествующие развитию внепеченочных холангиокарцином: склерозирующий аутоиммунный холангит, хронический холангит инфекционной природы, болезнь Кароли (Caroli), хроническая гельминтная инвазия (Оpisthorchisviverrini, Сlonorchissinensis и Оpisthorchisfelineus). Желчнокаменная болезнь не связана с этиологией холангиокарциномы.
Факторами риска развития рака желчного пузыря являются заболевания, связанные с наличием хронического воспаления, в том числе желчекаменная болезнь. К другим факторам риска относятся полипы желчного пузыря более 1 см в диаметре, хронические инфекции, склерозирующий холангит, аденоматоз желчного пузыря. Воспалительные заболевания кишечника (неспецифический язвенный колит) также ассоциируются с повышенным риском рака билиарного тракта [1 - 3].
1.3 Эпидемиология заболевания или состояния (группы заболеваний или состояний)
Рак билиарного тракта - редкий вид злокачественного опухолевого поражения. В отчетах по оценке заболеваемости и смертности в большинстве случаев нет разделения по локализации поражения тех или иных желчных протоков эти опухоли рассматриваются в единой группе. В Российской Федерации в 2020 году раком печени заболело 8957 пациентов. По грубым подсчетам рак внутрипеченочных желчных протоков составляет около 10% от этого числа, т.е. в 2020 году в России было зарегистрировано около 896 пациентов, заболевших раком внутрипеченочных желчных протоков. Внепеченочные холангиокарциномы и рак желчного пузыря зарегистрированы у 3539 первичных пациентов (1295 - мужчины и 2244 - женщины). Точная статистика смертности от билиарного рака в России отсутствует. Тем не менее от рака печени (гепато- и холангиоцеллюлярный раки) умерло 10625 пациентов, а от рака желчного пузыря, внепеченочных желчных протоков и других неуточненных органов пищеварения погибли 3783 пациентов. Заболеваемость повышается с возрастом; внутрипеченочная холангиокарцинома у женщин выявляется чаще, чем мужчин [7, 8].
Диагностика и лечение детей с указанными ЗНО проводится согласно рекомендаций для пациентов старше 18 лет (в связи с малочисленностью заболевших детей) в условиях национальных (федеральных) центров.
1.4 Особенности кодирования заболевания или состояния (группы заболеваний или состояний) по Международной статистической классификации болезней и проблем, связанных со здоровьем
С22.1 Рак внутрипеченочных желчных протоков
С23 Злокачественное новообразование желчного пузыря
С24.0 Внепеченочного желчного протока
Желчного протока или прохода БДУ
Общего желчного протока
Пузырного протока
Печеночного протока
С24.8 Поражение желчных путей, выходящее за пределы одной и более вышеуказанных локализаций
Злокачественное новообразование желчных путей, выходящее за пределы одной и более вышеуказанных локализаций, злокачественное новообразование, захватывающее внутрипеченочные и внепеченочные желчные протоки, злокачественное новообразование желчных путей, которое по месту возникновения не может быть отнесено ни к одной из рубрик С22.1-С24.8
С24.9 Поражение желчных путей неуточненное
1.5 Классификация заболевания или состояния (группы заболеваний или состояний)
Всемирная организация здравоохранения, 2019 г.
Опухоли печени и внутрипеченочных желчных протоков
Доброкачественные билиарные опухоли и предопухолевые процессы
8160/0 - Аденома желчных протоков (билиарная аденома)
9013/0 - Аденофиброма, БДУ
8148/0 - Билиарная интраэпителиальная неоплазия, low grade
8148/2 - Билиарная интраэпителиальная неоплазия, high grade
8503/0 - Внутрипротоковая папиллярная опухоль с интраэпителиальной неоплазией, low grade
8503/2 - Внутрипротоковая папиллярная опухоль с интраэпителиальной неоплазией, high grade
8503/3 - Внутрипротоковая папиллярная опухоль в сочетании с инвазивной карциномой
8470/0 - Муцинозная кистозная опухоль с интраэпителиальной неоплазией, low grade
8470/2 - Муцинозная кистозная опухоль с интраэпителиальной неоплазией, high grade
8470/3 - Муцинозная кистозная опухоль в сочетании с инвазивной карциномой
Злокачественные билиарные опухоли
8160/3 - Холангиокарцинома
Крупнопротоковая внутрипеченочная холангиокарцинома
Мелкопротоковая внутрипеченочная холангиокарцинома
8020/3 - Рак, недифференцированный, БДУ
8180/3 - Комбинированный гепатоцеллюлярный рак и холангиокарцинома
8240/3 - Нейроэндокринная опухоль, БДУ
8240/3 - Нейроэндокринная опухоль, grade 1
8249/3 - Нейроэндокринная опухоль, grade 2
8249/3 - Нейроэндокринная опухоль, grade 3
8246/3 - Нейроэндокринный рак, БДУ
8013/3 - Крупноклеточный нейроэндокринный рак
8041/3 - Мелкоклеточный нейроэндокринный рак
8154/3 - Смешанная нейроэндокринная/не нейроэндокринная опухоль (MiNEN)
Опухоли внепеченочных желчных протоков
8160/3 - Холангиокарцинома
8070/3 - Плоскоклеточный рак БДУ
8560/3 - Железисто-плоскоклеточный рак
8020/3 - Недифференцированный рак БДУ
Опухоли желчного пузыря
8140/3 - Аденокарцинома БДУ
8070/3 - Плоскоклеточный рак БДУ
8020/3 - Карцинома недифференцированная БДУ
Рак внепеченочных желчных протоков встречается значительно чаще внутрипеченочной холангиокарциномы: на опухолевое поражение проксимального отдела внепеченочных желчных протоков приходится 50% от числа холангиокарцином, на опухоли дистальной локализации - 42%, внутрипеченочное поражение встречается в 8% случаев [9]. Среди опухолей желчного пузыря чаще всего (80%) встречаются аденокарциномы, возможны и другие варианты: плоскоклеточный, анапластический, мелкоклеточный рак, лимфомы, саркомы [1]. Рак желчного характеризуется местной и сосудистой инвазией, обширным регионарным лимфогенным и гематогенным метастазированием. Более 90% случаев холангиокарцином составляют аденокарциномы, часто (>80%) муцинозные. Ранее опухоли макроскопически подразделялись по характеру роста на 4 типа [167]:
- Инфильтративный
- Нодулярный
- Нодулярно-инфильтративный
- Папиллярный
1.6 Клиническая картина заболевания или состояния (группы заболеваний или состояний)
Ранние симптомы рака внутрипеченочного желчного протока и рака желчного пузыря крайне неспецифичны: дискомфорт, тяжесть в правом подреберье или эпигастрии, снижение аппетита. Иногда наличие опухолевого поражения можно выявить по изменениям результатов биохимических анализов крови (повышение активности трансаминаз или показателей холестаза), а также по увеличению уровней опухолевых маркеров у пациентов из группы повышенного риска (желчекаменная болезнь, полипы желчного пузыря, первичный склерозирующий холангит, паразитарная инвазия и т.д.), что, впрочем, также не является специфичным.
Более значимые симптомы (боли в верхнем отделе живота, тошнота, рвота, потеря аппетита или даже отвращение к пище, снижение веса, желтуха, зуд, лихорадка, увеличение размеров печени и желчного пузыря, появление асцита) являются признаками поздних стадий заболевания. Симптомы билиарного рака могут маскироваться симптомами фоновых заболеваний (желчекаменной болезни, первичного склерозирующего холангита, язвенного колита).
Рак внепеченочных желчных протоков, напротив, часто манифестирует механической желтухой при обструкции общего печеночного/желчного протоков или в связи с двухсторонним блоком правого и левого долевых протоков. До полной обструкции с развернутой картиной механической желтухи могут быть неспецифические жалобы на тяжесть в подреберье, лихорадку, озноб, в последующем - кожный зуд, посветление кала, потемнение мочи. На доклиническом или субклиническом уровне возможны отклонения в биохимическом анализе крови (маркеры цитолиза, холестаза).
Стадирование TNM (8-я редакция)
Стадирование опухолей внутрипеченочных желчных протоков
T - первичная опухоль:
Tx - недостаточно данных для оценки первичной опухоли;
T0 - первичная опухоль не определяется;
Tis - рак in situ (внутрипротоковая опухоль);
T1 - солитарная опухоль без инвазии сосудов, < 5 см или > 5 см;
T1a - солитарная опухоль < 5 см без инвазии сосудов;
T1b - солитарная опухоль > 5 см без инвазии сосудов;
T2 - солитарная опухоль с внутрипеченочной инвазии сосудов или множественные опухолевые узлы, с или без инвазии сосудов;
T3 - опухоль, прорастающая висцеральную брюшину;
T4 - опухоль, вовлекающая внепеченочные местные структуры путем прямой инвазии.
N - регионарные лимфатические узлы
Nx - недостаточно данных для оценки состояния регионарных лимфатических узлов;
N0 - нет признаков метастатического поражения регионарных лимфатических узлов;
N1 - имеется поражение регионарных лимфатических узлов метастазами.
M - отдаленные метастазы:
M0 - нет признаков отдаленных метастазов;
M1 - имеются отдаленные метастазы.
К регионарным лимфатическим узлам при внутрипеченочной холангиокарциноме левой доли печени относятся лимфоузлы вдоль гепатодуоденальной связки (узлы вдоль общего желчного протока, печеночной артерии, воротной вены и пузырного протока), лимфатические узлы вдоль печеночно-желудочной связки, а также нижние диафрагмальные узлы (как частный вариант метастазирования).
При опухолях правой доли печени к регионарным относятся лимфатические узлы вдоль гепатодуоденальной связки, а также околодвенадцатиперстные и перипанкреатические лимфатические узлы.
Таблица 1.
Группировка по стадиям рака внутрипеченочных желчных протоков (AJCC)
Стадия
T
N
M
Стадия 0
Tis
N0
M0
Стадия IA
T1а
N0
M0
Стадия IB
T1в
N0
M0
Стадия II
T2
N0
M0
Стадия IIIA
T3
N0
M0
Стадия IIIB
T4
Любая N
M0
Любая T
N1
M0
Стадия IV
Любая T
Любая N
M1
Для всех внутрипеченочных холангиокарцином отдаленным считается метастазирование в чревные, парааортальные или паракавальные лимфатические узлы. Типичными участками отдаленного распространения являются внутрипеченочные очаги, а также поражение брюшины и далее в порядке убывания по частоте встречаемости кости, легкие и плевра.
Гистологическая градация:
Gx - недостаточно данных для оценки;
G1 - хорошо дифференцированная;
G2 - умеренно дифференцированная;
G3 - низкодифференцированная.
Стадирование рака проксимального отдела внепеченочных желчных протоков
T - первичная опухоль:
Tx - недостаточно данных для оценки первичной опухоли;
T0 - первичная опухоль не определяется;
Tis - рак in situ (высокая степень дисплазии);
T1 - опухоль, ограниченная желчным протоком, с расширением до мышечного слоя или волокнистой (фиброзной) ткани;
T2 - опухоль проникает за стенку желчного протока в окружающую жировую ткань, или опухоль проникает в соседнюю печеночную паренхиму:
T2a - опухоль прорастает за пределы стенки протока с инвазией в окружающую жировую ткань;
T2b - опухоль прорастает в прилежащую паренхиму печени;
T3 - опухоль прорастает в ветви воротной вены или печеночной артерии с одной стороны;
T4 - опухоль прорастает в главный ствол воротной вены или ее ветви с обеих сторон; или инвазия общей печеночной артерии; или распространение опухоли на протоки 2 порядка с обеих сторон; или поражение протоков 2 порядка с одной стороны с инвазией контралатеральной ветви воротной вены или вовлечением печеночной артерии.
N - регионарные лимфатические узлы - ворот печени, вдоль пузырного и общего желчного протоков, воротной вены, печеночной артерии, а также задние панкреатодуоденальные лимфоузлы.
NX - недостаточно данных для оценки поражения лимфоузлов;
N0 - нет признаков метастатического поражения регионарных лимфатических узлов;
N1 - от одного до трех положительных лимфатических узлов, поражение лимфоузлов вдоль пузырного протока, общего желчного протока, печеночной артерии, задние панкреатодуоденальной и/или воротной вены;
N2 - четыре или более положительных лимфатических узла из участков, описанных для N1.
М - отдаленные метастазы:
М0 - нет отдаленных метастазов;
М1 - есть отдаленные метастазы.
Метастазы в лимфатические узлы, расположенные дистальнее гепатодуоденальной связки, классифицируются как отдаленные метастазы.
Таблица 2.
Группировка по стадиям рака внепеченочных желчных протоков (в области ворот печени)
Стадия
Т
N
M
Стадия 0
Tis
N0
M0
Стадия I
T1
N0
M0
Стадия II
T2a-b
N0
M0
Стадия IIIA
T3
N0
M0
Стадия IIIB
T4
N0
M0
Стадия IIIC
Любая T
N1
M0
Стадия IVA
Любая T
N2
M0
Стадия IVB
Любая T
Любая N
M1
Гистологическая градация:
Gx - недостаточно данных для оценки;
G1 - хорошо дифференцированная;
G2 - умеренно дифференцированная;
G3 - низкодифференцированная.
Модифицированная система стадирования Вismuth-Corlette классифицирует опухоли проксимальных желчных протоков на 4 типа, основанные на степени поражения желчных протоков (Таблица 3).
Таблица 3.
Классификация Bismuth-Corlette (для рака проксимальных желчных протоков)
Тип I
Поражение общего печеночного протока
Тип II
Поражение слияния печеночных протоков
Тип IIIA
Поражение правого печеночного протока
Тип IIIB
Поражение левого печеночного протока
Тип IV
Поражение обоих печеночных протоков
Стадирование рака дистального отдела внепеченочных желчных протоков
T - первичная опухоль:
Tx - недостаточно данных для оценки первичной опухоли;
T0 - первичная опухоль не определяется;
Tis - рак in situ (высокая степень дисплазии).
T1 - опухоль проникает в стенку протока глубиной менее 5 мм;
T2 - опухоль проникает в стенку протока глубиной 5 - 12 мм;
T3 - опухоль проникает в стенку протока глубиной более 12 мм;
T4 - инвазия опухоли в чревный ствол, верхнюю брыжеечную и/или общую печеночную артерию.
N - регионарные лимфатические узлы: вдоль общего желчного протока, общей печеночной артерии, воротной вены, передние и задние панкреатодуоденальные узлы и лимфатические узлы, расположенные справа и вдоль верней брыжеечной артерии.
NX - недостаточно данных для оценки поражения лимфоузлов;
N0 - нет признаков метастатического поражения регионарных лимфатических узлов;
N1 - от одного до трех положительных лимфатических узлов;
N2 - четыре или более положительных лимфатических узла.
M - отдаленные метастазы:
M0 - нет отдаленных метастазов;
M1 - есть отдаленные метастазы.
Таблица 4.
Группировка по стадиям рака внепеченочных желчных протоков (дистальных)
Стадия
Т
N
M
Стадия 0
Tis
N0
M0
Стадия I
T1
N0
M0
Стадия IIA
T1
N1
M0
T2
N0
M0
Стадия IIB
T2
N1
M0
T3
N0
M0
T3
N1
M0
Стадия IIIA
T1
N2
M0
T2
N2
M0
T3
N2
M0
Стадия IIIB
T4
N0
M0
T4
N1
M0
T4
N2
M0
Стадия IV
Любая T
Любая N
M1
Гистологическая градация:
Gx - недостаточно данных для оценки;
G1 - хорошо дифференцированная;
G2 - умеренно дифференцированная;
G3 - низкодифференцированная.
Стадирование рака желчного пузыря
T - первичная опухоль:
TХ - недостаточно данных для оценки первичной опухоли;
T0 - первичная опухоль не определяется;
Tis - рак in situ;
T1 - опухоль прорастает в собственную пластинку или мышечный слой;
T1a - опухоль прорастает в собственную пластинчатую оболочку;
T1b - опухоль прорастает в мышечный слой;
T2 - опухоль проникает в перимускулярную соединительную ткань на брюшной стороне, без вовлечения серозы (висцеральной брюшины) или опухоль проникает в перимышечной соединительной ткани на печеночной стороне, без врастания в печень.
T2a - опухоль проникает в перимускулярную соединительную ткань на брюшной стороне, без вовлечения серозы (висцеральной брюшины).
T2b - опухоль проникает в перимускулярную соединительную ткань на печеночной стороне, без врастания в печень.
T3 - опухоль прорастает серозу (висцеральную брюшину) и/или прямая инвазия в печень и/или другие соседние органы и структуры (желудок, двенадцатиперстная кишка, ободочная кишка, поджелудочная железа, сальник, внепеченочные желчные протоки);
T4 - инвазия опухоли в воротную вену или печеночную артерию, или инвазия двух и более органов и структур.
N - регионарные лимфатические узлы относятся лимфатические узлы вдоль гепатодуоденальной связки, а также околодвенадцатиперстные и перипанкреатические лимфатические узлы.
Nx - недостаточно данных для оценки поражения лимфоузлов;
N0 - нет признаков метастатического поражения регионарных лимфатических узлов;
N1 - поражение от одного до трех регионарных лимфатических узлов;
N2 - поражение четырех и более лимфатических узлов.
M - отдаленные метастазы:
M0 - нет отдаленных метастазов;
M1 - есть отдаленные метастазы.
Таблица 5 Группировка рака желчного пузыря по стадиям
Стадия
T
N
M
Стадия 0
Tis
N0
M0
Стадия I
T1
N0
M0
Стадия IIA
T2а
N0
M0
Стадия IIB
T2в
N0
M0
Стадия IIIA
T3
N0
M0
Стадия IIIB
T1-3
N1
M0
Стадия IVA
T4
N0-1
M0
Стадия IVB
Любая T
N2
M0
Любая T
Любой N
M1
Гистологическая градация:
Gx - недостаточно данных для оценки;
G1 - хорошо дифференцированная;
G2 - умеренно дифференцированная;
G3 - низкодифференцированная.
2. Диагностика заболевания или состояния (группы заболеваний или состояний) медицинские показания и противопоказания к применению методов диагностики
Критерии установления диагноза:
1. Наличие опухолевого очага в печени по данным УЗКТ, МРТ или КТ.
2. Морфологическое подтверждение диагноза.
3. Исключение других первичных опухолевых очагов (рак толстой кишки, рак желудка и т.д.)
2.1 Жалобы и анамнез
- Рекомендуется тщательный сбор жалоб и анамнеза у пациента с целью выявления факторов, которые могут повлиять на выбор тактики лечения [10].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 5)
Комментарий: сбор информации о жалобах и деталях анамнеза, в том числе семейного анамнеза, проводится с целью выявления факторов, которые могут повлиять на выбор тактики лечения
2.2 Физикальное обследование
- Рекомендуется всем пациентам выполнить врачебный осмотр и оценку нутритивного статуса [10,13].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 5)
- Рекомендуется оценка всем пациентам статуса по ECOG для определения дальнейшей тактики лечения, в том числе оценки возможности проведения химиотерапии и ее выбора, а так же определения прогноза для пациента [14 - 18].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 4)
2.3 Лабораторные диагностические исследования
- Пациентам с внутрипеченочной холангиокарциномой рекомендуется выполнить определение основных групп крови по системе AB0, определение антигена D системы Резус (резус-фактор); молекулярно-биологическое исследование крови на вирус гепатита B (Hepatitis B virus), молекулярно-биологическое исследование крови на вирус гепатита C (Hepatitis C virus); общий (клинический) анализ крови развернутый клинический и биохимический общетерапевтический анализы крови, исследование уровня ракового эмбрионального антигена (РЭА) в крови, исследование уровня антигена аденогенных раков CA 19-9 в крови, исследование уровня альфа-фетопротеина (АФП), Ig4 в крови, коагулограмму (ориентировочное исследование системы гемостаза), а также общий (клинический) анализ мочи для определения тактики лечения и дифференциальной диагностики заболевания [10, 19 - 24].
Уровень убедительности рекомендаций - B (уровень достоверности доказательств 4)
Комментарий: данный объем лабораторной диагностики выполняется на этапе диагностики и перед планированием лечения. В процессе проведения терапии объем и кратность выполнения лабораторных исследований определяется клинической необходимостью. Клинический анализ крови должен быть выполнен не более чем за 5 дней до начала курса химиотерапии или лучевой терапии. Перечень параметров биохимического общетерапевтического анализа крови и коагулограммы лечащий врач должен определять для каждого пациента индивидуально с учетом его особенностей. Необходимо помнить, что уровень СА19-9 может быть повышен на фоне желтухи, холангита или иного воспалительного процесса в панкреатобилиарной области, в связи с чем исследование базового уровня антигена аденогенных раков СА 19-9 в крови должно проводиться после билиарной декомпрессии, нормализации уровня билирубина и купирования воспалительных явлений.
Внепеченочная холангиокарцинома (рак проксимального и дистального отделов внепеченочных желчных протоков
Комментарий: определение уровня АФП у больного при подозрении на внепеченочную холангиокарциному не обязательно.
Рак желчного пузыря
Комментарий: определение уровня АФП при наличии подозрения у больного на рак желчного пузыря не обязательно.
2.4 Инструментальные диагностические исследования
Внутрипеченочная холангиокарцинома
- Ультразвуковое исследование брюшной полости (комплексное) в качестве скрининга может выявить образование в печени при внутрипеченочной форме холангиокарциномы, так же возможно его применение для навигации в ходе чрескожной аспирационной/инцизионной биопсии опухолей опухолеподобных образований мягких тканей [168] и контроля за эффективность лекарственного лечения.
- Рекомендуется проведение биопсии с последующим патолого-анатомическим исследованием биопсийного (операционного) материала с проведением иммуно-гистохимического исследования при необходимости [169, 170].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 5).
Комментарий: Отрицательный результат биопсии при положительных данных лучевого исследования - повод для повторных процедур, пока не будет получен диагностически значимый материал. Наиболее оптимальным способом забора материала является чрескожная чреспеченочная биопсии под УЗКТ или РКТ контролем, допустима биопсия печени под эндовидеохирургическим контролем. Открытая биопсия печени должна применяться в крайних редких случаях.
Дифференциальная диагностика: Ключевые новообразования, с которыми стоит дифференцировать внутрипеченочный ХЦР при исключении метастатического процесса в печени, гепатоцеллюлярный рак, эпителиоидная гемангиоэндотелиома, билиарная аденома, дуктулярная реакция с атипией, билиарная аденофиброма. Каждая из нозологических единиц имеет характерную гистологическую картину. Для уточнения диагноза, как правило, используется метод ИГХ-диагностики [3, 164].
Гепатоцеллюлярный рак
При иммуногистохимическом исследовании
позитивные реакции с аргиназой-1, HepPar1, глипиканом 3, CD10 (каналикулярное окрашивание)
Метастатическая аденокарцинома
Анамнез (данные о наличии первичного очага)
Окончательный диагноз может быть установлен коллегиально (данные клинико-рентгенологического обследования, гистологического и иммуногистохимического исследований)
Эпителиоидная гемангиоэндотелиома
При иммуногистохимическом исследовании
позитивные реакции с CD31, CD34, FLI-1, ERG
Комбинированный гепатоцеллюлярный рак/холангиокарцинома
Наличие гепатоцеллюлярного компонента (при рутинном гистологическом исследовании, подтвержденным иммуногистохимическим методом)
Билиарная аденома
Меньшие размеры, четкие границы
Низкий индекс Ki67 (< 10%), p53 ("дикий" тип экспрессии)
Дуктулярная реакция с атипией
Дольковое строение, минимально выраженная атипия
Билиарная аденофиброма
Тубулокистозная пролиферация билиарного эпителия с минимально выраженной атипией
- При выявлении при УЗИ опухолевой патологии рекомендуется выполнить компьютерную томографию органов брюшной полости с внутривенным болюсным контрастированием и компьютерную томографию органов малого таза у женщин/у мужчин с контрастированием и/или магнитно-резонансную томографию (МРТ) органов брюшной полости с внутривенным контрастированием с магнитно-резонансной холангиопанкреатографией [10, 29, 30]. МРТ обладает преимуществом над КТ в оценке внутрипеченочной распространенности холангиокарциномы [171]
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 5).
Комментарий: КТ является более специфичным, чем УЗИ, для выявления поражения лимфатических узлов, инвазии органов и отдаленных метастазов; с помощью МРТ можно проводить дифференциальную диагностику между доброкачественными опухолями и раком [31].
- Перед началом лечения всем пациентам рекомендуется выполнить КТ органов грудной полости для определения распространенности опухолевого процесса [10, 32, 33].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 5).
- При планировании хирургического лечения взрослым пациентам рекомендовано выполнить позитронную эмиссионную томографию, совмещенную с компьютерной томографией с туморотропными РФП (ПЭТ-КТ), с целью исключения отдаленных метастазов в случае подозрения на их наличие по данным комплексного обследования [36, 37].
Уровень убедительности рекомендаций - B (уровень достоверности доказательств - 2)
Внепеченочная холангиокарцинома (рак проксимального и дистального отделов внепеченочных желчных протоков)
Ультразвуковое исследование брюшной полости в ходе первичной диагностики у больных с внепеченочной холангиокарциномой имеет ограниченное значение. В подавляющем большинстве случаев наличие опухолевой патологии возможно заподозрить только по косвенным признакам (расширение внутри- и внепеченочных желчных протоков, иногда утолщение стенки протоков в некоторых случаях определяется лимфаденопатия в проекции малого сальника)
- До начала лечения всем больным - кандидатам на проведение не хирургических методов терапии рекомендовано морфологическое подтверждение диагноза с патолого-анатомическим исследованием биопсийного (операционного) материала с применением иммуногистохимических методов [10, 40 - 42]. В случаях технических сложностей и рисков осложнений, связанных со взятием биопсийного материала возможно цитологическое подтверждение диагноза. Биопсия может выполняться чрескожным доступом под УЗКТ или РКТ при нодулярной форме роста опухоли, в остальных случаях применяется внутрипротоковая биопсия (антеградным либо ретроградным доступом в зависимости от метода ранее примененной билиарной декомпрессии или в ходе ее осуществления) под рентгенологическим и/или видеохолангиоскопическим контролем.
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 5)
Комментарий: биопсия необходима для назначения консервативных методов лечения, но не обязательна при планировании хирургического вмешательства в случаях явной клинико-инструментальной картины заболевания [40, 43].
- Всем пациентам с внепеченочной холангиокарциномой рекомендовано выполнить компьютерную томографию (КТ) органов брюшной полости и малого таза с внутривенным контрастированием и/или магнитно-резонансную томографию (МРТ) органов брюшной полости с внутривенным контрастированием с магнитно-резонансной холангиографией [10, 29, 30]. При подозрении на опухолевый процесс дистального отдела внепеченочных желчных протоков основными методами диагностики являются МСКТ. При подозрении на поражение проксимального отдела желчных протоков необходимо выполнять МРТ и магнитно-резонансная холангиопанкреатографию (МРХПГ). МСКТ с болюсным контрастированием в данном случае служит уточняющим способом диагностики. Окончательным методом определения уровня билиарного блока является прямая холангиография (ЭРХПГ или ЧЧХГ), используемая в настоящее время только в момент декомпрессии желчных потоков и непосредственно перед операцией [137 - 142].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 5)
Комментарий: КТ является более специфичным, чем УЗИ, для выявления поражения лимфатических узлов, инвазии органов и отдаленных метастазов; с помощью МРТ можно проводить дифференциальную диагностику между доброкачественными опухолями и раком [31]. При раке проксимального отдела внепеченочных желчных протоков МРТ и МРХГ проводится с целью уточнения степени разобщения внутрипеченочных желчных протоков и выявления опухолевого распространения. МСКТ с болюсным контрастированием проводится в случаях подозрения на вовлечение сосудов гепатопанкреатодуоденальной зоны.
- Перед началом лечения всем пациентам рекомендуется выполнить КТ органов грудной полости для определения распространенности опухолевого процесса [10, 32, 33].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 5)
- При планировании хирургического лечения у взрослых рекомендовано выполнить позитронную эмиссионную томографию, совмещенная с компьютерной томографией с туморотропными РФП (ПЭТ-КТ) с целью исключения отдаленных метастазов в случае наличия подозрения на их наличие по данным комплексного обследования [36, 37].
Уровень убедительности рекомендаций - A (уровень достоверности доказательств - 1)
- При планировании хирургического лечения у взрослых рекомендуется выполнить лапароскопию диагностическую для исключения отдаленных метастазов в случае подозрения на их наличие по данным комплексного обследования [2, 3, 38].
Уровень убедительности рекомендаций - A (уровень достоверности доказательств - 1).
- Пациентам с раком дистального отдела внепеченочных желчных протоков рекомендуется выполнить эндосонографию панкреатобилиарной зоны для дополнительной оценки местной распространенности опухоли и дифференциальной диагностики с опухолевым поражением головки поджелудочной железы. [195, 198]
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 5
Рак желчного пузыря
- Ультразвуковое исследование брюшной полости рекомендуется в ходе первичной диагностики у больных с подозрением на рак желчного пузыря имеет важное значение и может использоваться для скрининга. С его помощью можно выявить наличие инфильтрата в области желчного пузыря или рост ранее выявленного полипа, а также признаки билиарной гипертензии осложненных формах. [196, 197]
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 5).
Комментарий: Морфологическая верификация болезни крайне сложна на ранних стадиях и в большинстве случаев становится возможной только при распространении опухолевого процесса на паренхиму печени либо заполнении опухолевыми массами полости желчного пузыря [188, 189]. Биопсия необходима для назначения консервативных методов лечения, но не обязательна при планировании хирургического вмешательства в случаях явной клинико-инструментальной картины заболевания [40, 43].
- Всем пациентам с раком желчного пузыря для определения тактики лечения рекомендовано выполнить компьютерную томографию органов брюшной полости с внутривенным болюсным контрастированием и компьютерную томографию малого таза с внутривенным контрастированием и/или магнитно-резонансную томографию органов брюшной полости, магнитно-резонансную томографию забрюшинного пространства с внутривенным контрастированием с магнитно-резонансной холангиопанкреатографией [10, 29, 30].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 5).
Комментарий: при наличии подозрения по данным лучевых методов обследования на вовлечение в опухолевый процесс желудка и/или ободочной кишки больному необходимо выполнить эзофагогастродуоденоскопию и колоноскопию.
- Перед началом лечения всем пациентам рекомендуется выполнить КТ органов грудной полости для определения распространенности опухолевого процесса [10, 32, 33].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 5).
- При планировании хирургического лечения рекомендовано выполнить позитронную эмиссионную томографию, совмещенная с компьютерной томографией с туморотропными РФП, с целью исключения отдаленных метастазов в случае подозрения на их наличие по данным комплексного обследования [36, 37].
Уровень убедительности рекомендаций - B (уровень достоверности доказательств - 2)
- При планировании хирургического лечения рекомендуется выполнить лапароскопию диагностическую для исключения отдаленных метастазов в случае подозрения на их наличие по данным комплексного обследования [2, 3, 38].
Уровень убедительности рекомендаций - B (уровень достоверности доказательств - 2)
Комментарий: В связи с высокой частотой перитонеального диссеминирования у больных раком жечного пузыря данный метод позволяет отказаться от неоправданной лапаротомии у трети пациентов, которые по результатам МРТ/КТ/ПЭТ-КТ представляются резектабельными [2, 39].
2.5 Иные диагностические исследования
Большая часть внутрипеченочных холангиокарцином - умеренно-высокодифференцированные тубулярные аденокарциномы [1]. В последнее время [2] ХЦР подразделен на 2 типа с учетом локализации опухоли и ее иммуногистохимических особенностей:
а) билиарный тип с выраженной экспрессией S100P, TFF1, AGR2, в 23% случаев выявляется KRAS-мутация;
б) холангиолярный тип с выраженной экспрессией N-кадгерина, лишь в 1% случаев выявляется KRAS-мутация.
Внутрипеченочные ХЦР имеют иммуногистохимический профиль, сходный с другими опухолями панкреато-билиарной зоны и верхнего отдела желудочно-кишечного тракта. В настоящее время не существует ни одной однозначной окраски для подтверждения ХЦР [3]. Как правило, эти опухоли позитивны по отношению к цитокератинам 7,19 (90%), муцину 1 (73,8%) [162].
Возможна фокальная экспрессия цитокератина 20 в клетках опухоли, однако в сочетании с экспрессией цитокератинов 7 и 19 необходимо исключать другие опухоли желудочно-кишечного тракта [1].
К наиболее часто встречающимся вариантам данных опухолей относят высоко- и умеренно дифференцированные аденокарциномы билиарного типа. Большая часть их иммунопозитивна по отношению к раковому эмбриональному антигену, муцинам 1 и 2, p53, цитокератину 7.
ИГХ-картина аденокарцином холангиолярного типа отлична, характеризуется экспрессией муцина 2, ракового эмбрионального антигена и цитокератина 20 [162].
- Рекомендуется для определения тактики лекарственного лечения [10, 41, 44, 172] провести в биопсийном (операционном) материале (предпочтительно, методом высокопроизводительного панельного секвенирования - ДНК/РНК) образца (биоптата или операционного материала) опухолевой ткани:
- молекулярно-генетическое исследование мутаций в гене KRAS в биопсийном (операционном) материале
- молекулярно-генетическое исследование мутаций в гене BRAF в биопсийном (операционном) материале
- определение амплификации гена ERBB2 (HER2/Neu) методом флюоресцентной гибридизации in situ (FISH)
- определение мутаций в генах MLH1, MSH2, MSH6, PMS2 иммуногистохимическим методом
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 5)
Комментарий: при выявлении активирующей и таргетируемой (существует активный препарат, эффективно воздействующий на эту молекулярную альтерацию) мутации в опухоли пациента с распространенным/метастатическим процессом проведение таргетной терапии с учетом выявленного молекулярного нарушения может значимо увеличить продолжительность жизни; активирующие мутации, определяющие чувствительность опухоли к таргетной терапии, чаще всего (до 40% случаев) выявляются при внутрипеченочной холангиокарциноме. На данный момент определение транслокации генов NTRK, FGFR1-4 отсутствуют в номенклатуре медицинских услуг, однако выполнение данного молекулярно-генетического тестирования для пациентов с внутрипеченочной холангиокарциномой с целью возможного назначения молекулярно-направленной терапии обязательно.
3. Лечение, включая медикаментозную и немедикаментозную терапии, диетотерапию, обезболивание, медицинские показания и противопоказания к применению методов лечения
- Рекомендуется рассматривать хирургическое вмешательство, как основной метод радикального лечения больных раком билиарного тракта [10, 45, 46].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 5)
3.1 Предоперационное лечение
- При наличии явлений механической желтухи рекомендуется провести предоперационную декомпрессию желчевыводящих путей (чрескожная чреспеченочная холангиостомия, эндоскопическое назобилиарное дренирование, ретроградное стентирование) с целью купирования механической желтухи [51 - 53]. В клинической практике рекомендуется выбирать вид дренирования, исходя из уровня блока желчных протоков, цели дренирования (для последующего хирургического или паллиативного лечения), технологических возможностей клиники и опыта персонала [143].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 2)
- При I и II типе блока по Bismuth у больных раком проксимального отдела внепеченочных желчных протоков рекомендуется отдавать предпочтение эндоскопическому ретроградному доступу для билиарной декомпрессии при условии соответствующего оснащения лечебного учреждения аппаратурой и опытными специалистами по оперативной эндоскопии [190].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 5).
- При III - IV типе блока по Bismuth больным раком проксимального отдела внепеченочных желчных протоков и с внутрипеченочной холангиокарциномой, осложненной механической желтухой, предпочтительным методом желчной декомпрессии рекомендуется рентгенохирургическое чрескожное наружное дренирование желчных протоков печени [190, 191].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 3).
Комментарий: у больных раком проксимального отдела внепеченочных желчных протоков и больных с внутрипеченочной холангиокарциномой, течение болезни у которых осложнилось механической желтухой, необходимо адекватное дренирование обеих долей печени для купирования холангита и подготовки к радикальной операции, этого не могут дать ретроградные методы дренирования. [144, 145].
- Методом выбора билиарной декомпрессии при опухолевом поражении дистального отдела внепеченочных желчных протоков являются эндоскопическое назобилиарное дренирование или ретроградная установка стента [146, 147]. Установка саморасширяющихся металлических стентов перед радикальной операций недопустима, и может иметь место только при подтверждении нерезектабельности опухолевого процесса [163]. В случае невозможности выполнения эндоскопических ретроградных вмешательств следует отдать предпочтение чрескожной чреспеченочной холангиостомии [148, 149].
- При объеме предполагаемой остающейся паренхимы печени <40%, в качестве предоперационной подготовки взрослых пациентов с внутрипеченочной холангиокарциномой или раком проксимального отдела внепеченочных желчных протоков рекомендуется рассмотреть селективную эндоваскулярную эмболизацию ветвей воротной вены (как правило, правой, иногда в сочетании с эмболизацией ветвей четвертого сегмента печени), что позволяет снизить риск развития печеночной недостаточности в послеоперационном периоде [47 - 50].
Уровень убедительности рекомендаций - B (уровень достоверности доказательств 2)
Комментарий: предоперационная эмболизация ветвей воротной вены повышает объем предполагаемой остающейся паренхимы. Хирургическое лечение выполняется по мере достижения целевого объема предполагаемой остающейся паренхимы печени (>= 40%), оценка динамики его увеличения производится не ранее чем через 3 - 5 недель после эмболизации.
3.2 Хирургическое лечение
3.2.1. Внутрипеченочная холангиокарцинома
- При резектабельной внутрипеченочной холангиокарциноме у взрослых пациентов рекомендуется выполнение радикального вмешательства в объеме резекции печени в сочетании с регионарной лимфодиссекцией. Целью хирургического лечения является удаление опухолевого узла с достижением отрицательных краев резекции. В случае инвазии внепеченочных желчных протоков целесообразна их резекция с последующей реконструкцией [70].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 4)
Комментарий: Основным условием, которое должно выполняться при планировании резекции печени является сохранение в предполагаемой остающейся части паренхимы печени адекватного кровоснабжения, крово- и желчеоттока. Объем предполагаемой остающейся паренхимы печени должен составлять при отсутствии лабораторных и инструментальных признаков цирроза не менее 25% (от не пораженной паренхимы), при их наличии не менее 40%. Так же при наличии цирроза, следует учитывать степень нарушения печено-клеточной функции (резекция печени целесообразна у больных соответствующих классу А по шкале Child-Pugh) и выраженность портальной гипертензии (клинически значимые проявления: наличие варикозно-расширенных вен пищевода, тромбоцитопения менее 100 x 109/л).
В условиях специализированных центров (при наличии подготовленного персонала и оборудования) возможно выполнение резекций печени мини-инвазивным доступом под видеоэдоскопическим контролем. Предпочтительным для планирования применения данного доступа являются подкапсульно расположенные образования, а также узлы, располагающиеся в латеральных секторах печени [75].
Следует учитывать, что большой размер опухоли и/или множественное внутриорганное поражение, наличие инвазии магистральных сосудов, соседних органов, метастатическое поражение регионарных лимфатических узлов не являются абсолютным противопоказанием к резекции печени, однако результаты хирургического лечения в этих случаях предсказуемо хуже [72].
- При локальном рецидиве внутрипеченочной холангиокарциномы рекомендуется повторная резекция печени, в случаях, когда результаты предоперационного обследования указывают на возможность достижения отрицательного края резекции [73, 74].
Уровень убедительности рекомендаций - A (уровень достоверности доказательств 2)
Комментарий: повторная резекция печени у пациентов после рецидива внутрипеченочной холангиокарциномы ассоциирована со статистически значимым увеличение одно-, трех- и пятилетней общей выживаемости (ОВ): отношение шансов (odds ratio, OR) и 95% доверительный интервал (ДИ) соответственно были равны 2,70 (1,28 - 5,68), 2,89 (1,15 - 7,27) и 5,91 (1,59 - 21,90) [73].
- При внутрипеченочной холангиокарциноме у взрослых пациентов трансплантация печени рутинно не рекомендуется в связи с высокой вероятностью раннего прогрессирования заболевания [76 - 78].
Уровень убедительности рекомендаций - B (уровень достоверности доказательств 2)
Комментарий: При внутрипеченочной холангиокарциноме трансплантация печени может быть рассмотрена как метод лечения у пациентов с выраженным циррозом и ранней стадией опухолевого процесса, а так же отдельным пациентам с мультифокальным поражением печени после курса неоадъювантной терапии [79]. Использование данного подхода было ассоциировано с более длительной безрецидивной выживаемостью, но не влияло на ОВ. После трансплантации печени у пациентов с очень ранней стадией внутрипеченочной холангиокарциномы (один очаг ![]() 2 см) отмечали более высокую пятилетнюю безрецидивную выживаемость (67%, 95% ДИ 47 - 86%), чем у пациентов с распространенным раком (34%, 95% ДИ 23 - 46%) [79].
2 см) отмечали более высокую пятилетнюю безрецидивную выживаемость (67%, 95% ДИ 47 - 86%), чем у пациентов с распространенным раком (34%, 95% ДИ 23 - 46%) [79].
3.2.2. Рак проксимального отела внепеченочных желчных протоков
- При резектабельном раке проксимального отдела внепеченочных желчных протоков рекомендуется хирургическое лечение. Объем вмешательства определяется с учетом местной распространенности опухолевого процесса. В большинстве случаев необходимо выполнение расширенной право- или левосторонней гемигепатэктомии с резекцией пораженных опухолью желчных протоков с резекцией сегмента печени S1 с последующим формированием гепатикоеюноанастомоза. Обязательным условием при выполнении оперативного вмешательства является срочное интраоперационное изучение краев резекции внепеченочных желчных протоков для достижения гистологически отрицательного результата. Изолированная резекция внепеченочных желчных протоков возможна при опухоли I - II типа по Bismuth [45,80,81, 192, 193].
Уровень убедительности рекомендаций - B (уровень достоверности доказательств 3)
Комментарий: при инвазии воротной вены целесообразна ее резекция с последующей пластикой. [82, 83]
3.2.3. Рак дистального отдела внепеченочных желчных протоков
- При раке холедоха рекомендуется радикальная операция в объеме панкреатодуоденальной резекция с удалением регионарных лимфоузлов единым блоком со срочным интраоперационным гистологическим исследованием края отсечения протока с последующим формированием анастомозов [45].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 3)
Комментарий: в случае опухолевого поражения супрапанкреатического отдела общего желчного протока (без вовлечения в опухолевый процесс головки поджелудочной железы) радикальным объемом операции так же является резекция пораженной части желчных протоков с регионарной лимфодиссекцией при условии достижения отрицательного края резекции подтвержденного в ходе срочного интраоперационного гистологического исследования.
3.2.4. Рак желчного пузыря
- При стадии T1A рака желчного пузыря рекомендуется выполнение холецистэктомии [57].
Уровень убедительности рекомендаций - B (уровень достоверности доказательств 3).
- При резектабельном раке желчного пузыря рекомендуется выполнение расширенной холецистэктомии с резекцией S IV - V сегментов печени с удалением клетчатки и регионарных лимфоузлов с или без резекции желчных протоков в зависимости от их вовлечения в опухолевый процесс [58 - 64].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств 5).
Комментарий: противопоказания для хирургического лечения: наличие множественных метастазов в печень, асцит, перитонеальные метастазы, опухолевое поражение трубчатых структур гепатодуоденальной связки, окклюзию крупных сосудов, плохое общее состояние пациента, вовлечение в опухолевый процесс головки поджелудочной железы, двенадцатиперстной кишки.
- При раке желчного пузыря с инвазией мышечной оболочки (стадия I, T1в-2N0M0) в случае выявления после холецистэктомии по поводу холецистита для улучшения отдаленных результатов лечения рекомендуется выполнение в ближайший срок повторной операции в объеме резекции печени (ложе желчного пузыря) в сочетании с лимфодиссекцией и резекцией культи пузырного протока после исключения признаков нерезектабельности по данным методов обследования [46, 66, 68 - 71].
Уровень убедительности рекомендаций - B (уровень достоверности доказательств 3)
Комментарий: при применении в ходе первой операции видеоэндохирургического доступа в случаях, когда опухоль прорастает серозу (висцеральную брюшину) и/или выявляется прямая инвазия в печень следует рассмотреть вопрос о резекции мягких тканей по ходу портовых отверстий, использованных для экстракции желчного пузыря в связи с высоким риском имплантационного метастазирования в этой зоне. При ранней стадии (рТ1а) рака желчного пузыря, выявленного после холецистэктомии, повторное хирургическое лечение не требуется [69].
3.3 Химиотерапия
- Рекомендуется адъювантная химиотерапия рака билиарного тракта пациентам после радикального хирургического лечения вне зависимости от поражения лимфатических узлов и степени дифференцировки опухоли [84 - 88].
Уровень убедительности рекомендаций - A (уровень достоверности доказательств 2).
Комментарий: после радикального хирургического лечения рекомендовано проведение монотерапии #капецитабином** (8 курсов) вне зависимости от поражения лимфатических узлов и степени дифференцировки опухоли. (Таблица 6).
По данным метаанализа, проведение адъювантной химиотерапии как после радикальной резекции (R0), так и краевой (R1) было ассоциировано со статистически значимым увеличением ОВ в среднем на 4,3 мес. (95% ДИ 0,88-7,79;p = 0,014) и уменьшением риска смерти на 41% [отношение рисков [hazard ratio, HR] = 0,59; 95% ДИ 0,49 - 0,71; p < 0,001) [85].
По данным исследования BILCAP (восемь 3-недельных циклов химиотерапии #капецитабином** в сравнении с наблюдением) медиана ОВ достоверно увеличивалась в группе адъювантной химиотерапии [53 мес vs 36 мес; ОР 0.75, 95% ДИ 0.58 - 0.97, P = 0.028], что подтверждалось и с учетом влияния значимых факторов (статус лимфоузлов, степень дифференцировки и пол) (ОР 0.71, 95% ДИ 0.55 - 0.92, P = 0.010). Более того, анализ всей группы включенных в исследование (ITT analysis) продемонстрировал более высокую безрецидивную выживаемость с #капецитабином** в течение первых 24 мес.
По данным раннего метаанализа, проведение адъювантной химиотерапии как после радикальной резекции (R0), так и краевой (R1) было ассоциировано со статистически значимым увеличением ОВ в среднем на 4,3 мес. (95% ДИ 0,88 - 7,79; p = 0,014) и уменьшением риска смерти на 41% [отношение рисков [hazard ratio, HR] = 0,59; 95% ДИ 0,49 - 0,71; p < 0,001) [85].
Нет подтверждения эффективности адъювантной химиотерапии билиарного рака при применении режимов GEMOX (исследование PRODIGE-12) [150] и монотерапии гемцитабином** (исследование BCAT) [151].
После нерадикальной операции (R1/R2) или метастазах в лимфатических узлах возможно выполнение ре-резекции, необходимо проведение системной химиотерапии (согласно принципам лечения метастатического процесса), а также химио-лучевой терапии (ХЛТ) с фторпиримидинами (L01BC: Аналоги пиримидина).
Настоятельно рекомендуется проводить послеоперационную лучевую терапию (ЛТ) с использованием технологий 3D-конформной ЛТ или лучевой терапии модулированной интенсивности. Облучению подвергается ложе удаленной опухоли и регионарные зоны. Лучевая терапия проводится РОД 2Гр до СОД 46Гр, а при R1/R2 - до 50 - 60 Гр на ложе удаленной опухоли. После завершения ХЛТ показана монохимиотерапия #капецитабином** (при низкой степени дифференцировки опухоли и/или метастазах в лимфатических узлах возможно применение комбинированных режимов гемцитабин**/#цисплатин**, #гемцитабин**/#капецитабин**) [93 - 94].
- При локальном рецидиве рака билиарного тракта после радикального вмешательства рекомендуется рассмотреть варианты локального лечения с целью увеличения продолжительности жизни пациентов (повторная резекция печени, методы локальной деструкции или химиоэмболизация печеночной артерии при изолированном поражении печени после операции по поводу внутрипеченочной холангиокарциномы, фотодинамическая терапия или внутрипротоковая ЛТ при рецидиве рака внепеченочных желчных протоков) [73, 74, 91, 95, 96].
Уровень убедительности рекомендаций - B (уровень достоверности доказательств - 2)
- При неоперабельной локализованной внутрипеченочной ХК (стадии IIIa-IVa, T3-4N0-1M0) у взрослых рекомендуется рассмотреть применение локо-регионарных методов лечения (локальная деструкция (МВА, криоабляция), трансартериальная химиоэмболизация (ТАХЭ), селективная внутрипеченочная артериальная химиотерапия, стереотаксическая лучевая терапия с использованием 3-5-дневного режима фракционирования дозы до СОД 30 - 50 Гр) могут применяться у отдельных пациентов при исчерпанности возможностей других основных видов лечения и не рекомендуются к рутинному применению [97 - 103].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств 4).
Комментарий: при T3-4 РЧА не показана.
- При локализованном внутрипротоковом и перидуктально-инфильтративном поражении желчных протоков (стадии IIIa - IVa, T3-4N0M0) у взрослых рекомендуется рассмотреть применение внутрипротоковой фотодинамической терапии (ФДТ) с целью улучшения оттока желчи и улучшения качества (паллиативная помощь) жизни пациентов [104, 105].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств 4).
Комментарий: ФДТ включает в себя относительно селективное накопление патологической тканью химического агента (фотосенсибилизатора (L01XD: Сенсибилизирующие препараты, используемые для фотодинамической/лучевой терапии)), с последующей активацией накопленного фотосенсибилизатора при помощи света, что запускает каскад внутриклеточных реакций, называемых фотодинамическим эффектом, приводящих к гибели опухолевых клеток; улучшает общую выживаемость пациентов с внутрипротоковой неоперабельной холангиокарциномой и раком холедоха [104, 105].
- При поздних стадиях внепеченочной холангиокарциномы (стадии IIIa - IVa, T3-4N0-1M0) у взрослых может быть рекомендована химио-лучевая терапия с целью контроля симптомов, обусловленных локальным распространением опухоли [106].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств 4).
Комментарий: перед лучевой терапией может быть рекомендовано применение #гемцитабина** в дозе 1000 мг/м2 в 1 и 8 день цикла в комбинации с капецитабином в дозе 1500 мг/м2 с 1 по 14 день, каждые 21 день 4 курса с последующим одновременным приемом капецитабина** в дозе 1330 мг/м2 в день (вместе с лучевой терапией) [183, 184]. Лучевая терапия проводится в режиме стереотаксического облучения за 3 - 5 фракций до СОД 30 - 50Гр. Одновременное использование гемцитабина с лучевой терапией не рекомендуется в связи с ограниченным опытом и высокой токсичностью лечения.
- При диссеминированном раке билиарного тракта (стадия IVb, M1) у взрослых и удовлетворительном общем состоянии пациента рекомендуется рассмотреть лечение системной химиотерапией гемцитабином** в сочетании с производными препаратов платины +/- иммунотерапия в том числе или на основе фторпиримидинов (L01BC: Аналоги пиримидина). Вариантом лечения взрослых пациентов с распространенным нерезектабельным или метастатическим раком билиарного тракта в первой линии терапии рекомендовано рассмотреть сочетание иммунотерапии и химиотерапии. Добавление дурвалумаба** к терапии комбинацией гемцитабин**+ #цисплатин** и #пембролизумаба** к терапии комбинацией гемцитабин**+ #цисплатин** достоверно увеличивает выживаемость пациентов. Дозы препаратов приведены в таблице 6 [19, 107 - 114, 122, 173].
Уровень убедительности рекомендаций - A (уровень достоверности доказательств - 2).
Комментарии: по данным двойного слепого плацебо-контролируемого исследования III фазы (n = 685 пациентов) с ранее не леченым нерезектабельным или метастатическим раком билиарного тракта добавление дурвалумаба** к терапии комбинацией гемцитабин** + #цисплатин** приводило к значимому повышению эффективности терапии. Медианы ОВ в группах дурвалумаба** и плацебо составила 12,8 (95% ДИ = 11,1 - 14,0) и 11,5 (95% ДИ = 10,1 - 12,5) месяцев соответственно, а HR для ОВ составило 0,80 (95% ДИ = 0,66 - 0,97, p = 0,021). ОВ за 24 мес. составила 24,9% (95% ДИ = 17,9 - 32,5) для пациентов, получавших дурвалумаб**, и 10,4% (95% ДИ = 4,7 - 18,8) для пациентов, получавших плацебо. Медианная ВБП в группах дурвалумаба** и плацебо составила 7,2 (95% ДИ = 6,7 - 7,4) и 5,7 (95% ДИ = 5,6 - 6,7) месяцев, а HR для ВБП составило 0,75 (95% ДИ = 0,63 - 0,89, p = 0,001). Частота объективного ответа (ЧОО) достигла 26,7% у получавших комбинацию гемцитабин** + #цисплатин** + дурвалумаб**, при этом в группе сравнения показатель составил только 18,7%. Добавление дурвалумаба** к терапии комбинацией гемцитабин** + #цисплатин** не приводило к ухудшению переносимости и безопасности лечения: частота нежелательных явлений 3 и 4 степени составила 75,7% у пациентов, получавших дурвалумаб**, и 77,8% у пациентов, получавших плацебо [122].
По данным двойного слепого плацебо-контролируемого исследования III фазы с участием 1069 пациентов с ранее не леченым нерезектабельным или метастатическим раком билиарного тракта добавление пембролизумаба** к терапии комбинацией гемцитабин** + #цисплатин** приводило достоверному повышению ОВ. Комбинация пембролизумаба** и гемцитабин** + #цисплатин** улучшила общую выживаемость (р = 0,0034). Медиана ОВ составила 12,7 в группе пембролизумаба** и 10,9 месяцев в группе плацебо соответственно. Общая 12-месячная выживаемость составила 52% против 44%, а 24-месячная выживаемость - 25% против 18% соответственно [173].
Химиотерапия при наличии дренажей и стентов в билиарном дереве часто (>50% пациентов) осложняется обострением острого холангита, холестазом и холестатическим гепатитом. С целью профилактики инфекционных осложнений (холангит) необходим активный мониторинг состоятельности дренирования, своевременная замена дренажей, профилактические промывания дренажей растворами антибактериальных препаратов. При подозрении на инфицирование - своевременная антибактериальная терапия препаратами широкого спектра действия (J01: Антибактериальные препараты системного действия), при необходимости корригируемая на основании результатов бактериального посева с определением индивидуальной чувствительности микробной флоры к антибиотикам (J01: Антибактериальные препараты системного действия). Длительность лечения определяется переносимостью, влиянием на качество жизни пациента, непосредственной эффективностью, нет доказательств дополнительной пользы лечения длительностью более 6 мес. #Оксалиплатин** в дозе 100 мг/м2 в/в во 1-й день, интервал - 3 недели может заменить #цисплатин** в сочетании с гемцитабином** 1000 мг/м2 при нарушенной функции почек, высокой токсичности цисплатина**, других противопоказаниях к цисплатину** [154]. Химиотерапия гемцитабин** + #цисплатин** возможна при умеренно повышенном уровне билирубина вследствие внутрипеченочного холестаза при адекватном оттоке желчи [155].
- У пациентов старше 18 лет с первично неоперабельным местнораспространенным раком билиарного тракта при эффективной локо-регионарной и/или системной химиотерапии и уменьшении локальной распространенности опухоли до достижения критериев резектабельности за счет уменьшения размера опухоли целесообразно повторное обсуждение междисциплинарной командой возможности радикального хирургического лечения [115, 119, 120, 156].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств 4).
- Рекомендовано проведение химиотерапии второй линии диссеминированного рака билиарного тракта, при удовлетворительном состоянии пациента старше 18 лет с использованием режима лечения, учитывающего эффективность 1-й линии, с целью контроля симптомов заболевания и увеличения продолжительности жизни [10, 19, 43].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств 5).
Комментарии: Исследование ABC-06 подтвердило умеренное увеличение ОВ химиотерапии (FOLFOX) в сравнении с тактикой активной симптоматической терапии (ОР 0.69).
Лечение во второй линии с использованием фторурацила** и #иринотекана** (FOLFIRI) также принесло некоторую пользу пациентам. Рандомизированное исследование II фазы, сравнивающее mFOLFOX и mFOLFIRI у пациентов с местно-распространенным или метастатическим билиарным раком, ранее получавшими лечение гемцитабин** + #цисплатин** продемонстрировали одинаковую эффективность между двумя схемами [174]. Медиана ОВ и ВБП составила 6,3 месяца (95% ДИ = 4,4 - 8,2)) и 2,8 мес (95% ДИ = 2,3 - 3,3 мес) соответственно в группе mFOLFOX и 5,7 месяцев (95% ДИ = 4,7 - 6,7, р = 0,677) и 2,1 месяцев (95% ДИ = 1,1 - 3,1 месяца, р = 0,974) в группе mFOLIFIRI, соответственно. ЧОО 5,9% и 4,0% (р = 0,663) был достигнут в группах mFOLFOX и mFOLFIRI, соответственно, и частота контроля заболевания составила 66,7% и 64,0% (р = 0,778) соответственно.
Молекулярно-направленная терапия нерезектабельного билиарного рака может быть рекомендована при выявлении таргетируемых молекулярных альтераций в опухоли для лечения рефрактерного к стандартной химиотерапии распространенного опухолевого процесса, объективном статусе пациента ECOG не хуже 2 и компенсированной функции печени. Молекулярные альтерации HER2/neu (ERBB2 - гиперэкспрессия/амплификация), мутации BRAFV600E, микросателлитная нестабильность MSI-H/dMMR, мутационная нагрузка (TMB) транслокации гена FGFR2, генов ALK, NTRK, RET определяются доступным валидированным тестом [10, 19, 17]. (таблица 6)
Таблица 6 Режимы лекарственного лечения рака билиарного тракта у взрослых
Монохимио-терапия
- Гемцитабин** 1000 мг/м2 в 1-й, 8-й, 15-й дни. Интервал - 4 недели [10, 19, 109].
- #Капецитабин** по 1250 мг/м2 x 2 раза в день внутрь в 1 - 14-и дни каждые 21 день [187]
- #Иринотекан 240 мг/м2 в 1-й день. Интервал - 3 недели [182].
Полихимио-терапия
- Гемцитабин** 1000 мг/м2 в 1-й и 8-й дни.
#Цисплатин**25 мг/м2 в 1-й и 8-й дни, интервал - 3 недели) [109]
- #Гемцитабин** 1000 мг/м2 в 1-й и 8-й дни.
#Оксалиплатин** 100 мг/м2 в/в во 1-й день, интервал - 3 недели. [10, 19, 116].
- FOLFOX6 (#Оксалиплатин** 85 мг/м2 2-часовая инфузия в 1-й день, #кальция фолинат** по 400 мг/м2 в/в 2-часовая инфузия в 1-й день, #фторурацил** 400 мг/м2 в/в струйно в 1-й день, и 46-часовая инфузия #Фторурацил** 2400 мг/м2 (1200 мг/м2 в сутки). Интервал - 2 недели [89, 117].
- FOLFIRI (#Иринотекан** 180 мг/м2 90-минутная инфузия в 1-й день, #кальция фолинат** по 400 мг/м2 в/в 2-часовая инфузия в 1-й день, #фторурацил** 400 мг/м2 в/в струйно в 1-й день, и 46-часовая инфузия #Фторурацил** 2400 мг/м2 (1200 мг/м2 в сутки). Интервал - 2 недели [174]
- XELOX (#Оксалиплатин** 130 мг/м2 в 1-й день, #капецитабин** 1000 мг/м2 2 раза в сутки 1-й - 14-й дни). Интервал - 3 недели. [154].
- XELIRI (#Иринотекан** 200 мг/м2 в 1-й день, #капецитабин** 1700 мг/м2 в сутки в 2 приема 1-й - 14-й дни). Интервал - 3 недели. [182].
- GEMCAP (#Гемцитабин** 1000 мг/м2 в 1-й, 8-й дни + #капецитабин** 1250 мг/м2/сутки в 2 приема 1-й - 14-й дни. Интервал - 3 недели [89, 118].
Иммуно-химиотерапия
- Гемцитабин** 1000 мг/м2 в/в в 1 и 8 дни + #цисплатин** 25 мг/м2 в 1 и 8 дни + дурвалумаб 1500 мг в 1 день каждые 21 день до 8 циклов терапии, далее дурвалумаб 1500 мг в/в каждые 4 недели до прогрессирования или неприемлемой токсичности [122]
- Гемцитабин*** 1000 мг/м2 в/в в 1-й и 8-й дни без ограничения продолжительности применения + #цисплатин** 25 мг/м2 в/в в 1-й и 8-й дни, максимум 8 циклов + #пембролизумаб** 200 мг в/в в 1-й день каждые 3 недели, максимум 35 циклов [173]
Иммуно-терапия
Пембролизумаб** (только для MSI-H опухолей)
Пембролизумаб** 200 мг в/в капельно (30-минутная инфузия) 1 раз в 3 недели длительно (до двух лет) или по 400 мг в/в капельно каждые 42 дня [159]
#Трастузумаб** + #пертузумаб**
(при "диком" типе гена RAS и гиперэкспрессии или амплификации
HER2/neu)
#Трастузумаб** 8 мг/кг в/в - нагрузочная доза в 1 день первого цикла, затем 6 мг/кг в/в - каждые 21 день,
#Пертузумаб** - 840 мг в/в нагрузочная доза в 1 день первого цикла, затем 420 мг в/в - каждые 21 день [157]
Уровень убедительности рекомендаций - C (уровень достоверности доказательств 5).
Комментарий: применение молекулярно-направленной терапии в настоящее время не носит обязательного характера, но может быть рекомендовано в клинической практике при выявлении в опухоли соответствующих молекулярно-генетических альтераций по исчерпании стандартных терапевтических опций по решению консилиума.
- Амплификация/гиперэкспрессия HER2/neu (ERBB2) при билиарном (5% - 10% внутрипеченочных ХК и до 20% при раке желчного пузыря) раке - возможная мишень молекулярно-направленной анти-HER2 терапии: по данным корзинного исследования MyPathway комбинация #"пертузумаб** + трастузумаб**" позволяла достичь 23% объективных эффектов и медианой ВБП до 4 мес и медианой общей выживаемости до 10,9 мес [157]. Доза препарата указана в таблице 6. При ко-мутации BRAF/RAS отмечено значимое снижение эффективности лечения.
- Мутация BRAF выявляется < 5% случаев ХК. В исследовании ROAR комбинация #дабрафениба** (BRAF ингибитор (L01EC: Ингибиторы серин-треонинкиназы B-Raf (BRAF)) и #траметиниба** (MEK ингибитор (L01EE: Ингибиторы митоген-активированной протеинкиназы (MEK)) позволяла достичь объективный эффект у 51% пациентов при медиане ВБП 9 мес и ОВ 14 мес у ранее предлеченых больных с мутацией BRAFV600E, что предполагает высокую вероятность достижения клинической пользы в отсутствие других опций [158]. В исследовании TAPUR комбинация #вемурафениба** (BRAF ингибитор (L01EC: Ингибиторы серин-треонинкиназы B-Raf (BRAF)) и #кобиметиниба** (MEK ингибитор (L01EE: Ингибиторы митоген-активированной протеинкиназы (MEK)) позволяла достичь объективный эффект у 57% пациентов при медиане ВБП 5,8 мес и ОВ 15,2 мес у ранее предлеченых больных с мутацией BRAFV600E, что предполагает высокую вероятность достижения клинической пользы в отсутствие других опций [176]. Дозы препаратов указаны в таблице 6.
- Частота встречаемости дефицита неспаренных оснований (dMMR) при билиарном раке <1%. В случае выявления микросателлитной нестабильности - MSI-high (MSI-H) можно рассчитывать на возможную клиническую пользу иммунотерапии. В проспективном нерандомизированном исследовании II фазы KEYNOTE-158 trial, у 40.9% (из 22 пациентов) отмечен объективный эффект при медиане ВБП 4.2 мес и медианой ОВ 24.3 мес [159].
- #Селперкатиниб, селективный ингибитор киназы RET, исследовался в рамках клинического исследования LIBRETTO-001 фазы 1/2 у пациентов с транслокацией гена RET. Из 41 пациента, кроме рака легкого и щитовидной железы, ЧОО составило 43,9% (95% ДИ = 28,5 - 60,3%). Объективный ответ был получен у одного пациента с холангиокарциномой [179]. Доза препарата указана в таблице 6.
- Ингибиторы FGFR1-4 типа (L01: Противоопухолевые препараты) (#эрдафитиниб) высоко эффективны при выявлении проканцерогенных транслокаций генов FGFR1-4. Эффективность #эрдафитиниба продемонстрирована в исследовании II фазы RAGNAR. ЧОО составила 60%, при этом среднее время до начала противоопухолевого ответа составило 1,5 месяца. Медиана ВБП и ОВ составила 8,4 мес (95% ДИ = 5,5 - 9,7) и 18,7 мес (95% ДИ = 8,9 - не поддается оценке) соответственно. Наиболее частыми нежелательными явлениями, возникшими во время лечения, были гиперфосфатемия (82,9%), диарея (80,0%) и стоматит (74,3%) [185]. Доза препарата указана в таблице 6.
- Соответствующая таргетная терапия может также назначаться при других описанных редких молекулярных альтерациях (высокая TMB, IDH1/2, NTRK, ALK, MET и др.) или резистентности к ранее проведенной молекулярно-направленной терапии по решению врачебной комиссии пациентам в удовлетворительном объективном состоянии.
- При диссеминированном раке билиарного тракта (стадия IVb, M1) и ослабленном общем состоянии пациента (ECOG 2 - см. Приложение Г) с паллиативной целью рекомендуется монохимиотерапия гемцитабином** или #капецитабином**с учетом возможного профиля токсичности [10,19, 172]. Дозы препаратов указаны в таблице 6.
Уровень убедительности рекомендаций - C (уровень достоверности доказательств 5)
- При неудовлетворительном общем состоянии пациента (ECOG > 2), выраженной сопутствующей патологии рекомендуется проведение симптоматической терапии; не рекомендуется проведение химиотерапии [10, 18, 19].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств 4).
Комментарий: целью "наилучшей поддерживающей терапии" является профилактика и облегчение симптомов заболевания и поддержание качества жизни пациентов, независимо от стадии заболевания и потребности в других видах терапии. Проведение паллиативной химиотерапии пациентам со статусом по ECOG 3 - 4 (HR = 2,01, p = 0,016), гиперкалиемией (HR = 2,19, p = 0,005) и повышенным уровнем билирубина (HR = 3,17, p < 0,001) ассоциировано с повышенным риском смертности в течение 30 дней [18] и не рекомендуется.
3.4 Лучевая терапия
Лучевая терапия рекомендуется пациентам:
- в адъювантном режиме при внепеченочной холангиокарциноме [130 - 132] в сочетании с фторпиримидинами (L01BC: Аналоги пиримидина). Облучению подвергается ложе удаленной опухоли и регионарные зоны РД 2 Гр до СД 46 Г, при R1/R2 с последовательным "бустом" до 50 - 60 Гр на ложе удаленной опухоли. [90].
- Стереотаксическая дистанционная лучевая терапия при неоперабельном внутрипеченочном или хилярном расположении опухоли в случае отсутствия иных методов лечения с использованием 3 - 5-дневного режима фракционирования дозы до СД 30 - 50 Гр [165].
Уровень убедительности рекомендаций - B (уровень достоверности доказательств - 3)
Комментарий: по данным метаанализа проведение адъювантной ЛТ после радикальной резекции у пациентов с внепеченочной холангиокарциномой было ассоциировано с увеличением ОВ (HR = 0,62, 95% ДИ = 0,48 - 0,78, p < 0,001) [130]. У пациентов с внепеченочной холангиокарциномой или РЖП, получавших адъювантную ЛТ, пятилетняя ОВ была выше, чем у пациентов не получавших адъювантную ЛТ (OR = 0,63, 95% ДИ 0,50 - 0,81, p = 0,0002). Адъювантная ЛТ также увеличивала пятилетнюю ОВ у пациентов с распространением опухолевого процесса в лимфатические узлы (OR = 0,15, 95% ДИ 0,07 - 0,35, p < 0,00001) и у пациентов с наличием опухолевых клеток по краю резекции (OR = 0,40, 95% ДИ 0,19 - 0,85, p = 0,02) [131].
Данные об объемах и дозах ЛТ основаны на рандомизированном исследовании II фазы, в котором лучевая терапия пациентам применялась как с использованием технологии 3D-конформной лучевой терапии, так и технологии IMRT, однако отличался режим формирования последовательного "буста": при использовании 3D-конформной лучевой терапии после облучения лимфоколлектора и ложа удаленной опухоли проводился "буст" до 54 Гр и 59,4 Гр в случае R1-резекции, в случае использования технологии IMRT - до 52,5 Гр и 55 Гр в случае R1-резекции [90.]
Комментарий: в случае отсутствия возможности применения указанных выше методик и/или опыта проведения ЛТ билиарного тракта, пациент направляется в центры более высокого экспертного уровня.
Уровень убедительности рекомендаций - B (уровень достоверности доказательств - 4)
4. Медицинская реабилитация и санаторно-курортное лечение, медицинские показания и противопоказания к применению методов медицинской реабилитации, в том числе основанных на использовании природных лечебных факторов
- Рекомендуется проводить реабилитацию, ориентируясь на общие принципы реабилитации пациентов после проведенных хирургических вмешательств и/или химиотерапии [133].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 5)
5. Профилактика и диспансерное наблюдение, медицинские показания и противопоказания к применению методов профилактики
- После завершения лечения по поводу холангиокарциномы или после окончания хирургического лечения рекомендуется соблюдать следующую периодичность и методы наблюдения:
- обследование в первые 2 года рекомендуется проводить каждые 3 - 6 месяцев, далее - ежегодно до 5 лет в следующем объеме:
- осмотр у врача-онколога и физикальное обследование;
- онкомаркеры РЭА, СА-19.9, АФП (если были повышены исходно);
- УЗИ органов брюшной полости (комплексное);
- КТ или МРТ органов брюшной полости с внутривенным контрастированием;
- РКТ органов грудной клетки;
- холангиография (при наличии дренажей) [10, 19, 28, 134 - 136].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 4)
Комментарии: задачей наблюдения является раннее выявление прогрессирования заболевания после завершения лечения с целью раннего начала химиотерапии или хирургического лечения резектабельных метастатических очагов, рецидивных опухолей.
6. Организация оказания медицинской помощи
Медицинская помощь, за исключением медицинской помощи в рамках клинической апробации, в соответствии с Федеральным законом от 21.11.2011 N 323-ФЗ "Об основах охраны здоровья граждан в Российской Федерации", организуется и оказывается:
1) в соответствии с положением об организации оказания медицинской помощи по видам медицинской помощи, которое утверждается уполномоченным Федеральным органом исполнительной власти;
2) в соответствии с порядками оказания медицинской помощи, утверждаемыми уполномоченным федеральным органом исполнительной власти и обязательными для исполнения на территории Российской Федерации всеми медицинскими организациями
3) на основе настоящих клинических рекомендаций;
4) с учетом стандартов медицинской помощи, утвержденных уполномоченным Федеральным органом исполнительной власти.
Первичная специализированная медико-санитарная помощь оказывается врачом-онкологом и иными врачами-специалистами в центре амбулаторной онкологической помощи, а при его отсутствии в первичном онкологическом кабинете, поликлиническом отделении онкологического диспансера (онкологической больницы).
При подозрении или выявлении у пациента онкологического заболевания врачи-терапевты, врачи-терапевты участковые, врачи общей практики (семейные врачи), врачи-специалисты, средние медицинские работники в установленном порядке направляют пациента на консультацию в центр амбулаторной онкологической помощи, а при отсутствии в первичный онкологический кабинет, поликлиническое отделение онкологического диспансера (онкологической больницы) для оказания ему первичной специализированной медико-санитарной помощи.
Консультация в центре амбулаторной онкологической помощи либо в первичном онкологическом кабинете, поликлиническом отделении онкологического диспансера (онкологической больницы) должна быть проведена не позднее 3 рабочих дней с даты выдачи направления на консультацию. Врач-онколог центра амбулаторной онкологической помощи (в случае отсутствия центра амбулаторной онкологической помощи врач-онколог первичного онкологического кабинета или поликлинического отделения онкологического диспансера (онкологической больницы организует взятие биопсийного (операционного) материала, а также организует выполнение иных диагностических исследований, необходимых для установления диагноза, включая распространенность онкологического процесса и стадию заболевания.
В случае невозможности взятия в медицинской организации, в составе которой организован центр амбулаторной онкологической помощи (первичный онкологический кабинет) биопсийного (операционного) материала, проведения иных диагностических исследований пациент направляется врачом-онкологом в онкологический диспансер (онкологическую больницу) или в медицинскую организацию, оказывающую медицинскую помощь пациентам с онкологическими заболеваниями.
Срок выполнения патологоанатомических исследований, необходимых для гистологической верификации злокачественных новообразований не должен превышать 15 рабочих дней с даты поступления биопсийного (операционного) материала в патологоанатомическое бюро (отделение).
Сроки проведения диагностических инструментальных и лабораторных исследований в случае подозрения на онкологическое заболевание не должны превышать сроков, установленных в программе государственных гарантий бесплатного оказания гражданам медицинской помощи, утверждаемой Правительством Российской Федерации, 7 рабочих дней со дня назначения исследований.
Диагноз онкологического заболевания устанавливается врачом-специалистом на основе результатов диагностических исследований, включающих в том числе проведение цитологической и (или) гистологической верификации диагноза, за исключением случаев, когда взятие биопсийного и (или) пункционного материала не представляется возможным.
Врач-онколог центра амбулаторной онкологической помощи (первичного онкологического кабинета) направляет пациента в онкологический диспансер (онкологическую больницу) или иную медицинскую организацию, оказывающую медицинскую помощь пациентам с онкологическими заболеваниями, в том числе подведомственную федеральному органу исполнительной власти (далее - федеральная медицинская организация), для уточнения диагноза (в случае невозможности установления диагноза, включая распространенность онкологического процесса и стадию заболевания), определения тактики лечения, а также в случае наличия медицинских показаний для оказания специализированной, в том числе высокотехнологичной, медицинской помощи.
При онкологических заболеваниях, входящих в рубрики C37, C38, C40 - C41, C45 - C49, C58, D39, C62, C69 - C70, C72, C74 МКБ-10, а также соответствующих кодам международной классификации болезней - онкология (МКБ-О), 3 издания 8936, 906 - 909, 8247/3, 8013/3, 8240/3, 8244/3, 8246/3, 8249/3 врач-онколог онкологического диспансера (онкологической больницы) или иной медицинской организации, оказывающей медицинскую помощь пациентам с онкологическими заболеваниями, для определения лечебной тактики организует проведение консультации или консилиума врачей, в том числе с применением телемедицинских технологий, в федеральных государственных бюджетных учреждениях, подведомственных Министерству здравоохранения Российской Федерации, оказывающих медицинскую помощь (далее в целях настоящего Порядка - национальные медицинские исследовательские центры).
В сложных клинических случаях для уточнения диагноза (в случае невозможности установления диагноза, включая распространенность онкологического процесса и стадию заболевания) в целях проведения оценки, интерпретации и описания результатов врач-онколог организует направление:
- цифровых изображений, полученных по результатам патоморфологических исследований, в патолого-анатомическое бюро (отделение) четвертой группы (референс-центр) путем информационного взаимодействия, в том числе с применением телемедицинских технологий при дистанционном взаимодействии медицинских работников между собой;
- цифровых изображений, полученных по результатам лучевых методов исследований, в дистанционный консультативный центр лучевой диагностики, путем информационного взаимодействия, в том числе с применением телемедицинских технологий при дистанционном взаимодействии медицинских работников между собой;
- биопсийного (операционного) материала для повторного проведения патоморфологических, иммуногистохимических, и молекулярно-генетических исследований: в патолого-анатомическое бюро (отделение) четвертой группы (референс-центр), а также в молекулярно-генетические лаборатории для проведения молекулярно-генетических исследований.
Тактика лечения устанавливается консилиумом врачей, включающим врачей-онкологов, врача-радиотерапевта, врача-нейрохирурга (при опухолях нервной системы) медицинской организации, в составе которой имеются отделения хирургических методов лечения злокачественных новообразований, противоопухолевой лекарственной терапии, радиотерапии (далее - онкологический консилиум), в том числе онкологическим консилиумом, проведенным с применением телемедицинских технологий, с привлечением при необходимости других врачей-специалистов.
Диспансерное наблюдение врача-онколога за пациентом с выявленным онкологическим заболеванием устанавливается и осуществляется в соответствии с порядком диспансерного наблюдения за взрослыми с онкологическими заболеваниями.
С целью учета информация о впервые выявленном случае онкологического заболевания направляется в течение 3 рабочих дней врачом-онкологом медицинской организации, в которой установлен соответствующий диагноз, в онкологический диспансер или организацию субъекта Российской Федерации, исполняющую функцию регистрации пациентов с впервые выявленном злокачественным новообразованием, в том числе с применением единой государственной информационной системы в сфере здравоохранения. В случае подтверждения у пациента наличия онкологического заболевания информация об уточненном диагнозе направляется из онкологического диспансера или организации субъекта Российской Федерации, исполняющей функции регистрации пациентов с впервые выявленном злокачественным новообразованием, в медицинскую организацию, осуществляющую диспансерное наблюдение пациента
Специализированная, в том числе высокотехнологичная, медицинская помощь в медицинских организациях, оказывающих медицинскую помощь взрослому населению при онкологических заболеваниях, оказывается по медицинским показаниям, предусмотренным положением об организации оказания специализированной, в том числе высокотехнологичной, медицинской помощи.
Специализированная, за исключением высокотехнологичной, медицинская помощь в медицинских организациях, подведомственных федеральным органам исполнительной власти, оказывается по медицинским показаниям, предусмотренным пунктом 5 порядка направления пациентов в медицинские организации и иные организации, подведомственные федеральным органам исполнительной власти, для оказания специализированной (за исключением высокотехнологичной) медицинской помощи, предусмотренного в приложении к положению об организации оказания специализированной, в том числе высокотехнологичной, медицинской помощи. (Пункт 5: для получения специализированной медицинской помощи в плановой форме выбор федеральной медицинской организации осуществляется по направлению лечащего врача.) В случае если в реализации Программы принимают участие несколько федеральных медицинских организаций, оказывающих специализированную медицинскую помощь при заболеваниях, состояниях (группе заболеваний, состояний), соответствующих заболеваниям, состояниям (группе заболеваний, состояний) пациента, лечащий врач обязан проинформировать пациента (законного представителя пациента) о возможности выбора федеральной медицинской организации, в том числе о возможных сроках ожидания специализированной медицинской помощи, которые могут превышать сроки ожидания, установленные программой государственных гарантий бесплатного оказания гражданам медицинской помощи.
Сроки ожидания оказания специализированной (за исключением высокотехнологичной) медицинской помощи не должны превышать сроков, установленных в программе государственных гарантий бесплатного оказания гражданам медицинской помощи, утверждаемой Правительством Российской Федерации, 7 рабочих дней.
При наличии у пациента с онкологическим заболеванием медицинских показаний для проведения медицинской реабилитации врач-онколог организует ее проведение в соответствии с порядком организации медицинской реабилитации взрослых.
При наличии у пациента с онкологическим заболеванием медицинских показаний к санаторно-курортному лечению врач-онколог организует его в соответствии порядком организации санаторно-курортного лечения.
Паллиативная медицинская помощь пациенту с онкологическими заболеваниями оказывается в соответствии с положением об организации оказания паллиативной медицинской помощи, включая порядок взаимодействия медицинских организаций, организаций социального обслуживания и общественных объединений, иных некоммерческих организаций, осуществляющих свою деятельность в сфере охраны здоровья.
При подозрении и (или) выявлении у пациента онкологического заболевания в ходе оказания ему скорой медицинской помощи его переводят или направляют в медицинские организации, оказывающие медицинскую помощь пациентам с онкологическими заболеваниями, для определения тактики ведения и необходимости применения дополнительно других методов специализированного противоопухолевого лечения.
Показаниями для госпитализации в медицинскую организацию в экстренной или неотложной форме являются:
1) наличие осложнений онкологического заболевания, требующих оказания ему специализированной медицинской помощи в экстренной и неотложной форме;
2) наличие осложнений лечения онкологического заболевания (хирургическое вмешательство, ЛТ, лекарственная терапия и т.д.), требующих оказания ему специализированной медицинской помощи в экстренной и неотложной форме
Показаниями для госпитализации в медицинскую организацию в плановой форме являются:
1) необходимость выполнения сложных интервенционных диагностических медицинских вмешательств, а также проведение эндоскопических исследований при невозможности выполнить их амбулаторно, требуют последующего наблюдения в условиях круглосуточного или дневного стационара;
2) наличие показаний к специализированному противоопухолевому лечению (хирургическое вмешательство, ЛТ, в том числе контактная, ДЛТ и другие виды ЛТ, лекарственная терапия и др.), требующему наблюдения в условиях круглосуточного или дневного стационара.
Показаниями к выписке пациента из медицинской организации являются:
1) завершение курса лечения или одного из этапов оказания специализированной, в том числе высокотехнологичной, медицинской помощи в условиях круглосуточного или дневного стационара при условии отсутствия осложнений лечения, требующих медикаментозной коррекции и/или медицинских вмешательств в стационарных условиях;
2) отказ пациента или его законного представителя от специализированной, в том числе высокотехнологичной, медицинской помощи в условиях круглосуточного или дневного стационара, установленной консилиумом медицинской организации, оказывающей онкологическую помощь
3) в случаях несоблюдения пациентом предписаний или правил внутреннего распорядка лечебно-профилактического учреждения, если это не угрожает жизни пациента и здоровью окружающих;
4) необходимость перевода пациента в другую медицинскую организацию по соответствующему профилю оказания медицинской помощи.
Заключение о целесообразности перевода пациента в профильную медицинскую организацию осуществляется после предварительной консультации по предоставленным медицинским документам и/или предварительного осмотра пациента врачами-специалистами медицинской организации, в которую планируется перевод.
7. Дополнительная информация (в том числе факторы, влияющие на исход заболевания или состояния)
Отсутствует.
Критерии оценки качества медицинской помощи
N
Критерии качества
Оценка выполнения
1
Выполнен осмотр пациента врачом-онкологом
ДА/Нет
2
Выполнено патолого-анатомическое исследование биопсийного (операционного) материала до начала лечения, за исключением случаев хирургического лечения
ДА/Нет
3
Выполнена компьютерная томография органов грудной полости
ДА/Нет
4
Выполнены общий (клинический) анализ крови развернутый, анализ крови биохимический общетерапевтический
ДА/Нет
5
Выполнено ультразвуковое исследование брюшной полости (комплексное) с последующей контрастной компьютерной томографией или магнитно-резонансной томографией органов брюшной полости с внутривенным контрастированием с магнитно-резонансной холангиографией органов брюшной полости и забрюшинного пространства
ДА/Нет
6
Выполнено патологоанатомическое исследование операционного материала опухоли печени (в том числе, с применением иммуногистохимических методов)
ДА/Нет
8
Выполнена предоперационная декомпрессия желчевыводящих путей (чрескожная чреспеченочная холангиостомия, назобилиарное дренирование, стентирование) при механической желтухе
ДА/Нет
Примечание: * - при выявлении при УЗИ опухолевой патологии билиарного тракта рекомендуется выполнить компьютерную томографию (КТ) органов брюшной полости с внутривенным контрастированием и/или магнитно-резонансную томографию (МРТ) органов брюшной полости с внутривенным контрастированием с магнитно-резонансной холангиографией.
Список литературы
1. Sheth S., Bedford A., Chopra S. Primary gallbladder cancer: recognition of risk factors and the role of prophylactic cholecystectomy // The American Journal of Gastroenterology. 2000. Vol. 95, N 6. P. 1402 - 1410.
2. Hueman M.T., Vollmer C.M., Pawlik T.M. Evolving Treatment Strategies for Gallbladder Cancer // Ann Surg Oncol. 2009. Vol. 16, N 8. P. 2101 - 2115.
3. Hundal R., Shaffer E.A. Gallbladder cancer: epidemiology and outcome // Clin Epidemiol. 2014. Vol. 6. P. 99 - 109.
4. Patel T. Cholangiocarcinoma-controversies and challenges: 4 // Nat Rev Gastroenterol Hepatol. Nature Publishing Group, 2011. Vol. 8, N 4. P. 189 - 200.
5. Yamamoto S. et al. Hepatitis C virus infection as a likely etiology of intrahepatic cholangiocarcinoma // Cancer Science. 2004. Vol. 95, N 7. P. 592 - 595.
6. Welzel T.M. et al. Risk factors for intrahepatic and extrahepatic cholangiocarcinoma in the United States: a population-based case-control study // Clinical Gastroenterology and Hepatology. 2007. Vol. 5, N 10. P. 1221 - 1228.
7. Каприн А.Д., Старинский В.В., Шахзадова А.О. Злокачественные новообразования в России в 2020 году (заболеваемость и смертность). Москва: МНИОИ им. П.А. Герцена - филиал ФГБУ "НМИЦ радиологии" Минздрава России, 2021. 252 p.
8. Zhu A.X. et al. Current management of gallbladder carcinoma // The oncologist. Oxford University Press, 2010. Vol. 15, N 2. P. 168 - 181.
9. DeOliveira M.L. et al. Cholangiocarcinoma: thirty-one-year experience with 564 patients at a single institution. // Ann Surg. 2007. Vol. 245, N 5. P. 755 - 762.
10. Biliary tract cancer: ESMO Clinical Practice Guideline for diagnosis, treatment and follow-up. A. Vogel, J. Bridgewater, J. Edeline, J.W. Valle, M. Ducreux, on behalf of the ESMO Guidelines Committee // Annals of Oncology. VOl 34, issue 2, P 127 - 140, FEBR 2023. DOI:https://doi.org/10.1016/j.annonc.2022.10.506
11. Hawkins W.G. et al. Jaundice predicts advanced disease and early mortality in patients with gallbladder cancer // Annals of surgical oncology. Springer, 2004. Vol. 11, N 3. P. 310 - 315.
12. Jarnagin W.R. et al. Patterns of initial disease recurrence after resection of gallbladder carcinoma and hilar cholangiocarcinoma: implications for adjuvant therapeutic strategies // Cancer: Interdisciplinary International Journal of the American Cancer Society. Wiley Online Library, 2003. Vol. 98, N 8. P. 1689 - 1700.
13. Oh S.E., Park J.S., Jeung H.-C. Pre-treatment Nutritional Risk Assessment by NRS-2002 Predicts Prognosis in Patients With Advanced Biliary Tract Cancer: A Single Center Retrospective Study // Clinical Nutrition Research. 2022. Vol. 11, N 3. P. 183 - 193.
14. Ramaswamy A. et al. Second-Line Palliative Chemotherapy in Advanced Gall Bladder Cancer, CAP-IRI: Safe and Effective Option // Journal of Gastrointestinal Cancer. 2016. Vol. 47.
15. Bridgewater J. et al. Prognostic factors for progression-free and overall survival in advanced biliary tract cancer // Annals of Oncology. 2016. Vol. 27, N 1. P. 134 - 140.
16. Peixoto R.D., Renouf D., Lim H. A population based analysis of prognostic factors in advanced biliary tract cancer // J Gastrointest Oncol. 2014. Vol. 5, N 6. P. 428 - 432.
17. Horgan A. et al. Patterns of care and treatment outcomes in older patients with biliary tract cancer // Oncotarget. 2015. Vol. 6, N 42. P. 44995 - 45004.
18. Fiorin de Vasconcellos V. et al. Inpatient palliative chemotherapy is associated with high mortality and aggressive end-of-life care in patients with advanced solid tumors and poor performance status // BMC Palliative Care. 2019. Vol. 18, N 1. P. 42.
19. NCCN Clinical Practice Guidelines in Oncology ( ) Biliary Tract Cancers Version 3.2024. https://www.nccn.org/professionals/physician_gls/pdf/btc.pdf.
) Biliary Tract Cancers Version 3.2024. https://www.nccn.org/professionals/physician_gls/pdf/btc.pdf.
20. Schweitzer N. et al. Second-line chemotherapy in biliary tract cancer: Outcome and prognostic factors // Liver International. 2019. Vol. 39, N 5. P. 914 - 923.
21. Ikai I. et al. Reevaluation of prognostic factors for survival after liver resection in patients with hepatocellular carcinoma in a Japanese nationwide survey // Cancer. 2004. Vol. 101, N 4. P. 796 - 802.
22. Park H.S. et al. Prognostic Factors and Scoring Model for Survival in Metastatic Biliary Tract Cancer // Cancer Res Treat. Korean Cancer Association, 2017. Vol. 49, N 4. P. 1127 - 1139.
23. Seo J.W. et al. Prognostic impact of hepatitis B or C on intrahepatic cholangiocarcinoma // Korean J Intern Med. 2020. Vol. 35, N 3. P. 566 - 573.
24. Liu D. et al. The prognostic value of neutrophil-to-lymphocyte ratio in cholangiocarcinoma: a systematic review and meta-analysis: 1 // Sci Rep. Nature Publishing Group, 2022. Vol. 12, N 1. P. 12691.
25. Zhang Y. et al. A meta-analysis of the utility of transabdominal ultrasound for evaluation of gastric cancer // Medicine (Baltimore). 2021. Vol. 100, N 32. P. e26928.
26. Shi W. et al. Contrast-enhanced ultrasonography used for post-treatment responses evaluation of radiofrequency ablations for hepatocellular carcinoma: a meta-analysis // Br J Radiol. 2016. Vol. 89, N 1064. P. 20150973.
27. Pan K.-H. et al. Diagnostic Performance of Contrast-Enhanced Ultrasound in Renal Cancer: A Meta-Analysis // Front Oncol. 2020. Vol. 10. P. 586949.
28. Sungkasubun P. et al. Ultrasound screening for cholangiocarcinoma could detect premalignant lesions and early-stage diseases with survival benefits: a population-based prospective study of 4,225 subjects in an endemic area // BMC Cancer. 2016. Vol. 16. P. 346.
29. Ruys A.T. et al. Radiological staging in patients with hilar cholangiocarcinoma: a systematic review and meta-analysis // Br J Radiol. 2012. Vol. 85, N 1017. P. 1255 - 1262.
30. Lee H.Y. et al. Preoperative assessment of resectability of hepatic hilar cholangiocarcinoma: combined CT and cholangiography with revised criteria // Radiology. 2006. Vol. 239, N 1. P. 113 - 121.
31. Levy A.D., Murakata L.A., Rohrmann C.A. Gallbladder Carcinoma: Radiologic-Pathologic Correlation // RadioGraphics. Radiological Society of North America, 2001. Vol. 21, N 2. P. 295 - 314.
32. Zhai N. et al. Pulmonary metastasis of distal cholangiocarcinoma with multiple cavities in bilateral lungs: A case report // Thorac Cancer. 2020. Vol. 11, N 10. P. 2998 - 3000.
33. Fujino R. et al. Lung metastases from intraductal papillary neoplasm of the bile duct: a case report // World J Surg Oncol. 2020. Vol. 18. P. 271.
34. Sackmann M., Beuers U., Helmberger T. Biliary imaging: magnetic resonance cholangiography versus endoscopic retrograde cholangiography // Journal of Hepatology. Elsevier, 1999. Vol. 30, N 2. P. 334 - 338.
35. Hyodo T. et al. CT and MR cholangiography: advantages and pitfalls in perioperative evaluation of biliary tree // BJR. The British Institute of Radiology, 2012. Vol. 85, N 1015. P. 887 - 896.
36. Lamarca A. et al. 18F-fluorodeoxyglucose positron emission tomography (18FDG-PET) for patients with biliary tract cancer: Systematic review and meta-analysis // J Hepatol. 2019. Vol. 71, N 1. P. 115 - 129.
37. Petrowsky H. et al. Impact of integrated positron emission tomography and computed tomography on staging and management of gallbladder cancer and cholangiocarcinoma // Journal of hepatology. Elsevier, 2006. Vol. 45, N 1. P. 43 - 50.
38. Coelen R.J.S. et al. Diagnostic accuracy of staging laparoscopy for detecting metastasized or locally advanced perihilar cholangiocarcinoma: a systematic review and meta-analysis // Surg Endosc. 2016. Vol. 30, N 10. P. 4163 - 4173.
39. Khan Z.S., Livingston E.H., Huerta S. Reassessing the need for prophylactic surgery in patients with porcelain gallbladder: case series and systematic review of the literature // Archives of Surgery. American Medical Association, 2011. Vol. 146, N 10. P. 1143 - 1147.
40. Eckel F., Brunner T., Jelic S. Biliary cancer: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up // Annals of Oncology. Elsevier, 2011. Vol. 22. P. vi40 - vi44.
41. Sohal D.P.S. et al. Molecular characteristics of biliary tract cancer // Critical Reviews in Oncology/Hematology. 2016. Vol. 107. P. 111 - 118.
42. Zhang R. et al. Emerging treatment evolutions and integrated molecular characteristics of biliary tract cancers // Cancer Sci. 2021. Vol. 112, N 12. P. 4819 - 4833.
43. Lamarca A. et al. ABC-06| A randomised phase III, multi-centre, open-label study of active symptom control (ASC) alone or ASC with oxaliplatin/5-FU chemotherapy (ASC+ mFOLFOX) for patients (pts) with locally advanced/metastatic biliary tract cancers (ABC) previously-treated with cisplatin/gemcitabine (CisGem) chemotherapy. American Society of Clinical Oncology, 2019.
44. Tella S.H. et al. Second-line therapies in advanced biliary tract cancers // The Lancet Oncology. 2020. Vol. 21, N 1. P. e29 - e41.
45. Zografos G.N. et al. Cholangiocarcinoma: principles and current trends // Hepatobiliary & Pancreatic Diseases International. Elsevier, 2011. Vol. 10, N 1. P. 10 - 20.
46. Sternby Eilard M. et al. Surgical treatment for gallbladder cancer - a systematic literature review // Scandinavian Journal of Gastroenterology. Taylor & Francis, 2017. Vol. 52, N 5. P. 505 - 514.
47. Nagino M. et al. Two hundred forty consecutive portal vein embolizations before extended hepatectomy for biliary cancer: surgical outcome and long-term follow-up // Annals of surgery. Lippincott, Williams, and Wilkins, 2006. Vol. 243, N 3. P. 364.
48. Yamashita S. et al. Efficacy of Preoperative Portal Vein Embolization Among Patients with Hepatocellular Carcinoma, Biliary Tract Cancer, and Colorectal Liver Metastases: A Comparative Study Based on Single-Center Experience of 319 Cases // Ann Surg Oncol. 2017. Vol. 24, N 6. P. 1557 - 1568.
49. Kang M.J. et al. Role of radical surgery in patients with stage IV gallbladder cancer // HPB. Elsevier, 2012. Vol. 14, N 12. P. 805 - 811.
50. Huang Y. et al. Preoperative Portal Vein Embolization for Liver Resection: An updated meta-analysis // J Cancer. 2021. Vol. 12, N 6. P. 1770 - 1778.
51. Arakura N. et al. Efficacy of preoperative endoscopic nasobiliary drainage for hilar cholangiocarcinoma // J Hepatobiliary Pancreat Surg. 2009. Vol. 16, N 4. P. 473 - 477.
52. Завражнов А.А. et al. Значение малоинвазивных методов декомпрессии желчных протоков в лечении больных с механической желтухой // Журнал им. НВ Склифосовского Неотложная медицинская помощь. Межрегиональная общественная организация "Научно-практическое общество..., 2012. N 2. P. 54 - 58.
53. Moole H., Bechtold M., Puli S.R. Efficacy of preoperative biliary drainage in malignant obstructive jaundice: a meta-analysis and systematic review // World Journal of Surgical Oncology. 2016. Vol. 14, N 1. P. 182.
54. Sewnath M.E. et al. A Meta-analysis on the Efficacy of Preoperative Biliary Drainage for Tumors Causing Obstructive Jaundice // Ann Surg. 2002. Vol. 236, N 1. P. 17 - 27.
55. Qiu Y.-D. et al. Effect of preoperative biliary drainage on malignant obstructive jaundice: A meta-analysis // World J Gastroenterol. 2011. Vol. 17, N 3. P. 391 - 396.
56. Mehrabi A. et al. Meta-analysis of the efficacy of preoperative biliary drainage in patients undergoing liver resection for perihilar cholangiocarcinoma // European Journal of Radiology. 2020. Vol. 125. P. 108897.
57. Lee S.E. et al. Systematic review on the surgical treatment for T1 gallbladder cancer // World J Gastroenterol. 2011. Vol. 17, N 2. P. 174 - 180.
58. Coburn N.G. et al. Surgery for gallbladder cancer: a population-based analysis // Journal of the American College of Surgeons. Elsevier, 2008. Vol. 207, N 3. P. 371 - 382.
59. Downing S.R. et al. Early-stage gallbladder cancer in the Surveillance, Epidemiology, and End Results database: effect of extended surgical resection // Archives of surgery. American Medical Association, 2011. Vol. 146, N 6. P. 734 - 738.
60. Yuza K. et al. Outcome of radical surgery for gallbladder carcinoma according to TNM stage: implications for adjuvant therapeutic strategies // Langenbeck's Archives of Surgery. Springer, 2021. Vol. 406, N 3. P. 801 - 811.
61. Vega E.A. et al. Treatment of Resectable Gallbladder Cancer // Cancers (Basel). 2022. Vol. 14, N 6. P. 1413.
62. Zhang W. et al. Survival Benefits of Simple Versus Extended Cholecystectomy and Lymphadenectomy for Patients With T2 Gallbladder Cancer: A Propensity-Matched Population-Based Study (2010 to 2015) // Frontiers in Oncology. 2021. Vol. 11.
63. Park T.J. et al. The optimal surgical resection approach for T2 gallbladder carcinoma: evaluating the role of surgical extent according to the tumor location // Annals of Surgical Treatment and Research. 2018. Vol. 94, N 3. P. 135 - 141.
64. Lee S.E. et al. Surgical Strategy for T2 Gallbladder Cancer: Nationwide Multicenter Survey in Korea // Journal of Korean Medical Science. 2018. Vol. 33, N 28.
65. Burasakarn P. et al. The optimal extent of surgery in T2 gallbladder cancer and the need for hepatectomy: A meta-analysis // Asian Journal of Surgery. 2022. Vol. 45, N 1. P. 33 - 38.
66. Li G. et al. Significance of Hepatectomy in Patients Diagnosed With T2 Gallbladder Cancer // Surgical Laparoscopy Endoscopy & Percutaneous Techniques. 2020. Vol. 30, N 1. P. 35 - 39.
67. Cho J.-K. et al. Validation of the oncologic effect of hepatic resection for T2 gallbladder cancer: a retrospective study // World Journal of Surgical Oncology. 2019. Vol. 17, N 1. P. 8.
68.  . Systematic review of management of incidental gallbladder cancer after cholecystectomy // Journal of British Surgery. Oxford University Press, 2019. Vol. 106, N 1. P. 32 - 45.
. Systematic review of management of incidental gallbladder cancer after cholecystectomy // Journal of British Surgery. Oxford University Press, 2019. Vol. 106, N 1. P. 32 - 45.
69. Goetze T.O., Paolucci V. Benefits of reoperation of T2 and more advanced incidental gallbladder carcinoma: analysis of the German registry // Annals of surgery. LWW, 2008. Vol. 247, N 1. P. 104 - 108.
70. Murakami Y. et al. Prognostic Factors After Surgical Resection for Intrahepatic, Hilar, and Distal Cholangiocarcinoma // Ann Surg Oncol. 2011. Vol. 18, N 3. P. 651 - 658.
71. Bartlett D.L. et al. Long-term results after resection for gallbladder cancer. Implications for staging and management. // Ann Surg. 1996. Vol. 224, N 5. P. 639 - 646.
72. Rebelo A. et al. Systematic review and meta-analysis of surgery for hilar cholangiocarcinoma with arterial resection // HPB. 2022.
73. Ramouz A. et al. Repeat liver resection for recurrent intrahepatic cholangiocarcinoma: meta-analysis // Br J Surg. 2022. Vol. 109, N 7. P. 580 - 587.
74. Miyazaki Y. et al. Survival of surgery for recurrent biliary tract cancer: a single-center experience and systematic review of literature // Japanese Journal of Clinical Oncology. 2017. Vol. 47, N 3. P. 206 - 212.
75. Ziogas I.A. et al. Laparoscopic versus open hepatectomy for intrahepatic cholangiocarcinoma: An inpidual patient data survival meta-analysis // The American Journal of Surgery. 2021. Vol. 222, N 4. P. 731 - 738.
76. Meyer C.G., Penn I., James L. Liver transplantation for cholangiocarcinoma: results in 207 patients1 // Transplantation. LWW, 2000. Vol. 69, N 8. P. 1633 - 1637.
77. Goldstein R.M. et al. Is liver transplantation indicated for cholangiocarcinoma? // Am J Surg. 1993. Vol. 166, N 6. P. 768 - 771; discussion 771 - 772.
78. Li D.-B. et al. Long-term outcomes of combined hepatocellular-cholangiocarcinoma after hepatectomy or liver transplantation: A systematic review and meta-analysis // Hepatobiliary & Pancreatic Diseases International. 2019. Vol. 18, N 1. P. 12 - 18.
79. Ziogas I.A. et al. Liver Transplantation for Intrahepatic Cholangiocarcinoma: A Meta-analysis and Meta-regression of Survival Rates // Transplantation. 2021. Vol. 105, N 10. P. 2263 - 2271.
80. Pichlmayr R. et al. Surgical treatment in proximal bile duct cancer. A single-center experience. // Ann Surg. 1996. Vol. 224, N 5. P. 628 - 638.
81. Launois B. et al. Proximal Bile Duct Cancer: High Resectability Rate and 5-Year Survival // Ann Surg. 1999. Vol. 230, N 2. P. 266.
82. Neuhaus P. et al. Surgical management of proximal bile duct cancer: extended right lobe resection increases resectability and radicality // Langenbeck's archives of surgery. Springer, 2003. Vol. 388, N 3. P. 194 - 200.
83. Nagino M. et al. "Anatomic" right hepatic trisectionectomy (extended right hepatectomy) with caudate lobectomy for hilar cholangiocarcinoma // Annals of surgery. Lippincott, Williams, and Wilkins, 2006. Vol. 243, N 1. P. 28.
84. Valle J.W. et al. Cisplatin and gemcitabine for advanced biliary tract cancer: a meta-analysis of two randomised trials // Annals of Oncology. 2014. Vol. 25, N 2. P. 391 - 398.
85. Ghidini M. et al. Adjuvant chemotherapy for resected biliary tract cancers: a systematic review and meta-analysis // HPB. 2017. Vol. 19, N 9. P. 741 - 748.
86. Ma N. et al. Adjuvant therapy in the treatment of gallbladder cancer: a meta-analysis // BMC Cancer. 2015. Vol. 15, N 1. P. 615.
87. Messina C. et al. Adjuvant chemotherapy in resected bile duct cancer: A systematic review and meta-analysis of randomized trials // Critical Reviews in Oncology/Hematology. 2019. Vol. 143. P. 124 - 129.
88. Rangarajan K. et al. Systemic adjuvant chemotherapy for cholangiocarcinoma surgery: A systematic review and meta-analysis // European Journal of Surgical Oncology. 2020. Vol. 46, N 4, Part A. P. 684 - 693.
89. Бредер В.В., Косырев В.Ю., Ледин Е.В. Практические рекомендации по лекарственному лечению билиарного рака // Злокачественные опухоли. 2017. Vol. 7, N 3-S2. P. 352 - 366.
90. Ben-Josef E. et al. SWOG S0809: A Phase II Intergroup Trial of Adjuvant Capecitabine and Gemcitabine Followed by Radiotherapy and Concurrent Capecitabine in Extrahepatic Cholangiocarcinoma and Gallbladder Carcinoma // J Clin Oncol. 2015. Vol. 33, N 24. P. 2617 - 2622.
91. Fisher S.B. et al. Lymphovascular and perineural invasion as selection criteria for adjuvant therapy in intrahepatic cholangiocarcinoma: a multi-institution analysis // HPB. 2012. Vol. 14, N 8. P. 514 - 522.
92. Hyder O. et al. Recurrence after operative management of intrahepatic cholangiocarcinoma // Surgery. 2013. Vol. 153, N 6. P. 811 - 818.
93. Cereda S., Belli C., Reni M. Adjuvant treatment in biliary tract cancer: To treat or not to treat? // World J Gastroenterol. 2012. Vol. 18, N 21. P. 2591 - 2596.
94. Kelley S.T. et al. Cholangiocarcinoma: Advocate an Aggressive Operative Approach with Adjuvant Chemotherapy/DISCUSSION // The American Surgeon. SAGE PUBLICATIONS, INC., 2004. Vol. 70, N 9. P. 743.
95. Koh M. et al. Radiation therapy for recurrent extrahepatic bile duct cancer // PLoS One. 2021. Vol. 16, N 6. P. e0253285.
96. Gkika E. et al. The Evolving Role of Radiation Therapy in the Treatment of Biliary Tract Cancer // Frontiers in Oncology. 2020. Vol. 10.
97. Shitara K. et al. Hepatic arterial infusion of mitomycin C with degradable starch microspheres for unresectable intrahepatic cholangiocarcinoma // Clinical Oncology. Elsevier, 2008. Vol. 20, N 3. P. 241 - 246.
98. Inaba Y. et al. Phase I/II study of hepatic arterial infusion chemotherapy with gemcitabine in patients with unresectable intrahepatic cholangiocarcinoma (JIVROSG-0301) // American journal of clinical oncology. LWW, 2011. Vol. 34, N 1. P. 58 - 62.
99. Kemeny N.E. et al. Treating primary liver cancer with hepatic arterial infusion of floxuridine and dexamethasone: does the addition of systemic bevacizumab improve results // Oncology. Karger Publishers, 2011. Vol. 80, N 3 - 4. P. 153 - 159.
100. Boehm L.M. et al. Comparative effectiveness of hepatic artery based therapies for unresectable intrahepatic cholangiocarcinoma // Journal of surgical oncology. Wiley Online Library, 2015. Vol. 111, N 2. P. 213 - 220.
101. Paz-Fumagalli R. et al. Safety and initial efficacy of ablative radioembolization for the treatment of unresectable intrahepatic cholangiocarcinoma // Oncotarget. Impact Journals, LLC, 2021. Vol. 12, N 20. P. 2075.
102. Edeline J. et al. Radioembolization Plus Chemotherapy for First-line Treatment of Locally Advanced Intrahepatic Cholangiocarcinoma: A Phase 2 Clinical Trial // JAMA Oncology. 2020. Vol. 6, N 1. P. 51 - 59.
103. Ibrahim S.M. et al. Treatment of unresectable cholangiocarcinoma using yttrium-90 microspheres: results from a pilot study // Cancer. Wiley Online Library, 2008. Vol. 113, N 8. P. 2119 - 2128.
104. Ortner M.E.J. et al. Successful photodynamic therapy for nonresectable cholangiocarcinoma: a randomized prospective study // Gastroenterology. 2003. Vol. 125, N 5. P. 1355 - 1363.
105. Zoepf T. et al. Palliation of Nonresectable Bile Duct Cancer: Improved Survival After Photodynamic Therapy // Official journal of the American College of Gastroenterology | ACG. 2005. Vol. 100, N 11. P. 2426 - 2430.
106. Ghafoori A.P. et al. Radiotherapy in the treatment of patients with unresectable extrahepatic cholangiocarcinoma // International Journal of Radiation Oncology*Biology*Physics. 2011. Vol. 81, N 3. P. 654 - 659.
107. Eckel F., Schmid R.M. Chemotherapy in advanced biliary tract carcinoma: a pooled analysis of clinical trials // British journal of cancer. Nature Publishing Group, 2007. Vol. 96, N 6. P. 896 - 902.
108. Yonemoto N. et al. A multi-center retrospective analysis of survival benefits of chemotherapy for unresectable biliary tract cancer // Japanese journal of clinical oncology. Oxford University Press, 2007. Vol. 37, N 11. P. 843 - 851.
109. Valle J. et al. Cisplatin plus gemcitabine versus gemcitabine for biliary tract cancer // New England Journal of Medicine. Mass Medical Soc, 2010. Vol. 362, N 14. P. 1273 - 1281.
110. Kainuma O. et al. Feasibility and efficacy of gemcitabine plus cisplatin combination therapy after curative resection for biliary tract cancer // Journal of Hepato-Biliary-Pancreatic Sciences. 2015. Vol. 22, N 11. P. 789 - 794.
111. Song S. et al. The efficacy and safety of 5-fluorouracil based adjuvant therapy in resected biliary tract cancer: A systematic review and meta-analysis // Clinics and Research in Hepatology and Gastroenterology. 2022. Vol. 46, N 2. P. 101788.
112. Yang R. et al. Efficacy of gemcitabine plus platinum agents for biliary tract cancers: a meta-analysis // Anti-Cancer Drugs. 2013. Vol. 24, N 8. P. 871 - 877.
113. Zhu G.-Q. et al. Systematic review with network meta-analysis: adjuvant therapy for resected biliary tract cancer // Alimentary Pharmacology & Therapeutics. 2014. Vol. 40, N 7. P. 759 - 770.
114. Sharma A. et al. Best supportive care compared with chemotherapy for unresectable gall bladder cancer: a randomized controlled study // J Clin Oncol. 2010. Vol. 28, N 30. P. 4581 - 4586.
115. Kato A. et al. Surgical Resection after Downsizing Chemotherapy for Initially Unresectable Locally Advanced Biliary Tract Cancer: A Retrospective Single-center Study // Ann Surg Oncol. 2013. Vol. 20, N 1. P. 318 - 324.
116. Jang J.-S. et al. Gemcitabine and oxaliplatin in patients with unresectable biliary cancer including gall bladder cancer: a Korean Cancer Study Group phase II trial // Cancer chemotherapy and pharmacology. Springer, 2010. Vol. 65, N 4. P. 641 - 647.
117. Dodagoudar C. et al. FOLFOX-4 as second-line therapy after failure of gemcitabine and platinum combination in advanced gall bladder cancer patients // Japanese journal of clinical oncology. Oxford University Press, 2016. Vol. 46, N 1. P. 57 - 62.
118. Knox J.J. et al. Combining gemcitabine and capecitabine in patients with advanced biliary cancer: a phase II trial // J Clin Oncol. 2005. Vol. 23, N 10. P. 2332 - 2338.
119. Edeline J., Touchefeu Y., Guiu B., et al. Radioembolization Plus Chemotherapy for First-line Treatment of Locally Advanced Intrahepatic Cholangiocarcinoma: A Phase 2 Clinical Trial. JAMA Oncol. 2020; 6: 51 - 59
120. Cercek A., Boerner T., Tan B.R. et al. Assessment of Hepatic Arterial Infusion of Floxuridine in Combination With Systemic Gemcitabine and Oxaliplatin in Patients With Unresectable Intrahepatic Cholangiocarcinoma: A Phase 2 Clinical Trial. JAMA Oncol. 2020; 6: 60 - 67
121. Marabelle A. et al. Efficacy of pembrolizumab in patients with noncolorectal high microsatellite instability/mismatch repair-deficient cancer: Results from the phase II KEYNOTE-158 study // Journal of Clinical Oncology. American Society of Clinical Oncology, 2020. Vol. 38, N 1. P. 1.
122. Oh D.-Y. et al. Durvalumab plus Gemcitabine and Cisplatin in Advanced Biliary Tract Cancer // NEJM Evidence. Massachusetts Medical Society, 2022. P. EVIDoa2200015.
123. Yoo C., Kim K.P., Jeong J.H., et al. Liposomal irinotecan plus fluorouracil and leucovorin versus fluorouracil and leucovorin for metastatic biliary tract cancer after progression on gemcitabine plus cisplatin (NIFTY): a multicentre, open-label, randomised, phase 2b study. Lancet Oncol. 2021; 22: 1560 - 1572.
124. Rizzo A. et al. Anti-EGFR Monoclonal Antibodies in Advanced Biliary Tract Cancer: A Systematic Review and Meta-analysis // In Vivo. International Institute of Anticancer Research, 2020. Vol. 34, N 2. P. 479 - 488.
125. Singh P.M., Kapoor R., Kumar R. Best supportive care compared with chemotherapy and radiotherapy for unresectable gallbladder cancer: A tertiary care institute experience // Clinical Cancer Investigation Journal. 2014. Vol. 3, N 2. P. 153 - 156.
126. Lamarca A. et al. Second-line FOLFOX chemotherapy versus active symptom control for advanced biliary tract cancer (ABC-06): a phase 3, open-label, randomised, controlled trial // Lancet Oncol. 2021. Vol. 22, N 5. P. 690 - 701.
127. Phelip J.-M. et al. Gemcitabine plus cisplatin versus chemoradiotherapy in locally advanced biliary tract cancer: F d ration Francophone de Canc rologie Digestive 9902 phase II randomised study // Eur J Cancer. 2014. Vol. 50, N 17. P. 2975 - 2982.
128. Fuller C.D. et al. Image-guided intensity-modulated radiotherapy (IG-IMRT) for biliary adenocarcinomas: Initial clinical results // Radiotherapy and Oncology. Elsevier, 2009. Vol. 92, N 2. P. 249 - 254.
129. Al-Adra D.P. et al. Treatment of unresectable intrahepatic cholangiocarcinoma with yttrium-90 radioembolization: a systematic review and pooled analysis // European Journal of Surgical Oncology (EJSO). Elsevier, 2015. Vol. 41, N 1. P. 120 - 127.
130. Bonet Beltr n M. et al. Is adjuvant radiotherapy needed after curative resection of extrahepatic biliary tract cancers? A systematic review with a meta-analysis of observational studies // Cancer Treatment Reviews. 2012. Vol. 38, N 2. P. 111 - 119.
131. Ren B. et al. A meta-analysis of the efficacy of postoperative adjuvant radiotherapy versus no radiotherapy for extrahepatic cholangiocarcinoma and gallbladder carcinoma // Radiation Oncology. 2020. Vol. 15, N 1. P. 15.
132. Choi S.H. et al. Adjuvant Radiotherapy for Extrahepatic Cholangiocarcinoma: A Quality Assessment-Based Meta-Analysis // LIC. Karger Publishers, 2021. Vol. 10, N 5. P. 419 - 432.
133. Asher A., Ng A., Engle J. Principles of Cancer Rehabilitation // Cardio-Oncology: Principles, Prevention and Management. Elsevier Inc., 2017. P. 279 - 296.
134. Qin X.-L. et al. Utility of serum CA19-9 in diagnosis of cholangiocarcinoma: In comparison with CEA // World J Gastroenterol. 2004. Vol. 10, N 3. P. 427 - 432.
135. Yoo J. et al. Additional Value of Integrated 18F-FDG PET/MRI for Evaluating Biliary Tract Cancer: Comparison with Contrast-Enhanced CT // Korean Journal of Radiology. 2021. Vol. 22, N 5. P. 714 - 724.
136. Rizzo A. et al. Intensive Follow-Up Program and Oncological Outcomes of Biliary Tract Cancer Patients after Curative-Intent Surgery: A Twenty-Year Experience in a Single Tertiary Medical Center // Current Oncology. Multidisciplinary Digital Publishing Institute, 2022. Vol. 29, N 7. P. 5084 - 5090
137. Addlev J, Mitchell RM. Advances in the investigation of obstructive jaundice. CurrGastroenterol Rep. 2012; 14(6): 511 - 519
138. Нечипай А.М., Орлов С.Ю., ФедоровЕ.Д. ЭУСбука. Руководство по эндоскопической ультрасонографии. Практическаямедицина; 2013. NechipayAM, Orlov SYu, Fedorov ED. Manual of endoscopic ultrasonography. Prakticheskayameditsina; 2013. (In Russ.)
139. Hidalgo M, Alvarez R, Gallego J, et al. Consensus guidelines for diagnosis, treatment and follow-up of patients with pancreatic cancer in Spain. Clinical and Translational Oncology. 2017;19(6):667-681
140. Petrescu I, Bratu AM, Petrescu S. CT vs. MRCP in choledocholithiasis jaundice. J Med Life. 2015; 8(2): 226 - 231
141. Joo I, Lee JM, Yoon JH. Imaging Diagnosis of Intrahepatic and Perihilar Cholangiocarcinoma: Recent Advances and Challenges. Radiology. 2018 July; 288(1): 7-13. Epub 2018 Jun 5
142. Hekimoglu K, Ustundag Y, Dusak A, et al. MRCP vs. ERCP in the evaluation of biliary pathologies: review of current literature. J DigDis. 2008; 9: 162 - 169
143. Duan F, Cui L, Bai Y, Li X, Yan J, Liu X. Cancer Imaging.2017 Oct 16; 17(1): 27. doi: 10.1186/s40644-017-0129-1
144. Moole H, Dharmapuri S, Duvvuri A, etal. Endoscopic versus Percutaneous Biliary Drainage in Palliation of Advanced Malignant Hilar Obstruction: A Meta-Analysis and Systematic Review. Canad J Gastroenterol and Hepatol. 2016; 8: 1-8
145. Hameed A, Pang T, Chiou J, et al. Percutaneous vs. endoscopic preoperative biliary drainage in hilar cholangiocarcinoma - a systematic review and meta-analysis. HPB. 2016; 18(7): 400 - 410
146. Sasahira N, Hamada T, Togawa O, et al. Multicenter study of endoscopic preoperative biliary drainage for malignant distal biliary obstruction. World J Gastroenterol. 2016; 22(14): 3793 - 3802
147. Crippa S, Cirocchi R, Partelli S, Petrone MC, Muffatti F, Renzi C, Falconi M, Arcidiacono PG. Systematic review and meta-analysis of metal versus plastic stents for preoperative biliary drainage in resectableperiampullary or pancreatic head tumors. Eur J Surg Oncol. 2016; 42(9): 1278 - 1280
148. Wiggers JK, Coelen RJS, Rauws EAJ et al. Preoperative endoscopic versus percutaneous transhepatic biliary drainage in potentially resectableperihilar cholangiocarcinoma (DRAINAGE trial): design and rationale of a randomized controlled trial. BMC Gastroenterology. 2015;15-20. 149. Scheufele F, Schorn S, Demir IE, et al. Preoperative biliary stenting versus operation first in jaundiced patients due to malignant lesions in the pancreatic head: A meta-analysis of current literature. Surgery. 2017; 161(4): 939 - 950.
149. Ikeda M., Nakachi K., Konishi M., et al. Adjuvant S-1 versus observation in curatively resected biliary tract cancer: A phase III trial (JCOG1202: ASCOT). J Clin Oncol. 2022; 40: 382
150. Edeline J., Benabdelghani M., Bertaut A., et al. Gemcitabine and Oxaliplatin Chemotherapy or Surveillance in Resected Biliary Tract Cancer (PRODIGE 12-ACCORD 18-UNICANCER GI): A Randomized Phase III Study. J Clin Oncol. 2019; 37: 658 - 667).
151. Ebata T., Hirano S., Konishi M., et al., Randomized clinical trial of adjuvant gemcitabine chemotherapy versus observation in resected bile duct cancer. Br J Surg. 2018; 105: 192 - 202.
152. Glimelius B., Hoffman K., Sjoden P.O., et al. Chemotherapy improves survival and quality of life in advanced pancreatic and biliary cancer. Ann Oncol. 1996; 7: 593 - 600.
153. Sharma A., Dwary A.D., Mohanti B.K. et al. Best supportive care compared with chemotherapy for unresectable gall bladder cancer: a randomized controlled study. J Clin Oncol. 2010; 28: 4581 - 4586
154. Kim ST, Kang JH, Lee J et al. Capecitabine plus oxaliplatin versus gemcitabine plus oxaliplatin as first-line therapy for advanced biliary tract cancers: a multicenter, open-label, randomized, phase III, noninferiority trial. Ann Oncol. 2019 May 1; 30(5): 788 - 795. doi: 10.1093/annonc/mdz058.
155. Lamarca A., Benafif S., Ross P., et al. Cisplatin and gemcitabine in patients with advanced biliary tract cancer (ABC) and persistent jaundice despite optimal stenting: Effective intervention in patients with luminal disease. Eur J Cancer. 2015; 51: 1694 - 1703
156. Le Roy B., Gelli M., Pittau G., et al. Neoadjuvant chemotherapy for initially unresectable intrahepatic cholangiocarcinoma. Br J Surg. 2018; 105: 839 - 847
157. Javle M., Borad M.J., Azad N.S. et al. Pertuzumab and trastuzumab for HER2-positive, metastatic biliary tract cancer (MyPathway): a multicentre, open-label, phase 2a, multiple basket study.Lancet Oncol. 2021; 22: 1290 - 1300.
158. Subbiah V., Lassen U.,  Dabrafenib plus trametinib in patients with BRAF(V600E)-mutated biliary tract cancer (ROAR): a phase 2, open-label, single-arm, multicentre basket trial. Lancet Oncol. 2020; 21: 1234 - 1243
Dabrafenib plus trametinib in patients with BRAF(V600E)-mutated biliary tract cancer (ROAR): a phase 2, open-label, single-arm, multicentre basket trial. Lancet Oncol. 2020; 21: 1234 - 1243
159. Marabelle A., Le D.T., Ascierto P.A. et al. Efficacy of Pembrolizumab in Patients With Noncolorectal High Microsatellite Instability/Mismatch Repair-Deficient Cancer: Results From the Phase II KEYNOTE-158 Study. J Clin Oncol. 2020; 38: 1-1
160. Hong D.S., Shen L., van Tilburg C.M., et al. Long-term efficacy and safety of larotrectinib in an integrated dataset of patients with TRK fusion cancer. J Clin Oncol. 2021; 39: 3108
161. Doebele R.C., Drilon A., Paz- Ares L., et al. Entrectinib in patients with advanced or metastatic NTRK fusion-positive solid tumours: integrated analysis of three phase 1-2 trials. Lancet Oncol. 2020; 21: 271 - 282
162. Wong HH, Chu P. Immunohistochemical features of the gastrointestinal tract tumors. J Gastrointest Oncol. 2012 Sep; 3(3): 262-84. doi: 10.3978/j.issn.2078-6891.2012.019.
163. Rerknimitr R., Angsuwatcharakon P., Ratanachu-ek T., Khor C.J.L., Ponnudurai R., Moon J.H., Seo D.W., PantongragBrown L., Sangchan A., Pisespongsa P., Akaraviputh T., Reddy N.D., Maydeo A., Itoi T., Pausawasdi N., Punamiya S., Attasaranya S., Devereaux B., Ramchandani M., Goh K.-L. Asia-Pacific consensus recommendations for endoscopic and interventional management of hilar cholangiocarcinoma. J. Gastroenterol. Hepatol. 2013; 28 (4): 593 - 607.
164. Diagnostic pathology:Hepatobiliary and pancreas, Third edition, 2022. Elsevier edition.
165. Gkika E, Hawkins MA, Grosu AL, Brunner TB. The Evolving Role of Radiation Therapy in the Treatment of Biliary Tract Cancer. Front Oncol. 2020 Dec 14; 10: 604387.
166. Tao R, Krishnan S, Bhosale PR, Javle MM, Aloia TA, Shroff RT, Kaseb AO, Bishop AJ, Swanick CW, Koay EJ, Thames HD, Hong TS, Das P, Crane CH. Ablative Radiotherapy Doses Lead to a Substantial Prolongation of Survival in Patients With Inoperable Intrahepatic Cholangiocarcinoma: A Retrospective Dose Response Analysis. J Clin Oncol. 2016 Jan 20; 34(3): 219-26.
167. Sakamoto E, Nimura Y, Hayakawa N, Kamiya J, Kondo S, Nagino M, Kanai M, Miyachi M, Uesaka K. The pattern of infiltration at the proximal border of hilar bile duct carcinoma: a histologic analysis of 62 resected cases. Ann Surg. 1998 Mar; 227(3): 405-11.
168. Kim D.W., Kim S.Y., Kang H.J., Kang J.H., Lee S.S., Shim J.H. et al. Diagnostic performance of ultrasonography-guided core-needle biopsy according to MRI LI-RADS diagnostic categories. // Ultrasonography. 2021; 40: 387 - 397 https://doi.org/10.14366/usg.20110
169. Lamarca A, Edeline J, Goyal L. How I treat biliary tract cancer. ESMO Open. 2022; 7(1): 100378. doi:10.1016/j.esmoop.2021.100378
170. Park J.H. Kim J.H. Pathologic differential diagnosis of metastatic carcinoma in the liver. // Clin Mol Hepatol. 2019; 25: 12-20 https://doi.org/10.3350/cmh.2018.0067
171. Kim Y., Yeom S., Shin H., Choi S.H., Rhee H., Park J.H., et al.Clinical staging of mass-forming intrahepatic cholangiocarcinoma: computed tomography versus magnetic resonance imaging. // Hepatol Commun. 2021; 5: 2009 - 2018 https://doi.org/10.1002/hep4.1774
172. EASL-ILCA Clinical Practice Guidelines on the management of intrahepatic cholangiocarcinoma // European Association for the Study of the Liver Published:April 19, 2023 DOI:https://doi.org/10.1016/j.jhep.2023.03.010
173. Kelley RK, Ueno M, Yoo C, et al. Pembrolizumab in combination with gemcitabine and cisplatin compared with gemcitabine and cisplatin alone for patients with advanced biliary tract cancer (KEYNOTE-966): A randomised, double-blind, placebo-controlled, phase 3 trial. Lancet 2023; 401: 1853 - 1865. https://www.ncbi.nlm.nih.gov/pubmed/37075781.
174. Choi IS, Kim KH, Lee JH et al. A randomised phase II study of oxaliplatin/5-FU (mFOLFOX) versus irinotecan/5-FU (mFOLFIRI) chemotherapy in locally advanced or metastatic biliary tract cancer refractory to first-line gemcitabine/cisplatin chemotherapy. Eur J Cancer. 2021 Sep; 154: 288 - 295. doi: 10.1016/j.ejca.2021.06.019. Epub 2021 Jul 22. PMID: 34303267.
175. Ohba A, Morizane C, Ueno M et al. Multicenter phase II trial of trastuzumab deruxtecan for HER2-positive unresectable or recurrent biliary tract cancer: HERB trial. Future Oncol. 2022 Jun; 18(19): 2351 - 2360. doi: 10.2217/fon-2022-0214. Epub 2022 May 5. PMID: 35510484.
176. Meric-Bernstam F, Rothe M, Mangat PK et al. Cobimetinib Plus Vemurafenib in Patients With Solid Tumors With BRAF Mutations: Results From the Targeted Agent and Profiling Utilization Registry Study. JCO Precis Oncol. 2023 Sep; 7: e2300385. doi: 10.1200/PO.23.00385. PMID: 38096472; PMCID: PMC10735080.
177. He J, Kalinava N, Doshi P et al. Evaluation of tissue- and plasma-derived tumor mutational burden (TMB) and genomic alterations of interest in CheckMate 848, a study of nivolumab combined with ipilimumab and nivolumab alone in patients with advanced or metastatic solid tumors with high TMB. J Immunother Cancer. 2023 Nov 30; 11(11): e007339. doi: 10.1136/jitc-2023-007339. PMID: 38035725; PMCID: PMC10689409.
178. Subbiah V, Cassier PA, Siena S et al. Pan-cancer efficacy of pralsetinib in patients with RET fusion-positive solid tumors from the phase 1/2 ARROW trial. Nat Med. 2022 Aug; 28(8): 1640-1645. doi: 10.1038/s41591-022-01931-y. Epub 2022 Aug 12. PMID: 35962206; PMCID: PMC9388374.
179. Subbiah V, Wolf J, Konda B et al. Tumour-agnostic efficacy and safety of selpercatinib in patients with RET fusion-positive solid tumours other than lung or thyroid tumours (LIBRETTO-001): a phase 1/2, open-label, basket trial. Lancet Oncol. 2022 Oct; 23(10): 1261 - 1273. doi: 10.1016/S1470-2045(22) 00541-1. Epub 2022 Sep 12. PMID: 36108661.
180. Hong DS, Fakih MG, Strickler JH et al. KRASG12C Inhibition with Sotorasib in Advanced Solid Tumors. N Engl J Med. 2020 Sep 24; 383(13): 1207 - 1217. doi: 10.1056/NEJMoa1917239.
181. Demols A, Borbath I, Van den Eynde M et al. Regorafenib after failure of gemcitabine and platinum-based chemotherapy for locally advanced/metastatic biliary tumors: REACHIN, a randomized, double-blind, phase II trial. Ann Oncol. 2020 Sep; 31(9): 1169 - 1177. doi: 10.1016/j.annonc.2020.05.018. Epub 2020 May 25. PMID: 32464280.
182. Zheng Y, Tu X, Zhao P, Jiang W, Liu L, Tong Z, Zhang H, Yan C, Fang W, Wang W. A randomised phase II study of second-line XELIRI regimen versus irinotecan monotherapy in advanced biliary tract cancer patients progressed on gemcitabine and cisplatin. Br J Cancer. 2018 Aug; 119(3): 291 - 295
183. Ben-Josef E., Guthrie K.A., El-Khoueiry A.B., et al. SWOG S0809: a phase II intergroup trial of adjuvant capecitabine and gemcitabine followed by radiotherapy and concurrent capecitabine in extrahepatic cholangiocarcinoma and gallbladder carcinoma.J Clin Oncol. 2015; 33: 2617-2622
184. Wang SJ, Lemieux A, Kalpathy-Cramer J, et al. Nomogram for predicting the benefit of adjuvant chemoradiotherapy for resected gallbladder cancer. J Clin Oncol 2011; 29: 4627 - 4632
185. Pant S, Schuler M, Iyer G et al. Erdafitinib in patients with advanced solid tumours with FGFR alterations (RAGNAR): an international, single-arm, phase 2 study. Lancet Oncol. 2023 Aug; 24(8): 925 - 935. doi: 10.1016/S1470-2045(23) 00275-9. PMID: 37541273; PMCID: PMC11224843.
186. Wang SJ, Lemieux A, Kalpathy-Cramer J, et al. Nomogram for predicting the benefit of adjuvant chemoradiotherapy for resected gallbladder cancer. J Clin Oncol 2011; 29: 4627 - 4632
187. Primrose JN, Fox RP, Palmer DH et al. Capecitabine compared with observation in resected biliary tract cancer (BILCAP): a randomised, controlled, multicentre, phase 3 study. Lancet Oncol. 2019 May; 20(5): 663 - 673. doi: 10.1016/S1470-2045(18) 30915-X.
188. Gupta P, Dutta U, Rana P, Singhal M, Gulati A, Kalra N, et al.. Gallbladder reporting and data system (GB-RADS) for risk stratification of gallbladder wall thickening on ultrasonography: an international expert consensus. Abdom Radiol (NY). (2022) 47: 554-65. doi: 10.1007/s00261-021-03360-w
189. Konstantinoff KS, Feister KF, Mellnick VM. RadioGraphics update: new follow-up and management recommendations for polypoid lesions of the gallbladder. Radiographics. (2023) 43: e220189. doi: 10.1148/rg.220189
190. Хатьков И.Е., Аванесян Р.Г., Ахаладзе Г.Г., и др. Российский консенсус по актуальным вопросам диагностики и лечения синдрома механической желтухи. Pirogov Russian Journal of Surgery. 2020; (6): 5-17. (In Russ.) https://doi.org/10.17116/hirurgia20200615
191. Moll CF, de Moura DTH, Ribeiro IB, et al. Endoscopic Biliary Darinage (EBD) versus Percutaneous Transhepatic Biliary Drainage (PTBD) for biliary drainage in patients with Perihilar Cholangiocarcinoma (PCCA): A systematic review and meta-analysis. Clinics (Sao Paulo). 2023; 78: 100163. Published 2023 Jan 19. doi:10.1016/j.clinsp.2022.100163
192. Polyakov AN, Patyutko YuI, Kotelnikov AG, et al. Surgical treatment and prognostic factors in perihilar tumors. Pirogov Russian Journal of Surgery. 2024; (2): 14-23. (In Russ., In Engl.). https://doi.org/10.17116/hirurgia202402114
193. Zhang X. F., Squires M. H., 3rd, Bagante F., et al. The Impact of Intraoperative Re-Resection of a Positive Bile Duct Margin on Clinical Outcomes for Hilar Cholangiocarcinoma // Ann Surg Oncol. - 2018. - T. 25, N 5. - C. 1140 - 1149.
194. Abou-Alfa GK, Sahai V, Hollebecque A, et al. Pemigatinib for previously treated, locally advanced or metastatic cholangiocarcinoma: a multicentre, open-label, phase 2 study. Lancet Oncol. 2020; 21(5): 671 - 684.
195. Yokoyama Y, Ebata T, Igami T, et al. Different Clinical Characteristics Between Distal Cholangiocarcinoma and Pancreatic Head Carcinoma With Biliary Obstruction. Pancreas. 2017 Nov/Dec; 46(10): 1322 - 1326. doi: 10.1097/MPA.0000000000000942.
196. Gupta P, Dutta U, Rana P, Singhal M, Gulati A, Kalra N, et al.. Gallbladder reporting and data system (GB-RADS) for risk stratification of gallbladder wall thickening on ultrasonography: an international expert consensus. Abdom Radiol (NY). (2022) 47: 554-65. doi: 10.1007/s00261-021-03360-w
197. Konstantinoff KS, Feister KF, Mellnick VM. RadioGraphics update: new follow-up and management recommendations for polypoid lesions of the gallbladder. Radiographics. (2023) 43: e220189. doi: 10.1148/rg.220189
198. Del Vecchio Blanco G, Mossa M, Troncone E, et al. Tips and tricks for the diagnosis and management of biliary stenosis-state of the art review. World J Gastrointest Endosc. 2021; 13(10): 473 - 490. doi:10.4253/wjge.v13.i10.473
Приложение А1
СОСТАВ
РАБОЧЕЙ ГРУППЫ ПО РАЗРАБОТКЕ И ПЕРЕСМОТРУ
КЛИНИЧЕСКИХ РЕКОМЕНДАЦИЙ
1. Базин И.С., д.м.н., ведущий научный сотрудник отделения противоопухолевой лекарственной терапии N 2 НИИ клинической онкологии им. акад. РАН и РАМН Н.Н. Трапезникова ФГБУ "Национальный медицинский исследовательский центр онкологии им. Н.Н. Блохина" Министерства здравоохранения Российской Федерации.
2. Бредер В.В., д.м.н., заведующий отделом лекарственного лечения НИИ клинической онкологии им. акад. РАН и РАМН Н.Н. Трапезникова ФГБУ "Национальный медицинский исследовательский центр онкологии им. Н.Н. Блохина" Министерства здравоохранения Российской Федерации.
3. Виршке Э.Р., д.м.н., заведующий рентгенооперационным блоком НИИ клинической и экспериментальной радиологии ФГБУ "Национальный медицинский исследовательский центр онкологии им. Н.Н. Блохина" Министерства здравоохранения Российской Федерации.
4. Долгушин Б.И, академик РАН, профессор, д.м.н., директор НИИ клинической и экспериментальной радиологии ФГБУ "Национальный медицинский исследовательский центр онкологии им. Н.Н. Блохина" Министерства здравоохранения Российской Федерации.
5. Кудашкин Н.Е., к.м.н., старший научный сотрудник отделения абдоминальной онкологии N 2 (опухолей гепатопанкреатобилиарной зоны) НИИ клинической онкологии им. акад. РАН и РАМН Н.Н. Трапезникова ФГБУ "Национальный медицинский исследовательский центр онкологии им. Н.Н. Блохина" Министерства здравоохранения Российской Федерации.
6. Ледин Е.В., к.м.н., руководитель центра химиотерапии, заведующий отделением химиотерапии Международного центра онкологии на базе клинической больницы МЕДСИ в Боткинском проезде.
7. Лукьянченко А.Б., профессор, д.м.н., научный консультант рентгенодиагностического отделения НИИ клинической и экспериментальной радиологии ФГБУ "Национальный медицинский исследовательский центр онкологии им. Н.Н. Блохина" Министерства здравоохранения Российской Федерации.
8. Медведева Б.М., профессор, д.м.н., главный научный сотрудник рентгенодиагностического отделения НИИ клинической и экспериментальной радиологии ФГБУ "Российский онкологический научный центр им. Н.Н. Блохина" Минздрава России, г. Москва.
9. Мороз Е.А., к.м.н., старший научный сотрудник отдела патологической анатомии опухолей ФГБУ "Национальный медицинский исследовательский центр онкологии им. Н.Н. Блохина" Министерства здравоохранения Российской Федерации.
10. Патютко Ю.И., профессор, д.м.н., главный научный консультант отделения абдоминальной онкологии N 2 (опухолей гепатопанкреатобилиарной зоны) НИИ клинической онкологии им. акад. РАН и РАМН Н.Н. Трапезникова ФГБУ "Национальный медицинский исследовательский центр онкологии им. Н.Н. Блохина" Министерства здравоохранения Российской Федерации.
11. Погребняков И.В., к.м.н., заведующий отделением рентгенохирургических методов диагностики и лечения НИИ клинической и экспериментальной радиологии ФГБУ "Национальный медицинский исследовательский центр онкологии им. Н.Н. Блохина" Министерства здравоохранения Российской Федерации.
12. Поляков А.Н., к.м.н., старший научный сотрудник отделения абдоминальной онкологии N 2 (опухолей гепатопанкреатобилиарной зоны) НИИ клинической онкологии им. акад. РАН и РАМН Н.Н. Трапезникова ФГБУ "Национальный медицинский исследовательский центр онкологии им. Н.Н. Блохина" Министерства здравоохранения Российской Федерации.
13. Подлужный Д.В., доцент, к.м.н., заведующий отделением абдоминальной онкологии N 2 (опухолей гепатопанкреатобилиарной зоны) НИИ клинической онкологии им. акад. РАН и РАМН Н.Н. Трапезникова ФГБУ "Национальный медицинский исследовательский центр онкологии им. Н.Н. Блохина" Министерства здравоохранения Российской Федерации.
14. Сергеева О.Н., к.м.н., старший научный сотрудник отделения рентгенохирургических методов диагностики и лечения НИИ клинической и экспериментальной радиологии ФГБУ "Национальный медицинский исследовательский центр онкологии им. Н.Н. Блохина" Министерства здравоохранения Российской Федерации.
15. Францев Д.Ю., к.м.н., врач отделения рентгенохирургических методов диагностики и лечения НИИ клинической и экспериментальной радиологии ФГБУ "Национальный медицинский исследовательский центр онкологии им. Н.Н. Блохина" Министерства здравоохранения Российской Федерации.
16. Иванов В.А., к.м.н., врач отделения радиотерапии ФГБУ "Национальный медицинский исследовательский центр онкологии им. Н.Н. Блохина" Министерства здравоохранения Российской Федерации.
17. Федянин М.Ю., профессор, д.м.н., руководитель департамента науки ФГБУ "Национальный медицинский исследовательский центр онкологии им. Н.Н. Блохина" Министерства здравоохранения Российской Федерации. Руководитель службы химиотерапевтического лечения "ГБУЗ ММКЦ "Коммунарка" ДЗМ". Заведующий кафедрой онкологии ИУВ ФГБУ "НМЦХ им. Н.И. Пирогова" Министерства здравоохранения Российской Федерации
18. Трякин А.А., профессор, д.м.н., заместитель директора по научной работе, заведующий отделением противоопухолевой лекарственной терапии N 2 НИИ клинической онкологии им. акад. РАН и РАМН Н.Н. Трапезникова ФГБУ "Национальный медицинский исследовательский центр онкологии им. Н.Н. Блохина" Министерства здравоохранения Российской Федерации.
19. Владимирова Л.Ю., профессор, д.м.н., заведующая отделом лекарственного лечения опухолей, заведующая отделением противоопухолевой лекарственной терапии ФГБУ "Национальный медицинский исследовательский центр онкологии" Министерства здравоохранения Российской Федерации.
20. Петкау В.В., к.м.н., проректор по научно-исследовательской и инновационной деятельности Уральского государственного медицинского университета, Екатеринбург.
21. Зуков Р.А., профессор, д.м.н., главный врач КГБУЗ "Красноярский краевой онкологический диспансер им. А.И. Крыжановского". Заведующий кафедрой онкологии и лучевой терапии с курсом ПО ГБОУ ВПО "Красноярский государственный медицинский университет им. проф. В.Ф. Войно-Ясенецкого".
22. Покатаев И.А., д.м.н., руководитель службы химиотерапевтического лечения "Онкологический центр N 1 ГКБ им. С.С. Юдина ДЗМ".
23. Корниецкая А.Л., к.м.н., ведущий научный сотрудник отдела лекарственного лечения опухолей МНИОИ им. П.А. Герцена - филиал ФГБУ "Национальный медицинский исследовательский центр радиологии" Министерства здравоохранения Российской Федерации.
24. Варфоломеева С.Р., профессор, д.м.н., директор НИИ детской онкологии и гематологии им. акад. РАМН Л.А. Дурнова ФГБУ "Национальный медицинский исследовательский центр онкологии им. Н.Н. Блохина" Министерства здравоохранения Российской Федерации.
25. Киргизов К.И., доцент, к.м.н., заместитель директора по научной работе, и.о. заведующего отделением детской трансплантации костного мозга и гемопоэтических стволовых клеток НИИ детской онкологии и гематологии им. акад. РАМН Л.А. Дурнова ФГБУ "Национальный медицинский исследовательский центр онкологии им. Н.Н. Блохина" Министерства здравоохранения Российской Федерации
Блок Организация оказания медицинской помощи
1. Геворкян Тигран Гагикович, заместитель директора ФГБУ "НМИЦ онкологии им. Н.Н. Блохина" Минздрава России
2. Иванов Сергей Анатольевич, д.м.н., профессор РАН, директор МРНЦ им. А.Ф. Цыба - филиала ФГБУ "НМИЦ радиологии" Минздрава России
3. Невольских Алексей Алексеевич, д.м.н., заместитель директора по лечебной работе МРНЦ им. А.Ф. Цыба - филиала ФГБУ "НМИЦ радиологии" Минздрава России.
4. Хайлова Жанна Владимировна, к.м.н., заместитель директора по организационно-методической работе МРНЦ им. А.Ф. Цыба - филиал ФГБУ "НМИЦ радиологии" Минздрава России.
Конфликта интересов нет.
Приложение А2
МЕТОДОЛОГИЯ РАЗРАБОТКИ КЛИНИЧЕСКИХ РЕКОМЕНДАЦИЙ
Целевая аудитория данных клинических рекомендаций:
- врачи-онкологи;
- врачи-хирурги;
- врачи-радиологи;
- врачи-интервенционные радиологи;
- врачи-химиотерапевты;
- студенты медицинских вузов, ординаторы и аспиранты.
Методы, использованные для сбора/селекции доказательств: поиск в электронных базах данных; анализ современных научных разработок по проблеме ХЦР в РФ и за рубежом; обобщение практического опыта российских и зарубежных специалистов.
Таблица П1. Шкала оценки уровней достоверности доказательств (УДД) для методов диагностики (диагностических вмешательств).
УДД
Расшифровка
1
Систематический обзор рандомизированных клинических исследований с применением метаанализа
2
Отдельные рандомизированные клинические исследования и систематические обзоры исследования любого дизайна, за исключением рандомизированных клинических исследований, с применением метаанализа
3
Нерандомизированные сравнительные исследования, в том числе когортные исследования
4
Несравнительные исследования, описание клинического случая или серии случаев, исследования "случай - контроль"
5
Имеется лишь обоснование механизма действия вмешательства (доклинические исследования) или мнение экспертов
Таблица П2. Шкала оценки уровней достоверности доказательств (УДД) для методов профилактики, лечения и реабилитации (профилактических, лечебных реабилитационных вмешательств)
УДД
Расшифровка
1
Систематический обзор рандомизированных клинических исследований с применением метаанализа
2
Отдельные рандомизированные клинические исследования и систематические обзоры исследований любого дизайна, за исключением рандомизированных клинических исследований, с применением метаанализа.
3
Нерандомизированные сравнительные исследования, в том числе когортные исследования.
4
Несравнительные исследования, описание клинического случая или серии случаев, исследование "случай - контроль"
5
Имеется лишь обоснование механизма действия вмешательства (доклинические исследования) или мнение экспертов
Таблица П3 - Шкала оценки уровней убедительности рекомендаций (УУР) для методов профилактики, диагностики, лечения и реабилитации (профилактических, диагностических, лечебных, реабилитационных вмешательств)
УУР
Расшифровка
A
Сильная рекомендация (все рассматриваемые критерии эффективности (исходы) являются важными, все исследования имеют высокое или удовлетворительное методологическое качество, их выводы по интересующим исходам является согласованными)
B
Условная рекомендация (не все рассматриваемые критерии эффективности (исходы) являются важными, не все исследования имеют высокое или удовлетворительное методологическое качество и/или их выводы по интересующим исходам не являются согласованными)
C
Слабая рекомендация (отсутствие доказательств надлежащего качества (все рассматриваемые критерии эффективности (исходы) являются неважными, все исследования имеют низкое методологическое качество и их выводы по интересующим исходам не являются согласованными)
Методы, использованные для формулирования рекомендаций - консенсус экспертов.
Экономический анализ
Анализ стоимости не проводился и публикации по фармакоэкономике не анализировались.
Метод валидизации рекомендаций:
- внешняя экспертная оценка;
- внутренняя экспертная оценка.
Описание метода валидизации рекомендаций
Настоящие рекомендации в предварительной версии рецензированы независимыми экспертами, которых попросили прокомментировать, прежде всего, насколько интерпретация доказательств, лежащих в основе рекомендаций, доступна для понимания.
Получены комментарии со стороны врачей-онкологов первичного звена в отношении доходчивости изложения рекомендаций и их оценки важности рекомендаций как рабочего инструмента повседневной практики.
Комментарии, полученные от экспертов, тщательно систематизировались и обсуждались председателем и членами рабочей группы. Каждый пункт обсуждался, и регистрировались вносимые в результате этого изменения в рекомендации. Если же изменения не вносились, то регистрировались причины отказа от внесения изменений.
Консультации и экспертная оценка
Проект рекомендаций рецензирован также независимыми экспертами, которых попросили прокомментировать, прежде всего, доходчивость и точность интерпретации доказательной базы, лежащей в основе рекомендаций.
Для окончательной редакции и контроля качества рекомендации повторно проанализированы членами рабочей группы, которые пришли к заключению, что все замечания и комментарии экспертов приняты во внимание, риск систематических ошибок при разработке рекомендаций сведен к минимуму.
Обновления клинических рекомендаций: актуализация проводится не реже чем один раз в три года с учетом появившейся новой информации о диагностике и тактике ведения пациентов с раком желчевыводящей системы. Сформированные предложения должны учитывать результаты комплексной оценки лекарственных препаратов, медицинских изделий, а также результаты клинической апробации.
При отборе публикаций как потенциальных источников доказательств использованная в каждом исследовании методология изучается для того, чтобы убедиться в ее достоверности. Результат изучения влияет на уровень доказательств, присваиваемый публикации, что, в свою очередь, влияет на силу вытекающих из нее рекомендаций.
Приложение А3
СПРАВОЧНЫЕ МАТЕРИАЛЫ,
ВКЛЮЧАЯ СООТВЕТСТВИЕ ПОКАЗАНИЙ К ПРИМЕНЕНИЮ
И ПРОТИВОПОКАЗАНИЙ, СПОСОБОВ ПРИМЕНЕНИЯ И ДОЗ ЛЕКАРСТВЕННЫХ
ПРЕПАРАТОВ, ИНСТРУКЦИИ ПО ПРИМЕНЕНИЮ
ЛЕКАРСТВЕННОГО ПРЕПАРАТА
Нет.
Приложение Б
АЛГОРИТМЫ ДЕЙСТВИЙ ВРАЧА
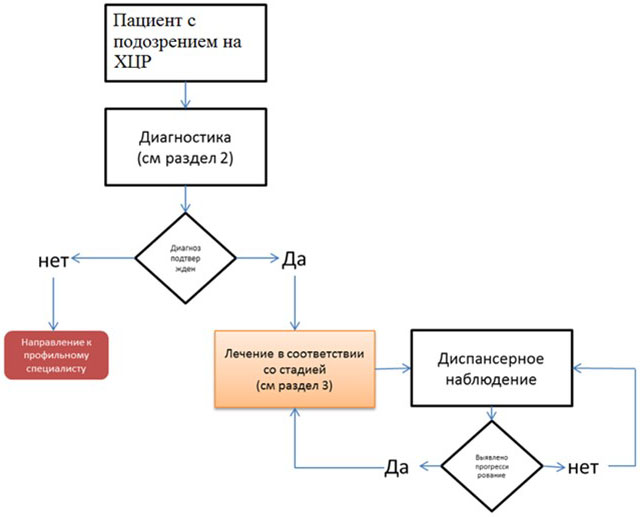
Блок-схема диагностики и лечения пациента с ХЦР
Приложение В
ИНФОРМАЦИЯ ДЛЯ ПАЦИЕНТА
- Рекомендации при осложнениях хирургического лечения - связаться с оперировавшим врачом-хирургом.
- Рекомендации при осложнениях химиотерапии - связаться с врачом-онкологом (химиотерапевтом).
При повышении температуры тела до 38 °C и выше:
- связаться с врачом-онкологом.
При стоматите:
- Диета - механическое, термическое щажение.
- Частое полоскание рта (каждый час) - ромашка, кора дуба, шалфей, смазывать полость рта облепиховым (персиковым) маслом.
- Обрабатывать полость рта по назначению врача-онколога.
При диарее:
- Диета - исключить жирное, острое, копченое, сладкое, молочное, клетчатку. Можно нежирное мясо, мучное, кисломолочное, рисовый отвар. Обильное питье.
- Принимать препараты по назначению врача-онколога.
При тошноте:
- Принимать препараты по назначению врача-онколога.
Приложение Г1 - ГN
ШКАЛЫ ОЦЕНКИ, ВОПРОСНИКИ И ДРУГИЕ ОЦЕНОЧНЫЕ ИНСТРУМЕНТЫ
СОСТОЯНИЯ ПАЦИЕНТА, ПРИВЕДЕННЫЕ В КЛИНИЧЕСКИХ РЕКОМЕНДАЦИЯХ
Приложение Г1
ШКАЛА ОЦЕНКИ ТЯЖЕСТИ СОСТОЯНИЯ ПАЦИЕНТА ПО ВЕРСИИ ВОЗ/ECOG
Название на русском языке: Шкала оценки тяжести состояния пациента по версии ВОЗ/ECOG
Оригинальноеназвание: The Eastern Cooperative Oncology Group/World Health Organization Performance Status (ECOG/WHO PS)
Источник (официальный сайт разработчиков, публикация с валидацией): https://ecog-acrin.org/resources/ecog-performance-status
Oken MM, Creech RH, Tormey DC, Horton J, Davis TE, McFadden ET, Carbone PP: Toxicity and response criteria of the Eastern Cooperative Oncology Group. Am J Clin Oncol 1982, 5(6): 649 - 655
Тип: шкала оценки
Назначение: описать уровень функционирования пациента с точки зрения его способности заботиться о себе, повседневной активности и физических способностях (ходьба, работа и т.д.).
Содержание:
Балл
Описание
0
Пациент полностью активен, способен выполнять все, как и до заболевания (90 - 100% по шкале Карновского)
1
Пациент неспособен выполнять тяжелую, но может выполнять легкую или сидячую работу (например, легкую домашнюю или канцелярскую работу, 70 - 80% по шкале Карновского)
2
Пациент лечится амбулаторно, способен к самообслуживанию, но не может выполнять работу. Более 50% времени бодрствования проводит активно - в вертикальном положении (50 - 60% по шкале Карновского)
3
Пациент способен лишь к ограниченному самообслуживанию, проводит в кресле или постели более 50% времени бодрствования (30 - 40% по шкале Карновского)
4
Инвалид, совершенно не способен к самообслуживанию, прикован к креслу или постели (10 - 20% по шкале Карновского)
5
Смерть
Ключ (интерпретация): приведен в самой шкале.
