"Клинические рекомендации "Рак вульвы"
МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ
КЛИНИЧЕСКИЕ РЕКОМЕНДАЦИИ
РАК ВУЛЬВЫ
Кодирование по Международной статистической классификации болезней и проблем, связанных со здоровьем: C51, D07.1
Год утверждения (частота пересмотра): 2024
Возрастная категория: Взрослые
Пересмотр не позднее: 2026
ID: 501
Разработчик клинической рекомендации
- Ассоциация онкологов России
- Общероссийская общественная организация "Российское общество клинической онкологии"
- Общероссийская общественная организация "Российское общество специалистов по профилактике и лечению опухолей репродуктивной системы"
Одобрено Научно-практическим Советом Минздрава РФ
Список сокращений
CTV - clinical target volume (клинический объем мишени)
ECOG - Eastern Cooperative Oncology Group (Восточная объединенная группа онкологов)
FIGO - Международная федерация гинекологов и акушеров
GTV - непосредственный опухолевый объем (макроскопически визуализируемый)
HSIL - поражение плоского эпителия тяжелой степени
IMRT - лучевая терапия с модулированной интенсивностью
LSIL - поражение плоского эпителия легкой степени
PTV - планируемый опухолевый объем
SCC - антиген плоскоклеточного рака
TNM - Международная классификация стадий злокачественных новообразований
VIN - интраэпителиальная неоплазия вульвы
в/в - внутривенно
в/м - внутримышечно
ВОЗ - всемирная организация здравоохранения
ВПЧ - вирус папилломы человека
Гр - грей
ЕД - единицы
КТ - компьютерная томография
ЛТ - лучевая терапия
ЛФК - лечебная физкультура
МРТ - магнитно-резонансная томография
ПЭТ - позитронно-эмиссионная томография
РВ - рак вульвы
РОД - разовая очаговая доза
СОД - суммарная очаговая доза
УЗИ - ультразвуковое исследование
ХТ - химиотерапия
ЭКГ - электрокардиография
Термины и определения
Предреабилитация (prehabilitation) - реабилитация с момента постановки диагноза до начала лечения (хирургического лечения/химиотерапии/лучевой терапии).
I этап реабилитации - реабилитация в период специализированного лечения основного заболевания (включая хирургическое лечение/химиотерапию/лучевую терапию) в отделениях медицинских организаций по профилю основного заболевания.
II этап реабилитации - реабилитация в стационарных условиях медицинских организаций (реабилитационных центров, отделений реабилитации), в ранний восстановительный период течения заболевания, поздний реабилитационный период, период остаточных явлений заболевания.
III этап реабилитации - реабилитация в ранний и поздний реабилитационный периоды, период остаточных явлений заболевания в отделениях (кабинетах) реабилитации, физиотерапии, лечебной физкультуры, рефлексотерапии, мануальной терапии, психотерапии, медицинской психологии, кабинетах логопеда (учителя-дефектолога), оказывающих медицинскую помощь в амбулаторных условиях, дневных стационарах, а также выездными бригадами на дому (в том числе в условиях санаторно-курортных организаций).
Широкое иссечение опухоли выполняется в пределах здоровых тканей, при этом линия разреза должна проходить не менее чем в 1 см от визуально определяемого края опухоли по всей ее окружности.
Вульвэктомия выполняется из лаврообразного разреза, окаймляющего снаружи вульву таким образом, что верхняя точка разреза находится на 1,5 - 2,0 см выше клитора, нижняя - на таком же расстоянии от задней спайки вульвы. Иссекаются кожа и слизистая оболочка вульвы, а также 1,0 - 1,5 см подлежащей жировой клетчатки.
Расширенная вульвэктомия выполняется из 3-х не соединяющихся между собой разрезов (один из вариантов). Послеоперационный материал состоит из 3-х отдельно удаленных блоков тканей - вульвы и 2-х кожно-жировых лоскутов, последовательно иссеченных из пахово-бедренных областей.
1. Краткая информация по заболеванию или состоянию (группы заболеваний или состояний)
1.1 Определение заболевания или состояния (группы заболеваний или состояний)
Рак вульвы (РВ) - злокачественное новообразование, возникающее из покровного плоского эпителия наружных половых органов женщины [1].
1.2 Этиология и патогенез заболевания или состояния (группы заболеваний или состояний)
В этиологии и патогенезе РВ ведущую роль играют 2 фактора: возрастные инволютивно-атрофические процессы наружных половых органов и инфицирование вирусом папилломы человека (ВПЧ). С наибольшей частотой обнаруживаются 6-й и 11-й генотипы ВПЧ, причем, как правило, эти 2 серотипа выявляются одновременно. Часто определяется ассоциация 18-го генотипа с 55, 59, 83-м, а также различные сочетания 31, 33 и 45-го генотипов. Генотип 16 в большинстве случаев встречается изолированно. В целом присутствие ВПЧ при РВ устанавливается в 75 - 85% наблюдений [2]. Немалое значение имеет часто диагностируемый у пациенток с РВ метаболический синдром.
К РВ ведет следующая патогенетическая цепь событий: возрастная инволюция кожи и слизистых оболочек (на фоне абсолютного дефицита эстрадиола, а также резкого снижения уровня стероидных рецепторов) -> развитие инволютивно-атрофических процессов -> изменение микробиоценоза вульвы (развитие условно-патогенной и патогенной микрофлоры) -> формирование хронических воспалительных и дистрофических изменений, появление травм и трещин -> хронические регенеративно-пролиферативные процессы -> присутствие ВПЧ -> развитие дисплазии -> прогрессирование дисплазии в преинвазивный и инвазивный рак [2]. Это в определенной мере объясняет тот факт, что РВ возникает у женщин относительно пожилого возраста [3].
В 90% наблюдений морфологически верифицируется плоскоклеточный рак - злокачественное новообразование, возникающее из покровного плоского эпителия наружных половых органов женщины [4].
1.3 Эпидемиология заболевания или состояния (группы заболеваний или состояний)
Первичный РВ - редко встречающаяся опухоль. РВ составляет 1% всех случаев рака у женщин. В структуре заболеваемости злокачественными новообразованиями женских половых органов доля первичного РВ составляет около 2 - 5% [5]. В 2021 г. заболеваемость РВ в России составила 2,57 случая на 100 тыс. женщин, что в абсолютных цифрах составило 2011 случаев [7].
1.4 Особенности кодирования заболевания или состояния (группы заболеваний или состояний) по Международной статистической классификации болезней и проблем, связанных со здоровьем
D07.1 - Карцинома in situ <*> вульвы
--------------------------------
<*> - Многие новообразования in situ рассматриваются как последовательные морфологические изменения между дисплазией и инвазивным раком. Например, для вульварной интраэпителиальной неоплазии (VIN) признаются три степени, из которых третья (VIN III) включает как выраженную дисплазию, так и карциному in situ. Эта система градаций распространена и на другие органы, например шейку матки и влагалище. Описание интраэпителиальной неоплазии III степени с указанием или без указания на тяжелую дисплазию представлены в данном разделе "карцинома in situ"; интраэпителиальной неоплазии I и II классифицируются как дисплазии вовлеченных систем органов и должны кодироваться по МКБ классам, соответствующим этим системам органов.
C51.0 - Злокачественное новообразование большой срамной губы
C51.1 - Злокачественное новообразование малой срамной губы
C51.2 - Злокачественное новообразование клитора
C51.8 - Злокачественное новообразование вульвы, выходящее за пределы одной и более вышеуказанных локализаций
C51.9 - Злокачественное новообразование вульвы неуточненной части
1.5 Классификация заболевания или состояния (группы заболеваний или состояний)
1.5.1. Международная морфологическая классификация РВ (классификация IARC, 5-е издание, Лион, 2020) [6]
ЭПИТЕЛИАЛЬНЫЕ ОПУХОЛИ
Опухоли из плоского эпителия и предрак
Вульварная интраэпителиальная неоплазия, ассоциированная с ВПЧ
Вульварная интраэпителиальная неоплазия, ВПЧ-независимая
Плоскоклеточная карцинома вульвы, ВПЧ-ассоциированная
Плоскоклеточная карцинома вульвы, ВПЧ-независимая
Плоскоклеточная карцинома вульвы без уточнения ВПЧ статуса
Базальноклеточная карцинома
Опухоли из железистого эпителия
Поражения желез маммарного типа
Филлоидная опухоль (злокачественная)
Аденокарцинома маммарного типа
Поражение бартолиневых желез
Аденокарцинома бартолиневой железы
Аденокарцинома других типов
Болезнь Педжета
Карцинома потовых желез
Аденокарцинома кишечного типа
ГЕРМИНОГЕННЫЕ ОПУХОЛИ
Герминогенные опухоли вульвы
Несмотря на то, что из международной гистологической классификации рака вульвы ВОЗ, 5-е издание, Лион, 2020 исключены меланоцитарные опухоли, учитывая их частоту встречаемости (5 - 10%) и клиническую значимость, решение о тактике лечения должно приниматься мультидисциплинарным консилиумом с участием онкогинеколога [62].
Стадирование плоскоклеточного РВ проводится по 2 классификациям: TNM (8-е издание, 2017) и FIGO (2009) (см. таблицу). Применяется только для первичного РВ. Должно быть гистологическое (патолого-анатомическое) подтверждение диагноза. Опухоль, распространяющаяся на влагалище, должна быть классифицирована как РВ.
1.5.2. Международная клиническая классификация рака вульвы в соответствии с критериями TNM 8 (2017) и комитета FIGO (2009)
TNM
FIGO
Распространение
TX
Недостаточно данных для оценки первичной опухоли
T0
Первичная опухоль не определяется
Tis
<*>
Карцинома in situ (преинвазивный рак)
T1
I
Опухоль ограничена вульвой и/или промежностью
T1a
IA
Опухоль <= 2 см в наибольшем измерении с глубиной инвазии стромы <= 1 мм
T1b
IB
Опухоль > 2 см в наибольшем измерении или с глубиной инвазии стромы > 1 мм
T2
II
Опухоль любого размера, распространяющаяся на нижнюю треть уретры и/или влагалища или анальное кольцо
T3
IVA
Опухоль любого размера, распространяющаяся на любую из следующих структур: на слизистую оболочку верхних двух третей мочеиспускательного канала, и/или мочевого пузыря, и/или прямой кишки, и/или опухоль фиксирована к костям таза
N1a
IIIA
1 - 2 метастатически измененных регионарных лимфатических узла < 5 мм в наибольшем измерении
N1b
IIIA
1 метастатически измененный регионарный лимфатический узел >= 5 мм в наибольшем измерении
N2a
IIIB
3 или более метастатически измененных регионарных лимфатических узла < 5 мм в наибольшем измерении
N2b
IIIB
2 или более метастатически измененных регионарных лимфатических узла >= 5 мм в наибольшем измерении
N2c
IIIC
Экстракапсулярное метастатическое поражение регионарных лимфатических узлов
N3
IVA
Неподвижные, изъязвленные метастатически измененные регионарные лимфатические узлы
M1
IVB
Отдаленные метастазы, включая метастазы в тазовых лимфатических узлах
--------------------------------
<*> В данной классификации стадия 0 (карцинома in situ) была удалена, поскольку это преинвазивное образование.
N - регионарные лимфатические узлы
Nx - регионарные лимфатические узлы не могут быть оценены
N0 - нет метастазов в регионарных лимфатических узлах
N1-3 - есть метастаз в регионарном лимфатическом узле
M - отдаленные метастазы
M0 - нет отдаленных метастазов
M1 - есть отдаленный метастаз
G - гистологическая степень злокачественности опухоли
Gx - степень дифференцировки опухоли не может быть определена
G1 - высокодифференцированная опухоль
G2 - умеренно-дифференцированная опухоль
G3 - низкодифференцированная или недифференцированная опухоль
Примечание. N - регионарные лимфатические узлы. Регионарными считают паховые и бедренные лимфатические узлы. Поражение тазовых лимфатических узлов (наружных и внутренних подвздошных, обтураторных и общих подвздошных) расценивают как отдаленные метастазы.
1.6 Клиническая картина заболевания или состояния (группы заболеваний или состояний)
Наиболее частые симптомы РВ - раздражение или постоянный и усиливающийся зуд вульвы, наличие опухоли в виде бородавки и/или ссадины ярко-розового, красного или белого цвета, болезненной язвы, не заживающей более 1 мес., боли в области вульвы, носящие длительный рецидивирующий и упорный характер, болезненное мочеиспускание. Участок вульвы может казаться бледным и негладким на ощупь. Реже первыми проявлениями заболевания бывают кровянистые или гнойные выделения, увеличение паховых лимфатических узлов.
2. Диагностика заболевания или состояния (группы заболеваний или состояний) медицинские показания и противопоказания к применению методов диагностики
Критерии установления диагноза заболевания или состояния производится на основании:
1) анамнестических данных;
2) физикального обследования, включающего тщательный гинекологический осмотр;
3) цитологического исследования биоптатов увеличенных или подозрительных лимфоузлов;
4) патолого-анатомического исследования биопсийного (операционного) материала вульвы, лимфоузлов;
5) инструментально-лучевого обследования, включающего комплексное ультразвуковое исследование органов малого таза (трансвагинальное и трансабдоминальное), ультразвуковое исследование лимфатических узлов: регионарных - паховых и бедренных лимфатических узлов и отдаленных лимфоузлов - наружных и внутренних подвздошных, обтураторных и общих подвздошных лимфоузлов. По показаниям - магнитно-резонансную томографию органов малого таза, мягких тканей промежности с внутривенным контрастированием или без него (при наличии противопоказаний) и др. и/или компьютерную (КТ) томографию органов грудной полости, органов брюшной полости, почек, забрюшинного пространства с внутривенным контрастированием или без него, а при наличии противопоказаний к МРТ - КТ органов малого таза, мягких тканей промежности с в\в контрастированием или без него; при подозрении на отдаленное метастазирование - позитронную эмиссионную томографию совмещенную с компьютерной томографией всего тела с туморотропными РФП (A07.30.043 Позитронная эмиссионная томография совмещенная с компьютерной томографией с туморотропными РФП) (см. Ниже раздел 2.4).
2.1 Жалобы и анамнез
Основной жалобой пациенток является зуд вульвы. В 30% наблюдений заболевание протекает бессимптомно. Для пациентов РВ также типичны жалобы на жжение, боли в зоне промежности, бели, кровянистые и гноевидные выделения. Из анатомических областей наиболее часто поражаются большие половые губы (52%), клитор (12 - 20%), реже - малые половые губы (7,1%), периуретральная зона (1,7%) [4].
2.2 Физикальное обследование
- Всем пациенткам с РВ и подозрением на РВ рекомендуется проводить в процессе первичного осмотра (приема, консультации) врача-онколога и/или врача акушера-гинеколога тщательное физикальное обследование, включающее в т.ч. визуальный осмотр наружных половых органов, вагинальный осмотр шейки матки и стенок влагалища в зеркалах, бимануальное влагалищное исследование, трансректальное пальцевое (ректовагинальное) исследование, пальпацию регионарных (паховых и бедренных) лимфатических узлов с целью верификации диагноза, определения тактики и алгоритма лечения, оценки прогноза заболевания [4].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 5)
Комментарии: Проводя визуальный осмотр наружных половых органов необходимо конкретизировать локализацию опухоли в анатомической области, указать распространение и размер опухоли, наличие инфильтрации окружающих тканей. При вагинальном осмотре шейки матки, стенок влагалища в зеркалах предпочтительнее использовать влагалищные ложкообразные зеркала по Симсу (02.20.001 Осмотр шейки матки в зеркалах), поскольку при использовании влагалищных двухстворчатых зеркал по Куско некоторые зоны влагалища (передняя и задняя стенки) плохо просматриваются, проводится. При пальпациии лимфоузлов особое внимание следует обращать на паховые и бедренные лимфоузлы, которые относят к регионарным лимфатическим узлам при ЗНО вульвы.
В медицинской документации уточняют:
- локализацию опухоли (анатомическую область - большие\малые половые губы\бартолиниевая железа\клитор\промежность);
- распространение опухолевого процесса (одностороннее\двухстороннее поражение\ближайшее расстояние до средней линии\уретры\влагалища, заднего прохода); - размер опухолевого очага, при наличии нескольких очагов - указывается размер каждого; - мобильность опухоли\наличие инфильтрации окружающих тканей.
- могут быть приложены фотографии или клинический рисунок
2.3 Лабораторные диагностические исследования
- Всем пациенткам с РВ и подозрением на РВ рекомендуется неспецифическая лабораторная диагностика, которая включает общий (клинический) анализ крови, анализ крови биохимический общетерапевтический, коагулограмму (ориентировочное исследование системы гемостаза), общий (клинический) анализ мочи в целях оценки их общего состояния, определения тактики и алгоритма лечения, оценки прогноза заболевания. Возможно исследование уровня антигена плоскоклеточной карциномы (SCC) в крови с целью последующего мониторинга плоскоклеточного РВ [4].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 5)
Комментарий: пациенткам с РВ и подозрением на РВ возможно проведение молекулярно-биологического исследования влагалищного отделяемого на вирус папилломы человека (Papilloma virus) (исследования отделяемого из влагалища на наличие ВПЧ онкогенных типов методом ПЦР) с целью выявления этиологических факторов развития заболевания [2, 3]
2.4 Инструментальные диагностические исследования
Для верификации диагноза используются цитологические, иммуноцитохимические, гистологические, иммуногистохимические методы. Биопсия опухоли, опухолеподобных образований мягких тканей промежности и патолого-анатомическое исследование биопсийного (операционного) материала - главный диагностический метод при РВ.
- Всем пациенткам с РВ и подозрением на РВ рекомендуется получение соскоба с вульвы; мазка-отпечатка с поверхности кожи; патолого-анатомическое исследование биопсийного (операционного) материала вульвы; выполнение пункции лимфатического узла; цитологическое исследование биоптатов лимфоузлов; патолого-анатомическое исследование биопсийного (операционного) материала лимфоузла с целью морфологической верификации [2, 6, 7].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 5)
Комментарий: для исключения первично-множественных злокачественных новообразований, вторичного поражения и диссеминации опухоли рекомендуется взятие мазков с шейки матки и цервикального канала (получение цервикального мазка) и проведение аспирационной биопсии тканей матки (эндометрия) с цитологическим и последующим патолого-анатомическим исследованиями [8].
- Рекомендуется выполнение вульвоскопии, вагиноскопии и кольпоскопии всем пациенткам с РВ и подозрением на РВ для верификации диагноза и диагностики сопутствующей патологии [8, 9].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 5)
Комментарий: вульвоскопия - наиболее простой метод визуализации опухолевого образования.
- Рекомендуется всем пациенткам с РВ и с подозрением на РВ выполнять ультразвуковое исследование (УЗИ) органов малого таза комплексное (трансвагинальное и трансабдоминальное), УЗИ органов брюшной полости (комплексное), УЗИ лимфатических узлов (пахово-бедренных, забрюшинных - подвздошных и парааортальных) для оценки распространенности опухолевого процесса [8, 9].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 5)
Комментарий: УЗИ является наиболее доступным методом визуализации, для оценки распространенности опухолевого процесса в брюшной полости, полости малого таза, а также в регионарных и отдаленных ЛУ.
- Рекомендуется выполнить цистоскопию и ректороманоскопию всем пациенткам с распространенными стадиями РВ с целью выявления инвазии опухоли в мочевой пузырь и прямую кишку [8, 9].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 5)
- Рекомендуется всем пациенткам с РВ выполнять КТ органов грудной полости с целью оценки распространенности опухолевого процесса [63].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 5)
Комментарий: При невозможности проведения КТ органов грудной полости выполняется прицельная рентгенография органов грудной клетки.
КТ органов грудной полости обладает более высокой диагностической эффективностью, по сравнению с рентгенографией, в выявлении метастатического поражения легких, плевры и внутригрудных ЛУ [9, 63].
- Рекомендуется всем пациенткам с РВ выполнять магнитно-резонансную томографию (МРТ) органов малого таза с внутривенным контрастированием и МРТ мягких тканей промежности с контрастированием с целью оценки местной распространенности и статуса регионарных ЛУ [63, 64, 65].
Уровень убедительности рекомендаций - B (уровень достоверности доказательств - 2)
Комментарий: При невозможности проведения МРТ и/или при наличии противопоказаний к нему показано проведение КТ органов малого таза у женщин с контрастированием.
МРТ в оценке органов малого таза, тканей тазового дна и промежности обладает более высокой диагностической информативностью по сравнению с КТ [63, 66, 67, 68]
- Рекомендуется пациенткам с РВ, при стадиях > T1b (IB, FIGO) для оценки статуса регионарных лимфатических узлов и диагностики отдаленных метастазов, позитронно-эмиссионная томография, совмещенная с компьютерной томографией с туморотропным РФП (ПЭТ-КТ) или КТ органов грудной и брюшной полостей с внутривенным болюсным контрастированием [63, 66, 67, 68, 69, 70].
Уровень убедительности рекомендаций - B (уровень достоверности доказательств - 1)
Комментарий: ПЭТ-КТ предпочтительнее в случае планирования хирургического лечения или лучевой терапии, в том числе после неоадьювантной терапии, при размере опухоли более 2 см [70, 71, 72].
- Рекомендуется пациенткам с метастатическим РВ, при клиническом подозрении на метастатическое поражение костей, проведение сцинтиграфии костей всего тела (остеосцинтиграфии), в случае невозможности выполнения ПЭТ-КТ [9, 73].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 5)
- Рекомендуется пациенткам с РВ, при подозрении на метастатическое поражение головного мозга выполнять МРТ головного мозга с контрастированием [12, 69, 74].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 5)
Комментарий: при невозможности проведения МРТ и/или при наличии противопоказаний возможно выполнение КТ головного мозга с внутривенным контрастированием. МРТ с контрастированием в диагностике метастатического поражения головного мозга обладает более высокой диагностической эффективностью, по сравнению с КТ [74, 75].
- Пациенткам с РВ при подготовке к хирургическому лечению или лучевой терапии рекомендовано в целях оценки общего состояния и их функционального статуса, по показаниям проводить дополнительное обследование: эхокардиографию, с учетом данных ЭКГ, холтеровское мониторирование сердечного ритма, исследование неспровоцированных дыхательных объемов и потоков, дуплексное сканирование экстракраниальных отделов брахиоцефальных артерий, ультразвуковая допплерография сосудов (артерий и вен) нижних конечностей, первичный и вторичный прием (осмотр, консультация) врача-кардиолога, врача-эндокринолога, врача-невролога и др. с учетом наличия сопутствующих заболеваний [9].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 5)
- Для планирования ЛТ как метод выбора рекомендована МРТ органов малого таза с внутривенным контрастированием, позволяющая наиболее информативно оценить местную распространенность опухоли и статус регионарных лимфатических узлов [76].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 5)
Комментарий: при невозможности выполнить МРТ, для планирования ЛТ возможно использование КТ органов малого таза у женщин с контрастированием. КТ без контрастного усиления для визуализации РВ не информативно [63]. Желательно рассмотреть возможность выполнения ПЭТ-КТ для более точного планирования ЛТ [77].
2.5 Иные диагностические исследования
- Рекомендуется проводить патолого-анатомическое исследование биопсийного (операционного) материала вульвы всем пациенткам с РВ и подозрением на РВ с целью верификации диагноза, при этом в заключении рекомендуется отразить следующие параметры:
1) размер и распространенность первичной опухоли;
2) глубину инвазии первичной опухоли;
3) гистологическое строение опухоли;
4) степень дифференцировки опухоли;
5) наличие периваскулярной, перилимфатической, периневральной инвазии (отрицательный результат также должен быть констатирован);
6) исследование лимфатических узлов должно включать статус регионарных лимфатических узлов (pN) с указанием общего числа исследованных и пораженных лимфатических узлов, размер наибольшего метастаза, признаков экстранодального распространения опухоли (ENE+/-);
7) микроскопическую оценку краев резекции (статус) R0-1 с указанием расстояния до ближайшего края резекции в мм;
8) степень лечебного патоморфоза в случае предоперационной терапии. [8, 10, 12].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 5)
Комментарий:
- при сомнительных или отрицательных результатах первичной биопсии новообразования вульвы по результатам патолого-анатомического исследования пациенткам с подозрением на РВ показано проведение или повторной биопсии, или, при возможности, хирургического вмешательства с патолого-анатомическим исследованием биопсийного (операционного) материала;
- при необходимости морфологической верификации диагноза РВ патолого-анатомическое исследование биопсийного (операционного) материала может дополняться иммуногистохимическим типированием - целесообразно патолого-анатомическое исследование биопсийного (операционного) материала с применением иммуногистохимических методов.
- Рекомендуется у всех пациенток с РВ установить стадию заболевания в соответствии с международными классификациями TNM и FIGO с целью определения тактики и алгоритма лечения, оценки прогноза заболевания (см. п 1.5.2) [12].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 5)
3. Лечение, включая медикаментозную и немедикаментозную терапии, диетотерапию, обезболивание, медицинские показания и противопоказания к применению методов лечения
Назначение и применение лекарственных препаратов, указанных в клинической рекомендации, направлено на обеспечение пациента клинически эффективной и безопасной медицинской помощью, в связи с чем их назначение и применение в конкретной клинической ситуации определяется в соответствии с инструкциями по применению конкретных лекарственных препаратов с реализацией представленных в инструкции мер предосторожности при их применении, также возможна коррекция доз с учетом состояния пациента. Лечение следует проводить в специализированной клинике, располагающей современными возможностями диагностики и опытом успешного лечения этой категории больных. Тактика лечения должна быть определена на мультидисциплинарном консилиуме.
- Рекомендуется рассматривать хирургическое вмешательство как основной метод радикального лечения пациентов с плоскоклеточным РВ [8].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 5)
Комментарий: по показаниям дополнительно проводятся адъювантная лучевая или химиолучевая терапия. Лучевая терапия (и как самостоятельный метод лечения, и в сочетании с химиотерапией) назначается при противопоказаниях к хирургическому лечению. Индивидуальный подход (сочетание лучевых, лекарственных и хирургических методик) - при IV стадии и рецидивах заболевания [8, 10 - 13, 14].
3.1. Общие принципы лечения в зависимости от стадии
3.1.1. Лечение рака вульвы TisN0M0
- Рекомендуется у молодых пациенток с РВ TisN0M0 выполнять широкое локальное иссечение новообразования мягких тканей вульвы на расстоянии 1 см от края поражения. Меньшее расстояние до латерального края резекции допустимо в случае близкого расположения опухоли к срединным структурам (уретре, анальному кольцу). Во всех других ситуациях целесообразно выполнение вульвэктомии [12]
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 5)
3.1.2. Лечение рака вульвы Ia стадии (T1aN0M0)
- Всем пациенткам с РВ Ia стадии (T1aN0M0) рекомендуется хирургическое лечение. Лучевое лечение в самостоятельном варианте проводится при общих соматических противопоказаниях к хирургическому лечению или отказе пациента от хирургического лечения. У пациенток при микроинвазивном РВ с диаметром опухоли <= 2 см и стромальной инвазией <= 1 мм возможно широкое локальное иссечение без пахово-бедренной лимфаденэктомии при отсутствии тяжелой диффузной дистрофии вульвы. У всех остальных пациенток необходимо выполнение вульвэктомии без пахово-бедренной лимфаденэктомии [12].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 5)
Комментарий: клинически линия разреза должна проходить на расстоянии не менее 1 см от визуально определяемого края опухоли по всей ее окружности. Вульвэктомия без пахово-бедренной лимфаденэктомии выполняется при мультифокальном поражении, при опухоли на фоне дистрофических изменений всей поверхности вульвы.
3.1.3. Лечение рака вульвы Ib стадии (TIbN0M0)
Хирургическое лечение
- Всем пациенткам с РВ Ib стадии (TIbN0M0) при латеральном поражении вульвы (>= 2 см от средней линии) рекомендуется выполнение вульвэктомии с двухсторонней подвздошно-пахово-бедренной лимфаденэктомией (радикальная вульвэктомия). При латеральном расположении опухоли в 2 - 4 см от средней линии рекомендуется вульвэктомия с определением сторожевых лимфатических узлов, по показаниям лимфаденэктомия [12].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 5)
Комментарии: клинически линия разреза должна проходить на расстоянии >= 1 см (но < 2 см) от визуально определяемого края опухоли по всей ее окружности.
- Всем пациенткам с РВ Ib стадии (TIbN0M0) при центральном поражении вульвы (переднем или заднем, в пределах 2 см от средней линии) рекомендуется выполнение вульвэктомии с двусторонней подвздошно-пахово-бедренной лимфаденэктомией (при обнаружении метастазов рекомендуются адъювантная химиолучевая терапия или лимфаденэктомия пахово-бедренная двусторонняя с последующей химиолучевой терапией) [12].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 5)
Комментарии: клинически линия разреза должна проходить на расстоянии >= 1 см (но < 2 см) от визуально определяемого края опухоли по всей ее окружности.
- Пациенткам с РВ Ib стадии (TIbN0M0) при размере опухоли вульвы <= 4 см рекомендовано выполнение вульвэктомии с двусторонней подвздошно-пахово-бедренной лимфаденэктомией или биопсией сторожевых лимфатических узлов (при обнаружении метастазов рекомендуется лимфаденэктомия пахово-бедренная двусторонняя с последующим химиолучевым лечением) [12].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 5)
Комментарии:
- клинически линия разреза должна проходить на расстоянии >= 1 см (но < 2 см) от визуально и пальпаторно определяемого края опухоли по всей ее окружности;
- послеоперационная лучевая (облучение вульвы) или химиолучевая терапия рассматривается при условии гистологического обнаружения признаков опухоли в краях резекции при линии разреза на расстоянии < 1 см от опухоли, лимфоваскулярного распространения, стромальной инвазии опухоли > 5 мм;
- для пациенток, у которых невозможно проведение хирургического вмешательства из-за сопутствующих заболеваний или распространенности процесса, альтернативный метод лечения - лучевая терапия по радикальной программе [13, 15, 16];
- Всем пациенткам с РВ Ib стадии (TIbN0M0) при размере опухоли >= 4 см рекомендован основной метод лечения - хирургический (вульвэктомия с двухсторонней подвздошно-пахово-бедренной лимфаденэктомией и возможной пластикой перемещенным кожно-фасциальным лоскутом (аутотрансплантация свободного лоскута с формированием сосудистых анастамозов) [12].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 5)
- Пациенткам с РВ Ib стадии (TIbN0M0) при сомнительной резектабельности опухоли рекомендуется неоадъювантная химиотерапия с последующей вульвэктомией с пахово-бедренной лимфаденэктомией (радикальной вульвэктомией). При неэффективной неоадъювантной химиотерапии и сомнительной резектабельности - химиолучевая терапия [12].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 5)
Комментарии: для пациенток, у которых невозможно проведение хирургического вмешательства из-за сопутствующих заболеваний или распространенности процесса, альтернативный метод лечения - лучевая терапия по радикальной программе [15, 16].
3.1.4. Лечение рака вульвы II стадии (TIIN0M0)
- Пациенткам с РВ II стадии (T2N0M0) рекомендована радикальная химиолучевая терапия. При минимальном распространении опухоли на нижнюю треть уретры и/или влагалища рекомендовано выполнение комбинированного вида хирургического вмешательства с дистальной уретроэктомией (резекцией уретры) и/или дистальной вагинэктомией (локальное иссечение влагалища) и последующей адъювантной лучевой терапией [8, 12].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 5)
Комментарии:
- лучевое лечение в самостоятельном варианте проводят при противопоказаниях к хирургическому лечению или отказе пациента от хирургического лечения;
- при распространении опухоли на анальное кольцо рекомендуется лечение как при IV стадии;
3.1.5 Лечение рака вульвы III стадии (T1-2N1a-bM0, T1-2N2a-bM0)
- Пациенткам с РВ III стадии (T1-2N1a-bM0, T1-2N2a-bM0) при резектабельных опухолях рекомендованы ниже следующие варианты лечения: операция + адъювантное химиолучевое лечение или операция + адъювантное лучевое лечение (при наличии противопоказаний к химиотерапии, отказе пациентки от химиотерапии) [12].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 5)
- Пациенткам с РВ III стадии (T1-2N1a-bM0, T1-2N2a-bM0) при нерезектабельных опухолях рекомендовано химиолучевое лечение по радикальной программе или лучевая терапия по радикальной программе (при наличии противопоказаний к химиотерапии, отказе пациентки от химиотерапии) [15, 16, 21].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 4)
- Пациенткам с РВ III стадии (T1-2N1a-bM0, T1-2N2a-bM0) возможно рекомендовать проведение неоадъювантной химиотерапии при перспективе последующего выполнения радикального хирургического лечения [21].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 4)
- Пациенткам с РВ III стадии (T1-2N1a-bM0, T1-2N2a-bM0) лучевое лечение в самостоятельном варианте рекомендовано при общих соматических противопоказаниях к хирургическому лечению, химиотерапии или отказе пациента от хирургического лечения, химиотерапии [12].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 5)
Комментарии:
- при распространении опухоли на нижнюю треть уретры и/или влагалища рекомендуется выполнение комбинированного хирургического вмешательства радикальной вульвэктомии, лимфаденэктомии пахово-бедренной двухсторонней с дистальной уретерэктомией (резекцией уретры) и/или дистальной вагинэктомией (локальное иссечение влагалища), послеоперационной химиолучевой терапии;
- при распространении опухоли на анальное кольцо рекомендуется такое же лечение, как при IV стадии;
- послеоперационная (на регионарные и наружные подвздошные лимфатические узлы) лучевая или химиолучевая терапия рассматривается в следующих случаях: при макроскопических метастазах в регионарных лимфатических узлах; при наличии > 2 микроскопических метастазов в регионарных лимфатических узлах, прорастании капсулы лимфоузла [8].
3.1.6 Лечение рака вульвы IV стадии
Каждый клинический случай должен быть обсужден на мультидисциплинарном консилиуме для определения оптимального метода и возможности лечения.
- Всем пациенткам с РВ IVA стадии (T1-2N3M0, T3N0-3M0) рекомендовано химиолучевое лечение [8, 9, 12].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 5)
Комментарий: В случаях персистенции первичного опухолевого процесса (неустойчивой стабилизации или локальном прогрессировании в ходе лучевого лечения на СОДэкв 40 Гр), зафиксированной по данным физикального и визуального осмотра, УЗИ органов малого таза комплексного (трансвагинального и трансабдоминального), вопрос о дальнейшей тактике лечения рассматривается на онкологическом консилиуме. В отдельных случаях возможно выполнение расширенных и комбинированных хирургических вмешательств, включая различные варианты эвисцерации малого таза, курсов консолидирующей химиотерапии [8, 9, 12].
- Всем пациенткам с РВ IVB стадии (T1-3N0-3M1) (отдаленные метастазы) рекомендуется проведение химиотерапии или лучевого лечения по индивидуальной программе [8, 12].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 5)
Комментарий: курс химиолучевой терапии следует начинать не позднее 28-го дня с момента выявления метастатической болезни или циторедуктивной операции при наличии метастазов (при отсутствии послеоперационных осложнений) [8, 12].
- Всем пациенткам с рецидивами плоскоклеточного РВ рекомендуется лечение по индивидуальной программе (хирургическое вмешательство любого объема с добавлением или без добавления лучевой терапии и платиносодержащей сенсибилизирующей химиотерапии при локальных рецидивах, или химиолучевое лечение с добавлением или без добавления оперативного лечения, или паллиативное лечение с химиотерапией) [12].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 5)
Комментарии:
- у пациентов с операбельным поражением подвздошных лимфатических узлов возможно проведение подвздошной двусторонней лимфаденэктомии с последующей химиолучевой терапией [12].
- особого внимания при проведении паллиативной терапии требует оценка состояния тяжести пациента по версии ВОЗ/ECOG и/или шкале Карновского (см. Приложение Г1 - 2).
3.2. Лучевая терапия
Общие принципы:
Лучевая терапия рекомендована как часть комбинированного лечения в качестве адъювантной терапии после хирургического лечения; как самостоятельный вид терапии при местнораспространенном опухолевом процессе; в качестве паллиативной помощи при рецидиве/метастазах. Использование конформной дистанционной лучевой терапии, основанных на индивидуальном объемном планировании параметров проводимого облучения по данным современных методов медицинской визуализации (см. п. 2 Диагностика заболевания) для обеспечения адекватных онкологических результатов лечения, его эффективности и безопасности. Конкретные методики проведения лучевой терапии зависят от локализации первичной опухоли, степени ее распространения и глубины опухолевой инфильтрации [12].
Уровень убедительности доказательств - C (уровень достоверности доказательств - 5)
Комментарии:
- Адъювантную лучевую терапию следует начинать не позднее 6-8 нед. после операции;
- дистанционная ЛТ проводится на область вульвы и/или зоны регионарного метастазирования: пахово-бедренные, наружные и внутренние подвздошные лимфатические узлы;
- внутритканевая ЛТ (брахитерапия) как локальный метод облучения в некоторых случаях проводится на область первичного очага - вульву;
- дистанционная ЛТ проводится в режиме ежедневного фракционирования (РОД 1,8 - 2,0 Гр) 5 раз в неделю. Перерывы во время курса лечения не допускаются. Важно подведение максимальных доз с использованием 3D-конформного облучения или технологии IMRT (конформная дистанционная лучевая терапия, в том числе IMRT, IGRT, ViMAT, стереотаксическая) (intense modulated radiotherapy - модулированной по интенсивности лучевой терапии) до СОД 46 - 50 Гр (РОД 2 Гр) или до СОД 45 - 50,4 Гр (РОД 1,8 Гр) при адъювантном лечении в послеоперационном периоде и до 60 - 64 Гр (РОД 2 Гр) или 59,4 - 64,8 Гр (при РОД 1,8 Гр) при радикальной самостоятельной лучевой терапии. На область клинически и/или рентгенологически не пораженных пахово-бедренные лимфоузлов СОД 45 - 50 Гр. Пахово-бедренные лимфоузлы (положительные, без экстракапсулярного распространения или выраженной остаточной опухолевой ткани) СОД 50 - 55 Гр Пахово-бедренные лимфоузлы СОД 54 - 64 Гр
- в ряде случаев при наличии больших регионарных лимфатических узлов (резидуальных или нерезектабельных) возможно подведение локального буста до суммарной дозы 60 - 70 Гр [22, 23];
- при поверхностной локализации опухолевого поражения вульвы или лимфатических узлов допускается применение болюса с целью адекватного поверхностного дозового распределения при дистанционной лучевой терапии
- купирование проявлений лучевой реакции на фоне дистанционного облучения, а также химиолучевой терапии (диареи, цистита, местной воспалительной реакции кожи и слизистой оболочки) проводится с помощью противовоспалительной симптоматической терапии (в том числе ухода за кожей и слизистой оболочкой половых губ). Это дает возможность избежать перерывов в лечении.
3.2.1. Топографическое и топометрическое планирование лучевой терапии
Топографическое и топометрическое планирование лучевой терапии к проведению дистанционной лучевой терапии проводится в положении лежа на спине или с иммобилизацией верхней и нижней части тела с помощью подголовника и индивидуального вакуумного матраса. Возможно использование наружных и эндовагинальных рентгеноконтрастных маркеров с целью верификации нижней границы опухоли (GTV) и входа во влагалище (introittus). Для более точного оконтуривания первичной опухоли (GTV), тазовых и паховых лимфатических узлов, включаемых в облучаемый объем (CTV, PTV), возможно использование данных методов медицинской визуализации (КТ/МРТ с внутривенным контрастированием, ПЭТ-КТ и др.), полученных как в ходе процедуры топометрии, так и при интеграции данных первичного обследовании с применением fusion-технологий.
3.2.2. Дистанционная лучевая терапия
- У пациенток с РВ при отсутствии поражения тазовых лимфатических узлов рекомендовано расположение верхней границы поля не ниже середины крестцово-подвздошного сочленения или не выше границ L4/L5 [12].
Уровень убедительности доказательств - C (уровень достоверности доказательств - 5)
Комментарий: В случае поражения тазовых лимфатических узлов верхняя граница поля должна быть на 5 см выше метастатически пораженного лимфатического узла. Верхняя граница поля должна проходить по горизонтали на уровне передней нижней подвздошной ости так, чтобы в объем облучения входили пахово-бедренные лимфатические узлы. Боковая граница поля - это вертикальная линия от передней нижней подвздошной ости. Для хорошего охвата паховых лимфатических узлов переднебоковая граница должна проходить параллельно паховой складке и ниже должна достаточно охватывать пахово-бедренные лимфатические узлы по межвертельной линии бедренной кости. Нижняя граница поля облучения должна быть ниже по крайней мере на 2 см наиболее дистальной части вульвы. Следует избегать лучевой нагрузки на головку и шейку бедренной кости [12].
После проведения топографического и топометрического планирования лучевой терапии проводится оконтуривание объема мишени - оконтуривание первичной опухоли и критических органов (одна анатомическая зона). Любой опухолевый объем вульвы обводится как GTV и включает в себя визуализируемый или пальпируемый объем инфильтрации опухолевого процесса влагалищной трубки [12].
Вульва:
- CTV-T включает себя GTV или ложе удаленной опухоли, прилегающую кожу, подкожную клетчатку, слизистую оболочку; исключаются кости;
- CTV-N включает тазовые и билатеральные пахово-бедренные лимфатические узлы. Тазовые лимфатические узлы (общие подвздошные, наружные и внутренние подвздошные) обводятся с включением сосудов на ширину 7 мм. Пресакральная область включается в объем в случае перехода инфильтрации на влагалище на 1 см кпереди от S1 - S2. У пациенток с переходом инфильтрации на ампулярную часть/прямую кишку регионарные периректальные лимфатические узлы входят в объем.
- Пахово-бедренные лимфатические узлы включаются в общий объем с окружающими сосудами до 1,0 - 1,5 см (исключаются кости, мышцы и кожа), так же, как и любые визуализируемые узлы в клетчатке;
PTV1 = CTV-T + 5 - 10 мм
PTV2 = CTV-N + 5 - 7 мм
PTVсум = PTV1 + PTV2
PTVсум может быть сокращен с поверхности кожи в области пахово-бедренной складки [12].
Органы риска. Обязательными для оконтуривания с целью расчета подводимых толерантных доз по гистограммам доза-объем являются мочевой пузырь, прямая кишка, петли тонкого кишечника, анус, костный мозг (крестцовая кость, копчик, тело L5, вертлужная впадина, проксимальная часть бедренной кости), головка бедренной кости [12].
3.3. Принципы системной химиотерапии
- Пациенткам с распространенным РВ, на первом этапе не подлежащих первичной операции или химиолучевой терапии, может быть рекомендована неоадъювантная комбинированная химиотерапия на основе соединений платины [12, 56, 45].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 5)
Комментарий:
В настоящее время при распространенном РВ проводится лучевая терапия с платиносодержащей сенсибилизирующей ХТ, как при РШМ, например, #цисплатин** [12, 56, 45]. Комбинированную химиотерапию со соединениями платины следует рассматривать как лечение первой линии при метастатическом или рецидивирующем заболевании [12].
Хотя лучшая комбинация с препаратами (соединениями) платины при распространенном РВ неясна, предпочтительным режимом можно считать #цисплатин** или #карбоплатин** и #паклитаксел** [12].
- Проведение ХТ возможно также при нерезектабельном РВ, во избежании экзентеративных операций, при положительных краях резекции опухоли в случае отказа от ЛТ и ее нецелесообразности в конкретной клинической ситуации [78].
- Рекомендованы следующие режимы химиотерапии:
- минимальный объем ХТ, который может рекомендоваться пациенткам с РВ, аналогично ХТ при РШМ: #цисплатин** 50 мг/м2 в/в в 1-й день с интервалом 21 день до 4 - 6 курсов [12, 59].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 5)
- оптимальный объем ХТ - следующие варианты ХТ:
- #паклитаксел** 175 мг/м2 в/в 1-й день + #цисплатин** 70 мг/м2 в/в 1-й день с интервалом 21 день до 6 курсов [12, 57];
- #паклитаксел** 175 мг/м2 в/в в 1-й день + #карбоплатин** AUC 5 - 6 в/в в 1-й день - с интервалом 21 день до 6 курсов [46];
- #паклитаксел** 175 мг/м2 в/в 1-й день с интервалом 21 день до 6 курсов [47];
- #пембролизумаб** 200 мг в/в 1 раз в 21 день при наличии высокого уровня микросателлитной нестабильности, включая нарушения системы репарации ДНК [48].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 4)
- При возникновении рецидива заболевания у пациенток с РВ рекомендована ХТ по схемам аналогичным для рецидива плоскоклеточного РШМ, указанным в соответствующих клинических рекомендациях по РШМ [49, 55 - 61].
Уровень убедительности рекомендаций - B (уровень достоверности доказательств - 3)
3.4. Обезболивание
Порядок и рекомендации по обезболиванию при злокачественных новообразованиях тела матки соответствуют рекомендациям, представленным в рубрикаторе "Хронический болевой синдром (ХБС) у взрослых пациентов, нуждающихся в паллиативной медицинской помощи" [http://cr.rosminzdrav.ru/#!/recomend/708]
3.5 Диетотерапия
- К настоящему моменту имеются данные о повышенном риске развития онкологических заболеваний у пациенток с избыточной массой тела (ожирением) [15]. В этой связи рекомендованы мероприятия, направленные на снижение избыточного веса пациенток до нормальных значений. Коррекция привычного рациона питания у таких пациенток будет способствовать профилактике осложнений проводимого лечения (хирургического, лекарственного или лучевого) [15 - 16].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 4)
4. Медицинская реабилитация и санаторно-курортное лечение, медицинские показания и противопоказания к применению методов медицинской реабилитации, в том числе основанных на использовании природных лечебных факторов
Проведение предреабилитации значительно ускоряет функциональное восстановление, сокращает сроки пребывания в стационаре после операции и снижает частоту развития осложнений и летальных исходов на фоне лечения онкологического заболевания. Предреабилитация включает лечебную физкультуру (ЛФК) при заболеваниях женских половых органов, психологическую и нутритивную поддержку, информирование пациентов [29].
- Рекомендуется пациенткам с РВ физическая предреабилитация (состоит из комбинации аэробной и анаэробной нагрузки) с целью улучшения толерантности к физическим нагрузкам, улучшения качества жизни и увеличения тонуса мышц [29].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 5)
- Рекомендуется пациенткам с РВ увеличение физической активности за 2 недели до операции - улучшает качество жизни в послеоперационном периоде, позволяя вернуться к полноценной повседневной активности уже через 3 нед. после операции [29].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 5)
- Рекомендуется пациенткам с РВ проведение ЛФК на предоперационном этапе - уменьшает частоту послеоперационных осложнений [29].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 5)
- Рекомендуется пациенткам с РВ тренировка дыхательных мышц в ходе предреабилитации - приводит к уменьшению частоты послеоперационных легочных осложнений и продолжительности пребывания в стационаре [29].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 5)
- Психологическая поддержка рекомендована всем пациенткам с РВ в плане предреабилитации - улучшает настроение, снижает уровень тревоги и депрессии. Пациентки, прошедшие курс психологической предреабилитации, лучше адаптируются к повседневной жизни после хирургического лечения [29].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 5)
Комментарий: Психологическая предреабилитация с использованием методик, направленных на работу со стрессом (методик релаксации, формирования позитивного настроя), которая начинается за 5 дней до операции и продолжается 30 дней после нее, проводится в течение 40 - 60 мин 6 дней в неделю [29].
- Всем пациенткам с РВ рекомендована тактика fast track rehabilitation ("быстрый путь") и ERAS (early rehabilitation after surgery - ранняя реабилитация после операции), включающая комплексное обезболивание, раннее энтеральное питание, отказ от рутинного применения зондов и дренажей, раннюю мобилизацию (активизацию и вертикализацию) пациентов уже с 1 - 2-х суток после операции с целью снижения риска развития ранних послеоперационных осложнений, частоту повторных госпитализаций [33, 52].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 5)
- Раннее начало выполнения комплекса ЛФК с включением в программу аэробной, силовой нагрузок и упражнений на растяжку рекомендовано всем пациентам с РВ для улучшения качества жизни пациенток [29].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 5)
- Раннее начало дыхательной гимнастики, подъем головного конца кровати и ранняя активизация рекомендована пациенткам с РВ - с целью предотвращать развитие застойных явлений в легких в послеоперационном периоде [34].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 5)
- Ранняя активизация, назначение антикоагулянтов (антитромботических средств) с профилактической целью и ношение компрессионного трикотажа рекомендована всем пациенткам с РВ с целью профилактики тромботических осложнений в послеоперационном периоде [37, 54].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 5)
- Для лечения болевого синдрома в послеоперационном периоде - носит междисциплинарный характер, помимо медикаментозной коррекции, рекомендованы лечебная физкультура при заболеваниях женских половых органов (ЛФК), лечение положением, психологические методы коррекции боли (релаксацию), чрескожную короткоимпульсную электростимуляцию (ЧЭНС), акупунктура (воздействие на точки акупунктуры другими физическими факторами) [38].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 5)
- Рекомендуется пациенткам с РВ проведение сеансов общего массажа медицинского, начиная со 2-х суток после операции, с целью уменьшения интенсивности болевого синдрома, беспокойства, напряжения, улучшения качества жизни [34, 39].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 5)
- Рекомендуется пациенткам с РВ проведение клинико-психологической коррекции и использование методик релаксации в послеоперационном периоде - позволяет снизить кратность обезболивания и улучшить качество жизни онкогинекологических пациентов [38].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 5)
- Рекомендуется при возникновении лимфостаза нижних конечностей проводить полную противоотечную терапию, включающую массаж нижней конечности медицинский, ношение компрессионного трикотажа, выполнение комплекса ЛФК, уход за кожей [44, 39].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 5)
- Рекомендуется пациенткам с РВ при возникновении лимфедемы нижних конечностей также назначить:
- прерывистую пневмокомпрессию нижних конечностей в сочетании с полной противоотечной терапией [44, 53].
- низкоинтенсивную лазеротерапию (внутривенное облучение крови) в сочетании с полной противоотечной терапией;
- глубокую осцилляцию (массаж переменным электрическим полем) в сочетании с полной противоотечной терапией [34, 39].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 5)
5. Профилактика и диспансерное наблюдение, медицинские показания и противопоказания к применению методов профилактики
- Рекомендуется соблюдать следующую периодичность приемом (осмотров, консультаций) врача-онколога после завершения лечения по поводу плоскоклеточного РВ:
- каждые 3 месяца. в течение первых 2 лет;
- каждые 6 мес. с 3-го по 5-й год после завершения лечения;
- каждые 12 мес. начиная с 6-го года после завершения лечения
- или при появлении жалоб [12].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 5)
Комментарии: у пациентов с высоким риском прогрессирования заболевания перерыв между обследованиями может быть сокращен.
- Рекомендуется использовать следующие методы после завершения лечения по поводу плоскоклеточного РВ:
- сбор анамнеза и физикальное обследование;
- УЗИ органов брюшной полости (комплексное), малого таза комплексное (трансвагинальное и трансабдоминальное), лимфатических узлов регионарных;
- МРТ органов малого таза с внутривенным контрастированием и КТ органов брюшной полости с внутривенным болюсным контрастированием (при невозможности выполнить КТ показано МРТ органов брюшной полости с внутривенным контрастированием, а при невозможности выполнить МРТ показано КТ органов малого таза у женщин с контрастированием;
- Прицельную рентгенографию органов грудной клетки или КТ органов грудной полости.
- ПЭТ-КТ с туморотропным РФП при подозрении на отдаленные метастазы при неинформативности КТ/МРТ [12].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 5)
Комментарии: задачей наблюдения является раннее выявление прогрессирования заболевания с целью раннего начала хирургического и/или химиолучевого лечения.
6. Организация оказания медицинской помощи
Медицинская помощь, за исключением медицинской помощи в рамках клинической апробации, в соответствии с Федеральным законом от 21.11.2011 N 323-ФЗ "Об основах охраны здоровья граждан в Российской Федерации", организуется и оказывается:
1) в соответствии с положением об организации оказания медицинской помощи по видам медицинской помощи, которое утверждается уполномоченным Федеральным органом исполнительной власти;
2) в соответствии с порядками оказания медицинской помощи, утверждаемыми уполномоченным федеральным органом исполнительной власти и обязательными для исполнения на территории Российской Федерации всеми медицинскими организациями
3) на основе настоящих клинических рекомендаций;
4) с учетом стандартов медицинской помощи, утвержденных уполномоченным Федеральным органом исполнительной власти.
Первичная специализированная медико-санитарная помощь оказывается врачом-онкологом и иными врачами-специалистами в центре амбулаторной онкологической помощи, а при его отсутствии в первичном онкологическом кабинете, поликлиническом отделении онкологического диспансера (онкологической больницы).
При подозрении или выявлении у пациента онкологического заболевания врачи-терапевты, врачи-терапевты участковые, врачи общей практики (семейные врачи), врачи-специалисты, средние медицинские работники в установленном порядке направляют пациента на консультацию в центр амбулаторной онкологической помощи, а при отсутствии в первичный онкологический кабинет, поликлиническое отделение онкологического диспансера (онкологической больницы) для оказания ему первичной специализированной медико-санитарной помощи.
Консультация в центре амбулаторной онкологической помощи либо в первичном онкологическом кабинете, поликлиническом отделении онкологического диспансера (онкологической больницы) должна быть проведена не позднее 3 рабочих дней с даты выдачи направления на консультацию. Врач-онколог центра амбулаторной онкологической помощи (в случае отсутствия центра амбулаторной онкологической помощи врач-онколог первичного онкологического кабинета или поликлинического отделения онкологического диспансера (онкологической больницы организует взятие биопсийного (операционного) материала, а также организует выполнение иных диагностических исследований, необходимых для установления диагноза, включая распространенность онкологического процесса и стадию заболевания.
В случае невозможности взятия в медицинской организации, в составе которой организован центр амбулаторной онкологической помощи (первичный онкологический кабинет) биопсийного (операционного) материала, проведения иных диагностических исследований пациент направляется врачом-онкологом в онкологический диспансер (онкологическую больницу) или в медицинскую организацию, оказывающую медицинскую помощь пациентам с онкологическими заболеваниями.
Срок выполнения патологоанатомических исследований, необходимых для гистологической верификации злокачественных новообразований не должен превышать 15 рабочих дней с даты поступления биопсийного (операционного) материала в патологоанатомическое бюро (отделение).
Сроки проведения диагностических инструментальных и лабораторных исследований в случае подозрения на онкологическое заболевание не должны превышать сроков, установленных в программе государственных гарантий бесплатного оказания гражданам медицинской помощи, утверждаемой Правительством Российской Федерации, 7 рабочих дней со дня назначения исследований.
Диагноз онкологического заболевания устанавливается врачом-специалистом на основе результатов диагностических исследований, включающих в том числе проведение цитологической и (или) гистологической верификации диагноза, за исключением случаев, когда взятие биопсийного и (или) пункционного материала не представляется возможным.
Врач-онколог центра амбулаторной онкологической помощи (первичного онкологического кабинета) направляет пациента в онкологический диспансер (онкологическую больницу) или иную медицинскую организацию, оказывающую медицинскую помощь пациентам с онкологическими заболеваниями, в том числе подведомственную федеральному органу исполнительной власти (далее - федеральная медицинская организация), для уточнения диагноза (в случае невозможности установления диагноза, включая распространенность онкологического процесса и стадию заболевания), определения тактики лечения, а также в случае наличия медицинских показаний для оказания специализированной, в том числе высокотехнологичной, медицинской помощи.
При онкологических заболеваниях, входящих в рубрики C37, C38, C40 - C41, C45 - C49, C58, D39, C62, C69 - C70, C72, C74 МКБ-10, а также соответствующих кодам международной классификации болезней - онкология (МКБ-О), 3 издания 8936, 906 - 909, 8247/3, 8013/3, 8240/3, 8244/3, 8246/3, 8249/3 врач-онколог онкологического диспансера (онкологической больницы) или иной медицинской организации, оказывающей медицинскую помощь пациентам с онкологическими заболеваниями, для определения лечебной тактики организует проведение консультации или консилиума врачей, в том числе с применением телемедицинских технологий, в федеральных государственных бюджетных учреждениях, подведомственных Министерству здравоохранения Российской Федерации, оказывающих медицинскую помощь (далее в целях настоящего Порядка - национальные медицинские исследовательские центры).
В сложных клинических случаях для уточнения диагноза (в случае невозможности установления диагноза, включая распространенность онкологического процесса и стадию заболевания) в целях проведения оценки, интерпретации и описания результатов врач-онколог организует направление:
цифровых изображений, полученных по результатам патоморфологических исследований, в патолого-анатомическое бюро (отделение) четвертой группы (референс-центр) [1] путем информационного взаимодействия, в том числе с применением телемедицинских технологий при дистанционном взаимодействии медицинских работников между собой;
цифровых изображений, полученных по результатам лучевых методов исследований, в дистанционный консультативный центр лучевой диагностики, путем информационного взаимодействия, в том числе с применением телемедицинских технологий при дистанционном взаимодействии медицинских работников между собой;
биопсийного (операционного) материала для повторного проведения патоморфологических, иммуногистохимических, и молекулярно-генетических исследований: в патолого-анатомическое бюро (отделение) четвертой группы (референс-центр), а также в молекулярно-генетические лаборатории для проведения молекулярно-генетических исследований.
Тактика лечения устанавливается консилиумом врачей, включающим врачей-онкологов, врача-радиотерапевта, врача-нейрохирурга (при опухолях нервной системы) медицинской организации, в составе которой имеются отделения хирургических методов лечения злокачественных новообразований, противоопухолевой лекарственной терапии, радиотерапии (далее - онкологический консилиум), в том числе онкологическим консилиумом, проведенным с применением телемедицинских технологий, с привлечением при необходимости других врачей-специалистов.
Диспансерное наблюдение врача-онколога за пациентом с выявленным онкологическим заболеванием устанавливается и осуществляется в соответствии с порядком диспансерного наблюдения за взрослыми с онкологическими заболеваниями.
С целью учета информация о впервые выявленном случае онкологического заболевания направляется в течение 3 рабочих дней врачом-онкологом медицинской организации, в которой установлен соответствующий диагноз, в онкологический диспансер или организацию субъекта Российской Федерации, исполняющую функцию регистрации пациентов с впервые выявленном злокачественным новообразованием, в том числе с применением единой государственной информационной системы в сфере здравоохранения. В случае подтверждения у пациента наличия онкологического заболевания информация об уточненном диагнозе направляется из онкологического диспансера или организации субъекта Российской Федерации, исполняющей функции регистрации пациентов с впервые выявленном злокачественным новообразованием, в медицинскую организацию, осуществляющую диспансерное наблюдение пациента
Специализированная, в том числе высокотехнологичная, медицинская помощь в медицинских организациях, оказывающих медицинскую помощь взрослому населению при онкологических заболеваниях, оказывается по медицинским показаниям, предусмотренным положением об организации оказания специализированной, в том числе высокотехнологичной, медицинской помощи.
Специализированная, за исключением высокотехнологичной, медицинская помощь в медицинских организациях, подведомственных федеральным органам исполнительной власти, оказывается по медицинским показаниям, предусмотренным пунктом 5 порядка направления пациентов в медицинские организации и иные организации, подведомственные федеральным органам исполнительной власти, для оказания специализированной (за исключением высокотехнологичной) медицинской помощи, предусмотренного в приложении к положению об организации оказания специализированной, в том числе высокотехнологичной, медицинской помощи. (Пункт 5: для получения специализированной медицинской помощи в плановой форме выбор федеральной медицинской организации осуществляется по направлению лечащего врача.) В случае если в реализации Программы принимают участие несколько федеральных медицинских организаций, оказывающих специализированную медицинскую помощь при заболеваниях, состояниях (группе заболеваний, состояний), соответствующих заболеваниям, состояниям (группе заболеваний, состояний) пациента, лечащий врач обязан проинформировать пациента (законного представителя пациента) о возможности выбора федеральной медицинской организации, в том числе о возможных сроках ожидания специализированной медицинской помощи, которые могут превышать сроки ожидания, установленные программой государственных гарантий бесплатного оказания гражданам медицинской помощи.
Сроки ожидания оказания специализированной (за исключением высокотехнологичной) медицинской помощи не должны превышать сроков, установленных в программе государственных гарантий бесплатного оказания гражданам медицинской помощи, утверждаемой Правительством Российской Федерации, 7 рабочих дней.
При наличии у пациента с онкологическим заболеванием медицинских показаний для проведения медицинской реабилитации врач-онколог организует ее проведение в соответствии с порядком организации медицинской реабилитации взрослых.
При наличии у пациента с онкологическим заболеванием медицинских показаний к санаторно-курортному лечению врач-онколог организует его в соответствии порядком организации санаторно-курортного лечения.
Паллиативная медицинская помощь пациенту с онкологическими заболеваниями оказывается в соответствии с положением об организации оказания паллиативной медицинской помощи, включая порядок взаимодействия медицинских организаций, организаций социального обслуживания и общественных объединений, иных некоммерческих организаций, осуществляющих свою деятельность в сфере охраны здоровья.
При подозрении и (или) выявлении у пациента онкологического заболевания в ходе оказания ему скорой медицинской помощи его переводят или направляют в медицинские организации, оказывающие медицинскую помощь пациентам с онкологическими заболеваниями, для определения тактики ведения и необходимости применения дополнительно других методов специализированного противоопухолевого лечения.
Показаниями для госпитализации в медицинскую организацию в экстренной или неотложной форме являются:
1) наличие осложнений онкологического заболевания, требующих оказания ему специализированной медицинской помощи в экстренной и неотложной форме;
2) наличие осложнений лечения онкологического заболевания (хирургическое вмешательство, ЛТ, лекарственная терапия и т.д.), требующих оказания ему специализированной медицинской помощи в экстренной и неотложной форме
Показаниями для госпитализации в медицинскую организацию в плановой форме являются:
1) необходимость выполнения сложных интервенционных диагностических медицинских вмешательств, а также проведение эндоскопических исследований при невозможности выполнить их амбулаторно, требуют последующего наблюдения в условиях круглосуточного или дневного стационара;
2) наличие показаний к специализированному противоопухолевому лечению (хирургическое вмешательство, ЛТ, в том числе контактная, ДЛТ и другие виды ЛТ, лекарственная терапия и др.), требующему наблюдения в условиях круглосуточного или дневного стационара.
Показаниями к выписке пациента из медицинской организации являются:
1) завершение курса лечения или одного из этапов оказания специализированной, в том числе высокотехнологичной, медицинской помощи в условиях круглосуточного или дневного стационара при условии отсутствия осложнений лечения, требующих медикаментозной коррекции и/или медицинских вмешательств в стационарных условиях;
2) отказ пациента или его законного представителя от специализированной, в том числе высокотехнологичной, медицинской помощи в условиях круглосуточного или дневного стационара, установленной консилиумом медицинской организации, оказывающей онкологическую помощь
3) в случаях несоблюдения пациентом предписаний или правил внутреннего распорядка лечебно-профилактического учреждения, если это не угрожает жизни пациента и здоровью окружающих;
4) необходимость перевода пациента в другую медицинскую организацию по соответствующему профилю оказания медицинской помощи.
Заключение о целесообразности перевода пациента в профильную медицинскую организацию осуществляется после предварительной консультации по предоставленным медицинским документам и/или предварительного осмотра пациента врачами-специалистами медицинской организации, в которую планируется перевод.
7. Дополнительная информация (в том числе факторы, влияющие на исход заболевания или состояния)
Дополнительной информации нет
Критерии оценки качества медицинской помощи
N п/п
Критерии качества
Оценка выполнения
1.
Выполнено патолого-анатомическое исследование биопсийного (операционного) материала вульвы всем пациенткам с РВ и подозрением на РВ с целью верификации диагноза
Да/Нет
2.
Выполнено стадирование заболевания, в соответсвии с международной классификацией FIGO и TNM.
Да/Нет
3.
Выполнено патолого-анатомическое исследование биопсийного (операционного материала) вульвы (при проведении хирургического лечения)
Да/Нет
4.
Проведена адъювантная лучевая терапия в соответствии с указанными рекомендациями
Да/Нет
Список литературы
1. Wilkinson E.J., Teixeira M.R. Tumors of the vulva. In: Pathology and genetics of tumors of the breast and female genital organs. Ed. by F.A. Tavassoli, P. Devilee. Lyon: IARC Press, 2003. Pp. 314 - 334.
2. Oonk M.H.M., Planchamp F., Baldwin P. et al. European Society of Gynaecological Oncology guidelines for the management of patients with vulvar cancer. Int J Gynecol Cancer. 2017; 27(4): 832 - 7.
3. Hacker N.F. Vulvar cancer. In: Berek and Hacker's gynecologic oncology. Ed. by J.S. Berek, N.F. Hacker. 5th ed. Philadelphia: Lippincott Williams & Wilkins, 2009. Pp. 536 - 575.
4. Ашрафян Л.А., Харченко Н.В., Киселев В.И. и др. Рак вульвы: этиопатогенетическая концепция. М.: Молодая гвардия, 2006. С. 7 - 38.
5. Siegel R.L., Miller K.D., Jemal A. Cancer statistics, 2016. CA Cancer J Clin 2016; 66(1): 7 - 30.
6. WHO classification of tumours of female reproductive organs. Ed. by R.J. Kurman, M.L. Carcangiu, C.S. Herrington, R.H. Young. 5th Edition, Volume 4, 2020
7. Злокачественные новообразования в России в 2021 году (заболеваемость и смертность). Под ред. А.Д. Каприна, В.В. Старинского, А.О. Шахзадовой. М.: МНИОИ им. П.А. Герцена - филиал ФГБУ "НМИЦ радиологии" Минздрава России, - 2022. - илл. - 252 с. ISBN 978-5-85502-280-3.
8. Коржевская Е.В., Кузнецов В.В. Рак вульвы. Клиническая онкогинекология. Руководство для врачей. Под ред. В.П. Козаченко. 2-е изд., перераб. и доп. М.: Бином, 2016. С. 72 - 96.
9. Кузнецов В.В., Коржевская Е.В. Плоскоклеточный рак вульвы. Рациональная фармакотерапия в онкологии. Руководство для практикующих врачей. Под общ. ред. М.И. Давыдова, В.А. Горбуновой. М.: Литтерра, 2015. С. 441 - 444.
10. Slomovitz B.M., Coleman R.L., Oonk M.H. et al. Update on sentinel lymph node biopsy for early-stage vulvar cancer. Gynecol Oncol 2015; 138: 472 - 7.
11. Kamran M.W., O'Toole F., Meghen K. et al. Whole-body [18F]fluoro-2deoxyglucose positron emission tomography scan as combined PETCT staging prior to planned radical vulvectomy and inguinofemoral lymphadenectomy for squamous vulvar cancer: a correlation with groin node metastasis. Eur J Gynaecol Oncol 2014; 35: 230 - 5.
12. Koh WJ et al. Vulvar Cancer, Version 2.2019, NCCN Clinical Practice Guidelines in Oncology./https://www.nccn.org/professionals/physician_gls/pdf/vulvar_blocks.pdf
13. Moore D.H., Ali S., Koh W.J. et al. A phase II trial of radiation therapy and weekly cisplatin chemotherapy for the treatment of locally-advanced squamous cell carcinoma of the vulva: a gynecologic oncology group study. Gynecol Oncol 2012; 124(3): 529 - 33.
14. Petereit D.G., Mehta M.P., Buchler D.A., Kinsella T.J. Inguinofemoral radiation of N0, N1 vulvar cancer may be equivalent to lymphadenectomy if proper radiation technique is used. Int J Radiat Oncol Biol Phys 1993; 27: 963 - 7.
15. Hallak S., Ladi L., Sorbe B. Prophylactic inguinal-femoral irradiation as an alternative to primary lymphadenectomy in treatment of vulvar carcinoma. Int J Oncol 2007; 31: 1077 - 85.
16. Mahner S., Jueckstock J., Hilpert F.J. et. al. Adjuvant therapy in lymph node-positive vulvar cancer: the AGO-CaRE-1 study. Natl Cancer Inst 2015; 107(3).
17. Byfield J.E., Calabro-Jones P., Klisak I., Kulhanian F. Pharmacologic requirements for obtaining sensitization of human tumor cells in vitro to combined 5-fluorouracil or ftorafur and X-rays. Int J Radiat Oncol Biol Phys 1982; 8(11): 1923 - 33.
18. Moore D.H., Thomas G.M., Montana G.S. et al. Preoperative chemoradiation for advanced vulvar cancer: a phase II study of the Gynecologic Oncology Group. Int J Radiat Oncol Biol Phys 1998; 42: 79 - 85.
19. Thomas G., Dembo A., DePetrillo A. et al. Concurrent radiation and chemotherapy in vulvar carcinoma. Gynecol Oncol 1989; 34(3): 263 - 7.
20. Wahlen S.A., Slater J.D., Wagner R.J. et al. Concurrent radiation therapy and chemotherapy in the treatment of primary squamous cell carcinoma of the vulva. Cancer 1995; 75: 2289 - 94.
21. Sebag-Montefiore D.J., McLean C., Arnott S.J. et al. Treatment of advanced carcinoma of the vulvawith chemoradiotherapy - can exenterative surgery be avoided? Int J Gynecol Cancer 1994; 4: 150 - 5.
22. Mell L.K., Mundt A.J., Survey of IMRT use in the United States, 2004. Cancer 2005; 104: 1296 - 303.
23. Lim K., Small W., Pertelance L. et al. Consensus guidelines for delineation of clinical target volume for intensity-modulated pelvic radiotherapy for the definitive treatment of cervical cancer. Int J Radiat Oncol Biol Phys 2011; 79: 348 - 55.
24. Raspagliesi F et al. Role of paclitaxel and cisplatin as the neoadjuvant treatment for locally advanced squamous cell carcinoma of the vulva./J Gynecol Oncol. 2014 Jan; 25(1): 22 - 9. doi: 10.3802/jgo.2014.25.1.22. Epub 2014 Jan 8
25. Raitanen M., Rantanen V., Kulmala J. et al. Paclitaxel combined with fractionated radiation in vitro: a study with vulvar squamous cell carcinoma cell lines Int J Cancer 2002; 97: 853 - 7.
26. Raitanen M., Rantanen V., Kulmala J. et al. Supra-additive effect with concurrent paclitaxel and cisplatin in vulvar squamous cell carcinoma in vitro. Int J Cancer 2002; 100: 238 - 43.
27. Gill B.S., Bernard M.E., Lin J.F. et al. Impact of adjuvant chemotherapy with radiation for node-positive vulvar cancer: a National Cancer Data Base (NCDB) analysis. Gynecol Oncol 2015; 137(3): 365 - 72.
28. Tsimopoulou I., Pasquali S., Howard R. et al. Psychological prehabilitation before cancer surgery: a systematic review. Ann Surg Oncol 2015; 22(13): 4117 - 23.
29. Silver J.A., Baima J. Cancer prehabilitation: an opportunity to decrease treatmentrelated morbidity, increase cancer treatment options, and improve physical and psychological health outcomes. Am J Phys Med Rehabil 2013; 92: 715 - 27.
30. Nilsson H.,  U., Bock D. et al. Is preoperative physical activity related to post-surgery recovery? BMJ Open 2016; 6(1): e007997.
U., Bock D. et al. Is preoperative physical activity related to post-surgery recovery? BMJ Open 2016; 6(1): e007997.
31. Hijazi Y., Gondal U., Aziz O. A systematic review of prehabilitation programs in abdominal cancer surgery. Int J Surg 2017; 39: 156 - 62.
32. Tsimopoulou I., Pasquali S., Howard R. et al. Psychological prehabilitation before cancer surgery: a systematic review. Ann Surg Oncol 2015; 22(13): 4117 - 23.
33. Carter J. Fast-track surgery in gynaecology and gynaecologic oncology: a review of a rolling clinical audit. ISRN Surgery 2012; 2012: 368014.
34. Nelson G., Bakkum-Gamez J., Kalogera E. et al Guidelines for perioperative care in gynecologic/oncology: Enhanced Recovery After Surgery (ERAS) Society recommendations - 2019 update. Int J Gynecol Cancer 2019 Mar 15.
35. De Almeida E.P.M., De Almeida J.P., Landoni G. et al. Early mobilization programme improves functional capacity after major abdominal cancer surgery: a randomized controlled trial. Br J Anaesth 2017; 119(5): 900 - 7.
36. Wren S.M., Martin M., Yoon J.K., Bech F. Postoperative pneumonia-prevention program for the inpatient surgical ward. J Am Coll Surg 2010; 210(4): 491 - 5.
37. Peedicayil A., Weaver A., Li X. et al. Incidence and timing of venous thromboembolism after surgery for gynecological cancer. Gynecol Oncol 2011; 121(1): 64 - 9.
38. Swarm R., Abernethy A.P., Anghelescu D.L. et al. Adult cancer pain. J Natl Compr Canc Netw 2010; 8: 1046 - 86.
39. Ben-Arye E., Samuels N., Lavie O. Integrative medicine for female patients with gynecologic cancer. J Altern Complement Med 2018; 24(9-10): 881 - 9.
40. Goerling U., Jaeger C., Walz A. et al. The efficacy of psycho-oncological interventions for women with gynaecological cancer: a randomized study. Oncology 2014; 87: 114 - 24.
41. Smits A., Lopes A., Bekkers R. et al. Body mass index and the quality of life of endometrial cancer survivors - a systematic review and meta-analysis. Gynecol Oncol 2015; 137: 180 - 7.
42. Schmitz K.H., Courneya K.S., Matthews C. et al. American College of Sports Medicine roundtable on exercise guidelines for cancer survivors. Med Sci Sports Exerc 2010; 42: 1409 - 26.
43. Zhou Y., Chlebowski R., LaMonte M.J. et al. Body mass index, physical activity, and mortality in women diagnosed with ovarian cancer: results from the Women"s Health Initiative. Gynecol Oncol 2014; 133(1): 4 - 10.
44. Biglia N., Zanfagnin V., Daniele A. et al. Lower body lymphedema in patients with gynecologic cancer. Anticancer Res 2017; 37(8): 4005 - 15.
45. Oonk. M. H.M. et al. European Society of Gynaecological Oncology Guidelines for the Management of Patients With Vulvar Cancer/Int J Gynecol Cancer 2017; 27: 832Y837
46. Amant, F., Nooij, L., Annibali, D., van Rompuy, A.-S., Han, S., van den Bulck, H., & Goffin, F. (2018). Brief Report on 3-Weekly Paclitaxel Carboplatin Efficacy in Locally Advanced or Metastatic Squamous Vulvar Cancer. Gynecologic and Obstetric Investigation, 1 - 7. doi: 10.1159/000487435
47. Witteveen P.O.et al. Phase II study on paclitaxel in patients with recurrent, metastatic or locally advanced vulvar cancer not amenable to surgery or radiotherapy: a study of the EORTC-GCG (European Organisation for Research and Treatment of Cancer - Gynaecological Cancer Group)./Ann Oncol. 2009 Sep; 20(9): 1511 - 6. doi: 10.1093/annonc/mdp043. Epub 2009
48. Shields LBE, Gordinier ME Pembrolizumab in Recurrent Squamous Cell Carcinoma of the Vulva: Case Report and Review of the Literature./Gynecol Obstet Invest. 2019; 84(1): 94 - 98. doi: 10.1159/000491090. Epub 2018
49. Santeufemia D. A. Et al. Cisplatin-gemcitabine as palliative chemotherapy in advanced squamous vulvar carcinoma: report of two cases./Eur J Gynaecol Oncol. 2012; 33(4): 421 - 422
50. Peri M. A Case of Stage I Vulvar Squamous Cell Carcinoma with Early Relapse and Rapid Disease Progression/Case Reports in Oncological Medicine Volume 2019, Article ID 1018492, 4 pages https://doi.org/10.1155/2019/1018492
51. Rose PG et al Concurrent cisplatin-based radiotherapy and chemotherapy for locally advanced cervical cancer./N Engl J Med. 1999 Apr 15; 340(15): 1144 - 53
52. Minig L. Clinical outcomes after fast-track care in women undergoing laparoscopic hysterectomy/Int J Gynaecol Obstet. 2015 Dec; 131(3): 301 - 4. doi: 10.1016/j.ijgo.2015.06.034. Epub 2015 Sep 8
53. Borman P. Lymphedema diagnosis, treatment, and follow-up from the view point of physical medicine and rehabilitation specialists. Turk J Phys Med Rehab 2018; 64(3): 179 - 97.
54. Shimizu A et al. Direct oral anticoagulants are effective and safe for the treatment of venous thromboembolism associated with gynecological cancers./Int J Gynaecol Obstet. 2019 Nov; 147(2): 252 - 257. doi: 10.1002/ijgo.12944. Epub 2019 Aug 29
55. Oken MM, Creech RH, Tormey DC, Horton J, Davis TE, McFadden ET, Carbone PP: Toxicity and response criteria of the Eastern Cooperative Oncology Group. Am J Clin Oncol 1982, 5(6): 649 - 655
56. Karnofsky DA, Burchenal JH: The clinical evaluation of chemotherapeutic agents in cancer. In: Evaluation of chemotherapeutic agents. edn. Edited by MacLeod C. New York: Columbia University Press; 1949: 191 - 205
57. Raspagliesi F. et al. Role of paclitaxel and cisplatin as the neoadjuvant treatment for locally advanced squamous cell carcinoma of the vulva. J Gynecol Oncol. 2014 Jan; 25(1): 22 - 29. https://doi.org/10.3802/jgo.2014.25.1.22
58. Bellati F., et al. Single agent cisplatin chemotherapy in surgically resected vulvar cancer patients with multiple inguinal lymph node metastases (2005) Gynecologic Oncology, 96 (1), pp. 227 - 231.
59. Mazzotta, M.; Pizzuti, L.; Krasniqi, E.; Di Lisa, F.S.; Cappuzzo, F.; Landi, L.; Sergi, D.; Pelle, F.; Cappelli, S.; Botti, C.; et al. Role of Chemotherapy in Vulvar Cancers: Time to Rethink Standard of Care? Cancers 2021, 13, 4061. https://doi.org/10.3390/cancers13164061
60. Rose PG., et al. "Paclitaxel and cisplatin as first-line therapy in recurrent or advanced squamous cell carcinoma of the cervix: a gynecologic oncology group study". Journal of Clinical Oncology 17.9 (1999): 2676 - 2680.
61. Lepori S, Fontanella C, Maltese G et al. Phase II study of the safety and efficacy of oral capecitabine in patients with platinum-pretreated advanced or recurrent cervical carcinoma. Annals of Oncology, 2017, 28: mdx372.053.
62. Сафронова К.В., Артемьева А.С., Сидорук А.А. и др. Меланома нижнего женского полового тракта (вульвы, влагалища и шейки матки): обзор литературы и собственные наблюдения. Опухоли женской репродуктивной системы 2019; 15(3): 44 - 53.
63. L. Chow, B.Q. Tsui, S. Bahrami et al. Gynecologic tumor board: a radiologist's guide to vulvar and vaginal malignancies//Abdominal Radiology volume 46, p. 5669 - 5686 (2021)
64. J. Heidkamp, P. L.M. Zusterzee et al/. MRI evaluation of vulvar squamous-cell carcinoma in fresh radical local excision specimens for cancer localization and prediction of surgical tumor-free marginsl//NMR in Biomedicine. 2019. 32: e4025. https://doi.org/10.1002/nbm.4025;
65. Kataoka MY, Sala E, Baldwin P, et al. The accuracy of magnetic resonance imaging in staging of vulvar cancer: a retrospective multi-centre study. Gynecol Oncol. 2010; 117(1): 82 - 87
66. Andersen K, Zobbe V, Thranov IR, Pedersen KD (2015) Relevance of computerized tomography in the preoperative evaluation of patients with vulvar cancer: a prospective study. Cancer Imaging 15: 8;
67. Pounds R, O'Neill D, Subba K et al (2020) The role of preoperative computerized tomography (CT) scan of the pelvis and groin in the management of clinically early staged vulva squamous cell carcinoma. Gynecol Oncol 157: 444 - 449;
68. Selman TJ, Luesley DM, Acheson N, Khan KS, Mann CH (2005) A systematic review of the accuracy of diagnostic tests for inguinal lymph node status in vulvar cancer. Gynecol Oncol 99: 206 - 214;
69. NCCN Version 1.2023 - December 22, 2022; Robertson NL, Hricak H, Sonoda Y, et al. The impact of FDG-PET/CT in the management of patients with vulvar and vaginal cancer. Gynecol Oncol 2016; 140: 420 - 424;
70. Dalla Palma M, Gregianin M, Fiduccia P, et al. PET/CT imaging in gynecologic malignancies: a critical overview of its clinical impact and our retrospective single center analysis. Crit Rev Oncol Hematol. 2012; 83(1): 84 - 98
71. Viswanathan C, Kirschner K, Truong M, et al. Multimodality imaging of vulvar cancer: staging, therapeutic response, and complications. AJR AM J Roentgenol 2013; 200: 1387 - 1400.
72. Robertson NL, Hricak H, Sonoda Y, et al. The impact of FDGPET/CT in the management of patients with vulvar and vaginal cancer. Gynecol Oncol. 2016; 140(3): 420 - 424
73. Albuquerque K.S. Zoghbi K.K., Nunes Gomes N.B., et al. Vaginal cancer: Why should we care? Anatomy, staging and in-depth imaging-based review of vaginal malignancies focusing on MRI and PET/CT. Clinical imaging 2022; 84: 65 - 78
74. K.R. Fink, J.R. Fink/Imaging of brain metastases//Surg Neurol Int. 2013 May 2; 4 (Suppl 4): S209 - 19. doi: 10.4103/2152-7806.111298. Print 2013;
75. Eichler AF, Loeffler JS. Multidisciplinary management of brain metastases. Oncologist. 2007; 12(7): 884 - 98. doi: 10.1634/theoncologist.12-7-884
76. A. Mastmeyera, G. Pernelleb, R. Mac et al. Accurate Model-based Segmentation of Gynecologic Brachytherapy Catheter Collections in MRI-images//Med Image Anal. 2017 December; 42: 173 - 188. doi: 10.1016/j.media.2017.06.011
77. Cohn DE, Dehdashti F, Gibb RK, et al. Prospective evaluation of positron emission tomography for the detection of groin node metastases from vulvar cancer. Gynecol Oncol. 2002; 85(1): 179 - 184].
78. Oonk, M. H. M., Planchamp, F., Baldwin, P., Bidzinski, M., Brannstrom, M., Landoni, F., ... van der Zee, A. G. J. (2017) European Society of Gynaecological Oncology Guidelines for the Management of Patients With Vulvar Cancer. International Journal of Gynecological Cancer, 27(4), 832 - 837. DOI: 10.1097/IGC.0000000000000975https://www.esgo.org/media/2015/12/Vulvar-cancer-Russia-preview.pdf
Приложение А1
СОСТАВ
РАБОЧЕЙ ГРУППЫ ПО РАЗРАБОТКЕ И ПЕРЕСМОТРУ
КЛИНИЧЕСКИХ РЕКОМЕНДАЦИЙ
1. Ашрафян Л.А., академик РАН, д.м.н., профессор, заместитель директора ФГБУ "НМИЦ АГП им. В.И. Кулакова" Минздрава России, директор института онкогинекологии и маммологии.
2. Новикова Е.Г., д.м.н., профессор, начальник отделения онкогинекологии МНИОИ им. П.А. Герцена - филиала ФГБУ "НМИЦ радиологии" Минздрава России.
3. Хохлова С.В., д.м.н., заведующая онкологическим отделением противоопухолевой лекарственной терапии ФГБУ "НМИЦ АГиП им. академика В.И. Кулакова" Минздрава РФ.
4. Урманчеева А.Ф., д.м.н., профессор, ведущий научный сотрудник отделения онкогинекологии ФГБУ "НМИЦ онкологии им. Н.Н. Петрова" Минздрава России.
5. Берлев И.В., д.м.н., профессор, заведующий научным отделением онкогинекологии ФГБУ "НМИЦ онкологии им. Н.Н. Петрова" Минздрава России.
6. Антонова И.Б., д.м.н., заведующая лабораторией профилактики, ранней диагностики и комбинированного лечения онкологических заболеваний ФГБУ "Российский научный центр рентгенорадиологии" Минздрава России.
7. Бабаева Н.А. д.м.н., ведущий научный сотрудник Института онкогинекологии и маммологии, врач-онколог онкологического отделения хирургических методов лечения ФГБУ "НМИЦ АГП им. В.И. Кулакова" Минздрава России.
8. Алешикова О.И., к.м.н., старший научный сотрудник Института онкогинекологии и маммологии, врач-онколог онкологического отделения хирургических методов лечения ФГБУ "НМИЦ АГиП им. академика В.И. Кулакова" Минздрава РФ.
9. Румянцев А.А., к.м.н., заведующий отделением противоопухолевой лекарственной терапии N 4 отдела лекарственного лечения ФГБУ "Национальный медицинский исследовательский центр онкологии им. Н.Н. Блохина" Минздрава России, Москва
10. Мухтаруллина С.В., д.м.н., заведующая отделением онкогинекологии МНИОИ им. П.А. Герцена - филиала ФГБУ "НМИЦ радиологии" Минздрава России.
11. Вереникина Е.В., к.м.н., заведующая отделением онкогинекологии ФГБУ "Ростовский научно-исследовательский онкологический институт" Минздрава России.
12. Демидова Л.В., д.м.н., ведущий научный сотрудник отдела лучевой терапии МНИОИ им. П.А. Герцена - филиала ФГБУ "НМИЦ радиологии" Минздрава России.
13. Шевчук А.С., к.м.н., заведующий отделением комбинированных и лучевых методов лечения онкогинекологических заболеваний НИИ клинической онкологии ФГБУ "НМИЦ онкологии им. Н.Н. Блохина" Минздрава России.
14. Ульрих Е.А., д.м.н., профессор, главный научный сотрудник научно-исследовательской лаборатории репродуктивных технологий, руководитель центра компетенций "Онкофертильность" НМИЦ им. В.А. Алмазова.
15. Красильников С.Э., д.м.н., профессор, директор института онкологии и нейрохирургии, врач-онколог ФГБУ "НМИЦ имени академика Е.Н. Мешалкина" Минздрава России
16. Давыдова И.Ю., д.м.н., ведущий научный сотрудник отдела онкохирургии тазового дна ГБУЗ МКНЦ имени А.С. Логинова ДЗМ
17. Крикунова Л.И., д.м.н., профессор, заведующая отделения лучевых и комбинированных методов лечения гинекологических заболеваний ФГБУ "НМИЦ радиологии" Минздрава России.
18. Мещерякова Л.А., д.м.н., эксперт в диагностике лечении трофобластических опухолей, ФГБУ "НМИЦ онкологии им. Н.Н. Блохина" Минздрава России.
19. Коломиец Л.А., д.м.н., профессор, заведующая гинекологическим отделением НИИ онкологии ФГБНУ "Томский НИМЦ РАН".
20. Крейнина Ю.М., д.м.н., ведущий научный сотрудник лаборатории инновационных технологий радиотерапии и химиолучевого лечения злокачественных новообразований ФГБУ "Российский научный центр рентгенорадиологии" Минздрава России.
21. Дубинина А.В., к.м.н., старший научный сотрудник отделения радиотерапии, ФГБУ "НМИЦ онкологии им. Н.Н. Блохина" Минздрава России
22. Карселадзе А.И., профессор, д.м.н., ФГБУ "НМИЦ АГП им. В.И. Кулакова" Минздрава России.
23. Рубцова Н.А., д.м.н., заведующая отделом лучевой диагностики, врач-рентгенолог МНИОИ им. П.А. Герцена - филиал ФГБУ "НМИЦ радиологии" Минздрава России
24. Быченко В.Г., к.м.н, заведующий отделением лучевой диагностики ФГБУ "НМИЦ АГП им. В.И. Кулакова" Минздрава России.
25. Солопова А.Е., д.м.н., доцент, врач-рентгенолог отделение лучевой диагностики ФГБУ "НМИЦ АГП им. В.И. Кулакова" Минздрава России.
26. Рыжкова Д.В., д.м.н., профессор РАН, заведующая кафедрой ядерной медицины и радиационных технологий с клиникой, главный научный сотрудник НИО ядерной медицины и тераностики ФГБУ "НМИЦ им В.А. Алмазова" Минздрава России
27. Оводенко Д.Л., д.м.н., заведующий отделением инновационной онкологии и гинекологии ФГБУ "НМИЦ "НМИЦ АГиП им. академика В.И. Кулакова" Минздрава РФ.
28. Гриневич В.Н., к.м.н., заведующий отделением онкопатологии МНИОИ им. П.А. Герцена - филиала ФГБУ "НМИЦ радиологии" Минздрава России.
29. Снеговой А.В., д.м.н., заведующий отделением амбулаторной химиотерапии дневного стационара ФБГУ "НМИЦ онкологии им. Н.Н. Блохина" Минздрава России.
30. Юренева С.В., зам. директора по науке Института онкогинекологии и маммологии ФГБУ "НМИЦ АГП им. В.И. Кулакова" Минздрава России, д.м.н., профессор кафедры акушерства и гинекологии.
31. Слонов А.В., к.м.н., главный врач КБ N 123 ФГБУ ФНКЦ ФХМ им. Ю.М. Лопухина ФМБА России
Блок по медицинской реабилитации:
1. Кончугова Т.В., д.м.н., профессор, врач-физиотерапевт, заведующая отделом преформированных физических факторов ФГБУ "НМИЦ реабилитации и курортологии" Минздрава России.
2. Еремушкин М.А., д.м.н., профессор, заведующий отделением ЛФК и клинической биомеханики ФГБУ "НМИЦ реабилитации и курортологии" Минздрава России.
3. Гильмутдинова И.Р., к.м.н., заведующая отделом биомедицинских технологий и лаборатории клеточных технологий, врач-трансфузиолог, дерматовенеролог, специалист в области клеточных технологий ФГБУ "НМИЦ реабилитации и курортологии" Минздрава России.
4. Буланов А.А., д.м.н., старший научный сотрудник отделения клинической фармакологии и химиотерапии ФГБУ "НМИЦ онкологии им. Н.Н. Блохина" Минздрава России.
5. Бутенко А.В., д.м.н., профессор, главный врач НИИ клинической онкологии ФГБУ "НМИЦ онкологии им. Н.Н. Блохина" Минздрава России, председатель НС "Ассоциация специалистов по онкологической реабилитации".
6. Назаренко А.В., к.м.н., врач высшей квалификационной категории, заведующий отделением радиологии ФГБУ "НМИЦ онкологии им. Н.Н. Блохина" Минздрава России, член Российской ассоциации терапевтических радиационных онкологов (РАТРО), European Society for Radiotherapy & Oncology (ESTRO), Российско-Американского альянса по изучению рака (ARCA), представитель РФ в МАГАТЭ.
7. Обухова О.А., к.м.н., врач-физиотерапевт, заведующий отделением реабилитации ФГБУ "НМИЦ онкологии им. Н.Н. Блохина" Минздрава России, член Европейской ассоциации парентерального и энтерального питания (ESPEN), Российской ассоциации парентерального и энтерального питания (RESPEN).
8. Хуламханова М.М., врач-физиотерапевт, врач-онколог отделения реабилитации ФГБУ "НМИЦ онкологии им. Н.Н. Блохина" Минздрава России.
9. Ткаченко Г.А., психолог отделения реабилитации ФГБУ "НМИЦ онкологии им. Н.Н. Блохина" Минздрава России.
10. Петрова Т.А., логопед-педагог отделения реабилитации ФГБУ "НМИЦ онкологии им. Н.Н. Блохина" Минздрава России.
11. Семиглазова Т.Ю., д.м.н., ведущий научный сотрудник научного отдела инновационных методов терапевтической онкологии и реабилитации ФГБУ "НМИЦ онкологии им. Н.Н. Петрова" Минздрава России, доцент кафедры онкологии ФГБОУ ВО "СЗГМУ им. И.И. Мечникова" Минздрава России.
12. Пономаренко Г.Н., д.м.н., профессор, заслуженный деятель науки РФ, генеральный директор ФГБУ "ФНЦРИ им. Г.А. Альбрехта" Минтруда России, заведующий кафедрой курортологии и физиотерапии ФГБВОУ ВО "ВМА им. С.М. Кирова" Минобороны России.
13. Ковлен Д.В., д.м.н., доцент кафедры курортологии и физиотерапии ФГБВОУ ВО "ВМА им. С.М. Кирова" Минобороны России.
14. Каспаров Б.С., к.м.н., заместитель главного врача по амбулаторной помощи заведующий клинико-диагностическим отделением ФГБУ "НМИЦ онкологии им. Н.Н. Петрова" Минздрава России.
15. Крутов А.А., врач-онколог клинико-диагностического отделения ФГБУ "НМИЦ онкологии им. Н.Н. Петрова" Минздрава России.
16. Зернова М.А., инструктор-методист по лечебной физкультуре ФГБУ "НМИЦ онкологии им. Н.Н. Петрова" Минздрава России.
17. Кондратьева К.О., медицинский психолог ФГБУ "НМИЦ онкологии им. Н.Н. Петрова" Минздрава России.
18. Иванова Г.Е., д.м.н., главный специалист по медицинской реабилитации Минздрава России, заведующая отделом медико-социальной реабилитации инсульта НИИ ЦВПиИ ФГБОУ ВО "РНИМУ им. Н.И. Пирогова" Минздрава России.
19. Романов А.И., академик РАН, д.м.н., профессор, главный врач ФГБУ "Центр реабилитации" Управления делами Президента РФ.
20. Филоненко Е.В., д.м.н., профессор, заведующая центром лазерной и фотодинамической диагностики и терапии опухолей МНИОИ им. П.А. Герцена - филиала ФГБУ "НМИЦ радиологии" Минздрава России, врач-онколог.
21. Степанова А.М., заместитель директора по науке, заведующая отделением реабилитации частного многопрофильного диагностического и реабилитационного центра "Восстановление".
Блок по организации медицинской помощи:
1. Невольских А.А., д.м.н., профессор, заместитель директора по лечебной работе МРНЦ им. А.Ф. Цыба - филиала ФГБУ "НМИЦ радиологии" Минздрава России.
2. Хайлова Ж.В., к.м.н., главный врач клиники МРНЦ им. А.Ф. Цыба - филиала ФГБУ "НМИЦ радиологии" Минздрава России.
3. Иванов С.А., профессор РАН, д.м.н., директор МРНЦ им. А.Ф. Цыба - филиала ФГБУ "НМИЦ радиологии" Минздрава России.
4. Геворкян Т.Г., заместитель директора НИИ клинической и экспериментальной радиологии ФГБУ "НМИЦ онкологии им. Н.Н. Блохина" Минздрава России.
Конфликта интересов нет.
Приложение А2
МЕТОДОЛОГИЯ РАЗРАБОТКИ КЛИНИЧЕСКИХ РЕКОМЕНДАЦИЙ
Целевая аудитория данных клинических рекомендаций:
- врачи-онкологи;
- врачи-хирурги;
- врачи-радиологи;
- врачи-онкологи (специалисты по химиотерапии);
- врачи-генетики;
- врачи-дерматовенерологи;
- врачи-патологоанатомы;
- студенты медицинских вузов, ординаторы и аспиранты.
Методы, использованные для сбора/селекции доказательств: поиск в электронных базах данных; анализ современных научных разработок по проблеме РБ в РФ и за рубежом; обобщение практического опыта российских и зарубежных специалистов.
Таблица 1. Шкала оценки уровней достоверности доказательств (УДД) для методов диагностики (диагностических вмешательств)
УДД
Расшифровка
1
Систематические обзоры исследований с контролем референсным методом или систематический обзор рандомизированных клинических исследований с применением метаанализа
2
Отдельные исследования с контролем референсным методом или отдельные рандомизированные клинические исследования и систематические обзоры исследований любого дизайна, за исключением рандомизированных клинических исследований, с применением метаанализа
3
Исследования без последовательного контроля референсным методом или исследования с референсным методом, не являющимся независимым от исследуемого метода или нерандомизированные сравнительные исследования, в том числе когортные исследования
4
Несравнительные исследования, описание клинического случая
5
Имеется лишь обоснование механизма действия или мнение экспертов
Таблица 2. Шкала оценки уровней достоверности доказательств (УДД) для методов профилактики, лечения, медицинской реабилитации, в том числе основанных на использовании природных лечебных факторов (профилактических, лечебных, реабилитационных вмешательств)
УДД
Расшифровка
1
Систематический обзор РКИ с применением метаанализа
2
Отдельные РКИ и систематические обзоры исследований любого дизайна, за исключением РКИ, с применением метаанализа
3
Нерандомизированные сравнительные исследования, в т.ч. когортные исследования
4
Несравнительные исследования, описание клинического случая или серии случаев, исследования "случай-контроль"
5
Имеется лишь обоснование механизма действия вмешательства (доклинические исследования) или мнение экспертов
Таблица 3. Шкала оценки уровней убедительности рекомендаций (УУР) для методов профилактики, диагностики, лечения, медицинской реабилитации, в том числе основанных на использовании природных лечебных факторов (профилактических, диагностических, лечебных, реабилитационных вмешательств)
УУР
Расшифровка
A
Сильная рекомендация (все рассматриваемые критерии эффективности (исходы) являются важными, все исследования имеют высокое или удовлетворительное методологическое качество, их выводы по интересующим исходам являются согласованными)
B
Условная рекомендация (не все рассматриваемые критерии эффективности (исходы) являются важными, не все исследования имеют высокое или удовлетворительное методологическое качество и/или их выводы по интересующим исходам не являются согласованными)
C
Слабая рекомендация (отсутствие доказательств надлежащего качества (все рассматриваемые критерии эффективности (исходы) являются неважными, все исследования имеют низкое методологическое качество и их выводы по интересующим исходам не являются согласованными)
Методы, использованные для формулирования рекомендаций - консенсус экспертов.
Экономический анализ
Анализ стоимости не проводился и публикации по фармакоэкономике не анализировались.
Метод валидизации рекомендаций:
- внешняя экспертная оценка;
- внутренняя экспертная оценка.
Описание метода валидизации рекомендаций
Настоящие рекомендации в предварительной версии рецензированы независимыми экспертами, которые попросили прокомментировать, прежде всего, насколько интерпретация доказательств, лежащих в основе рекомендаций, доступна для понимания.
Комментарии, полученные от экспертов, тщательно систематизировались и обсуждались председателем и членами рабочей группы. Каждый пункт обсуждался и вносимые в результате этого изменения в рекомендации регистрировались. Если же изменения не вносились, то регистрировались причины отказа от внесения изменений.
Консультации и экспертная оценка: проект рекомендаций рецензирован также независимыми экспертами, которых попросили прокомментировать, прежде всего, доходчивость и точность интерпретации доказательной базы, лежащей в основе рекомендаций.
Для окончательной редакции и контроля качества рекомендации повторно проанализированы членами рабочей группы, которые пришли к заключению, что все замечания и комментарии экспертов приняты во внимание, риск систематических ошибок при разработке рекомендаций сведен к минимуму.
Порядок обновления клинических рекомендаций
Механизм обновления клинических рекомендаций предусматривает их систематическую актуализацию - не реже чем 1 раз в 3 года, а также при появлении новых данных с позиции доказательной медицины по вопросам диагностики, лечения, профилактики конкретных заболеваний и реабилитации пациентов, при наличии обоснованных дополнений/замечаний к ранее утвержденным клиническим рекомендациям, но не чаще 1 раза в 6 мес.
Приложение А3
СПРАВОЧНЫЕ МАТЕРИАЛЫ,
ВКЛЮЧАЯ СООТВЕТСТВИЕ ПОКАЗАНИЙ К ПРИМЕНЕНИЮ
И ПРОТИВОПОКАЗАНИЙ, СПОСОБОВ ПРИМЕНЕНИЯ И ДОЗ ЛЕКАРСТВЕННЫХ
ПРЕПАРАТОВ, ИНСТРУКЦИИ ПО ПРИМЕНЕНИЮ
ЛЕКАРСТВЕННОГО ПРЕПАРАТА
Актуальные инструкции к лекарственным препаратам, упоминаемым в данных клинических рекомендациях, можно найти на сайте http://grls.rosminzdrav.ru.
Приложение Б
АЛГОРИТМЫ ДЕЙСТВИЙ ВРАЧА
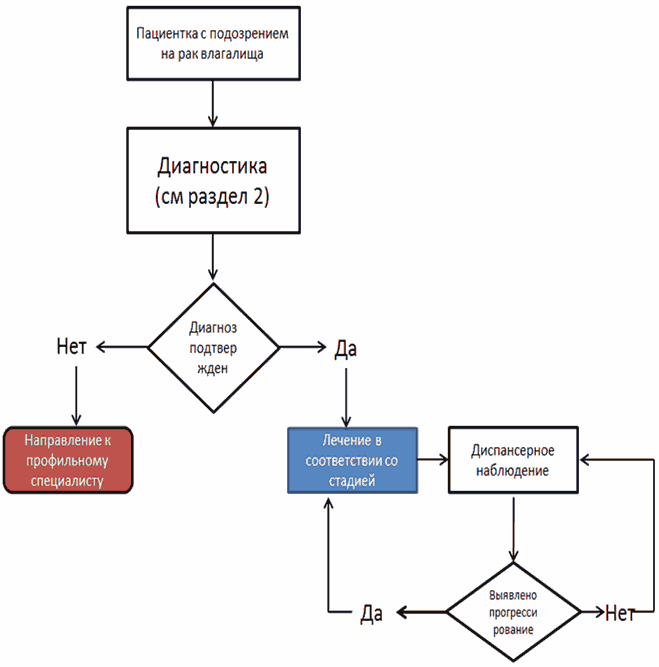
Приложение В
ИНФОРМАЦИЯ ДЛЯ ПАЦИЕНТА
Рекомендация при осложнениях химиотерапии: связаться с врачом-онкологом.
Рекомендации при осложнениях лучевой терапии: связаться с врачом-радиологом.
1. При повышении температуры тела до 38 °C и более:
- начать прием антибактериальных препаратов системного действия: по назначению врача-онколога.
2. При стоматите:
- диета - механически и термически щадящая;
- часто (каждый час) полоскать рот отварами ромашки, коры дуба, шалфея, смазывать рот облепиховым (персиковым) маслом;
- обрабатывать полость рта по рекомендации врача-онколога.
3. При диарее:
- диета: исключить жирное, острое, копченое, сладкое, молочное, клетчатку;
- можно нежирное мясо, мучное, кисломолочное, рисовый отвар;
- обильное питье;
- принимать препараты по назначению врача-онколога.
При тошноте:
- принимать препараты по назначению врача-онколога.
Большинство побочных эффектов (усталость, которая может усилиться примерно через 2 нед. после начала лечения; тошнота и рвота, диарея, изменения кожи, низкие показатели крови) носят временный характер и прекращаются после завершения лечения.
Приложение Г1 - ГN
ШКАЛЫ
ОЦЕНКИ, ВОПРОСНИКИ И ДРУГИЕ ОЦЕНОЧНЫЕ ИНСТРУМЕНТЫ СОСТОЯНИЯ
ПАЦИЕНТА, ПРИВЕДЕННЫЕ В КЛИНИЧЕСКИХ РЕКОМЕНДАЦИЯХ
Приложение Г1
ШКАЛА ОЦЕНКИ ТЯЖЕСТИ СОСТОЯНИЯ ПАЦИЕНТА ПО ВЕРСИИ ВОЗ/ECOG
Название на русском языке: Шкала оценки тяжести состояния пациента по версии ВОЗ/ECOG [55]
Оригинальное название: The Eastern Cooperative Oncology Group/World Health Organization Performance Status (ECOG/WHO PS)
Источник (официальный сайт разработчиков, публикация с валидацией): https://ecog-acrin.org/resources/ecog-performance-status
Oken MM, Creech RH, Tormey DC, Horton J, Davis TE, McFadden ET, Carbone PP: Toxicity and response criteria of the Eastern Cooperative Oncology Group. Am J Clin Oncol 1982, 5(6): 649 - 655
Тип: шкала оценки
Назначение: описать уровень функционирования пациента с точки зрения его способности заботиться о себе, повседневной активности и физических способностях (ходьба, работа и т.д.).
Содержание:
Балл
Описание
0
Пациент полностью активен, способен выполнять все, как и до заболевания (90 - 100% по шкале Карновского)
1
Пациент неспособен выполнять тяжелую, но может выполнять легкую или сидячую работу (например, легкую домашнюю или канцелярскую работу, 70 - 80% по шкале Карновского)
2
Пациент лечится амбулаторно, способен к самообслуживанию, но не может выполнять работу. Более 50% времени бодрствования проводит активно - в вертикальном положении (50 - 60% по шкале Карновского)
3
Пациент способен лишь к ограниченному самообслуживанию, проводит в кресле или постели более 50% времени бодрствования (30 - 40% по шкале Карновского)
4
Инвалид, совершенно не способен к самообслуживанию, прикован к креслу или постели (10 - 20% по шкале Карновского)
Ключ (интерпретация): приведен в самой шкале
Приложение Г2
ШКАЛА КАРНОВСКОГО
Название на русском языке: Шкала Карновского [56]
Оригинальное название (если есть): KARNOFSKY PERFORMANCE STATUS
Источник (официальный сайт разработчиков, публикация с валидацией): Karnofsky DA, Burchenal JH: The clinical evaluation of chemotherapeutic agents in cancer. In: Evaluation of chemotherapeutic agents. edn. Edited by MacLeod C. New York: Columbia University Press; 1949: 191-205
Тип: шкала оценки
Назначение: описать уровень функционирования пациента с точки зрения его способности заботиться о себе, повседневной активности и физических способностях (ходьба, работа и т.д.).
Содержание (шаблон):
Шкала Карновского
100 - Состояние нормальное, жалоб нет
90 - Способен к нормальной деятельности, незначительные симптомы или признаки заболевания
80 - Нормальная активность с усилием, незначительные симптомы или признаки заболевания
70 - Обслуживает себя самостоятельно, не способен к нормальной деятельности или активной работе
60 - Нуждается порой в помощи, но способен сам удовлетворять большую часть своих потребностей
50 - Нуждается в значительной помощи и медицинском обслуживании
40 - Инвалид, нуждается в специальной помощи, в т.ч. медицинской
30 - Тяжелая инвалидность, показана госпитализация, хотя смерть непосредственно не угрожает
20 - Тяжелый больной. Необходимы госпитализация и активное лечение
10 - Умирающий
0 - Смерть
Ключ (интерпретация): приведен в самой шкале
