"Клинические рекомендации "Аномалия развития коронарных сосудов"
МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ
КЛИНИЧЕСКИЕ РЕКОМЕНДАЦИИ
АНОМАЛИЯ РАЗВИТИЯ КОРОНАРНЫХ СОСУДОВ
Кодирование по Международной статистической классификации болезней и проблем, связанных со здоровьем: Q24.5
Год утверждения (частота пересмотра): 2024
Возрастная категория: Дети
Пересмотр не позднее: 2026
ID: 829
Разработчик клинической рекомендации
- Ассоциация сердечно-сосудистых хирургов России
- Общероссийская общественная организация содействия развитию лучевой диагностики и терапии "Российское общество рентгенологов и радиологов"
- Всероссийская общественная организация "Ассоциация детских кардиологов России"
- Национальная ассоциация экспертов по санаторно-курортному лечению
Одобрено Научно-практическим Советом Минздрава РФ
Список сокращений
- АКГ - ангиокардиография (ретроградная катетеризация левых отделов сердца с коронарографией и панаортографией);
- Ао - аорта;
- КА - коронарная артерия;
- КГ - коронарография;
- КДО - конечно-диастолический объем;
- КДР - конечно-диастолический размер;
- КСО - конечно-систолический объем;
- КСР - конечно-систолический размер;
- КТ - компьютерная томография;
- КСФ - коронаро-сердечная фистула;
- ЛА - легочная артерия;
- ЛГ - легочная гипертензия;
- ЛКА - левая коронарная артерия;
- ЛС - легочный ствол;
- ЛЖ - левый желудочек;
- МК - митральный клапан;
- МРТ - магнитно-резонансная томография;
- ОАП - открытый артериальный проток;
- ОВ - огибающая ветвь;
- ОФЭКТ - однофотонная эмиссионная компьютерная томография;
- ПКА - правая коронарная артерия;
- ПМЖВ - передняя межжелудочковая ветвь;
- ПЭТ - позитронно-эмиссионная томография;
- РФП - радиофармпрепарат (V09 Диагностические радиофармацевтические средства)
- СБУГ - синдром Бланд-Уайт-Гарланда;
- ФВ - фракция выброса;
- ФК - фиброзное кольцо;
- ФП - фибрилляция предсердий;
- ЭКГ - электрокардиография (регистрация электрокардиограммы, расшифровка, описание и интерпретация электрокардиографических данных);
- Эхо-КГ - эхокардиография.
Термины и определения
Синдром Бланд-Уайт-Гарланда (СБУГ) - ВПС с аномальным отхождением ЛКА от ЛС, характеризующийся развитием тяжелой сердечной недостаточности уже в младенческом возрасте и имеющий крайне неблагоприятное прогностическое течение.
Инфантильный тип коронарного кровоснабжения - клинический вариант течения СБУГ с отсутствием хорошо развитых коллатералей между системой правой и левой венечных артерий, приводящий к серьезному ишемическому поражению миокарда ЛЖ сразу же после рождения ребенка, что в ряде случаев проявляется развитием терминальной сердечной недостаточности.
Катетеризация сердца (ретроградная катетеризация левых отделов сердца) - инвазивная процедура, проводимая с лечебными или диагностическими целями при патологии сердечно-сосудистой системы путем введения катетеров в полость сердца или просвет магистральных сосудов.
Компьютерная томография (КТ) - неинвазивный метод лучевой диагностики, позволяющий получить серию послойных субмиллиметровых аксиальных изображений органов и структур тела человека, основанный на измерении и сложной компьютерной обработке разности ослабления рентгеновского излучения различными по плотности тканями; для улучшения дифференцировки органов друг от друга, а также нормальных и патологических структур. Применяются различные методики контрастного усиления/контрастирования, с использованием рентгеноконтрастных средств, содержащих йод. Для визуализации структур сердечно-сосудистой системы применяют КТ-ангиографию (компьютерная томография сердца с контрастированием) - методику внутривенного болюсного введения контрастного средства в кровоток с помощью системы внутрисосудистого введения контрастного средства, с установленной скоростью и временем введения препарата. На основе полученных данных посредством компьютерной постобработки с 3D-реконструкцией строится трехмерная модель сердца и сосудов.
Магнитно-резонансная томография (МРТ) - неинвазивный метод получения томографических медицинских изображений без ионизирующего излучения для исследования внутренних органов и тканей, основанный на явлении ядерного магнитного резонанса и на измерении электромагнитного отклика атомных ядер, находящихся в сильном постоянном магнитном поле, в ответ на возбуждение их определенным сочетанием электромагнитных волн; такими ядрами являются ядра атомов водорода, присутствующие в теле человека в составе воды и других веществ. МР-ангиография - метод получения изображения просвета сосудов при помощи магнитно-резонансного томографа. Метод позволяет оценивать как анатомические, так и функциональные особенности кровотока. МР-ангиография основана на отличии сигнала от перемещающихся протонов (крови) от окружающих неподвижных тканей, что позволяет получать изображения сосудов без использования каких-либо контрастных средств - бесконтрастная ангиография (например: фазово-контрастная МР-ангиография). В ряде случаев применяется внутривенное болюсное контрастирование с использованием контрастных препаратов на основе парамагнетиков (гадолиний).
Позитронно-эмиссионная томография - радионуклидный метод исследования перфузии миокарда, позволяющий выявить зоны измененного коронарного кровотока, с использованием флудезоксиглюкозы [18F], способной аккумулироваться только в жизнеспособном миокарде.
Уровень достоверности доказательств (УДД) - степень уверенности в том, что найденный эффект от применения медицинского вмешательства является истинным [1].
Уровень убедительности рекомендаций (УУР) - степень уверенности в достоверности эффекта вмешательства и в том, что следование рекомендациям принесет больше пользы, чем вреда в конкретной ситуации [1].
Эхокардиография - метод ультразвукового исследования, направленный на исследование морфологических и функциональных изменений сердца и его клапанного аппарата.
1. Краткая информация по заболеванию или состоянию (группы заболеваний или состояний)
1.1 Определение заболевания или состояния (группы заболеваний или состояний)
Аномалии коронарных артерий (КА) представляют собой разнообразную группу врожденных патологических изменений коронарных сосудов, формирующихся вследствие аномального отхождения, следования или строения терминального русла коронарных артерий. Частота встречаемости изолированных аномалий коронарных артерий составляет 0,6 - 1,8% от объема всех проводимых коронарографий [2].
В НМИЦ ССХ им. А.Н. Бакулева разработана следующая классификация аномалий КА, отражающая морфологические особенности выше обозначенного ВПС [3]:
I. Аномалии отхождения венечных (коронарных) артерий от аорты.
1. варианты единственной КА (ЕКА).
1.1. аномальная ЕКА с нормальным распределением коронарных артерий.
1.2. сочетание ЕКА со свищами КА.
1.3. ЕКА, сочетающаяся с другими ВПС.
1.4. аномальная ЕКА с аномальным межартериальным следованием основных ветвей КА.
А) межартериальное следование аномальной ветви левой КА.
Б) межартериальное следование аномальной правой КА.
2. интрамуральные КА.
3. эктопии КА.
II. Аномалии отхождения венечных артерий от легочной артерии.
1. Аномальное отхождение левой КА от ЛА - 90% от всех случаев коронарных аномалий.
2. Аномальное отхождение правой КА от ЛА - 0,003% по данным коронарографии. Высокая частота встречаемости сочетания аномалии с дефектом аорто-легочной перегородки и 2-х створчатым аортальным клапаном.
3. Аномальное отхождение ветвей правой и левой КА от ЛА.
4. Тотальное аномальное отхождение КА от ЛА
III. Аномалии следования и ветвления венечных артерий, отходящих от аорты.
1. Отсутствие огибающей ветви.
2. Отсутствие передней межжелудочковой ветви.
IV. Коронаро-сердечные фистулы.
А. Аномальное отхождение ЛКА от ЛА (синдром Бланд-Уайт-Гарланда) представляет собой редкий врожденный порок сердца (ВПС), характеризующийся неблагоприятным течением уже в периодах новорожденности и младенчества и крайне сомнительным прогнозом при естественном развитии.
Б. Коронаро-сердечные фистулы (КСФ) - аномальное сообщение между коронарными артериями с полостью сердца или другими сосудистыми структурами минуя капиллярное русло, приводящее к нарушению структуры коронарных артерий и кровотока по ним [2, 3, 5, 6 - 10].
1.2 Этиология и патогенез заболевания или состояния (группы заболеваний или состояний)
А. При СБУГ правая КА отходит от первого лицевого синуса аорты и ход ее сохранен. При этом ее характерной особенностью является резкая дилатация (диаметр ее в 86,5% случаев превышает таковой ЛКА в 1,5 - 2 раза) и извитость [4].
Характерным для аномального отхождения ЛКА от ЛА является правый доминантный тип кровоснабжения сердца с задней межжелудочковой ветвью, сформированной за счет правой КА. Левая КА (ЛКА) отходит от задней поверхности ЛС, делясь практически сразу на переднюю межжелудочковую ветвь (ПМЖВ) и огибающую ветвь (ОВ), с дальнейшим неизмененным распределением и ходом артерий.
Из характерных анатомических особенностей аномально отходящей ЛКА следует отметить, что ствол ЛКА очень короткий и может вообще отсутствовать, ЛКА и ее ветви не окружают ствол ЛА, как в норме, ЛКА может отходить от задней стенки ЛС в проекции заднего лицевого, нелицевого синусов легочного клапана, либо на их границе. Существует сеть коллатеральных сосудов, осуществляющих перетоки из системы правой КА в аномально отходящую левую КА. Как правило, это анастомозы между ветвями правой венечной артерии (конусная ветвь, ветвь острого края, задняя межжелудочковая ветвь и септальные коллатерали) и ПМЖВ. ПМЖВ и ОВ соединяются под острым углом (как и в сердцах со сформированной двухкоронарной системой кровоснабжения), а заполнение бассейна огибающей ветви ЛКА, в большинстве случаев, происходит ретроградно из ПМЖВ [4].
Вследствие нарушения эмбриологической закладки желудочкового комплекса при пороке формируется так называемая "доминантность" ЛЖ с соответствующими изменениями гемодинамики. Подобный феномен возникает при изменении пространственного взаимоотношения передней и задней межжелудочковых перегородок, формирующих при СБУГ угол равный в среднем 97° (+/- 7,6° +/- 1,1°). Подобные нарушения являются результатом смещения задней межжелудочковой перегородки в полость правого желудочка. В результате - полость правого желудочка уменьшается и в приточном, и в выводном отделах, а также резко сужается проходимость правого атриовентрикулярного отверстия за счет эквивалентного увеличения левого [3].
В основе нарушений гемодинамики при пороке лежит дефицит перфузии либо патологическое перераспределение крови со сниженным содержанием кислорода по системе ЛКА. Таким образом, особенности кровообращения при СБУГ зависят от соотношения давления в аорте и легочной артерии.
Во внутриутробном периоде аномальное отхождение ЛКА от ЛА не приводит к нарушению кровоснабжения миокарда ЛЖ - в обоих венечных сосудах имеется антеградный ток крови с примерно одинаковой оксигенацией. После рождения прогноз и манифестация заболевания определяются степенью развития межкоронарных анастомозов и выраженностью ишемии миокарда ЛЖ. Без хирургического лечения около 90% больных погибают в первый год жизни [3, 27, 30 - 32]. Причиной смерти при отсутствии хороших коллатералей между системами ЛКА и ПКА, является возникающая после рождения острая ишемия миокарда ЛЖ, вплоть до образования обширных инфарктов. Согласно данным статистики, частота инфаркта миокарда в детской популяции составляет, приблизительно, 20 случаев на 100 тыс. этой популяции. При этом летальность от острого инфаркта миокарда у детей младше 1 года составляет 0,2 на 100 тыс., и причиной этого в 20% случаев является именно аномальное отхождение ЛКА от ЛА [33]. Таким образом, при отсутствии своевременной диагностики и хирургической коррекции неонатальный период переживают только больные с хорошо развитой сетью коллатеральных сосудов. Однако, даже среди пациентов, переживших этот возраст, часты случаи так называемой внезапной смерти в результате ишемических повреждений миокарда и возникновения желудочковых аритмий [34]. Согласно данным литературы, 80 - 90% этих больных погибают внезапно в возрасте 35 лет [3, 16, 31, 33, 34]. Тем не менее, в литературе описаны случаи первичной диагностики порока у взрослых пациентов, даже старше 70 лет, единственным проявлением СБУГ в этих ситуациях являлись нарушения ритма или недостаточность МК [24, 34 - 39].
В соответствии со степенью нарушения гемодинамики Edwards J.I., впервые описавший патофизиологические изменения при СБУГ, предложил различать 3 фазы в клиническом течении заболевания. Первая включает в себя период плацентарного кровообращения и первые 6 - 8 недель жизни, когда, в силу высокого давления в ЛА, поддерживается достаточное давление в аномальном коронарном сосуде, и признаки коронарной недостаточности отсутствуют. Вторая или "критическая" фаза, обусловленная физиологическим снижением давления в ЛА, наступает в 6 - 8-недельном возрасте и длится, как правило, от 1,5 до 4 мес. Большинство детей погибают в этом возрасте вследствие ишемии миокарда, связанной со снижением кровотока по ЛКА [70, 71]. Выживают лишь дети с хорошо выраженной сетью межкоронарных анастомозов. Выживаемость в этом возрасте зависит как от скорости образования межкоронарных анастомозов и их плотности, так и от типа кровоснабжения сердца и скорости снижения давления в ЛА. На этом этапе диагностика порока уже возможна ввиду имеющихся характерных клинических симптомов. Третья фаза (фаза "компенсации"), характеризующаяся кровоснабжением бассейна ЛКА за счет перфузии ПКА и наличием ретроградного кровотока в аномальной венечной артерии, наблюдается у больных с хорошо развитой сетью межкоронарных коллатералей.
Некоторые авторы [59, 60] предлагали различать еще и 4-ую гемодинамическую стадию течения порока, в которой становление однокоронарной системы кровоснабжения уже закончено, и идет усиление синдрома обкрадывания вследствие увеличения сброса из правой КА в ЛА, что ведет к повторному нарастанию симптомов ишемии и резкому (иногда внезапному) ухудшению состояния вследствие развития выраженной сердечной недостаточности и жизнеугрожающих аритмий.
При сочетании СБУГ с другими внутрисердечными аномалиями гемодинамика порока может кардинальным образом изменяться. В одних случаях, сопутствующий ВПС может компенсировать коронарную аномалию (при сочетании с пороками сердца, сопровождающимися гиперволемией малого круга кровообращения), в других - отягчающим фактором выступает аномальное отхождение ЛКА (при пороках "синего" типа с недостаточным кровотоком в системе ЛА).
Б. Сообщения между КА и полостями сердца (КСФ) образуются в результате аномалии эмбрионального развития сосудов коронарно-артериального дерева.
КСФ происходят из ПКА примерно в 50 - 60% случаев, передней межжелудочковой ветви ЛКА - в 32% случаев и огибающей ветви ЛКА - в 18% случаев [11]. Более 90% фистул от КА впадают в правые отделы сердца. В правых отделах фистула впадает в правый желудочек в 40% случаев. Далее по частоте встречаемости следую правое предсердие, легочный ствол и коронарный синус [12], еще реже - левые отделы сердца [13, 14].
Фистулы могут локализоваться в любом участке КА, но чаще они располагаются в дистальных ее отделах, при этом сообщение бывает в виде одного или нескольких отверстий, в большинстве случаев имеющих небольшой диаметр. Артерия, как правило, бывает расширенной, извитой, а стенка истонченной. Это является следствием действия компенсаторного механизма в ответ на сброс крови в обход коронарного русла. В месте сообщения с полостью сердца эти изменения более выражены, имеют сходство с аневризматическим расширением сосуда [8 - 10]. Фистула чаще всего дренируется в полость сердца одним отверстием небольшого размера, при этом устье и проксимальный отдел артерии бывают расширенными, а дистальный отдел (в месте впадения) значительно суженным [8 - 10].
Гемодинамика при КСФ обусловлена сбросом крови из пораженной коронарной артерии в камеру сердца или магистральный сосуд [3, 8, 9]. Нарушение гемодинамики и развитие клинических симптомов определяются объемом сброса артериальной крови непосредственно в сердечную камеру, а также ухудшением кровоснабжения всей зоны миокарда, питаемой патологически измененной артерией, спонтанным разрывом фистулы, нарушением ритма сердца, развитием бактериального эндокардита [9, 40]. Объем шунтируемой через фистулу крови может достигать 50% минутного объема левого желудочка (ЛЖ), и лишь небольшая часть этой крови поступает в дистальное русло коронарной артерии [8, 9, 16, 41]. Величину миокардиального кровотока обусловливает разница сопротивлений на уровне отверстия фистулы и в интрамуральных миокардиальных сосудах. Поскольку сопротивление последних всегда выше, то при больших размерах фистулы через нее поступает большая часть артериальной крови, и определенная зона сердечной мышцы получает недостаточное кровоснабжение, что приводит к прогрессивному уменьшению диастолической перфузии миокарда. Аномальная коронарная артерия расширяется, формируются аневризмы, происходит дегенерация медии, ульцерация интимы, возникают трещины, атеросклеротические изменения и кальцификация, обструкция боковых ветвей, муральный тромбоз, а также разрыв артерии [5, 9, 41].
При сообщении с правыми сердечными камерами имеется сброс крови слева направо и соответствующая объемная перегрузка правых и левых отделов сердца, обусловленная градиентом давления системы венечного русла и дренажной камеры. Сообщение с левым желудочком и левым предсердием вызывает перегрузку левых камер сердца и в дальнейшем может привести к развитию недостаточности митрального и аортального клапанов [9, 42].
Следует отметить, что сердце довольно длительное время может переносить наличие коронарно-сердечного сообщения без существенного нарушения своей функции, хотя признаки очаговой ишемии миокарда могут наблюдаться как в зоне, расположенной дистальнее фистулы, так и во всей кровоснабжаемой артерией зоне [3, 8, 9, 15].
Коронарно-сердечные фистулы могут протекать без симптомов и не вызывать осложнений в первые два десятилетия жизни. Однако, несмотря на то, что большинство пациентов детского возраста с врожденными коронарно-сердечными фистулами асимптоматичны, этот порок в большинстве случаев представляет собой гемодинамически значимую коронарную аномалию, а с возрастом приводить к возникновению осложнений. К последним можно отнести синдром обкрадывания миокарда, тромбоз и эмболию, сердечную недостаточность, фибрилляцию предсердий и другие аритмии, эндокардит/эндартериит [8, 43]. Тромбоз фистулы встречается редко, но может вызвать инфаркт миокарда, пароксизмальную ФП и желудочковые аритмии [8]. Также возможен самопроизвольный разрыв аневризматического расширения фистулы, приводящий к гемоперикарду [8, 9, 12, 41]. В редких случаях КСФ могут закрываться спонтанно.
1.3 Эпидемиология заболевания или состояния (группы заболеваний или состояний)
А. Частота встречаемости аномального отхождения ЛКА от ЛА, согласно данным литературы, составляет 0,25 - 0,5% среди всех ВПС [4, 16 - 23]. По данным различных авторов порок встречается у 1 из 300 тыс. живых новорожденных [17 - 19, 22 - 26]. В то же время, среди всех пороков венечных артерий, данная патология встречается наиболее часто - в 90% всех случаев [3, 4, 16, 27].
Б. Частота встречаемости КСФ среди всех ВПС составляет 0,2 - 2%, а среди врожденных аномалий КА - вторую позицию после аномального отхождения коронарных артерий (48,7%) [2, 5, 6 - 10, 28, 29]. У 33000 пациентов, подвергнутых коронарографии, КСФ была выявлена в 0,1% случаев [15].
Данная патология может сочетаться с такими ВПС как критический клапанный стеноз легочной артерии, атрезия легочной артерии с интактной межжелудочковой перегородкой, периферические стенозы легочной артерии, коарктация и перерыв дуги аорты, а также с различными коронарными заболеваниями и травматическими повреждениями сердца [2, 3, 10, 15].
Ятрогенные КСФ в структуре КСФ составляют 20 - 25%. Наиболее часто они развиваются после операций реконструкции путей оттока из правого желудочка при ВПС, сопровождающихся обеднением кровотока в малом круге кровообращения (тетрада Фалло, атрезия ЛА, изолированный стеноз ЛА) [9, 15].
1.4 Особенности кодирования заболевания или состояния (группы заболеваний или состояний) по Международной статистической классификации болезней и проблем, связанных со здоровьем
Q24.5 - аномалия развития коронарных сосудов
1.5 Классификация заболевания или состояния (группы заболеваний или состояний)
А. Выделяют 2 варианта аномалии отхождения ЛКА от ЛА (СБУГ), различные по клинико-инструментальным показателям и прогнозу [45]:
1. инфантильный
2. взрослый.
Инфантильный тип - встречается в 85 - 90% всех случаев аномалии и характеризуется отхождением ЛКА от ЛА и отсутствием хорошо развитых коллатералей между системой правой и левой венечных артерий, вследствие чего сразу после рождения ребенка развивается серьезное ишемическое поражение миокарда ЛЖ со снижением его сократительной способности и дилатацией полости. Также возникает недостаточность митрального клапана (МК) за счет ишемии папиллярных мышц и дилатации фиброзного кольца [46, 47].
Частота встречаемости "взрослого" типа СБУГ составляет 10 - 15% [17, 23, 40, 47, 48]. При данном типе порока ЛКА также отходит от ЛА, но имеется сеть многочисленных и хорошо развитых межсосудистых анастомозов в системе коронарных артерий. При подобном типе порока отмечается доминантность правой КА, а сообщение между ЛКА и ЛА является рестриктивным (рис. 3Б) [41, 45 - 47].
Б. Существуют несколько классификаций КСФ:
I. По этиологии:
1. Врожденные изолированные.
2. Врожденные в сочетании с другими ВПС:
- СГЛС с атрезией аорты;
- АЛА с ИМЖП;
- ТФ;
3. Приобретенные:
- после радикальной коррекции ТФ с резекцией мышечного пучка;
- вследствие травмы грудной клетки;
- после эндомиокардиальной резекции/биопсии;
- после РЧА;
- как осложнение ЧКВ.
II. В зависимости от отхождения КА:
1. ПКА - 40 - 50%.
2. ПМЖВ - 30 - 40%.
3. ОВ - 10 - 20%.
4. Ствол ЛКА - 10 - 20%.
5. Единственная коронарная артерия <*> [10, 49].
--------------------------------
<*> - единичные описания случаев
III. В зависимости от размера КСФ:
1. Малые - меньше диаметра дистального отдела коронарной артерии.
2. Средние - > 1 - 2 раза больше дистального отдела коронарной артерии.
3. Большие - > 2 - 3 раза дистального отдела коронарной артерии [50].
1.6 Клиническая картина заболевания или состояния (группы заболеваний или состояний)
А. Клиническая картина инфантильного типа течения СБУГ может проявиться сразу после рождения развитием терминального состояния вследствие обширного инфаркта миокарда либо множественных инфарктов (у некоторых младенцев - с кардиогенным шоком). При более благоприятном течении заболевания первые симптомы могут манифестировать в первые 3 месяца жизни, реже - во втором полугодии. Первыми признаками являются нарушение общего состояния - вялость, бледность кожных покровов, повышенная потливость, рвота, срыгивания, одышка и тахикардия. У половины малышей отмечаются приступы внезапного резкого беспокойства с усилением одышки, бледности, потливости - именно они иногда становятся первыми признаками болезни. Как правило, приступы беспокойства возникают после или во время кормления и могут длиться несколько минут. В промежутках между приступами ребенок выглядит вполне здоровым, и настораживающим фактором может явиться только наличие одышки. В литературе эти приступы носят название "стенокардия кормления" из-за сходства с клиникой стенокардии у взрослых. Общность явлений подтверждается и данными аутопсии (признаки старых и свежих инфарктов миокарда).
Многие дети на этой стадии заболевания отстают в физическом развитии. У них рано развивается левосторонний сердечный горб. С ростом ребенка к клиническим проявлениям порока присоединяется митральная недостаточность, возникающая вследствие хронической ишемии или инфаркта папиллярных мышц, дилатации полости ЛЖ и деформации створок клапана. В ряде клинических случаев (при серьезном ишемическом поражении клапанных и подклапанных структур) регургитация на МК может развиваться и в более раннем (грудном) возрасте, маскируя проявления основного порока, что может привести к диагностической ошибке и неправильной хирургической тактике [51]. Таким образом, на этой стадии заболевания у ребенка превалируют признаки сердечной недостаточности преимущественно по левожелудочковому типу, а клиническая картина "инфантильного" типа порока у детей младшей возрастной группы может напоминать таковую при миокардите, дилатационной кардиомиопатии, врожденной недостаточности МК или обструктивном поражении выводного отдела ЛЖ (стеноз аорты, коарктация аорты).
При "взрослом" типе порока отмечается доминантность правой КА, а сообщение между ЛКА и ЛА является рестриктивным [45, 52 - 54]. Родители детей, как правило, не предъявляют жалоб, свидетельствующих о заболевании сердца, а развитие ребенка может соответствовать возрасту. При подобном компенсированном течении порока клинические проявления могут длительно отсутствовать и проявиться уже в подростковом и/или даже взрослом возрасте. Первыми симптомами СБУГ у подростков могут быть плохое самочувствие или же появление дискомфорта в области сердца при спортивных занятиях, в редких случаях возможно возникновение типичных загрудинных стенокардитических болей. В отдельных случаях порок протекает настолько малосимптомно, что впервые выявляется у взрослых в возрасте 50 - 60 лет при проведении стандартной электрокардиографии в связи с инфарктом миокарда и/или проведении коронарографии [33]. Важным моментом при подобном клиническом варианте течения порока является то, что даже при отсутствии клинических симптомов имеет место прогрессирование ишемии миокарда, что связано с наличием коллатерального кровотока между ПКА и ЛКА на уровне высокого деления коронарных артерий - 2 - 3 порядка, а миокард, кровоснабжаемый более мелкими венечными артериями, продолжает испытывать гипоксию. Потому в этой подгруппе пациентов в 80 - 90% случаев существует риск внезапной сердечной смерти [31, 32, 34, 36, 52, 53], а диагноз СБУГ является находкой на аутопсии.
У взрослых нередко первыми проявлениями порока могут явиться нарушения ритма, что может привести к диагностической ошибке. Вследствие этого диагностический алгоритм обследования таких пациентов должен быть расширен с привлечением методов диагностики, позволяющих выявить скрытую ишемию миокарда и коронарную аномалию [52].
В литературе встречается описание единичных случаев первичной диагностики СБУГ у пожилых больных при обследовании их в связи с наличием нарушений ритма или митральной недостаточности [24, 34, 36 - 40]. Подобные ситуации являются казуистикой в кардиологической практике.
Б. Клинические проявления КСФ малоспецифичны, зависят от ее размеров и величины коронарного сброса крови. Наиболее частой жалобой является появление несоответствующей обычной нагрузке одышки, связанной с постепенным увеличением фистулы, нарастанием степени легочной гипертензии и усилением сброса крови "слева - направо" [2, 5, 8 - 10, 16].
По сравнению с взрослыми у детей бессимптомные фистулы встречаются редко. Описаны случаи, когда КФ диагностируется в неонатальном периоде [5]. Средние по величине и большие КСФ могут приводить к появлению продолжительного шума. Приступы стенокардии у детей грудного возраста распознаются по появлению раздражительности, потливости, бледности, одышки и тахикардии. У детей КСФ часто манифестируют в возрасте 2 - 3 месяцев, когда снижается сопротивление легочных сосудов. В старшем возрасте могут быть проявления сердечной недостаточности, аритмии, синкопе, боль в грудной клетке, изредка эндокардит. При большой величине сброса крови может появляться картина застойной сердечной недостаточности и стенокардия.
К числу заболеваний, с которыми обычно приходится дифференцировать КСФ, относят:
- аномальное отхождение ЛКА от ЛА;
- артериовенозные легочные фистулы;
- инфаркт миокарда у детей;
- открытый артериальный проток;
- аневризма синуса Вальсальвы;
- дефект межжелудочковой перегородки.
Взрослых пациентов, обратившихся за медицинской помощью, наиболее часто беспокоят одышка, боли в области сердца при физической нагрузке, перебои в работе сердца. При клиническом обследовании больных могут быть выявлены увеличенные размеры сердца, постоянный систолодиастолический шум с максимальным звучанием в третьем - четвертом межреберье. Данные признаки являются показаниями к проведению обследования.
2. Диагностика заболевания или состояния (группы заболеваний или состояний) медицинские показания и противопоказания к применению методов диагностики
Диагноз аномалии КА верифицируется на основании сводных данных жалоб родителей пациентов, клинических проявлений порока, данных лабораторных и инструментальных методов исследования.
Диагноз устанавливается на основании данных:
1. Регистрация электрокардиограммы;
2. Эхокардиографии;
3. Ретроградной катетеризации левых отделов сердца с коронарографией и панаортографией;
4. Сцинтиграфии миокарда;
5. Однофотонной эмиссионной компьютерной томографии миокарда перфузионной;
6. Спиральной компьютерной томографии сердца с ЭКГ-синхронизацией;
7. Магнитно-резонансной томографии сердца и магистральных сосудов.
2.1 Жалобы и анамнез
- Рекомендуется на этапе диагностики сбор анамнеза и жалоб у всех пациентов (родителей пациентов) с подозрением на аномалии КА с целью верификации диагноза, определения тяжести состояния и тактики лечения [2, 5, 10, 16, 50, 54, 56].
(УУР C, УДД 4)
Комментарии: При наличии у пациента со СБУГ взрослого типа порока жалобы могут отсутствовать. Данный тезис также правомочен для детей с малыми размерами КСФ.
- Рекомендуется при сборе анамнеза и жалоб у всех пациентов (родителей пациентов) с подозрением на аномалии КА расспросить о наличии у ребенка отставания в физическом развитии, повышенной потливости, одышки, учащенного сердцебиения, приступах беспокойства со срыгиванием во время или же сразу после кормления ("стенокардия кормления") для уточнения степени тяжести состояния [16, 27, 30, 33, 35, 50, 54, 56].
(УУР C, УДД 4)
Комментарии: Подобные жалобы могут быть свидетельством наличия у ребенка инфантильного типа течения СБУГ или же гемодинамически значимых КСФ больших размеров, требующих неотложной диагностики и последующего хирургического вмешательства.
- Рекомендуется при сборе анамнеза и жалоб у всех пациентов (родителей пациентов) с подозрением на аномалии КА расспросить о появлении дискомфорта в области сердца или типичных загрудинных стенокардитических болей при повышенной физической нагрузке или занятии спортом с целью верификации диагноза, определения тяжести состояния и тактики лечения [16, 23, 27, 30, 33, 35, 50, 54, 56].
(УУР C, УДД 4).
- При осмотре у всех пациентов с подозрением на аномалии КА рекомендуется обратить внимание на наличие деформации грудной клетки в виде сердечного горба с целью определения гемодинамической значимости выявленной аномалии [23, 27, 30, 33, 35, 51, 56, 57].
(УУР C, УДД 5)
Комментарии: При неблагоприятном клиническом течении СБУГ (инфантильном типе порока) возможно раннее образование левостороннего сердечного горба на фоне быстрого развития дилатации ЛЖ сердца.
2.2 Физикальное обследование
- Рекомендуется у всех пациентов с подозрением на аномалии КА во время физикального обследования обратить внимание на пальпацию при патологии сердца и перикарда и перкуссию при патологии сердца и перикарда области сердца с целью верификации диагноза [27, 30, 33, 35, 51, 56, 57].
(УУР C, УДД 5)
Комментарии: При аномальном отхождении ЛКА от ЛС пальпаторно может определяться разлитой верхушечный толчок, ослабленный, смещенный в шестое межреберье. При перкуссии выявляется расширение границ сердца, преимущественно влево. При КСФ среднего и большого размера также может наблюдаться перкуторное расширение границ сердца в основном за счет левых отделов.
- Рекомендуется у всех пациентов с подозрением на аномалии КА во время физикального обследования выполнить аускультацию при патологии сердца и перикарда с целью оценки степени выраженности сброса крови на уровне КСФ/аномального отхождения ЛКА от ствола ЛА или выявления сопутствующих врожденных пороков сердца [23, 27, 30, 33, 35, 51, 56, 57].
(УУР C, УДД 5)
Комментарии: При аускультации пациента с аномальным отхождением ЛКА от ЛА - тоны сердца, как правило, приглушены, какие-либо шумы могут не выслушиваться на первом году жизни. Ко 2 - 3-ему году жизни над областью сердца может появиться продолжительный негрубый систолический шум с максимумом во втором межреберье слева, напоминающий шум при ОАП и отражающий сброс крови из ЛКА в легочную артерию. С ростом ребенка к клиническим проявлениям порока присоединяется митральная недостаточность, возникающая вследствие хронической ишемии или инфаркта папиллярных мышц, дилатации полости ЛЖ и деформации створок клапана. В результате - аускультативно начинает выслушиваться систолический шум недостаточности МК с максимумом на верхушке сердца.
При аускультации КСФ средних и больших размеров может выслушиваться продолжительный шум, напоминающий таковой при открытом артериальном протоке, но нетипичной локализации (ниже у края грудины), с усилением шума в средней/поздней фазе диастолы, а не в период систолы, как у больных с открытым артериальным протоком. При больших фистулах определяется патологический III тон. Тоны сердца часто приглушены. На верхушке может выслушиваться голосистолический шум митральной недостаточности.
2.3 Лабораторные диагностические исследования
- Рекомендуется исследование кислотно-основного состояния и газов крови (pH, BE, pCO2, PO2, Lac - анализ капиллярной/артериальной/венозной проб) для новорожденных с аномалиями КА в тяжелом состоянии с целью оценки степени выраженности метаболических нарушений [103 - 105].
(УРР C, УДД 5)
- Рекомендуется всем пациентам с аномалиями КА выполнение общего (клинического) анализа мочи и общего (клинического) анализа крови с исследованием уровня общего гемоглобина в крови и оценкой гематокрита, исследованием уровня эритроцитов, лейкоцитов, тромбоцитов в крови, исследованием скорости оседания эритроцитов в рамках первичного обследования, при поступлении в стационар, в т.ч. для оперативного лечения, в процессе динамического наблюдения не менее 1 раза в год, а также в послеоперационном периоде при необходимости с целью исключения сопутствующей патологии [56, 60, 99, 118].
(УУР C, УДД 5)
Комментарий: Проведение общего (клинического) анализа крови всем пациентам с аномалиями развития коронарных сосудов при диспансерном наблюдении и перед проведением хирургического лечения важно с позиции выявления анемии и ее своевременной коррекции. У пациентов со средним объемом эритроцитов менее 80 фл целесообразно исследование уровня железа сыворотки крови, ферритина, трансферрина в крови и железосвязываюшей способности сыворотки с целью своевременной коррекции железодефицитных состояний. У пациентов со средним объемом эритроцитов более 100 фл целесообразно определение уровня витамина B12 (цианокобаламин) в крови и исследование уровня фолиевой кислоты в сыворотки крови с целью своевременной коррекции B12- или фолиеводефицитных состояний. Указанные выше состояния способны негативно отразиться на клинико-функциональном статусе и характере течения заболевания пациента, а также результатах оперативного лечения [99].
- Рекомендуется всем пациентам с аномалиями КА, поступающим в стационар для оперативного лечения, которым предполагается переливание донорской крови и (или) ее компонентов, определение основных групп крови по системе AB0, определение антигена D системы Резус (резус-фактор), определение фенотипа по антигенам C, c, E, e, Cw, K, k и определение антиэритроцитарных антител [97, 98].
(УУР C, УДД 5)
- Рекомендуется всем пациентам с аномалиями КА, поступающим в стационар для оперативного лечения определение антигена (HbsAg) вируса гепатита B (Hepatitis B virus) в крови; определение антител к вирусу гепатита C (Hepatitis C virus) в крови; определение антител к бледной трепонеме (Treponema pallidum) в крови; определение антител классов M, G (IgM, IgG) к вирусу иммунодефицита человека ВИЧ-1 (Human immunodeficiency virus HIV-1) в крови; определение антител классов M, G (IgM, IgG) к вирусу иммунодефицита человека ВИЧ-2 (Human immunodeficiency virus HIV-2) в крови для исключения ассоциации с ВИЧ-инфекцией, гепатитом и сифилисом [60, 99 - 102].
(УУР C, УДД 5)
- Рекомендуется всем пациентам с аномалиями КА, поступающим в стационар для оперативного лечения, выполнение коагулограммы (ориентировочного исследования системы гемостаза) (активированное частичное тромбопластиновое время, исследование уровня фибриногена в крови, а также определение международного нормализованного отношения (МНО)) с целью исключения врожденных и приобретенных нарушений в системе свертывания крови, прогноза послеоперационных тромбозов и кровотечений [35, 56, 60, 99, 119, 120].
(УУР C, УДД 5)
- Рекомендуется проведение анализа крови биохимического общетерапевтического (исследование уровня калия, натрия, хлоридов, глюкозы, креатинина, общего белка, альбумина, мочевины, общего и связанного (конъюгированного) билирубина в крови, железа в сыворотке крови, определение активности аспартатаминотрансферазы и аланинаминотрансферазы в крови) для оценки почечной и печеночной функции у всех пациентов с аномалиями развития коронарных сосудов в рамках первичного обследования, при поступлении в стационар, в т.ч. для оперативного лечения, в процессе динамического наблюдения не менее 1 раза в год, а также в послеоперационном периоде при необходимости [56, 60, 106 - 108].
(УУР C, УДД 5)
- Рекомендуется исследования уровня N-терминального фрагмента натрийуретического пропептида мозгового (NT-proBNP) в крови у пациентов с СБУГ или другими аномалиями КА и предполагаемой хронической сердечной недостаточностью, ЛГ, при первичном обследовании и каждые 3 - 6 месяцев при поздней диагностике для определения риска летальности [109 - 114, 125 - 126].
(УУР C, УДД 4)
- Рекомендуется проведение анализа крови биохимического общетерапевтического (исследование уровня калия, натрия, хлоридов, глюкозы, креатинина, общего белка, альбумина, мочевины, общего и связанного (конъюгированного) билирубина в крови, железа в сыворотке крови, определение активности аспартатаминотрансферазы и аланинаминотрансферазы в крови) для оценки почечной и печеночной функции у всех пациентов с аномалиями развития коронарных сосудов в рамках первичного обследования, при поступлении в стационар, в т.ч. для оперативного лечения, в процессе динамического наблюдения не менее 1 раза в год, а также в послеоперационном периоде при необходимости [56, 60, 106 - 108].
(УУР C, УДД 5)
- Всем пациентам с аномалиями развития коронарных сосудов, которым после оперативного лечения проводится тромбопрофилактика препаратами гепарина и его производными (B01AB Группа гепарина), рекомендуется лабораторный контроль эффективности применения лекарственных препаратов [119, 121 - 123].
ЕОК нет (УУР D, УДД 3)
Комментарии: При применении нефракционированного гепарина (гепарин натрия**, B01AB Группа гепарина) необходимо выполнять определение АЧТВ (оптимальный диапазон значений у взрослых - 40 - 60 с, у детей - 60 - 85 сек) и анти-Xa активности (оптимальный диапазон - 0,35 - 0,7). При применении препаратов низкомолекулярного гепарина (B01AB Группа гепарина) необходимо применять определение анти-Xa активности (оптимальный диапазон - 0,5 - 1,0) [119, 121 - 123].
2.4 Инструментальные диагностические исследования
- Рекомендуется всем пациентам с подозрением на аномалии коронарных сосудов регистрация электрокардиограммы для определения признаков ишемии миокарда, перегрузки левых и правых отделов сердца, оценки сердечного ритма и проводимости [5, 8, 10, 21, 23, 51, 56, 62 - 64].
(УУР C, УДД 4).
Комментарии: Характерными ЭКГ-признаками, свидетельствующими о наличии аномального отхождения ЛКА от ЛС являются [66, 70, 76, 81, 86] глубокий (> 3 мм) и расширенный (> 30 мс) зубец Q в отведениях I, aVL, V5 - 6, сочетание глубокого зубца Q с инвертированным зубцом T в отведении aVL (при свежем инфаркте), элевация сегмента ST выше изолинии и уменьшение амплитуды зубца R (при свежем инфаркте), "провал" амплитуды зубца R в отведениях V3 и V4 - формирование комплексов типа rS, QS, Qr (свидетельствует о ранее перенесенном инфаркте миокарда и формировании рубца).
Дифференциальными ЭКГ признаками СБУГ от дилатационной кардиомиопатии и миокардита являются наличие зубца Q глубиной более 3 мм и шириной более 30 мс, по крайней мере, в одном из следующих отведений - I, aVL, V5 - 7, комплекс QR той же локализации, отсутствие зубца Q во II, III и aVF отведениях, элевация сегмента ST в отведении aVL [64].
В 15 - 20% случаев типичные ЭКГ-признаки СБУГ могут отсутствовать. Как правило, это касается пациентов старшего возраста и взрослых больных, имеющих хорошо развитые перетоки между ЛКА и ПКА и относительно сохранный миокард ЛЖ. В этой возрастной когорте вышеуказанные электрокардиографические критерии могут отсутствовать, быть "стертыми" и/или же проявляться только при проведении нагрузочных проб. Как уже указывалось ранее, нередко первым проявлением СБУГ у взрослых могут явиться различные нарушения ритма, представляющие риск развития "внезапной" сердечной смерти. Тем не менее, ЭКГ-признаки гипертрофии и перегрузки левых отделов присутствуют в 100% у всех пациентов со СБУГ.
При КСФ маленьких и средних размеров ЭКГ обычно нормальная. При значительных размерах фистулы могут быть проявления объемной перегрузки левого предсердия и левого желудочка; при коронарном обкрадывании - признаки ишемии и/или нарушения ритма [5, 8, 10, 56].
- Рекомендуется всем пациентам с подозрением на аномалии КА выполнение прицельной рентгенографии органов грудной клетки в прямой проекции для верификации диагноза и/или выявления патологии легких [4, 17, 27, 33, 35, 51, 54, 55, 57].
(УУР C, УДД 4)
Комментарии: Прицельная рентгенография органов грудной клетки является самым простым и общедоступным методом, позволяющим заподозрить аномальное отхождение ЛКА еще до появления первых клинических симптомов. Анализ рентгенограмм включает в себя оценку состояния легочного рисунка и размеров сердца [51, 55, 57].
У больных с СБУГ легочный рисунок может быть не изменен и/или же усилен по "венозному" типу, что свидетельствует о наличии митральной недостаточности и снижении насосной функции ЛЖ. В том случае, если у пациента имеет место длительно существующая прогрессирующая митральная недостаточность на фоне СБУГ, возможно формирование рентгенологических признаков хронического альвеолярного отека легких.
Кардиомегалия может явиться одним из первых маркеров, настораживающих врача в отношении возможной коронарной аномалии и заставляющих расширить диагностический алгоритм, что может способствовать своевременной диагностике порока. Увеличение размеров сердца является патогномоничным симптомом для больных с аномальным отхождением ЛКА от ЛА, особенно в период новорожденности и грудном возрасте [4, 17, 27, 33, 35, 51, 54, 55, 57].
При анализе прицельной рентгенографии органов грудной клетки у больных с КСФ обычно отклонений нет, но при больших фистулах может определяться кардиомегалия, признаки венозного типа застоя, интерстициального отека легких [56].
- Рекомендуется всем пациентам с подозрением на аномалии КА выполнение эхокардиографии (Эхо-КГ) с применением режима цветного допплеровского картирования с целью определения наличия и гемодинамической значимости аномалии КА [66 - 80].
(УУР C, УДД 4)
Комментарии: Эхокардиография, включающая в себя одно-, двухмерное и допплерэхокардиографическую методики, является одним из важнейших методов диагностики порока, позволяющим неинвазивно оценить анатомию отхождения КА, размеры камер сердца, морфологическое состояние атриовентрикулярных клапанов и функцию миокарда, а также дать качественную и количественную оценку гемодинамических параметров внутрисердечного кровотока.
Эхо-КГ дает возможность визуализировать устья и проксимальные отделы КА: ПКА, ЛКА, бифуркацию, определять диаметр этих отделов, визуализировать место отхождения КА [66 - 70], оценивать размеры полостей сердца и сократительную способность (глобальную или регионарную) ЛЖ, признаки фиброэластоза эндокарда [71 - 73]. При СБУГ цветное двухмерное допплеровское картирование регистрирует кровоток в ЛКА и ретроградный кровоток из ЛКА в проксимальный отдел легочного ствола [74 - 76], визуализирует патологический диастолический кровоток по межжелудочковой перегородке, связанный с дилатированными межкоронарными коллатералями [77, 78], а также может выявлять антеградный кровоток, направленный из ЛА в аномально отходящую ЛКА [70].
Отмечено 9 косвенных допплерэхокардиографических признаков, наличие которых может свидетельствовать об аномальном отхождении ЛКА от ЛА, а именно: выраженная дилатация ЛЖ (в 95% случаев), снижение насосной функции ЛЖ (68% случаев), формирование аневризмы ЛЖ (47% случаев), уплотнение эндокарда ЛЖ (42% случаев), расширение фиброзного кольца МК (95% случаев), недостаточность МК (97% случаев), расширение устья и проксимального отдела ПКА (68% случаев), отсутствие визуализации устья ЛКА в месте ее обычного отхождения (100% случаев), систолодиастолический поток в ЛА по данным Эхо-КГ (79% случаев) [79, 80].
Также при проведении Эхо-КГ важным моментом является оценка функционального состояния МК, ибо он может явиться "мишенью" для хирургических манипуляций при хирургической коррекции основного порока.
Эхо-КГ исследование у больного с КСФ в большинстве случаев позволяет диагностировать коронарные фистулы. Эхокардиографическими признаками КСФ могут являться:
увеличение левого предсердия и левого желудочка в результате шунтирования значительного объема крови, локальное или диффузное снижение сократимости ЛЖ вследствие ишемии;
расширение коронарных артерий;
высокоскоростной поток крови, выявляемый при цветной допплерографии в месте отхождения или по ходу сосуда;
место дренирования фистулы может проявляться при тщательном исследовании, как зона турбулентного кровотока, как правило, в правом желудочке;
голодиастолический поток в нисходящей аорте;
расширение коронарного синуса при впадении в него фистулы.
- Рекомендуется всем пациентам с диагностированными аномалиями КА выполнение ретроградной катетеризации левых отделов сердца с коронарографией и панаортографией (АКГ) [16, 23, 27, 51, 56, 127].
(УУР C, УДД 5)
Комментарии: Ангиографическая семиотика аномального отхождения ЛКА от ЛА включает в себя оценку отхождения коронарных артерий, оценку типа кровоснабжения миокарда в зависимости от периферического ветвления и окончания коронарных артерий, анализ степени развития межкоронарных коллатералей, определение направленности коронарного кровотока.
Существующие варианты клинического течения СБУГ ("инфантильный" и "взрослый" типы) во многом определяют результат АКГ-исследования и специфичность ангиографической картины.
При инфантильном типе при выполнении панаортографии и/или селективной правой коронарографии обнаруживается единственная расширенная ПКА, отходящая от правого синуса Вальсальвы. ЛКА заполняется ретроградно по системе межкоронарных анастомозов со сбросом крови в ЛА. О развитии коллатералей можно судить по степени расширения и извитости обоих КА, быстроте заполнения системы ЛКА и объему сброса в ЛА. Для данного типа порока характерно наличие узкой ЛКА, заполняющейся ретроградно из бассейна ПКА по системе слабо развитых коллатералей. Сброс крови из ЛКА в ЛА, как правило, не превышает 15 - 20%, а в ряде случаев может не определяться. Иногда он может быть настолько небольшим и быстрым, что при анализе ангиограммы в прямой проекции может сложиться впечатление отхождения ЛКА от Ао. В сомнительных случаях решающей может оказаться оценка боковой проекции, позволяющей увидеть устье ЛКА в проекции задней стенки ЛА.
При взрослом типе при введении контраста в аорту и/или селективно в устье ПКА также обнаруживается единственная КА, отходящая от аорты, резко расширенная и извитая. ЛКА имеет вид резко расширенного извитого сосуда, быстро ретроградно заполняется из бассейна ПКА через множественные, хорошо развитые коллатерали. Из ЛКА контрастное вещество поступает в ЛА с контрастированием ЛС и ветвей. Объем сброса артериальной крови из ЛКА в ЛА может быть гемодинамически значимым, приводящим к повышению давления в системе ЛА.
Вентрикулография сердца при СБУГ дает возможность оценить функциональное состояние ЛЖ, в частности: обнаружить регионарные нарушения функции ЛЖ в виде локальных ограниченных участков акинезии, гипокинезии и дискинезии, диагностировать аневризму ЛЖ и оценить ее локализацию и размеры, выявить внутриполостные образования (пристеночные тромбы и опухоли), рассчитать важные и информативные показатели гемодинамики - КСО и КДО, ударный объем (УО), минутный объем (МО), сердечный индекс (СИ), УИ (ударный индекс), показатели насосной функции ЛЖ - фракцию выброса (ФВ) и конечно-диастолическое давление в ЛЖ, оценить визуально регургитацию на МК.
При выполнении вентрикулографии сердца у пациентов с "инфантильным" типом СБУГ выявляются резкое расширение левого желудочка и предсердия, слабые сокращения ЛЖ, почти полное отсутствие сокращений верхушечной зоны сердца с ее выбуханием, напоминающим аневризму ЛЖ, недостаточность МК различной степени выраженности. Вентрикулография сердца при "взрослом" типе порока, в большинстве случаев не выявляет зон асинергий ЛЖ, регургитация на МК, как правило, минимальная [16, 23, 27, 51, 55 - 57].
Для пациентов с диагностированными КСФ АКГ-исследование и коронарография остаются методами выбора для оценки строения КА и коронарного кровотока. Кроме того, катетеризации полостей сердца и сосудов может проводиться с лечебной целью эмболизация КСФ. Данные диагностической ретроградной катетеризации левых отделов сердца позволяют оценить гемодинамическое значение КСФ и обеспечивают детальную ангиографическую характеристику аномального сосуда, что является отправной точкой для выбора тактики лечения. Проведение данных методов исследования позволяют оценить количество фистул, характер питающего фистулу сосуда или сосудов, места дренирования, количество миокарда, который может пострадать при развитии ишемии, и гемодинамическое значение шунта [16, 56].
- Рекомендуется пациентам с диагностированным аномальным отхождением ЛКА от ЛА выполнение сцинтиграфии миокарда (перфузионной) [51, 55 - 57, 81, 82, 124].
(УУР C, УДД 4)
Комментарии: Для больных с аномальным отхождением ЛКА от ЛА по данным сцинтиграфии миокарда характерно снижение перфузии преимущественно в области передней (92%) и переднебоковой (85%) стенок ЛЖ [81, 82], а в ряде случаев, перфузионные дефекты могут распространяться на область верхушки, переднюю часть межжелудочковой перегородки, заднебоковую и даже заднюю стенку ЛЖ. При наличии хорошо развитых коллатералей между ПКА и ЛКА дефект перфузии может ограничиться областью передней и переднебоковой стенок. Слабое развитие межкоронарных анастомозов ведет к большему распространению дефектов перфузии с захватом задней стенки. Поэтому обнаружение распространенных перфузионных нарушений с захватом задних и заднебоковых отделов ЛЖ у маленьких детей может расцениваться как неблагоприятный прогностический признак.
Помимо высокой диагностической ценности у больных со СБУГ сцинтиграфия миокарда имеет большое значение для оценки результатов выполненных хирургических вмешательств. У больных с жизнеспособным миокардом улучшается регионарная и глобальная сократительная функция миокарда ЛЖ. Причем, это наблюдается как после перевязки или ушивания аномально отходящей ЛКА (A16.12.014 перевязка сосуда), так и после выполнения маммарно-коронарных анастомозов (A16.12.004.001 коронарное шунтирование в условиях искусственного кровообращения), и после прямой имплантации ЛКА в Ао (A16.12.004 наложение анастомоза на коронарные сосуды).
Данное исследование не является "идеальным" прогностическим маркером для больных с аномальным отхождением ЛКА от ЛА. Обычно дефекты накопления РФП, выявленные в покое, трактуются как рубцовые изменения, что, при отсутствии данных о состоянии метаболизма в этой области, может привести к гипердиагностике и неправильной хирургической тактике [81]. Именно поэтому важно сопоставлять данные сцинтиграфии миокарда с показателями метаболизма миокарда, полученными с помощью позитронно-эмиссионной томографии миокарда (ПЭТ).
- Рекомендуется пациентам с диагностированным аномальным отхождением ЛКА от ЛА выполнение ПЭТ совмещенной с компьютерной томографией миокарда с контрастированием (с флудезоксиглюкозой [18F] (18F-ФДГ)) [51, 56, 57, 81] с целью оценки его перфузии.
(УУР C, УДД 4)
Комментарии: Принцип метода ПЭТ совмещенной с компьютерной томографией миокарда с контрастированием (с 18F-ФДГ) заключается в том, что нормальная или повышенная аккумуляция 18F-ФДГ (аналога обычной глюкозы), возможна только в жизнеспособном миокарде [81].
Использование метода ПЭТ совмещенной с компьютерной томографией миокарда с контрастированием при обследовании больных с аномальным отхождением ЛКА от ЛА позволяет выявлять жизнеспособный миокард в состоянии гиперметаболизма, мелкоочаговые рубцовые изменения в сочетании с жизнеспособным миокардом, крупноочаговые рубцовые изменения. Последние из двух состояний могут сочетаться с наличием гиперметаболического миокарда в других сегментах ЛЖ.
Помимо этого, возможности метода позволяют рассчитать площади гибернированного миокарда и рубцовых изменений, в том числе, и площадь аневризмы. Полученные в результате ПЭТ-исследования данные позволяют сделать выбор хирургической тактики и имеют большое прогностическое значение для результатов. Немаловажным является возможность использования ПЭТ совмещенной с компьютерной томографией миокарда с контрастированием для оценки функциональных результатов выполненной реконструкции коронарного русла в отдаленные сроки после операции [51].
- Рекомендуется пациентам с диагностированными аномалиями КА проведение спиральной компьютерной томографии сердца с ЭКГ-синхронизацией (КТ-коронарографии) [51, 55 - 57, 83, 84, 124, 128 - 130].
(УУР C, УДД 4)
Комментарии: Выполнение КТ коронарографии рекомендуется для уточнения анатомии коронарных сосудов. КТ коронарография превосходит все методы лучевой диагностики в оценке анатомии коронарных артерий. Приоритетное значение КТ коронарографии заключается в превосходном пространственном разрешении [51, 55 - 57, 83, 84].
- Рекомендуется выполнение магнитно-резонансной томографии (МРТ) сердца с контрастированием и МРТ сердца и магистральных сосудов пациентам при сложных ВПС для определения тактики и сроков хирургического вмешательства у пациентов в стабильном состоянии и при рутинном обследовании после операции, срок и кратность проведения определяется в индивидуальном порядке (3 - 5 лет) в зависимости от данных ЭхоКГ при ежегодном наблюдении для получения объемных данных сердца, определения функции желудочков и объема регургитации [51, 55 - 57].
(УУР C, УДД 5)
Комментарии: МРТ (магнитно-резонансная томография сердца и магистральных сосудов) является наиболее точным методом оценки функции сердца и методом, визуализирующим фиброз миокарда. МРТ (магнитно-резонансная томография сердца и магистральных сосудов) в настоящее время рассматривается как "золотой стандарт" визуализации для оценки функции камер сердца. МРТ является уникальным методом, позволяющим при использовании контрастирования неинвазивно оценить очаговый и диффузный фиброз миокарда.
2.5 Иные диагностические исследования
- Рекомендуется перед выпиской из стационара всем пациентам с аномалиями КА с целью контроля после выполненного оперативного вмешательства выполнить регистрацию электрокардиограммы для выявления наличия возможных нарушений ритма и проводимости [5, 8, 17, 31, 32, 51, 55 - 57].
(УУР C, УДД 4)
- Рекомендуется перед выпиской из стационара всем пациентам с аномалиями КА с целью контроля после выполненного оперативного вмешательства выполнить ЭхоКГ с целью оценки эффективности хирургической коррекции порока [5, 8, 17, 31, 32, 51, 55 - 57].
(УУР C, УДД 4)
3. Лечение, включая медикаментозную и немедикаментозную терапии, диетотерапию, обезболивание, медицинские показания и противопоказания к применению методов лечения
3.1 Консервативное лечение
Единственным признанным эффективным вариантом лечения сердечной недостаточности у пациентов с аномальным отхождением ЛКА от ЛС остается хирургическая коррекция порока. Однако, у пациентов, имеющих выраженные проявления недостаточности кровообращения на фоне данного ВПС, показано назначение медикаментозной терапии, направленной на лечение сердечной недостаточности. Грамотное и своевременное назначение соответствующих фармакологических средств способствует стабилизации состояния больного, а в ряде случаев улучшению клинического статуса, что позволяет выполнить хирургическую коррекцию порока на более благоприятном фоне.
- Пациентам с аномалиями развития коронарных сосудов с высоким риском тромбоза после проведенного оперативного лечения рекомендуется тромбопрофилактика препаратами низкомолекулярного или нефракционированного гепарина (B01AB группа гепарина) [119, 121 - 123].
(УУР C, УДД 5)
Комментарии: К группе высокого риска тромбозов относятся пациенты с эпизодами тромбозов в анамнезе, тромбофилиями, инфекционными осложнениями, полиорганной недостаточностью [119].
Тромбопрофилактика #гепарином натрия** должна быть инициирована болюсом, который у детей - 75 МЕ/кг с последующей внутривенной инфузией со скоростью: у детей младше 1 года - 28 МЕ/кг, у детей старше 1 года - 20 МЕ/кг, у взрослых - 18 МЕ/кг. Коррекция дозы производится на основании результатов лабораторных исследований [119].
Тромбопрофилактика препаратами гепарина и его производными (B01AB группа гепарина) проводится из расчета: #эноксапарин натрия** (off-label у детей до 18 лет) у детей младше 2 месяцев - 0,75 мг/кг, у детей старше 2 месяцев - 0,5 мг/кг, через 12 часов подкожно, #далтепарин натрия - у детей от 1 месяца до 2 лет 150 Ед/кг, от 2 до 8 лет - 125 Ед/кг, старше 8 лет - 100 Ед/кг, через 12 часов подкожно. #Фондапаринукс натрия** может применяться у детей старше 1 года (off-label у детей до 17 лет) в дозе 0,1 мг/кг в сутки подкожно. Коррекция дозы производится на основании результатов лабораторных исследований [119, 121, 123].
3.2 Хирургическое лечение
- Рекомендуется хирургическая коррекция аномального отхождения ЛКА от ЛА всем пациентам сразу же после установки инструментально подтвержденного диагноза порока с целью коррекции выявленной аномалии [16, 17, 21, 23, 24, 31, 32, 35, 39, 51, 55 - 57].
(УУР C, УДД 5)
Комментарии: Выбор метода оперативного вмешательства определяется в первую очередь анатомией порока (особенности венечно-артериальной системы, локализация устья левой коронарной артерии по отношению к легочному стволу, а также наличием осложнений в виде митральной регургитации и аневризмы левого желудочка), клиническим состоянием больного, а также опытом и приверженностью врача-хирурга одной из методик.
В настоящее время существует два варианта подходов к хирургическому лечению аномального отхождения ЛКА от ЛА. Первый - рассчитан на прекращение сброса крови по аномально отходящей ЛКА и, соответственно, приводящий к повышению перфузионного давления в венечно-артериальной системе. Это достигается путем перевязки либо ушивания устья ЛКА, а кровоснабжение сердца осуществляется за счет одной коронарной артерии. Второй - направлен на восстановление нормального артериального кровотока в системе венечных артерий (а, следовательно, нормализацию перфузии поврежденного миокарда) путем прямой или непрямой (при помощи внутрилегочного тоннеля) имплантации аномально отходящей коронарной артерии в аорту (A16.12.004 наложение анастомоза на коронарные сосуды) или же создание анастомоза между системной и венечной артериями с помощью различного рода аллотрансплантатов.
- При выборе метода хирургического лечения аномального отхождения ЛКА от ЛА рекомендуется восстановление двухкоронарной системы кровоснабжения миокарда с целью создания физиологичного кровотока в системе коронарных артерий [16, 17, 31, 32, 35, 51, 55 - 57].
(УУР C, УДД 4)
Комментарии: Восстановление двухкоронарной системы кровоснабжения миокарда с использованием различных методик является в настоящее время "золотым стандартом" в хирургическом лечении синдрома Бланд-Уайт-Гарланда. Предпочтительной методикой нормализации коронарного кровотока у маленьких детей является прямая имплантация левой венечной артерии в аорту (A16.12.004 наложение анастомоза на коронарные сосуды).
- При неблагоприятной анатомии аномально отходящей ЛКА (короткий ствол, раннее деление на ветви) рекомендуется применение одной из модификаций прямой имплантации КА с использованием для удлинения ствола собственных тканей аорты и ЛС [51, 57, 85 - 90].
(УУР C, УДД 4)
Комментарии: Данные методики позволяют избежать натяжения реимплантируемой ЛКА, а также ее стенозирования при использовании имплантатов.
- У детей старшего возраста при невозможности выполнения операции прямой имплантации ЛКА в Ао рекомендуется выполнение маммаро-коронарного шунтирования (A16.12.004.001 коронарное шунтирование в условиях искусственного кровообращения) [16, 36, 38, 39, 51, 56, 57].
(УУР C, УДД 5)
Комментарии: Прямая имплантация левой коронарной артерии у детей старшего возраста может быть технически трудна и опасна вследствие снижения эластичности сосуда, затрудняющего ее мобилизацию, что приводит к неравномерному натяжению, а также несет высокий риск развития кровотечения. В этих случаях предпочтительным является шунтирование аномальной ЛКА внутренней грудной артерией.
- При хирургической коррекции аномального отхождения левой коронарной артерии от ЛА всем пациентам, имеющим исходную недостаточность митрального клапана с регургитацией более 2 степени (средней степени тяжести), рекомендуется устранение митральной регургитации с помощью клапан сохраняющих операций (пластика митрального клапана в условиях искусственного кровообращения), а при невозможности их выполнения показано протезирование митрального клапана в условиях искусственного кровообращения (протез митрального клапана механический двустворчатый***) [51, 55 - 57, 91, 93, 131].
(УУР C, УДД 4)
- У пациентов с диагностированным аномальным отхождением ЛКА от ЛС при наличии аневризмы ЛЖ рекомендуется выполнение одного из видов вентрикулопластики (реконструкция левого желудочка сердца) при хирургической коррекции аномалии КА с целью нормализации внутрисердечной гемодинамики и улучшения прогноза отдаленной выживаемости [16, 51, 56 - 57, 92, 93].
(УУР C, УДД 5)
Комментарии: Показаниями к выполнению одного из видов вентрикулопластики (реконструкции левого желудочка сердца) при коррекции синдрома Бланд-Уайт-Гарланда следует считать: 1) наличие аневризмы левого желудочка по данным эхокардиографии; 2) резкую дилатацию полости левого желудочка с наличием зон асинергии по данным ретроградной катетеризации левых отделов сердца; 3) признаки аневризмы с площадью рубцовых изменений более 20% по данным позитронно-эмиссионной томографии миокарда. Спектр хирургических вмешательства устранения аневризмы ЛЖ включает в себя следующие методики: 1) аневризмораффия; 2) пластика аневризмы ЛЖ по Жатене; 3) пластика аневризмы ЛЖ по Дору.
- У пациентов с диагностированным аномальным отхождением ЛКА от ЛС в ряде клинических ситуаций рекомендуется использование трансмиокардиальной лазерной реваскуляризации с целью отдаленного улучшения кровоснабжения миокарда [51, 56, 57].
(УУР C, УДД 4)
Комментарии: Применение метода трансмиокардиальной лазерной реваскуляризации у больных с синдромом Бланд-Уайт-Гарланда в качестве альтернативы коронарному шунтированию в условиях искусственного кровообращения может быть оправдано у пациентов, находящихся в критическом состоянии по основному пороку и имеющих неблагоприятную анатомию венечной системы с отсутствием или слабым развитием межкоронарных анастомозов и большой площадью рубцового поражения левого желудочка.
- У пациентов с диагностированным аномальным отхождением ЛКА от ЛС в ряде клинических ситуаций рекомендуется выполнение трансплантации сердца как безальтернативного варианта коррекции порока с целью спасения жизни пациента [51, 56, 57].
(УУР C, УДД 5)
Комментарии: У пациентов с массивным инфарктом миокарда либо аневризмой ЛЖ, особенно в тех случаях, когда предполагаемая реваскуляризация миокарда не приведет к полной ликвидации патоморфологических изменений в сердце, то есть при документально подтвержденном отсутствии жизнеспособного миокарда (по данным ПЭТ и ОФЭКТ), показана трансплантация сердца. К сожалению, данная рекомендация трудно применима в отношении больных детей раннего возраста в нашей стране, ввиду отсутствия законодательной базы по трансплантологии у детей в России, а донором может быть лишь взрослый пациент. В редких ситуациях возможно выполнение пересадки ребенку от взрослого донора (зависит от росто-весовых показателей донора).
- У ряда пациентов с диагностированным аномальным отхождением ЛКА от ЛС при хирургической коррекции коронарной аномалии рекомендуется использование введение стволовых клеток [51, 56, 57, 92].
(УУР C, УДД 4)
Комментарии: Применение методики имплантации стволовых клеток (фетальных кардиомиобластов, ангиогенного фактора CD133+) при синдроме Бланд-Уайт-Гарланда в коронарное русло и интрамиокардиально может быть использовано, как во время основной коррекции порока, так и в отдаленные сроки после операции в случаях сохраняющейся сниженной контрактильной способности левого желудочка.
- Пациентам с диагностированными КСФ больших размеров рекомендуется устранение КСФ, вне зависимости от симптоматики, с использованием открытой хирургической или же эндоваскулярной методик после анализа их анатомии и возможности окклюзии [5 - 11, 13, 15, 44, 49, 50].
(УУР C, УДД 5)
Комментарии: Успешный результат хирургического закрытия фистулы во многом предопределен дооперационным определением ее точной локализации и возможности адекватной хирургической экспозиции. При недооценке анатомических особенностей фистулы и ее затрудненной экспозиции, особенно дистального сегмента, возможна недостаточно адекватная коррекция с дальнейшей реканализацией фистулы.
- Рекомендуется устранение КСФ пациентам с диагностированными КСФ большого, среднего и малого размера в сочетании с симптомами ишемии миокарда, жизнеугрожающими нарушениями ритма, необъяснимой дисфункцией желудочка, гипертензией в полости левого предсердия или же сопутствующей кардиальной патологией [5 - 11, 13, 15, 44, 49, 50].
(УУР C, УДД 5)
- Не рекомендуется устранение КСФ у пациентов с асимптомной КСФ небольшого диаметра [50].
(УУР C, УДД 4)
3.3 Эндоваскулярные вмешательства
- Рекомендуется пациентам с диагностированными КСФ выполнение эндоваскулярных вмешательств только в специализированных кардиохирургических центрах, обладающих опытом подобных вмешательств с целью устранения выявленной фистулы [132 - 134].
(УУР C, УДД 4)
Комментарии: Многочисленные публикации свидетельствуют об успешном частичном или полном закрытии КСФ эндоваскулярным методом с помощью спиралей для эмболизации сосудов*** или окклюдера кардиологического***. Основными показаниями для эмболизации КСФ являются: 1) диаметр фистулы более 3 мм, 2) проксимальное расположение свищевого хода, 3) единичная КСФ, 4) прямой фистулярный ход, 5) отсутствие сопутствующей внутрисердечной патологии [132 - 134].
3.4 Иное лечение
Нет
4. Медицинская реабилитация и санаторно-курортное лечение, медицинские показания и противопоказания к применению методов медицинской реабилитации, в том числе основанных на использовании природных лечебных факторов
- Рекомендуется в течение 6 месяцев после выполнения хирургической коррекции аномалий КА в условиях искусственного кровообращения пациенту с осложненным течением послеоперационного периода (НК, инфекционные осложнения, повторные хирургические вмешательства в течение одной госпитализации) пройти реабилитацию в условиях специализированного лечебного учреждения кардиологического профиля [93 - 95, 115, 135].
(УУР C, УДД 5)
Комментарии: После коррекции аномалий КА могут встречаться следующие состояния:
- формирование стеноза устья и ствола реимплантированной ЛКА после прямой имплантации ЛКА в Ао при коррекции СБУГ;
- прогрессирование ишемии миокарда, сопровождающееся снижением контрактильной функции;
- формирование надклапанного стеноза ЛА после операции прямой реимплантации ЛКА в Ао;
- развитие дисфункции шунтов (окклюзии, стенозы) при шунтировании аномально отходящей ЛКА при коррекции СБУГ;
- реканализация внутрилегочного тоннеля с формированием коронарно-легочных фистул при операциях гемодинамической коррекции типа Hamilton и Takeuchi;
- стеноз внутрилегочного тоннеля при операциях гемодинамической коррекции типа Hamilton и Takeuchi;
- прогрессирование регургитации на МК;
- развитие протез-зависимых осложнений при имплантации протеза в митральную позицию (протез митрального клапана механический двустворчатый***) при коррекции СБУГ (эндокардит, тромбоз, системные эмболии, парапротезная регургитация или окклюзия, связанная с развитием паннуса);
- развитие нарушений ритма сердца, в ряде случаев приводящее к внезапной сердечной смерти на фоне острой коронарной недостаточности;
- реканализация КСФ
- Рекомендуется ограничить физическую нагрузку в течение трех месяцев с момента выписки из стационара после выполнения хирургической коррекции аномалий КА с целью избегания нарушения регенерации грудины и деформации грудной клетки [93, 94].
(УУР C, УДД 5)
- В течение 6 месяцев после выполнения хирургической коррекции аномалий КА пациенту с осложненным течением послеоперационного периода (резидуальная легочная гипертензия, СН, инфекционные осложнения, повторные хирургические вмешательства в течение одной госпитализации) рекомендуется пройти реабилитацию в условиях специализированного санаторно-курортного учреждения кардиологического профиля [115 - 116].
(УУР C, УДД 5)
5. Профилактика и диспансерное наблюдение, медицинские показания и противопоказания к применению методов профилактики
- Рекомендуется диспансерный прием (осмотр, консультация) врача - детского кардиолога всем оперированным или неоперированным пациентам с диагностированными аномалиями КА с целью своевременного выявления и купирования возникших до или послеоперационных осложнений [5, 8, 10, 22, 35, 36, 44, 47, 51, 55 - 57, 93].
(УУР C, УДД 5)
- Пациентам, перенесшим операцию хирургической коррекции аномалий КА, рекомендуется диспансерный прием (осмотр, консультация) врача - детского кардиолога с выполнением ЭКГ и Эхо-КГ 1 раз в 7 дней в течение 1 месяца после выписки из кардиохирургического стационара. В дальнейшем при стабильном клиническом состоянии пациента, диспансерный прием (осмотр, консультация) врача - детского кардиолога с выполнением ЭКГ и Эхо-КГ должен проводиться 1 раз в 3 месяца на протяжении года, далее частота определяется индивидуально [33, 35, 51, 56, 57].
(УУР C, УДД 5)
Комментарии: Проведение диспансерного приема (осмотр, консультация) врача - детского кардиолога с выполнением ЭКГ и Эхо-КГ с подобной кратностью позволяет своевременно обнаружить прогрессирование ишемии миокарда, а также возможных осложнений корригированных аномалий КА.
- Рекомендуется пациентам с небольшими асимптомными КСФ 1 раз в год проходить диспансерный прием (осмотр, консультация) врача - детского кардиолога с выполнением ЭКГ и Эхо-КГ-исследования [50, 93].
(УУР C, УДД 5)
Комментарии: целью проведения подобных осмотров является исключение появления ишемической симптоматики, нарушений ритма, дилатации камер сердца, что может повлиять на дальнейшую тактику ведения пациента.
- Пациентам с аномалиями КА после хирургического лечения рекомендуется обследование в стационаре не реже 1 раза в год после хирургического лечения порока с целью своевременного выявления и устранения возможных возникших послеоперационных осложнений [93].
(УУР C, УДД 5)
- Рекомендуется в отдаленные сроки наблюдения всем оперированным пациентам с аномалиями КА выполнение МРТ сердца по показаниям при появлении повторных жалоб или ухудшении состояния и невозможности определения причины другими инструментальными методами [33, 35, 51, 56, 57].
(УУР C, УДД 5)
Комментарии: Выполнение данного исследования у пациентов, перенесших хирургическую коррекцию аномалии КА, необходимо для выявления дисфункции ЛЖ, оценки его объемных характеристик и сократительной способности, обнаружения возможной коронарной ишемии, очагов фиброза и рубцовых изменений.
6. Организация оказания медицинской помощи
Показания для плановой госпитализации в медицинскую организацию:
1. наличие симптомов сердечной недостаточности;
2. плановое оперативное лечение коронарной аномалии;
3. исследование отдаленных результатов ранее выполненного хирургического лечения;
Показания для экстренной госпитализации:
1. ухудшение функционального статуса пациента в связи с прогрессированием симптомов недостаточности кровообращения, нарушениями ритма сердца;
2. развитие острой коронарной недостаточности;
3. развитие дисфункции ЛЖ;
4. инфекционный эндокардит;
Показания к выписке пациента из медицинской организации:
1. наличие документально подтвержденного кровотока по реимплантированной ЛКА при коррекции СБУГ;
2. отсутствие гемодинамически значимой реканализации КСФ;
3. отсутствие/компенсация симптомов недостаточности кровообращения;
4. отсутствие признаков коронарной ишемии;
5. отсутствие гемодинамически значимых нарушений ритма сердца.
7. Дополнительная информация (в том числе факторы, влияющие на исход заболевания или состояния)
Контингент пациентов, подлежащий алгоритму обследования для выявления коронарной аномалии:
а) новорожденные с необъяснимой кардиомегалией, сочетающейся в анамнезе с приступами "стенокардии кормления";
б) дети первых лет жизни с признаками необъяснимой, документально подтвержденной дисфункции ЛЖ сердца (ЭКГ-признаки ишемии миокарда и гипертрофии ЛЖ, увеличение его линейных и объемных характеристик со снижением контрактильной способности по данным ЭхоКГ) и/или с впервые диагностированной выраженной регургитацией на МК;
в) подростки с впервые выявленными стенокардитическими болями, нарушениями ритма сердца и/или с наличием впервые выявленной выраженной недостаточности МК.
Среди первичных анатомических факторов, определяющих выживаемость больных с аномальным отхождением ЛКА от ЛС после операции, первостепенное значение имеют: степень развития межкоронарных анастомозов, тип доминантности кровоснабжения сердца, гипоплазия правого желудочка сердца. Все прочие анатомические факторы, такие как повреждение миокарда, дилатация ЛЖ (иногда с формированием огромной аневризмы), митральная недостаточность, являются вторичными [8, 27, 60].
Операционная летальность при операции перевязки или ушивания устья аномально отходящей ЛКА из просвета ЛА колеблется от 20 до 50% [44, 114], а в отдаленные сроки после операции может достигать 33% [84, 114, 115]. В середине 80-х гг. летальность после операций перевязки или ушивания устья аномально отходящей ЛКА составляла в ближайшем и отдаленном послеоперационном периодах 40,0% и 111% соответственно [116]. Достаточно высокие цифры послеоперационной летальности объясняются тем, что подобные вмешательства не приводят к нормализации объема ЛЖ и восстановлению его сократительной способности, что, в свою очередь, ведет к возникновению критической сердечной недостаточности и, соответственно, к ухудшению отдаленных результатов [36, 84, 114, 117, 118]. В то же время, эти хирургические вмешательства технически легко выполнимы и могут служить первым этапом коррекции порока, направленным на предотвращение необратимой дисфункции миокарда, сосочковых мышц и клапанного аппарата сердца [119].
При анализе результатов шунтирующих операций в ранние сроки после операции у больных с функционирующими анастомозами результаты, как правило, хорошие [44, 59]. Однако, венозные шунты, в силу своих морфологических особенностей со временем стенозируются или окклюзируются. Таким образом, основными причинами неудовлетворенности врачей-хирургов результатами операции при применении данных методик являются осложнения, связанные со стенозированием, окклюзией или тромбозом "вставочных" шунтов, особенно у маленьких детей.
Прямая имплантация ЛКА в аорту (A16.12.004 наложение анастомоза на коронарные сосуды) является наиболее часто используемой операцией в практике кардиохирургических клиник. Летальность при этой операции колеблется от 0 до 16%.
Отдаленные результаты операции прямой имплантации ЛКА в аорту (A16.12.004 наложение анастомоза на коронарные сосуды) являются обнадеживающими, особенно, если вмешательство выполнено в раннем детском возрасте. В отдаленные сроки после вмешательства большая часть пациентов (порядка 85 - 90%) является асимптоматичной; при проведении функциональных проб отмечается восстановление функции ЛЖ в виде сокращения его линейных размеров и объемных характеристик, а также улучшения его насосной функции. Митральная недостаточность, как правило, регрессирует.
В отношении операций гемодинамической коррекции ряд авторов предпочитают использование операции Takeuchi у новорожденных и детей, другие же считают подобное вмешательство методом выбора у взрослых пациентов. Летальность при выполнении операции колеблется от 0 до 23%, что сопоставимо с результатами прямого перемещения аномально отходящей ЛКА.
Неудовлетворенность результатами данного вмешательства связана с достаточно высоким процентом послеоперационных осложнений, таких как надклапанный стеноз ЛА различной степени выраженности, большая вероятность возникновения коронарно-легочных фистул при формировании внутрилегочного тоннеля, а также развитие недостаточности аортального клапана. Как свидетельствуют данные литературных источников, у 30% этих больных возникает необходимость в реоперации в условиях искусственного кровообращения либо выполнении эндоваскулярных процедур.
В настоящее время значительное улучшение результатов при хирургической коррекции СБУГ связано с развитием и широким внедрением в клиническую практику систем вспомогательного кровообращения в послеоперационном периоде в качестве "моста" к восстановлению сократительной функции ЛЖ. Именно аномальное отхождение ЛКА от ЛА является классическим примером посткардиотомной дисфункции ЛЖ, где механическая поддержка особенно эффективна. Наиболее часто используемыми системами механической поддержки сердца являются внутриаортальная баллонная контрпульсация (ВАБКП), левожелудочковый обход (ЛЖО), экстракорпоральная мембранная оксигенация (ЭКМО).
В отношении пациентов с устраненными КСФ - при успешном хирургическом лечении имеется хороший прогноз. Долгосрочный прогноз определяется вероятностью развития послеоперационной реканализации и/или появления новой фистулы, включая ранее не диагностированную.
После открытых хирургических вмешательств летальность в группе пациентов до 20 лет достигает 1%, а в группе пациентов старше 20 лет - 7%. Из возможных осложнений в отдаленные сроки после операции отмечены ишемия и инфаркт миокарда (3 - 7% случаев), реканализация фистулы (до 4% случаев). Полная окклюзия КСФ на операционном столе спиралями для эмболизации сосудов*** достигается в 79% случаев, в отдаленном периоде - в 96% случаев. Среди зафиксированных осложнений при выполнении эндоваскулярного вмешательства можно отметить миграцию спирали в ЛА, миграцию баллона, развитие инфаркта миокарда (с возможным летальным исходом).
Критерии оценки качества медицинской помощи
N п/п
Критерии качества
Оценка выполнения
1
Выполнен сбор анамнеза и жалоб у всех пациентов (родителей пациентов) с подозрением на аномалии КА
Да/Нет
2
Выполнена пальпация и перкуссия при патологии сердца и перикарда
Да/Нет
3
Выполнена аускультация при патологии сердца и перикарда
Да/Нет
4
Выполнена регистрация электрокардиограммы
Да/Нет
5
Выполнена прицельная рентгенография органов грудной клетки
Да/Нет
6
Выполнена эхокардиография
Да/Нет
7
Выполнена ретроградная катетеризация левых отделов сердца с коронарографией и панаортографией
Да/Нет
8
Выполнена сцинтиграфия миокарда
Да/Нет
9
Выполнена ПЭТ совмещенная с компьютерной томографией миокарда с контрастированием (с флудезоксиглюкозой [18F])
Да/Нет
10
Выполнено проведение спиральной компьютерной томографии сердца с ЭКГ-синхронизацией (КТ-коронарография)
Да/Нет
11
Выполнена магнитно-резонансная томография сердца и магистральных сосудов
Да/Нет
12
Выполнено хирургическое лечение по устранению аномалии КА при наличии показаний (чрезкожное вмешательство или операция на открытом сердце)
Да/Нет
13
Выполнена регистрация электрокардиограммы перед выпиской из стационара
Да/Нет
14
Выполнена эхокардиография перед выпиской из стационара
Да/Нет
Список литературы
1. Андреева Н.С., Реброва О.Ю., Зорин Н.А., др. Системы оценки достоверности научных доказательств и убедительности рекомендаций: сравнительная характеристика и перспективы унификации. Медицинские технологии. Оценка и выбор 2012; 4: 10 - 24.
2. Багманова, З.А. Аномалии коронарных артерий/Багманова З.А.//Кардиология - 2010, N 8. - С. 48 - 55.
3. Бокерия, Л.А. Хирургическая анатомия венечных артерий/Л.А. Бокерия, И.И. Беришвили//М: Издательство НЦССХ им. А.Н. Бакулева РАМН. - 2003. - С. 229 - 230.
4. Абдуллаев, Ф.З. Характерные особенности патологической анатомии и поражения миокарда при аномальном отхождении левой коронарной артерии от легочного ствола (клинико-анатомические сопоставления)/Ф.З. Абдуллаев, М.Ж. Наседкина, А.А. Можина и др.//Архив патологии. - 1988. - N 6. - С. 35 - 41.
5. И.Ю. Барышникова, Д.О. Беришвили, В.Н. Макаренко, И.Е. Нефедова Крупные коронаросердечные фистулы у грудных детей/Детские болезни сердца и сосудов. - 2014. N 4. - С. 42 - 46.
6. Fischer G., Apostolopoulou S.C., Rammos S., Kiaffas M., Kramer H.H. Transcatheter closure of coronary arterial fistulas using the new Amplatzer(R) Vascular Plug. Cardiol. Young. 2007; 20: 1 - 5.
7. Kassaian S.E., Alidoosti M., Sadeghian H., Dehkordi M.R. Transcatheter closure of a coronary fistula with an Amplatzer(R) Vascular Plug. Tex. Heart Inst. J. 2008; 35 (1): 58 - 61.
8. Л.А. Бокерия, О.Л. Бокерия, М.Б. Биниашвили и соавт. Опыт лечения врожденных коронарно-сердечных фистул в сочетании с нарушениями ритма сердца./Анналы аритмологии. - 2013. - Т. 10, N 1. - С. 52 - 60.
9. Л.А. Бокерия, Б.Г. Алекян, В.П. Подзолков и соавт. Применение окклюдеров Amplatzer для закрытия больших коронарно-сердечных фистул./Грудная и сердечно-сосудистая хирургия - 2014. - N 1. - С. 40 - 48.
10. Бокерия Л.А., Шаталов К.В., Арнаутова И.В. и соавт. Успешная коррекция коронарно-сердечной фистулы в выводном отделе правого желудочка у ребенка с единственной коронарной артерией./Детские болезни сердца и сосудов. - N 4. - 2005. - С. 73 - 77.
11. Chirantan V. Mangukia. Coronary artery fistula. Ann. Thorac.Surg. 2012; 93: 2084 - 92.
12. Bauer H.H., Allmendinger P.D., Flaherty J., Owlia D et al. Congenital coronary arteriovenous fistula: spontaneous rupture and cardiac tamponade. Ann. Thorac. Surg. 1996; 62: 1521 - 3.
13. Liang C.D., Ko S.F., Lin Y.J., Fang C.Y. Transcatheter closure of a left circumflex coronary artery fistula in two children using the Amplatzer vascular plug. Pediatr. Cardiol. 2009; 30 (8): 1172 - 5.
14. Qureshi Sh.A. Coronary arterial fistulas. Orphanet J. Rare Dis. 2006; 1: 51.
15. Balanescu S. et al. Coronary artery fistulas: clinical consequences and methods of closure. A literature review. Ital. Heart J. 2001; 2: 669 - 76.
16. Бураковский, В.И. Руководство по сердечно-сосудистой хирургии/В.И. Бураковский, Л.А. Бокерия//М. 1996. - С. 340 - 341.
17. Dodge-Khatami, A. Anomalous origin of the left coronary artery from the pulmonary artery: collective review of surgical therapy (Review)/A. Dodge-Khatami, C. Mavroudis, C.L. Backer//Ann. Thorac. Surg. - 2002. - Vol. 74. - P. 946 - 955.
18. Kaushal, S.K. Anomalous origin the left anterior descending coronary artery from the pulmonary artery/S.K. Kaushal, S. Radhakrisnan, K.S. Dagar et al.//J. Thorac. Cardiovasc. Surg. - 1998. - Vol. 116. - P. 1078 - 1080.
19. Keith, J.D. The anomalous origin of the left coronary artery from the pulmonary artery/J.D. Keith//Br. Heart J. - 1959. - Vol. 21. - P. 149 - 61.
20. Kirklin, J.W. Congenital anomalies of the coronary arteries/J.W. Kirklin, B.G. Barrat-Boyes//In: Cardiac surgery. New York: John Wiley. - 1986. - P. 945 - 69.
21. Kreutzer, C. Emergency ligation of anomalous left coronary artery arising from the pulmonary artery/C. Kreutzer, A.J. Schlichter, M.I. Roman, G.O. Kreutzer//Ann. Thorac Surg. - 2000. - Vol. 69. - P. 1591 - 1592.
22. Lange, R. Long-term results of repair of anomalous origin of the left coronary artery from the pulmonary artery/R. Lange, M. Vogt, J. ![]() et al.//Ann. Thorac. Surg. - 2007. - Vol. 83. - P. 1463 - 1471.
et al.//Ann. Thorac. Surg. - 2007. - Vol. 83. - P. 1463 - 1471.
23. Murala, J.S.K. Anomalous origin of the left coronary artery from pulmonary artery in adults/J.S.K. Murala, M.N. Sankar, R. Agarwal et al.//Asian Cardiovasc. Thorac. Ann. - 2006. - Vol. 14. - P. 38 - 42.
24. Korach, A. Anomalous left main coronary artery from the main pulmonary artery in an elderly patient: Case report/A. Korach, P. Menon, M. Dhadly et al//Ann. Thorac. Surg. - 2006. - Vol. 82. - P. 2285 - 2287.
25. Moodie, D.S. Thallium 201 imaging in young adult with anomalous left coronary artery arising from the pulmonary artery/D.S. Moodie, S.A. Coor, C.C. Gill, C.A. Napoli//J. Nurt. Med. - 1980. - Vol. 21. - P. 1076 - 1082.
26. Ogden, J.A. Patterns of distribution of single coronary artery/J.A. Ogden, A.V. Goodyer//Jale J. Biol. Med. - 1970. - Vol. 43. - P. 11.
27. Петросян, Ю.С. Аномальное отхождение левой коронарной артерии от легочной артерии (клиника и диагностика)/Ю.С. Петросян, И.И. Беришвили//Тер. архив. - 1979. - N 10. - С. 17 - 24.
28. Angelini P. Coronary artery anomalies: an entity in search of an identity. Circulation 2007; 115: 1296 - 1305.
29. Angelini, P. Normal and anomalous coronary arteries in humans./Angelini P., Villason S., Chan A.V., Diez J.G.//In Angelini P. ed. Coronary artery anomalies: a comprehensive approach. Philadelphia: Lippincott Williams & Wilkins 1999; 27 - 150.
30. Wesselhoeft, H. Anomalous origin of the left coronary artery from the pulmonary trunk. Its clinical spectrum, pathology and pathophysiology, based on review of 140 cases with seven further cases/H. Wesselhoeft, J.S. Fawcett, A.L. Johnson//Circulation. - 1968. - Vol. 38. - P. 403.
31. Alexi-Meskishvili, V. Anomalous origin of the left coronary artery from the pulmonary artery. Early results with direct aortic reimplantation/V. Alexi-Meskishvili, R. Hetzer, Y. Weng et al.//J. Thorac. Cardiovasc. Surg. - 1994. - Vol. 108. - N 2. - P. 354 - 362.
32. Alexi-Meskishvili, V. Repair of anomalous origin of the left coronary artery from the pulmonary artery in infants and children/V. Alexi-Meskishvili, B.A. Nasseri, S. Nordmeyer, B. Schmitt, Yu-Guo Weng, W. Beottcher, M. Heubler, F. Berger, R. Hetzer//J. Thorac. Cardiovasc. Surg. - 2011. - Vol. 142. - P. 868 - 874.
33. Белозеров, Ю.М. Детская кардиология//М.: МЕДпресс-информ. - 2004. - С. 324.
34. Frapier, Jean-Marc. Malignant ventricular arrhythmias revealing anomalous origin of the left coronary artery from the pulmonary artery in two adults/Jean-Marc Frapier, F. Leclercg et al.//European J. of Cardio-thoracic Surg. - 1999. - Vol. 15. - P. 539 - 541.
35. Шарыкин, А.С. Врожденные пороки сердца. Руководство для педиатров, кардиологов, неонатологов/А.С. Шарыкин//М: Изд-во "Теремок". - 2005. - С. 289 - 299.
36. Moodie, D.S. Anomalous origin of the left coronary artery from the pulmonary artery (Bland-White-Garland syndrome) in adult patients: long-term follow up after surgery/D.S. Moodie, D. Fyfe, C.C. Gill et al.//Am. Heart J. 1983. - Vol. 106. - P. 381 - 388.
37. Бокерия, Л.А. Аномальное отхождение левой коронарной артерии от правой легочной артерии/Л.А. Бокерия, И.И. Беришвили, М.Н. Вахромеева и др.//Грудная и сердечно-сосудистая хирургия. - 1997. - N 4. - С. 65.
38. Fierence, C. A 72 year old woman with ALCAPA/C.A. Fierence, W. Budts, B. Denef, F.A. Van de Werf//Heart. - 2000. - Vol. 83. - P. 22.
39. Kawara, T. Anomalous origin of the left coronary artery arising from the pulmonary artery: successful direct reimplantation in a 50-year-old man/T. Kawara, E. Tayama, N. Hayashida et al.//Ann. Thorac. Cardiovasc. Surg. - 2003. - Vol. 9, N 3 - P. 197 - 201.
40. Kobayashi, J. Maze procedure and anomalous coronary artery repair/J. Kobayashi, Y. Kosakai, Y. Kawashima//Ann. Thorac. Surg. - 1996. - Vol. 61. - P. 1008 - 1011.
41. Pedra C.A.C., Pihkala J., Nykanen D.G., Benson L.N. Antegrade transcatheter closure of coronary artery fistulae using vascular occlusion devices. Heart. 2000; 83: 94 - 6.
42. Haberman J.H., Howard M.L., Johnson E.S. Rupture of the coronary sinus with haemopericardium. Circulation. 1963; 28: 1143 - 4.
43. Tokala A.B., Cowling M., Gunning M.G. Percutaneous closure of a coronary to pulmonary artery fistula. Heart. 2006; 92: 1888.
44. Valente A.M., Lock J.E., Gauvreau K. Predictors of long-term adverse outcomes in patient with congenital coronary artery fistulae. Circulation: cardiovascular interventions. 2010. Doi: 10.1161/CIRCINTERVENTIONS.109.883884.
45. Agustsson, M.H. Anomalous origin of the left coronary artery from the pulmonary artery diagnosis and treatment of infantile and adult types/M.H. Agustsson, B.M. Gasul, H. Fell, et al.//JAMA 1962. - Vol. 180. P. 15 - 21.
46. Edwards, J.I. The direction of blood flow in coronary arteries arising from the pulmonary trunk/J.I. Edwards//Circulation. - 1964. - Vol. 29. - P. 163 - 166.
47.
48. Neufeld H.N., Schneeweiss A./Coronary artery disease in infant and children.//Lea Febinger, Philadelphia, 1983.
49. Y. Xiao, M.D., S. T. Gowda Transcatheter Closure of Coronary Artery Fistulae: Considerations and Approaches Based on Fistula Origin Journal of Interventional Cardiology Vol. 28, No. 4, 2015;
50. S. T. Gowda, MD, T. J. Forbes Remodeling and Thrombosis Following Closure of Coronary Artery Fistula With Review of Management: Large Distal Coronary Artery Fistula - To Close or Not to Close? Catheterization and Cardiovascular Interventions 82: 132 - 142 (2013).
51. Бокерия, Л.А. Аномальное отхождение левой коронарной артерии от легочной артерии (синдром Бланда-Уайта-Гарланда)/Л.А. Бокерия, К.В. Шаталов, И.В. Арнаутова//М.: НЦССХ им. А.Н. Бакулева, РАМН. - 2010.
52. Arciniegas, E. Management of anomalous left coronary artery from the pulmonary artery/E. Arciniegas, Z.Q. Farooki, M. Hakimi, E.W. Green//Circulation 1980. - Vol. 62 (2 Pt 2). - P. 180 - 189.
53. Berdjis, F. Anomalous left coronary artery from the pulmonary artery: significance of intercoronary collaterals//F. Berdjis, M. Takahashi, W.J. Wells, Q.R. Stiles, G.G. Lindesmith//J. Thorac. Cardiovasc. Surg. - 1994. - Vol. 108. - P. 17 - 20.
54. Bland, E.F. Congenital anomalies of the coronary arteries: Report of an unusual case associated with cardiac hypertrophy/E.F. Bland, P.D. White, J. Garland//Amer. Heart J. - 1933. - Vol. 8. - P. 787 - 801.
55. Махалин, М.В. Хирургическое лечение дисфункции митрального клапана при синдроме Бланда-Уайта-Гарланда в раннем детском возрасте: дис. ... канд. мед. наук/Махалин М.В.//М. - 2007.
56. Детская кардиохирургия: Руководство для врачей. Под ред. Л.А. Бокерия, К.В. Шаталова. М.: НЦССХ им. А.Н. Бакулева; 2016: с. 700 - 733.
57. Арнаутова, И.В. Эволюция подходов к хирургическому лечению аномального отхождения левой коронарной артерии от легочной артерии: дис. ... докт. мед. наук/Арнаутова И.В.//М. - 2013. 58
58. Baue, A.E. A later stage of anomalous coronary circulation with origin of the left coronary artery from the pulmonary artery/A.E. Baue, S. Baum, W.S. Blackmore, H.F. Zinsser//Circulation. - 1967. - Vol. 36. - P. 878 - 885.
59. Goor, D.A. Anomalous origin of the coronary arteries/D.A. Goor, C.W. Lillechei//Congenital Malformations of the Heart. - London. - 1975. - P. 363 - 371.
60. Рыбка М.М., Хинчагов Д.Я., Мумладзе К.В., Лобачева Г.В., Ведерникова Л.В. Под ред. Л.А. Бокерия. Протоколы анестезиологического обеспечения кардиохирургических операций, выполняемых у новорожденных и детей. Методические рекомендации. М.: НЦССХ им. А.Н. Бакулева РАМН; 2014.
61. Рыбка М.М., Хинчагов Д.Я. Под ред. Л.А. Бокерия. Протоколы анестезиологического обеспечения кардиохирургических операций, выполняемых при ишемической болезни сердца, патологии клапанного аппарата, нарушениях ритма, гипертрофической кардиомиопатии, аневризмах восходящего отдела аорты у пациентов различных возрастных групп. Методические рекомендации. М.: НЦССХ им. А.Н. Бакулева РАМН; 2015.
62. Бокерия, Л.А. Хирургическое лечение аномального отхождения левой коронарной артерии от легочной артерии в сочетании с имплантацией фетальных кардиомиобластов человека у ребенка 2 лет/Л.А. Бокерия, Г.Т. Сухих, К.В. Шаталов, А.И. Ким, И.В. Арнаутова и др.//Детские болезни сердца и сосудов. - 2004. - N 2. - С. 91 - 94.
63. Макаров, Л.М. - ЭКГ в педиатрии/Л.М. Макаров//"Медпрактика-М". - М. - 2006. - С. 259 - 264.
64. Johnrude, C.L. Differentiating anomalous left main coronary artery originating from the pulmonary artery in infants from myocarditis and dilated cardiomyopathy by electrocardiogram/C.L. Johnrude, J.S. Perry, F. Cecchin et al.//Am. J. Cardiol. - 1995. - Vol. 75. - P. 71 - 74.
65. Бокерия, Л.А. Эволюция подходов к хирургическому лечению синдрома Бланда - Уайта - Гарланда/Л.А. Бокерия, К.В. Шаталов, И.В. Арнаутова, А.И. Ким//Детские болезни сердца и сосудов. - 2004. - N 3. - С. 28 - 39.
66. Митина, И.Н. Эходопплерография в диагностике коронарных фистул./И.Н. Митина//Визуализация в клинике. - март 1993. - вып. 1. - N 2.
67. Fisher, E.A. Two dimensional echocardiographic visualization of the left coronary artery in anomalous origin of the left coronary artery//E.A. Fisher, B. Sepehri, B. Lendrum et al.//Circulation. - 1981. - Vol. 63(3). - P. 698 - 704.
68. Fun-Chung, Lin. Multiplane transesophageal echocardiography in the diagnosis of congenital artery fistula/Lin Fun-Chung, Chang Hern-Lia, Chern Ming-Shyan et al.//Am. Heart J. - 1995. - Vol. 130. - N 6. - P. 1236 - 1244.
69. Salasar, J. Non-invasive diagnosis of a right coronary artery - right ventricle fistula by cross-sectional and Doppler Echocardiography/J. Salasar, L. Placer, A. Artal//Rer. Esp. Cardiol. - 1991. - Vol. 44. - P. 341 - 343.
70. Sharon S. Karr, MD, Ira A. Parness, MD, Philip J. Spevak et al. - Diagnosis of anomalous left coronary artery by Doppler color flow mapping: distinction from other causes of dilated cardiomyopathy//Pediatric Cardiology. - 1992. - Vol. 19, N 6. - P. 1271 - 1275.
71. Зубкова, Г.А. Двухмерная и допплерэхокардиография в диагностике врожденных пороков сердца у новорожденных и детей первого года жизни/Г.А. Зубкова//Автореф. дисс. докт. мед. наук//М. - 1992.
72. Фейгенбаум, Х. Эхокардиография/Х. Фейгенбаум//Перевод с английского под редакцией Митькова В.В. - М.: Видар. - 1999. - С. 63 - 162, 290 - 292, 315.
73. Andrade, M.J. Anomalous origin of the left coronary artery from the pulmonary artery in adults: diagnosis with bidimensional, pulsed and color Doppler echocardiography/M.J. Andrade, M. Canada, R. Gouveia, J. Carmona et al.//Rev. Port. Cardiol. - 1992 May. - Vol. 11(5). - P. 465 - 470.
74. Jureidini, S.B. Reliability of echocardiography in the diagnosis of anomalous origin of the left coronary artery from the pulmonary trunk/S.B. Jureidini, S. Nouri, C.J. Crawford et al.//Am. Heart J. - 1991. - Vol. 122. - P. 61 - 68.
75. Maire, R. Initial detection in a teenager of anomalous left coronary artery by color Doppler echocardiography/R. Maire, A. Gallino, R. Jenni//Am. Heart J. - 1993, Jun. - Vol. 125 (6). - P. 1802 - 1805.
76. Suzuki, Y. Detection of anomalous origin of the left coronary artery from pulmonary artery by real-time Doppler color flow mapping in a 53-year-old asymptomatic female/Y. Suzuki, T. Murakami T, C. Kawai//Int. J. Cardiol. - 1992, Mar. - Vol. 34 (3). - P. 339 - 342.
77. Daniels, C. Anomalous origin of the left main coronary artery from the pulmonary trunk masquerading as peripartum cardiomyopathy/C. Daniels, J. Bacon, M.E. Fontana et al.//Am. J. Cardiol. - 1997, May 1. - Vol. 79(9). - P. 1307 - 1308.
78. Takeshita, S. Anomalous origin of the left coronary artery from the pulmonary artery: direct assessment of anomalous and collateral coronary flow by pulsed Doppler echocardiography/S. Takeshita, T. Yamaguchi, K. Kuwako, T.A. Isshiki//Cathet. Cardiovasc. Diagn. - 1992, Nov. - Vol. 27(3). - P. 220 - 222.
79. Алексеева, М.А. Возможности эхокардиографических методов исследования в диагностике аномалий коронарных артерий при врожденных пороках сердца: дисс. ... канд. мед. наук/М.А. Алексеева//М. - 2001.
80. Drinkovic, N. Echocardiographic diagnosis of anomalous origin of the left coronary artery from the pulmonary artery/N. Drinkovic, E. Margetic, A. Smalcelj, V. Brida//Eur. J. Echocardiogr. - 2008. - Vol. 9, N 2. - P. 309 - 310.
81. Асланиди, И.П. Особенности перфузии и метаболизма миокарда у пациентов с аномальным отхождением левой коронарной артерии от легочной артерии по данным перфузионной сцинтиграфии с 99mTc-технетрилом и позитронно-эмиссионной томографии с 18F-фтордезоксиглюкозой/И.П. Асланиди, И.В. Шурупова, Т.В. Рогова и др.//Бюллетень НЦССХ им. А.Н. Бакулева РАМН. - 2009. - N 6. - т. 10. - С. 39 - 48.
82. Бокерия, Л.А. Возможности сцинтиграфии миокарда с 201TL при аномальном отхождении коронарных артерий от легочной артерии/Л.А. Бокерия, И.П. Асланиди, М.Н. Вахромеева и др.//Грудная и сердечно-сосудистая хирургия. - 1999. - N 4. - С. 21 - 28.
83. Early S.A., Meany T.B., Fenlon H.M., Hurley J. Coronary artery fistula; coronary computed topography - the diagnostic modality of choice. J. Cardiothorac. Surg. 2008; 3: 41.
84. Schroeder S., Achenbach S., Bengel F., Burgstahler C., Cademartiri F., de Feyter P. et al. Cardiac Computed tomography: indications, applications, limitations and training requirements. Eur. Heart J. 2008, 29: 531 - 56.
85. Katsumata, T. Anomalous Left Coronary Artery From the Pulmonary Artery: A Simple Method for Aortic Implantation With Autogenous Arterial Tissue/T. Katsumata, S. Westaby//Ann. Thorac. Surg. - 1999. - Vol. 68. - P. 1090 - 1.
86. Shinkawa, T. Anomalous origin of the left coronary artery from the pulmonary artery. A case using the autologous pulmonary arterial wall graft/T. Shinkawa, M. Yamaguch, N. Yoshimura, S. Oka//Eur. J. Cardiothorac. Surg. - 2002. - Vol. 21. - P. 105 - 107.
87. Barth, M.J. Experience with an alternative technique for the management of anomalous left coronary artery from the pulmonary artery/M.J. Barth, B.S. Allen, M. Gulecyuz et al.//Ann. Thorac. Surg. - 2003. - Vol. 76. - P. 1429 - 1434.
88. Sese, A. New Technique in the Transfer of an Anomalously Originated Left Coronary Artery to the Aorta/A. Sese, Y. Imoto//Ann. Thorac. Surg. - 1992. - Vol. 53. - P. 527 - 529.
89. Wu, Q. An Alternative Procedure for Correction of Anomalous Origin of Left Coronary Artery From the Pulmonary Artery/Q. Wu, Z. Xu//Ann. Thorac. Surg. - 2007. - Vol. 84. - P. 2132 - 3.
90. El-Rassi, I. Transfer Technique of an Anomalous Coronary Artery From the Anterior Pulmonary Artery/I. El-Rassi, A. Soueide, O. Sweid, B. Chabb//Ann. Thorac. Surg. - 2012. - Vol. 93. - P. 1738 - 1740.
91. Caliani, J. A. Correction of anomalous origin of left coronary artery with mitral insufficiency and mechanical hemolisys/J.A. Caliani, A.A. Machado, J.A.T. Marinho, L.C.,  , O.N. Barbosa//Brazilian Journal of Cardiovascular Surgery. - 2004. - Vol. 19.N 4.
, O.N. Barbosa//Brazilian Journal of Cardiovascular Surgery. - 2004. - Vol. 19.N 4.
92. Бокерия, Л.А. Хирургическое лечение аномального отхождения левой коронарной артерии от легочной артерии в сочетании с имплантацией фетальных кардиомиобластов человека у ребенка 2 лет/Л.А. Бокерия, Г.Т. Сухих, К.В. Шаталов, А.И. Ким, И.В. Арнаутова и др.//Детские болезни сердца и сосудов. - 2004. - N 2. - С. 91 - 94.
93. Подзолков В.П., Кассирский Г.И. (ред.). Реабилитация больных после хирургического лечения врожденных пороков сердца. М.: НЦССХ им. А.Н. Бакулева; 2015.
94. Физическая и реабилитационная медицина. Национальное руководство. Краткое издание//Под ред. Г.Н. Пономаренко. М.: ГЭОТАР-Медиа, 2017. - 512 с./Глава 21. Хан М.А., Куянцева Л.В. Заболевания сердечно-сосудистой системы. - С. 447 - 452.
95. Bjarnason-Wehrens B. et al. Cardiac rehabilitation in congenital heart disease//Cardiovascular Prevention and Rehabilitation. - Springer, London, 2007. - С. 361 - 375.
96. Tikkanen A. U. etal. Paediatric cardiac rehabilitation in congenital heart disease: a systematic review//Cardiology in the young. - 2012. - Т. 22. - N. 3. - С. 241 - 250.
97. Приказ Минздрава РФ от 20 октября 2020 г. N 1134н "Об утверждении порядка медицинского обследования реципиента, проведения проб на индивидуальную совместимость, включая биологическую пробу, при трансфузии донорской крови и (или) ее компонентов".
98. Аксельрод Б.А., Балашова Е.Н., Баутин А.Е., Баховадинов Б.Б., Бирюкова Л.С., Буланов А.Ю., Быстрых О.А., Виноградова М.А., Галстян Г.М., Гапонова Т.В., Головкина Л.Л., Гороховский В.С., Еременко А.А. и др. Клиническое использование эритроцитсодержащих компонентов донорской крови. Гематология и трансфузиология. 2018; 63(4): 372 - 435.
99. Baumgartner H., De Backer J., Babu-Narayan S.V. et al. 2020 ESC Guidelines for the management of adult congenital heart disease. The Task Force for the management of adult congenital heart disease of the European Society of Cardiology (ESC)//Eur Heart J, Volume 42, Issue 6, 2021, Pages 563 - 645.
100. Dickstein K. et al. ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure 2008: the Task Force for the Diagnosis and Treatment of Acute and Chronic Heart Failure 2008 of the European Society of Cardiology. Developed in collaboration with the Heart Failure Association of the ESC (HFA) and endorsed by the European Society of Intensive Care Medicine (ESICM). EurHeart J 2008; 29: 2388 - 2442.
101. Постановление Главного государственного санитарного врача РФ от 28 января 2021 г. N 4 "Об утверждении санитарных правил и норм СанПиН 3.3686-21 "Санитарно-эпидемиологические требования по профилактике инфекционных болезней".
102. Национальные рекомендации по ведению детей с врожденными пороками сердца. Ред. Л.А. Бокерия. М., 2014.
103. Kirklin J.W., Barratt-Boyes B.G. Patent ductus arteriosus. In: Kirklin J.W., Barratt-Boyes B.G. (eds). Cardiac Surgery. Fourth edition, 2013
104. Writing Committee Members; Isselbacher E.M., Preventza O., Hamilton Black Iii J. et al. 2022 ACC/AHA Guideline for the Diagnosis and Management of Aortic Disease: A Report of the American Heart Association/American College of Cardiology Joint Committee on Clinical Practice Guidelines. J Am Coll Cardiol. 2022 Dec 13; 80(24): e223 - e393. doi: 10.1016/j.jacc.2022.08.004.
105. Warnes CA, Williams RG, Bashore TM, et al. ACC/AHA 2008 guidelines for the management of adults with congenital heart disease: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines (Writing Committee to Develop Guidelines on the Management of Adults With Congenital Heart Disease). Developed in collaboration with the American Society of Echocardiography, Heart Rhythm Society, International Society for Adult Congenital Heart Disease, Society for Cardiovascular Angiography and Interventions, and Society of Thoracic Surgeons. J Am Coll Cardiol 2008; 23: e143 - 263.
106. Park J.S. et al. Risk factors and effects of severe late-onset hyponatremia on long-term growth of prematurely born infants. Pediatr. Gastroenterol. Hepatol. Nutr. 2020. Vol. 23, N 5. P. 472 - 483.
107. Zhang X. Y. et al. The clinical outcomes of ventricular septal rupture secondary to acute myocardial infarction: a retrospective, observational trial//Journal of Interventional Cardiology. - 2021. - Т. 2021.
108. Anderson's Pediatric Cardiology, 4th Edition. Editor-in-Chiefs: Robert H. Anderson, Kumar Krishna, Andrew Redington, James S. Tweddell, Justin Tretter, Gil Wernovsky. Elsevier, 2019 - 1650 p.].
109. Mauritz G.J., Rizopoulos D., Groepenhoff H. et al. Usefulness of serial N-terminal pro-B-type natriuretic peptide measurements for determining prognosis in patients with pulmonary arterial hypertension. Am J Cardiol. 2011. 108(11): 1645 - 50.
110. Roberts E, Ludman AJ, Dworzynski K, Al-Mohammad A, Cowie MR, McMurray JJ, Mant J; NICE Guideline Development Group for Acute Heart Failure. The diagnostic accuracy of the natriuretic peptides in heart failure: systematic review and diagnostic meta-analysis in the acute care setting. BMJ. 2015 Mar 4; 350: h910.
111. Zaphiriou A, Robb S, Murray-Thomas T, Mendez G, Fox K, McDonagh T, Hardman SM, Dargie HJ, Cowie MR. The diagnostic accuracy of plasma BNP and NTproBNP in patients referred from primary care with suspected heart failure: results of the UK natriuretic peptide study. Eur J Heart Fail. 2005 Jun; 7(4): 537 - 41.
112. Fuat A, Murphy JJ, Hungin AP, Curry J, Mehrzad AA, Hetherington A, Johnston JI, Smellie WS, Duffy V, Cawley P. The diagnostic accuracy and utility of a B-type natriuretic peptide test in a community population of patients with suspected heart failure. Br J Gen Pract. 2006 May; 56(526): 327 - 33.
113. Yamamoto K, Burnett JC Jr, Bermudez EA, Jougasaki M, Bailey KR, Redfield MM. Clinical criteria and biochemical markers for the detection of systolic dysfunction. J Card Fail. 2000 Sep; 6(3): 194 - 200.
114. Svobodov A.A., Kupryashov A.A., Dobroserdova T.K., Levchenko E.G., Tumanyan M.R., Anderson A.G. A new approach to the interpretation of B-type natriuretic peptide concentration in children with congenital heart disease. Journal of Laboratory Medicine, 2023; 47(5): 225 - 232.
115. Физическая и реабилитационная медицина. Национальное руководство. Краткое издание//Под ред. Г.Н. Пономаренко. М.: ГЭОТАР-Медиа, 2017. - 512 с./Глава 21. Хан М.А., Куянцева Л.В. Заболевания сердечно-сосудистой системы. - С. 447 - 452.
116. Bjarnason-Wehrens B. et al. Cardiac rehabilitation in congenital heart disease//Cardiovascular Prevention and Rehabilitation. - Springer, London, 2007. - С. 361 - 375.
117. Tikkanen A.U. et al. Paediatric cardiac rehabilitation in congenital heart disease: a systematic review//Cardiology in the young. - 2012. - Т. 22. - N. 3. - С. 241 - 250.
118. McDonagh TA, Metra M, Adamo M, Gardner RS, Baumbach A, ![]() M, Burri H, Butler J,
M, Burri H, Butler J,  J, Chioncel O, Cleland JGF, Coats AJS, Crespo-Leiro MG, Farmakis D, Gilard M, Heymans S, Hoes AW, Jaarsma T, Jankowska EA, Lainscak M, Lam CSP, Lyon AR, McMurray JJV, Mebazaa A, Mindham R, Muneretto C, Francesco Piepoli M, Price S, Rosano GMC, Ruschitzka F, Kathrine Skibelund A; ESC Scientific Document Group. 2021 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure: Developed by the Task Force for the diagnosis and treatment of acute and chronic heart failure of the European Society of Cardiology (ESC). With the special contribution of the Heart Failure Association (HFA) of the ESC. Eur J Heart Fail. 2022; 24(1): 4 - 131.
J, Chioncel O, Cleland JGF, Coats AJS, Crespo-Leiro MG, Farmakis D, Gilard M, Heymans S, Hoes AW, Jaarsma T, Jankowska EA, Lainscak M, Lam CSP, Lyon AR, McMurray JJV, Mebazaa A, Mindham R, Muneretto C, Francesco Piepoli M, Price S, Rosano GMC, Ruschitzka F, Kathrine Skibelund A; ESC Scientific Document Group. 2021 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure: Developed by the Task Force for the diagnosis and treatment of acute and chronic heart failure of the European Society of Cardiology (ESC). With the special contribution of the Heart Failure Association (HFA) of the ESC. Eur J Heart Fail. 2022; 24(1): 4 - 131.
119. Купряшов А.А., Токмакова К.А. Нарушения системы свертывания крови в сердечно-сосудистой хирургии. В кн.: Система гемостаза. Теоретические основы и клиническая практика: Национальное руководство/О.А. Рукавицын, С.В. Игнатьев, А.Г. Румянцев [и др.]. Москва: Общество с ограниченной ответственностью Издательская группа "ГЭОТАР-Медиа", 2024. 944 с. ISBN 978-5-9704-8497-5.
120. Купряшов А.А. Бережное отношение к крови пациента. В кн.: Система гемостаза. Теоретические основы и клиническая практика: Национальное руководство/О.А. Рукавицын, С.В. Игнатьев, А.Г. Румянцев [и др.]. - Москва: Общество с ограниченной ответственностью Издательская группа "ГЭОТАР-Медиа", 2024. - 944 с. - ISBN 978-5-9704-8497-5.
121. Giglia T., Massicotte M., Tweddell J. et al. Prevention and Treatment of Thrombosis in Pediatric and Congenital Heart Disease: A Scientific Statement From the American Heart Association. Circulation. 2013; 128: 2622 - 2703.
122. Boucher AA, Heneghan JA, Jang S, Spillane KA, Abarbanell AM, Steiner ME, Meyer AD. A Narrative review of postoperative anticoagulation therapy for congenital cardiac disease. Front Surg. 2022 Jun 14; 9: 907782. doi: 10.3389/fsurg.2022.907782. PMID: 35774388; PMCID: PMC9237365.
123. Monagle P, Chan AKC, Goldenberg NA, Ichord RN, Journeycake JM,  U, Vesely SK. Antithrombotic therapy in neonates and children: Antithrombotic Therapy and Prevention of Thrombosis, 9th ed: American College of Chest Physicians Evidence-Based Clinical Practice Guidelines. Chest. 2012 Feb; 141(2 Suppl): e737S - e801S.
U, Vesely SK. Antithrombotic therapy in neonates and children: Antithrombotic Therapy and Prevention of Thrombosis, 9th ed: American College of Chest Physicians Evidence-Based Clinical Practice Guidelines. Chest. 2012 Feb; 141(2 Suppl): e737S - e801S.
124. ![]() E, Nguyen ET, Merchant N, Dennie C. ALCAPA syndrome: not just a pediatric disease. Radiographics. 2009 Mar-Apr; 29(2): 553 - 65.
E, Nguyen ET, Merchant N, Dennie C. ALCAPA syndrome: not just a pediatric disease. Radiographics. 2009 Mar-Apr; 29(2): 553 - 65.
125. Yunfei L, Qiang F, Yue W, Yongjun Q. N-terminal pro-brain natriuretic peptide levels in patients with anomalous left coronary artery from pulmonary artery. J Cardiothorac Surg. 2020 Jan 13; 15(1): 15.
126. Zhang H, Sun T, Liu G, Krittanawong C, El-Am EA, Karam RAA, Sun Y, Yang J, Li J, Zhang X, Xue L, Wang J, An Y, Ma G, Ma N. Impact of Reverse Left Ventricular Remodeling on Outcomes of Patients with Anomalous Left Coronary Artery from the Pulmonary Artery after Surgical Correction. Pediatr Cardiol. 2021 Feb; 42(2): 425 - 431.
127. Harrison DJ, Kane DA, Emani SM, Sanders SP, Miller TA, Marx GR. Anomalous Left Coronary Artery Arising from the Pulmonary Artery (ALCAPA): The Critically Important Role of Color Flow Doppler in Identifying a Rare Intramural Course. CASE (Phila). 2022 Mar 10; 6(3): 119 - 123.
128. Zou JN, Gao YH, Huang B, Luo JX, Jiang YL, Lu R, Tan HB, Li BX, Huang WC. The diagnostic value of dynamic volume computed tomography angiography in children with anomalous origin of the left coronary artery from the pulmonary artery. Am J Transl Res. 2021 Sep 15; 13(9): 10348 - 10355.
129. Heermann P, Heindel W,  C. Coronary Artery Anomalies: Diagnosis and Classification based on Cardiac CT and MRI (CMR) - from ALCAPA to Anomalies of Termination. Rofo. 2017 Jan; 189(1): 29 - 38. English.
C. Coronary Artery Anomalies: Diagnosis and Classification based on Cardiac CT and MRI (CMR) - from ALCAPA to Anomalies of Termination. Rofo. 2017 Jan; 189(1): 29 - 38. English.
130. Juan CC, Hwang B, Lee PC, Meng CC. Diagnostic application of multidetector-row computed tomographic coronary angiography to assess coronary abnormalities in pediatric patients: comparison with invasive coronary angiography. Pediatr Neonatol. 2011 Aug; 52(4): 208 - 13.
131. Brown JW, Ruzmetov M, Parent JJ, Rodefeld MD, Turrentine MW. Does the degree of preoperative mitral regurgitation predict survival or the need for mitral valve repair or replacement in patients with anomalous origin of the left coronary artery from the pulmonary artery? J Thorac Cardiovasc Surg. 2008 Sep; 136(3): 743 - 8.
132. Ilkay E, Celebi OO, Kacmaz F, Ozeke O. Percutaneous closure of coronary artery fistula: long-term follow-up results. Postepy Kardiol Interwencyjnej. 2015; 11(4): 318 - 22.
133. Abo-Salem E, Decanio R, Leesar M, Abruzzo T, Vu D, Alkhawam H, Ristagno R. Percutaneous closure of right coronary to superior vena cava fistula. Future Cardiol. 2019 May; 15(3): 161 - 167.
134. Bao Y, Xiong TY, Li X, Feng Y. Percutaneous closure of a fistula from the left circumflex coronary artery to the coronary sinus in an infant. J Int Med Res. 2021 Jun; 49(6): 3000605211021732.
135. Beyaz MO, Coban S, Ulukan MO, Dogan MS, Erol C, Saritas T, Erdem A, Akdeniz C, Ugurlucan M, Akcevin A, Turkoglu H. Current Strategies for the Management of Anomalous Origin of Coronary Arteries from the Pulmonary Artery. Heart Surg Forum. 2021 Jan 20; 24(1): E065 - E071.
Приложение А1
СОСТАВ
РАБОЧЕЙ ГРУППЫ ПО РАЗРАБОТКЕ И ПЕРЕСМОТРУ
КЛИНИЧЕСКИХ РЕКОМЕНДАЦИЙ
1. Авраменко А.А., (Самара)
2. Апханова Т.В., д.м.н. "Национальная ассоциация экспертов по санаторно-курортному лечению"
3. Арнаутова И.В., д.м.н., "Ассоциация сердечно-сосудистых хирургов России", (Москва),
4. Богданов В.Н., (Челябинск)
5. Бокерия Л.А., академик РАН, "Ассоциация сердечно-сосудистых хирургов России", (Москва)
6. Борисков М.В., д.м.н., (Краснодар)
7. Борисова Н.А., "Российское научное общество специалистов по рентгенэндоваскулярной диагностике и лечению", (Санкт-Петербург)
8. Горбатиков К.В., д.м.н., (Тюмень)
9. Горбатых Ю.Н., д.м.н., (Новосибирск)
10. Калашников С.В., к.м.н. (Москва)
11. Ким А.И., д.м.н., "Ассоциация сердечно-сосудистых хирургов России", (Москва)
12. Ковалев И.А., д.м.н., "Ассоциация детских кардиологов России", (Москва)
13. Кончугова Т.В., д.м.н., профессор, "Национальная ассоциация экспертов по санаторно-курортному лечению" Кривощеков Е.В., д.м.н., (Томск)
14. Купряшов А.А., д.м.н., (Москва)
15. Левченко Е.Г., д.м.н. (Москва)
16. Мовсесян Р.Р., д.м.н., "Ассоциация сердечно-сосудистых хирургов России", (Санкт-Петербург)
17. Плотников М.В., к.м.н., (Астрахань)
18. Пурсанов М.Г., д.м.н., (Москва)
19. Ручьева Н.А., к.м.н. (Москва) Общероссийская общественная организация содействия развитию лучевой диагностики и терапии "Российское общество рентгенологов и радиологов"
20. Синицын В.Е., д.м.н., профессор (Москва) Общероссийская общественная организация содействия развитию лучевой диагностики и терапии "Российское общество рентгенологов и радиологов" Синельников Ю.С., д.м.н., (Пермь)
21. Трунина И.И., д.м.н., "Ассоциация детских кардиологов России", (Москва)
22. Фесюн Анатолий Дмитриевич, д.м.н., доцент, президент Национальной Ассоциации экспертов по санаторно-курортному лечению
23. Шаталов К.В., д.м.н., "Ассоциация сердечно-сосудистых хирургов России", (Москва)
24. Яковлев Максим Юрьевич, д.м.н. "Национальная ассоциация экспертов по санаторно-курортному лечению"
Конфликт интересов отсутствует.
Все члены Рабочей группы подтвердили отсутствие финансовой поддержки/конфликта интересов, о которых необходимо сообщить.
Приложение А2
МЕТОДОЛОГИЯ РАЗРАБОТКИ КЛИНИЧЕСКИХ РЕКОМЕНДАЦИЙ
Целевая аудитория данных клинических рекомендаций:
1. Врач-детский кардиолог
2. Врач-кардиолог
3. Врач-сердечно-сосудистый хирург
4. Врач ультразвуковой диагностики
5. Врач-педиатр
6. Врач по рентгенэндоваскулярной диагностике и лечению
7. Врач-рентгенолог
8. Врач функциональной диагностики
9. Врач-неонатолог
В ходе разработки КР использованы новая система шкал УДД и УУР для лечебных, реабилитационных, профилактических вмешательств и диагностических вмешательств (Таблицы 1, 2 и 3), введенная в 2018 г. ФГБУ ЦЭККМП Минздрава РФ.
Таблица 1. Шкала оценки уровней достоверности доказательств (УДД) для методов диагностики (диагностических вмешательств).
УДД
Расшифровка
1
Систематические обзоры исследований с контролем референсным методом или систематический обзор рандомизированных клинических исследований с применением метаанализа
2
Отдельные исследования с контролем референсным методом или отдельные рандомизированные клинические исследования и систематические обзоры исследований любого дизайна, за исключением рандомизированных клинических исследований с применением метаанализа
3
Исследования без последовательного контроля референсным методом, или исследования с референсным методом, не являющимся независимым от исследуемого метода, или нерандомизированные сравнительные исследования, в том числе когортные исследования
4
Несравнительные исследования, описание клинического случая
5
Имеется лишь обоснование механизма действия или мнение экспертов
Таблица 2. Шкала оценки уровней достоверности доказательств (УДД) для методов профилактики, лечения, медицинской реабилитации, в том числе основанных на использовании природных лечебных факторов (профилактических, лечебных, реабилитационных вмешательств)
УДД
Расшифровка
1
Систематический обзор РКИ с применением метаанализа
2
Отдельные РКИ и систематические обзоры исследований любого дизайна, за исключением РКИ, с применением метаанализа
3
Нерандомизированные сравнительные исследования, в т.ч. когортные исследования
4
Несравнительные исследования, описание клинического случая или серии случаев, исследования "случай-контроль"
5
Имеется лишь обоснование механизма действия вмешательства (доклинические исследования) или мнение экспертов
Таблица 3. Шкала оценки уровней убедительности рекомендаций (УУР) для методов профилактики, диагностики, лечения, медицинской реабилитации, в том числе основанных на использовании природных лечебных факторов (профилактических, диагностических, лечебных, реабилитационных вмешательств)
УУР
Расшифровка
A
Сильная рекомендация (все рассматриваемые критерии эффективности (исходы) являются важными, все исследования имеют высокое или удовлетворительное методологическое качество, их выводы по интересующим исходам являются согласованными)
B
Условная рекомендация (не все рассматриваемые критерии эффективности (исходы) являются важными, не все исследования имеют высокое или удовлетворительное методологическое качество и/или их выводы по интересующим исходам не являются согласованными)
C
Слабая рекомендация (отсутствие доказательств надлежащего качества (все рассматриваемые критерии эффективности (исходы) являются неважными, все исследования имеют низкое методологическое качество и их выводы по интересующим исходам не являются согласованными)
Порядок обновления клинических рекомендаций.
Механизм обновления клинических рекомендаций предусматривает их систематическую актуализацию - не реже чем один раз в три года, а также при появлении новых данных с позиции доказательной медицины по вопросам диагностики, лечения, профилактики и реабилитации конкретных заболеваний, наличии обоснованных дополнений/замечаний к ранее утвержденным КР, но не чаще 1 раза в 6 месяцев.
Приложение А3
СПРАВОЧНЫЕ МАТЕРИАЛЫ,
ВКЛЮЧАЯ СООТВЕТСТВИЕ ПОКАЗАНИЙ К ПРИМЕНЕНИЮ
И ПРОТИВОПОКАЗАНИЙ, СПОСОБОВ ПРИМЕНЕНИЯ И ДОЗ
ЛЕКАРСТВЕННЫХ ПРЕПАРАТОВ, ИНСТРУКЦИИ ПО ПРИМЕНЕНИЮ
ЛЕКАРСТВЕННОГО ПРЕПАРАТА
1. Об основах охраны здоровья граждан в Российской Федерации (ФЗ N 323 от 21.11.2011)
2. Порядок оказания медицинской помощи больным с сердечно-сосудистыми заболеваниями (Приказ Минздрава России N 918н от 15.11.2012)
3. Приказ Минздрава России N 560н от 9 июня 2020 года "Об утверждении Правил проведения рентгенологических исследований"
4. Приказ Минздрава России от 08.06.2020 N 557н "Об утверждении Правил проведения ультразвуковых исследований".
Технология выполнения трансторакальной эхокардиографии
Требования:
У новорожденных и детей раннего возраста: датчики с частотой 7.5 - 12 МГц, у подростков и взрослых - 2.5 - 7 МГц.
Противопоказания: нарушение целостности кожных покровов в месте проведения исследования.
Ограничения: случаи неудовлетворительного акустического окна.
Приложение Б
АЛГОРИТМЫ ДЕЙСТВИЙ ВРАЧА
Алгоритмы действий врача при подозрении на аномалии КА
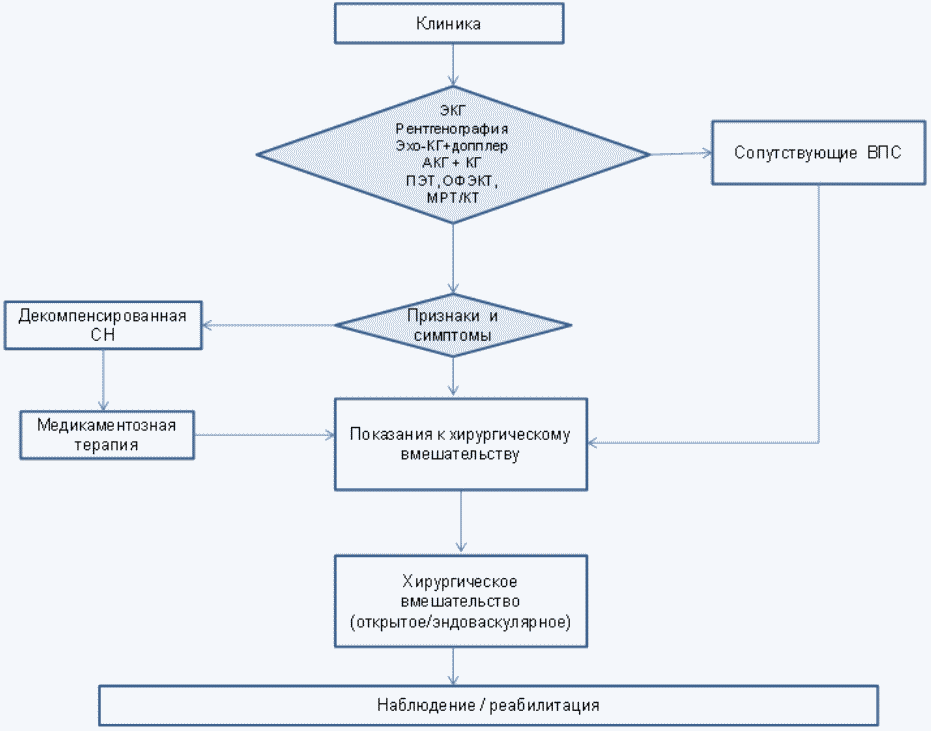
Алгоритм действий врача у больного с подозрением на аномальное отхождение ЛКА от ЛА
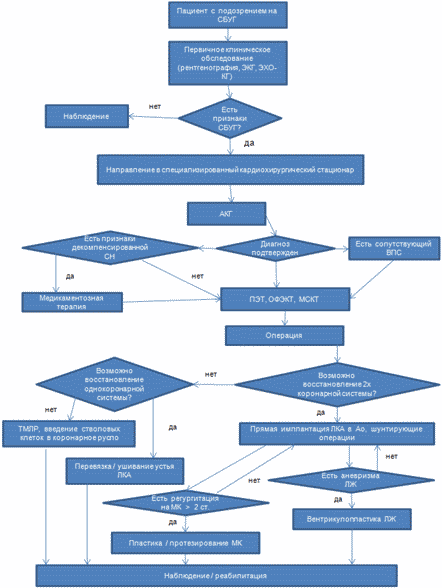
Алгоритм ведения пациентов с диагностированными КСФ в зависимости от размеров и локализации [50].
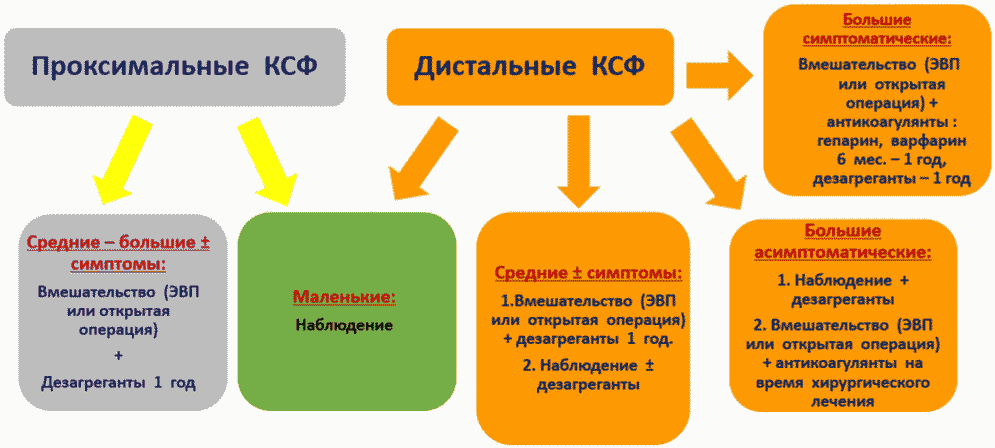
Приложение В
ИНФОРМАЦИЯ ДЛЯ ПАЦИЕНТА
Уважаемый пациент (родители пациента), результаты обследования выявили у Вас (Вашего ребенка) врожденный порок сердца - аномалии коронарных артерий.
Аномалии коронарных артерий представляют собой разнообразную группу врожденных патологических изменений коронарных сосудов, формирующихся вследствие аномального отхождения, следования или строения терминального русла коронарных артерий.
Большинство аномалий коронарных артерий являются случайными находками при диспансерном обследовании пациентов и часто не представляют угрозы для пациента (поэтому и не требуют ни консервативного, ни хирургического лечения). Но следует понимать, что есть и исключения. К жизнеугрожающим аномалиям КА относится:
1) Аномальное отхождение ЛКА от ЛА (синдром Бланд-Уайт-Гарланда - СБУГ) представляет собой редкий врожденный порок сердца (ВПС), характеризующийся неблагоприятным течением уже в периодах новорожденности и младенчества и крайне сомнительным прогнозом при естественном развитии.
2) Коронаро-сердечные фистулы (КСФ) - аномальное сообщение между коронарными артериями с полостью сердца или другими сосудистыми структурами минуя капиллярное русло, приводящее к нарушению структуры коронарных артерий и кровотока по ним.
Клиническая картина инфантильного типа течения СБУГ может проявиться сразу после рождения развитием терминального состояния вследствие обширного инфаркта миокарда либо множественных инфарктов (у некоторых младенцев - с кардиогенным шоком). При более благоприятном течении заболевания первые симптомы могут манифестировать в первые 3 месяца жизни, реже - во втором полугодии. Первыми признаками являются нарушение общего состояния - вялость, бледность кожных покровов, повышенная потливость, рвота, срыгивания, одышка и тахикардия. У половины малышей отмечаются приступы внезапного резкого беспокойства с усилением одышки, бледности, потливости - именно они иногда становятся первыми признаками болезни. Как правило, приступы беспокойства возникают после или во время кормления и могут длиться несколько минут. В промежутках между приступами ребенок выглядит вполне здоровым, и настораживающим фактором может явиться только наличие одышки. В литературе эти приступы носят название "стенокардия кормления" из-за сходства с клиникой стенокардии у взрослых. Общность явлений подтверждается и данными аутопсии (признаки старых и свежих инфарктов миокарда). Многие дети на этой стадии заболевания отстают в физическом развитии. У них рано развивается левосторонний сердечный горб. С ростом ребенка к клиническим проявлениям порока присоединяется митральная недостаточность, возникающая вследствие хронической ишемии или инфаркта папиллярных мышц, дилатации полости ЛЖ и деформации створок клапана. В ряде клинических случаев (при серьезном ишемическом поражении клапанных и подклапанных структур) регургитация на МК может развиваться и в более раннем (грудном) возрасте, маскируя проявления основного порока, что может привести к диагностической ошибке и неправильной хирургической тактике [51].
Таким образом, на этой стадии заболевания у ребенка превалируют признаки сердечной недостаточности преимущественно по левожелудочковому типу, а клиническая картина "инфантильного" типа порока у детей младшей возрастной группы может напоминать таковую при миокардите, дилатационной кардиомиопатии, врожденной недостаточности МК или обструктивном поражении выводного отдела ЛЖ (стеноз аорты, коарктация аорты). При наличии любых из вышеописанных признаков у Вашего ребенка следует незамедлительно обратиться в кардиохирургический стационар для уточнения диагноза.
При "взрослом" типе порока (СБУГ) отмечается доминантность правой КА, а сообщение между ЛКА и ЛА является рестриктивным [45, 52 - 54]. Родители детей, как правило, не предъявляют жалоб, свидетельствующих о заболевании сердца, а развитие ребенка может соответствовать возрасту. При подобном компенсированном течении порока клинические проявления могут длительно отсутствовать и проявиться уже в подростковом и/или даже взрослом возрасте. Первыми симптомами СБУГ у подростков могут быть плохое самочувствие или же появление дискомфорта в области сердца при спортивных занятиях, в редких случаях возможно возникновение типичных загрудинных стенокардитических болей. Важным моментом при подобном клиническом варианте течения порока является то, что даже при отсутствии клинических симптомов имеет место прогрессирование ишемии миокарда, что связано с наличием коллатерального кровотока между ПКА и ЛКА на уровне высокого деления коронарных артерий - 2 - 3 порядка, а миокард, кровоснабжаемый более мелкими венечными артериями, продолжает испытывать гипоксию. Потому в этой подгруппе пациентов в 80 - 90% случаев существует риск внезапной сердечной смерти [31, 32, 34, 36, 52, 53]. Поэтому при наличии любых из вышеописанных признаков у Вашего ребенка следует незамедлительно обратиться в кардиохирургический стационар для уточнения диагноза.
У взрослых нередко первыми проявлениями порока могут явиться нарушения ритма, что может привести к диагностической ошибке. Вследствие этого диагностический алгоритм обследования таких пациентов должен быть расширен с привлечением методов диагностики, позволяющих выявить скрытую ишемию миокарда и коронарную аномалию [52].
Клинические проявления КСФ малоспецифичны, зависят от ее размеров и величины коронарного сброса крови. Наиболее частой жалобой является появление несоответствующей обычной нагрузке одышки, связанной с постепенным увеличением фистулы, нарастанием степени легочной гипертензии и усилением сброса крови "слева-направо" [2, 5, 8 - 10, 16].
По сравнению с взрослыми у детей бессимптомные фистулы встречаются редко. Описаны случаи, когда КФ диагностируется в неонатальном периоде [5]. Средние по величине и большие КСФ могут приводить к появлению продолжительного шума. Приступы стенокардии у детей грудного возраста распознаются по появлению раздражительности, потливости, бледности, одышки и тахикардии. У детей КСФ часто манифестируют в возрасте 2 - 3 месяцев, когда снижается сопротивление легочных сосудов. В старшем возрасте могут быть проявления сердечной недостаточности, аритмии, синкопе, боль в грудной клетке, изредка эндокардит. При большой величине сброса крови может появляться картина застойной сердечной недостаточности и стенокардия.
Взрослых пациентов наиболее часто беспокоят одышка, боли в области сердца при физической нагрузке, перебои в работе сердца. При клиническом обследовании больных могут быть выявлены увеличенные размеры сердца, постоянный систолодиастолический шум с максимальным звучанием в третьем-четвертом межреберье. Любые из вышеперечисленных признаков или жалоб - являются показаниями к проведению обследования пациента в специализированном кардиохирургическом стационаре.
При своевременном выявлении данных аномалий прогноз в подавляющем большинстве случаев - благоприятный, но лишь при условии хирургического устранения аномалии. При несвоевременном обращении или затягивании с хирургической коррекции прогноз с высокой степенью может быть неблагоприятным.
Поэтому при наличии вышеописанных жалоб у Вас или Вашего ребенка необходимо незамедлительно обратиться к специалисту (детскому/взрослому кардиологу) для дальнейших рекомендаций.
Добровольно соглашаясь на операцию, Вы должны понимать цель и возможные осложнения операции, о которых Вам расскажет лечащий врач.
Приложение Г1 - ГN
ШКАЛЫ
ОЦЕНКИ, ВОПРОСНИКИ И ДРУГИЕ ОЦЕНОЧНЫЕ ИНСТРУМЕНТЫ СОСТОЯНИЯ
ПАЦИЕНТА, ПРИВЕДЕННЫЕ В КЛИНИЧЕСКИХ РЕКОМЕНДАЦИЯХ
Нет.
